Изобретение относится к лекарственному средству для лечения нарушений пищеварения, содержащему ферменты из инфузорий.
В общемедицинской и терапевтической практике нарушения пищеварения играют все большую роль. Эти нарушения пищеварения во многих случаях являются следствием более или менее выраженного дефицита так называемых ферментов поджелудочной железы. Эти ферменты в здоровом состоянии в поджелудочной железе синтезируются высокоспециализированными клетками, так называемыми ацинозными клетками, и выделяются за счет экзоцитоза через слюнные железы и главный выводной проток (Ductus pancreatics) в двенадцатиперстную кишку. Суточное количество панкреатического секрета составляет примерно 2 л. Наряду с переваривающей жиры липазой в панкреатическом секрете находятся также ферменты для переваривания протеинов (трипсин, химотрипсин и карбоксипептидазы) и углеводы (α-амилаза). При этом секреция ферментов поджелудочной железы точно регулируется эндогенными регулирующими механизмами с помощью гормонов, как гастрин, секретин и панкреозимин. Этот регулирующий механизм может нарушаться из-за множества причин, так что наступает дросселирование секреции ферментов поджелудочной железы или полная регрессия экзокринной функции поджелудочной железы. Это приводит к тому, что пищевая кашица в тонком кишечнике не переваривается и возникает нарушение пищеварения. Это, называемое также экзокринной недостаточностью поджелудочной железы, заболевание пищеварительного тракта может быть вызвано различными причинами. Наряду с медикаментозно обусловленными диспепсиями, хроническим атрофическим гастритом и хроническим, провоцируемым зачастую потреблением алкоголя, панкреатитом, этиологическими факторами недостаточности поджелудочной железы являются оперативно обусловленные нарушения (например, резекция желудка по Бильроту I и II, ваготомия, резекция поджелудочной железы) и кистозные фиброзы. В каждом случае хронические нарушения пищеварения имеют важное социально-медицинское и вместе с тем экономическое значение, так как пациенты за счет симптоматики зачастую являются ограниченно работоспособными или неработоспособными и имеют более короткую продолжительность жизни.
Панкреатогенные нарушения пищеварения вызывают у пациентов множество недугов, как диарея, массовый стул, чувство наполнения, затруднения в эпигастральной области, уменьшение массы тела и другие.
Независимо от причин и проявления панкреатогенных нарушений пищеварения или недостаточности поджелудочной железы для устранения нарушений пищеварения всегда необходима заместительная терапия с помощью ферментов. Это означает, что извне нужно вводить отсутствующие ферменты, предпочтительно липазу, протеазу и амилазу, а также другие ферменты. При терапии ферменты вводят пациенту перорально, чаще всего в середине приема пищи, и через желудок они попадают в тонкий кишечник, где осуществляют переваривание пищевой кашицы (химуса) и таким образом выполняют функцию отсутствующих, присущих организму ферментов поджелудочной железы. При этом нужно использовать препараты, которые содержат достаточное количество ферментов. К тому же ферменты должны быть устойчивы к кислоте желудочного сока, иметь незначительные размеры частиц и полностью биодоступны в пищеварительном тракте.
Для лечения нарушений пищеварения, которые основываются на отсутствии ферментов поджелудочной железы, в особенности главного фермента липазы и протеазы, в продаже уже имеется множество препаратов, содержащих ферменты. Они базируются отчасти на ферментах поджелудочной железы свиней, как, например, препараты Combizym®, Festal®, Pankreon®, Kreon®, Panzytrat®, Meteozym® или Enzym-Lefax N®, или, как Citrapepsin®, на желудочных ферментах. Отчасти, однако, препараты содержат также ферменты из экстрактов плесневых грибков, как, например, Combizym® и Festal®. Далее, описывается использование ферментов из рыб или других морских животных (патент Франции 1015566), а также композиции ферментов из желудочно-кишечного тракта криля (виды раков класса Euphauslaceae) и мойвы (патент США 4695457). Препараты, содержащие ферменты поджелудочной железы, чаще всего получают из отходов при разделке рыбы, или из поджелудочных желез свиней. Конечным продуктом процесса приготовления является панкреатин. Панкреатин представляет собой гомогенат из клеток панкреатической ткани (как правило, свиньи). За счет разрушения множества ацинозных клеток он содержит наряду с ферментами поджелудочной железы множество других ферментов и протеинов, а также другие высоко- и низкомолекулярные соединения. Состав панкреатина обусловлен промышленным способом его получения. Для получения панкреатина поджелудочные железы свиней после убоя по возможности быстро подвергают замораживанию, собирают и механически разрушают. Для стабилизации и активации ферментов в гомогенат вводят различные добавки. Затем осуществляют обезжиривание с помощью органических растворителей, как, например, ацетон, удаление волокнистых веществ, а также обезвоживание и высушивание путем лиофилизации. Для приготовления определенных форм применения можно осуществлять дальнейшую галеновую переработку с получением микрогранул, таблеток, капсул, паст, кремов, гелей, масел или других готовых лекарственных форм. Часто панкреатин смешивают с различными носителями и буферными веществами. Далее, для защиты от низкого значения рН человеческого желудочного сока гранулированный панкреатин покрывают кислотоустойчивыми пленками или лаками. Обе, указанные последними, стадии переработки при этом должны обеспечивать выполнение неустойчивыми к кислоте ферментами поджелудочной железы в месте назначения, двенадцатиперстной кишке (тонкий кишечник), ее пищеварительной функции.
Наряду с обычным приготовлением панкреатина в конечном продукте можно повышать содержание липазы путем поэтапной экстракции хлороформом, бутанолом и ацетоном. Подобно тому, как в случае панкреатина, композиции ферментов получают из криля вида Euphausia suberba и из кишок мойвы (называемой на немецком языке Lodden) (см. заявку США А-4695457). Также в этом случае прежде всего получают гомогенат из ткани, затем его очищают путем центрифугирования, экстракции хлороформом, лиофилизации и хроматографических стадий. В каждом случае целью процесса переработки является достижение по возможности высокого содержания ферментов поджелудочной железы, как липаза, протеаза и α-амилаза. Далее, композиция ферментов для лечения нарушений пищеварения должна быть по возможности устойчивой к кислоте желудочного сока. Кроме того, в пищеварительном тракте, и в особенности в двенадцатиперстной кишке, ферменты должны по возможности быстро высвобождаться и оказывать свое биологическое действие. Во избежание аллергий композиция ферментов по возможности не должна содержать неактивных протеинов, т.е. должна иметь высокую степень чистоты. Кроме того, с фармакоэкономических точек зрения процесс приготовления должен быть недорогостоящим.
В случае панкреатина обычно не осуществляют никакой дальнейшей очистки хроматографическими методами, так что целевые ферменты не находятся ни в очищенной, ни в гомогенной форме. Недостатком таких протеиновых смесей из клеточных гомогенатов является то, что они содержат множество протеинов из внутриклеточных компартментов (цитозоль, клеточные ядра, мембраны органелл) свиных панкреатических клеток. Они не обладают никакой или никакой желательной ферментной активностью и таким образом значительно снижают количество биологически активного вещества на вводимую форму применения. То же самое происходит, если получают концентрированные клеточные гомогенаты из криля или желудочно-кишечного тракта мойвы.
Другим недостатком приготовления ферментов и композиций ферментов из отходов при разделке рыбы (поджелудочная железа, желудочно-кишечный тракт рыб) и криля является периодический способ получения. Обычно органы (поджелудочные железы) на различных стадиях размельчают и гомогенизируют. Гомогенат затем обезжиривают и высушивают. Эти стадии получения ферментов нельзя осуществлять непрерывно, так как всегда работают со значительной долей твердого вещества, которую из-за стадий экстракции и центрифугирования нельзя перерабатывать далее непрерывно. Для получения ферментов, однако, оптимальны непрерывные или частично непрерывные производственные процессы, так как выход в единицу времени на единицу объема в случае таких процессов выше и, таким образом, ниже затраты. Для непрерывного получения ферментов, однако, необходимо, чтобы они находились внеклеточно в растворенной форме и не высвобождались только за счет размельчения, или гомогенизации клеток.
Для непрерывного получения ферментов поэтому процесс приготовления панкреатина непригоден.
Другим недостатком ферментов из поджелудочной железы является их неустойчивость к кислоте. Ферменты поджелудочной железы представляют собой нейтральные или щелочные гидролазы. Это означает, что, во-первых, они проявляют максимум своей активности при значениях рН от 7 до 8 и в кислых условиях они имеют сильно пониженную активность. Во-вторых, низкие значения рН инактивируют их каталитическую функцию за счет обратимой или необратимой денатурации. По этой причине получаемые из поджелудочной железы ферменты (панкреатин) с помощью специальных способов инкапсулирования или добавления буферных веществ нужно защищать от низкого значения рН кислоты желудочного сока при прохождении через желудок. Такие способы также повышают стоимость лекарственных средств, основанных на действии панкреатина.
К тому же, отрицательным моментом в отношении использования ферментов поджелудочной железы для определенных групп пациентов с нарушениями пищеварения является происхождение панкреатина. Обычно используют поджелудочные железы свиней, что является неприемлемым для пациентов еврейской и мусульманской религиозной принадлежности из-за религиозных предписаний.
Наконец, ферменты поджелудочной железы свиней нельзя использовать в случае пациентов с нарушениями пищеварения, которые обладают аллергией по отношению к белкам свиней. Свиней к тому же считают естественным "резервуаром" патогенных для человека вирусов гриппа, так что нельзя исключать контаминацию панкреатина такими вирусами.
Задачей изобретения поэтому является получение ферментов соответственно композиций ферментов для лекарственных средств, которые:
1) находятся во внеклеточной области и могут быть получены и очищены без гомогенизации (разрушения) тканей или клеток из свободного от клеток супернатанта;
2) можно получать непрерывно в биотехнологическом процессе из безопасного, неизмененного путем генной инженерии микроорганизма;
3) представляют собой кислые гидролазы, следовательно, имеют максимум своей активности при кислом значении рН и более устойчивы к кислоте, чем ферменты из поджелудочной железы;
4) не происходят из тканей или органов свиней.
Поставленная задача решается благодаря лекарственному средству, которое содержит ферменты, выбираемые из группы, состоящей из гидролаз, липаз, протеаз, амилаз, гликозидаз, фосфолипаз, фосфодиэстераз, фосфатаз, которые получают из инфузорий.
Объектом изобретения являются в особенности лекарственные средства, которые используют для способствования пищеварению и для лечения нарушений пищеварения.
Предлагаемые согласно изобретению лекарственные средства предпочтительно содержат ферменты, используемые для переваривания содержащихся в пищевых продуктах макромолекул, как протеины, нуклеиновые кислоты и углеводы, а также прочих компонентов пищевых продуктов, как, например, жиры или фосфолипиды, в желудочно-кишечном тракте людей или животных.
Специалисту ясно, что согласно изобретению для способствования пищеварению или для лечения нарушений пищеварения также можно использовать ферменты из инфузорий, которые не относятся к используемым до сих пор липазам, протеазам или амилазам, так как также другие ферменты за счет каталитического расщепления компонентов пищи могут способствовать пищеварению в желудочно-кишечном тракте.
Согласно одному варианту осуществления изобретения ферменты обладают оптимальным значением рН от 4 до 6.
Предлагаемые согласно изобретению лекарственные средства предпочтительно содержат ферменты, которые происходят из инфузорий рода Tetrahymena, Colpidium, Paramecium.
В предлагаемых согласно изобретению лекарственных средствах предпочтительно содержатся фармацевтически приемлемые вспомогательные вещества и носители.
Предлагаемые согласно изобретению лекарственные средства используют в особенности в форме таблеток, микрогранул, масел, соков, гелей, суппозиториев, капсул, драже.
Объектом изобретения является также применение ферментов из инфузорий, выбираемых из группы, состоящей из гидролаз, липаз, протеаз, амилаз, гликозидаз, фосфолипаз, фосфодиэстераз и/или фосфатаз, для получения лекарственного средства в целях лечения нарушения пищеварения, в особенности медикаментозно обусловленной диспепсии, хронического атопического гастрита, хронического панкреатита, острого панкреатита, оперативно обусловленного нарушения пищеварения или вызванного кистозным фиброзом нарушения пищеварения.
Ферменты, которые продуцируют простейшие отряда инфузорий и которые используют в предлагаемых согласно изобретению лекарственных средствах, особенно пригодны для лечения нарушений пищеварения. Кроме того, ферменты и композиции ферментов из инфузорий, которые содержатся в предлагаемых согласно изобретению лекарственных средствах, а также их получение, не обладают недостатками вышеуказанных ферментов поджелудочной железы или ферментов из мойвы или криля.
Ферменты из инфузорий поступают в окружающую их культуральную среду. В таблице 1 представлены, например, ферментные активности различных ферментов в культуральной среде инфузорий. Указанные в таблице 1 ферментные активности определяли обычными, описанными в литературе способами. Для определения активности в случае липазы использовали азоказеиновый тест (Muricane, 1986). Для определения активности в случае липазы и амилазы осуществляли тесты в соответствии с методиками FIP для грибковой амилазы и микробной липазы (Demeester и др. " Pharmaceutical Enzymes", отв. ред. A. Lauwers и S. Scharpe, Marcel Dekker, Нью-Йорк, 1997, с. 372-382). Для определения активности в случае кислой фосфатазы и β-гексозаминидазы использовали п-нитрофенилфосфатный, соответственно п-нитро-фенил-N-ацетил-β-D-глюкозаминный субстрат, которые описаны Kiy и др. (1996). Активность фосфолипазы А1 определяли с помощью радиометрического ферментного теста (Hartmann и др., 2000).
Ферментная активность во внеклеточной культуральной среде
(Ед/л) после культивирования в течение 72 часов при использовании среды на основе обезжиренного молока в ферментере емкостью 2 л
аминидаза
А1
Фосфатаза
Инфузории, которые выделяют ферменты в культуральную среду, можно при меньших издержках ферментировать при использовании недорогостоящих ферментационных сред при высокой плотности клеток и непрерывно. При этом ферменты можно отфильтровывать свободными от клеток из ферментера через перфузионный модуль (микрофильтр) и таким образом непрерывно удалять из ферментационной среды. Процесс ферментации можно поддерживать в течение более длительных промежутков времени за счет постоянного подвода недорогостоящих питательных сред (компоненты: среда на основе обезжиренного молока и дрожжевой экстракт).
Пример 1
На фигуре 1 представлена кинетика секреции инфузории в течение 14-дневного периода ферментации. В случае непрерывной ферментации с перфузионным модулем при этом поступают следующим образом.
Система биореактора базируется на управляемом процессором ферментере емкостью 2 л (BIOSTAT MD, Braun Diessel Biotech, Melsungen, Германия) с цифровым DCU-блоком регулировки и насосным блоком. Сбор свободного от клеток супернатанта осуществляли через перфузионный модуль, в качестве мешалки применяли лопастной импеллер. При этом использовали концентрацию силиконового масла 1 мл/л. Число оборотов мешалки для защиты от повреждения клеток ограничивали 800 об./мин. Концентрацию растворенного кислорода поддерживали постоянно при 60% с помощью каскадного регулирования. При этом выбирали, в первую очередь, скорость аэрации в качестве первого регулируемого параметра и, во вторую очередь, число оборотов мешалки в качестве следующего параметра регулирования. Измерение концентрации кислорода осуществляли с помощью амперметрического О2-электрода (Ingold Messtechnik, Steinbach). Температуру в ферментере поддерживали при 30оС за счет использования сосуда с двойными стенками и термостата, регулирование значения рН 7 во время непрерывной фазы ферментации осуществляли через DCU-регулируемый насос для корректирующего средства с помощью 4 М уксусной кислоты. На непрерывной фазе ферментации в ферментер вводили среду на основе обезжиренного молока и израсходованную, содержащую ферменты среду удаляли из процесса ферментации. За счет использования насоса, которым управляли через электропроводящий зонд, рабочий объем 2 л могли поддерживать постоянным. Свободный от клеток супернатант собирали без частиц через перфузионный модуль с размером пор мембраны примерно 0,3 мкм. Перфузионный модуль состоял из расположенного на держателе полипропиленового капилляра S6/2 (ENKA, Wuppertal) с наружным, соответственно внутренним диаметром 2, соответственно 1 мм и длиной 2,8 м. Обмен объема среды в единицу времени определяли как скорость перфузии. Подачу среды на основе обезжиренного молока могли регулировать числом оборотов рукавного насоса таким образом, что устанавливали скорость перфузии одного объема ферментера (2 л) в день. Перед автоклавированием ферментер доводили до полного осаждения пены и загружали 1,8 л среды на основе обезжиренного молока без глюкозы. После автоклавирования через впускной штуцер насосом подавали 200 мл 10%-ного раствора глюкозы. Соединение склянки со средой и склянки со сбором осуществляли через быстродействующие муфты в стерильной камере. В стерильной камере затравочные культуры переливали в колбу Эрленмейера емкостью 500 мл путем слива на дно и через шланг и отдельные патрубки для затравки подавали насосом в биореактор.
Инфузории при ферментации остаются неповрежденными, так что культуральная среда содержит только извлеченные из инфузорий протеины и не содержит никаких внутриклеточных компонентов. Благодаря этому из ферментационной, соответственно культуральной среды с помощью небольшого числа хроматографических стадий очистки можно достигать высокой степени чистоты.
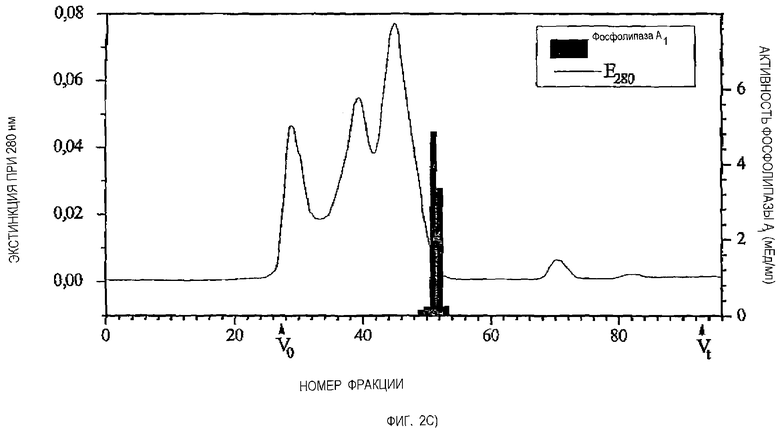
Пример 2
На фигуре 2 в качестве примера представлены осуществляемые с помощью колоночной хроматографии стадии очистки фосфолипазы из культуральной среды инфузории Tetrahymena. В данном случае представлены профили элюирования трех последовательных стадий колоночной хроматографии. В частности, при этом на фигуре 2а в качестве стадии 1 представлен профиль элюирования в случае хроматографии с гидрофобным взаимодействием; на фигуре 2b в качестве стадии 2 представлен профиль элюирования в случае анионообменной хроматографии и на фигуре 2с в качестве стадии 3 представлен профиль элюирования в случае высокоэксклюзионной хроматографии. Для последующих хроматографий использовали активные фракции предыдущих хроматографий. Таким образом, фермент после последней стадии могли очищать до почти полной гомогенности (никаких чужеродных активностей, незначительная доля чужеродных протеинов). В соответствии с этой схемой очистки можно также очищать другие ферменты из инфузорий, как протеаза, липаза, амилаза или β-гексозаминидаза.
Инфузории представляют собой, вплоть до необязательно патогенных представителей (Balantidium coli), свободноживущие (не паразитические) непатогенные микроорганизмы. Так, например, для инфузории Tetrahymena в литературе доказан GRAS-статус ("general recognized as save") (Tledtke, 1994). К тому же считается достоверным, что инфузории не содержат никаких эндопаразитов, которые могут быть перенесены на другие организмы. В случае важных для биотехнологии видов инфузорий, как Tetrahymena или Colpidium, отсутствуют вирусы или прочие эндопаразиты. Поэтому можно исключить контаминацию композиции ферментов токсическими или пирогенными загрязнениями.
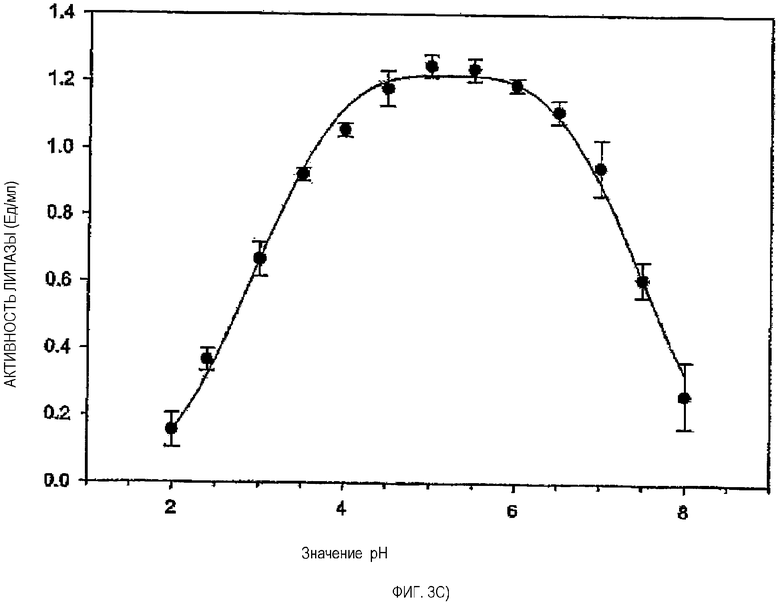
На фигуре 3 представлено получение относительных ферментных активностей трех ферментов из культуральной среды инфузории Tetrahymena при различных значениях рН (а - фосфолипаза А1; b - триацилглицеринлипаза; с - β-гексозаминидаза).
Ферменты из инфузорий как кислые гидролазы имеют оптимальное значение рН в кислой области. На фигуре 3 представлены ферментные активности трех ферментов из культуральной среды инфузории Tetrahymena при различных значениях рН. В частности, представлены относительные ферментные активности фосфолипазы А1 (фигура 3а) и β-гексозаминидазы (фигура 3b), а также абсолютная ферментная активность липазы (фигура 3с).
Отсюда ясно, что оптимальное значение рН для ферментов из инфузорий составляет 4,1-6,5. Протеаза из инфузорий обладает высокой ферментной активностью даже еще при значении рН, равном 3. В следующей таблице 2 представлена активность протеазы инфузорий из свободного от клеток супернатанта (культуральная среда) в зависимости от значения рН. Ферментные активности при этом, как уже описано выше, определяли в соответствии с методиками FIP для грибковой амилазы и микробной липазы.
протеазы
(единиц/литр)
На этом основании ферменты инфузорий также являются более кислотоустойчивыми, чем ферменты поджелудочной железы. Вследствие этого после прохождения через желудок они имеют значительно более высокую активность в двенадцатиперстной кишке, чем ферменты поджелудочной железы.
На фигуре 4 представлена кислотоустойчивость протеазы из инфузории Tetrahymena по сравнению с панкреатином в случае 10-минутной фазы воздействия типичного значения рН, которое имеется в желудочном соке (рН 1,5). Низкое значение рН имитировали путем воздействия высокой молярной концентрации буфера со значением рН в кислой области (1 М глицин/HCl, рН 1,5) при температуре 37оС.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИСПОЛЬЗОВАНИЕ ФЕРМЕНТОВ, АКТИВНЫХ В ШИРОКОМ ДИАПАЗОНЕ ЗНАЧЕНИЙ pH, В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ СТИМУЛЯЦИИ ПИЩЕВАРЕНИЯ | 2016 |
|
RU2721708C2 |
| ПИЩЕВАРИТЕЛЬНОЕ СРЕДСТВО НА ОСНОВЕ ФЕРМЕНТОВ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2009 |
|
RU2429291C1 |
| ФЕРМЕНТЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2005 |
|
RU2389504C2 |
| ВЫСОКОЭФФЕКТИВНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ПАНКРЕАТИНА | 2014 |
|
RU2686460C2 |
| СПОСОБ ПРОВЕДЕНИЯ ТЕСТА НА РАСТВОРЕНИЕ ТВЕРДЫХ КОМПОЗИЦИЙ, СОДЕРЖАЩИХ ПИЩЕВАРИТЕЛЬНЫЕ ФЕРМЕНТЫ | 2012 |
|
RU2602183C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЬНЫХ СО СНИЖЕННОЙ ВНЕШНЕСЕКРЕТОРНОЙ ФУНКЦИЕЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 1994 |
|
RU2068698C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО "ГАСТРОПЕК" ДЛЯ УЛУЧШЕНИЯ ПРОЦЕССОВ ПИЩЕВАРЕНИЯ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2004 |
|
RU2276974C2 |
| КОМПОЗИЦИЯ ПИЩЕВАРИТЕЛЬНЫХ ФЕРМЕНТОВ, ПОДХОДЯЩАЯ ДЛЯ ЭНТЕРАЛЬНОГО ВВЕДЕНИЯ | 2014 |
|
RU2679832C2 |
| ПОЛИФЕРМЕНТНОЕ СРЕДСТВО ФЕРЕСТАЛ | 2001 |
|
RU2201763C1 |
| ПРОТЕАЗЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2006 |
|
RU2420578C2 |





Изобретение относится к медицине и фармакологии и касается лекарственного средства, содержащего ферменты, выбираемые из группы, состоящей из гидролаз, липаз, протеаз, амилаз, гликозидаз, фосфолипаз, фосфодиэстераз, фосфатаз и полученных из инфузорий, а также касается применения указанных ферментов, полученных из инфузорий для улучшения пищеварения или для лечения нарушений пищеварения. Изобретение обеспечивает повышение устойчивости к кислой среде желудка и получение из безопасного микроорганизма. 2 н. и 5 з.п. ф-лы, 4 ил., 2 табл.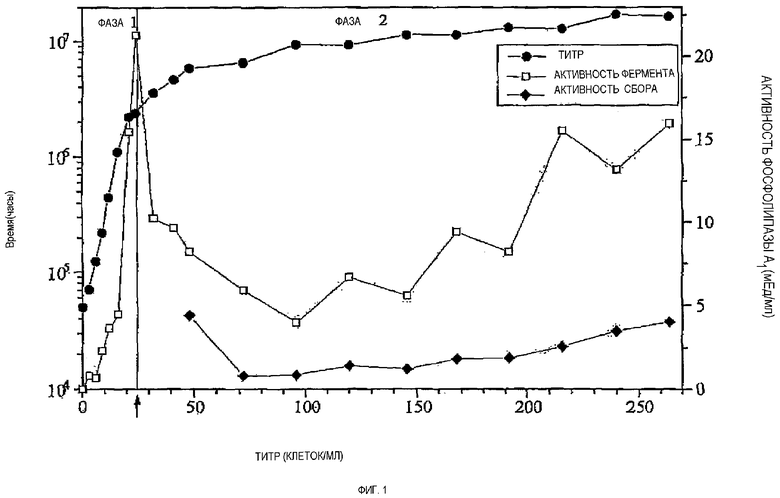
| US 4695457, 22.09.1987 | |||
| DE 4238842, 19.05.1994 | |||
| Arai H et al | |||
| J | |||
| Biochem (Tokyo), 1986, Jan, 99(1):125-33 | |||
| Blum JJ | |||
| J Cell Physiol | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
Авторы
Даты
2007-05-20—Публикация
2001-11-02—Подача