Способ выделения биологически активных антоцианов.
Изобретение относится к биотехнологии, в частности к способам получения биологически активных антоцианов из растительного сырья - красного винограда, и может быть применено в медицинской, косметической, пищевой промышленностях. Антоцианы, относящиеся к группе флавоноидов, известны и применяются, с одной стороны, как природные пигменты, а с другой - как биологически активные соединения.
Известны антоциановые натуральные красители, которые являются широко распространенными водорастворимыми колорантами и содержат в качестве основных пигментов антоцианы, являющиеся представителями флавоноидных соединений [Танчев С.С. Антоцианы в плодах и овощах. - М.: Пищевая промышленность, 1980, 304 с.].
Природным сырьем антоциановых пигментов различного цвета являются такие растения, как черная смородина (Ribes Nigrum), черноплодная рябина (Aronia melanocarpd), каркадэ (Hibiscus Sabdariffa L.), а также красный виноград (Vitis viniferd).
Известно, что антоцианы - перспективные ингридиенты косметических композиций для защиты организма, в частности кожи, от окислительного стресса. Антоцианы относятся к флавоноидам, вторичным метаболитам растений и служат им для защиты от неблагоприятных факторов, прежде всего от ультрафиолетового излучения, поражения вирусными инфекциями и плесенью. Антоцианы обладают широким спектром биологического действия. Они сочетают в себе антиоксидантные, бактерицидные, солнцезащитные свойства [Сизова Н.В. Биофлавоноиды - антиоксиданты, имуномодуляторы, капиляропротекторы. Сырье и упаковка. Вып.22. N.5. С.17-18.], обладают высокой капиляро-протекторной (Р-витаминной активностью) [Costantini A., De Bemardi Т., Gotti A. Clinical and capillaroscopic evaluation of chronic uncomplicated venous insufficiency with procyanidins extracted from Vitis vinifera. Minerva Cardioangiol. 1999. V.47. N.1-2. P.39-46.]. Кроме того, в последнее время стало известно о противоопухолевых [Hou D.X., Ose Т., Lin S., Harazoro К., Imamura I., Kubo М., Uto Т., Terahara N., Yoshimoto М., Fujii М. Anthocyanidins induce apoptosis in human promyelocytic leukemia cells: structure-activity relationship and mechanisms involved. Int. J. Oncol. 2003. V.23. N.3. P.705-712.], антимутагенных [Cody V., Middleton E., Harbome J.B. Plant flavonoids in biology and medicine: biochemical, pharmacological, and structure-activity relationships. Alan. R. Liss. Inc., New York. 1986. 330 p.], кардиопротекторных [Fremont L., Belguendouz L., Delpal S. Antioxidant activity of resveratrol and alcohol-free wine polyphenols related to LDL oxidation and polyunsaturated fatty acids. Life Sci. 1999. V.64. N.26. P.2511-2521.] и гепато-протекторных свойствах антоцианов [Ray S.D., Kumar M.A., Bagchi D.A novel proanthocyanidin IH636 grape seed extract increases in vivo bcl-Xl expression and prevents acetaminophen-induced programmed and unprogrammed cell death in mouse liver. Arch. Biochem. Biophys. 1999. N.369. P.42-58.]. Одним из условий эффективного применения антоцианов в качестве биологически активных компонентов в лечебно-косметических составах является их чистота.
Известно много способов выделения фракции антоцианов из экстрактов. Часто атоцианы от танинов отделяют в двухфазной системе этилацетат - вода [Markham K.R., Mabry T.J. Flavonoids. Chapman and Hall, London. 1975. 1197 p.]. Также для очистки антоцианов от флавоноидов других классов используют хроматографию на целлюлозе [Costa C.T., Hoiton D., Margolis S.A. Analysis of anthocyanins in food by lipid chromatography, liquid chromatography-mass spectrometry and capillary electrophoresis. J. of Chromatog. A. 2000. N.81. P.403-410.], полистирольных ионообменных смолах, амберлитах, ДЕАЕ-смолах, таких как DEM-63 и Toyopearl DEAE-650M [US 6780442, А61К 31/352, 2002, WO 03039569 A61K 9/70, 2003]. В качестве элюента используют водные растворы муравьиной и уксусной кислот и подкисленные соляной кислотой водно-спиртовые или водно-метанольные смеси в различных концентрациях. В результате этих операций получают смесь антоцианов со степенью обогащения до 88%. Танины с молекулярным весом более 500 Да от антоцианов отделяли гель-хроматографией на сефадексе-25 [Somers T.C. Wine tannins - isolated of condensed flavonoid pigments by gel-filtration. Nature. 1966. V.209. P.368-370.]. Известен также более простой способ выделения антоцианов с помощью сорбции на тальке [Валуйко Г.Г. Биохимия и технология красного вина. М:. Пищевая промышленность. 1973. 295 с.]. Первоначально для выделения индивидуальных антоцианов применялась БХ, впоследствии заменная ТСХ на силикагеле и полиамиде [Бандюкова В.А., Шинкаренко А.Л. Тонкослойная хроматография флавоноидов. Методические рекомендации, Пятигорск - 1975. 15 с.]. Эту операцию обычно проводят в две стадии: разделение антоцианов в водно-спиртовых смесях растворителей и в водных растворах кислот для отделения продуктов окисления [Валуйко Г.Г. Биохимия и технология красного вина. М:. Пищевая промышленность. 1973. 295 с].
Выявлено, что продукт, выделяемый из красного винограда, содержит не только комплекс антоцианов, но еще и пектины, липиды, танин. Смесь антоцианов, в свою очередь, состоит из: 3-глюкозилокси-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида (Соединение I); 3-глюкозилокси-(6-О-(4-гидроксициннамоил)-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида (Соединение II); 3-глюкозилокси-(6-O-(3,4-дигидроксициннамоил))-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида (Соединение III).
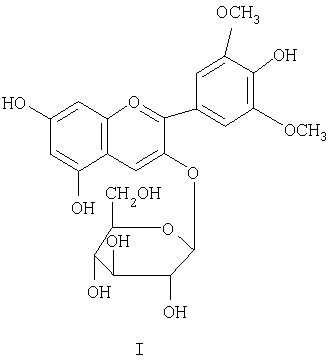
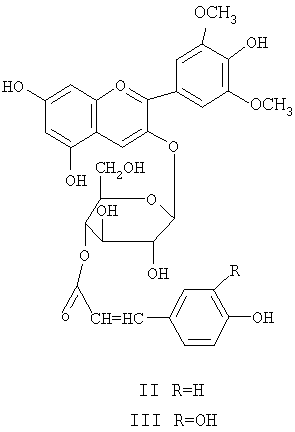
Одним из основных условий использования антоцианов в таких областях как медицина, косметология является чистота смеси антоцианов или индивидуальных антоцианов, существенно влияющая на биологическую активность.
Для создания новых эффективных биологически активных антоцианов разработан новый способ выделения индивидуальных антоцианов из экстракта жмыха красного винограда, включающий стадии сорбции смеси антоцианов на тальке, элюирование их подкисленным водно-спиртовым раствором с последующим хроматографическим разделением антоцианов на индивидуальные компоненты пропусканием их под вакуумом через хроматографическую колонку или фильтр, заполненные силикагелем с размером частиц 0.04-0.063 мм. В качестве элюента использовали смесь растворителей: этилацетат/уксусная кислота/вода в объемных соотношениях от 0.67/1/1 до 4.67/1/1. Хроматографию под вакуумом предпочтительно проводить при 10-14 мм рт.ст.
В качестве исходного сырья используют жмых красного винограда сорта "Изабелла", что позволяет получать определенные антоцианы в заданных количествах. При использовании этого сырья конечный продукт содержит биологически активные антоцианы: 3-глюкозилокси-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорид; 3-глюкозилокси-(6-O-(4-гидроксициннамоил)-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорид; 3-глюкозилокси-(6-O-(3,4-дигидроксициннамоил))-4',7-дигидрокси-3',5' -диметоксифлавилиум хлорид.
Использование жмыха красного винограда другого сорта, например каберне или саперави, позволяет получать смесь антоцианов другого состава.
Метод хроматографии на колонке или фильтре является промышленно осуществимым в отличие от метода хроматографии на бумаге или ТСХ. Существенным отличительным признаком нового способа являются условия проведения этапа хроматографии.
Технический эффект от использования нового способа заключается в том, что он обеспечивает, с одной стороны, получение чистой смеси антоцианов, обладающей высокой интенсивностью окрашивания растворов (коэффициент молярной экстинции ε=28000), так и высокой биологической активностью, и с другой стороны, он обеспечивает получение индивидуальных биологически активных антоциановых пигментов (I, II, III), которые могут являться составной частью медицинских средств широкого профиля, высокая биологической активность которых подтверждена нашими исследованиями. Весь процесс выделения антоцианов состоит из нескольких стадий. Очистка смеси антоцианов достигается тем, что водно-спиртовой экстракт красного винограда, содержащий 5-9% антоцианов, подвергают сорбционному отделению антоцианов от прочих веществ экстракта винограда на тальке. Для этого упаренный экстракт смешивают именно с порошком талька, избирательно сорбирующим антоцианы, суспензию этой смеси переносят на воронку Бюхнера и сначала элюируют дистиллированной водой, отделяя примеси, затем подкисленным этанолом элюируют антоцианы, после чего фракцию, содержащую антоцианы, упаривают.
Обогащенный таким способом антоциановый комплекс содержит 83-89 вес.% антоцианов. Далее для выделения из данного комплекса индивидуальных компонентов (I, II, III) проводят колоночную хроматографию на колонке или фильтре, заполненными силикагелем с размером частиц 0.040-0.063 мм, например, выпускаемом фирмой Merck. Выбор данного сорбента объясняется как его высокими хроматографическими свойствами, так и экономичностью использования за счет возможности его эффективной регенерации. Процесс проводят под вакуумом - так называемой флэш-хроматографией, предпочтительно при 10-14 мм рт.ст, что позволяет достигать оптимального разделения. При этом вакуум подается от водоструйного насоса, обеспечивающего остаточное давление на указанном выше уровне. Существенной характеристикой нового метода, которая в комплексе с другими принципами способа обеспечивает высокую эффективность процесса, является применение экспериментально подобранной хроматографической системы этилацетат/уксусная кислота/вода в соотношении 0.67-4.67/1/1. Использование метода элюции антоцианов данной хроматографической системой с различным соотношением компонентов на силикагеле позволяет достигнуть качественного разделения компонентов смеси антоцианов. Эффективность данных хроматографических систем видна из таблицы 1, в которой также указаны растворимости компонентов (I, II, III) - параметры, определяющие загрузку на процесс хроматографии.
Как видно из таблицы 1, экспериментально подобранный элюент позволяет с большей эффективностью разделять антоцианы по сравнению с ранее известными элюентами (бутанол/уксусная кислота/вода).
Применение системы этилацетат/уксусная кислота/вода также позволяет получать продукты, обладающие более высокой биологической активностью.
Ниже изобретение иллюстрируется примером 1-3.
Пример 1
ТП 1 Экстракция
Жмых массой 32 г, предварительно растертый в ступке, вносили в плоскодонную колбу объемом 0.5 л, в которую приливали 130 мл 70% спирта, содержащего 0.1 вес.% HCl. Колбу термостатировали на водяной бане при температуре 50°С. Экстракцию вели 1 ч при перемешивании (180 об/мин). Жмых отделяли на воронке Бюхнера.
Получали 132 мл экстракта, содержащего 1.15 мг/мл антоцианов.
ТП 2 Обогащение антоцианов
Водно-спиртовой экстракт, полученный на стадии ТП1, упаривали до объема 30 мл, доводили дистиллированной водой до 60 мл, вливали в стакан объемом 250 мл. К раствору присыпали 40 г талька, смесь суспензировали, переносили на воронку Бюхнера и фильтровали под вакуумом водоструйного насоса. Танин, частично адсорбирующийся на тальке, элюировали 500 мл дистиллированной воды. Антоцианы элюировали с талька 200 мл 80% раствора спирта, содержащего 0.1% HCl. Получали 192 мл смеси антоцианов с концентрацией 0.78 мг/мл. Выход 96%.
ТП 3 Колоночная хроматография антоцианов
Раствор антоцианов, полученный на стадии ТП 2, упаривали при температуре 40°С до сухого веса, после чего растворяли до насыщения в смеси растворителей этилацетат/уксусная кислота/вода в соотношении 0.67/1/1.
На колонку 250×25 мм, заполненную силикагелем Merck массой 90 г с размером частиц 0.04-0.063 мм, наносили 20 мл насыщенного раствора антоцианов с содержанием 1.950 мг/мл. Антоцианы элюировали под вакуумом описанной выше системой. Фракции собирали по 15-20 мл. Суммарный выход 3-глюкозилокси-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида; 3-глюкозилокси-(6-O-(4-гидроксициннамоил)-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида; 3-глюкозилокси-(6-O-(3,4-дигидроксициннамоил))-4',7-дигидрокси-3',5'-диметоксифлавилиум хлорида составил 86% от исходного количества антоцианов.
Пример 2
ТП 1 Экстракция
Жмых массой 40 г, предварительно растертый в ступке, вносили в плоскодонную колбу объемом 0.5 л, в которую приливали 160 мл 95% спирта, содержащего 0.1 вес.% HCl. Колбу термостатировали на водяной бане при температуре 40°С. Экстракцию вели 1 ч при перемешивании (180 об/мин). Жмых отделяли на воронке Бюхнера.
Получали 169 мл экстракта, содержащего 1.24 мг/мл антоцианов.
ТП2 Обогащение антоцианов
Водно-спиртовой экстракт, полученный на стадии ТП 1, упаривали до сухого вещества, полученную массу растворяли в дистиллированной воде до 90 мл, вливали в стакан объемом 250 мл. К раствору присыпали 60 г талька, смесь суспензировали, переносили на воронку Бюхнера и фильтровали под вакуумом водоструйного насоса. Танин, частично адсорбирующийся на тальке, элюировали 600 мл дистиллированной воды. Антоцианы элюировали с талька 200 мл 80% раствора спирта, содержащего 0.1% HCl. Получали 195 мл смеси антоцианов с концентрацией 1.02 мг/мл. Выход 95%.
Флэш-хроматография антоцианов
Раствор антоцианов, полученный на стадии ТП 2, упаривали при температуре 40°С до сухого веса, после чего растворяли до насыщения в смеси растворителей этилацетат/уксусная кислота/вода в соотношении 4.67/1/1.
На стеклянный фильтр Шота диаметром 100 м, заполненный силикагелем Merck массой 340 г с размером частиц 0.04-0.063 мм с высотой слоя и высотой 80 мм, наносили 50 мл насыщенного раствора антоцианов с содержанием 0.170 мг/мл. Элюцию вели под вакуумом водоструйного насоса. Фракции собирали по 25-40 мл. Суммарный выход составил 95% от исходного количества антоцианов.
Пример 3
ТП 1 Экстракция
Жмых массой 55 г, предварительно растертый в ступке, вносили в плоскодонную колбу объемом 0.5 л, в которую приливали 220 мл 50% спирта, содержащего 0.1 вес.% HCl. Колбу термостатировали на водяной бане при температуре 55°С. Время эктстракции 1 ч при перемешивании (180 об/мин). Жмых отделяли на воронке Бюхнера.
Получали 224 мл экстракта, содержащего 1.09 мг/мл антоцианов.
ТП2 Обогащение антоцианов
Водно-спиртовой экстракт, полученный на стадии ТП1, упаривали до объема 50 мл, доводили дистиллированной водой до 100 мл, вливали в стакан объемом 250 мл. К раствору присыпали 70 г талька, смесь суспензировали, переносили на воронку Бюхнера и фильтровали под вакуумом водоструйного насоса. Танин, частично адсорбирующийся на тальке, элюировали 800 мл дистиллированной воды. Антоцианы элюировали с талька 300 мл 80% раствора спирта, содержащего 0.1% HCl. Получали 287 мл смеси антоцианов с концентрацией 0.81 мг/мл. Выход 95%.
Флэш-хроматография анпюцианов
Раствор антоцианов, полученный на стадии ТП 2, упаривали при температуре 40°С до сухого веса, после чего растворяли до насыщения в смеси растворителей этилацетат/уксусная кислота/вода в соотношении 1.75/1/1.
На стеклянный фильтр Шота диаметром 100 м, заполненный силикагелем Merck массой 340 г с размером частиц 0.04-0.063 мм с высотой слоя и высотой 80 мм, наносили 50 мл насыщенного раствора антоцианов с содержанием 0.955 мг/мл. Элюцию вели под вакуумом водоструйного насоса. Фракции собирали по 25-40 мл. Суммарный выход составил 95% от исходного количества антоцианов.
Из-за своих уникальных спектральных характеристик (максимум поглощения 540 нм и коэффициент молярной экстинции 28000 моль-1) антоцианы являются мощными красителями. Благодаря различным заместителям в своей сопряженной системе и в комплексах с различными металлами они могут менять цвет от оттенков красного до фиолетового. Ограничением является значение рН - в щелочной среде они обесцвечиваются и окисляются.
Высокая антиоксидантная и антирадикальная активности по нашим данным более высокая, чем активность синтетических антиоксидантов, позволяет использовать их в медицине, косметических композициях, в том числе и в солнцезащитной косметике. Для применения в медицине, в виде лекарственных форм, необходимо выделение чистых антоцианов, наиболее эффективных при обезвреживании свободных радикалов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хроматографического выделения и концентрирования антоцианов | 2020 |
|
RU2727130C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРИРОВАННОГО КРАСИТЕЛЯ | 2008 |
|
RU2381245C1 |
| СПОСОБ ОЦЕНКИ БИОЛОГИЧЕСКОЙ ЦЕННОСТИ АНТОЦИАНОВОГО КРАСИТЕЛЯ, ПОЛУЧЕННОГО БЕСКИСЛОТНЫМ СПОСОБОМ | 2006 |
|
RU2329284C2 |
| Способ получения красного пищевого красителя | 1987 |
|
SU1693001A1 |
| Способ определения 3,5-диглюкозида мальвидина в растениях винограда | 1977 |
|
SU641921A1 |
| Способ получения и состав для получения сухих лиофилизированных форм антоцианов | 2015 |
|
RU2626505C2 |
| АНТОЦИАНОВАЯ КРАСЯЩАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2628398C2 |
| Способ экспрессного определения суммарного содержания антоцианов | 2020 |
|
RU2768114C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТОЦИАНОВОГО КРАСИТЕЛЯ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2009 |
|
RU2399639C1 |
| СПОСОБ СТАБИЛИЗАЦИИ АНТОЦИАНОВОГО ПИГМЕНТА | 2024 |
|
RU2834867C1 |
Изобретение относится к усовершенствованному способу выделения индивидуальных биологически активных антоцианов пигментов, применяемых в качестве природных пигментов или биологически активных компонентов лекарственных и косметических средств, из водно-спиртового экстракта жмыха красного винограда, получаемых сорбцией антоцианов на тальке с последующим элюированием водно-спиртовым раствором и хроматографическим разделением на индивидуальные антоцианы, в котором хроматографическое разделение антоцианов осуществляют пропусканием их под вакуумом через колонку или фильтр, заполненные силикагелем с размером частиц 0,040-0,063 мм при использовании в качестве элюента следующей 3-х компонентной смеси: этилацетат/уксусная кислота/вода в объемных соотношениях 0,67-4,67/1/1. Достигается эффект более качественной очистки антоцианов, имеющих наибольшую биологическую активность. 1 з.п. ф-лы, 1 табл.
| Способ определения 3,5-диглюкозида мальвидина в растениях винограда | 1977 |
|
SU641921A1 |
| US 5762936 A, 09.06.1998 | |||
| US 6800433 A, 05.10.2004 | |||
| US 5525341 A, 11.06.1996. | |||
Авторы
Даты
2007-07-10—Публикация
2005-06-10—Подача