ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к композициям, содержащим полифенолы, например полифенолы какао, такие как процианидины, в комбинации, по крайней мере, с одним реагентом, снижающим уровень холестерина, и к способам улучшения состояния сосудистой системы, включая лечение и профилактику атеросклероза и сердечно-сосудистого заболевания.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Заболевание коронарных артерий, первичная форма сердечно-сосудистого заболевания (CVD), является главной причиной смертности в Соединенных Штатах на сегодняшний день. На третьем месте находится цереброваскулярное заболевание. Этиологию заболевания коронарных артерий и цереброваскулярных заболеваний связывают с атеросклерозом. На основании клинических проявлений установлено, что атеросклероз является главной причиной более одного миллиона сердечных приступов, приблизительно 400000 инсультов, которые происходят каждый год, и причиной многочисленных проблем, связанных с кровообращением. Многие больные страдают от гипертензии.
На основании значительного количества доказательств установлена причинная взаимосвязь между гиперхолестеринемией и ранним атеросклерозом; чем выше уровень холестерина в плазме крови, тем больше риск последующего сердечного приступа (см., например, Steinberg, D., JAMA 264: 3047 (1990)). Полагают, что в цепи событий, приводящих к атеросклерозу, инициирующим событием является образование "прожилок жира" в сонных, венечных и церебральных артериях и в аорте. Указанные патологические изменения включают в себя жировые отложения холестерина и холестерилового эфира, которые обнаружены в основном в гладкомышечных клетках и макрофагах слоя интимы. Миграция и пролиферация гладкомышечных клеток сосудов играет решающую роль в патогенезе атеросклероза после первоначального отложения липида.
Кроме того, развитие атеросклероза и сердечно-сосудистого заболевания модулируется и/или связано с окислением ЛПНП (LDL), активностью циклооксигеназы (СОХ), активностью липоксигеназы (LOX), синтезом оксида азота (NO) и активностью синтазы оксида азота (NOS). Связи между различными путями и процессами, вовлеченными в данную патологию, представлены на фиг.1 и детально описаны в международной заявке № PCT/US97/05693, опубликованной как международная патентная заявка WO 97/36497, соответствующие части которой включены в данный текст в виде ссылки. Кратко, окисление LDL является критической стадией в появлении повреждений (атеросклеротических бляшек), которые возникают тогда, когда макрофаги поглощают модифицированные окислением LDL и превращаются в так называемые «пенистые клетки». Ферменты СОХ и LOX включаются в путь метаболизма арахидоновой кислоты, что приводит к продукции простагландинов и тромбоксана А2, причем последний, как известно, вызывает сужение кровеносных сосудов и агрегацию тромбоцитов, и, следовательно, прогрессирование атеросклероза. Известно, что оксид азота ингибирует агрегацию тромбоцитов, адгезию/хемотаксис моноцитов и пролиферацию гладкомышечных клеток сосудов, причем все указанные факторы, как полагают, ответственны за прогрессирование атеросклероза. Было показано, что полифенолы какао оказывают благоприятное воздействие на вышеописанные процессы путем ингибирования окисления LDL, увеличения активности NO/NOS и ингибирования активности COX/LOX. Указанные эффекты продемонстрированы, например, в международной заявке № PCT/US97/05693, опубликованной как международная патентная заявка WO97/36497, и в примерах, приведенных в заявке. Полифенолы какао могут быть использованы для лечения или профилактики состояний, на которые, как известно, воздействуют введением нестероидных противовоспалительных средств, например аспирина.
Несмотря на благоприятное воздействие полифенолов какао на ряд путей метаболизма и состояний, связанных с индукцией и прогрессированием атеросклероза и CHD (ишемической болезни сердца), было показано, что указанные соединения не оказывают заметного холестеринснижающего эффекта. Таким образом, заявители приготовили улучшенную композицию, содержащую полифенолы в комбинации, по крайней мере, с одним реагентом, снижающим уровень холестерина. Композиция обладает усиленным воздействием на состояние сосудистой системы млекопитающего, в частности человека, по сравнению с ранее известными композициями, содержащими полифенол или холестеринснижающие реагенты.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Изобретение относится к композициям и способам улучшения общего состояния сосудистой системы у млекопитающего, в частности человека или животного.
В одном аспекте изобретение относится к композиции, такой как пищевой продукт, пищевая добавка, дополнение к пищевому рациону или фармацевтический препарат, содержащий полифенол какао и реагент, снижающий уровень холестерина. Необязательно композиция может содержать L-аргинин.
В другом аспекте изобретение относится к кондитерскому изделию, снижающему уровень холестерина, наиболее предпочтительно к холестеринснижающему шоколаду (например, темному шоколаду) и к кондитерскому изделию, содержащему холестеринснижающий шоколад.
В другом аспекте изобретение относится к способу улучшения общего состояния сосудистой системы, включая профилактику или лечение атеросклероза и сердечно-сосудистого заболевания у млекопитающего, такого как человек или домашнее животное, путем введения композиции, содержащей полифенол какао и холестеринснижающее соединение и, необязательно, L-аргинин. Полифенолы из других источников, обладающие такими же свойствами, как и полифенолы какао, также могут быть использованы в композициях и способах согласно изобретению в комбинации с реагентами, снижающими уровень холестерина, такими как холестеринснижающие реагенты на основе стерина и/или станола.
Кроме того, в других аспектах изобретение относится к способу увеличения всасывания полифенола, например флаванола или флавонола, путем введения млекопитающему полифенола в комбинации с фитостерином и/или фитостанолом. Также представлены композиции и продукты промышленного производства для использования в способе.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1 представляет собой схему, в которую включены основные факторы, которые вносят вклад в развитие ишемической болезни сердца (CHD), показывающую, как полифенолы какао способствуют предотвращению развития заболевания.
На фиг.2 A-D показано действие фитосоединений на синтез базальными эндотелиальными клетками простаноидов и эндотелинов в BAECS. (*= значительно отличается от контроля при р<0,05).
На фиг.3 А-В показано влияние типов клеток на вызванные процианидином изменения в высвобождении эндотелиальными клетками простациклина и эндотелина.
На фиг.4 А-С показано влияние потребления напитка какао на экспрессию на поверхности тромбоцитов активированного GPIIb-IIIa со стимуляцией слабыми агонистами или без нее.
На фиг.5 А-С показано влияние потребления напитка какао на экспрессию на поверхности тромбоцитов активированного Р-селектина со стимуляцией слабыми агонистами или без нее.
На фиг.6 показано влияние фитостеринов, процианидинов какао и их комбинации на всасывание эпикатехина в плазму крови.
На фиг.7 показано влияние фитостеринов, процианидинов какао и их комбинации на окислительное повреждение ДНК.
На фиг.8 показано влияние фитостеринов, процианидинов какао и их комбинации на окислительное повреждение липидов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Все патенты, патентные заявки и справки, процитированные в данной заявке, включены в текст посредством ссылки. В случае какого-либо несоответствия в настоящем описании оно урегулировано.
Настоящее изобретение относится к композиции, содержащей полифенол какао в комбинации с холестеринснижающим реагентом, например холестеринснижающим реагентом на основе стерина и/или станола, причем композицию применяют для улучшения или поддержания здорового состояния сосудистой системы у млекопитающего. Необязательно, композиция может содержать L-аргинин, кальций, калий, магний, витамин Е, витамин С, любой из витаминов комплекса В, каротиноид, гуаровую смолу или моно- или полиненасыщенную жирную кислоту (например, омега-3 жирную кислоту). Композиции, содержащие полифенолы из других источников, которые обладают свойствами, подобными свойствам полифенолов из какао, также могут быть использованы в композициях и способах согласно изобретению в комбинации с холестеринснижающими реагентами, например холестеринснижающими реагентами на основе стерина и/или станола, и они также находятся в объеме притязаний изобретения.
Употребляемый в данном тексте термин «полифенол какао» (СР) относится к полифенольному веществу, включая проантоцианидин, особенно процианидин, присутствующий в бобах какао или экстрагированный из бобов какао или ингредиентов из какао. Термин «процианидин» включает в себя как мономеры, так и олигомеры катехина и эпикатехина. Следует учесть, что любая употребляемая в данном тексте ссылка на полифенол из какао также применима к процианидину из какао. Термин "ингредиент какао" относится к материалу из какао, содержащему твердые вещества, полученному из освобожденных от оболочек плодов какао, такому как шоколадная жидкая масса и частично или полностью обезжиренное твердое вещество какао (например, брикет или порошок). Фраза «холестеринснижающий реагент» означает любое соединение, комбинацию соединений, экстракт или растительный компонент, природного происхождения или синтезированный, который обладает способностью снижать уровень холестерина у млекопитающего при введении его в эффективном количестве. Когда таким холестеринснижающим реагентом является соединение или комбинация соединений, т.е. типа стерина или станола, включая производные и изомерные формы, холестеринснижающий реагент называют «холестеринснижающий реагент на основе стерина и/или станола». Когда фразу употребляют при ссылке на композицию, например, "холестеринснижающий темный шоколад", то это означает, что композиция обладает способностью снижать уровень холестерина. Как можно понять специалисту в данной области, что употребляемый в тексте термин «сосудистый» относится ко всей сосудистой системе, т.е. он охватывает сердце, и термин «здоровое состояние сосудистой системы» включает в себя здоровое состояние сердечно-сосудистой системы и/или здоровое состояние коронарных сосудов. «Поддержание здорового состояния сосудов» относится к достижению благоприятных результатов в отношении состояния сосудов, описанных в данном тексте.
Полифенолы какао могут быть природного происхождения, т.е. получены из бобов какао, или синтезированы. Специалист в данной области может выбирать природный или синтетический полифенол какао на основании доступности или стоимости. Полифенолы какао могут быть включены в композицию в качестве ингредиента какао, содержащего полифенолы какао, например шоколадной, жидкой массы в шоколаде, или могут быть добавлены независимо от ингредиентов из какао, например, в виде экстракта, фракции экстракта, объединенных фракций экстракта или в виде синтезированного соединения. Полифенолы какао включают в себя процианидины какао, которые представляют собой мономеры и/или олигомеры эпикатехина и катехина. Мономеры процианидина включают в себя (+)-катехин, (-)-эпикатехин и их соответствующие эпимеры (например, (-)-катехин и (+) -эпикатехин) и имеют структуру
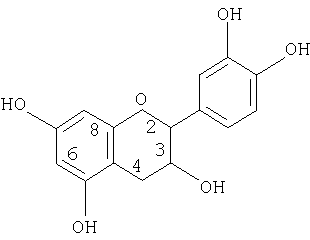
Олигомеры процианидина могут иметь от 2 до приблизительно 18, предпочтительно от 2 до приблизительно 12 и самое предпочтительное от 2 до приблизительно 10, мономерных единиц. Например, олигомеры могут быть димерами, тримерами, тетрамерами, пентамерами, гексамерами, септамерами, октамерами, нонамерами и декамерами. В олигомере мономеры соединены посредством межфлавановых связей (4→6) и/или (4→8). Олигомеры с исключительно (4→8) связями являются линейными, в то время как присутствие, по крайней мере, одной (4→6) связи приводит к разветвленному олигомеру.
Полифенол какао может быть получен путем экстракции из бобов какао, плодов какао (очищенных от шелухи) или ингредиентов какао, таких как шоколадная жидкая масса, частично обезжиренные твердые частицы из какао и/или полностью обезжиренные твердые вещества какао. Предпочтительно, экстракт получают из полностью или частично обезжиренного порошка какао. Бобы из любых видов Theobroma, Herrania или из их межвидовых или внутривидовых скрещиваний могут быть использованы. Экстракт может быть получен из ферментированных, неполностью ферментированных или неферментированных бобов, ферментированных бобов с наименьшим содержанием полифенолов какао и не ферментированных с наибольшим количеством полифенолов. Выбор бобов может быть сделан на основе фактора ферментации бобов, например, экстракт может быть получен из бобов с фактором ферментации 275 или меньше. Оптимизация уровня полифенолов в ингредиенте какао и его экстракте может быть сделана путем регуляции степени ферментации, как это описано в международной заявке № PCT/US97/15893, опубликованной как международная патентная заявка WO 98/09533, соответствующие части которой включены в данный текст в виде ссылки.
Полифенолы какао можно экстрагировать из ингредиентов какао, которые были получены традиционными способами обработки какао (описанными, например, в Industrial Chocolate Manufacture and Use, ed. Beckett, S.T., Blackie Acad. & Professional, New York, 1997, в разделах 1, 5 и 6) или улучшенным способом обработки, описанным в патенте США № 6015913 на имя Kealey et al., с помощью которого сохраняются полифенолы (путем предотвращения их деструкции) в ингредиентах какао по сравнению с традиционными способами. Улучшенный способ обработки какао исключает традиционную стадию обжаривания. Таким образом, могут быть использованы ингредиенты какао, получаемые путем (а) нагревания бобов какао в течение времени и при температуре, достаточными для освобождения от какаовеллы без обжаривания зерен какао; (b) отделения зерен какао от какаовеллы веянием; (с) отжима зерен какао с помощью винтового пресса и (d) извлечения масла какао и частично обезжиренных твердых частиц, которые содержат полифенолы какао на сохраненном уровне. Указанный способ позволяет сохранять уровень высших олигомеров процианидина намного выше, чем традиционный способ. Полученные указанным способом твердые частицы какао могут содержать больше чем 20000 мкг всех процианидинов на грамм необезжиренных твердых частиц, предпочтительно более чем 25000 мкг/г, более предпочтительно выше чем 28000 мкг/г и наиболее предпочтительное выше чем 30000 мкг/г. Для целей настоящего изобретения общее количество процианидина определяют, как описано в примере 3.
Полифенолы какао можно экстрагировать из указанных выше источников, используя растворители, в которых полифенолы растворяются. Подходящие растворители включают в себя воду или органический растворитель, такой как метанол, этанол, ацетон, изопропиловый спирт и этилацетат. Также можно использовать смеси растворителей. Когда воду используют в качестве растворителя, то предпочтительно, чтобы она была слегка подкислена, например, уксусной кислотой. Предпочтительными растворителями являются смеси воды и органического растворителя, например водный метанол, этанол или ацетон. Водноорганические растворители могут содержать, например, приблизительно от 50% до 95% органического растворителя. Таким образом, может быть использован 50%, 60%, 70%, 80% и 90%-ный органический растворитель в воде. Кроме того, растворитель может содержать небольшое количество кислоты, такой как уксусная кислота, например, в количестве приблизительно от 0,5% до 1,0%. Композиция из экстрактов, т.е. представительность (т.е. профиль олигомеров) и количество олигомеров процианидина, будет зависеть от выбора растворителей. Например, водный экстракт содержит главным образом мономеры, этилацетатный экстракт содержит мономеры и низшие олигомеры, в основном, димеры и тримеры, и воднометанольный, водноэтанольный и водноацетоновый экстракт содержит мономеры и ряд высокомолекулярных олигомеров. Одним из предпочтительных растворителей для экстракции мономера, а также высокомолекулярных олигомеров является 70%-ный ацетон. Однако в изобретении применяют любой экстракт, содержащий полифенолы. Способы экстракции полифенола какао известны в данной области и описаны, например, в патенте США № 5554645 на имя Romanczyk et al. и в международной заявке № PCT/US97/05693, опубликованной как международная патентная заявка WO 97/36497. Таким образом, в одном аспекте, экстракт какао получают путем измельчения бобов какао до порошка какао, обезжиривания порошка, экстрагирования полифенолов какао и очистки экстракта. Порошок какао можно получить путем сублимационной сушки бобов какао и пульпы, дробления пульпы и лущения бобов какао, высушенных сублимационно, и измельчения лущеных бобов.
Экстракт полифенолов какао можно очистить, например, путем удаления кофеина и/или теобромина и далее очисткой с помощью гель-фильтрации и/или высокоэффективной жидкостной хроматографии (ВЭЖХ). Гель-фильтрацию (например, на Сефадексе LH-20) можно использовать для обогащения экстракта высшими олигомерами процианидина. Например, элюат, содержащий мономеры и низшие олигомеры, можно не собирать до тех пор, пока с колонки не начнет элюироваться выбранный олигомер (олигомеры). Пример такого экстракта известен в данной области и описан в примере 5 международной заявки № PCT/US97/05693, опубликованной как международная патентная заявка WO 97/36497, соответствующие разделы которой включены в данный текст в виде ссылки. С помощью препаративной ВЭЖХ, например нормально-фазовой ВЭЖХ, экстракт можно фракционировать, например, на фракции мономеров и олигомеров, содержащие, по меньшей мере, 50 мас.% мономера или специфического олигомера (олигомеров). Когда фракции содержат мономеры и низшие олигомеры (вплоть до и включая тетрамер), фракции содержат приблизительно от 90 до 95 мас.% отдельной олигомерной фракции. Желаемые фракции можно объединить после разделения с получением комбинации олигомеров по выбору, например, с содержанием олигомеров 3-10 или 5-10. Специалист в данной области может регулировать условия хроматографии для достижения желаемого профиля процианидинов с учетом указаний, описанных в данном тексте, знаний в данной области и, например, руководств, описанных в патенте США № 5554645 заявителем Romanczyk et al., и в международной заявке № PCT/US97/05693, опубликованной как международная патентная заявка WO 97/36497.
Полифенол какао может быть представлен в композиции согласно изобретению путем включения ингредиентов какао, содержащих полифенолы, или путем включения шоколада, который может быть молочным, сладким и полусладким, и предпочтительным является темный шоколад и шоколад с низким содержанием жира. Ингредиенты какао могут быть получены традиционными способами обработки какао, но предпочтительным является способ, описанный в патенте США № 6015913 заявителем Kealey et al. В качестве альтернативы, для повышения уровня полифенолов какао может быть использована шоколадная, жидкая масса и твердые частицы какао, полученные из бобов какао с фактором ферментации 275 или менее. Указанные ингредиенты имеют такое содержание полифенола какао, которое выше, чем содержание полифенола, полученного при использовании традиционных способов обработки какао (например, с обжариванием) и из полностью ферментированных бобов. Шоколад может быть получен обычными методами из описанных выше ингредиентов и улучшенным способом для сохранения полифенолов какао при изготовлении шоколада, как описано в международной заявке № PCT/US99/05414, опубликованной как международная патентная заявка WO 99/45788, соответствующие разделы которой включены в данный текст в виде ссылки. Шоколад, полученный, по крайней мере, одним из следующих нетрадиционных способов, называют в тексте как «шоколад, содержащий сохраненное количество полифенолов какао»: (i) получение ингредиентов какао из не полностью ферментированных или неферментированных бобов какао; (ii) сохранение полифенола какао при способе промышленного производства ингредиента какао и (iii) сохранение полифенола какао при способе промышленного производства шоколада.
Также могут быть использованы синтетические процианидины, и их получают способами, известными в данной области и описанными, например, в международной заявке № PCT/US98/21392, опубликованной как международная патентная заявка WO 99/19319, соответствующие разделы которой включены в данный текст в виде ссылки. Также могут быть использованы производные полифенола какао. Указанные производные включают в себя галлатированные мономеры и олигомеры, гликозилированные мономеры и олигомеры и их смеси; метаболиты мономеров и олигомеров процианидина, такие как сульфированные, глюкуронидированные и метилированные формы, и продукты ферментативного расщепления процианидинов, образованные в процессе метаболизма микрофлоры кишечника или в результате обменных процессов в организме млекопитающего. Производные могут быть получены из природных источников или синтезированы.
Кроме того, композиция содержит холестеринснижающий реагент. Любой холестеринснижающий реагент может быть использован независимо от его способа действия. Подходящие реагенты могут воздействовать путем снижения поглощения холестерина в желчь млекопитающего или путем снижения синтеза холестерина. Примерами подходящих реагентов являются фитостерины, фитостанолы и их производные и изомеры; соевый белок; растворимые волокна, например бета-глюкан из, например, овса и псилиума, орехов, масла из рисовых отрубей, каждый из которых является особенно подходящим для включения в композиции на основе пищевого продукта, дополнения к рациону и пищевой добавки. Также могут быть использованы известные лекарственные средства, снижающие уровень холестерина, но они являются менее предпочтительными для включения в пищевые композиции и композиции с пищевыми добавками, однако они могут быть использованы в фармацевтической промышленности. Специалисту в данной области будет очевидно, что выбор холестеринснижающего реагента зависит от предполагаемого средства доставки (например, пищевой продукт, добавка, фармацевтический препарат) и способа введения. Таким образом, реагент, который снижает всасывание холестерина в желчь, не является предпочтительным для внутривенного введения. Аналогично, если средством доставки является пищевой продукт, холестеринснижающий реагент с резким вкусом и запахом не может быть желаемым.
Фитостерины являются растительными стеринами, которые не растворяются в воде и имеют молекулярный вес и структуру, подобные холестерину. Фитостерин снижает степень всасывания холестерина в желчь (как эндогенного, так и холестерина из пищи), а также уровни холестерина в сыворотке (общего или LDL) без его поглощения. Свыше сорока растительных стеринов идентифицировано, но бета-ситостерин, кампестерин и стигмастерин являются самыми распространенными. Другими примерами полезных стеринов являются брассикастерин, десмостерин, чалиностерин, пориферастерин, клионастерин. Индивидуальные стерины или смеси стеринов, выделенные из природных источников или синтезированные, и изомеры и их производные могут быть использованы. Особенно пригодными являются насыщенные производные стеринов, известные как станолы, у которых все углерод-углеродные связи в кольцах являются насыщенными. Подходящие для использования станолы имеют 28 или 29 атомов углерода и включают в себя бета-ситостанол, клионастанол, 22,23-дигидробрассикастанол и кампестанол. Фитостерины могут быть в твердом (например, порошок, гранулы) или жидком (например, масло) состоянии.
Стерины и станолы обнаружены в некоторых растительных материалах, как описано, например, в международной заявке № РСТ/ЕР96/02344. Примерами источников стеринов/станолов являются кора сосны, соевое масло, талловое масло, экстракт из побегов бамбука (описаны в международной заявке № PCT/US98/12556, опубликованной как международная патентная заявка WO 98/57545), оболочки какао и масло какао, и масло рисовых отрубей. Талловое масло, побочный продукт целлюлозной и бумажной промышленности, является хорошим источником станола, т.е. бета-станола.
Растительный стерин может быть получен из природных источников, таких как растительные масла, осадок растительного масла, дистилляты растительного масла и другие источники растительного масла, такие как талловое масло, с помощью относительно простых и недорогих способов. Например, получение стеринов из осадка растительного масла с помощью растворителей, таких как метанол, описано в патенте США № 4420427 заявителем Hamunen. Станолы обнаружены в небольших количествах в природных источниках, но легко могут быть получены из стеринов гидрированием стеринов любым из нескольких способов, известных специалистам в данной области. Когда исходный стериновый материал получают из растительного материала, он содержит смесь нескольких различных стеринов, таким образом, после гидрирования образовавшийся станол будет также представлять собой смесь различных станолов. Указанные смеси являются подходящими для их использования в настоящем изобретении. Однако чистые специальные препараты стерина могут быть также гидрированы для получения чистых станолов, которые также могут быть использованы.
Масло какао, экстрагированное из оболочек какао, является хорошим источником фитостерина. Фитостерины какао представляют собой смесь свободных и связанных стеринов, причем содержание свободных стеринов составляет вплоть до приблизительно 90% от присутствующих фитостеринов. Фитостерины включают в себя кампестерин, β-ситостерин, стигмастерин, циклоартеноил, 24-метиленциклоартеноил, а также минорные количества других фитостеринов. Связанные фитостерины включают в себя сложные эфиры жирных кислот или ферулатные производные фитостеринов. Масло какао также содержит токолы, которые включают в себя токоферолы (которые обладают антиоксидантными свойствами) и токотриенолы (которые могут обладать холестеринснижающей способностью). Масло какао получают способом, который включает в себя стадии: (i) измельчение оболочек какао; (ii) экстрагирование измельченных оболочек какао растворителем для фитостеринов; (iii) удаление растворителя, и (iv) извлечение масла какао. Оболочки какао, представляющие собой побочный продукт при обжаривании бобов какао, могут быть получены из высушенных ферментированных бобов какао, тонкоизмельченных бобов какао, обжаренных бобов какао и предпочтительно из высушенных неферментированных бобов, которые имеют самое высокое содержание всех стеринов. Предпочтительными бобами какао являются бобы из вида Theobroma cacao. Предпочтительными растворителями являются петролейный эфир, гексан, пентан и этилацетат. Растворитель может быть удален вакуумной дистилляцией. В одном аспекте высушенные при температуре ниже 0°С оболочки измельчают до тонкого порошка с помощью устройства Tekmat Mill (Cincinatti, ОН) и измельченную массу подвергают экстрагированию в течение ночи дважды перегнанным петролейным эфиром (точка кипения 38-39,6°С) в аппарате Сокслета (Fisher Scientific, Springfield, NJ). На следующее утро растворитель осторожно удаляют путем медленного выпаривания в токе азота и полученный экстракт хранят при -40°С. Затем фитостерины могут быть очищены препаративной ВЭЖХ или колоночной хроматографией.
Этерифицированные формы как стеринов, так и станолов могут быть использованы. Этерификация стеринов/станолов приводит к лучшему растворению в жирах и маслах, что может, в некоторых случаях, помочь их включению в пищевые продукты или другие средства доставки. Например, стерины могут быть этерифицированы сложными эфирами жирных кислот. Примеры таких этерифицированных стеринов включают в себя ситостерина ацетат, ситостерина олеат и стигмастерина олеат. Сложные эфиры станола могут быть получены способами, известными в данной области, и, например, описаны в патенте США № 6031118 заявителем van Amerongen et al, в патенте США № 5892068 заявителем Higgins, в патенте США № 5502045 заявителем Miettenen et al и в международной заявке № РСТ/СА99/00655 (опубликованной как международная патентная заявка WO 00/04887). В одном аспекте применяемые сложные эфиры станола получают путем этерификации, по крайней мере, одного стерина с помощью сложного эфира С2-С22 жирной кислоты, как описано в патенте США № 5958913 заявителем Miettenen et al. Другие способы, известные в данной области, могут быть использованы для увеличения растворимости стеринов/станолов при введении млекопитающему. Один такой способ описан в патенте США № 5932562 заявителем Ostlund, в котором стерин/станол смешивают с лецитином с получением водорастворимого порошка.
Стерины/станолы могут быть добавлены к композиции в виде порошка путем перемешивания с другими ингредиентами. В случае пищевой композиции стерины/станолы, а также другие холестеринснижающие реагенты подходящим образом добавляют на стадии смешивания. В процессе приготовления холестеринснижающего шоколада, например, стерины/станолы могут быть добавлены к сухой смеси, содержащей сахар, мягкое масло, плоды до измельчения или к расплавленному шоколаду, который является менее предпочтительным. Чтобы облегчить перемешивание, стерины/станолы могут быть вначале растворены в солюбилизирующем реагенте, таком как жир, растительное масло, моноглицериды, диглицериды, триглицериды, токоферолы и их смеси. Эффективными носителями для получения суспензий и эмульсий стеринов/станолов являются вода, спирт, полиол, другие пищевые соединения, например шоколадная жидкая масса, в которой стерины/станолы, по крайней мере, частично растворимы, и их смеси.
Соевый белок может быть добавлен к композиции в любом известном виде, например, он может быть в виде выделенного белка сои, белкового концентрата сои, структурированного белка сои или соевой муки, хлопьев и круп. Целое зерно или его фрагмент могут быть использованы, как описано, например, в примере 5. Различные виды соевого белка хорошо известны в данной области и являются коммерчески доступными. Свойства соевого белка и способы его получения описаны, например, в публикации Soy Protein and Human Nutrition, Wilcke et al., eds., Acad. Press, NY, 1979. Соевый белок может быть использован в комбинации с любым холестеринснижающим реагентом на основе стерина и/или станола.
Растворимые волокна растения, например бета-глюкан, проявляют способность снижать уровень холестерина плазмы. Волокна для применения в настоящем изобретении могут быть получены из любого источника бета-глюкана, предпочтительно из зерен овса и овсяных отрубей. Волокна могут быть получены и добавлены к композиции способами, известными в данной области. Особенно они являются подходящими для композиций, доставляемых пероральным путем, таких как пищевые продукты и дополнения к рациону. Бета-глюкан и другие растворимые растительные волокна могут быть использованы в комбинации с любым холестеринснижающим реагентом, основанным на стерине и/или станоле.
Композиция согласно изобретению также может содержать L-аргинин, который может присутствовать в композиции согласно изобретению в различном виде, например в виде очищенного соединения, экстракта из L-аргининсодержащего растения или в качестве ингредиента семени/ореха, например ореховой муки, или в качестве цельного семени/ореха. Любой источник L-аргинина может быть использован, синтетический или природный. Предпочтительными источниками L-аргинина являются соевые бобы и ядра орехов, таких как земляные орехи, грецкие орехи, миндальные орехи и лесные орехи. Могут быть использованы обезжиренные или частично обезжиренные ядра орехов. Они могут быть измельчены и называются ореховой мукой.
Композиция может также содержать кальций, калий, магний, витамин Е, витамин С и любой из витаминов комплекса В, каротиноид, гуаровую смолу или моно- или полиненасыщенную жирную кислоту (например, омега-3 жирную кислоту), которая может быть получена способами, известными в данной области. Моно- или полиненасыщенные жирные кислоты могут быть применены как оливковое масло, рыбий жир или орех. Подходящими для такого применения примерами орехов являются земляные орехи, миндальные орехи и грецкие орехи.
Также в сфере изобретения находится композиция, содержащая полифенол, который проявляет, по крайней мере, одно из следующих свойств: снижение тонуса сосудов (релаксации), ингибирование активности СОХ, ингибирование активности LOX, ингибирование окисления LDL, увеличение активности NOS, повышение уровня NO, ингибирование агрегации тромбоцитов, адгезии моноцитов и пролиферации гладкомышечных клеток сосудов, снижение кровяного давления, снижение тромбоза и регуляция окислительного стресса, а также холестеринснижающий реагент. Любой холестеринснижающий реагент, например, холестеринснижающий реагент на основе стерина и/или станола может быть использован. В такой композиции холестеринснижающий реагент на основе стерина и/или станола усиливает биодоступность полифенола. Примерами таких полифенолов являются флаванолы (например, катехин, эпикатехин и их галлатированные производные), флавонол (например, кверцетин, кемпсерол, мирицетин и их гликозилированные производные) и процианидины (например, димер процианидина, который может быть получен из какао).
Композицию изобретения применяют в качестве пищевого продукта, пищевой добавки, дополнения к рациону или фармацевтического препарата. Композиции могут содержать носитель, разбавитель или наполнитель. В зависимости от предназначения, носитель, разбавитель или наполнитель могут быть выбраны таким образом, чтобы быть подходящими для употребления человеком или в ветеринарии в качестве пищи, добавки, дополнения или фармацевтического препарата.
Употребляемый в тексте термин «пищевой продукт» означает материал, состоящий в основном из белка, углевода и/или жира, который употребляется организмом для того, чтобы поддержать процессы роста, восстановления и жизненно важные процессы и поставлять энергию. Пищевые продукты могут также содержать дополнительные вещества, такие как минералы, витамины и приправы. См. Merriam-Webster's Collegiate Dictionary, 10th Edition, 1993. Термин «пищевой продукт» включает в себя напиток, приспособленный для потребления человеком или животным. Употребляемый в тексте термин «пищевая добавка» имеет значение, определенное FDA in 21 C.F.R. 170.3 (е) (1) и включает в себя прямые и непрямые добавки. Употребляемый в тексте термин «фармацевтический препарат» означает лекарственное средство. См. Merriam-Webster's Collegiate Dictionary, 10th Edition, 1993. Фармацевтический препарат может называться лекарственным препаратом. Употребляемый в тексте термин «дополнение к рациону» означает продукт (отличный от табака), который предназначен для пополнения рациона, который вносит или содержит один или более пищевых ингредиентов: витамин, минерал, растение или другой ботанический материал, аминокислоту, диетическое вещество для употребления человеком, чтобы дополнить рацион путем увеличения общего ежедневного потребления, или концентрат, метаболит, составную часть, экстракт или комбинацию указанных ингредиентов.
Любой обычный пищевой продукт, включающий любой напиток, который улучшен добавлением холестеринснижающего реагента в комбинации с полифенолом, таким как полифенол какао, или его производным, и необязательно в комбинации с L-аргинином, кальцием, калием, магнием, витамином Е, витамином С, любым из витаминов комплекса В, каротиноидом, гуаровой смолой и/или моно- или полиненасыщенной жирной кислотой (например, омега-3), находится в сфере изобретения.
В случае полифенола какао, улучшение достигается либо (i) путем добавления полифенола какао или его производного к пищевому продукту, который не содержит полифенола какао, либо (ii) когда пищевой продукт традиционно содержит полифенолы какао, такой как, например, шоколад, то улучшение достигается путем увеличения уровня полифенола выше того уровня, который находится в пищевом продукте, приготовленном традиционным образом. Указанное увеличение уровня полифенола может быть достигнуто путем добавления дополнительных полифенолов какао, например, в виде экстракта; путем добавления полифенола какао в комбинации с другим полифенолсодержащим ингредиентом (например, кожура ореха); путем регулирования способа обработки ингредиентов какао и выбора бобов какао, как описано выше, чтобы сохранить полифенол какао в ингредиенте какао, употребляемом в производстве пищевого продукта, или путем регулирования способа промышленного производства шоколада, как описано выше. Таким образом, указанные пищевые продукты (включая напитки) содержат «повышенный уровень полифенолов» (включая процианидины какао) по сравнению со сравниваемыми обычными пищевыми продуктами (включая напитки). Пример шоколада с повышенным уровнем полифенолов имеет место, когда производитель шоколада добавляет экстракт какао, содержащий полифенолы какао, к ранее производимому коммерчески доступному продукту. Пищевые продукты также могут называться как «пищевые продукты с высоким содержанием полифенолов какао», т.е. они содержат более высокие уровни полифенола, чем их традиционные аналоги.
Пищевые продукты, содержащие полифенолы какао и, по крайней мере, один холестеринснижающий реагент (например, холестеринснижающий реагент на основе стерина и/или станола), и необязательно L-аргинин, кальций, калий, магний, витамин Е, витамин С, любой из витаминов комплекса В, каротиноид, гуаровую смолу или моно- или полиненасыщенную жирную кислоту (например, омега-3), могут быть приспособлены для употребления человеком или в ветеринарии и включать в себя пищевые продукты для домашнего животного. Пищевые продукты могут отличаться от кондитерских изделий, однако предпочтительным холестеринснижающим пищевым продуктом является кондитерское изделие, такое как стандартный (SOI) и нестандартный SOI шоколад, такой как молочный, сладкий и полусладкий шоколад, включая темный шоколад, шоколад с низким содержанием жира и конфета, которая может быть конфетой, покрытой шоколадом. Другие примеры включают в себя выпеченный продукт (например, шоколадное пирожное с орехами, выпеченная закуска, булочка, крекер), приправу, батончик из гранолы, жевательную ириску, батончик из мучного заменителя, пастообразные изделия, сироп, порошковую смесь для приготовления напитка, какао или шоколадный ароматизированный напиток, пудинг, рисовую лепешку, рисовую смесь, соус для придания вкуса и тому подобное. Если желательно, пищевые продукты на основе шоколада или какао могут быть ароматизированы. Предпочтительными пищевыми продуктами, которые содержат L-аргинин, кроме полифенола какао и холестеринснижающего реагента, являются шоколад и конфеты, такие как батончики из гранолы, содержащие орехи, например земляные орехи, грецкие орехи, миндальные орехи и лесные орехи. Следует отметить, что добавление орехов с оболочками к пище, описанной в данном тексте, также может повысить общее содержание полифенола, поскольку, например, оболочки земляного ореха содержат приблизительно 17% процианидинов, а оболочки миндального ореха содержат приблизительно 30% процианидинов. В одном аспекте оболочки орехов добавляют к нуге шоколадных конфет, содержащих холестеринснижающий реагент.
В предпочтительных аспектах нешоколадные пищевые продукты, содержащие холестеринснижающий реагент, включают в себя, по крайней мере, приблизительно от 5 мкг/г до приблизительно 10 мг/г и, например, по крайней мере, 5 мкг/г пищевого продукта, предпочтительно, по крайней мере, 10 мкг, более предпочтительно, по крайней мере, 100 мкг/г процианидинов какао. Если желательно, то нешоколадные пищевые продукты могут содержать уровни процианидинов какао намного выше уровней, имеющихся в шоколадных пищевых продуктах, описанных ниже.
Особенно предпочтительным пищевым продуктом является холестеринснижающий кондитерский шоколад, и самым предпочтительным является темный шоколад. В некоторых аспектах шоколад содержит, по крайней мере, 3600 мкг, предпочтительно, по крайней мере, 4000 мкг, предпочтительно, по крайней мере, 4500 мкг, более предпочтительно, по крайней мере, 5000 мкг и самое предпочтительное, по крайней мере, 5500 мкг процианидинов какао на грамм шоколада, на основании общего количества нежирных твердых компонентов какао в продукте. В другом варианте шоколад содержит, по крайней мере, 6000 мкг, предпочтительно, по меньшей мере, 6500 мкг, более предпочтительно, по крайней мере, 7000 мкг и наиболее предпочтительно 8000 мкг процианидов какао на грамм, и даже более предпочтительнее 10000 мкг, на основании общего количества нежирных твердых компонентов какао в продукте.
Холестеринснижающий кондитерский молочный шоколад может содержать, по крайней мере, 1000 мкг, предпочтительно, по крайней мере, 1250 мкг, более предпочтительно, по крайней мере, 1500 мкг и самое предпочтительное, по крайней мере, 2000 мкг процианидинов какао на грамм, на основании общего количества нежирных твердых компонентов какао в молочном шоколадном продукте. В предпочтительном аспекте молочный шоколад содержит, по крайней мере, 2500 мкг, предпочтительно, по крайней мере, 3000 мкг, более предпочтительно, по крайней мере, 4000 мкг и самое предпочтительное, по крайней мере, 5000 мкг процианидинов какао на грамм, на основании общего количества нежирных твердых компонентов какао в молочном шоколадном продукте.
Количество L-аргинина в пищевых продуктах может варьировать. Обычно, какао содержит между 1 и 1,1 граммами L-аргинина на 100 граммов частично обезжиренных твердых компонентов какао. Количество может колебаться от 0,8 до 1,5 на 100 граммов какао. Шоколадные пищевые продукты согласно изобретению содержат L-аргинин в количестве, которое является выше того количества, которое имеется в природе в ингредиентах какао. Зная количество ингредиентов какао и L-аргинина, используемое в пищевом продукте, специалист в данной области сможет легко определить общее количество L-аргинина в конечном продукте. Пищевой продукт будет содержать, как правило, по крайней мере, 5 мкг/г, предпочтительно, по крайней мере, 30 мкг/г или, по крайней мере, 60 мкг/г, даже более предпочтительно, по крайней мере, 200 мкг/г пищевого продукта.
Количество холестеринснижающего реагента в пищевом продукте будет зависеть от типа применяемого реагента и может быть определено специалистом в данной области на основании данных в описании рекомендаций, в частности на основании ежедневных дозировок, приведенных ниже, и знаний в данной области. Пищевая композиция может содержать, например, приблизительно от 0,5 до приблизительно 10 г на 45 г порции, предпочтительно приблизительно от 1,5 до приблизительно 5 г на 45 г порции, самое предпочтительное приблизительно от 2 до приблизительно 4,5 г на 45 г порции стеринов/станолов. Что касается соевого белка и растворимого волокна из овса, то FDA рекомендует минимальные количества на порцию пищи. Согласно FDA содержащая бета-глюкан порция пищи должна включать в себя, по крайней мере, 0,75 г бета-глюкана, и порция пищи, содержащая соевый белок, должна включать в себя, по крайней мере, 6,25 г соевого белка. Указанные величины могут быть использованы как руководство для определения количества холестеринснижающих реагентов в пище.
В одном предпочтительном аспекте ежедневное, эффективное количество холестеринснижающего реагента и полифенола какао заложено в одной порции. Таким образом, холестеринснижающее кондитерское изделие (например, шоколад) содержит, по крайней мере, 1,5 г (например, 1,5-4,5 г) стерина/станола на порцию и, по крайней мере, 100 мг/порцию приблизительно (например, 150-200, 200-400 мг) процианидинов какао.
Фармацевтические препараты, содержащие полифенолы, имеющие перечисленные в данном тексте свойства (например, полифенолы какао или их производные), в комбинации с холестеринснижающим реагентом и, необязательно, L-аргинином могут быть введены различными путями, такими как пероральный, трансбуккальный, назальный, ректальный, внутривенный, парентеральный и местный. Специалист в данной области способен определить подходящий холестеринснижающий реагент в зависимости от способа введения. Таким образом, дозированные формы, приспособленные для каждого способа введения, находятся в сфере изобретения и включают твердые, жидкие и полутвердые дозированные формы, такие как таблетки, капсулы, желатиновые капсулы (гелькапы), массу доз или однократную дозу порошков или гранул, эмульсии, суспензии, пасты, кремы, гели, пены или желе. Дозированные формы с пролонгированным действием также находятся в сфере изобретения и могут быть получены, как описано в патентах США № 5024843; 5091190; 5082668; 4612008 и 4327725, соответствующие разделы которых включены в данный текст в виде ссылки. Подходящие фармацевтически приемлемые носители, разбавители или наполнители обычно известны в данной области и могут быть легко определены специалистом в данной области. Таблетка, например, может включать в себя эффективное количество композиции, содержащей полифенол какао, и необязательно носитель, такой как сорбит, лактоза, целлюлоза или дикальция фосфат. Добавка к рациону, содержащая полифенолы какао, по крайней мере, один холестеринснижающий реагент и, необязательно, L-аргинин, может быть получена способами, известными в данной области, и может включать в себя, например, питательное вещество, такое как дикальция фосфат, магния стеарат, кальция нитрат, витамины и минералы.
Кроме того, в сфере изобретения находится упаковка, содержащая пищевой продукт, дополнение к рациону или фармацевтический препарат, и этикетку, указывающую на (i) присутствие или повышенное содержание полифенолов и/или их производных и (ii) присутствие холестеринснижающего реагента. Необязательно, этикетка может указывать на содержание L-аргинина, благоприятное действие комбинации полифенола (полифенолов), холестеринснижающего реагента (реагентов) и, необязательно, L-аргинина и содержать инструкции для употребления. Как употребляют в данном тексте, благоприятное действие включает в себя снижение холестерина плазмы, общего и LDL, ингибирование активности СОХ (включая активность СОХ 1), ингибирование активности LOX, усиление синтеза оксида азота, увеличение отношения атеростатических факторов к атерогенным факторам (например, продуцированные эйкозаноид и эндотелины) и ингибирование окисления LDL, что в свою очередь, индивидуально или в комбинации, способствует уменьшению вазоконстрикции и агрегации тромбоцитов, ингибированию адгезии моноцитов, ингибированию избыточной пролиферации гладкомышечных клеток сосудов, уменьшению тромбоза, снижению кровяного давления и, таким образом, снижению риска, связанного с сосудистыми и сердечно-сосудистыми заболеваниями, такими как атеросклероз и сердечно-сосудистое заболевание.
Также в сфере изобретения находится упаковка, включающая (i) композицию, содержащую полифенол, который проявляет, по крайней мере, одно из следующих свойств: индукцию расширения сосудов, ингибирование активности СОХ, ингибирование активности LOX, ингибирование окисления LDL, увеличение активности NOS, повышение уровня NO, ингибирование агрегации тромбоцитов, адгезии моноцитов и пролиферации гладкомышечных клеток сосудов, снижение кровяного давления, уменьшение тромбоза и регуляцию окислительного стресса, и холестеринснижающий реагент, например холестеринснижающий реагент на основе стерина и/или станола; и (ii) этикетку и/или инструкции для применения композиции для поддержания сосудов в здоровом состоянии (термин здоровье сердечно-сосудистой системы также может быть использован) и/или снижения риска сердечного заболевания. Когда используют холестеринснижающий реагент на основе стерина и/или станола, этикетка и/или инструкции могут указывать, что композиция сохраняет или усиливает всасывание полифенола. Этикетка и/или инструкции также могут указывать на другие благоприятные свойства, упомянутые выше. Указанными свойствами являются снижение уровня холестерина плазмы, общего и LDL, ингибирование активности СОХ, ингибирование активности LOX, увеличение синтеза оксида азота, увеличение отношения атеростатических факторов к атерогенным факторам (например, продуцированные эйкозаноид и эндотелины) и ингибирование окисления LDL, что в свою очередь, индивидуально или в комбинации, способствует уменьшению вазоконстрикции и агрегации тромбоцитов, ингибированию адгезии моноцитов, ингибированию избыточной пролиферации гладкомышечных клеток сосудов, уменьшению тромбоза, снижению кровяного давления и, таким образом, снижению риска, связанного с сосудистыми и сердечно-сосудистыми заболеваниями, такими как атеросклероз и сердечно-сосудистое заболевание.
Также в сфере изобретения находятся способы лечения и/или профилактики заболеваний и/или состояний, ассоциированных с, или модулируемых, активностью СОХ, активностью LOX, синтезом NO, активностью NOS, окислением LDL и повышенным уровнем общего и LDL холестерина плазмы. Применяемый в описании термин «лечение» означает улучшение существующего медицинского состояния, например высокого кровяного давления или атеросклероза, путем влияния на патологию заболевания или симптомы, связанные с заболеванием. Термин «профилактика» означает снижение риска, связанного с развитием заболевания, включая ослабление начала заболевания. Предупреждение или профилактику можно применять в отдельном случае при высоком риске развития заболевания у индивидуума или у всего населения для поддержания хорошего здоровья, например поддержания здорового состояния сосудов. Способы могут быть применены для человека или ветеринарного животного, такого как собака, кошка и лошадь.
Заболевания и/или состояния, ассоциированные с, или модулируемые, активностью СОХ, активностью LOX, синтезом NO, активностью NOS, окислением LDL и/или высоким уровнем холестерина, включают в себя атеросклероз, гипертензию, ишемическую болезнь сердца (CHD), цереброваскулярное заболевание, сердечный приступ, удар, заболевание периферических сосудов и почечную недостаточность. Также включенными в сферу изобретения являются способы лечения или профилактики гиперхолестеринемии (включая легкую гиперхолестеринемию), индуцирования снижения тонуса сосудов, ингибирования активности СОХ (включая СОХ 1) и активности LOX, ингибирования окисления LDL, увеличения активности NOS и повышения уровня NO, ингибирования агрегации тромбоцитов, адгезии моноцитов и пролиферации гладкомышечных клеток сосудов, снижения кровяного давления, уменьшения тромбоза и регуляции окислительного стресса.
Способы включают в себя введение млекопитающему, предпочтительно человеку или ветеринарному животному, количества композиции, содержащей полифенол, например полифенол какао, и холестеринснижающий реагент, и, необязательно, L-аргинин, эффективного для лечения, профилактики или достижения, по крайней мере, одного из вышеупомянутых благотворных эффектов, в дополнении к снижению уровня холестерина. Кроме того, способы могут включать в себя определение эффективности лечения, например, путем определения уровней холестерина плазмы.
Композиция может быть введена здоровому млекопитающему с целью профилактики или млекопитающему, нуждающемуся в лечении или имеющему, по крайней мере, один из факторов риска заболевания. Любой индивидуум, имеющий, по крайней мере, один из факторов риска, связанных с проблемами здоровья сосудов, является объектом введения композиций, описанных в данном тексте. Индивидуумы с семейным анамнезом повышенных уровней холестерина, женщины в предклимактерическом или постклимактерическом периоде, женщины в постклимактерическом периоде с постишемическим повреждением миокарда, женщины с недостатком эстрогена, вызванным хирургическим или химическим вмешательством, старые люди, индивидуумы с гипергликемией, диабетом, гипертензией и ожирением и курильщики сигарет являются все чувствительными индивидуумами, нуждающимися в лечении, описанном в данном тексте. Другие популяции млекопитающих, которые являются чувствительными к возникновению проблем, связанных с состоянием сосудов, будут очевидны специалисту в данной области.
Указанные способы являются особенно пригодными для лечения или профилактики рестеноза. Каждый год около 330000 больных в Соединенных Штатах подвергаются ангиопластике на коронарных и/или периферических сосудах (Marx, 265 Science 320, 1994), операции, которая способствует расширению кровеносных сосудов, например коронарных артерий, забитых атеросклеротическими бляшками, для восстановления нормального кровотока. Приблизительно у 33% из таких больных, однако, развивается рестеноз, т.е. вылеченные артерии вновь быстро забиваются бляшками. Такие больные не поправляются и иногда чувствуют себя хуже, чем до ангиопластики. Повышенная пролиферация гладкомышечных клеток (SMCs) в стенках кровеносных сосудов вносит вклад в рестеноз. Таким образом, композиции, содержащие полифенол какао и холестеринснижающий реагент (и, необязательно, L-аргинин), могут быть введены до ангиопластики или вскоре после операции, что может определить опытный врач-практик.
Ветеринарным животным, например собакам, кошкам и лошадям, могут быть введены описанные выше композиции для лечения или профилактики сердечной недостаточности, вальвулярной дегенерации и хронической почечной недостаточности. Например, композиции согласно изобретению могут быть введены собакам, адресуясь к следующим состояниям: хроническому вальвулярному заболеванию (эндокардиоз или миксоматозная дегенерация атриовентрикулярных клапанов), дилатационной кардиомиопатии, перикардиальному заболеванию, эндокардиту, первичной аритмии и заболеванию сердца, вызванному нематозами.
Способ повышения всасывания полифенола в кровь человека или ветеринарного животного (например, домашнее животное) также описан. Способ, с помощью которого, в сущности, повышается биодоступность полифенолов, являющихся благотворными для здоровья человека или животного, включает в себя введение человеку или ветеринарному животному, в комбинации, (i) полифенола, проявляющего, по крайней мере, одно из следующих свойств: индуцирование расширения сосудов, ингибирование активности СОХ, ингибирование активности LOX, ингибирование окисления LDL, увеличение активности NOS, повышение уровня NO, ингибирование агрегации тромбоцитов, адгезии моноцитов и пролиферации гладкомышечных клеток в стенках сосудов, снижение кровяного давления, уменьшение тромбоза и регулирование окислительного стресса, и (ii) холестеринснижающего реагента на основе стерина и/или станола. Полифенол может быть, например, флаванолом или флавонолом, примеры которых описаны выше. Способ может быть выполнен на практике путем введения полифенола и стерина/станола в качестве компонентов такой композиции или путем раздельного введения.
Эффективное количество может быть определено специалистом в данной области, используя данные в тексте рекомендации и знания в данной области. Например, чтобы достичь эффекта снижения уровня холестерина с помощью стеринов/станолов, следует ввести их в количестве, превышающем количество, находящееся, в среднем, в рационе невегетарианца. Человек на севере Америки обычно потребляет приблизительно 200-400 мг/день. Таким образом, когда фитостерин, такой как ситостерин, применяют для снижения уровней холестерина, то его следует ввести в количестве, по крайней мере, приблизительно 1 г/день, предпочтительно, по крайней мере, приблизительно 3 г/день. Предпочтительно, когда применяют, по крайней мере, приблизительно от 1 г/день, предпочтительно, по крайней мере, приблизительно от 4,5 г/день до приблизительно 20 г/день. Однако количество будет изменяться в зависимости от эффективности фитостерина таким образом, что, если применяют более мощный по действию ситостанол, то эффективное количество может быть снижено приблизительно от одного до трех г/день. Количества можно определить аналитическим методом, описанным в публикациях Roger et al., J. Amer. Oil Chem. Soc, 70(30), 1993 и Carpenter et al., J. Amer. Oil Chem. Soc., 71(8), 1994. Соевый белок может быть введен, например, в количестве, по крайней мере, приблизительно 25 г/день. Кроме того, рекомендации можно найти в Recommended Daily Allowances, 9th ed., National Res. Council/National Acad. Sci., Washington, D.C. Растворимое волокно может быть введено в количестве, например, по крайней мере, 3 г/день. Полифенол какао может быть введен приблизительно от 50 мг/день до приблизительно 1000 мг/день, предпочтительно приблизительно от 100-150 мг/день до приблизительно 900 мг/день и самое предпочтительное приблизительно от 300 мг/день до приблизительно 500 мг/день. Однако установлено, что природные полифенолы, находящиеся в пищевых продуктах и являющиеся нетоксичными, могут быть применены в количествах, превышающих указанное выше количество. L-аргинин может быть введен в количестве приблизительно от 2 г/день до приблизительно 50 г/день, предпочтительно приблизительно от 3 г/день до приблизительно 10 г/день и самое предпочтительное приблизительно от 6 г/день до приблизительно 8 г/день. Также установлено, что природный L-аргинин, находящийся в пищевых продуктах, может быть применен в количествах, превышающих указанное выше количество. Полифенолы обычно можно вводить в количествах, известных в данной области. При определении эффективного количества следует принять во внимание тот факт, что в присутствии стеринов/станолов увеличивается всасывание.
С целью лечения/профилактики введение может продолжаться в виде схемы приема, например, ежедневно, ежемесячно, дважды в месяц, дважды в год, ежегодно или в виде другой схемы, для проведения которой необходимый период времени определяет опытный врач-практик. Предпочтительно, композицию вводят ежедневно, самое предпочтительное два или три раза в день, например утром и вечером для поддержания достаточных уровней эффективных соединений в организме млекопитающего.
Кроме того, изобретение описывают в следующих не ограничивающих примерах.
ПРИМЕРЫ
Пример 1: Влияние процианидинов какао на активность липоксигеназы.
Фенольные фракции (от мономера до гексамера) и экстракты (неочищенные ацетоновые и обогащенные пентамером) получали, как описано в примерах 1-5 патента США № 5554645 заявителем Romanczyk et al. и примере 5 международной заявки № PCT/US97/05693, опубликованной как международная патентная заявка WO 97/36497. Липоксигеназа типа I-B из бобов сои, линолевая кислота (приблизительно 99%), твин 20 (полиоксиэтилен-сорбитанмонолаурат) и контрольные фенолы (нордигидрогваяретовая кислота (NDGA), (+)-катехин и (-)-эпикатехин) были получены от фирмы Sigma Chemical.
Линолевую кислоту солюбилизировали с помощью эмульгатора твина 20 согласно способу, опубликованному Grossman & Zakut (Methods Biochem. Anal. 25: 303-329, 1979). Липоксигеназу растворяли в PBS рН 8,6, получая 5000 ед./мл. Фенолы какао растворяли в очищенной воде и разбавляли из следующих основных растворов: мономер-гексамер растворяли до концентрации 1 мМ, экстракты до 1 мг/мл (1 г неочищенного ацетонового экстракта/л, ˜3,0 мМ мономер, 1 г обогащенного пентамером экстракта/л, ˜3,4 мМ).
Степень ингибирования липоксигеназы рассчитывали для каждой серии образцов из 6 реакционных кювет (1 контрольная с водой, 5 опытных с фенолом в воде) соответственно формуле: % ингибирования = (Δ абс. контроля - Δ абс. опыта)/Δ абс. контроля)×100. Реакционные смеси содержали растворенную линолевую кислоту (100 мкМ) в PBS рН 7,4 плюс/минус испытуемые фенолы в воде. Реакцию инициировали добавлением липоксигеназы при конечной концентрации 100 ед./мл. Определение сопряженных диеновых связей гидроперекисного продукта, образованного из линолевой кислоты, осуществляли с помощью регистрации кинетики в течение периода от 5 до 10 минут на спектрофотометре Beckman DU-600 UV (при 37°С, поглощение 234 нм).
Высокое поглощение компонентов какао в УФ-области не позволило измерить IC50 при текущих концентрациях. По этой причине величина IC50 была рассчитана путем экстраполяции кривой логарифмической регрессии (% ингибирования над логарифмом концентрации фенола) к концентрации, при которой ингибирование активности липоксигеназы испытуемым веществом достигает 50%. Экстраполированные величины IC50 дают приблизительное значение ингибиторной активности экстрактов полифенолов какао по отношению к липоксигеназе.
NDGA является установленным ингибитором липоксигеназ из бобов сои и некоторых липоксигеназ млекопитающих (Kemal et al., Biochemistry 26: 7064-7072, 1987). Указанный ингибитор является коммерчески применяемым ингибитором в качестве антиоксиданта в жирах и маслах. NDGA служит положительным контролем, поскольку величина IC50, составляющая 2×10-6 М, не была достигнута другими испытуемыми фенолами. Полагают, что (+)-катехин и (-)-эпикатехин являются структурно подобными мономеру полифенола какао.
Фенолы сравнивали на основе концентраций в молях. Ингибирование липоксигеназы (+)-катехином (3×10-3 М) было на два порядка выше, чем (-)-эпикатехином (3×10-1 М) и подобно ингибированию мономером какао (5×10-3 М), димером (2×10-3 М) и тримером (2×10-3 М). Ингибирование липоксигеназы более высокими олигомерами коррелировало в меньшей степени с логарифмом молярных концентраций. При конечных концентрациях от 0,3 до 25 мкМ тетрамер, пентамер и гексамер ингибировали активность липоксигеназы на 5-30%. Однако концентрация фенола и степень ингибирования существенно не коррелировали. Неочищенный ацетоновый экстракт оказывал зависимое от концентрации ингибирование липоксигеназы (IC50=5 мкМ, сравненное на основе мономера) приблизительно на 3 порядка слабее, чем ингибирование фракциями от мономера до тримера. Экстракт, обогащенный пентамером (IC50=59 М), не ингибировал активность липоксигеназы на значимом уровне.
Ингибиторная активность экстрактов фенолов какао по отношению к липоксигеназе из бобов сои имела сходство с таковой для (+)-катехина. Наблюдается небольшая разница среди активностей от мономера до тримера при сравнении на молярной основе, предполагая, что стерические факторы вносят вклад в ингибирование фермента. Полагают, что ингибирование является специфическим для компонентов с низким молекулярным весом (от мономера до тримера), поскольку соединения от тетрамеров до гексамеров проявили значительно меньшее ингибирование активности липоксигеназы, и пентамером обогащенный экстракт ингибировал в меньшей степени, чем неочищенный экстракт, который содержит больше олигомерных фракций, включающих соединения от мономеров до тримеров. Таким образом, полифенолы какао ингибируют липоксигеназу из бобов сои либо путем хелатирования простетического иона железа или путем «уборки» свободных радикалов посредством фенольных гидроксильных групп в реакции окисления, которая включает свободнорадикальные интермедиаты. Большие олигомеры (от тетрамеров до гексамеров) могут быть стерически блокированы и поэтому не способны «прочитывать» каталитический участок фермента.
Пример 2: Влияние экстрактов процианидинов какао и олигомерных фракций процианидинов какао на высвобождение простаноидов и общего эндотелина (ЕТ) базальными эндотелиальными клетками.
Изучали влияние очищенных мономеров и пентамеров процианидина из экстракта полифенолов какао на высвобождение простаноидов простациклина, простагландина (PGE2) и тромбоксана, а также общего эндотелина на эндотелиальные клетки крупного рогатого скота и человека в культуре.
Индометацин был получен от Cayman (Ann Arbor, MI USA).
Мономерные и пентамерные фракции процианидина очищали из какао-бобов, обогащенных процианидинами (обработанных способами, описанными в патенте США 6015913, зарегистрированном 18 января 2000), способами, описанными в примерах 1-5 патента США 5554645, зарегистрированного 10 сентября 1996.
Образцы анализировали способом Hammerstone et al., (J. Agric. Food Chem., 47: 2: 490-496, 1999). Подтверждение правильности молекулярного веса получали масс-спектрометрией.
Эндотелиальные клетки аорты крупного рогатого скота (ВАЕС) и эндотелиальные клетки аорты человека (НАЕС) культивировали в минимальной среде Игла (ЕМЕМ), как описано ранее исследователем Schramm et al., (J. Nutr. Biochem. 8: 647-651, 1997; J. Agric. and Food Chem. 46(5): 1900-1905, 1998).
Эндотелиальные клетки (ECs) (пассажи<11) засевали в 24-луночные планшеты со средой ЕМЕМ, содержащей 2 ммоль глутамина/л, 10% фетальной телячьей сыворотки, 100 единиц пенициллина/л, 0,1 мг стрептомицина/л и 0,25 пг амфотерицина/л. Конфлюентные клетки обрабатывали в 250 мл свободной от фенолового красного среды ЕМЕМ, содержащей рассматриваемые соединения, когда их применяли. Среду, инкубированную с EC's, анализировали после добавления фракции процианидина (10, 20 и 30 пмоль/л) и инкубации с ECs в течение 0 и 20 минут. Среду хранили при -70°С до проведения иммунного анализа, как описано ниже. Целостность клеток ЕС проверяли с исключением с помощью трипанового синего, как описано в публикации Bioadjieras et al., Methods in Lab. Invest. 50: 239-246, 1984.
Процедуры иммунного анализа выполняли, как описано в публикациях Westcott et al., Prostaglandins 32: 857-873, 1986; Yakota et al., Adv. Prostgl. Thrombox. Leukot. Res. 15: 33-34, 1985; Schramm et al., 1997; 1998; 1999. Общие эндотелины ET (ЕТ-1+ЕТ-2+ЕТ-3) в среде определяли с помощью Cayman иммуноанализа #583151. Метаболит простациклина (PGI2) 6-кетопростагландин F1-альфа определяли с помощью Cayman иммуноанализа #515211, метаболит тромбоксана (TXA2) TXB2 определяли с помощью Cayman иммуноанализа 519031 и PGE2 определяли с помощью Cayman иммуноанализа #514016.
Указанные условия анализа воспроизводили те условия, которые ранее использовали, чтобы показать, что фракция вина с массой <3000 да. оказывала отличающее воздействие на синтез простаноидов клетками ЕС, чем фракция вина с массой >3000 (Schramm et al., J. Agric. and Food Chem. 46(5): 1900-1905, 1998). Проверяли воздействие на функцию базальных клеток. Обработка процианидинами какао не воздействовала ни на клеточную жизнеспособность, ни на клеточную морфологию. Каждый миллилитр контрольной среды, инкубированной с BAECs в течение 20 минут, содержал 73,5+/-0,044 нг ТХВ2 и 294+/-6,3 пг PGE2.
Как показано на фиг.2, добавление мономерных или пентамерных процианидинов какао к среде, инкубированной с BAECs в течение 20 минут, изменяло концентрации простаноида и ET в среде при сравнении с контрольной средой. Среда, содержащая или мономерные (А1) или пентамерные (А2) процианидины, включала в себя больше 6-кето-PCF1-альфа, чем контрольная среда. Уровень PGE2 был снижен с помощью мономерной фракции (В1) дозо-зависимым образом и с помощью пентамерной фракции (В2) при концентрации 30 мкМ. Никакого значительного воздействия любой фракции процианидина на ТХВ (С1-2) среды не было замечено. Хотя мономерные и пентамерные фракции процианидина какао оказывали подобное воздействие на 6-кето-PCF1-альфа и PGE2 среды, они имели противоположное действие на ET среды, причем мономерная фракция (D1) увеличивала концентрацию ET в культуральной среде на 30 мкМ, и пентамерная фракция (D2) уменьшала концентрацию ET среды дозо-зависимым образом.
Данные на фиг.3 А-В демонстрируют подобные результаты, где мономерные и пентамерные процианидины какао воздействуют на ECs аорты коровы (ВАЕС) и человека (НАЕС).
Вышеприведенные данные показывают, что процианидины какао стимулируют эффекты эйкозаноида и эндотелина, которые уменьшают релаксацию сосудов и уменьшают агрегацию тромбоцитов/образование тромба, т.е. вызывают индукцию простациклина и ингибирование эндотелина и простагландина.
Пример 3: Влияние потребления процианидин-обогащенного напитка из какао на активность тромбоцитов.
Изучали влияние потребления напитка какао на регуляцию активации тромбоцитов и первичный гемостаз.
Тридцать здоровых некурящих взрослых субъектов без сердечных заболеваний или гемостатических нарушений в истории болезни разделяли на три исследуемые группы: (а) 10 субъектов (4 мужчин и 6 женщин в возрасте 24-49 лет), которые потребляли напиток какао, (b) 10 субъектов (4 мужчин и 6 женщин в возрасте 26-50 лет), которые потребляли напиток с кофеином в качестве контроля, и (с) 10 субъектов (4 мужчин и 6 женщин в возрасте 24-50 лет), которые потребляли воду в качестве контроля. Все женщины находились в предклимактерическом периоде и не принимали эстрогены. Участникам рекомендовали воздерживаться от лекарственной терапии нестероидными противовоспалительными средствами в течение, по крайней мере, 4 дней, от алкогольных напитков в течение, по крайней мере, 2 дней и от кофеин- или теоброминсодержащих пищевых продуктов в течение, по крайней мере, 24 часов до испытания и в течение дня испытания.
Кровь получали от каждого субъекта между 8 и 10 утра. Образцы собирали в две 5-мл вакуумированные пробирки, содержащие 0,5 мл 3,2% буферного раствора цитрата натрия (Becton Dickinson, Franklin Lakes, NJ). Затем испытуемые субъекты выпивали по 300 мл напитка, содержащего 18,75 г обогащенного процианидинами порошка какао (который включал в себя 960 мг всех процианидинов, 17 мг кофеина и 285 мг теобромина) и 12,5 г сахарозы, смешанной с дистиллированной водой (см. Adamson, G.E. et al., J. Ag. Food Chem., 1999, 47(10) 4184-4188). Контрольные субъекты выпивали или напиток, содержащий 17 мг кофеина и 12,5 г сахарозы, или простую воду. Дополнительные образцы крови получали через 2 и 6 часов после потребления напитков. Одна женщина отсутствовала в момент забора крови после 6 часов потребления какао.
Процианидины оценивали количественно следующим образом: стандартную смесь приготовляли, используя коммерчески доступный (-)-эпикатехин и соединения от димеров до декамеров, полученных в очищенном состоянии способами, описанными в публикации Hammerstone, J.F. et al., J. Ag. Food Chem., 1999, 47(10) 490-496, Lazarus, S.A. et al., J. Ag. Food Chem., 1999, 47(9) 3693-3701 и Adamson, G.E. et al., J. Ag. Food Chem., 1999, 47(10) 4184-4188. Стандартные основные растворы с указанными соединениями анализировали с помощью метода нормально-фазовой ВЭЖХ, описанного в ранее цитированной ссылке на Adamson, с флуоресцентной детекцией при возбуждении и эмиссии при длинах волн 276 нм и 316 нм соответственно. Пики группировали и их площади суммировали, чтобы соединить вклады от всех изомеров в пределах любого одного класса олигомеров, и строили кривые, используя квадратичное усреднение. Графики для мономеров и небольших олигомеров носили почти линейный характер, что находится в соответствии с результатами, полученными при предыдущем применении линейной регрессии для построения калибровочных кривых на основе мономера и димера.
Затем указанные калибровочные кривые использовали, чтобы рассчитать уровни процианидинов в образцах, приготовленных следующим образом: вначале образцы какао или шоколада (около 8 грамм) обезжиривали посредством трех экстракций гексаном (45 мл каждая). Затем один грамм обезжиренного материала экстрагировали 5 мл смеси ацетон/вода/уксусная кислота (70:29,5:0,5 об./об.). Затем определяли количество процианидинов в обезжиренном материале путем сравнения данных ВЭЖХ образцов с калибровочными кривыми, полученными, как описано выше (где использовали очищенные олигомеры). Процент жира для образцов (используя однограммовое количество для образца шоколада или полуграммовое количество для образца жидкостей) определяли стандартизированным способом, опубликованным в Association of Official Analytical Chemists (AOAC Official Method 920.177). Затем рассчитывали количество всех процианидинов в исходном образце (с жиром). Калибровку осуществляли до каждого эксперимента с образцом, чтобы избежать изменений, наблюдающихся от колонки к колонке.
В пределах 10 минут сбора образцов крови целую кровь инкубировали в полистироловых пробирках в течение 5 минут при комнатной температуре с 10 мкл буфера HEPES (рН 7,4, нестимулированный контроль), 20 или 100 мкМ ADP или 20 мкМ эпинефрина (BioData, Horsham, PA) в присутствии или отсутствие пептида Arg-Gly-Asp-Ser (Sigma, St. Louis, МО). После 5 минут образцы суспендировали в 1 мл буфера HEPES и 100 мкл образца переносили в пробирки, содержащие насыщающие концентрации (20 мкл) каждого из следующих флуоресцентно-меченых моноклональных антител: PAC1-флуоресцеинизотиоцианат (FITC), анти-СD62Р-фикоэритрин (РЕ) и анти-СD42а-PerCP. РАС1 распознает активированную конформацию фибриноген-связанного рецептора GPIIb-IIIa, и анти-СD62Р распознает Р-селектин, присутствующий на поверхности активированных тромбоцитов. Анти-СD42а распознает рецептор GPIb-IX, который находится на поверхности как активированных, так и покоящихся тромбоцитов. Мышиный IgG, FITC и мышиный IgG, РЕ использовали в качестве изотипных контролей. Пептид Arg-Gly-Asp-Ser использовали, чтобы блокировать связывание РАС1 антитела с тромбоцитами и, таким образом, установить отрицательный контрольный маркер на проточном цитометре. Антитела и изотипные контроли приобретали из Becton Dickinson Immunocytometry Systems, Inc., San Jose, CA.
Образцы целой крови, в присутствии и отсутствие агонистов ADP и эпинефрина, инкубировали с моноклональными антителами или изотипным контролем в течение 20 минут в темноте при комнатной температуре. Затем образцы фиксировали в отфильтрованном 1%-ном параформальдегиде (рН 7,2) и хранили в темноте при 2-8°С. Все образцы анализировали в течение 48 часов на FACScan проточном цитометре, используя программу LYSYS II. Разрешение проточного цитометра изменялось с помощью 1, 2 и 10 мкм калибровочных гранул (Becton Dickinson Immunocytometry Systems, Inc., San Jose, CA и Flow Cytometry Systems, Research Triangle Park, NC). Двадцать тысяч случаев было собрано в таблицу в виде перечня со всеми параметрами светорассеяния и флуоресценции в логарифмической форме. Тромбоциты идентифицировали на основе светорассеяния и экспрессии CD42a. Активированные тромбоциты определяли как процент положительных в отношении CD42a случаев с коэкспрессией активированной конформации GPIIb-IIIa или Р-селектина. Микрочастицы тромбоцитов определяли как процент положительных в отношении CD42a случаев менее чем 2 мкм по величине.
Один образец крови, взятый в каждой из трех исследуемых временных точек, анализировали в течение четырех часов, используя анализатор функции тромбоцитов (PFA-100TM, Dade Behring International, Miami, FL), согласно инструкциям производителя. См. Mammen et al., Sem. Thromb. Hemostas. 24: 195-202, 1998 и Fressinaud et al., Blood 91: 1325-31, 1998. Функция была измерена как время закрытия в секундах, которое определяют как время, требуемое для закупорки кровью отверстия в испытуемой мембране.
Данные из каждой подвергнутой обработке или контрольной группы анализировали для выявления различий, используя программу ANOVA для повторных измерений по рангам по Friedman (SigmaStat for Windows, SPSS, Richmond, CA). Метод множественного сравнения Student-Newman-Keuls использовали для идентификации различий между базовой линией и результатами, полученными через 2 и 6 часов после потребления. Значения Р менее 0,05 рассматривали как статистически достоверные.
Потребление какао подавляло нестимулированную (Р=0,035, фиг.4А) и ex vivo эпинефрин-индуцированную (Р=0,008, фиг.4В) экспрессию активированного GPITb-IIIa через 2 часа и 6 часов после приема пищи. Величины средних процентов тромбоцитов, экспрессирующих активированный рецептор GPIIb-IIIa без стимуляции, были 0,9, 0,5 и 0,3% и в ответ на эпинефрин были 9,6, 6,8 и 3,3% во временных точках нуль, 2 часа и 6 часов соответственно после потребления. По сравнению с этим, наблюдали увеличение стимулированной эпинефрином экспрессии активированного GPIIb-IIIa в контрольной группе, которая пила напиток с кофеином (Р=0,048, средние значения = 5,3, 6,5 и 7,5% во временных точках нуль, 2 часа и 6 часов после потребления). В контрольной группе, которая пила воду, никаких изменений не наблюдали.
Какао уменьшал индуцированную 20 мкМ ADP экспрессию активированного GPIIb-IIIa на тромбоцитах через 2 часа и 6 часов после потребления (Р<0,001, фиг.4С, средние величины = 58,5, 44,2 и 38,8% во временных точках нуль, 2 часа и 6 часов после потребления соответственно). Предполагаемая тенденция была направлена на уменьшение экспрессии на тромбоцитах активированного GPIIb-IIIa после потребления какао в тех случаях, когда активация была индуцирована 100 пмоль ADP (Р=0,067, средние величины = 76,5, 68,7 и 57,6% во временных точках нуль, 2 часа и 6 часов после потребления соответственно). В группах, потребляющих напиток с кофеином и воду в качестве контроля, не наблюдали изменения в индуцированной ADP экспрессии активированного GPIIb-IIIa.
Несущественную тенденцию к уменьшению экспрессии Р-селектина наблюдали после потребления какао (Р=0,053, фиг.5А). Потребление какао снижало индуцированную 20 мкМ ADP экспрессию Р-селектина через 2 часа и 6 часов после потребления (Р=0,007, фиг.5С) и индуцированную 100 мкМ ADP экспрессию Р-селектина, которая составила 56,1, 54,7 и 41,7% во временных точках нуль, 2 часа и 6 часов после потребления соответственно.
Данные, свидетельствующие о стимуляции или ингибировании тромбоцитов в контрольных группах, которые потребляли кофеинсодержащий напиток или воду, отсутствуют.
Число микрочастиц тромбоцитов, определенное с помощью проточной цитометрии после потребления напитка какао, уменьшалось по отношению к базовой линии через 2 часа и далее уменьшалось через 6 часов (см. табл.1). По сравнению с этим, число микрочастиц тромбоцитов увеличивалось через 2 часа и 6 часов после потребления воды и через 6 часов после потребления кофеинсодержащего напитка. Микрочастицы тромбоцитов являются гемостатически активными, богатыми фосфолипидами микровезикулами, которые образуются в течение физиологической активации тромбоцитов.
γПроцент микрочастиц всех CD42 положительных случаев. Величины представляют средние значения (диапазон), n=10 на группу.
*Значимо отличаются от "До потребления" (Р<0,05).
Через шесть часов после потребления напитка какао время закрытия, индуцированного коллаген-эпинефрином, удлинялось (см. табл.2). Полученные данные указывают на замедление первичного связанного с тромбоцитом гемостаза с потреблением какао. Тенденцию к пролонгированному времени закрытия наблюдали после коллаген-ADP-индукции (р=0,097); время закрытия не изменялось в контрольной группе, которая потребляла кофеин.
γВремя закрытия первичного связанного с тромбоцитом гемостаза в секундах. Величины представляют средние значения (диапазон), n=10 на группу.
*3начимо отличаются от «До потребления» (Р<0,05). Программа ANOVA для повторных измерений по рангам по Friedman с последующим множественным сравнением по Student-Newnan-Keuls.
Полученные результаты показали, что потребление напитка шоколада модифицировало функцию тромбоцитов у человека. Во-первых, активация тромбоцитов, определенная с помощью экспрессии маркера активации тромбоцитов в ответ на влияние слабых агонистов in vitro, уменьшалась после потребления какао. Во-вторых, образование микрочастиц тромбоцитов уменьшалось после потребления какао. И в-третьих, потребление какао вызывало аспирин-подобное действие на функцию тромбоцитов, как определено посредством связанного с тромбоцитом первичного гемостаза. Тот факт, что напиток с кофеином в качестве контроля вызывал увеличение эпинефрин-индуцированной экспрессии активированного GPIIb-IIIa и образования микрочастиц, означает, что процианидины какао, присутствующие в напитке какао, ответственны за ингибирование активации тромбоцитов и их функцию.
Пример 4: Влияние перорального потребления какао на ингибирование холестерином эндотелий-зависимой релаксации сосудов (EDR).
Было показано, что некоторые растительные экстракты, содержащие флавоноиды, индуцируют EDR in vitro в аортах кролика. Заявители исследовали влияние какао при пероральном введении в постоянном режиме на EDR и его защитное действие против утраты EDR, которая наблюдается при питании с холестерином. Новозеландских белых кроликов кормили с использованием 4-х режимов питания в течение 7 дней: (1) еда, (2) еда+200 мг какао/день, (3) 2% холестерин в течение 3 недель с последующими 4 неделями потребления пищи, (4) 2% холестерин в течение 3 недель с последующими 4 неделями потребления пищи + 200 мг какао/день. EDR определяли на кольцах аорты, суспендированных в ванночке для органов (20 мл). Кольца были предварительно сокращены под действием норэпинефрина (NE) (10-5 М). EDR по отношению к ацетилхолину (Ach) и экстракту пентамера какао (10-7-10-5 М) измеряли как % релаксации по отношению к NE.
(3 недели)
*Значимо отличаются от остальных в колонке
Пример 5: Влияние потребления пероральным путем процианидинов какао, фитостеринов и их комбинаций
Результаты данного эксперимента показывают влияние потребления комбинации неэтерифицированных фитостеринов и фитостанолов, имеющихся в талловом масле («фитостерин») и порошка какао (CPd), содержащего приблизительно 70 мг/г всех процианидинов какао, на (1) показатели окислительного стресса и повреждение и (2) на уровни холестерина, а также синергическое действие комбинированного введения фитостеринов и процианидинов какао.
В пищевой рацион, включающий очищенную яичную скорлупу, добавляли фитостерины (2 мас.%) и/или CPd (0,5, 1, 2 мас.%) и кормили крыс самцов в течение 2 недель. Крыс разделяли на восемь групп (по три крысы на группу) и давали 20-25 г/день контрольной пищи и тестируемой пищи согласно следующей схеме:
Воду крысам давали до насыщения и потребление определяли путем взвешивания оставшейся/просыпанной пищи, собранной под кормушками. Потребление пищи определяли ежедневно и крыс взвешивали через день.
В плазме крови определяли параметры окислительного поражения/стресса, уровни холестерина и поглощение эпикатехина.
TBARS плазмы определяли, используя модификацию способа, описанного в публикации Yagi (Biochem. Med., 15: 212-216, 1976). Сто мкл целой крови добавляли к одному мл физиологического солевого раствора и центрифугировали при 1700 g в течение 15 минут. Супернатант собирали и замораживали при -70°С до анализирования. Липиды выделяли посредством их осаждения системой кислот фосфорновольфрамовая/серная. Затем липидную фракцию подвергали взаимодействию с тиобарбитуровой кислотой и полученные аддукты измеряли флуориметрически, используя 1,1', 3,3'-тетраэтоксипропан в качестве стандарта. Результаты выражали в виде зависимости наномолей MDA на миллилитр плазмы от концентрации полиненасыщенных жирных кислот плазмы.
8-Гидрокси-2'-дезоксигуанозин (8OН2'dG) определяли следующим образом. Ядерную ДНК выделяли, используя Wako DNA Extractor WB kit (Wako Chemical USA, Inc., Richmond, VA). Ткань (100-250 г) или клетки (106 клеток) гомогенизировали в буфере для лизиса из набора и центрифугировали при 10000 g в течение 20 секунд при 4°С. Осадок обрабатывали буфером для лизиса и полученный осадок растворяли в растворе для ферментативной реакции из набора. РНКазу добавляли до конечной концентрации 20 мкг/мл и образец инкубировали при 50°С в течение 10 минут. Затем добавляли раствор протеиназы из набора и инкубацию продолжали при 50°С в течение дополнительного часа. Образец центрифугировали при 10000 g в течение 5 минут при комнатной температуре и супернатант обрабатывали раствором NaI и изопропанола из набора, чтобы очистить ДНК. Осадок собирали при 10000 g в течение 10 минут при комнатной температуре и промывали растворами А и В из набора. Конечный осадок недолго сушили на воздухе и ресуспендировали в 200 мкл 0,1 мМ дезферил/20 мМ Na-ацетат, рН 4,8. Расщепление ДНК и анализ продуктов выполняли согласно способу Shigenaga et al. (Methods Enzymol. 234: 16-33, 1994) с некоторой модификацией. Кратко, ДНК расщепляется до нуклеотид 5'-монофосфата при инкубации с нуклеазой Р1 при конечной концентрации 0,1 мг/мл в течение 15 минут при 65°С. рН раствора доводили с помощью 1 М трис-HCl, рН 8,5, и далее использовали щелочную фосфатазу из кишечника теленка, чтобы гидролизовать образец до нуклеотидов (один час, 37°С). рН раствора образца доводили с помощью 3 М натрий-ацетатного буфера, рН 5,1, и добавляли 0,1 мМ EDTA/0,1 мМ дезферила, чтобы предотвратить окисление, вызванное металлом. Образец пропускали через фильтр, отсекающий фракции с молекулярной массой 30000, при вращении и помещали в инжекционный пузырек для ВЭЖХ. Образцы анализировали в течение 48 часов приготовления, чтобы предотвратить появление артефактов. Что касается анализа, образцы впрыскивали в прибор Hewlett Packard 1100 ВЭЖХ, снабженный электрохимическим детектором (ESA, Coulochem II). Разделения достигали с использованием колонки Supelcosil LC-18-DB (150×4,6 мм, размер частиц 3 микрона) и подвижной фазы, состоящей из 100 мМ Na-ацетатного буфера, рН 5,2 с 5% метанола, в режиме изократического разделения, со скоростью потока 1,0 мл/мин. OH8dG определяли при 450 мВ, используя электрохимическую детекцию, и 2'-дезоксигуанозин (dG) определяли при 248 нм, используя детекцию в УФ-области. Уровни OH8dG выражали относительно количества dG в образцах.
Поглощение эпикатехина измеряли, как описано в публикации Rein et al., J. of Nutr., 2000, 130 (8S), 2109S-2114S.
РЕЗУЛЬТАТЫ
Полученные результаты неожиданно продемонстрировали благоприятное воздействие комбинированного введения фитостеринов и полифенолов.
Как показано на фиг.6, количество поглощенного эпикатехина увеличивалось дозо-зависимым образом. Неожиданно, введение фитостеринов повышало всасывание эпикатехина таким образом, например, что при содержании в пищевом рационе 2 мас.% CPd уровни эпикатехина в плазме увеличивались приблизительно на 30% по сравнению со сравниваемым пищевым рационом без фитостеринов. Следовательно, фитостерин усиливал биодоступность эпикатехина.
Как показано на фиг.7, CPd ингибировал повреждение ДНК при окислении дозо-зависимым образом. Неожиданно, при более высоких дозах CPd (2 мас.%) наблюдали неожиданное уменьшение повреждения ДНК при окислении, что указывает на синергическое действие фитостеринов и CPd в предотвращении повреждения ДНК при окислении.
Как показано на фиг.8, принятие пищи, содержащей фитостерины, неожиданно вызывало более высокий окислительный стресс, чем при приеме контрольной пищи, т.е., потребление фитостерина вместе с пищей (без процианидинов какао), которая была рекомендована в данной области до времени подачи данной заявки, усиливало окислительный стресс. Потребление с пищей процианидинов какао обращало или притупляло указанный отрицательный эффект фитостеринов.
Кроме того, измеряли уровень общего холестерина плазмы, и полученные результаты представлены в табл.3.
Как показано в табл.3, как и ожидали, фитостерины снижали уровни холестерина.
Неожиданно, однако, когда фитостерины вводили с CPd, уровни холестерина снижались даже еще больше дозо-зависимым образом. Например, среднее значение уровня общего холестерина у трех крыс, которых кормили пищей, содержащей фитостерин, было 84 мг/дл. Добавление к данному рациону 2 мас.% CPd приводило к дополнительному снижению общего холестерина до 80 мг/дл, что указывает на синергический эффект двух соединений. У крыс, которых кормили контрольной пищей, средний уровень холестерина составлял 88,3 мг/дл.
Пример 6: Пищевые композиции с холестеринснижающими реагентами в комбинации с какао или шоколадом, содержащими процианидины какао.
Приготовляли темный шоколад, жевательную ириску и батончики из гранолы, содержащие холестеринснижающие реагенты.
Жевательную ириску приготовляли из ингредиентов, показанных в табл.4, путем предварительного смешивания сахара и какао и последующего смешивания с карамелью. Свободные фитостерины (как есть или диспергированные) добавляли к смеси сахара и какао.
Темный шоколад, содержащий свободный стерин, получали с использованием коммерчески доступного темного шоколада (DOVE темный от Mars Inc.). Чтобы облегчить смешивание с расплавленным шоколадом и избежать какого-либо вредного воздействия на текстуру шоколада, гранулированные формы растительного стерина/станола измельчали с помощью устройства Universal Muche M20, произведенного IKA, в течение 30-60 секунд, смешивали и измельчали в течение дополнительных 30 секунд до тех пор, пока размер частиц не становился сравнимым с размером частиц шоколада. Темный шоколад расплавляли и добавляли стерин путем медленного смешивания, чтобы обеспечить однородное распределение частиц стерина. Полученная композиция представлена в табл.5.
Батончики из гранолы, содержащие холестеринснижающее волокно овса, получали из ингредиентов, перечисленных в табл.6 и 7. Сироп в качестве связующего приготовляли путем плавления пальмоядрового масла до 45°С и держали при данной температуре до тех пор, пока оно не было готово для использования. Кукурузный сироп, глицерин, порошок какао, коричневый сахар, соль, лецитин и пропилгаллат комбинировали и добавляли пальмоядровое масло. Смесь оставляли теплой. Для приготовления гранолы пылеобразные овес и сою (получены от Sovex Food, Collegedale, TN) смешивали с кусочками шоколада и связующий компонент в виде теплого сиропа, приготовленного как описано выше, добавляли к смеси. Смесь гранолы затем формовали в виде пластин, посыпанных смесью 10Х сахара (62%), порошка какао (33%) и корицы (5%), и разрезали на куски. Используемый в смеси порошок какао приготовляли способом, опубликованным в патенте США № 6015913 заявителем Kealey et al.
холестеринснижающийхолестеринснижающийхолестеринснижающий
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДЕФЕКТНОЙ КОММУНИКАЦИЕЙ ПОСРЕДСТВОМ ЩЕЛЕВЫХ КОНТАКТОВ | 2003 |
|
RU2351325C2 |
| ПРИМЕНЕНИЕ ПРОЦИАНИДИНОВ КАКАО В СОЧЕТАНИИ С АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТОЙ КАК ПРОТИВОТРОМБОЦИТНОГО ТЕРАПЕВТИЧЕСКОГО СРЕДСТВА | 2001 |
|
RU2286778C2 |
| ПРОДУКТЫ, СОДЕРЖАЩИЕ ПОЛИФЕНОЛ(Ы) И L-АРГИНИН, ДЛЯ СТИМУЛЯЦИИ ПРОДУКЦИИ ОКИСИ АЗОТА | 1999 |
|
RU2269268C2 |
| СОЕДИНЕНИЕ ЭКСТРАКТА КАКАО И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2004 |
|
RU2394562C2 |
| ПРОДУКТЫ, СОДЕРЖАЩИЕ ПОЛИФЕНОЛЫ | 2006 |
|
RU2417711C2 |
| ПИЩЕВОЙ ПРОДУКТ ДЛЯ ДИАБЕТИКОВ | 2005 |
|
RU2380983C2 |
| ПИЩЕВЫЕ ПРОДУКТЫ С ВЫСОКИМ СОДЕРЖАНИЕМ ПОЛИФЕНОЛОВ КАКАО, УЛУЧШЕННЫМ ВКУСОМ И АРОМАТОМ И ИЗМЕЛЬЧЕННЫМИ ЭКСТРАКТАМИ КАКАО | 2008 |
|
RU2476075C2 |
| СПОСОБ ПЕРЕРАБОТКИ КАКАО-БОБОВ, ЧАСТИЧНО ОБЕЗЖИРЕННЫЕ ТВЕРДЫЕ ВЕЩЕСТВА КАКАО И СОДЕРЖАЩИЙ ИХ ПИЩЕВОЙ ПРОДУКТ | 1997 |
|
RU2242880C2 |
| СПОСОБЫ ЛЕЧЕНИЯ, ТРЕБУЮЩИЕ ФИТОКОМПОНЕНТОВ | 2005 |
|
RU2394576C2 |
| ПИЩЕВОЙ ПРОДУКТ, ИМЕЮЩИЙ ПОВЫШЕННОЕ СОДЕРЖАНИЕ ПОЛИФЕНОЛОВ КАКАО, СПОСОБ ЕГО ПРОИЗВОДСТВА И ДИЕТИЧЕСКАЯ ДОБАВКА | 1999 |
|
RU2271115C2 |
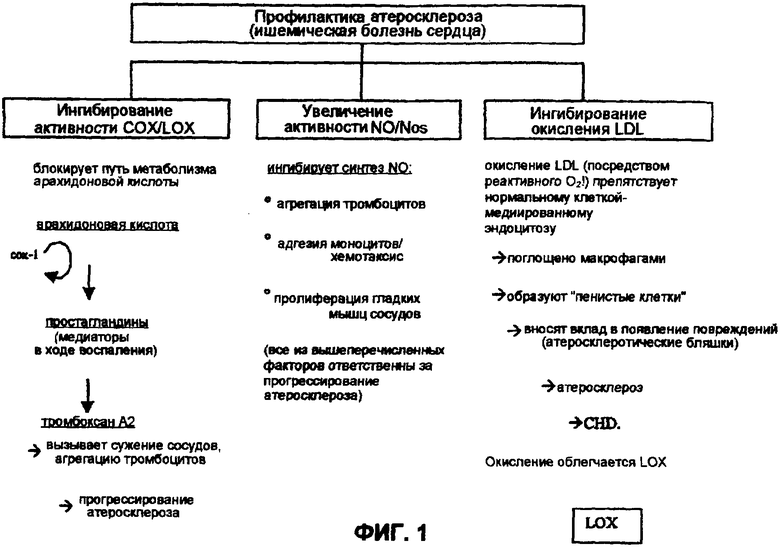
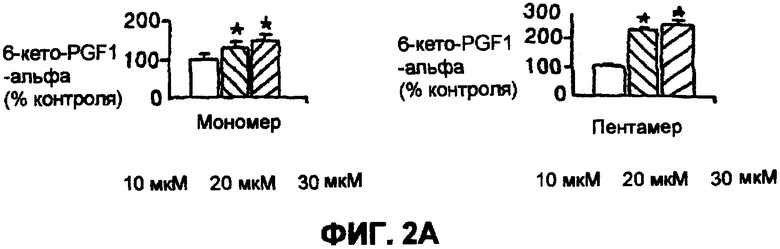
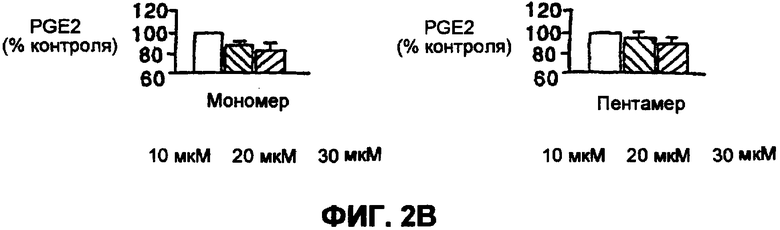
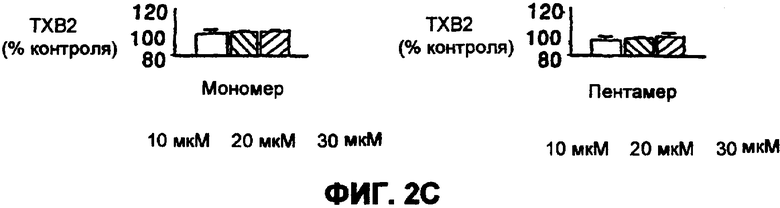
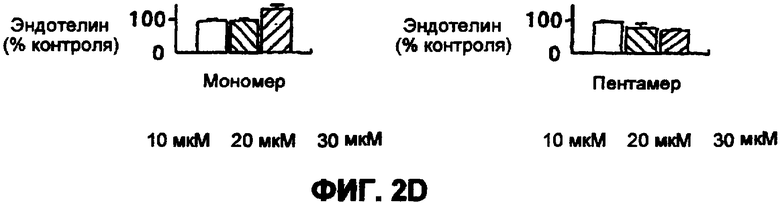
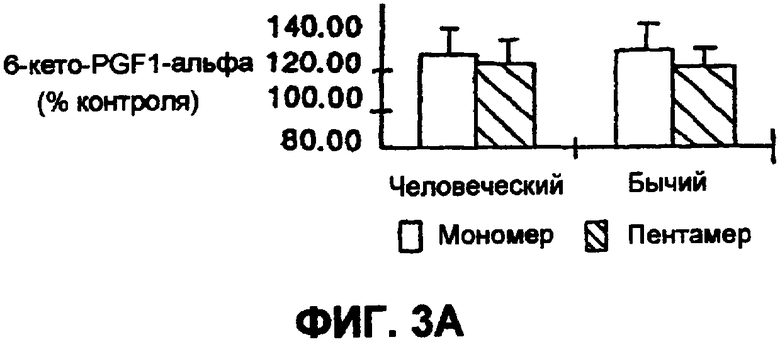
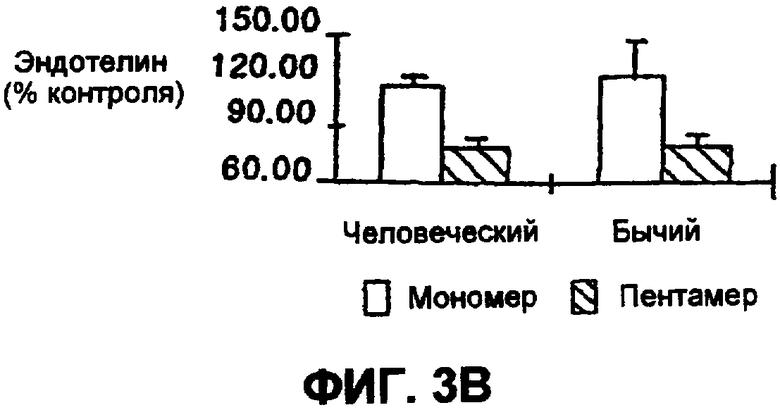

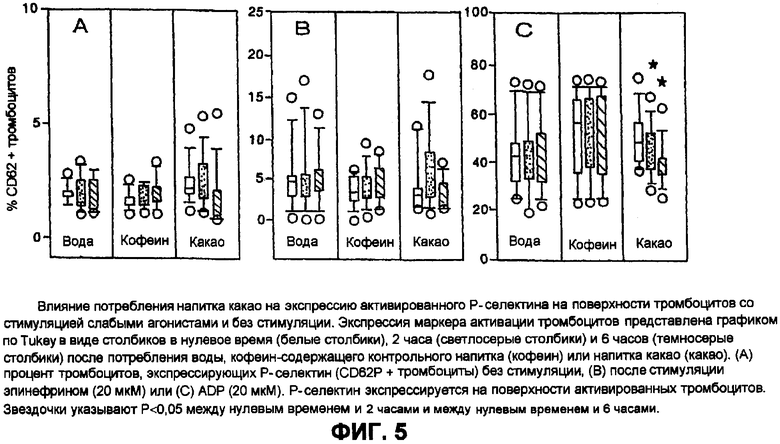
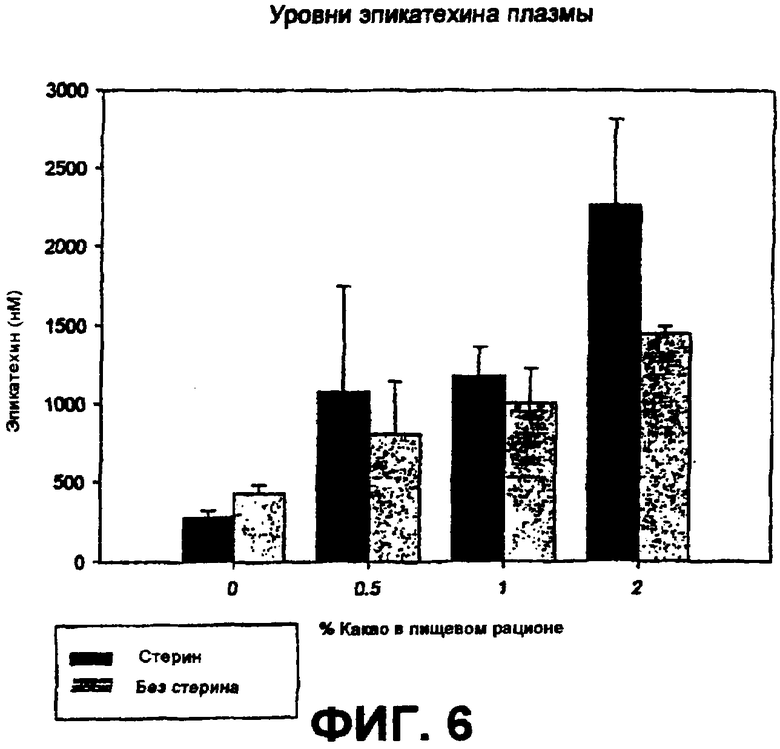
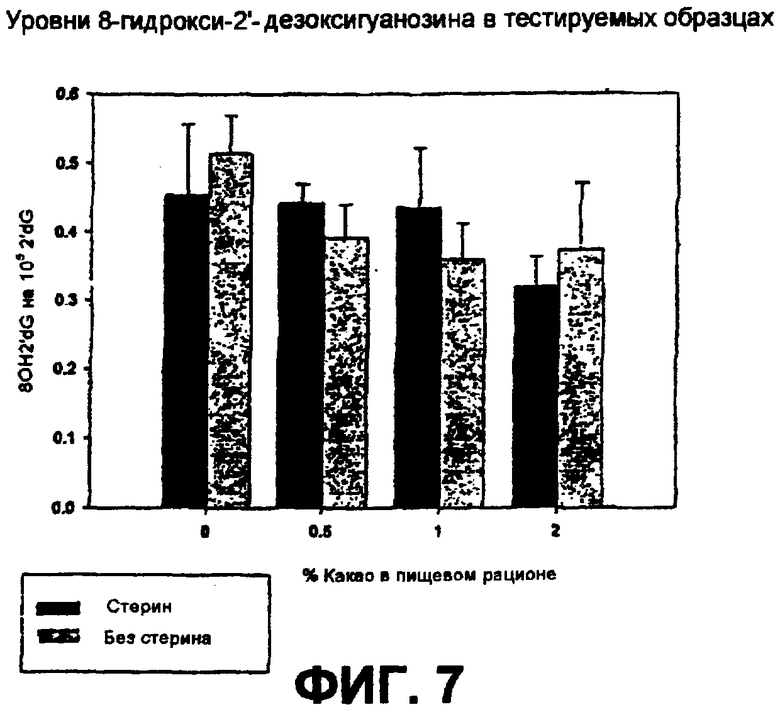
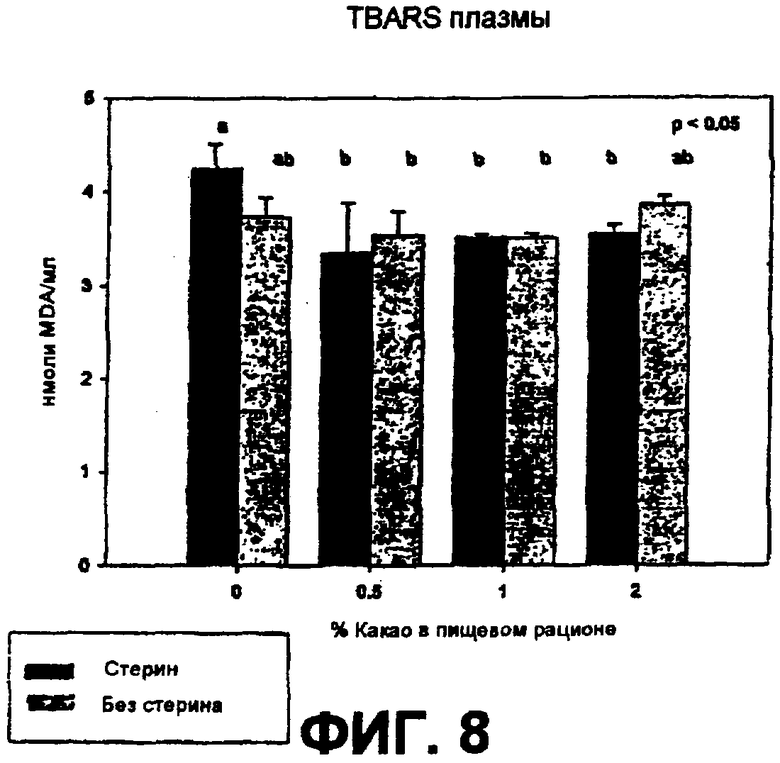
Изобретение относится к композициям для поддержания сердечно-сосудистой системы и/или сосудов в здоровом состоянии, содержащим эффективное количество мономера и/или олигомера процианидина какао и эффективное количество холестеринснижающего реагента на основе стерина и/или станола, и к способам поддержания сосудистой системы в здоровом состоянии, включая лечение и профилактику атеросклероза и сердечно-сосудистого заболевания. Технический результат: усиленное воздействие на состояние сосудистой системы млекопитающего, в частности человека, по сравнению с ранее известными композициями при лечении и профилактике атеросклероза и сердечно-сосудистого заболевания. 12 н. и 26 з.п. ф-лы, 7 табл., 8 ил.
| WO 9736497 A1, 09.10.1997 | |||
| WO 9833494 A1, 06.08 | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| WO 9948386 A1, 30.09.1999 | |||
| US 4808574 A, 28.02.1989 | |||
| ЗАГУЩЕННЫЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2132370C1 |
Авторы
Даты
2007-07-27—Публикация
2001-04-10—Подача