Предпосылки изобретения
Данная заявка касается применения комбинации процианидинов какао и аспирина в качестве противотромбоцитного терапевтического средства.
Соединение, состоящее из одного ароматического кольца, которое содержит, по меньшей мере, одну гидроксильную группу, классифицируют как простой фенол. Следовательно, полифенол включает более одного ароматического кольца, причем каждое кольцо содержит, по меньшей мере, одну гидроксильную группу. Флавоноиды представляют полифенолы, которые имеют структуру дифенилпропана (С6-С3-С6) и обнаружены повсеместно в царстве растений. Класс флавоноидов, называемых проантоцианидинами, представляет олигомеры мономерных единиц флаван-3-ола, наиболее часто связанных 4-6 или 4-8. Одним из наиболее общих классов проантоцианидинов являются процианидины, которые представляют олигомеры катехина и эпикатехина и их эфиры галловой кислоты.
Известно, что регулярное потребление пищевых полифенолов, обычно обнаруживаемых в разнообразных фруктах и овощах, способствует снижению смертности от сердечно-сосудистых заболеваний (CVD), включая инсульт, болезнь сердца и тромбоз сосудов. Красное вино, зеленый чай и какао идентифицированы как продукты, богатые полифенолами, а для красного вина и зеленого чая показано, что в промышленно развитых странах их употребление обратно пропорционально связано со смертностью от болезней сердца.
Показано, что кроме снижения риска атерогенеза пищевые полифенолы обладают другими разнообразными потенциально выгодными биологическими активностями. Например, показано, что они ингибируют вирусную обратную транскриптазу, ингибируют репликацию ВИЧ I in vitro, подавляют образование язв и являются антимутагенными, нейрозащитными, противовоспалительными, антибактериальными, гипотензивными агентами и цитотоксичны относительно разных типов раковых клеток.
Механизмы, по которым пищевые полифенолы проявляют свои биологические функции, понятны неполностью, но известно, что они обладают сильными антиоксидантными свойствами и оказывают ингибирующее действие на активность тромбоцитов.
Аспирин (ацетилсалициловая кислота) является прототипом нестероидного противовоспалительного агента. Его применяют в течение многих лет в противотромбоцитной терапии для снижения риска повторяющихся временных ишемических приступов или цереброваскулярных нарушений. Механизм действия аспирина хорошо известен (Vane J., Nature, 1971). Вкратце, он ингибирует метаболический путь арахидоновой кислоты, вызывая изменение простагландин G\H синтазы 1 тромбоцитов, что является причиной необратимой потери их циклооксигеназной активности. Это приводит к снижению превращения арахидоновой кислоты в простагландины, которые являются сильнодействующими медиаторами разнообразных групп физиологических процессов. Именно пониженное образование данных простагландинов, в особенности тромбоксана А2 и простагландина Е2, которое отвечает за разнообразные фармакологические эффекты аспирина, образует основу их терапевтического применения. К сожалению, те же факторы являются причиной хорошо изученной токсичности аспирина.
У тромбоцитов отсутствуют возможности для синтеза новых белков, что означает, что нарушение, обусловленное аспирином, нельзя устранить в течение периода жизни тромбоцита. Это означает, что ингибирующее действие повторяющихся дневных доз аспирина является кумулятивным и в конечном счете приводит к почти полному подавлению биосинтеза тромбоксана тромбоцитов через 7-10 дней. Биохимические, фармакологические и клинические данные подтверждают теорию, что подавление тромбоксана ведет к предотвращению тромбоксан-зависимой активации тромбоцитов, которая отвечает за антитромбоцитные эффекты аспирина.
Однако различные другие простагландины, продуцируемые по метаболическому пути арахидоновой кислоты, ответственны за некоторые важные гомеостатические механизмы, такие как секреция желудочной кислоты, первичный гемостаз, регуляция кровяного давления и почечная функция. Следовательно, длительное лечение аспирином дает вредные эффекты. Они включают серьезные желудочно-кишечные осложнения, включая кровотечение и перфорацию, осложнения, связанные с кровотечением, такие как случаи кровоизлияния, и повышение риска хронического почечного заболевания.
На протяжении многих лет повышенное понимание положительных и отрицательных аспектов длительного лечения аспирином привело к тенденции уменьшения рекомендуемой дневной дозы, иногда в сочетании со слабыми антикоагулянтами для перорального приема (у пациентов с высоким риском).
Ясно, что открытие противотромбоцитного агента, который не вызывает серьезных побочных эффектов аспирина и который можно применять для замещения аспирина при длительных схемах профилактики/лечения или в сочетании с очень малыми дозами аспирина, было бы громадным шагом вперед в лечении и профилактике любого заболевания или нарушения, вызванного дисфункцией тромбоцитов. Такое открытие было бы встречено с огромным энтузиазмом медиками и людьми с риском таких нарушений или желающих предупредить возможность появления таких заболеваний.
Краткое содержание изобретения
Показано, что процианидины, присутствующие в какао, оказывают противотромбоцитное действие in vitro и in vivo. Показано также, что механизм противотромбоцитного действия осуществляется не через ингибирование метаболического пути арахидоновой кислоты. Кроме того, должно быть ясно, что лечение низкими дозами аспирина в сочетании с процианидинами какао обеспечивает усиленный противотромбоцитный эффект, превышающий противотромбоцитные эффекты данных двух отдельных режимов лечения. Следовательно, данное изобретение обеспечивает альтернативный длительный способ противотромбоцитной терапии без неприятных и опасных побочных эффектов, свойственных аспирину.
Описание фигур
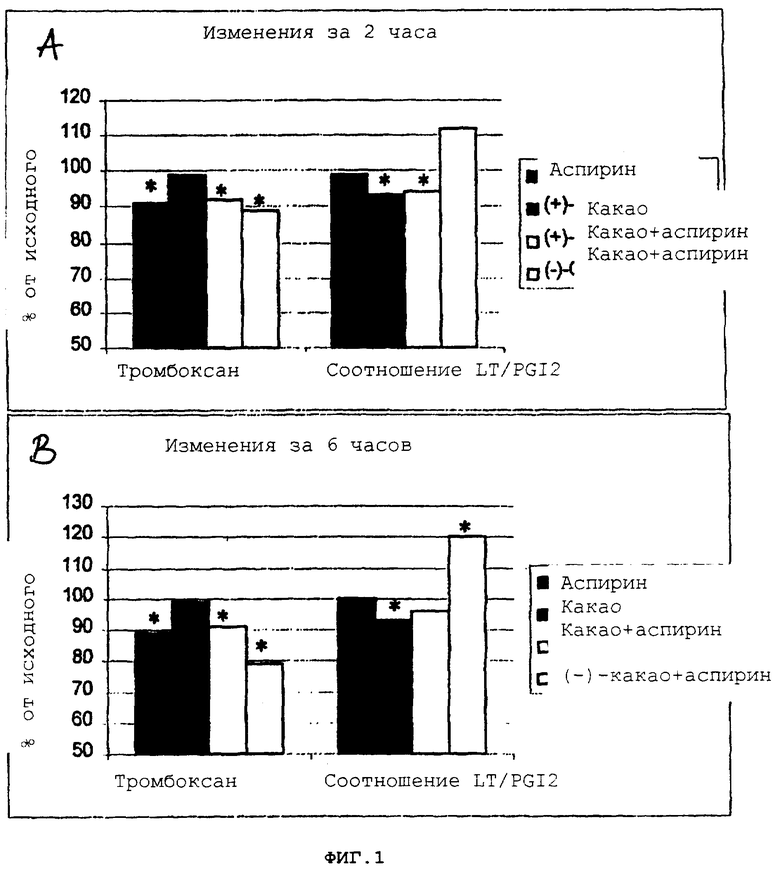
На фигуре 1А-В представлены сравнительные значения содержания тромбоксана и соотношения LT/PGI2 для четырех режимов лечения: аспирин, (+)-какао, аспирин в сочетании с (+)-какао и аспирин в сочетании с (-)-какао, регистрируемые через два временных интервала.
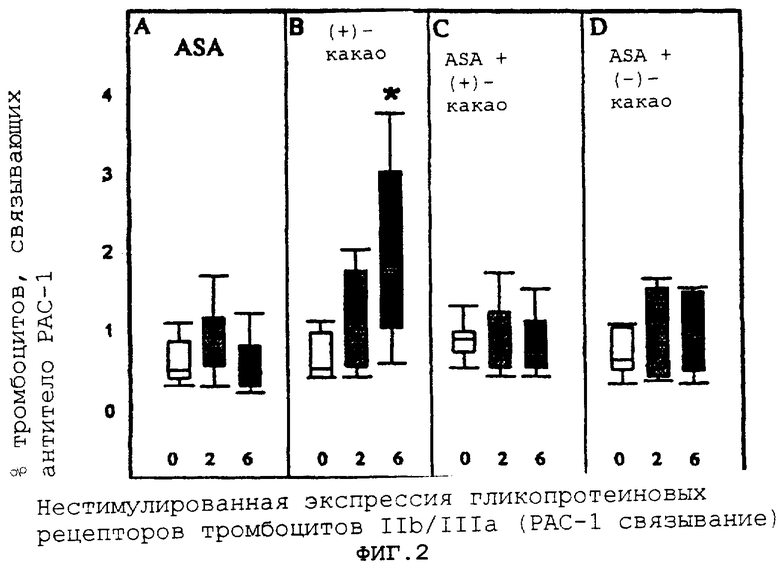
На фигуре 2A-D представлена сравнительная нестимулированная экспрессия рецепторов IIb/IIIa тромбоцитов для четырех режимов лечения: аспирин, (+)-какао, аспирин в сочетании с (+)-какао и аспирин в сочетании с (-)-какао, регистрируемая через два временных интервала.
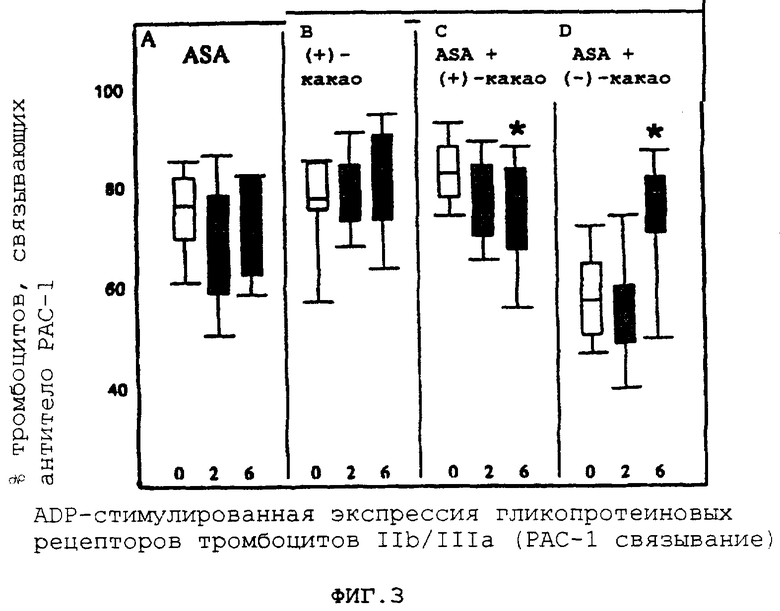
На фигуре 3A-D представлена сравнительная ADP-стимулированная экспрессия рецепторов IIb/IIIa тромбоцитов для четырех режимов лечения: аспирин, (+)-какао, аспирин в сочетании с (+)-какао и аспирин в сочетании с (-)-какао, регистрируемая через два временных интервала.
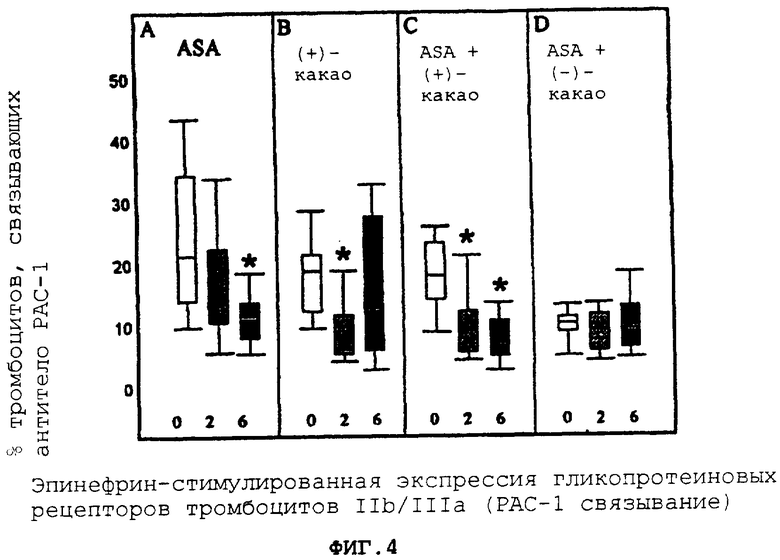
На фигуре 4A-D представлена сравнительная эпинефрин-стимулируемая экспрессия рецепторов IIb/IIIa тромбоцитов для четырех режимов лечения: аспирин, (+)-какао, аспирин в сочетании с (+)-какао и аспирин в сочетании с (-)-какао, регистрируемая через два временных интервала.
Подробное описание
Данное изобретение касается применения процианидинов какао в сочетании с аспирином в качестве противотромбоцитного терапевтического средства и композиций, содержащих процианидины какао и аспирин (ацетилсалициловую кислоту).
Использованное здесь выражение «процианидины какао» представляет мономеры и/или олигомеры эпикатехина и катехина. Термин «процианидины» также используют в данной области с более ограниченным значением, т.е. для обозначения олигомеров (но не мономеров) эпикатехина и катехина. Однако для краткости данный термин использован здесь для обозначения и мономеров, и олигомеров.
Данное изобретение касается композиции, включающей аспирин и процианидины какао. Композиция может быть приготовлена в любой подходящей форме, но обычно готовят в виде фармацевтической композиции, пищевого продукта, диетической добавки или пищевой добавки.
В одном варианте настоящее изобретение обеспечивает композицию, подходящую для приема внутрь, включающую аспирин и процианидины какао в физиологически приемлемом носителе. Данную композицию можно приготовить в любой подходящей форме, но обычно готовят в виде фармацевтической композиции, пищевого продукта, диетической добавки или пищевой добавки.
Настоящее изобретение обеспечивает также:
- применение аспирина и процианидинов какао в производстве медикамента, пищевого продукта, диетической добавки или пищевой добавки для лечения или профилактики заболевания или нарушения, вызванного дисфункцией тромбоцитов (такой как патологическая активация тромбоцитов, в противоположность нормальной активации тромбоцитов, что ведет к образованию сгустков и предотвращению кровотечения);
- применение аспирина в производстве медикамента, пищевого продукта, диетической добавки или пищевой добавки для использования с процианидином какао при профилактике или лечении заболевания или нарушения, вызванного дисфункцией тромбоцитов; и
- применение процианидина какао в производстве медикамента, пищевого продукта, диетической добавки или пищевой добавки для использования с аспирином при профилактике или лечении заболевания или нарушения, вызванного дисфункцией тромбоцитов.
Полифенолы какао включают процианидины, которые являются мономерами и/или олигомерами эпикатехина и катехина.
Мономеры процианидинов имеют структуру
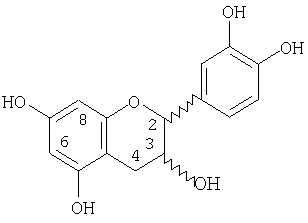
Процианидины включают вещества, обнаруженные в бобах какао, полученных от какао Theobroma и различных родственных видов какао, а также рода Herrania и их меж- и внутригенетических гибридов.
Мономеры процианидинов включают (+)-катехин, (-)-эпикатехин и их соответствующие эпимеры, (например, (-)-катехин, (+)-эпикатехин).
Синтетические линейные и/или разветвленные олигомеры, имеющие следующие структуры, являются иллюстрациями процианидинов какао.
Линейные олигомеры, где n равно целому числу от 0 до 16
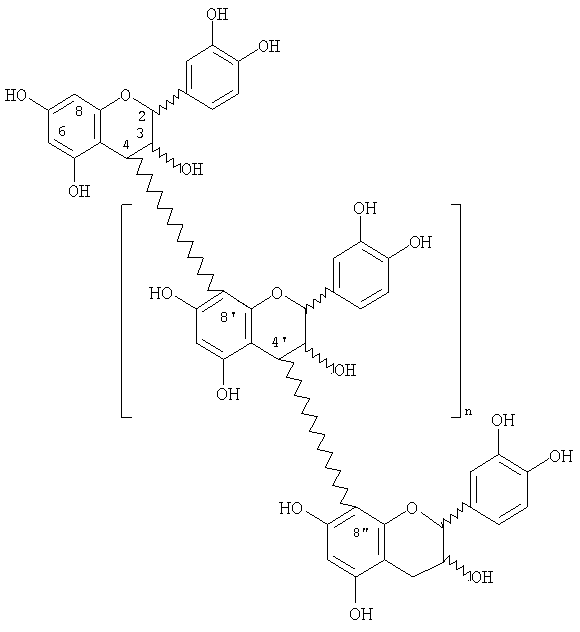
Разветвленные олигомеры, где А и В представляют собой независимые олигомеры от 1 до 15 при общем количестве звеньев в конечном олигомере 3-18.
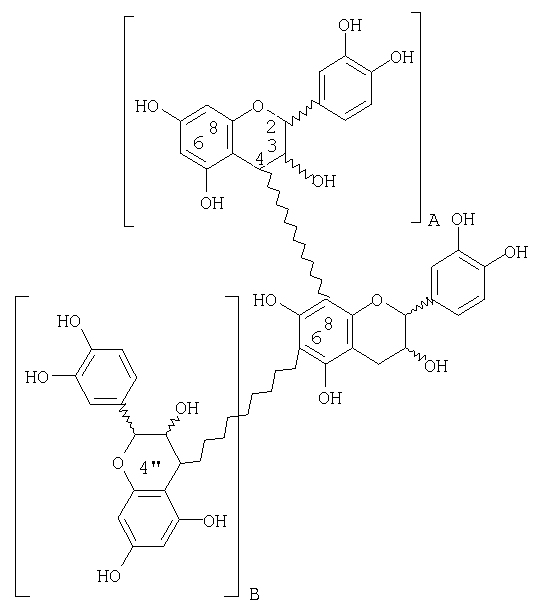
В данных олигомерах n равно целому числу от 2 до 18, предпочтительно от 3 до 12, более предпочтительно от 5 до 12 и наиболее предпочтительно 5. Олигомеры имеют связи между флаванами (4-6) и/или (4-8). Олигомеры могут быть представлены структурами, приведенными выше. Для линейного олигомера, если х равно 0, то олигомер называется «димером»; если х равно 1, то олигомер называется «тримером»; если х равно 2, то олигомер называется «тетрамером»; если х равно 3, то олигомер называется «пентамером»; и аналогично можно обозначить олигомеры, имеющие х до 18 включительно и выше, так, если х равно 18, то олигомер называется «октадекамером». Для разветвленного олигомера, если А или В равно 1, олигомер называется «тримером» с аналогичными обозначениями, как описано для линейных олигомеров.
Процианидины какао можно получить с помощью ингредиентов какао, в особенности ингредиентов какао, имеющих повышенное содержание процианидинов какао, или их можно получить синтетически. Ингредиентами какао являются вещества, получаемые из бобов какао, которые содержат процианидины какао и включают, например, шоколадный экстракт, масло какао, частично обезжиренные твердые вещества какао и/или полностью обезжиренные твердые вещества какао. Процианидины какао можно использовать в виде ингредиентов какао или их можно экстрагировать из бобов какао, молотых бобов какао или ингредиентов какао, которые упомянуты выше.
Способы определения содержания полифенолов какао описаны в патенте США №5554645 (от 10 сентября 1996), который включен здесь в виде ссылки. Собранные коробочки какао открывают и бобы с мякотью удаляют для сушки вымораживанием. Из высушенной вымораживанием массы вынимают вручную мякоть и проводят с бобами следующие манипуляции. Сначала высушенные вымораживанием бобы какао очищают от кожуры и измельчают до тонкой порошкообразной массы при помощи мельницы TEKMAR. Полученную массу далее обезжиривают в течение ночи экстракцией по Сокслету, используя в качестве растворителя повторно перегнанный гексан. Остаток растворителя удаляют из обезжиренной массы в вакууме при комнатной температуре.
Полифенолы какао, включая мономеры и/или олигомеры процианидина какао, можно также экстрагировать из свежих бобов какао, молотых бобов какао или фракций молотых бобов какао, предпочтительно из неферментированных, не полностью ферментированных бобов какао, которые имеют более высокое содержание полифенолов какао. Их можно также экстрагировать из шоколадного экстракта, частично обезжиренных твердых веществ какао и/или полностью обезжиренных твердых веществ какао, которые предпочтительно имеют более высокое содержание полифенолов. Используют растворитель, который растворяет полифенолы какао, включая процианидины.
Таким образом, в одном аспекте настоящего изобретения процианидины какао представляют олигомеры, мономеры или их смесь, причем данные олигомеры, мономеры или их смесь получают:
(а) подвергая обезжиренные молотые бобы какао, фракции молотых бобов какао, шоколадный экстракт, частично обезжиренные твердые вещества какао или полностью обезжиренные твердые вещества какао экстракции растворителем, используя растворитель, в котором растворимы процианидины какао; и
(b) выделяя из полученного экстракта какао фракцию, включающую мономер, олигомер процианидина или их смесь.
Подходящие растворители включают воду, метанол, этанол, ацетон, этилацетат или их смеси. Предпочтительные растворители представляют смеси воды и метанола или ацетона. Предпочтительная процедура экстракции представляет две экстракции смесью ацетон/вода/уксусная кислота (70%:29,5%:0,5%), с последующей третьей экстракцией смесью метанол/вода/уксусная кислота (70%:29,5%:0,5%). Растворители предпочтительно слегка подкислять. В некоторых случаях экстракт очищают, например, удаляя кофеин и/или теобромин, и далее очищают способом гель-проникающей хроматографии и/или жидкостной хроматографии высокого давления. Во время жидкостной хроматографии высокого давления экстракт можно фракционировать на мономерную и олигомерную фракции, содержащие, по меньшей мере, 50 мас.% мономеров или специфических олигомеров. Если фракции содержат мономеры и низшие олигомеры (до тетрамера включительно), фракции содержат примерно от 90 до 95 мас.% специфической олигомерной фракции.
В другом варианте полифенолы какао, обычно мономеры и/или олигомеры процианидина какао, присутствуют в ингредиентах какао (например, как описано выше), имеющих повышенные или сохраняемые уровни полифенолов какао. Повышенного содержания полифенолов какао можно достичь, добавляя к ингредиентам какао полифенолы какао, например мономеры, олигомеры процианидина или их смеси. Сохраняемого уровня полифенолов какао можно достичь, регулируя степень ферментации бобов какао, как обсуждается ниже, содержание полифенолов какао, включая содержание процианидинов какао, жаренных молотых бобов какао, шоколадного экстракта и частично обезжиренных или необезжиренных твердых веществ какао выше, если их получают из бобов какао или их смесей, которые неполностью ферментированы.
Сохраняемого уровня полифенолов какао можно также достичь, регулируя условия обработки бобов. Таким образом, способ получения из бобов какао масла какао и/или твердых веществ какао, имеющих сохраняемые уровни полифенолов какао, применяет уникальную комбинацию стадий обработки, которые не требуют отдельного оборудования для обжаривания бобов или измельчения экстракта, допуская выбор обработки бобов какао без тяжелой термической обработки в течение длительных периодов времени и/или экстракции жира. Выгода данного способа заключается в повышенной сохранности полифенолов в противоположность традиционным способам обработки какао, так что соотношение начального количества полифенола, обнаруженное в необработанных бобах к количеству, получаемому после обработки, составляет величину менее или равную 2.
Частично обезжиренные твердые вещества какао, имеющие высокое содержание полифенолов какао, включая высокое содержание процианидинов какао, можно получить при обработке бобов какао непосредственно до твердых веществ какао без стадии обжаривания бобов или молотых бобов. Данный способ сохраняет полифенолы какао, так как он опускает стадию традиционного обжаривания. Данный способ состоит, главным образом, из стадий: (а) нагревания бобов какао до внутренней температуры бобов, достаточной для снижения содержания влаги примерно до 3 мас.% и ослабления кожуры какао; (b) отсеивания молотых бобов какао от кожуры какао; (с) прессование с отжимом молотых бобов какао и (d) выделения масла какао и частично обезжиренных твердых веществ какао, которые содержат полифенолы какао, включая процианидины какао. До стадии нагревания бобы какао необязательно очищают, например, в воздушном сепараторе по плотности с псевдоожиженным слоем. Отсеивание также можно проводить в воздушном сепараторе по плотности с псевдоожиженным слоем. Предпочтительно нагревать бобы какао до внутренней температуры примерно от 100 до 110°С, более предпочтительно до температуры менее примерно 105°С, обычно применяя прибор инфракрасного нагревания в течение примерно 3-4 минут. Если требуется, твердые вещества какао можно подщелочить и/или размолоть до порошка какао.
Внутреннюю температуру бобов (IBT) можно измерить, заполнив бобами изолированный контейнер, такой как колба термоса (примерно 80-100 бобов). Затем изолированный контейнер закупоривают подходящим образом, чтобы сохранить температуру образца внутри него. В заполненный бобами изолированный контейнер вставляют термометр, и температура термометра уравновешивается с температурой бобов в термосе. Значение температуры представляет IBT бобов. IBT можно также считать равновесной температурой массы бобов.
Бобы какао можно разделить на четыре категории на основании их цвета: преобладающе коричневые (полностью ферментированные), пурпурно-коричневые, пурпурные и темно-серые (неферментированные). Предпочтительно, как указано выше, получать твердые вещества какао из неполностью ферментированных бобов какао, которые имеют более высокое содержание полифенолов какао, чем ферментированные бобы. Неполностью ферментированные бобы включают темно-серые бобы какао, пурпурные бобы какао, смесь темно-серых, пурпурных и коричневых бобов какао. Более предпочтительны темно-серые и/или пурпурные бобы какао. Неполностью ферментированные бобы обычно имеют коэффициент ферментации 275 или менее.
«Коэффициент ферментации» определяют, используя систему градации для характеристики ферментации бобов какао. Темно-серые обозначают 1, пурпурные - 2, пурпурно-коричневые - 3 и коричневые - 4. Процент бобов, попадающих в каждую категорию, умножают на массовое число. Таким образом, «коэффициент ферментации» для образца, состоящего из 100% коричневых бобов, составил бы 100×4 или 400, тогда как для образца из 100% пурпурных бобов он составил бы 100×2 или 200. Образец, состоящий из 50% темно-серых бобов и 50% пурпурных бобов, имеет коэффициент ферментации 150 [(50×1)+(50×2)].
В одном варианте можно применять в сочетании с аспирином производные процианидинов какао, например производные процианидинов и галловой кислоты и метилированные процианидины. К производным процианидина применимы также любые ссылки, сделанные здесь в отношении процианидинов какао и их применения. Производные процианидинов и галловой кислоты можно получить, как описано в международной патентной заявке №PCT/US98/21392, опубликованной как WO 99/19319. Метилированные процианидины можно получить, как описано, например, в примере 6.
В одном аспекте данного изобретения метилированный процианидиновый мономер или олигомер имеет формулу (А)n, где n равно от 1 до 18, и А представляет мономерное звено формулы
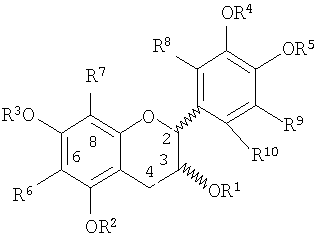
где каждый из R1-R5 и R8-R10, которые являются одинаковыми или разными, представляет собой Н или СН3; и R6 и R7, которые являются одинаковыми или разными, представляют собой Н, СН3 или связь с соседним мономерным звеном; при условии, что, по меньшей мере, одна группа от R1 до R10, по меньшей мере, в одном мономерном звене является СН3. Мономеры могут быть связаны, например, по одному или двум кольцевым положениям 4, 6 и 8 связями между флаванами, описанными выше.
В другом аспекте данного изобретения метилированный процианидиновый мономер или олигомер имеет формулу (А')n, где n равно от 1 до 18 и А' представляет мономерное звено формулы
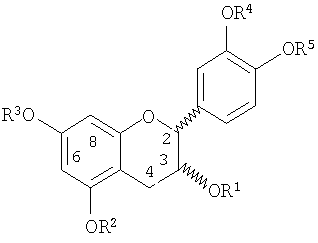
где каждый из R1-R5 и R8-R10, которые являются одинаковыми или разными, представляет Н или СН3; при условии, что, по меньшей мере, одна группа от R1 до R5, по меньшей мере, в одном мономерном звене является СН3. Мономеры могут быть связаны, например, по одному или двум кольцевым положениям 4, 6 и 8 связями между флаванами, описанными выше.
Например, олигомер может быть линейным олигомером следующей структуры, где n равно от 0 до 16
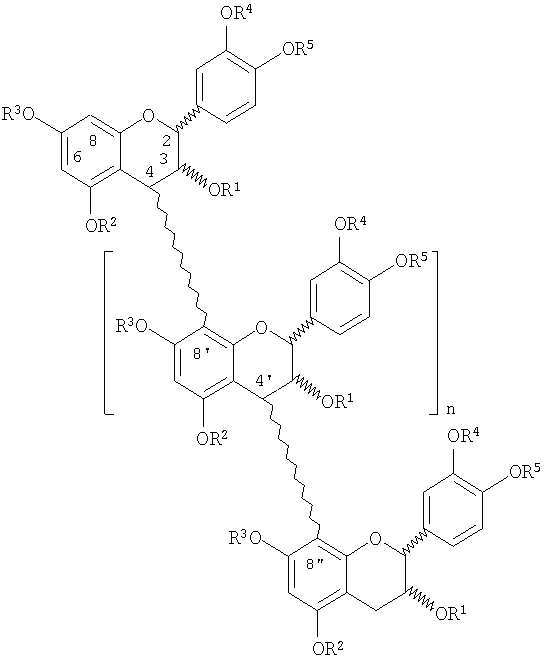
где R1-R5 такие, как определены выше.
Альтернативно, или дополнительно, олигомер может быть разветвленным олигомером следующей структуры, где А и В представляют собой независимые олигомеры от 1 до 15 с общим количеством звеньев в конечном олигомере 3-18
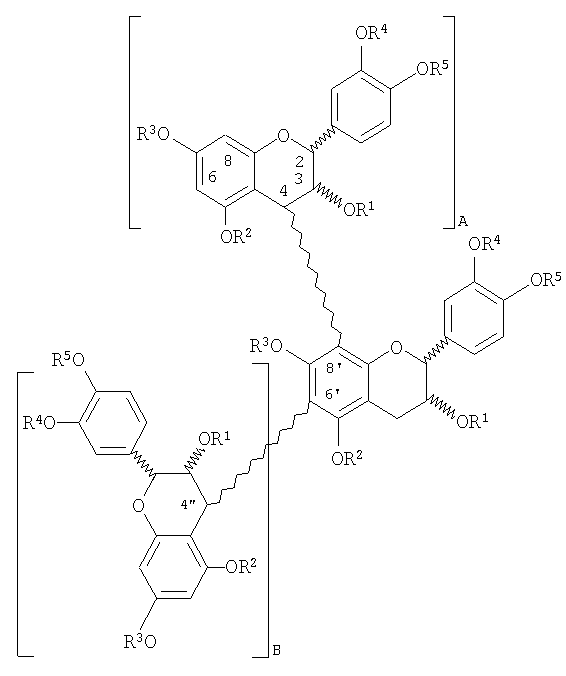
где R1-R5 определены выше.
В другом варианте данное изобретение обеспечивает олигомер процианидина или смесь олигомеров, где каждый указанный олигомер представляет метилированный тетрамер.
Например, метилированный тетрамер является соединением формулы (А)4, где А представляет мономерное звено формулы
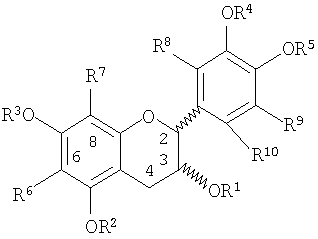
где каждый из R1-R5 и R8-R10, которые являются одинаковыми или разными, представляет собой Н или СН3; и R6 и R7, которые являются одинаковыми или разными, представляют собой Н, СН3 или связь с соседней мономерной единицей; при условии, что, по меньшей мере, одна группа от R1 до R10, по меньшей мере, в одном мономерном звене является СН3. Мономеры могут быть связаны, например, по одному или двум кольцевым положениям 4, 6 и 8 связями между флаванами, описанными выше.
Альтернативно, метилированный тетрамер может быть соединением формулы (А')4, где А' представляет мономерное звено формулы
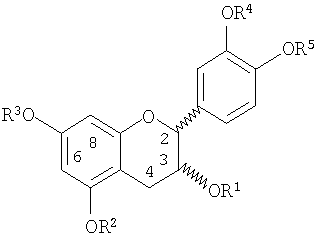
где каждый из R1-R5, которые являются одинаковыми или разными, представляет собой Н или СН3; при условии, что, по меньшей мере, одна группа от R1 до R5, по меньшей мере, в одном мономерном звене является СН3. Мономеры могут быть связаны, например, по одному или двум кольцевым положениям 4, 6 и 8 связями между флаванами, описанными выше.
Тетрамер метилированного процианидина какао или смесь тетрамеров данного изобретения можно получить метилированием выделенной фракции экстракта какао, содержащей тетрамеры процианидинов, или полученного синтетически тетрамера. Например, тетрамер может иметь формулу (А)4, приведенную выше.
В одном варианте обеспечен тетрамер метилированного процианидина какао или смесь тетрамеров данного изобретения, причем данный тетрамер или смесь можно получить:
(a) подвергая обезжиренные молотые бобы какао, фракции молотых бобов какао, шоколадный экстракт, частично обезжиренные твердые вещества какао или полностью обезжиренные твердые вещества какао экстракции растворителем, в котором растворимы процианидины какао;
(b) выделяя фракцию, содержащую тетрамеры процианидинов, из полученного экстракта какао и
(c) метилируя выделенную фракцию.
Метилированный олигомер процианидина какао или смесь олигомеров, где указанный олигомер или смесь можно также получить:
(a) подвергая обезжиренные молотые бобы какао, фракции молотых бобов какао, шоколадный экстракт, частично обезжиренные твердые вещества какао или полностью обезжиренные твердые вещества какао экстракции растворителем, в котором растворимы процианидины какао;
(b) выделяя фракцию, содержащую олигомеры процианидинов, из полученного экстракта какао и
(с) метилируя выделенную фракцию.
Композиция настоящего изобретения находится в виде, подходящем для пероральной доставки, таком как таблетки, капсулы, гранулы, концентраты, порошки, жидкости, растворы или суспензии. Предпочтительно представлять ее в виде фармацевтической композиции, пищевого продукта, диетической или пищевой добавки. Она может также быть в виде ингредиента для корма домашних животных. Композиция может быть приготовлена в виде стандартных дозированных форм.
Активные соединения можно приготовить в виде формы с немедленным или отсроченным высвобождением. Таблетка может включать эффективное количество полифенола какао, мономеров и/или олигомеров процианидинов какао или композицию, содержащую полифенолы или процианидины какао, в сочетании с эффективным количеством аспирина и необязательно носитель или систему высвобождения активного ингредиента. В приготовлении композиции с регулируемым высвобождением особо полезны синтетические полимеры. Капсула может включать желатиновую капсулу, содержащую предварительно определенную дозу полифенола какао и аспирин-содержащую композицию. Продукт для пероральной доставки может также включать диетическую пищевую добавку, такую как дикальцийфосфат, стеарат магния, нитрат кальция, витамины и минералы. Препараты комбинаций процианидинов какао/аспирина и содержащие их композиции можно получить по стандартным методикам, хорошо известным специалистам в фармацевтической, пищевой науке, медицине и ветеринарии.
Получают композицию для доставки объединенной эффективной дозы процианидина (процианидинов) какао и аспирина. Эффективное количество процианидина какао можно вводить в виде однократной дозы или, альтернативно, два-три раза в день. Для человека эффективное дневное количество составляет, по меньшей мере, 50 мг, предпочтительно 100 мг и более предпочтительно 150 мг процианидинов какао. Максимальная доза не ограничена. Например, можно принимать процианидины в количестве примерно от 50 до 1000 мг, примерно от 100 до 800 мг, примерно от 300 до 600 мг, или принимать минимальные указанные дозы без ограничения максимальной дозы, например, по меньшей мере, 50, 100 или 300 мг/мл. Если препарат применяют в ветеринарии, например вводят кошкам, лошадям или собакам, специалист в данной области может определить эффективное количество из указанных выше дозировок, принимая во внимание, например, вес животного. Количество процианидинов можно определить способами, описанными в работе Adamson и др. ("HPLC Method for the Quantification of Procianidins in Cocoa and Chocolate Samples and Correlation to Total Antioxidant Capacity", J. Ag. Food Chem., Vol.7:10, 4184-4188), часть которой, относящаяся к делу, включена здесь в виде ссылки. Благодаря усиленным эффектам, достигаемым при введении аспирина в сочетании с процианидинами какао, его можно принимать с меньшей дозой, чем это необходимо, если применяют только аспирин в противотромбоцитной терапии, для достижения защитных сердечно-сосудистых эффектов, что составляет, например, 80 мг/день для человека. Таким образом, в способах и/или композициях данного изобретения аспирин можно использовать в количестве менее 80 мг/день, например, примерно от 10 до 80 мг/день и предпочтительно примерно от 20 до 80 мг/день. В других вариантах аспирин можно принимать примерно от 40 до 80 мг/день или при введении менее 70 мг/день примерно от 20 до 70 мг/день или примерно от 30 до 70 мг/день.
Кроме объединенной единой композиции для перорального приема процианидин (процианидины) какао и аспирин можно готовить в виде препаратов для раздельного приема. Согласно настоящему изобретению обеспечен также продукт, содержащий аспирин и процианидин какао, для раздельного одновременного или последовательного приема при лечении заболевания или нарушения, вызванного дисфункцией тромбоцитов. При раздельном приеме процианидин какао и аспирин следует вводить в течение периода времени, который гарантирует, что они одновременно присутствуют в организме млекопитающего при достаточных концентрациях для сочетанного эффекта. Специалист в данной области может определить такой период времени, основываясь на знаниях биологической доступности процианидинов какао и аспирина. Например, процианидины какао и аспирин следует вводить млекопитающему в течение 8 часов друг за другом, предпочтительно в течение 6 часов друг за другом и более предпочтительно в течение двух часов друг за другом.
Полифенол какао обычно присутствует в ингредиенте какао с повышенным или сохраняемым уровнем полифенолов какао, обеспеченным, например, как описано выше. Таким образом, в одном аспекте ингредиент какао содержит твердые вещества какао, которые можно получить:
(a) нагреванием бобов какао до внутренней температуры бобов, достаточной для снижения содержания влаги примерно до 3 мас.% и ослабления кожуры какао;
(b) отсеиванием молотых бобов какао от кожуры какао;
(c) прессованием с отжимом молотых бобов какао и
(d) выделением масла какао и частично обезжиренных твердых веществ какао, которые содержат полифенолы какао.
В предпочтительном варианте ингредиент какао с повышенным или сохраняемым уровнем полифенолов какао содержится в смеси для напитков, из которой готовят напитки для совместного приема с эффективным количеством аспирина. Предпочтительный напиток или смесь напитков включает: твердые высшие полифенолы какао и/или экстракт какао и необязательно природный или искусственный подслащающий агент, природный или синтетический ароматизатор и пищевой продукт. Напиток также может быть насыщен углекислым газом. Подслащающий агент может представлять сахарный сироп, твердый сахар или заменитель сахара. Термин «заменитель сахара» включает объемные агенты, сахарный спирт (т.е. полиолы, такие как глицерин), высокоэффективные подслащающие агенты или их комбинации. Пищевыми углеводородными подслащающими агентами с разными степенями интенсивности подслащивания могут быть любые из обычно применяемых в данной области агентов, включая (но не ограничиваясь этим) сахарозу, декстрозу, фруктозу, лактозу, мальтозу, твердые сиропы глюкозы, твердые кукурузные сиропы, инвертированный сахар, гидролизованную лактозу, мед, кленовый сахар, коричневый сахар, мелассу и подобное. Заменители сахара могут частично или полностью заменять пищевой углеводородный подслащающий агент. Высокоэффективные заменители сахара включают аспартам, цикламаты, сахарин, ацесульфам-К, неохесперидин, дигидрохалькон, сукралозу, алитам, подсластитель на основе посконника крапиволистного, глицирризин, тауматин и подобное, а также их смеси. Примеры сахарных спиртов включают обычно применяемые в данной области спирты, такие как сорбит, маннит, ксилит, мальтит, изомальт, лактит и подобные. Примерами молочных компонентов являются сухое обезжиренное молоко, молочный жир, сладкие сливки, кефир и снятое молоко.
Для целей данной заявки следующие определения позволят яснее понять то, что раскрыто и заявлено.
Используемый здесь термин «пищевой продукт» обозначает материал, состоящий по существу из белка, углевода и/или жира, который используется в организме для процессов поддержания роста, восстановления и жизнедеятельности и снабжения энергией. Пищевые продукты могут также содержать дополнительные вещества, такие как минералы, витамины и приправы. Смотри Merriam-Webster's Collegiate Dictionary, издание 10-е, 1993.
Используемые здесь термины «фармацевтический препарат» или «медикамент» обозначают лекарственные средства. Смотри Merriam-Webster's Collegiate Dictionary, издание 10-е, 1993.
Используемые здесь термины «пищевая добавка» или «диетическая добавка» обозначают продукт (отличный от табака), который, как подразумевается, дополняет пищу, который имеет или содержит один или более из следующих пищевых ингредиентов: витамин, минерал, трава или другой растительный продукт, аминокислота, пищевое вещество для применения человеком с целью добавления к пище при повышении общего дневного потребления, или концентрат, метаболит, составная часть, экстракт или комбинация данных ингредиентов. Смотри Merriam-Webster's Collegiate Dictionary, издание 10-е, 1993.
Используемый на этикетках пищевых продуктов термин «добавка» обычно означает, что к питательным веществам добавлено количество, более чем на 50% превышающее U.S. RDA («Understanding Normal and Clinical Nutirition, Third Edition», редакторы Whitney, Cataldo and Rolfes, стр.525).
Для лечения или профилактики любых нарушений или заболеваний, вызванных дисфункцией тромбоцитов, можно вводить (человеку или животному, такому как домашнее животное) процианидин какао, или смесь мономеров и/или олигомеров процианидинов какао, или композицию, содержащую мономеры и/или олигомеры процианидинов какао, в сочетании с эффективным количеством только аспирина, или аспирина с другими лекарственными средствами, как описано практикующими специалистами-медиками, в соответствии со способами, включенными в данное описание и известными в данной области. Например, лечение, включающее совместное введение аспирина и процианидинов какао, может быть назначено практикующим специалистом-медиком при первых признаках или симптомах дисфункции тромбоцитов или вскоре после этого, как требуется, без необходимости чрезмерного исследования. Таким образом, композиция и способы лечения данного изобретения можно применять, например, на пациентах, страдающих или с риском развития сердечно-сосудистых заболеваний, которые включают инфаркт, инсульт и периферические сосудистые заболевания, периферические артериальные заболевания, заболевание коронарных артерий, заболевание сонной артерии, атеросклероз, рестиноз.
Совместное введение процианидинов какао и аспирина или их композиции, отдельно или совместно с другими лекарственными средствами, можно продолжать по схеме, например, в течение месяца, в течение двух месяцев, в течение двух лет, в течение года, или по другой схеме лечащего специалиста-медика в течение необходимого периода времени без необходимости чрезмерного исследования.
Кроме того, область данного изобретения включает упаковку, содержащую пищевой продукт, диетическую добавку или медикамент и этикетку, указывающую повышенное содержание полифенолов какао, включая процианидины какао, в сочетании с аспирином, или указывающую полезные свойства данных соединений, и необязательно инструкции по применению. Используемое здесь понятие «полезные свойства» включает ингибирование дисфункции тромбоцитов, например, при профилактике или лечении сердечно-сосудистых заболеваний и нарушений, вызванных воспалением.
Данное изобретение описано, кроме того, в следующих неограничительных примерах.
Пример 1
Аналитические способы количественного определения процианидинов какао
Описанный ниже аналитический способ применяют для разделения и количественного определения по степени полимеризации композиции процианидинов в семенах Theobroma cacao и шоколаде. Описанный ниже аналитический способ основан на работе, представленной Hammerston J.F., Lazarus S.A., Mitchel A.E., Rucker R., Schmitz H.H., Identification of Procyanidins in Cocoa (Theobroma cacao} and Chocolate Using High-Performance Liquid Chromatography/Mass Spectrometry, J. Ag. Food Chem., 1999, 47(10), 490-496). Описанный ниже аналитический способ применяют для количественного исследования широкого диапазона образцов пищевых продуктов и напитков, которые содержат разнообразные типы проантоцианидинов, как сообщается в работе Lazarus S.A., Adamson G.E., Hammerston J.F., Schmitz H.H, High-Performance Liquid Chromatography/Mass Spectrometry Analysis of Proanthocyanidins in Foods and Beverages, J. Ag. Food Chem., 1999, 47(9), 3693-3701). В работе Lazarus S.A. и др. (1999) излагается исследование, использующее детектирование флюоресценции вследствие ее высокой селективности и чувствительности.
Для каждого олигомера процианидина до декамера получают стандартные составные основные растворы и калибровочные кривые, применяя описанный ниже аналитический способ, который приведен в работе Adamson G.E., Lazarus S.A., Mitchel A.E., Prior R.L., Cao G., Jacobs P.H., Kremers B.G., Hammerston J.F., Rucker R., Ritter K.A., Schmitz H.H., HPLC Method for the Quantification of Procyanidins in Cocoa and Chocolate Samples and Correlation to Total Antioxidant Capacity, J. Ag. Food Chem., 1999, 47(10), 4184-4188. Затем образцы сравнивают с составными стандартами для точного определения содержания процианидинов.
Экстракция
Свежие семена (бразильских бобов какао) размалывают на высокоскоростной лабораторной мельнице с жидким азотом до уменьшения размера частиц примерно до 90 микрон. Из 220 граммов (г) семян удаляют липиды, трижды проводя экстракцию 1000 мл гексана. Не содержащие липидов твердые вещества сушат на воздухе, получая примерно 100 г обезжиренного материала. Фракцию, содержащую процианидины, получают экстракцией 1000 мл 70 об.% ацетона в воде. Суспензию центрифугируют в течение 10 мин. при 1500 g. Ацетоновый слой декантируют через воронку со стекловолокном. Затем водный ацетон повторно экстрагируют гексаном (˜75 мл), удаляя остаток липидов. Гексановый слой отбрасывают, а водный ацетон выпаривают на роторе в частичном вакууме при 40°С до конечного объема 200 мл. Водный экстракт сушат вымораживанием, получая примерно 19 г ацетонового экстрагированного материала.
Гель-хроматография
Примерно 2 г ацетонового экстракта (полученного выше) суспендируют в 10 мл 70% водного метанола и центрифугируют при 1500 g. Супернатант полуочищают на колонке Sephadex LH-20 (70×3 см), которую предварительно уравновешивают метанолом, при скорости потока 3,5 мл/мин. Через два с половиной часа после загрузки образца собирают фракции каждые 20 мин и анализируют способом ВЭЖХ на теобромин и кофеин. Смотри работу Clapperton J., Hammerstone J.F., Romanczyk L.J., Yow S., Lim D., Lockwood R., Polyphenols and Cocoa Flavour, Proceedings, 16th International Conference of Groupe Polyphenols, Lisbon, Portugal, Groupe Polyphenols: Norbonne, France, 1992; т.II, стр.112-115. После того, как теобромин и кофеин будут элюированы из колонки (˜3,5 час), оставшийся элюат собирают еще 4,5 час и выпаривают на роторе в частичном вакууме при 40°С для удаления органического растворителя. Затем экстракт суспендируют в воде и сушат вымораживанием.
Очистка олигомеров процианидина способом препаративной ВЭЖХ с нормальной фазой
Полученный выше экстракт какао (0,7 г) растворяют в смеси (7 мл) ацетон/вода/уксусная кислота с объемным соотношением 70%:29,5%:0,5% соответственно. Для разделения фракций процианидинов применяют линейный градиент (показан ниже в таблице), используя 5 мкм колонку Supelcosil LC (Silica, 100 ангстрем Å)(50x2 см) (Supelco, Inc., Bellefonte, Pennsylvania), под контролем УФ при длине волны 280 нм.
Фракции собирают на плато между пиками, соответствующими олигомерам. Фракции с равными временами удерживания от нескольких препаративных делений объединяют, выпаривают на роторе в частичном вакууме и сушат вымораживанием.
Анализ очищенных фракций способом ВЭЖХ/МС
Для определения чистоты индивидуальных олигомерных фракций проводят анализ, применяя способ высокоэффективной жидкостной хроматографии (ВЭЖХ), сопряженный с масс-спектральным (МС) анализом в диалоговом режиме, используя камеру для ионизации при атмосферном давлении электрораспылением (API-ES), как описано в работе Lazarus и др. (1999), выше. Хроматографический анализ проводят на приборе серии HP 1100 (Hewlett-Packard, Palo Alto, California), оснащенном автоматическим инжектором, четвертичной ВЭЖХ-помпой, нагревателем колонки, диодным матричным детектором и HP ChemStation для сбора данных и манипуляций. Разделение на нормальной фазе олигомеров процианидинов проводят на колонке с диоксидом кремния Phenomenex (Torrance, California) Luna (25×4,6 мм) при 37°С. УФ-детектирование проводят при длине волны 280 нм. Тройная подвижная фаза состоит из (А) дихлорметана, (В) метанола и (С) уксусной кислоты и воды (1:1 об./об.). Деление осуществляют сериями линейных градиентов (В) в (А) при постоянных 4% (С) со скоростью потока 1 мл/мин следующим образом: начинают элюирование при 14% (В) в (А); 14-28,4% (В) в (А), 0-30 мин; 28,4-50% (В) в (А), 30-60 мин; 50-86% (В) в (А), 60-65 мин и 65-70 мин изократически.
ВЭЖХ/МС-анализ очищенных фракций проводят, используя описанный выше хроматограф ВЭЖХ серии HP 1100, который сопряжен с масс-селективным детектором HP серии 1100 (модель G1946A) и оснащен ионизационной камерой API-ES. В поток элюента ВЭЖХ непосредственно перед масс-спектрометром добавляют через тройник буферный реагент и доставляют при помощи ВЭЖХ-помпы серии HP 1100, обходя дегазатор. Условия анализа в модели с отрицательными ионами включают в качестве буферного реагента 0,75М гидроксид аммония при скорости потока 0,04 мл/мин, капиллярный вольтаж 3 кВ, фрагментацию при 75 В, давление распыления 25 фунтов/кв.дюйм и температуру осушающего газа 350°С. Данные собирают на HP ChemStation, используя способ сканирования и мониторинга выбранных ионов (SIM). Спектры сканируют в диапазоне масс m/z 100-3000 при 1,96 сек./цикл. Гидроксид аммония используют для регулировки рН элюирующего раствора около нейтрального значения рН посредством дополнительной вспомогательной помпы непосредственно перед входом в МС. Данная обработка противодействует подавлению отрицательной ионизации (-)-эпикатехинового стандарта в результате повышенной концентрации кислоты в подвижной фазе. Чистоту каждой фракции определяют по площади пика, применяя УФ-детектирование при длине волны 280 нм в комбинации со сравнением соотношения содержания ионов для каждого класса олигомеров.
Количественное определение процианидинов в какао и шоколаде
Готовят составной стандарт для мономера, используя коммерчески доступный (-)-эпикатехин. Димеры получают из декамеров в очищенном виде описанными выше способами. Стандартные основные растворы, использующие данные соединения, анализируют с применением способа ВЭЖХ с нормальной фазой, описанного выше, с детектированием флуоресценции при возбуждении и эмиссии при 276 нм и 316 нм соответственно. Пики группируют, суммируют их площади для включения вкладов от всех изомеров внутри одного класса олигомеров и получают калибровочные кривые, применяя квадратичную подгонку. Мономеры и небольшие олигомеры имеют почти линейные графики, которые согласуются с предыдущим применением линейной регрессии для получения калибровочных кривых на основе мономера и на основе димера.
Данные калибровочные кривые затем используют для расчета содержания процианидинов в образцах, приготовленных следующим образом: сначала образец какао или шоколада (около 8 г) обезжиривают, трижды экстрагируя гексаном (45 мл каждый раз). Затем один грамм обезжиренного материала экстрагируют 5 мл смеси ацетон/вода/уксусная кислота (70:29,5:0,5 об./об.). Затем определяют количество процианидинов в обезжиренном материале, сравнивая данные ВЭЖХ образцов с калибровочными кривыми, полученными, как описано выше (которые используют очищенные олигомеры). Процентное содержание жира в образцах (используя образец весом один грамм для шоколада или полграмма для экстракта) определяют, применяя способ, стандартизованный Association of Official Analytical Chemists (AOAC Official Method 920.177). Затем рассчитывают общее количественное содержание процианидинов в исходном образце (с жиром). Перед прогоном каждого образца проводят калибровку для защиты от вариаций при переходе от одной колонки к другой.
Пример 2
Клинические исследования
В рандомизированном клиническом испытании участвовало шестнадцать пациентов, которые принимают аспирин, напиток с высоким содержанием процианидина или их комбинацию. Пациенты практически здоровы, не курили, и их возраст составлял от 20 до 55 лет. Конкретные участники представляли объекты случайного выбора.
Участников инструктируют, чтобы они воздерживались от приема нестероидных противовоспалительных препаратов в течение, по меньшей мере, 4 дней, от алкогольных напитков, по меньшей мере, в течение 2 дней и от пищи, содержащей кофеин или теобромин, по меньшей мере, в течение 24 часов до исследования и в день исследования. Пациентов инструктируют, чтобы вечером перед исследованием они употребляли в пищу продукты с низким фитохимическим содержанием и не ели с 22 час [Фитохимические продукты являются компонентами растений. Примеры пищевых продуктов и напитков, которые имеют высокое фитохимическое содержание, включают многие фрукты, кофе, некоторые чаи, зеленый перец, чеснок, лук, йогурт, отруби и крестоцветные овощи, такие как брокколи, капуста и цветная капуста].
До приема пищи у пациентов берут кровь. После начального отбора крови пациентов делят на четыре группы. Одна группа принимает 81 мг аспирина (ацетилсалициловой кислоты, детского аспирина Bayer). Вторая группа принимает напитки с высоким содержанием полифенолов какао, включающие 18,75 г обогащенного процианидинами порошка какао, полученного из бобов Sulawesi (с общим содержанием процианидинов 51,1 мг/г, жиров 11,2%, кофеина 0,092%, теобромина 1,618%), и 12,5 г сахарозы в смеси с 300 мл дистиллированной воды. Третья группа принимает напиток с высоким содержанием процианидинов какао и 81 мг детского аспирина. Последняя группа принимает 81 мг детского аспирина напиток какао с дефицитом процианидинов, состоящий из 18,75 г порошка какао (с общим содержанием процианидинов 0,45 мг/г, жиров 9,87%, теобромина 2,063%, кофеина 0,234%) к 12,5 г сахарозы в смеси с 300 мл дистиллированной воды. Во время исследования пациентам позволяют пить воду, содовую воду без кофеина, бублики, сливочный сыр с низким содержанием жира и бананы. У каждого пациента берут кровь через два часа и через шесть часов после приема препарата. Венозную кровь помещают в пробирки под вакуумом, содержащие 0,5 мл 3,2% буферированного раствора цитрата натрия.
Ингибирование агрегации тромбоцитов определяют, используя анализатор функции тромбоцитов (PFA-100™, Dade Behring International, Miami, Fla.) в соответствии с инструкциями производителей. Данная система содержит микропроцессор - регулируемый прибор и сменный тестовый картридж, содержащий биологически активную мембрану. Прибор отбирает образец крови из резервуара с образцом при постоянном вакууме через капилляр и микроскопическое отверстие, прорезанное в мембране. Мембрану покрывают коллагеном и эпинефрином. Присутствие данных биохимических раздражителей и высокие скорости сдвига, генерируемые при стандартизованных условиях потока, приводят к прикреплению, активации и агрегации тромбоцитов, медленно создавая устойчивую пробку из тромбоцитов на отверстии. Время в секундах, необходимое для получения полной закупорки отверстия, называют «временем закрытия» (Kundu и др., «Description of an in vitro platelet function analyzer - PFA-100» Semin Thromb Hemost., 21 Supple 2: 106-12, 1995). Хорошо известно, что в результате лечения аспирином происходит снижение агрегации тромбоцитов, которое является причиной повышения времени закрытия, измеряемого при помощи PFA-100 (Marshall и др., «A comparison of the effects of aspirin on bleeding time measured using the Simplate method and closure time measured using the PFA-100, in healthy volunteers», Br. J. Clin. Pharmacol., 44: 151-155, 1997).
Результаты показывают, что во временной точке, соответствующей двум часам, все четыре режима лечения приводят к увеличению времени закрытия по сравнению с исходным уровнем (р<0,05). Кроме того, сравнение режима лечения аспирин и какао плюс аспирин показывает разницу во времени закрытия для данных двух режимов лечения (р<0,08). Это показывает, что сочетание аспирина с олигомерами процианидинов какао усиливает способность аспирина ингибировать активацию тромбоцитов. Нет разницы во временах закрытия после применения только аспирина и аспирина плюс какао с СР-дефицитом, это показывает, что эффект усиления зависит от присутствия в какао процианидинов. Данные результаты также демонстрируют, что режимы лечения аспирином плюс какао и аспирином плюс какао с СР-дефицитом существенно различаются по своим временам закрытия (р<0,06), подтверждая, что эффекты усиления комбинации какао/аспирин зависят от присутствия процианидинов.
Образцы крови также анализируют на изменения содержания лейкотриена, простациклина и тромбоксана в результате четырех режимов лечения. Процедуры иммунологического исследования проводят, как описано в работах Westcott и др. «Analysis of 6-Keto PGF1 Alpha, 5-HETE, and LTC4 in Rat Lung: Comparison of GM/MS, RIA and EIA», Prostaglandins, 32: 857-873, 1986; Yakota и др. «Enzyme Immunoassay of Prostanoids in Blood and Urine», Adv. Prostgl. Thrombox. Leukot. Res., 15: 33-34, 1985 и Schramm и др. «Differential Effects of Small and Large Molecular Weight Phytochemicals on Endothelial Cell Eicosanoid Secretion», J. Agric Food Chem., 46: 1900-1998. Простациклин (PGI2), метаболит 6-кетопростагландина Fl-альфа, определяют в иммунологическом исследовании с ферментом Cayman #515211, тромбоксан (TXA2), метаболит ТХВ2, определяют в иммунологическом исследовании с ферментом Cayman #519031 и лейкотриены С4, D4 и Е4 количественно определяют, применяя иммунологическое исследование ЕА-39 от Oxford Biomedical Research. Величины Р рассчитывают, используя Т-тест парных образцов. Величины р<0,05 считают статистически значимыми. Данные исследования эйкозаноидов представлены в таблице 1 и на фигуре 1. Все режимы лечения кроме лечения аспирином плюс какао без процианидина дают в результате снижение отношения атерогенных эйкозаноидов к атеростатическим, показывая, что все режимы лечения положительно влияют на состояние сосудов и профилактику ишемических приступов, и что увеличение времени закрытия после лечения, по крайней мере, частично происходит в результате модуляции эйкозаноидов. Результаты показывают, что препарат СР-обогащенного какао плюс аспирин вызывает снижение содержания атерогенных лейкотриенов и увеличение содержания атеростатического простациклина. По сравнению с этим лечение препаратом какао с СР-дефицитом плюс аспирин дает в результате снижение содержания простациклина и повышение содержания лейкотриенов. Данные результаты показывают, что атеростатические эффекты какао зависят от присутствия процианидинов.
Интересно, что данные результаты предполагают, что механизмы, которые обеспечивают антитромбоцитную активность, различны при режиме лечения аспирином и какао с высоким содержанием процианидинов. Механизм действия аспирина осуществляется через ингибирование метаболического пути арахидоновой кислоты (ингибированием продуцирования простагландина), что приводит к понижению уровней тромбоксана, приводя к предотвращению тромбоксан-зависимой активации тромбоцитов. Это объясняет антитромбоцитное действие аспирина. Как можно видеть из таблицы 1, все три способа, включающие применение аспирина, приводят к существенному снижению уровней тромбоксана в плазме через два и через шесть часов после лечения, тогда как применение какао с высоким содержанием процианидинов не изменяет содержания тромбоксана в плазме. Это подтверждается результатами, которые показывают, что совместное лечение какао с высоким содержанием процианидинов и аспирином не дает уменьшения содержания тромбоксана ниже того, которое достигается при лечении только аспирином. В противоположность этим результатам данные PFA-100 обнаруживают, что совместное лечение какао с высоким содержанием процианидинов и аспирином приводит к увеличению времени закрытия, большее, чем при индивидуальных режимах лечения, т.е. эффекты лечения усиливаются.
Таким образом, антитромбоцитная активность процианидинов какао, по-видимому, не зависит от ингибирования метаболического пути арахидоновой кислоты. Есть два существенных значения данного факта. Во-первых, побочные эффекты, которые зафиксированы для аспирина и являются результатом ингибирования метаболического пути арахидоновой кислоты, не должны возникать при лечении процианидинами какао. Во-вторых, лечение данной комбинацией, вероятно, дает синергический антитромбоцитный эффект, в котором каждый компонент (аспирин и богатое процианидинами какао) способствует антитромбоцитной активности по разным механизмам.
Суммируя, лечение комбинацией аспирина и обогащенного процианидинами какао приводит к снижению активности тромбоцитов, которое является аддитивным и, очевидно, синергическим. Очевидно также, что совместный прием какао и аспирина усиливает активность аспирина, позволяя использовать значительно меньшие дозы для достижения сравнимой эффективности лекарства, снижая тем самым вредные побочные эффекты аспирина.
Пример 3
Эффекты потребления процианидин-обогащенного напитка в сочетании с аспирином на активность тромбоцитов
Исследуют эффекты потребления напитка какао в сочетании с эффективным количеством аспирина на активацию тромбоцитов.
Пациенты предыдущего исследования участвуют также в исследовании поверхностной экспрессии белков. Методология в отношении схем приема препарата и отбора крови идентична той, которая описана в предыдущем примере.
В течение 10 мин после отбора цельную кровь инкубируют в полистирольных пробирках в течение 5 мин при комнатной температуре с 10 мкМ HEPES-буфера (рН 7,4, нестимулированный контроль), 20 или 100 мкМ ADP или 20 мкМ эпинефрина (BioData, Horsham, PA) в присутствии или в отсутствие пептида Arg-Gly-Ser (Sigma, St. Louis, МО). Через 5 мин образцы суспендируют в 1 мл HEPES-буфера и 100 мкМ образца переносят в пробирки, содержащие насыщенные концентрации (20 мкМ) каждого из следующих флуоресцентно-меченых моноклональных антител: РАС1-флуоресцеин изотиоцианат (FITC), анти-СD62Р-фикоэритрин (РЕ) и анти-СП42а-РегСР. РАС1 распознает активированную конформацию фибриноген-связанного рецептора GPIIb-IIIa, и анти-СD62Р распознает Р-селектин, присутствующий на поверхности активированных тромбоцитов. Анти-СD42а распознает GP1b-1X, который находится на поверхности активированных и покоящихся тромбоцитов. В качестве изотипного контроля используют мышиный IgG FITC и мышиный IgG РЕ. Arg-Gly-Asp-Ser-пептид используют для блокирования связывания антитела РАС1 с тромбоцитами и, таким образом, устанавливают отрицательный контрольный маркер на проточный цитометр. Антитела и изотипные контроли приобретают у Becton Dickinson Immunometry Systems, Inc., San Jose, CA.
Образцы цельной крови в присутствии или в отсутствие агонистов ADP и эпинефрина инкубируют с моноклональными антителами или изотипным контролем в течение 20 мин в темноте при комнатной температуре. Затем образцы фиксируют в фильтрованном 1% параформальдегиде (рН 7,2) и хранят в темноте при 2-8°С. Все образцы анализируют в течение 48 час на проточном цитометре FACScan с программным обеспечением LYSYS II. Производительность проточного цитометра варьируют, используя калибровочные гранулы 1, 2 и 10 мкм (Becton Dickinson Immunocytometry Systems, Inc., San Jose, CA и Flow Cytometry Systems, Research Triangle Park, NC). Суммируют двадцать тысяч данных в реестр со всеми параметрами светорассеяния и флюоресценции в логарифмической кодировке. Тромбоциты отбирают на основании светорассеяния и экспрессии CD42a. Активированные тромбоциты определяют как процент CD42a-положительных данных, совместно экспрессирующих активированную конформацию GPIIb-IIIa или Р-селектин. Микрочастицы тромбоцитов определяют как процент СD42а-положительных данных, размер менее 2 мкм.
Для проведения статистического анализа результатов применяют повторяемые измерения ANOVA по Friedman по рядам (ANOVA по рядам), сравнивая исходные результаты и результаты через 2 и 6 час в каждой исследуемой группе. Все парные сравнения по Tukey используют для последующих множественных сравнений. Р-величины менее 0,05 считают значимыми. Тромбоцит-зависимые данные по гемостазу также анализируют на статистические различия между исследуемыми группами лечения в каждый период времени: исходные, через 2 и 6 час.
Результаты
Влияние потребления какао и аспирина на ex vivo экспрессию активированных конформаций рецепторов тромбоцитов GPIIb/IIIa со стимуляцией или без стимуляции слабыми агонистами ADP и эпинефрином показано на фигурах 2, 3 и 4.
После активации тромбоцитов рецептор GPIIb/IIIa претерпевает конформационное изменение, делающее его способным связывать фибриноген и фактор von Willebrand. Образование межтромбоцитных мостиков посредством связывания лигандов с активированными рецепторами GPIIb/IIIa является существенным для агрегации тромбоцитов и образования тромбов.
Обращаясь к фигуре 2В, прием (+)-какао повышает экспрессию нестимулированных GPIIb/IIIa через 6 час по сравнению с исходным значением (Р<0,001). Никакие другие способы лечения существенно не влияют на экспрессию нестимулированных GPIIb/IIIa.
Обращаясь к фигуре 3С, ADP-индуцированная экспрессия GPIIb/IIIa подавляется через 6 час после приема ASA + (+)-какао по сравнению с исходным значением (Р+0,004). В противоположность этому, как показано на фигуре 3D, прием ASA + (-)-какао повышает ADP-индуцированную экспрессию GPIIb/IIIa через 6 час по сравнению с исходными данными или данными через 2 часа (Р=0,005).
Как показано на фигуре 4А, прием ASA подавляет эпинефрин-индуцированную экспрессию GPIIb/IIIa через 6 час по сравнению с исходным значением (Р=0,003). Прием (+)-какао подавляет эпинефрин-индуцированную экспрессию GPIIb/IIIa через 2 час по сравнению с исходным значением (Р=0,005, фигура 4В). Совместный прием ASA + (+)-какао подавляет эпинефрин-индуцированную экспрессию GPIIb/IIIa через 2 час и через 6 час по сравнению с исходным значением (Р=0,006, фигура 4С). В противоположность этому при потреблении ASA + (-)-какао существенных изменений в эпинефрин-индуцированной экспрессии GPIIb/IIIa не происходит (фигура 4D).
Эффекты потребления какао и аспирина на ex vivo экспрессию Р-селектина (CD62) на поверхности тромбоцитов со стимуляцией или без стимуляции слабыми агонистами ADP и эпинефрином показаны в таблице 2. Р-селектин экспрессируется на поверхности активированных тромбоцитов. Ни один из режимов лечения существенно не влияет на нестимулированную экспрессию Р-селектина. Прием ASA + (-)-является единственным режимом лечения, который подавляет ADP-индуцированную экспрессию Р-селектина через 2 час (Р=0,001).
Прием ASA подавляет эпинефрин-индуцированную экспрессию Р-селектина через 6 час по сравнению с исходными значениями (Р=0,028), тогда как (+)-какао не оказывает никакого влияния. Совместный прием ASA + (+)-какао подавляет эпинефрин-индуцированную экспрессию Р-селектина через 2 час и через 6 час по сравнению с исходным значением (Р=0,014). В противоположность этому совместный прием ASA + (-)-какао не дает существенных изменений в эпинефрин-индуцированной экспрессии Р-селектина.
Пример 4
Препараты в виде таблеток
Препараты в виде таблеток получают, используя твердые вещества какао с высоким содержанием процианидинов какао, полученные способами, описанными в патенте США №6015913, который включен здесь в виде ссылки. Вкратце, данный годный в пищу материал получают способом, который увеличивает природное содержание процианидинов какао, в противоположность уровням, обнаруженным в традиционно обработанном какао, так что отношение исходного количества процианидинов какао, обнаруженного в необработанных бобах, к количеству после обработки равно 2 или менее. Для простоты данный материал из твердых веществ какао обозначен здесь как твердые вещества СР-какао.
В состав таблетки включены следующие вещества (доли выражены в процентах массы):
твердые вещества СР-какао 24,0%
4-кратный экстракт природной ванили (Bush Boake Allen) 1,5%
стеарат магния - сухое смазывающее вещество (AerChem, Inc.) 0,5%
Dipac сахар для таблеток (Amstar Sugar Corp.) 37,0%
Ксилит (American Xyrofin, Inc.) 37,0%
Аспирин 50 мг
Твердые вещества СР-какао и экстракт ванили смешивают вместе в пищевом процессоре в течение 2 мин. Осторожно смешивают вместе аспирин, сахар и стеарат магния, а затем подмешивают в смесь твердых веществ СР-какао/ванили. Данный материал пропускают через пресс Manesty Tablet Press (B3B) при максимальном давлении и уплотнении, получая круглые таблетки (15 мм × 5 мм) весом 1,5-1,8 г.
Альтернативно, СР используют в виде экстракта, содержащего около 600 мг всех мономеров и олигомеров процианидинов.
Специалист в данной области может легко получить другие препараты в виде таблеток, охватывающие широкий диапазон ароматизаторов, красителей, наполнителей, витаминов, минералов, безрецептурных медикаментов, сахарных наполнителей, уф-защитных агентов (например, диоксид титана, красители и др.), связующих, гидрогелей и подобного за исключением поливинилпирролидона, который необратимо связывает процианидины какао, или сочетание соединений.
Пример 5
Препарат в виде капсулы
Готовят вариант препарата таблетки, раскрытой в примере 4, дозированную форму для перорального приема, включающую процианидин какао в сочетании с аспирином, используя заполняемые сборные капсулы из желатина, а также мягкие герметичные капсулы из желатина и пластификатор, такой как глицерин. Заполняемые сборные капсулы содержат соединение данного изобретения, или комбинацию соединений, или твердые вещества СР-какао, которые описаны в примере 4, в виде порошка, который может быть необязательно смешан с наполнителями, такими как лактоза или сахароза, для регулировки дозы процианидинов какао. В мягких капсулах выделенные процианидины какао или твердые вещества СР-какао суспендированы в подходящей жидкости, такой как жирные масла, или масло какао, или их комбинации. Капсулы могут содержать Уф-защитный агент, такой как диоксид титана или подходящие красители для защиты от УФ-излучения. Капсулы также могут содержать наполнители, такие, которые упоминаются в примере 4.
Пример 6
Метилированные процианидины
В данном примере показано действие метилированных процианидинов какао на гладкую мускулатуру сосудов. Используют in vitro способ, который измеряет эндотелий-зависимое расслабление (EDR) на кольцах аорты кролика.
Получение полифенолов какао и метаболитов процианидинов
Метилированный тетрамер получают взаимодействием очищенной фракции тетрамеров процианидинов какао (выделенных, как описано в патенте США №5554645, Romanczyk и др.) с диазометановым реагентом.
Для получения диазометанового реагента применяют генератор Diazald Kit Diazomethane Generator (Aldrich Chemicals). В реакции участвуют два реагента. Для первого реагента 5 г КОН растворяют в 8 мл воды, затем добавляют 10 мл МеОН. Данный реагент помещают в круглодонную колбу, используемую в качестве реакционного сосуда. Данный реакционный сосуд присоединяют к холодильнику и приемной колбе, которую охлаждают на ледяной бане. Сбоку на держателе помещают ловушку для эфира. Второй реагент получают, растворяя 5 г Diazald в 45 мл повторно перегнанного этилового эфира. Данный реагент помещают в делительную воронку над реакционным сосудом. Реакционный сосуд нагревают до 65°С на водяной бане. Раствор Diazald по каплям вливают в раствор КОН со скоростью, эквивалентной скорости отгонки. Когда Diazald использован, делительную воронку ополаскивают 10 мл эфира.
100 мг тетрамера суспендируют в 3 мл метанола. Добавляют 12 мл диазометанового реагента. Смесь взаимодействует в течение 20 мин при комнатной температуре, затем ее оставляют для взаимодействия на ночь (16 час) в морозилке (-7°С). Реакцию прекращают, добавляя 2,5 мл 10% уксусной кислоты в метаноле. Растворитель удаляют в потоке азота и твердое вещество сушат в вакууме.
Реакцию контролируют способом API-ES масс-спектрометрии с отрицательными ионами. 10 мкл вводят, применяя скорость 1 мл/мин потока, составленного из 8% 10 мМ ацетата аммония в метаноле и 92% метанола. Ионизацию проводят, используя капиллярный вольтаж 3500 В и вольтаж фрагментации 100 В. Спектры сканируют в диапазоне m/z 500-1500. Масс-спектральные данные указывают, что по окончании реакции не остается неметилированных тетрамеров. Основная часть реакционных продуктов метилируется по 14-18 положениям гидроксила. Некоторые тетрамеры полностью метилированы по всем 20 положениям.
Эндотелий-зависимое расслабление
Самцов новозеландских кроликов (массой 2,5-3 кг) умерщвляют пентобарбиталом (50 мг/кг). Грудную аорту вырезают и тщательно очищают от прилипшего жира и соединительной ткани. Затем аорту разрезают на кольца (длиной 3-4 мм), закрепляют в обычных банях для исследования органов на 20 мл, заполненных бикарбонатным буфером Кребса (мМ/л): NaCl 116,0; KCl 5,4; CaCl2 1,2; NaHCO3 22,0; NaH2PO4 1,2; MgCl2 1,2 и глюкоза 10,1, выдерживают при 37°С, рН 7,4 и при постоянной аэрации смесью 95% O2 - 5% С02. Ткани присоединяют к силовому сдвиговому преобразователю (Grass Instrument Co., Quincy MA Model FT03C) и растягивают до основного натяжения 8g.
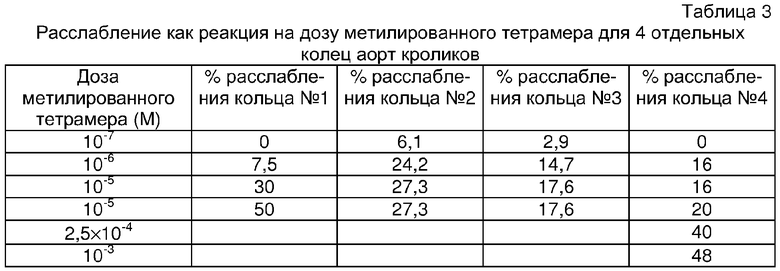
Кольца уравновешивают в банях для органов в течение 90 мин, после чего проводят их предварительное сокращение при помощи норпинефрина (10-5 М). Во всех препаратах оценивают наличие функционального эндотелия по способности ацетилхолина (10-5 М) индуцировать 40% или большее расслабление предварительно сокращенных колец. Данные методики подробно опубликованы ранее (Kappagoda, Cardiovascular Res. 25: 270-82, 1991). Кольца аорт с функциональным эндотелием предварительно сокращают при помощи норпинефрина (10-5 М). Когда сокращение достигает устойчивого состояния, добавляют метилированный тетрамер при концентрации 10-3, 10-4, 10-5, 10-6, 10-7 и 2,5×10-4. Результаты представлены в таблице 3. Результаты по 4 отдельным кольцам аорт показывают, что метилированный тетрамер оказывает расслабляющее действие. Таким образом, данные производные эффективны, как и исходные соединения, в способности поддерживать состояние сосудов и при лечении сосудистых заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ УЛУЧШЕНИЯ СОСТОЯНИЯ СОСУДИСТОЙ СИСТЕМЫ | 2001 |
|
RU2303373C2 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДЕФЕКТНОЙ КОММУНИКАЦИЕЙ ПОСРЕДСТВОМ ЩЕЛЕВЫХ КОНТАКТОВ | 2003 |
|
RU2351325C2 |
| СПОСОБ ПЕРЕРАБОТКИ КАКАО-БОБОВ, ЧАСТИЧНО ОБЕЗЖИРЕННЫЕ ТВЕРДЫЕ ВЕЩЕСТВА КАКАО И СОДЕРЖАЩИЙ ИХ ПИЩЕВОЙ ПРОДУКТ | 1997 |
|
RU2242880C2 |
| ПРОДУКТЫ, СОДЕРЖАЩИЕ ПОЛИФЕНОЛ(Ы) И L-АРГИНИН, ДЛЯ СТИМУЛЯЦИИ ПРОДУКЦИИ ОКИСИ АЗОТА | 1999 |
|
RU2269268C2 |
| УСОВЕРШЕНСТВОВАННЫЙ СПОСОБ ЭКСТРАГИРОВАНИЯ ПРОЦИАНИДИНОВ КАКАО (ВАРИАНТЫ) И ЭКСТРАКТ КАКАО (ВАРИАНТЫ) | 2001 |
|
RU2281653C2 |
| СОЕДИНЕНИЕ ЭКСТРАКТА КАКАО И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2004 |
|
RU2394562C2 |
| ПРОДУКТЫ, СОДЕРЖАЩИЕ ПОЛИФЕНОЛЫ | 2006 |
|
RU2417711C2 |
| НЕПРЕРЫВНЫЙ СПОСОБ ЭКСТРАГИРОВАНИЯ ПРОЦИАНИДИНОВ КАКАО И ЭКСТРАКТ КАКАО, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2001 |
|
RU2311041C1 |
| ЭКСТРАКТ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ С ВЫСОКИМ СОДЕРЖАНИЕМ ПОЛИФЕНОЛА | 2007 |
|
RU2466736C2 |
| ПИЩЕВОЙ ПРОДУКТ, ИМЕЮЩИЙ ПОВЫШЕННОЕ СОДЕРЖАНИЕ ПОЛИФЕНОЛОВ КАКАО, СПОСОБ ЕГО ПРОИЗВОДСТВА И ДИЕТИЧЕСКАЯ ДОБАВКА | 1999 |
|
RU2271115C2 |
Изобретение относится к химико-фармацевтической и пищевой промышленности и касается композиции для приема внутрь, включающей в физиологически приемлемом носителе а) ацетилсалициловую кислоту и b) процианидин какао или производное процианидина какао, совместное количество которых эффективно для лечения или предотвращения дисфункции тромбоцитов, при этом количество ацетилсалициловой кислоты составляет менее 80 мг. Изобретение также касается продукта, содержащего ацетилсалициловую кислоту и процианидины какао, и способа лечения или предупреждения дисфункции тромбоцитов. Композиция нетоксична и обладает высокой эффективностью. 3 н. и 26 з.п. ф-лы, 4 ил., 3 табл.
(a) подвергая обезжиренные молотые бобы какао, фракции молотых бобов какао, шоколадный экстракт, частично обезжиренные твердые вещества какао или полностью обезжиренные твердые вещества какао экстракции растворителем, в котором растворяются процианидины какао; и
(b) выделяя из полученного экстракта какао фракцию, включающую интересующий мономер, олигомер процианидина или их смесь.
(a) нагреванием бобов какао до внутренней температуры бобов, достаточной для снижения содержания влаги примерно до 3 мас.% и для ослабления кожуры какао;
(b) отсеиванием молотых бобов какао от кожуры какао;
(c) прессованием с отжимом молотых бобов какао; и
(d) выделением масла какао и частично обезжиренных твердых веществ какао, которые содержат процианидины какао.
(а) подвергая обезжиренные молотые бобы какао, фракции молотых бобов какао, шоколадный экстракт, частично обезжиренные твердые вещества какао или полностью обезжиренные твердые вещества какао экстракции растворителем, в котором растворимы процианидины какао; и
(b) выделяя фракцию, содержащую каждый олигомер процианидина из полученного экстракта какао.
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| RU 97106832 А, 10.05.1999 | |||
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ АГРЕГАЦИИ ТРОМБОЦИТОВ В КРОВЕНОСНОЙ СИСТЕМЕ | 1995 |
|
RU2095064C1 |
Авторы
Даты
2006-11-10—Публикация
2001-03-22—Подача