Права Правительства США
[0001] Настоящее изобретение было сделано во время совместного научно-исследовательского проекта, который финансировался Министерством Энергетики США по Соглашению о Совместных Исследованиях и Разработках (CRADA) No. 99-USIC-MULTILAB-04 и Лос-Аламосской Национальной Лабораторией CRADA No. LA99CI0429. В связи с этим правительство имеет определенные права на это изобретение.
Описание
ССЫЛКА НА СВЯЗАННУЮ ЗАЯВКУ
[0002] Настоящая заявка использует информацию, приведенную в предварительной заявке на Патент США №60/300,184, поданную 22 июня 2001 г.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0003] Предмет данного изобретения относится к области нановолокон и более точно к использованию нановолокон как фильтрующего материала, а также в процессах биологического разделения.
ЛИТЕРАТУРНЫЙ ОБЗОР
[0004] Патогенные микроорганизмы, обитающие в воде, являются основным источником болезней среды населения во всем мире. Несмотря на меры предосторожности, принятые для обеспечения микробиологической безопасности питьевой воды, болезнетворные микроорганизмы регулярно проникают к потребителю через системы водоснабжения. Основным источником беспокойства являются бактерии, обитающие в воде, такие как Salmonella spp., Shigella spp., Yersinia spp., Mycobacterium spp., enterocolitica, так же как и Escherichia coli, Campylobacter jejuni, Legionella, Vibrio cholerae. Эти бактерии имеют размеры от 0,5 до нескольких микрон и имеют овальную (cocci) или цилиндрическую (bacillus) форму. Cryptosporidium и другие примитивные организмы имеют размер приблизительно 3-5 микрон и они устойчивы к многим видам химического дизенфицирования. Gtyptosporidium ответственен за ряд эпизодов загрязнения окружающей среды со многими смертными случаями.
[0005] Комитет по Научным Консультациям при Агентстве по Защите Окружающей Среды США (ЕРА) относят вирусы к одним из наиболее опасных факторов риска для здоровья. Патогенные микроорганизмы, обитающие в воде, включают этеровирусы (Enteroviruses), (такие как полиовирусы, Coxsackievirus (группы А и В), эковирусы, вирус гепатита А), ротавирусы и другие реовирусы (reoviruses (Reoviridae)), аденовирусы, и агенты типа Norwalk. Число вирусов, определяемых в литре сточных вод, колеблется от менее чем 100 инфекционных единиц до более чем 100000 инфекционных единиц. В некоторых случаях попадание даже одной инфекционной единицы в организм человека может вызвать инфекционное заболевание в определенной части наиболее подверженной части населения. Постоянное присутствие даже небольшого количества вирусов, вызывающих кишечные заболевания, в больших объемах воды, потребляемой большой группой населения, может привести к эпидемическому распространению и присутствию вируса в данной местности. В настоящее время не существует рекомендаций Агентства по Защите Окружающей Среды США (ЕРА), которые бы требовали удаление вирусов в связи с отсутствием количественных оценок степени опасности. Однако имеются спецификации, принятые в военных рекомендациях, которые требует удаление вирусов (таких как вирус гепатита) больше, чем 4 logs (>99.99%), так же как бактерии (такие как Е. coli) больше, чем 5 logs (>99.999%), и Cryptosporidium больше, чем 3 logs (>99.9%).
[0006] Основными методами дезинфекции являются химическое окисление и микрофильтрация. Химические окислители включают озон, хлор и производные хлора. Вирусы более жизнестойки по отношению к окружающим условиям и процессам очистки сточных вод, включая методы хлорирования и ультрафиолетового излучения, чем многие бактерии, существующие в очистных водах. В лабораторных экспериментах было показано, что вирусы, вызывающие кишечные заболевания, могут выживать вплоть до 130 дней в сточных водах, что превосходит данные для бактерии типа кишечной палочки.
[0007] Существует подозрение относительно токсичности и потенциальной канцерогенности вторичных продуктов от дизинфецирующих средств, которые формируются в результате химической обработки. В системах водоснабжения населения не удалось применить стерилизацию фильтрацией по причинам высокой стоимости и низкой производительности фильтров, предназначенных для удаления вирусов. Более того, поскольку болезнетворные бактерии могут размножаться в водопроводных трубах, очистка воды в месте ее использования является наиболее предпочтительной. Системы очистки питьевой воды как в месте входа питьевой воды, так и месте ее использования, основанные на принципах обратного осмоса через полупроницаемую мембрану или с использованием ультрафиолетового излучения, в основном используются для удаления болезнетворных микробов как из городских источников воды, так и из источников грунтовых вод. Обе системы очистки имеют недостатки, связанные с низкой скоростью фильтрования, а также требуют наличия резервуара для того, чтобы обеспечить требуемый расход воды, в случае необходимости. В дополнение, полная очистка воды с помощью ультрафиолетового излучения вряд ли возможна, поскольку болезнетворные организмы могут экранироваться коллоидными частицами. Таким образом, фильтрация является необходимым дополнением к существующим системам. Обе вышеупомянутые системы очистки весьма дорогостоящие для того, чтобы их можно было использовать в небольших системах в месте потребления воды, а также они очень сложные, пробующие дорогостоящего обслуживания. Поэтому фильтр, способный удалить все болезнетворные организмы, обладает большим потенциальным значением. Более того, было бы экономически выгодно иметь такой фильтр, который мог бы быть установлен с такой же легкостью, как и существующие химические фильтры.
[0008] Очистка воды также важна в медицинских и зубоврачебных кабинетах. Системы очистки воды в зубоврачебных кабинетах создают бактериальные пленки, которые обеспечивают благоприятные условия для роста болезнетворных организмов, которые зачастую превышают общепринятые нормы врачебной ассоциации. Обнаруженные болезнетворные организмы включают такие опасные виды как Legionella pneumophila, а также загрязнение линий подачи воды вирусами и, возможно, вирусами HIV или гепатита может происходить за счет обратного сифонирования от больного пациента. Фильтр, способный стерилизовать воду в зубоврачебных кабинетах в месте ее использования методом удаления бактерий и вирусов на высокой скорости фильтрования, желателен для использования в зубоврачебных кабинетах.
[0009] Загрязнение воды коллоидными частицами вносит свой вклад к мутности воды (дымчатый вид). Такие коллоидные частицы обычно включают в себя органические вещества, такие как составные части почвы, болезнетворные организмы, а также наночастицы неорганических веществ. Коллоидные частицы служат как подложка для адсорбции микробов, пестицидов, других синтетических органических химикатов, а также тяжелых металлов. Наноразмерные частицы могут забивать фильтрующие системы.
[0010] Необходима усовершенствованная технология для определении и идентифицировании болезнетворных организмов и, в частности, вирусов, поскольку методы их концентрация недостаточно эффективны. Нужны недорогие приборы для сбора вирусов и для анализа поверхностных вод. Хотя такие фильтры не должны обеспечивать стерилизацию, сборник вирусов должен быть способным удалить большую часть вирусов из 500-1000 литров воды в течение двух часов. Затем вирусы должны быть смыты с фильтра в неповрежденном виде и оставаться жизнеспособными для последующего анализа. Фильтр MDS-1 компании AMF Cuno наиболее часто используется для анализа загрязнений природной воды вирусами. К сожалению, такие фильтры очень дороги для их повседневного использования, тем более что они одноразового использования. Цена фильтра одноразового использования должна быть значительно снижена, прежде чем Агентство по Защите Окружающей Среды США (ЕРА) могло бы дать рекомендацию на проверку воды на вирусы в качестве повседневной процедуры. В настоящее время усилилась угроза применения биологического оружия террористическими группами как в воде, так и в воздухе, что увеличило необходимость для его раннего определения и диагностики. Эффективное определение затруднено из-за низкой чувствительности современных биоаналитических методов, особенно в отношении вирусов, которые много меньше по размеру и которые труднее сконцентрировать, но которые более вероятно могут быть инфекционными. Необходимо отобрать десятки тысяч литров воздуха или воды для того, чтобы обеспечить достаточное количество частиц для анализа. Сборники частиц из воздуха ограничиваются циклонным разделением и ударом о препятствие и являются непрактичными для сбора частиц с размерами вирусов.
[0011] Волокнистые глубинные фильтры захватывают частицы в основном за счет удара частицы о волокно, где они прилипают за счет адсорбции, в то время как мембраны захватывают частицы в основном за счет разделения по размеру. Имеются в наличии мембраны с размером пор достаточно маленьким для обеспечения разделения бактерий и вирусов, однако нет в наличии волокнистых глубинных фильтров, способных очистить воду от нежелательных примесей. В смысле разделения частиц с помощью фильтрации, размер пор в полупроницаемых мембранах обратного осмоса колеблется от 1 до 10 Ангстрем и 20 Ангстрем, размер пор мембран для ультрафильтрования колеблется от 1 нанометра (10 Ангстрем) до 200 нм, размер пор мембран для микрофильтрации колеблется от 50 нм, или 0,05 микрон до приблизительно 2 микрона, и размер пор мембран для фильтрования частиц колеблется от 1 до 2 микрон и выше. Размер пор фильтровальной мембраны должен быть уменьшен с уменьшением размеров болезнетворных организмов. Это приводит к резкому увеличению перепада давления и к уменьшению скорости потока. Многие вирусы имеют размер около 30 нм и имеющиеся промышленные мембраны обеспечивают удаление вирусов на уровне от 2 до 3 log [Willcommen]. Мембраны подвержены к забиванию пор и требуется предварительная фильтрация для удаления крупных частиц и увеличения ресурса работы дорогостоящих мембран. Более того, мембраны подвержены к локальным дефектам, таким как перекрытие пор и поры с пальчиковой структурой, которые существенно ухудшают качество их работы.
[0012] Вирусы должны быть удалены из медицинских продуктов, так же как из человеческой крови и продуктов, получаемых из плазмы. FDA рекомендует, чтобы все схемы очистки использовали одну или более "устойчивых" стадий удаления или инактивации вирусов. Устойчивые методы определены как те, которые работают при различных условиях и включают в себя низкую рН, нагревание, инактивацию с помощью растворителя-очистителя, а также фильтрацию. Удаление вирусов с помощью нагревания, химических методов и с помощью ультрафиолетового и гамма-излучения могут повредить чувствительные протеины, а также требует последующего удаления вышеуказанных химикатов и поврежденных протеинов. Соответственно, фильтрация рассматривается как предпочтотельный метод для удаления вирусов.
[0013] В настоящее время биотехнология заметно расширилась и включает в себя синтез новых протеинов, созданных с помощью рекомбинантных методов, удаление протеинов из плазмы крови, изменение в продуктах из гемоглобина и в продуктах сыворотки млекопитающих, так же как и защиту ферментных реакторов от загрязнения вирусами. Прионы - это протеины, которые могут вызывают болезнь Creutzfeldt-Jacob (CJC). Они приблизительно 10 нм в размере и таким образом меньше, чем вирусы. В фармацевтической промышленности микропористые мембраны используются для очистки входящего потока воды, так же как для контроля выходящей водных потоков и отходов для того, чтобы быть уверенным, что сбрасываемая вода не имеет загрязнений.
[0014] Вначале мембраны с размерами пор 0,45 микрон рассматривались как "стерилизационные", основываясь на их способности эффективно задерживать Serratia marcescens организмы, но исследования показали, что фильтр может оказаться скомпрометированным. Более маленькая бактерия Pseudomonus diminuta (P. diminuta) (0,3 микрона) в настоящее время все чаще используется для проверки целостности фильтра, и фильтр с порами 0,22 микрон в настоящее время принят как "стерилизационный" стандарт для удаления бактерий. Ультрапористые мембраны с размером пор 20 нм используются для фильтрования вирусов. Нанопористые мембраны, такие как полупрозрачные мембраны обратного осмоса, способны очистить воду от вирусов, однако приводят к еще большему ограничению по скорости потока. При производстве протеинов инструкции предполагают, что стерилизация от вирусов должна составлять по меньшей мере 12 порядков величины. Это значение обеспечивает содержание менее чем одной инфекционной частицы на 10.sup.6 доз. Такой уровень удаления вирусов требует многоступенчатого процесса.
[0015] Фильтрующие материалы, содержащие многовалентные катионы, такие как Al3+ и Mg2+ при рН около 3,5 могут задерживать вирусы. Lukasik et al. смогли эффективно удалить вирусы из сточных вод в течение длительного периода времени с использованием фильтровальных слоев из песка, обработанного с помощью гидроксидов железа и алюминия. Farrah внедрял оксиды алюминия и других металлов в порошки диатомитных земель и достиг заметного увеличения в поглощении вирусов. Farrah и Preston улучшили поглощение нескольких вирусов, изменив целлюлозные фильтры флоккулированными частицами гидроксидов железа и алюминия.
[0016] Фильтры могут быть сделаны из широкого круга материалов. Фильтры, изготовленные из стекловолокон, имеют тенденцию быть непрочными, однако химические связующие могут увеличивать их физические свойства и изменять их химические характеристики. Керамические фильтры часто имеют желаемый набор характеристик, но они хрупкие. Металлические фильтры зачастую могут преодолеть эти ограничения, но они дорогостоящие. Преимущество в использовании керамических и металлических фильтров в том, что они часто могут быть очищены и вновь использованы. Волокна для фильтров и мембраны производятся из многих полимеров, включая дифлорид поливинилидина, полиолефин и акрилаты. Сорбенты, такие как гранулированный оксид кремния, диатомиты или гранулированный уголь, также внедрялись в фильтрующий материал.
[0017] Электрокинетические силы помогают захватывать частицы из воды. Hou описал количественную картину фильтрования с помощью электрокинетических сил, концепция которой объяснена в терминах, принятых в коллоидной химии. Если электростатические заряды на фильтрующем материале и на частице противоположны, электростатическое притяжение будет способствовать отложению и удержанию частиц на поверхности фильтровальной среды. Если они одинакового знака, то возникает отталкивание и, тем самым, отложение и удержание частиц будет затруднено. Поверхностный заряд фильтра изменяется с изменением рН и с изменением концентрации фильтруемого раствора. Это явление объясняется теорией двойного электрического слоя, принятой в коллоидной химии. Частица, погруженная в водный раствор, создает вокруг себя поверхностный заряд, поглощая ионы на своей поверхности. Фиксированный слой противоположно заряженных ионов создается на поверхности фильтра. Для поддержания электронейтральности образуется диффузный слой, содержащий достаточное количество противоположно заряженных ионов, которые проникают на определенное расстояние в раствор. Если концентрация ионов раствора увеличивается путем добавления катионных солей или увеличением рН, тогда протяженность этого слоя уменьшается, так как требуется меньший объем раствора для того, чтобы нейтнализовать заряд поверхности. Уменьшение толщины этого слоя приводит к приближению этих двух поверхностей, позволяя Ван-дер-Ваальсовским силам начать играть главную роль. Уменьшение рН или добавление катионных солей уменьшает электроотрицательность, улучшая поглощение при этих условиях. Поглощение вирусов улучшается в большинстве случаев грунтовых вод и воды из под крана, имеющих рН в районе 5-9 [Sobsey]. Добавки кислоты или соли часто необходимо для эффективного удаление вирусов с помощью электроотрицательных фильтров. Hou утверждает, что электроположительные фильтры могут найти широкое применение в удалении микроорганизмов из воды для концентрирования бактерий и вирусов из воды, для сбора эндотоксинов и их удаления из загрязненных жидкостей для инъекций и пищевых продуктов, а также для иммобилизации микробных клеток и антигенов.
[0018] Фибриллированный асбест, имеющий электроположительный заряд поверхности и удельную площадь поверхности приблизительно 50 кв. м/г, широко использовался при производстве целлюлозоасбестовых фильтровальных листов для фильтрования патогенов. Волокна асбеста имеют поры с очень тонкой структурой, что способствует механическому захвату. Однако, беспокоясь о вреде для здоровья, прекратили его использование, и были предприняты попытки для замены асбеста. Эти усилия включали в себя попытки химического изменения поверхностей гидрофобных полимерных материалов с целью создания покрытий с электроположительным поверхностным зарядом.
[0019] Например, патенты США №4007113; 4007114; 4321288 и 4617128 (Ostreicher) описывают применение меламин-формальдегидных катионных коллоидов для изменения зарядов поверхностей волокон и частиц в фильтре. Патенты США №4305782 и 4366068 (Ostreicher, et al.) описывают применение неорганических катионных коллоидов оксида кремния для изменения зарядов таких элементов. В патенте США №4366068 "тонкие" частицы оксида кремния имеют средний размер частиц около 10 микрон и покрыты с по меньшей мере 15% оксида алюминия. Патент США №4230573 (Kilty, et al.) описывает использование эпихлоридина полиамина для изменения заряда волокон фильтровальных элементов, см. также патенты США №4288462 (Hou, et al), и №4282261 (Greene). Предпочтительный метод производства фильтровальных материалов описан в патенте США №4309247 (Hou, et al.) и продается компанией, Cuno, Inc. под маркой ZETA PLUS. Похожие попытки изменения заряда фильтров катионами были сделаны в патентах США №3242073 и 3352424 (Guebert, et al.) и в патенте США №4178438 (Hasse, et al.). Патент США №5855788 (Everhart) описывает метод изменения поверхности фильтров на тканой и нетканой основе или на апертурных полимерах путем поглощения амфифильных протеинов, таких же, как получаемые из молока. Протеины модифицируются с помощью гидроксидов алюминия, полученных в результате золь-гельной реакции. Фильтры удаляют болезнетворные организмы из воды в основном за счет химического и электрокинетического взаимодействия вместо механического разделения. Уменьшение концентрации на три порядка было достигнуто в случае бактерии Vibrio cholerae. Разработчики отметили, что фильтры, имеющие измененный заряд поверхности, имеют различные адсорбционные характеристики для различных видов болезнетворных организмов в воде, таких как бактерии.
[0020] Патент США №5085784 (Ostreicher) предлагает фильтровальную среду с измененным зарядом, состоящую из целлюлозных волокон, частиц оксида кремния и катионного водно-растворимого органического полимера. Полимер поглощается на фильтр, который включает также эпоксидную и четвертичную группу аммония, способную прикрепляться ко вторичному агенту, изменяющему заряд поверхности. Модификатор заряда предпочтительно выбирается из числа алифатических полиаминов. Патент США №4523995 (Pall) описывает фильтровальную среду, приготовленную смешиванием стекла с полиамин-эпихлорохидринной смолой в виде суспензии. К смеси добавляется реагент, вызывающий осаждение смолы, которая покрывает микроволокна. Предпочтительным осадителем являются высокомолекулярные полимеры, содержащие анионные заряды. Как результат, покрытые микроволокна описываются как имеющие положительный зета-потенциал в шелочной среде и повышенную поглощательную способность для мелких частиц, включая бактерии и эндотоксины (пирогены). Однако Robinson et al., Mandaro и Meltzer описали ограничения на предыдущие фильтровальные среды с измененным зарядом в терминах ухудшения фильтрующих свойств при высоких рН и неспособности такой среды достичь эффективного удаления очень маленьких частиц и/или пирогенов (эндотоксинов).
[0021] Положительно заряженные мембраны, используемые для удаления анионных загрязняющих частиц, также известны и описаны в патентах США №2783894 (Lovell) и №3408315 (Paine). Патенты США №№4473475 и 4743418 (Bames, et al.) описывают катионную модифицированную микропористую мембрану, имеющую необходимое количество алифатического амина или полиамина, предпочтительно тетраэтилен-пентамина, связанного с нейлоном. Патент США №4604208 (Chu, et al.) описывает анионный зарядно-модифицированную нейлоновую микропористую мембрану. Система изменения заряда состоит из полимера, растворимого в воде и способного связываться с мембраной и анионными функциональными группами, такими как карбоксильные, фосфористые, фосфорные и серные группы. Патенты США №№4473474; 4673504; 4708803 и 4711793 (Ostreicher, et al.), описывают нейлоновую мембрану с измененным зарядом поверхности с использованием модифицированного эпихлорохидринового полиамида, имеющего третичный амин или четвертичную группу аммония, а также вторичный зарядно-изменяющий агент, который может быть алифатическим полиамином. Катионные зарядно-измененные нейлоновые мембраны, описанные выше в патентах Ostreicher, et al. и Barnes, et al. в настоящее время продаются Cuno, Inc. под торговой маркой ZETAPOR. Положительная, зарядно-измененная микропористая фильтровальная среда продается Pall Corp., которая использует нейлон 66 или положительно заряженную полиэфирсульфон-сульфатную мембрану. Micropore Corp. производит зарядно-измененные поливинилидин-дифторидные мембраны.
[0022] В основном фильтры используются в двух различных модах. В глубинном, или в тупиковом фильтре вся жидкость протекает через мембрану или фильтровальную среду. В тангенциальных фильтрах входящая жидкость течет вдоль оси, в то время как чистая жидкость проходит через фильтровальную среду в перпендикулярном направлении. Этот тип фильтра ограничивает толщину осадка на поверхности, поэтому позволяя большие скорости потока, в то время как в случае с глубинным фильтром, поверхностная корка увеличивается в толщине со временем, вызывая увеличение перепада давления с последующей полной остановкой потока. Скорость фильтрации важна практически во всех индустриальных процессах, включая фармацевтическое производство, биологические превращения и лабораторные эксперименты. Мембраны, используемые при фильтровании субмикронных и наноразмерных частиц, имеют очень низкий поток, если это не скомпенсировать увеличением входного давления или увеличением площади поверхности мембраны. Увеличение давления или площади поверхности существенно увеличивает капитальные и эксплуатационные расходы. Закупорка пор также ухудшает и без того низкий поток через мембраны с малыми порами.
[0023] Пирогены - это вещества, которые содержат эндотоксины, вызывающие увеличение температуры тела. Эндотоксины - это высокомолекулярные комплексы (молекулярный вес между 10000 и 1 миллионом), которые выделяются грам-отрицательными бактериями, сбрасывающими внешнюю мембрану в окружающую среду, вызывая поднятие температуры тела. Эндотоксины не подвергаются изменениям при автоклавировании в течение нескольких часов на 250°С. Эндотоксины могут быть удалены в процессе фильтрации через полупроницаемую мембрану обратным осмосом, однако этот процесс сложный из-за малого размера пор мембраны. Более того, ценные вещества, такие как соли, удаляются полупроницаемыми мембранами, и это является недостатком в приготовлении непирогенных медицинских сывороток для внутривенных инъекций. Патент США №5104546 описывает керамический ультрафильтр, способный разделять пирогены от медицинских сывороток для внутривенных инъекций. Керамический ультрафильтр состоит из слоя оксида циркония, нанесенного на подложку из окиси алюминия и имеющего номинальный размер пор около 5 нанометров. Фильтр способен разделять пирогены с эффективностью 5 logs, однако при высоком давлении (5,5 атмосфер) и длине поперечного сечения 20 см, при этом скорость потока в начале работы только 50 л/ч/кв.м/атм.
[0024] Новые аналитические схемы развиваются для производства фармакологических и биохимических материалов, где специфические реагенты удерживаются подложками с высокой площадью поверхности. Мембраны обычно также используются как подложка для диагностических анализов, подобных электрофорезису, цитологии жидкостей и гибридизации ДНК. Многие аналитические методы используют иммобилизацию биологически связываемого партнера биомолекулы на поверхности. Поверхность приводится в контакт со средой, для которой имеются основания полагать, что она содержит эту молекулу, и таким образом определяется наличие или диапазон связывания молекул с поверхностно-иммобилизованным связывающим партнером. Например, в патенте США №5798220 макромолекула прикрепляется к поверхности подложки и используется как иммунотест для анализа биологических жидкостей на присутствие иммуноглобулинов для макромолекулы. Патент США №5219577 описывает синтетическую, биологически активную композицию с нанокристаллическим ядром. Патент США №6197515 описывает метод захвата биологической молекулы, например на поверхности биодатчика, исследуя биологические взаимодействия. Наличие подложек, которые бы эффективно связывали первую биологическую молекулу, может облегчить такие методы-анализы. Нуклеиновые кислоты сорбируются на подложках из оксидов металлов, таких как оксид-алюминия, для последующего использования в гибридизации, маркировке, программировании и синтезе.
[0025] Электрофорезис - это один из наиболее широко используемых методов в биологических науках. Молекулярные формирования, такие как пептиды, протеины и олигонуклеотиды разделяются как результат миграции в растворе буфера под влиянием электрического поля. Буферный раствор обычно используется совместно с концентрациями от низких до средних с соответствующими загустителями, такими как арагоз или полиакриламид, для того чтобы уменьшить влияние конвективного смешивания. Наибольшее разрешение получается, когда некоторая неоднородность вводится в жидкую фазу. Такие элементы как градиент рН, либо эффект просеивания высокоплотными гелями имеют большое влияние на разделение молекул различного размера. Мембранные барьеры также могут быть установлены на пути миграции частиц. Электроположительные адсорбенты с большой удельной площадью поверхности, будучи добавлены к таким гелям, могут улучшить фактор разделения.
[0026] "Революция в Генетике" создает необходимость для технологий, относящихся к биоразделению. Поскольку рекомбинантные ретровирусы и саденовирусы из группы аденовирусов представляют собой идеальные системы для эффективной доставки и внедрения генетического материала, имеется очевидная необходимость для методов разделения вирусов, которые одновременно эффективны и не причиняют вреда вирусным частицам. Центрифугирование с использованием градиента плотности всегда играло важную часть в концентрации и очистке вирусных частиц, однако градиентная среда, используемая в большинстве случаев, как например, сукроза и CsCl, имеет несколько собственных проблем. Обе среды высоко гиперосмотичны, и материалы, используемые для связывания вирусов, обычно удалялись с помощью ультрафильтрации перед дальнейшей обработкой или анализом. Более того, осаждающий агент, который удаляет вирусы методом осаждения или эффективной фильтрации при небольшом перепаде давления, мог бы улучшить такую обработку [Nycomed].
[0027] Разделение макромолекул, таких как протеины, составляет существенную часть затрат в производстве фармакологических продуктов. Хроматография использовалась десятилетиями для целей биологического разделения. В хроматографии смесь вводится в узкую начальную область неподвижного сорбента и компоненты испытывают дифференциальную миграцию в потоке жидкости. В случае ионной хроматографии, дифференциальная миграция вызывается различным притяжением заряженных молекул к противоположно заряженной стационарной фазе. Химически измененная целлюлоза, содержащая оксид кремния, используется как стационарная фаза в производстве коммерчески важных биомолекул в пищевой, биофармацевтической, фармацевтической промышленностях и в биотехнологии. Например, такая среда использовалась во многих различных промышленных процессах для производства иммуноглобулинов, энзимов, пептидов, плазмидов и гормонов. Альтернативными стационарными фазами могут быть металлы, оксиды металлов и в частности порошкообразный оксид алюминия. Мембранные сорбенты - это мембраны с функционализированными поверхностными центрами для целей хроматографии. Разрешение традиционной хроматографической колонны, основанной на гранулах, обратно пропорционально размеру гранул и поэтому приборы, основанные на мембранных сорбентах, производят очень высокую степень разделения, поскольку они имеют большую площадь поверхности по сравнению с гранулами. Волокнистая среда, способная иметь такое разрешение и имеющая меньше ограничений на скорость потока, могла бы обеспечить более быстрое и экономичное разделение для целей очистки растворов и для аналитических целей.
[0028] Гели и золи гидроксида алюминия использовались как активаторы осаждения и как порошкообразные сорбенты для органических молекул. Например, Al(ОН)3 используется для связывания витамина К. Нуклеиновые кислоты зачастую являются загрязнителями в растворах протеинов и могут быть высаждены при соприкосновении с нуклеазами [Ahuja, стр. 368] перемешиванием, низкой ионной силой или высоким рН. Большинство из этих методов имеют эффект на протеины и имеют довольно низкую степень селективности. Поскольку нуклеиновые кислоты имеют отрицательно заряженные фосфатные группы, осаждающие вещества с положительно заряженными группами могут селективно удалять нуклеиновые кислоты из растворов. Этот принцип дал начало поиску ряда осаждающих агентов, используемых для разделения нуклеиновых кислот.
[0029] Клетки часто культивируются в реакторах для производства биологических и фармацевтических продуктов. Такие клетки могут быть как бактериальными, так и клетками млекопитающих. Для поддержания жизнедеятельности клеточной культуры, она должна снабжаться кислородом и питательными веществами. Клеточные культуры обычно поддерживаются в реакторах потоком жидкости, при котором питательная среда, включающая кислород и другие питательные инградиенты, направляется через реактор роста клеточных культур. Однако реакторы роста клеточных культур могут быть использованы только небольшим количеством клеток на единицу объема реактора. Они могут оперировать только внутри небольшого диапазона скоростей потока или перемешивания. Пористые подложки, на которых клетки можно иммобилизовать и более эффективно осуществлять обмен питательными веществами и растворенными газами, могли бы позволить большие загрузки реактора. Также, биокаталитические реакции могут быть осуществлены в объеме реактора с помощью катализатора, основанного на энзимах, прикрепленных к пористой неорганической подложке. Иммобилизация увеличивает сопротивляемость энзимов к тепловым и химическим факторам, при этом поддерживая их высокую каталитическую активность в широком диапазоне изменений в окружающей среде. Электроположительная подложка с высокой удельной площадью поверхности могла бы удерживать и иммобилизовать энзимы, стимулируя более быстрые химические реакции.
[0030] Ультрачистая вода используется во многих отраслях промышленности. Мембранные ультрафильтры используются для производства особо чистой воды в микроэлектронику. Спиральные мембраны, другая общеиспользуемая область технологии, весьма чувствительны к наличию частиц в потоке, что ограничивает поток жидкости через их чрезвычайно узкие проходы. Повреждение полимерных ультрафильтров является их основным недостатком, так как это вызывает необходимость в периодической чистке этих фильтров вне рабочей линии [Sinha].
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0031] Настоящее изобретение использует наноразмерные формы волокон или пластинок оксида алюминия, которые были найдены высоко электроположительными, удерживающими биообъекты в растворе воды. Мы обнаружили, что эти волокна притягивают и удерживают коллоидные и особенно вирусные частицы, а также являются инициаторами осаждения частиц. При введении их в матрицу на основе волокон они способны фильтровать бактерии и, в частности, субмикронные частицы, такие как вирусы или коллоиды с эффективностью, далеко превосходящей выпускаемые промышленностью фильтры, особенно при фильтрации нейтральной воды. Вирусы и наноразмерные частицы удерживаются при скоростях потока, в десятки и сотни раз превосходящих скорости фильтрации ультрапористых мембран с размером пор, меньшим, чем размер фильтруемых частиц. Такие фильтры с волокнами оксида алюминия имеют большую сопротивляемость к забиванию ультрамелкими частицами. Фильтровальный материал может быть применен в стерилизации питьевой воды, а также в медицинских или фармацевтических процессах. Замещая адсорбированные частицы, фильтры могут быть использованы как предварительный концентратор для целей определения и измерения адсорбированных болезнетворных организмов. Такие фильтры чрезвычайно эффективны как разделители в мембранной хроматографии, применяемой для очистки и анализа. Волокнистый сорбент, либо в форме гранул, или как фильтровальный материал может быть использован для разделения частиц и макромолекул на основе их заряда. Такие волокна или сделанные на их основе фильтры возможно будут служить как подложки для использования в биореакторах.
[0032] Соответственно, предмет данного изобретения сделать доступным электроположительный сорбент и метод его приготовления и использования.
[0033] Дальнейшие цели и преимущества настоящего изобретения становятся более ясны из иллюстраций к последующему детальному описанию изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
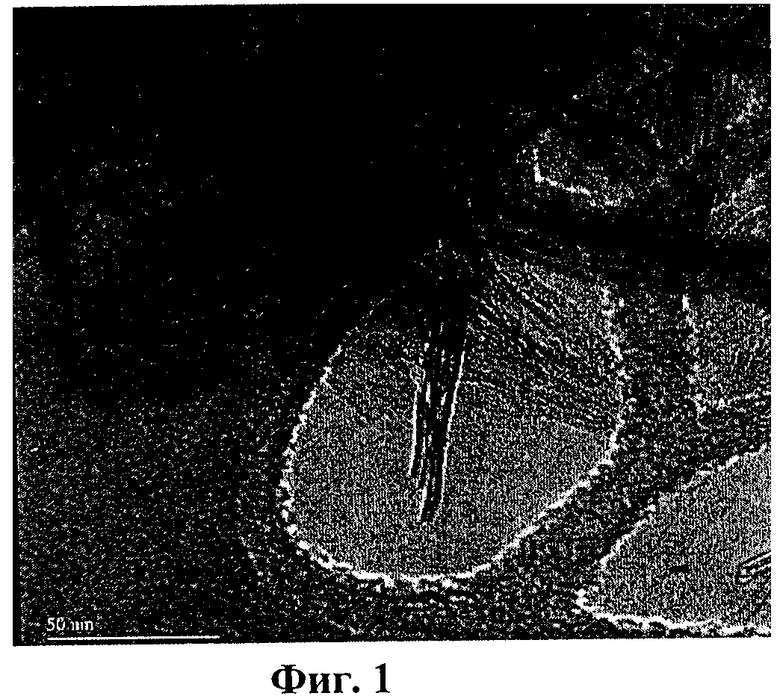
[0034] ФИГ.1 - электронная микроскопическая фотография в проходящих лучах нановолокон, изготовленных гидролизом наноалюминия, полученного в аргоне. Нанометровые волокна 2-х нанометров в диаметре видны на переднем плане при фокусировке в центре фотографии.
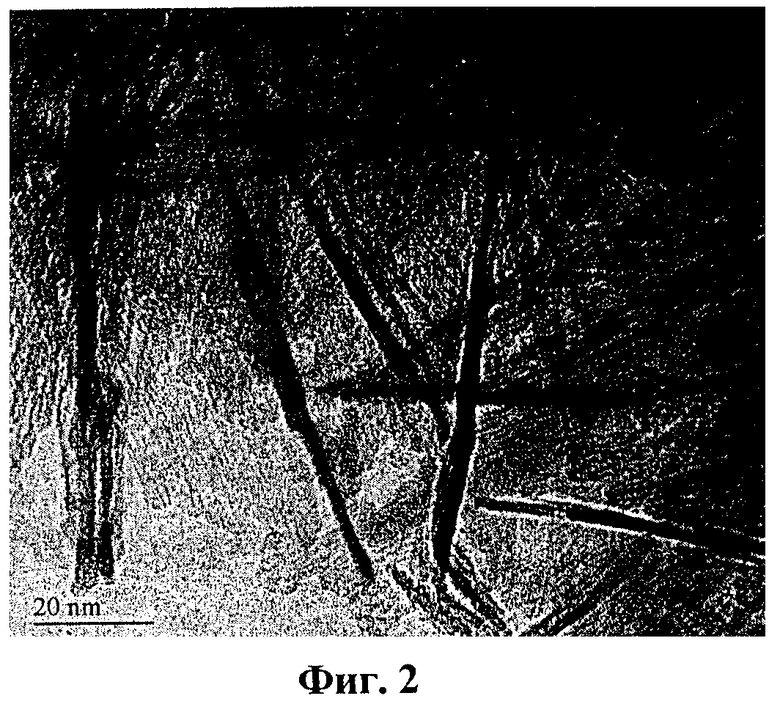
[0035] ФИГ.2 - электронная микроскопическая фотография в проходящих лучах нановолокон, изготовленных гидролизом наноалюминия, произведенного в азоте.
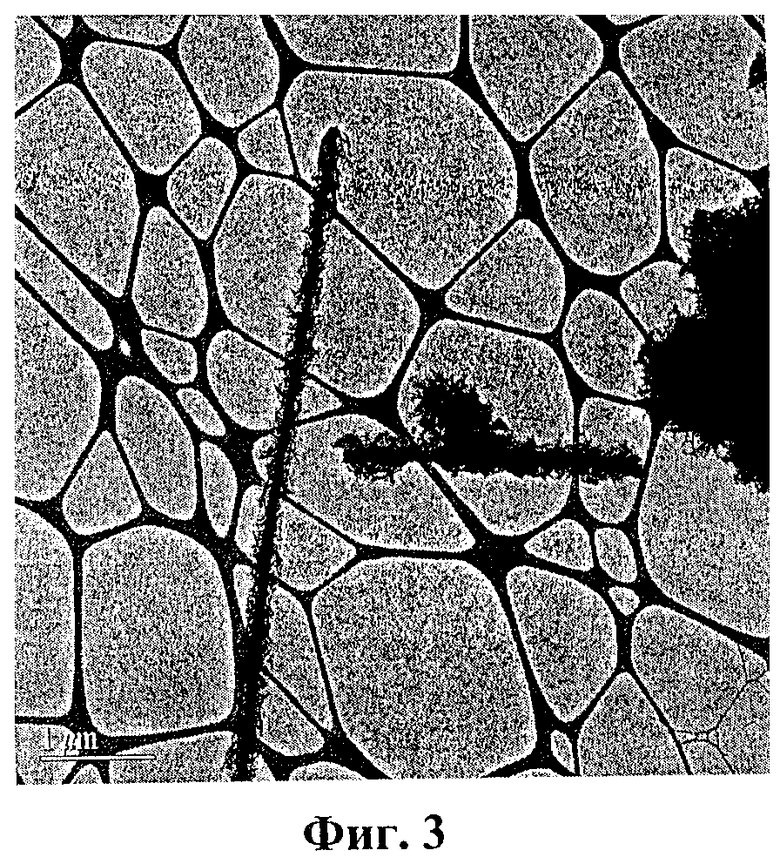
[0036] ФИГ.3 - микрофотография композитного материала - нанооксид алюминия/микростекло.
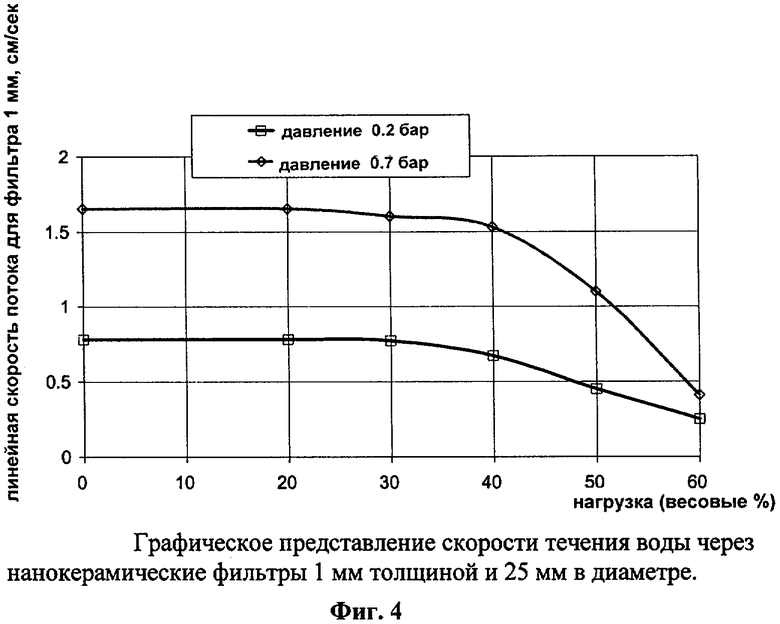
[0037] ФИГ.4 - графическое представление скорости течения воды через нанокерамические фильтры 1 мм толщиной и 25 мм в диаметре.
[0038] ФИГ.5 - графическое представление, иллюстрирующее пробой 30 нм резиновыми сферами фильтра, 25 мм в диаметре.
[0039] ФИГ.6 - графическое представление, иллюстрирующее пробой фильтра (30 нм резиновые сферы) в зависимости от весового процентного содержания нановолокон оксида алюминия.
[0040] ФИГ.7 - сканирующая электронная микрофотография фильтра из нановолокон оксида алюминия, насыщенного с помощью 30 нм резиновых сфер.
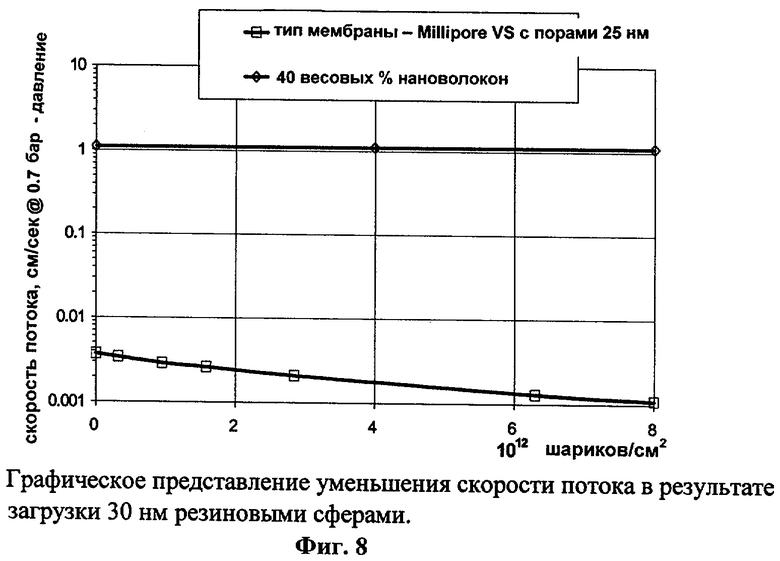
[0041] ФИГ.8 - графическое представление уменьшения скорости потока в результате загрузки 30 нм резиновыми сферами.
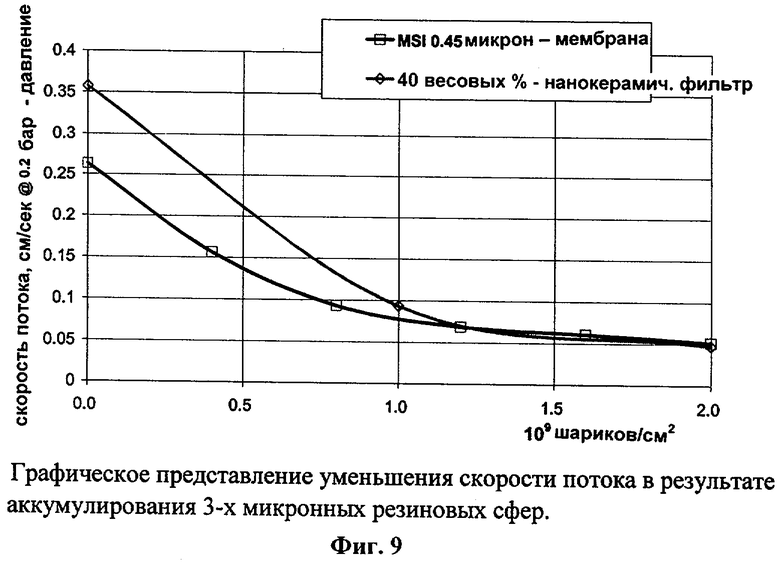
[0042] ФИГ.8 - графическое представление уменьшения скорости потока в результате аккумулирования 3-х микронных резиновых сфер.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0043] Для того, чтобы улучшить понимание некоторых терминов, используемых в описании патента, ниже приводятся их определения.
[0044] Термин электроотрицательная частица, используется здесь как индивидуальная частица, имеющая электроотрицательный заряд поверхности, за исключением атомов в форме ионов, но включая такие индивидуальные частицы как вирусы, бактерии, пирогены, прионы, макромолекулы, нуклеиновые кислоты, коллоиды, протеины и энзимы.
[0045] Термин десорбция используется для обозначения процесса удаления адсорбированных электроотрицательных частиц с поверхности электроположительного сорбента.
[0046] Термин нанооксид алюминия используется для обозначения частицы с отношением длины к поперечному сечению не менее 5, где наименьший из размеров меньше, чем приблизительно 100 нм. Поперечное сечение "волокна" может быть либо окружностью (цилиндрические волокна), либо прямоугольной формы (пластины). Волокна состоят из оксида алюминия с различным содержанием связанной воды и состоят либо из чистого Al(OH).sub.3 или AlOOH, или их смеси с возможными небольшим содержанием гамма- и альфа-оксидов алюминия.
[0047] Термин NanoCeram.TM., используемый здесь, определен как нанооксид алюминия, описанный выше.
[0048] Термин золь, используемый здесь, определен как жидкостная коллоидная система.
[0049] Наноразмерные волокна гидроксида алюминия можно получить несколькими различными методами. Патенты США №№2915475 и 3031417 описывают приготовление волокон бемита из очень дешевых химикатов (квасцы, бикарбонат натрия и уксусная кислота) при помощи гидротермальной реакции. Gitzen описывает несколько методов приготовления волокон, включая реакцию амальгамы алюминия с водой и реакцию алюминия с уксусной кислотой. После старения золя, произведенного в ходе последней реакции, формируются кристаллические волокна гидрата оксида алюминия с размером 20 нм-50 нм в диаметре. Волокна оксида алюминия также были получены в результате контролируемого окисления расплавленного алюминия смесью кислорода и газа- разбавителя. Однако небольшие сферические частицы алюминия загрязняют волокна. Патент США №3947562 описывает приготовление волокон путем реакции окисления газообразного трифторида алюминия с углекислым газом при 1275°С - 1700°С с достаточным количеством водорода для реакции с хлором и образованием HCl. Получающиеся волокна очень большие и, в дополнение, в них обнаруживаются частицы равно как и другие формы. Патент США №4331631 описывает формирование волокон оксида алюминия путем окисления нержавеющей стали, содержащей алюминий. Волокна алюминия образуют покрытия с хорошим сцеплением и используются для производства автомобильных катализаторов окисления выхлопных газов после нанесения на них покрытия платины. Khalil произвел длинные и короткие волокна бемита гидролизом алькоксида алюминия.
[0050] Предпочтительным методом производства волокон оксида алюминия в данном изобретении является реакция микронного и предпочтительно наноразмерного порошка алюминия с водой. Предпочтительный наноразмерный порошок алюминия производится с помощью предпочтительного способа, используемого в методе взрыва металлических проволочек. Алюминиевый провод диаметром 0,3 мм подается в реактор, содержащий примерно 3 абсолютных атмосферы аргона. Отрезок провода примерно 100 мм длиной взрывается в результате подачи 500 Джоулей (примерно 25 кВ напряжения и 20 кА электрический ток при емкости набора конденсаторов около 2,4 мкФ). В течение импульса тока, который длится приблизительно 1 микросекунду, достигается температура, превышающая 10000 К, и при этом излучаются рентгеновское и ультрафиолетовое излучения. Кластеры металла расширяются в аргон, в результате чего достигается большая скорость охлаждения и сложная микроструктура в алюминии, когда он превращается в твердофазную форму. Yavorovski описывает детали процесса и установку. Порошок алюминия может быть открыт к доступу сухого воздуха для пассивации (окисления) поверхности, так что с ним можно дальше работать в открытом воздухе без его самовоспламенения. Результирующие сферы наноалюминия получаются без внутренних пустот со средним размером частиц 110 нм и до некоторой степени агломерированы. Определенная БЭТ удельная поверхность порошков составляет приблизительно 20 м2/гр.
[0051] Полученный таким путем металлический алюминий реагирует с водой при 75°С, в результате чего получается золь алюминия, который фильтруется и затем нагревается. На первом этапе порошок нагревается до 100°С. Результирующий порошок прогревается на 200°С - 450°С, создавая смесь гидроксида алюминия Al(OH).sub.3 и бемита (AlOOH). Чем выше температура, тем выше содержание бемита и тем ниже содержание гидроксида алюминия.
[0052] Альтернативным методом является использование алюминия, полученного в результате взрыва алюминиевой проволоки в атмосфере азота при трех атмосферах абсолютного давления. Азот дешевле, чем аргон, и при этом исключается необходимость в пассивация порошка, поскольку порошок, покрытый нитридом алюминия, не пирофорен. В этом случае металлические частицы алюминия покрыты слоем нитрида алюминия (AlN). В ходе гидролиза производятся волокна бемита. При этом образуются аммиак и водород как вторичные газообразные продукты.
[0053] ФИГ.1 и 2 показывают электронные микроскопические фотографии в проходящих лучах нановолокон, имеющих диаметр 2-3 нм. ФИГ.1 показывает волокна, изготовленные гидролизом наноалюминия, полученного в аргоне и окисленного сухим воздухом. Нановолокна оксида алюминия, показанные на ФИГ.2, были приготовлены из наноалюминия, полученного в атмосфере азота и имевшего покрытие из AlN. Волокна выглядят агрегированными в виде открытой сети с отношением длины к диаметру до 100 и более. Непрозрачные области являются результатом недостаточного диспергирования волокон и их наложение друг на друга в поле зрения. Удельная поверхность волокон, показанных на ФИГ.1 и 2, и определенная методом БЭТ, составляет приблизительно 475 M.sup-2/гр. Рассчитанная площадь удельной поверхности при предположении, что нановолокна имеют диаметр 2 нм, точно такая же, как получена в результате измерения с помощью метода БЭТ, что указывает на то, что большинство поверхности (по меньшей мере доступной для поглощения азота) находится на внешней поверхности волокон. Волокна, полученные из алюминия, приготовленного пассивированием кислородом или азотом, имеют похожие размеры и имеют похожие кристаллографические картины, когда увеличение на электронно-микроскопических фотографиях в проходящих лучах примерно одно и то же. Во всех примерах, приведенных ниже, использовался наноалюминий, полученный в аргоне, если не указано иное.
[0054] Химическая и структурная характеризация волокон. Потеря веса при нагревании до 200°С составляет 5,4%, при нагревании до 550°С составляет еще 6.7%, и еще 2.7% при кальцинировании до 1100°С или в сумме 14% химически связанной воды. Дериватограмма сопоставима с коммерческим бемитом, альфа-моногидрата оксида алюминия; альфа.-Al.sub.2O.sub.3.H.sub.2O, который имеет 15% воды. Результаты рентгеновской дифракционной картины показывают, что порошок, нагретый до 300°С состоит в основном из гидроксида алюминия, Al(OH).sub.3 и бемита (AlOOH) со следами гамма-фазы оксида алюминия (Al.sub.2O.sub.3). После нагревания при 465°С в течение 3 часов и затем при 200°С в течение 24 часов пики гидроксида и бемита исчезают. Спектры, полученные с помощью метода рентгеновского возбуждения с последующим анализом на различных длинах волн (XED) и с помощью метода Фурье преобразования инфракрасного спектра (FTIR), также подтверждают структуру оксида алюминия (включая оксид-гидроксидные фазы) как главные компоненты нановолокон.
[0055] Нижеприведенные примеры иллюстрируют процедуры применения настоящего изобретения. Эти примеры не должны рассматриваться как единственно возможные. Все процентные соотношения приведены по весу и все смеси жидкостей по объему, если не указано иное.
ПРИМЕР 1
[0056] Таблица 1 представляет данные по адсорбции вирусов несвязанными нановолокнами оксида алюминия (0,7 гр), приготовленного, как описано выше. Нановолокна были помещены на серию обычных микропристый фильтров диаметром 25 мм (Millipore НА, 0,45 микрон средний размер пор) и испытывались в сравнении с контрольными фильтрами Millipore НА. Два фильтра были использованы последовательно для минимизации возможности шунтирования первого фильтра, поскольку волокна были в свободном виде. Два вида вирусов-бактериофагов MS-2 и phi.Х174 с размером примерно 30 нм и сферичной формы были использованы для проведения испытаний. Их детектирование велось в единицах бляшкообразования (PFU) с использованием метода двойного слоя с использованием Escherichia coli C-3000 как организма-хозяина. Тесты проводились при рН 7,5, что, как известно, не является благоприятным для электроадсорбции вирусов на мембранах. Тест был проведен при протекании раствора через фильтры с равной скоростью потока в каждом испытании.
Поглощение вирусов нанокерамическими волокнами
[0057] Результаты показывают, что в результате добавления нановолокон на поверхность мембран получилась очень высокая степень удержания вирусов. Не желая быть связанным любой предложенной теории, ниже предложен следующий механизм. Сами по себе нановолокна являются гидрофильными. Удельная площадь их поверхности в 5-10 раз выше той же величины для волокнистого асбеста. На их поверхности находится большое количество гидроксильных групп. Основные компоненты волокон это либо гидроксид алюминия Al(OH).sub.3, либо бемит (AlOOH), либо их смесь. Увеличенная концентрация гидроксильных групп дает волокнам электрически положительных заряд. Форма волокон позволяет распределить заряд соответствующим образом вместо того, чтобы аккумулировать его, как это случилось бы, если бы частицы были сферичны.
[0058] Высокое значение положительного заряда притягивает и удерживает электроотрицательные частицы или макромолекулы. Если бактерии не задерживаются в межволоконном пространстве, то они будут адсорбироваться на волокнах электростатически. Бактерии электроотрицательны из-за их клеточно-мембранной химии. Грам-позитивные бактерии содержат тейкойную кислоту, фосфатсодержащий полимер, который сообщает отрицательный заряд поверхности. Грам-отрицательные бактерии, в изобилии присутствующие в воде, содержат негативно заряженные группы COO.sup.-, ассоциирующиеся с протеинами и липополисахаридами в клеточных стенках. Другие тела с отрицательным зарядом включают в себя грам-отрицательные бактериальные эндотоксины (пирогены), вирусы, органические и неорганические коллоидные частицы. В добавление к высокой плотности заряда большая площадь поверхности волокон увеличивает скорость адсорбции/адгезии, что позволяет использовать тонкие слои, необходимые в случае фильтров, в которых весь поток полностью проходит через них. Это также приводит к более коротким путям обмена при использовании фильтров в режиме поперечного потока.
ПРИМЕР 2
[0059] Бактериофаг MS-2 разбавлялся в 150 мл буферном растворе 0.02М имидазола/0.02М глицина (рН 7.2), что дает эффективную концентрацию приблизительно 8-10.sup.5/мл. Нановолокнистый оксид алюминия (0,5 грам) помещали в 15 мл коническую пробирку центрифуги с 10 мл раствора бактриофага. Порошок был полностью диспергирован вихревой мешалкой и встряхиваением на столике в течение 15 минут. Смесь центрифугировалась при малой скорости (2500 об/мин) для осаждения порошка на дне пробирки и оставшаяся на поверхности жидкости анализировалась на присутствие вируса. Начальная и конечная проба бралась из буферного раствора с бактриофагом для проверки постоянства концентрации вируса в нем за время эксперимента. Таблица 2 показывает, что температуры обработки волокон 150°С и 450°С не влияют на адсорбцию вируса. Данные показывают также, что наноксидные волокна являются веществом, которое активирует осаждение, удаляя вирус из раствора с эффективностью до >3,9 logs за один цикл.
Поглощение вирусов из воды нанокерамическими волокнами
[0060] Устройство, состоящее из волокон оксида, заключенных внутри сетчатого контейнера или в форме волокнистого слоя, который будет собирать на себя вирусы или другие электроотрицательные частицы в статической системе. Если поместить такое устройство в сосуд с предварительно стерилизованной водой, то оно соберет бактерии вирусы, циркулирующие по сосуду в результате естественной или принудительной конвекции и будет поддерживать стерильность в случае какого-либо загрязнения. Таким, образом это будет работать как микробная ловушка. Устройство поэтому заменяет собой использование химических дезинфектантов (таблеток хлорина, в настоящее время используемых для поддержания стерильности в полевых условиях). Микробная ловушка обеспечит также лучший вкус воде и снизит отрицательное влияние на здоровье побочных продуктов дезинфекции.
ПРИМЕР 3
[0061] Для того, чтобы устранить шунтирование и просачивание жидкости вокруг волокнистого фильтрующего слоя, волокна лучше интегрировать в композит. Нетканые сечатые фильтры диаметром 25 мм в диаметре (площадь поверхности 5 см.sup.2) приготавливались путем смешивания нановолокон со стекловолокном (Type B-06-F от Lauscha Fiber International, размеры - диаметром 0,6 микрон и 2-3 мм в длину) в воде. Примерно 1,5-2 г микростекла смешивали с 400 мл дистиллированной воды и затем добавляли различные количества нановолокон оксида алюминия для получения различных соотношений между стекловолокном и нановолокном. Смесь затем гомогенизировалась в миксере при высоких оборотах. После приготовления композитная смесь принудительно прокачивалась через фильтр с размером пор 5 микрон для получения тонкого фильтрующего композитного слоя. Этот слой отделялся от грубого фильтра и высушивался на воздухе при комнатной температуре. Одним из преимуществ нановолокон по сравнению со сферическими частицами является то, что их форма позволяет делать фильтры с очень высокой пористостью (приблизительно 70-80 об.%). Образцы. А7-52 (Таблица 3) были получены из наноалюминия (термообработка при 400°С), как описано в Примере 2, и смешаны с микростеклом. Нановолокна, использованные в образцах 53-62, были просеяны через сито с ячейкой 400-mesh для получения волокон, которые могут быть достаточно равномерно распределены по объему фильтра. Образцы испытывались на MS-2, как описано в Примере 1, и на вирусе PRD-1. Вирус PRD-1 приблизительно 60 нм в размере и отличается от MS-2 и phi.X174 тем, что он более гидрофобен благодаря липидам во внешней оболочке. Таблица 3 показывает, что задержка вируса увеличивается с увеличением процентного содержания нановолокон в фильтре. Кроме того, этот результат показывает, что лучшее диспергирование нановолокон (при отсеивании агрегатов) дает улучшение задержки вирусов на порядок величины или более.
Тест на удержание вирусов фильтрами на основе нановолокон оксида алюминия/микроволокна стекла
ПРИМЕР 4
[0062] Фильтры, приведенные в примерах с 4 по 14, изначально были изготовлены с нанопорошком алюминия. Алюминий реагировал с водой в присутствии смеси стекловолокона (см. Табл. 4 образцы №63-68). Примерно 1,5-2 г микростекла смешивались с 400 мл дистиллированной воды с наноалюминием. Количество наноалюминия варьировалось в зависимости от отношения микростекло/нановолокно в фильтре. Смесь нагревалась до 75°С в течение 3-10 минут, реакция становилась очень энергичной и продолжалась еще в течение 3-5 минут. Фильтр приготавливался, как описано в Примере 3. Образцы 69 и 70 приготавливались так же, как и 63-68, но кроме того были обработаны ультразвуком с помощью Fisher ultrasonic cleaner, модель FS20, в ходе реакции алюминия с водой. По другому варианту процесса золь нанооксида образовывался без удаления частиц из маточного раствора. Микростекло добавлялось к смеси потом (образцы №71 и 73). Начальная концентрация вируса была 5-10.sup.4 pfu/мл в буфере рН 7,5 при скорости потока через фильтр 1 см/с для образцов 63-68, и 0,5 см/с для образцов 71 и 73. Когда наноалюминий прореагировал в присутствии микростекла, то скорость потока была выше, чем если бы стекло добавляли к смеси позднее. Примеры 5-14 использовали реакцию алюминия водой в присутствии микростекла.
[0063] На ФИГ.3 свежеприготовленные образцы фильтров были изучены с помощью электронно-микроскопической фотографии в проходящих лучах (ПЭМ). Нановолокна оксида алюминия собираются в агрегаты или диспергируются и присоединяются к волокнам микростекла. Такое диспергирование как раз и отвечает за улучшенную адсорбцию вирусов (Таблица 3).
Тест на удержание вирусов смесевыми фильтрами на основе нановолокон оксида алюминия/микроволокна стекла
ПРИМЕР 5
[0064] На ФИГ.4 показаны фильтры диаметром 25 мм, 1 мм толщиной, полученные, как описано в примере 4. Эти фильтры были испытаны на скорость фильтрации при давлениях 0.2 и 0.7 атм (0.2 и 0.7 бар). ФИГ.4 показывает, что линейная скорость потока при 0.7 бар была относительно постоянна и равна 1.6 см/с при 40 весовых процентах (вес.%) нанооксида в фильтре. Такая скорость потока существенно выше (примерно на два порядка), чем для ультрапористых мембран. Скорость потока мембран Millipore для ультрапористых фильтров VS (25 нм - размер пор) только 0.0025 см/с при давлении 0.7 бар, примерно в 660 раз меньше, чем в приведенном примере. В общем, скорости потоков мембран годятся для фильтрования вирусов при 300-600 л/м2/ч. Нановолокнистые фильтры достигают высокой эффективности задержки для вирусов 30 нм размером при скоростях от 10,000 до 20,000 л/м2/ч.
[0065] Причина такой высокой пропускной способности - увеличенная пористость нановолокнистого фильтра. При содержании нановолокон до 40 вес.% они полностью распределены по микростеклу и не увеличивают гидравлическое сопротивления фильтра. Дополнительным фактором является гидрофильность фильтра. Мембраны делаются из целлюлозных эфиров, пластиков и поэтому являются гидрофобными. Вода может проходить через гидрофобный фильтр, но требуемое давление очень сильно увеличивается в зависимости от величины пор (менее чем 1 микрон) и тем самым создается значительный перепад давлений. Кроме того, увеличивается риск неравномерного смачивания. Мембраны часто обрабатывают различными веществами, увеличивающими смачиваемость, такими как глицерин, Tween, и Triton Х-100. Такие вещества могут однако влиять на обработку специальных продуктов, например в фармацевтике.
ПРИМЕР 6
[0066] Целью этой серии экспериментов было определить максимально возможную эффективность удаления вирусов. Пример 4 показал, что начальная концентрация вируса была недостаточной для различения каких-либо отклонений и поэтому мы увеличили ее до 1-10.sup.7 pfu/мл. Были осуществлены следующие эксперименты (Таблица 5) в буфере с рН 7,5 (вода) при скорости потока 1 см/с. Задержка вируса с эффективностью >6 logs (>99.9999%) была получена, начиная с 20 wt % наноксида в фильтре. Когда все образцы были последовательно испытаны, то все они показали удержание вирусов >6 logs, тогда фильтры с <20 весовых % были приготовлены и испытаны (образцы 113-120). Данные показывают, что увеличение эффективности при увеличении загрузки нановолокн до 20 вес.%. Любое другое испытание на вирусы ограничивается трудностью получения потока с концентрацией >107 pfu/мл. Данные предполагают, что задержка вирусов фильтрами с 30-6 в % нановолокон будет значительно выше, чем данные в Таблице 5.
Удержание вирусов фильтрами на основе нановолокон оксида алюминия
ПРИМЕР 7
[0067] Целью этой серии является измерение эффективности задержки бактерий (В. coli 0157H7) и вирусов (MS-2 и полимиелит) в присутствии аналога морской воды, а также сточных вод. Образцы фильтров (Табл.6) приготавливали, как показано в Примере 6. Искусственная морская вода (образцы №135, 136) не влияет или влияет в очень малой степени на задержку вирусов и бактерий по сравнению с контрольными образцами (образцы №131, 132), тем самым показывая, что фильтры эффективны в соленой или подсоленной воде. Данные также указывают на то, что нановолокнистые фильтры могут быть использованы как предварительные фильтры для минимизации забивания мембран обратного осмоса, используемых для опреснения воды. Сточные воды приготавливались из стоков путем пропускания сточной воды через 100 мк фильтр, затем смешивались с вирусами и Е. coli перед пропусканием через тестовый фильтр. Никакой разницы в эффективности не было замечено между фильтрацией сточных вод и буферного раствора, т.е. фильтр может удалять вирусы и бактерии из сточных вод.
Удержание вирусов и бактерий из соленой и сточных вод
2 - Сточная вода получена со станции по очистке сточной воды при Университете Флориды и затем профильтрована через фильтр с размером пор 100 микрон
3 - Коммерчески выпускаемая смесь солей, имитирующая морскую воду (Instant Ocean®), подъюстированная к рН 7,8.
4 - Е. coli O157Н7 была сделана устойчивой к Rifarnpicin и высеяна на пластинки с агаром, при этом заражая Tryptic Soy с добавлением 0,1 г Rifarnpicin /1000 мл.
[0068] Результаты Таблицы 6 показывают, что бактерии могут удерживаться на нановолокнистом фильтре. DiCosmo обнаружил, что слои стекловолокна могут эффективно иммобилизовывать биомассу Catharanthus roseus. Добавление нановолокон оксида еще больше улучшает иммобилизацию и такие композиционные слои могут быть использованы как подложки для сбора продуктов и размножения бактерий в биосинтезе. Заявка на патент U.S. Serial No. 60/324398 (поданный в сентябре 24, 2001 Purdue Univ) демонстирует, что клеточная костная ткань (клетки кости) присоединяются и затем растут на нановолокнах оксида, и значит слои такого материала могут быть использованы как эффективная подложка для роста клеток млекопитающих.
ПРИМЕР 8
[0069] Цель этого примера (Табл.7) - определение возможности сбора живых вирусов с образца для последующего анализа. Все образцы содержали 40 вес.% нановолокон с микростеклом, приготовленных как описано в примера 4. Фильтры были подвергнуты действию раствора вирусов 1-10.sup.5 pfu/мл в буферном растворе на рН 7,5, как описано в примере 4. После пропускания 10 мл вирусного раствора через фильтр, через него, в обратном направлении, пропускался раствор 10 мл 1,5% мясного экстракта и 0,25% глицин при рН 9,3. Результаты показывают, что живые вирусы могут быть вытеснены из нанововлокнистых фильтров для целей дальнейшего анализа.
Удержание/смыв MS-2 и полио вирусов
морская вода
[0070] Фильтр может быть регенерирован несколькими способами, включая, но не ограничиваясь следующими:
[0071] А. Увеличение рН элюата до тех пор, пока фильтр не приобретет нулевой или отрицательный заряд.
[0072] В. Элюирование с помощью макромолекул, таких как мясной экстракт, который является более предпочтительным для адсорбции частицей, чем частица, которую он вытесняет.
[0073] С. Высушивание и/или нагрев фильтра для удаления связанной и адсорбированной воды уничтожением ионого заряда, который вносит вклад в электростатический заряд. Фильтр высушивается при температурах, когда сохраняется жизнеспособность патогенов, или при более высоких, для их уничтожения на месте. Как нановолокна оксида, так и микростекло термически стабильны до температур выше, чем 300°С, при которых бактерии и вирусы полностью уничтожаются.
[0074] D. Электрохимическая регенерация фильтра. Отрицательный электрод может быть введен в фильтр для генерации отрицательных ионов и замещения адсорбированных частиц. Электрод делается из нержавеющей стали (сетка) и вводится в состав фильтра вместе с частицами графита или графитизированного углерода. По крайней мере 5 объемных % графита можно ввести в состав фильтра для увеличения его проводимости. Позитивный металлический электрод, устойчивый к электроокислению (нержавеющая сталь, вольфрам или тантал), помещается вне фильтра. После цикла адсорбции фильтр электрохимически регенерируется пропусканием жидкости в направлении, противоположном фильтрованию, при этом адсорбированные частицы замещаются отрицательными ионами.
ПРИМЕР 9
[0075] Данные на ФИГ.5 были получены с целью измерения емкости фильтров по частицам путем фильтрования монодисперсных латексных шариков размером 30 нм (Duke Scientific Corp.) согласно методу Hou. Фильтры были изготовлены, как показано в Примере 4. Оптический турбидиметр (LaMotte Model 2020) использовался для измерения мутности профильтрованного раствора. Начальный раствор состоял из дистиллированной воды и латексных шариков с концентрацией 1012 частиц.мл. Мы испытывали фильтры диаметром 25 мм (эффективная площадь поверхности - 5 см.sup.2) при постоянной скорости потока и в сравнении с фильтром Cuno MDS-1. Нановолокнистые фильтры укладывались так, чтобы сзади них находился мембранный фильтр с 5 мк порами для страховки от вываливания микростекла в фильтрат. Такой сэндвич уплотнялся с помощью O-колец так чтобы не происходило просачивание раствора вне области фильтрации. ФИГ.5 иллюстрирует кривые пробоя для двух типов фильтров. Единицы по оси абсцисс представляют общее количество латексных шариков в изначальном растворе на 1 кв. см площади фильтра. Эти данные указывают на то, что емкость сорбции (точка, при которой появляется мутность) нановолокон для 30 нм частиц в три раза выше, чем у фильтра Cuno.
ПРИМЕР 10
[0076] На ФИГ.6 проставлены результаты теста по сравнению емкости сорбции фильтров в зависимости от содержания в них нанооксида. Емкость почти прямо пропорциональна содержанию нанооксида в фильтре. Способность к увеличению емкости за счет увеличения толщины является главным преимуществом нановолокнистых фильтров по сравнению с мембранами. Удвоение толщины нановолокнистого фильтра (НФ) приводит к удвоению емкости за счет лишь половинного сокращения скорости фильтрации, тогда как удвоение толщины мембраны приводит не только к быстрому ее забиванию, но также не увеличивает ни ее емкость, ни ее эффективность. Начальная эффективность задержки вирусов у более толстого фильтра существенно выше, чем 7 logs.
[0077] Кривые пробоя на ФИГ.5 и 6 являются типичными кривыми адсорбции для колонок жидкостной хроматографии, за исключением того, что адсорбция в этом случае является результатом противоположных электрических зарядов сорбента и частицы. Поэтому слой нановолокон может служить в качестве эффективной колонки для сепарации вирусов и других макромолекул на основе их зарядов.
[0078] На ФИГ.7 предоставлены изображения, полученные с помощью сканирующего электронного микроскопа (СЭМ), микростекла из фильтра с адсорбированными латексными шариками после насыщения и пробоя их в фильтрат. Можно заметить, что микростекло полностью покрыто слоем шариков и в свободном виде их нет. Это показывает то, что шарики адсорбируются довольно прочным образом на микростекле.
ПРИМЕР 11
[0079] На ФИГ.8 показано ухудшение скорости фильтрации, показатель возрастающего сопротивления фильтра при его забивании, которое измерялось в сравнении между НФ и мембраной с 25 нм порами (Millipore VS). Начальный раствор содержал 1012 шариков/мл. Прилагалось давление на уровне 0,7 атм (0.7 бар). НФ приготавливался, как показано в Примере 4, и был 1 мм толщиной и содержал 40 вес.% нановолокон. До самой точки насыщения фильтра шариками (8-1012 шариков/кв.см) не было замечено сколь-нибудь заметного изменения скорости фильтрации, тогда как мембрана потеряла 70% скорости в том же самом интервале, предположительно из-за забивания поверхности пор. В точке насыщения поток через НФ был примерно на три порядка величины больше, чем для мембраны. Отсутствие постепенного ухудшения скорости фильтрации у НФ происходит скорее всего из-за того, что шарики не уменьшают поперечное сечение пор в фильтре.
ПРИМЕР 12
[0080] Пример 11 был повторен, но уже с 3-микронными шариками, в сравнении между НФ с 40 вес.% нановолокон и мембраной с порами 0.45 мк (Millipore-HA). Цель такого эксперимента была определить уменьшение скорости фильтрации при фильтрации частиц, по размеру своему соответствующих бактериям и инфузориям. Фиг.9 демонстрирует, что падения скорости фильтрации на НФ было аналогичным мембране с порами 0.45 мк. Скорость потока через НФ спадала до тех пор, пока не соответствовала скорости потока через мембрану. Оказалось, что микронные частицы собираются (отсеиваются) на поверхности обоих фильтров и затем накапливаются, после чего поток контролируется толщиной нароста и его пористостью. Это подтверждается тем, что слой больших латексных шариков можно отделить от поверхности фильтров, тогда как на НФ не наблюдалось формирования такого слоя, если использовались шарики размером 30 нм. (см ФИГ.5-8). На ФИГ.9 показано, что фильтр с 40 вес.% нановолокон и сделанный согласно методу в Примере 4 будет фильтровать частицы с размерами бактерий за счет чисто размерного эффекта пор, а не за счет электростатического эффекта, как в случае вирусов. Однако НФ могут быть оптимизированы для электростатической адсорбции бактерий путем увеличения пористости и номинального размера пор. Такое увеличение пористости может быть достигнуто за счет добавления более крупных волокон к начальной смеси. Кроме того, слой, оптимизированный для улавливания вирусов, может стоять позади фильтра для микронных частиц. Общий эффект таких ступенчатых фильтров будет заключаться в меньшем забивании, более высоких скоростях фильтрации и длительном сроке службы перед регенерацией или заменой.
ПРИМЕР 12А
[0081] Золь бемитных нановолокон был получен реакцией между крупным порошком алюминия (Valimet Corp. №Н-5) и водой при 100°С в присутствии смеси микростеклянных волокон. Фильтры были приготовлены и испытаны, как в Примере 4, на MS-2 с концентрацией 1·107 pfu/мл. Данные показали эффективность задержки вируса, эквивалентную фильтрам, полученным из нанопорошков алюминия. Другой вариант нановолокон был получен из гидротермической реакции между гидроксидом алюминия и гидроксидом аммония (NH4OH). Смесь примерно 6 грамм стекловолокон, 5,2 грамм Al(ОН)3, и 1 мл 30% NH4OH в 100 мл воды нагревалась до 170°С. (давление пара приблизительно 10 бар) в течение 2 часов. После охлаждения порошок фильтровался и приготавливался фильтровальный материал, как для образцов 63-68 в Примере 4. Данные Таблицы 8 показывают >99.9% эффективность задержки вируса фильтрами толщиной 2 мм.
Удержание вирусов фильтрами на основе нановолокон оксида алюминия, приготовленных альтернативными методами
ПРИМЕР 13
[0082] Трехслойный фильтр, состоящий из внешнего слоя целлюлозы (смесь из распушенного хлопка GR 505 Buckeye Cellulose Corp с водой) толщиной приблизительно 0.2 мм и внутренний слой из 40% смеси нановолокон и микростекла, толщиной 1.2 мм. На первой стадии смесь из целлюлозы была приготовлена, как описано в Примере 4, и затем выливалась в воронку Бюхнера с фильтром №5, таким образом формируя первый слой целлюлозы. Будучи еще во влажном состоянии, смесь нановолокон и микростекла выливалась на первый слой целлюлозы. После часа сушки выливался дополнительно еще один слой целлюлозной смеси. Поскольку композитный слой нановолокон и микростекла обладал небольшой прочностью в сухом и влажном виде, то слоистая структура обеспечивала более высокую прочность на отрыв и жесткость, необходимую для использования в различных условиях.
ПРИМЕР 14
[0083] Структура, подобная той, которая приведена в Примере 13, где вместо целлюлозного слоя использовали плавкую органическую пористую ленту (Singer Sewing Co. Fusing Tape). Полученный композит имел повышенную прочность на разрыв, чем образец в Примере 12. Характеристики потока были близки к образцам Примера 4.
ПРИМЕР 15
[0084] Синтетическая ткань (Delnet P620, Delstar Technologies, Middletown, Del.) была использована для покрытия трубчатого сетчатого фильтра 1,325 дюйма в диаметре и 8,4375 дюйма в длину. Фильтр был закрыт с одного конца, а с другого присоединен к вакуумному трубопроводу. Все устройство погружалось в смесь примерно 2 л дистиллированной воды, смешанной с 3,7 г микростекла и 2,5 г нановолокон оксида алюминия. Вакуум создавался по центральной оси погруженного в жидкость фильтра. Смесь осаждалась на поверхности фильтра, и после сушки слой достигал толщины 1 мм и площади поверхности 35 кв. дюйма.
[0085] Следующие (но не ограниваясь этими) модификации нановолокнистого материала могут быть сформулированы так: они увеличат прочность и снизят выпадение волокнистого материала в водный поток:
[0086] А. Добавки силана, например триметоксил силана к смеси;
[0087] В. Добавка более длинных или крепких волокон, таких так рубленая целлюлоза или волокна выдутого через тонкие отверстия расплавленного полимера к смеси нанооксид алюминия/микростекло;
[0088] С. Добавка термопластического волокна к смеси нанооксид алюминия/микростекло, которое можно расплавить нагревом или приклеить для обеспечения связи между компонентами после сушки фильтра;
[0089] D. Осаждение нановолокон на сетку из целлюлозы, пластика или металла;
[0090] Е. Помещение дисков, сделанных влажным методом и включающее в себя нановолокна оксида алюминия, между сеточками термопластика и его нагрев до частичного расплавления композита;
[0091] F. Добавление связующих материалов, включая крахмал, полиакриламиды, которые увеличат прочность нановолокнистого слоя водородными связями, или
[0092] G. Добавление клея (формальдегидная мочевина) или термопастческих формальдегидно-меламиновых смол к ядру из нанооксида алюминия.
[0093] Фильтровальный материал в виде листов может быть применен самостоятельно или в сочетании с другими материалами для удаления субмикронных и наноразмерных частиц из жидкостей, включая стерилизацию воды от вирусов, обработку фармацевтических продуктов - антибиотиков, растворов солей, декстрозы, вакцин, плазмы крови, сывороток, очистки напитков - вина и крепких напитков, косметики, соков, антисептиков, фоторастворов, чистящих средств и т.д.
[0094] Материал может быть использован для сбора и отбора проб микробных патогенов с целью обнаружения и анализа.
[0095] Волокна оксида алюминия можно использовать для разделения двух макромолекул, таких как протеины. Это можно сделать либо хроматографически на основе различия между зарядами молекулам, либо при наложении электрического поля (электрофорезис).
[0096] Так как предыдущие изложение представляет наилучший вариант от изобретателя по использованию изобретения и предназначено для воспроизводства квалифицированными специалистами, то ясно, что методы, включающие улучшения и вариации, будут очевидными для специалистов в соответствующих областях. Поэтому эта заявка не должна истолковываться так, что все ограничивается только вышеупомянутым, но должна также включать в себя очевидные изменения и, в основном, должна определяться духом и областью применимости следующих утверждений.
Патенты цитируемого класса
[0097] U.S. Pat. No. 2783894-March 1957 Lovell, et al. 210/500.38
[0098] U.S. Pat. No. 2915475-December 1959 Bugash 516/94
[0099] U.S. Pat. No. 3031417 April 1962 Bruce 516/94
[0100] U.S. Pat. No. 3408315-October 1968 Payne 264/49
[0101] U.S. Pat. No. 3242073-March 1966 Guebert 210/64
[0102] U.S. Pat. No. 3352424-November 1967 Guebert 502/62
[0103] U.S. Pat. No. 3947562-March 1976 Grimshaw 423/630
[0104] U.S. Pat. No. 4007113-February 1977 Ostreicher 210/504
[0105] U.S. Pat. No. 4007114-February 1977 Ostreicher 210/504
[0106] U.S. Pat. No. 4178438-December 1979 Haase, et al. 536/30
[0107] U.S. Pat. No. 4230573-October 1980 Kilty, et al. 210/767
[0108] U.S. Pat. No. 4282261-August 1981 Greene 426/330.4
[0109] U.S. Pat. No. 4288462-September 1981 Hou, et al. 426/423
[0110] U.S. Pat. No. 4305782-December 1981 Ostreicher, et al. 162/181.6
[0111] U.S. Pat. No. 4309247-January 1982 Hou, et al. 162/149
[0112] U.S. Pat. No. 4321288 March 1982 Ostreicher 427/244
[0113] U.S. Pat. No. 4331631 May 1982 Chapman 422/180
[0114] U.S. Pat. No. 4366068-December 1982 Ostreicher, et al. 210/767
[0115] U.S. Pat. No. 4473474-August 1984 Ostreicher, et al. 210/636
[0116] U.S. Pat. No. 4523995-June 1985 Pall, et al. 210/504
[0117] U.S. Pat. No. 4604208-August 1986 Chou, et al. 210/636
[0118] U.S. Pat. No. 4617128-October 1986 Ostreicher 10/679
[0119] U.S. Pat. No. 4673504-June 1987 Ostreicher, et al. 210/500.22
[0120] U.S. Pat. No. 4708803 November 1987 Ostreicher, et al. 210/650
[0121] U.S. Pat. No. 4711793-December 1987 Ostreicher, et al. 427/244
[0122] U.S. Pat. No. 4743418-May 1988 Bames, et al. 264/48
[0123] U.S. Pat. No. 5085784-February 1992 Ostreicher 210/767
[0124] U.S. Pat. No. 5104546-April 1992 Filson, et al 210/650
[0125] U.S. Pat. No. 5219577-June 1993 Kossovsky, et al 424/494
[0126] U.S. Pat. No. 5798220-August 1998 Kossovsky, et al 435/13
[0127] U.S. Pat. No. 5855788-January 1999 Everhart, et al. 210/653
[0128] U.S. Pat. No. 6197515-March 2001 Bamdad ,et al 435/6
СПИСОК ЛИТЕРАТУРЫ
[0129] Ahuja, S, (2000) Handbook of Bioseparations-Academic Press.
[0130] DiCosmo, et al., (1994)-Cell Immobilization by Adsorption to Glass Fibre Mats-in Immobilized Biosystems, Edited by Veliky, I. A. and McLean, R J. C-Blackie Academic & Professional.
[0131] Farrah, S.R. and Preston, D.R., (December 1985) Concentration of Viruses from Water by Using Cellulose Filters Modified by m-situ Precipitation of Ferric and Aluminum Hydroxides, Applied and Environmental Microbiology, 1502-04.
[0132] Farrah, S.R. and Preston, D.R. (1991) Adsorption of Viruses by Diatomaceous Earth Coated with Metallic Oxides and Metallic Peroxides, Water Sci. Tech., V. 24:2, 235-40.
[0133] Gitzen, W.H., (1970) Alumina as a Ceramic Material, American Ceramic Soc., Special publication 4, pp. 13-14
[0134] Hou, K. et al. (November 1980), Capture of Latex Beads, Bacteria, Endotoxin and Viruses by Charge-Modified Filters, Appl. And Environmental Microbiology, 892-96.
[0135] Khali, Kamal M.S., (1998), Journal of Catalysis, 178,198-206.
[0136] Lukasik, J., et al., Influence of Salts on Virus Adsorption to Microporous Filters-Appl. Environ. Micro. 66:2914-20 (Lukasik I).
[0137] Lukasik, J., et al. (1999). Removal of Microorganisms from Water by Columns Containing Sand Coated with Ferric and Aluminum Hydroxides, Wat Res. 33: 3,769-77, (Lukasik II).
[0138] Mandaro, (1987) "Charge Modified Depth Filters: Cationic-Charge Modified Nylon Membranes" in Filtration in the Pha in maceutical Industry, T. H. Meltzer Ed., Marcel Dekker, Inc., New York, N.Y.
[0139] Meltzer, T.H. and Jomitz, M.W., (1998), Filtration in the Biopharmaceutical Industry-Marcel Dekker, New York, 1998, pp.262-265
[0140] Nycomed Applications and Products brochure, (2000) 39.
[0141] Robinson et al. (1985), "Depyrogenation by Microporous Membrane Filters", in Technical Report No. 7, Depyrogenation, Parenteral Drug Association, Inc., Phila, Pa.
[0142] Sinha, D., (1990) "Pretreatment Process Considerations for the Semiconductor Industry" in Ultrapure Water 7:6, 21-30.
[0143] Sobsey, M.D. and Jones, B.L., (March 1979), Concentration ofPoliovirus from Tap water Using Positively Charged Microporous Filters-Appi and Environmental Microbiology, 588-595.
[0144] Willkommen, H., (Oct. 1-3, 2001), Virus Validation of Filtration Procedures, PDA/PDA Viral Clearance Forum, Bethesda, Md.
[0145] Yavorovsky, N.A., (1996) Izvestiia VUZ. Fizika 4:114-35.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕТКАНЫЙ МАТЕРИАЛ, ВКЛЮЧАЮЩИЙ УЛЬТРАМЕЛКИЕ ИЛИ НАНОРАЗМЕРНЫЕ ПОРОШКИ | 2007 |
|
RU2394627C1 |
| ФИЛЬТРУЮЩЕЕ УСТРОЙСТВО ДЛЯ ПИТЬЕВОЙ ВОДЫ | 2007 |
|
RU2426579C2 |
| ФИЛЬТРУЮЩИЙ МАТЕРИАЛ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ФИЛЬТРОВАНИЯ | 2005 |
|
RU2317843C2 |
| АГЛОМЕРАТЫ ОКСИГИДРОКСИДОВ МЕТАЛЛОВ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2560432C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФИЛЬТРУЮЩЕГО МАТЕРИАЛА | 2005 |
|
RU2297269C1 |
| Способ получения микро-мезопористых наноматериалов на основе складчатых нанолистов оксигидроксида алюминия и материал, полученный данным способом | 2017 |
|
RU2674952C1 |
| ФИЛЬТРУЮЩАЯ СРЕДА ДЛЯ ОЧИСТКИ ЖИДКОСТИ И ГАЗА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ФИЛЬТРОВАНИЯ | 2008 |
|
RU2398628C2 |
| Сорбционно-бактерицидный материал из нетканого полимерного волокнистого материала, способ диализа жидких сред | 2023 |
|
RU2835016C2 |
| ФИЛЬТРУЮЩИЙ МАТЕРИАЛ ДЛЯ ОЧИСТКИ ВОЗДУХА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2349368C1 |
| КОМПОЗИТНЫЕ ФИЛЬТРЫ ИЗ ПОРИСТОГО БЛОКА С НАНОВОЛОКНАМИ | 2008 |
|
RU2502543C2 |



Изобретение относится к нановолокнистому фильтрующему материалу. Предложен материал, состоящий из несферических частиц гидроксида алюминия, имеющий диаметр волокон менее 50 нм, полученный при взаимодействии исходного алюминиевого компонента с водным раствором при температуре до 100°С и нанесенный непосредственно на волокнистую поверхность. Изобретение обеспечивает высокую степень очистки текучих сред от патогенных микроорганизмов. 3 н. и 57 з.п. ф-лы, 9 ил., 8 табл.
| ФИЛЬТРУЮЩИЙ ЭЛЕМЕНТ ДЛЯ МИКРО- И УЛЬТРАФИЛЬТРАЦИИ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1994 |
|
RU2079349C1 |
| US 4361486 A, 30.11.1982 | |||
| RU 2075345 C1, 20.03.1997 | |||
| US 5417889 A, 23.05.1995 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| US 6057488 А, 02.05.2000. | |||
Авторы
Даты
2007-08-20—Публикация
2002-06-21—Подача