Способ неинвазивного сбора и анализа транскутантного газа из живого организма в режиме реального времени предназначен для медицинских, физиологических или иных исследований, включая медицинскую и физиологическую экспресс-диагностику, определение динамики кожного дыхания, системных отклонений в организме, выявление маркеров заболеваний, токсических и иных поражений организма, следов воздействия лекарственных и иных веществ в организме, контактов со специфическими агентами, например анестетиками, взрывчатыми веществами и т.п. Область техники включает в себя: измерение для медицинских диагностических целей со сбором воздуха и направлением его через измерительное устройство (А61В 5/097); получение и подготовку образцов для исследования (G01N 35/00); исследование или анализ материалов с помощью электрических, электрохимических или магнитных средств (G01N 27/00); электрические измерения для определения состава газовых смесей путем исследования ионизации газов (G01N 27/62); исследование свойств частиц, определение размеров частиц и их распределения по размерам, в том числе масс-спектрометрическим методом (G01N 15/02); исследование или анализ материалов путем разделения на компоненты, разделение и ввод образцов (G01N 30/00); использование масс-спектрометра (G01N 30/72).
В основе транскутантных методов лежит положение о том, что парциальные значения концентрации газов, растворенных в крови, сохраняются в процессе неинвазивной диффузии из живого организма, и, следовательно, могут быть измерены снаружи после прохождения слоя подкожных тканей, жидкостей и кожного покрова [1]. Масс-спектральный анализ транскутантного газа становится эффективным неинвазивным экспресс-методом выявления патологий в организме. Для развития этого метода необходимо создание новых способов и устройств.
Известны аналоги изобретения, включающие входной интерфейс с входной поверхностью и входной диафрагмой в ней, через которую поступает транскутантная газовая смесь, прижимаемый в рабочем состоянии указанной входной поверхностью к участку кожи человека или животного, и систему транспортировки газовой смеси к анализатору, в качестве которого используется масс-спектрометр [2-3].
Аналоги [4-5] основаны на использовании герметичного контейнера, в котором собранную с помощью интерфейса транскутантную газовую смесь переносят в масс-спектрометр.
В способах-аналогах могут быть сохранены, в принципе, простые газы в пропорциях, близких к исходным в экстрагируемой парогазовой смеси. Однако для многих компонентов эти пропорции нарушаются из-за адсорбционно-десорбционного взаимодействия со стенками трубопровода или контейнера, наличия натеканий атмосферного воздуха, утечек на двух этапах: сбора газа из входного модуля и инжекции в масс-спектрометр. Сорбционные и иные потери примесных компонентов летучей органики, присутствующих в исходной пробе на следовом уровне миллиграмм - нанограмм на литр и ниже, принципиально препятствуют их обнаружению в газовой смеси, поступающей в масс-спектрометр. Неконтролируемое натекание примесных компонентов летучей органики из атмосферного воздуха в контейнер, в системы забора смеси и инжекции ее в масс-спектрометр, смешение натекающего газа с анализируемой газовой смесью также искажают исследование. Исследования требуют большой продолжительности, нет возможности обеспечить режим реального времени, выявить динамику кожного дыхания, произвести экспресс-обследования. Кроме того, транскутантная диффузия в устройствах-аналогах не обладает достаточной интенсивностью.
Известен способ, по которому используется входной интерфейс для сбора транскутантного газа, к интерфейсу подключены трубопроводы для доставки указанного газа в масс-спектрометр, а также резистивный нагреватель [6]. По трубопроводам доставляют неионизованную смесь газов и паров воды в масс-спектрометр, и на участке транспортировки происходит изменение структуры пробы за счет взаимодействия со стенками. Указанные недостатки аналогов частично устранены в прототипе данного изобретения [7].
Прототипом является способ неинвазивного транскутантного сбора и исследования биологической пробы - газовой смеси - в режиме реального времени. Согласно прототипу в канале транспортировки создается вакуумное разрежение вместе с камерой масс-спектрометра, и ионизация поступающей газовой смеси, прошедшей указанный канал транспортировки, производится в ионном источнике масс-спектрометра в указанной камере. Вместо трубопроводов используется прямолинейный короткий канал. Канал напрямую соединяет участок кожного покрова и указанный ионный источник. Натекания атмосферного воздуха и их смешение с анализируемой газовой смесью понижены до минимальных значений, существенно увеличено быстродействие, обеспечен режим сбора, транспортировки и получения масс-спектральных характеристик транскутантной газовой смеси в режиме реального времени.
Недостатком прототипа является отсутствие изоляции парогазовой смеси от стенок канала. Искажение структурного состава транскутантной газовой смеси в канале транспортировки происходит из-за взаимодействий частиц указанной смеси со стенками канала транспортировки, а также между собой на стенках канала и с другими частицами, имеющимися на стенках канала. Указанные взаимодействия могут приводить к потерям примесных компонентов малой концентрации, преобразованиям химического состава смеси, изменениям размеров частиц из-за синтеза или фрагментации. Искажение структурного состава транскутантной газовой смеси в канале транспортировки приводит к потере аналитической информации и снижению эффективности исследования биологической пробы с поверхности кожи в целом. Согласно прототипу используется поверхностный нагрев за счет повышения температуры входного интерфейса. С помощью нагрева ускоряют транскутантную неинвазивную диффузию газов, однако при нагреве всего интерфейса ускоряются также и потери транскутантного газа на большой поверхности кожного покрова вокруг интерфейса, что вызывает обеднение газовой смеси в области измерения. Тепловая волна от поверхностного нагревателя не проникает в глубь подкожного слоя и не инициирует диффузию из удаленных слоев.
Сущность изобретения состоит в том, что оптимизируют нагрев кожного покрова и подкожного слоя путем применения высокочастотного электрического поля и возникающих при этом токов, нагрев происходит в глубь подкожного слоя локально вблизи входной диафрагмы, производят ионизацию непосредственно вблизи входной диафрагмы и фокусируют полученный ионный поток с помощью электрического поля, тем самым улучшают условия изоляции потока пробы от стенок канала и сбора пробы в анализаторе масс-спектрометра. Указанный положительный эффект достигается тем, что с помощью установленных во входном интерфейсе электродов и контактных линий передачи, подключенных к генераторам электрических сигналов, создают электрическое поле, посредством которого производят разряд и ионизацию транскутантной газовой смеси во входном интерфейсе непосредственно в области входной диафрагмы, и осуществляют направленный дрейф полученных ионов в канале транспортировки. Конструкция входного интерфейса с входной поверхностью и входной диафрагмой с установленными в нем электродами, служащими для создания электрического поля, и каналом транспортировки ионов показана на чертеже. Конструкция состоит из следующих основных частей. Входной электрод с диафрагмой Д1 прижат к участку кожного покрова и служит анодом разрядной камеры. Постоянное положительное напряжение на аноде составляет несколько единиц вольт. Катодом является электрод К с диафрагмой. При подаче на катод высокочастотного напряжения в области входной диафрагмы в подкожном слое возникают высокочастотные токи, стимулирующие диффузию парогазовой смеси и ее поступление в разрядную камеру. Основная составляющая смеси - водяной пар. В высокочастотном поле разряда происходит его ионизация с образованием активных ионов. Нейтральные компоненты газа вместе с активными ионами распространяются вдоль оси системы в дрейфовом пространстве ДП. В диэлектрической трубке ДТ дрейфовое пространство ДП образовано набором кольцевых электродов с отверстиями на оси системы. С помощью делителя напряжения в ДП создается дрейфовое электрическое поле с напряженностью порядка 100 В/см для обеспечения совместного дрейфа активных ионов и ионов, образующихся при протонировании ЛОК. Безмасляный форнасос ФН создает во входном интерфейсе в области Д1-ДП вакуумное разрежение порядка 10 Topp. При открытом положении входного шибера Ш ионы попадают на диафрагму напуска ДН. Прошедшие через диафрагму ионы поступают в камеру, откачиваемую турбомолекулярным насосом ТМН, и далее - в основной ионизатор ИИ с ЭУ и квадрупольный масс-анализатор КвАн.
Область разряда и траектория ионов показаны кружком и стрелкой, ИС - ионный сигнал на выходе масс-анализатора.
В результате достигаются экстракция, ионизация и транспортировка ионизованной компоненты для анализа. В этом режиме накал катода ионного источника с электронным ударом масс-спектрометра отключен. При включенном накале возможен второй режим анализа транскутантной пробы: при отключении напряжений на электродах интерфейса возможна транспортировка нейтралов напрямую в ионный источник с электронным ударом, и производится динамический анализ концентрации простых газов: кислорода, двуокиси углерода и других.
Согласно формуле изобретения предлагается способ неинвазивного сбора и анализа транскутантного газа из живого организма в режиме реального времени, по которому используют входной интерфейс с входной поверхностью и входной диафрагмой в ней, имеющий вакуумированный канал транспортировки газовой смеси к анализатору, в качестве которого используется масс-спектрометр, ОТЛИЧАЮЩИЙСЯ тем, что с помощью установленных во входном интерфейсе электродов и контактных линий передачи, подключенных к генераторам электрических сигналов, создают электрическое поле, посредством которого производят разряд и ионизацию транскутантной газовой смеси во входном интерфейсе непосредственно в области входной диафрагмы, и осуществляют направленный дрейф в канале транспортировки полученных ионов в масс-анализатор.
Способ реализуют следующим образом.
Входной интерфейс с входной поверхностью и входной диафрагмой прижимают указанной входной поверхностью к участку кожи человека или животного, в канале транспортировки вместе с камерой масс-спектрометра создают вакуумное разрежение, с помощью контактных линий подают электрические сигналы на электроды, установленные во входном интерфейсе непосредственно в области входной диафрагмы и в канале транспортировки, регулируют генераторы электрических сигналов, устанавливают требуемые параметры указанных электрических сигналов, тем самым создают электрическое поле, посредством которого производят разряд и ионизацию транскутантной газовой смеси во входном интерфейсе непосредственно в области входной диафрагмы, и осуществляют направленный дрейф в канале транспортировки полученных ионов в масс-анализатор, получают поток ионов в анализаторе масс-спектрометра, производят масс-спектрометрический структурный анализ поступающего в анализатор потока ионов, осуществляют интерпретацию полученного масс-спектра и делают вывод о результатах исследования.
Рассмотрим сведения, подтверждающие возможность осуществления изобретения.
Глубинный нагрев подкожного слоя осуществляется с помощью высокочастотного тока, наведенного электрическим полем, провисающим через входную диафрагму. Применение высокочастотного тока и его эффективное тепловое воздействие, а также сопутствующее повышение скорости кровотока и диффузии газов в области нагрева хорошо известны в медицине (Токи Д′Арсонваля). Использованный в данном изобретении метод ионизации посредством электрического поля основан на следующей последовательности операций:
- вакууммирование входного интерфейса вместе с каналом транспортировки;
- создание электрического поля напряженностью до 1000 В/см в полосе частот до 10 МГц в области входной диафрагмы Д1 при подаче напряжения на катод К;
- стимулированная созданным электрическим полем диффузия, возникновение разряда, ионизация с образованием активных ионов;
- ионизация в разряде и в канале транспортировки, поступление ионов в анализатор;
- запись, анализ и интерпретация масс-спектра.
Транскутантная газовая смесь содержит значительное количество паров воды. Во входном интерфейсе в присутствии транскутантного пара воды в электрическом поле получается поток активных ионов с высоким содержанием Н3О+. Активные ионы взаимодействуют с транскутантным газом (в котором содержатся анализируемые примеси ЛОК на следовом уровне). Ионы Н3O+ с большой вероятностью производят недиссоциативную реакцию ионизации (передачу протона) при столкновениях с атомами, имеющими сродство к протону выше, чем у молекул Н2О (166.5 ккал/моль). Поскольку основные атомы и молекулы компонентов воздуха (Не, Н2, Ne, Ar, О2, Kr, N2, Xe, СО2, СО) имеют более низкие значения сродства к протону, они не ионизуются передачей протона и не дают ионного фона. Летучие органические молекулярные компоненты обычно имеют более высокое сродство к протону, чем молекула Н2О, поэтому они в реакциях взаимодействия с ионом Н3О+ приобретают протон с высокой вероятностью. Поскольку метод ионизации передачей протона является мягким, недиссоциативным, каждому нейтралу примеси соответствует только один образующийся ион.
В канале транспортировки обеспечивается дрейфовое движение полученных ионов, а также продолжение реакции ионизации передачей протона. Ионы ускоряются в электрическом поле (порядка 102 В/см) при давлении порядка 1 Торр. При использовании в качестве масс-анализатора магнитного сектора или квадруполя достигается разрешение порядка 1000-5000 в диапазоне масс 1-400 Да с чувствительностью анализа порядка ppm-ppb-ppt. Приведенные параметры характеризуют данный способ как высокоэффективный способ медицинской экспресс-диагностики.
Масс-спектральный состав транскутантной газовой смеси содержит большой объем медико-биологической информации, на основе которой могут быть сделаны диагностические заключения по широкому комплексу направлений исследования [8-9]. Информация содержится в значениях и динамике парциальной концентрации простых газов: кислород, оксид и диоксид углерода, азот, а также уровня содержания изотопа углерода С13. Критическим параметром в масс-спектрометрии является способ ионизации. Традиционное применение ионизации электронным ударом (МС ЭУ) в масс-спектрометрах для анализа следовых количеств газовых примесей существенно ограничено, поскольку трудно избежать фрагментации молекул, и интерпретация спектров смесей зачастую невозможна. МС ЭУ позволяет измерять относительную концентрацию обычных, беспримесных составляющих газовых смесей. Анализ примесей летучих органических компонентов (ЛОК) в воздухе затруднен, поскольку компоненты воздуха также ионизуются и дают высокий уровень фона. Наиболее информативным является измеряемый уровень содержания и динамика этого уровня примесей летучих органических компонентов на следовом уровне, имеют большой потенциал для клинической диагностики и терапевтического мониторинга, особенно для быстрого скрининга больших групп пациентов с целью выявления факторов риска заболеваний.
Анализ ЛОК в выдыхаемых и транскутантных газах применяется для научных исследований и диагностики заболеваний, а также эффектов применения лекарств. Эндогенные ЛОК (более чем 3000 регистрируемых субстанций) производятся в организме человека метаболическими процессами и бактериями. В выдыхаемом и транскутантном газах измеряют динамику метанола, этанола, изопрена, ацетона, кетона, изопропанола и других эндогенных ЛОК на следовом уровне.
Рассмотрим конкретный пример осуществления заявленного способа для определения концентрации ЛОК, например ацетона, в транскутантном газе пациента (все ссылки ниже даны на чертеже описания заявки).
Начиная измерения по заявляемому способу, подают постоянное положительное напряжение порядка несколько единиц вольт на входной электрод, изготовленный, например, из нержавеющей стали, с диафрагмой Д1 диаметром порядка 50 мкм в нем, и прижимают указанный электрод к участку кожного покрова (например, к внутренней поверхности локтевого сгиба) человека или животного. С помощью форнасоса ФН создают в области Д1-ДП (протяженностью порядка 3-10 см), ограниченную диэлектрической трубкой ДТ (диаметром порядка 1-2 см), вакуумное разрежение порядка 10 Top, откачивают турбомолекулярным насосом ТМН камеру масс-анализатора КвАн, например квадрупольного, до давления порядка 10-5 Topp, открывают входной шибер Ш. Подают на катод К отрицательное импульсное напряжение длительностью 1-10 мкс амплитудой 1-5 кВ, а на делитель напряжения в ДП, соединенный с цепочкой электродов (например, 3-10 штук), подают постоянное напряжение 300-500 В. Как вариант подают указанное импульсное напряжение положительной полярности на указанный входной электрод. Получают локализованный импульсный разряд между указанным входным электродом и катодом К, в котором ионизуют преимущественно молекулы воды, получают протонированные первичные активные ионы, а в дрейфовом пространстве ДП получают ионы примеси ЛОК, например ацетона, которым первичные активные ионы передают протоны (область разряда и траектория ионов показаны кружком и стрелкой). Полученные в дрейфовом пространстве ДП ионы пропускают через диафрагму напуска ДН в камеру масс-анализатора КвАн. Получают поток ионов в анализаторе масс-спектрометра, производят масс-спектрометрический структурный анализ поступающего в анализатор потока ионов, получают ионный сигнал ИС на выходе масс-анализатора, записывают масс-спектр, осуществляют интерпретацию полученного масс-спектра и делают вывод о результатах исследования. Например, сравнивают измеренный уровень содержания примеси ацетона в транскутантном газе пациента с уровнем, который измерен для контрольной группы здоровых людей, и делают медицинское заключение. Подобную процедуру можно проделать и с иными компонентами газов крови, например с глюкозой.
Предлагаемый способ является неинвазивным и высокоэффективным для анализа практически всех газовых компонентов, растворенных в крови, лимфе и находящихся в подкожном слое.
Список цитированной литературы
1. S.Dawson, C.Cave, I.Pavord, and J.F.Potter. Transcutaneous monitoring of blood gases. Respiratory Medicine, 1998, 92, 584-587.
2. Parker D., Delpy, Reynolds E.O. Transcutaneous bloof gas measurements by mass spectrometry. Acta Anaesthesiol Scand Suppl. 1978, 68&131-6.
3. Baumgardner J.D., Quinn J.A., Neufeld G.R. Micropore membrane inlet mass spectrometer probes suitable for measurement of tissue surface gas tensions. J Mass Spectrom 30: 563-571, 1995.
4. Patent US 2004147885, publ. 2004-07-29.
5. Левшанков А.И., Пушкина М.А., Слуцкая М.Е., Уваров Б.С. / Определение локального газообмена поверхности тела методом масс-спектрометрии. // Медицинская техника. М., Медицина, №1, 1983. С.21-26.
6. Patent US 4439679, publ. 1984-03-27.
7. Цыбин О.Ю., Цыбина М.Л., Маркелов И.М. / Способ исследования биологической пробы с поверхности кожи. А.С. №1772745, рег. 01.07.1992 г.
8. F.Di Francesco, R.Fuoco, M.G.Trivella, A.Ceccarini. Breath analysis: trends in techniques and clinical applications. Microchemical Journal, 79 (2005), 405-410.
9. Левшанков А.И., Озеров Л.Н., Павленко В.А. и др. / Медицинская техника, 1977, №1, С.19-22.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГАЗОВЫЙ МЕДИЦИНСКИЙ МАСС-СПЕКТРОМЕТР ДЛЯ ДИАГНОСТИКИ ЖИВОГО ОРГАНИЗМА В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ | 2010 |
|
RU2436506C1 |
| Способ предварительной сепарации потока заряженных частиц в источнике ионов с ионизацией при атмосферном давлении | 2019 |
|
RU2732075C1 |
| СПОСОБ ТРАНСПОРТИРОВКИ ИОННЫХ ПОТОКОВ В ИСТОЧНИКАХ ИОНОВ С ИОНИЗАЦИЕЙ ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ ДЛЯ ХРОМАТО-МАСС-СПЕКТРОМЕТРОВ ГХ-МС | 2014 |
|
RU2584272C2 |
| УСТРОЙСТВО НЕПРЕРЫВНОГО СТАБИЛЬНОГО ЭЛЕКТРОРАСПЫЛЕНИЯ РАСТВОРОВ В ИСТОЧНИКЕ ИОНОВ ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ | 2014 |
|
RU2587679C2 |
| СПОСОБ ПРЕОБРАЗОВАНИЯ НЕПРЕРЫВНОГО ПОТОКА ИОНОВ В ИСТОЧНИКАХ С ИОНИЗАЦИЕЙ ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ В ИМПУЛЬСНЫЙ | 2018 |
|
RU2744235C2 |
| Способ диагностики электрических полей в электронных приборах | 1975 |
|
SU548126A1 |
| УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ И АНАЛИЗА ИОНОВ АНАЛИТА | 2007 |
|
RU2346354C1 |
| СПОСОБ АНАЛИЗА ПРИМЕСЕЙ В ЖИДКОСТЯХ ИЛИ ГАЗАХ ПРИ ИХ МИКРОКАНАЛЬНОМ ИСТЕЧЕНИИ В ВАКУУМ ПОД ВОЗДЕЙСТВИЕМ СВЕРХЗВУКОВОГО ГАЗОВОГО ПОТОКА, СОДЕРЖАЩЕГО ИОНЫ И МЕТАСТАБИЛЬНО ВОЗБУЖДЁННЫЕ АТОМЫ, С ФОРМИРОВАНИЕМ И ТРАНСПОРТИРОВКОЙ АНАЛИЗИРУЕМЫХ ИОНОВ В РАДИОЧАСТОТНОЙ ЛИНЕЙНОЙ ЛОВУШКЕ, СОПРЯЖЁННОЙ С МАСС-АНАЛИЗАТОРОМ | 2016 |
|
RU2640393C2 |
| СПОСОБ ПОЛУЧЕНИЯ И АНАЛИЗА ИОНОВ АНАЛИТА | 2007 |
|
RU2346249C1 |
| ИСТОЧНИК ИОНОВ С ФОТОИОНИЗАЦИЕЙ ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ | 2014 |
|
RU2572358C1 |
Изобретение относится к медицине и может быть использовано для медицинских, физиологических, фармацевтических, криминалистических и других исследований. Согласно способу используют входной интерфейс с входной поверхностью и входной диафрагмой в ней, прижатый к участку поверхности кожи человека или животного, имеющий вакуумированный канал транспортировки газовой смеси к анализатору, в качестве которого используется масс-спектрометр, с помощью электрического поля во входном интерфейсе производят ионизацию газовой смеси, осуществляют дрейф ионов в канале транспортировки, производят масс-спектрометрический структурный анализ поступающего в анализатор потока частиц, осуществляют интерпретацию полученного масс-спектра и делают вывод о результатах исследования. Технический результат состоит в снижении искажений состава транскутантной газовой смеси для анализа. 1 ил.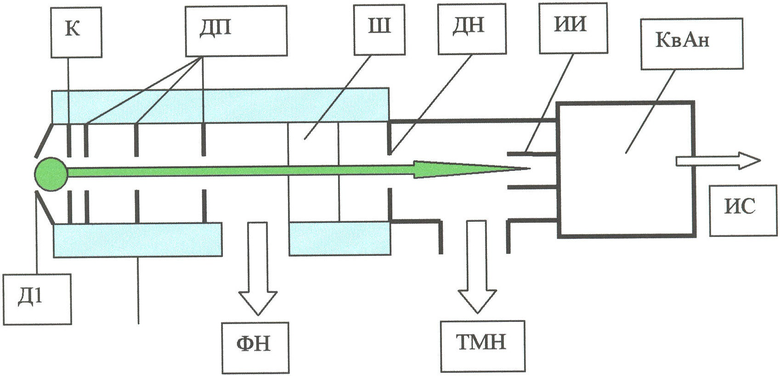
Способ неинвазивного сбора и анализа транскутантного газа из живого организма в режиме реального времени, согласно которому используют входной интерфейс с входной поверхностью и входной диафрагмой в ней, имеющий вакуумированный канал транспортировки газовой смеси к анализатору, в качестве которого используется масс-спектрометр, отличающийся тем, что с помощью установленных во входном интерфейсе электродов и контактных линий передачи, подключенных к генераторам электрических сигналов, создают электрическое поле, посредством которого производят разряд и ионизацию транскутантной газовой смеси во входном интерфейсе непосредственно в области входной диафрагмы, и осуществляют направленный дрейф в канале транспортировки полученных ионов в масс-ионизатор.
| Способ исследования биологической пробы с поверхности кожи | 1990 |
|
SU1772745A1 |
| US 4439679 A, 27.03.1984 | |||
| US 2004147885 A1, 29.07.2004 | |||
| F.Dr FRANCESCO et al | |||
| Breath analysis: trends in techniques and clinical applications, Microchemical Journal, 79 (2005), 405-410. | |||
Авторы
Даты
2008-07-10—Публикация
2005-12-26—Подача