Изобретение относится к медицине, а именно к хирургии, и может быть использовано для хирургического лечения местнораспространенного рака с обширной опухолевой инвазией нижней полой вены и ее висцеральных ветвей.
Злокачественные новообразования органов забрюшинного пространства характеризуются весьма низкой резектабельностью - порядка 60.4%, что обусловлено высокой частотой местного распространения этих опухолей. Радикальные операции при местнораспространенном раке органов забрюшинного пространства с инвазией магистральных вен выполняют крайне редко и лишь в единичных клиниках, что обусловлено сложностью оперативной техники и анестезиолого-реанимационного обеспечения.
Ограничения в операции во многом обусловлены отсутствием эффективных технологий протезирования системной и локальной гемодинамики, позволяющих обеспечить адекватную компенсацию магистрального кровообращения, профилактику реперфузионного синдрома, тромботических и других осложнений на этапе резекции опухоли и реконструкции магистральных сосудов.
Эти обстоятельства обусловливают актуальность разработки эффективных и доступных хирургических технологий временного шунтирования магистрального кровообращения при обширной резекции нижней полой вены и ее висцеральных ветвей.
Заявителями обнаружен единственный источник информации, раскрывающий временное шунтирование магистрального кровообращения при обширной резекции нижней полой вены и ее висцеральных ветвей, при этом в качестве ближайшего аналога взят способ временного сосудистого кардиопульмонального байпаса при радикальной нефрэктомии с резекцией нижней полой вены в связи с опухолевой инвазией (Kapasi A., Mullen J.C., Bentley M.J., Moore R.B., Todd G.T. Resection of renal cell carcinomas with inferior vena caval extension using deep hypothermic circulatory arrest. Can. J. Cardiol. 2001, Nov.; 17(11):1183-8), который осуществляют следующим образом: выделяют пораженный участок нижней полой вены, налаживают работу аппарата искусственного кровообращения, именуемую кардиопульмональным байпасом.
Более подробно способ описан в «Руководстве по сердечно-сосудистой хирургии» под редакцией В.И.Бураковского и Л.А.Бокерия, Москва, «Медицина», 1989 г.
Способ предусматривает подключение аппарата искусственного кровообращения (АИК) к магистральным сосудам. Сначала канюлируют аорту. Эту канюлю подключают к артериальной магистрали, эвакуируют воздух. Затем канюлируют верхнюю и нижнюю полые вены через ушко правого предсердия одной или двумя канюлями и подсоединяют венозную магистраль, также стараясь не допустить попадания в нее воздуха. Отдельный резервуар обычно используют для сбора крови из полости сердца и перикарда. Эта кровь фильтруется через фильтры с диаметром пор 15 мк. Фильтрация внутрисердечного возврата важна для исключения попадания материальных частиц в аппарат искусственного кровообращения (АИК). Оксигенатор располагают на 50 см ниже сердца оперируемого. Перфузию проводят под умеренной гипотермией (26-30°С) и гемодилюцией (гематокрит 25-30%, гемоглобин не ниже 80 г/л). Операцию проводят в условиях кардиоплегии и остановки сердца, при этом гемодинамику контролируют работой системы кардиопульмонального байпаса.
Недостатки:
а) Технология использования способа предполагает остановку и последующее восстановление сердечной деятельности, что влечет за собой высокий риск фатальных осложнений кардиопульмонального байпаса: анемия, тяжелые нарушения сердечного ритма, острый инфаркт миокарда и возможность летального исхода на этом этапе операции.
б) Способ предусматривает проведение системной гепаринизации, что существенно увеличивает объем интраоперационной кровопотери, требует применения антидотов гепарина.
в) Технология в связи с выраженной потерей клеток тромбоцитарного звена на полихлорвиниловых элементах системы кардиопульмонального байпаса и аппарата искуствекнного кровообращения (АИК) приводит к значительному возрастанию риска развития неконтролируемого диссименированного внутрисосудистого свертывания крови (ДВС-синдрома), особенно при длительном функционировании системы, которая в ряде случаев служит причиной летального исхода.
г) Использование способа сопряжено с разрушением значительной части эритроцитов элементами принудительной подачи крови байпаса, выраженность которого прямо коррелирует с продолжительностью осуществления кардиопульмонального байпаса, что в значительной части случаев приводит к острой почечной недостаточности в послеоперационном периоде.
д) Способ предполагает выполнение стернотомии, перикардиотомии, что значительно увеличивает травматичность операции и повышает частоту послеоперационных осложнений.
е) Технология способа в большинстве случаев предполагает применение гипотермии, которая значительно увеличивает риск операционного вмешательства за счет выраженного патологического влияния на систему гемостаза больного.
ж) Способ предусматривает необходимость применения фармакологической и холодовой кардиоплегии и использование многочисленных методов защиты миокарда, что повышает риск манифестации тяжелых нарушений сердечного ритма в послеоперационном периоде.
з) Технология осуществления данного сосудистого байпаса предусматривает использование дорогостоящей аппаратуры, большого числа одноразовых расходных материалов, что существенно увеличивает себестоимость операции.
Задача
Разработать способ временного сосудистого шунтирования, обеспечивающий адекватное временное протезирование магистрального кровообращения при резекции нижней полой вены и ее ветвей, различных вариантов мультиваскулярных поражений, исключающий необходимость применения искусственного кровообращения и существенно уменьшить общий риск специфических осложнений.
Сущностью изобретения является то, что правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, нижнюю полую вену - непосредственно над ее бифуркацией в зависимости от особенностей опухолевого поражения, пораженные опухолевым процессом почечные вены канюлируют проксимальнее их инвазии, при этом канюли почечных вен соединяют с системой нижнекавально-правопредсердного обхода, или устанавливают отдельно в нижнюю полую вену в области расположения канюли системы нижнекавально-правопредсердного обхода.
По отношению к ближайшему аналогу заявляемый способ имеет следующий технический результат. Временное шунтирование осуществляют в условиях сохраненной сердечной деятельности, нормотермии и без использования аппарата для принудительной подачи крови. Применение технологий временного сосудистого байпаса магистрального кровотока позволяет во всех случаях добиться необходимого лимита времени для резекции местнораспространенных опухолей органов забрюшинного пространства в сочетании с обширной опухолевой инвазией сосудов и последующей реконструкцией магистральных сосудов. Применение технологий временного сосудистого байпаса позволяет избежать случаев венозного тромбоза, а также тяжелой печеночной и почечной недостаточности, функциональных нарушений деятельности кишечника. Предлагаемая технология временного венозного байпаса при резекции магистральных вен отличается высокой эффективностью и воспроизводимостью.
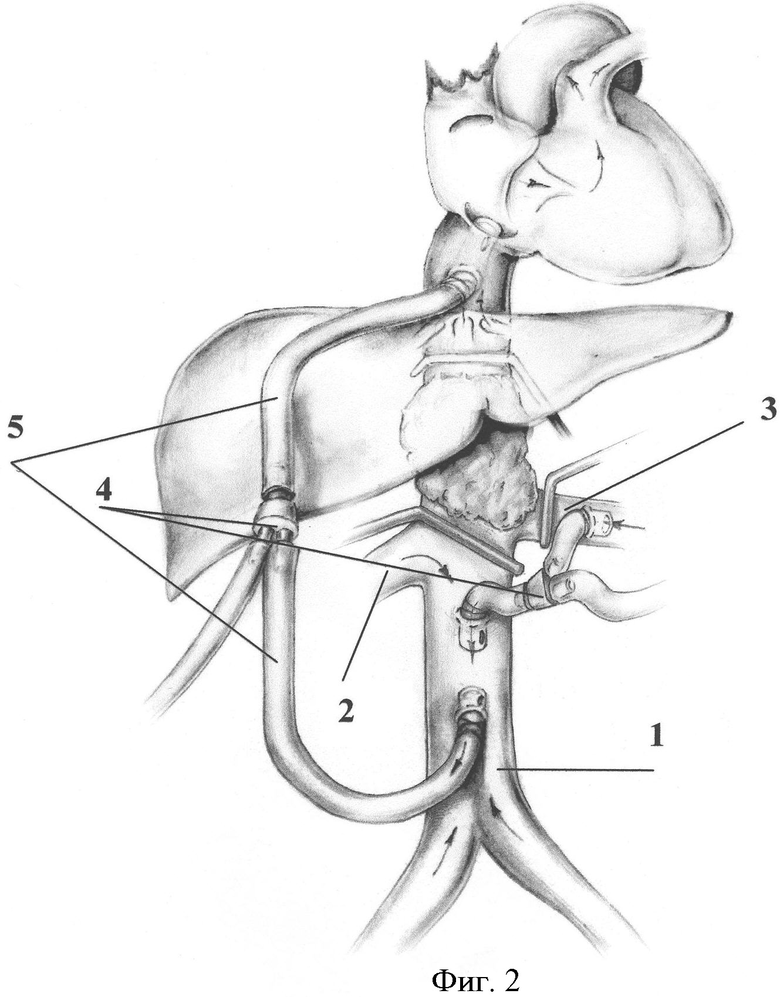
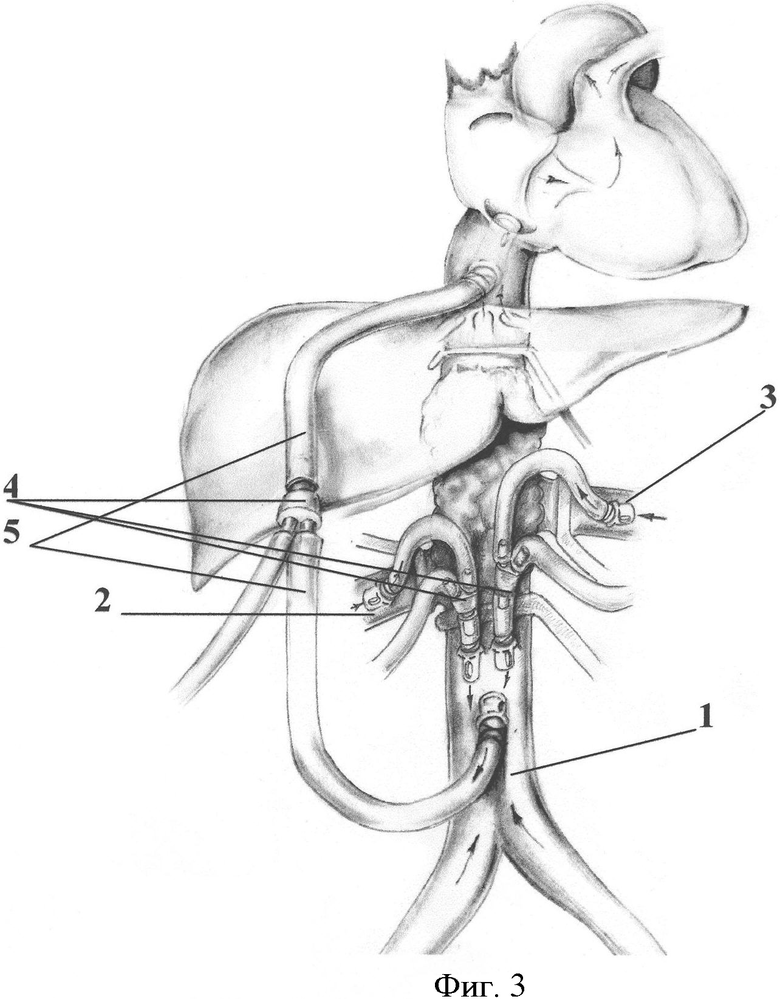
Способ поясняется чертежами 1, 2, 3, где 1 - нижняя полая вена, 2 - правая почечная вена, 3 - левая почечная вена, 4 - тройник, 5 - венозная канюля.
Способ осуществляют следующим образом.
Возможны три основных случая поражения полых вен и их висцеральных ветвей. Принцип осуществления временного шунтирования при этом общий. После выделения магистральных вен стволы одной или обеих почечных вен и инфраренальную часть нижней полой вены берут на турникеты. Мобилизуют кавальные ворота печени. Над ними в сагиттальной плоскости рассекают диафрагму по сухожильному центру и частично перикард. Выделяют супрапеченочный и интраперикардиальный сегменты нижней полой вены. На переднюю стенку интраперикардиальной части нижней полой вены, нижнюю полую вену (п.1) непосредственно над ее бифуркацией, одну или обе почечные вены (п.2, п.3) проксимальнее их опухолевого поражения накладывают кисетные швы. В условиях временного отжатия сосудов последовательно в них устанавливают силиконовые канюли (п.5) с антитромбогенным покрытием, которые фиксируют к стенкам сосудов кисетами. Канюли соединяют между собой посредством тройников (п.4) и подключают к системе гепаринизации обхода. Таким образом формируют временный нижнекавально-ренально-правопредсердный байпас, в условиях которого выполняют все последующие этапы резекции опухоли вместе с магистральными сосудами и их реконструкции. По окончании реконструктивного сосудистого этапа венозные канюли снимают в условиях бокового отжатия, дефекты в стенках вен устраняют непрерывным швом. В ситуациях, когда вовлечены обе почечные вены в опухолевый процесс, используют нижнекавально-правопредсердный и нижнекавально-ренальные с двух сторон обходы.
Заявляемый способ временного сосудистого байпаса при резекции магистальных вен в связи с их опухолевой инвазией апробирован у 20 больных с местнораспространенным раком почки, надпочечника, внеорганных забрюшинных опухолях. Осложнений в связи с применением заявляемого способа, а также случаев венозного тромбоза не отмечено. Почечной недостаточности в послеоперационном периоде не было, выявлена у 2 больных умеренная транзиторная уремия (10,0%). Общая частота послеоперационных осложнений составила 10,0%. Госпитальной летальности не было.
Возможность практического использования заявляемого способа иллюстрируется примером его выполнения в клинической практике.
Пример 1. Больной Л., 45 лет, поступил в клинику с диагнозом: местнораспространенный рак правой почки Т3вN0М0 3 стадия, 2 кл. группа с инвазией нижней полой вены и левой почечной вены. По данным инструментального обследования данных за наличие отдаленных метастазов не получено. Выполнена операция: Расширенная радикальная нефроадреналэктомия справа, резекция нижней полой вены и левой почечной вены в условиях нижнекавально-правопредсердного рено-кавального обхода, протезирование нижней полой вены FLL-кондуитом, ренально-кавальное протезирование протезом из политетрофторэтилена (ПТФЭ), дренирование забрюшинного пространства, брюшной полости и полости перикарда. Способ отображен на фиг.1, где выполнено выделение магистральных вен, стволы левой почечной вены и инфраренальную часть нижней полой вены берут на турникеты. Мобилизованы кавальные ворота печени. Над ними в сагиттальной плоскости рассечена диафрагма по сухожильному центру и частично перикард. Выделены супрапеченочный и интраперикардиальный сегменты нижней полой вены. На переднюю стенку интраперикардиальной части нижней полой вены, нижнюю полую вену (п.1) непосредственно над ее бифуркацией, левую почечную вену (п.3) проксимальнее их опухолевого поражения накложены кисетные швы. В условиях временного отжатия сосудов последовательно в них устанавлены силиконовые канюли (п.5) с антитромбогенным покрытием, которые фиксированы к стенкам сосудов кисетами. Канюли соединнены между собой посредством тройников (п.4) и подключены к системе гепаринизации обхода. Таким образом сформирован временный нижнекавально-ренально-правопредсердный байпас, в условиях которого выполннены все последующие этапы резекции опухоли вместе с магистральными сосудами и их реконструкции. По окончании реконструктивного сосудистого этапа венозные канюли сняты в условиях бокового отжатия, дефекты в стенках вен устранены непрерывным швом.
Послеоперационный период протекал без осложнений. Больной выписан из клиники в удовлетворительном состоянии на 16-е сутки после операции. После операции больной неоднократно обследован. Через 3 года после операции состояние удовлетворительное, данных за рецидив заболевания не выявлено, проходимость нижней полой вены и правой почечной вены удовлетворительная.
Пример 2. Больная С., 58 лет поступила в клинику с диагнозом: фибросаркома забрюшинного пространства с поражением нижней полой вены и вовлечением обоих почечных вен. По данным проведенного обследования данных за наличие отдаленных метастазов не получено. Выполнена операция: Удаление забрюшинной опухоли единым блоком с сегментом нижней полой вены, резекцией обоих почечных вен в условиях временного нижнекавально-правопредсердного и биренально-нижнекавального обхода, протезирования нижней полой вены и левой почечной вены PTFE-протезами, имплантацией правой почечной вены в PTFE-кондуит нижней полой вены, дренирование брюшной полости и полости перикарда. Способ отображен на фиг.3, где выделены магистральные вены, стволы обеих почечных вен и инфраренальная часть нижней полой вены взяты на турникеты. Мобилизованы кавальные ворота печени. Над ними в сагиттальной плоскости рассечена диафрагма по сухожильному центру и частично перикард. Выделены супрапеченочный и интраперикардиальный сегменты нижней полой вены. На переднюю стенку интраперикардиальной части нижней полой вены, нижнюю полую вену (п.1) непосредственно над ее бифуркацией, обе почечные вены (п.2, п.3) проксимальнее их опухолевого поражения накложены кисетные швы. В условиях временного отжатия сосудов последовательно в них устанавливают силиконовые канюли (п.5) с антитромбогенным покрытием, которые фиксируют к стенкам сосудов кисетами. Канюли соединяют между собой посредством тройников (п.4) и подключают к системе гепаринизации обхода. Таким образом формируют временный кава-правопредсердный и биренально-нижнекавальный обход, в условиях которого выполнены все последующие этапы резекции опухоли вместе с магистральными сосудами и их реконструкции. По окончании реконструктивного сосудистого этапа венозные канюли сняты в условиях бокового отжатия, дефекты в стенках вен устранены непрерывным швом.
Послеоперационный период протекал без осложнений. Больная выписана на 21-е сутки после операции. После операции больная неоднократно обследована. Через год после операции состояние удовлетворительное, данных за рецидив заболевания не получено. Проходимость нижней полой вены и почечных вен удовлетворительная.
Пример 3. Больной К., 57 лет, поступил в клинику с диагнозом: местнораспространенный рак правого надпочечника ТЗвN0М0 3 стадия, 2 кл. группа с инвазией нижней полой вены и левой почечной вены. По данным инструментального обследования данных за наличие отдаленных метастазов не получено. Выполнена операция: Расширенная радикальная нефроадреналэктомия справа, резекция нижней полой вены и левой почечной вены в условиях нижнекавально-правопредсердного и биренально-нижнекавального обхода, протезирование нижней полой вены FLL-кондуитом, ренально-кавальное протезирование протезом из политетрофторэтилена (ПТФЭ), дренирование забрюшинного пространства, брюшной полости и полости перикарда. Способ отображен на фиг.2, где выделены магистральные вены левая почечная вена и инфраренальная часть нижней полой вены взяты на турникеты. Мобилизованы кавальные ворота печени. Над ними в сагиттальной плоскости рассечена диафрагма по сухожильному центру и частично перикард. Выделены супрапеченочный и интраперикардиальный сегменты нижней полой вены. На переднюю стенку интраперикардиальной части нижней полой вены, нижнюю полую вену (п.1) непосредственно над ее бифуркацией, левую почечную вену (п.3) проксимальнее их опухолевого поражения накложены кисетные швы. В условиях временного отжатия сосудов последовательно в них установлены силиконовые канюли (п.5) с антитромбогенным покрытием, которые фиксированы к стенкам сосудов кисетами. Канюли соединены между собой посредством тройников (п.4) и подключены к системе гепаринизации обхода. Таким образом, сформирован временный нижнекавально-правопредсердный и ренально-нижнекавальный обход, в условиях которого выполнены все последующие этапы резекции опухоли вместе с магистральными сосудами и их реконструкция. По окончании реконструктивного сосудистого этапа венозные канюли сняты в условиях бокового отжатия, дефекты в стенках вен устранены непрерывным швом. Послеоперационный период протекал без осложнений. Больной выписан из клиники в удовлетворительном состоянии на 16-е сутки после операции. После операции больной неоднократно обследован. Через 3 года после операции состояние удовлетворительное, данных за рецидив заболевания не выявлено, проходимость нижней полой вены и правой полой вены удовлетворительная.
Таким образом, применение заявляемого способа позволяет выполнить радикальную операцию у больных с местнораспространенным раком органов забрюшинного пространства с обширной инвазией магистральных вен с распространением опухоли на почечные вены, осуществить адекватную и наиболее физиологичную реконструкцию резецированных сосудов, существенно снизить частоту послеоперационных осложнений, связанных с сосудистым этапом вмешательства.
Социально-экономическое значение. Разработанный способ позволяет значительно повысить операбельность и отдаленную выживаемость больных местнораспространенным раком органов забрюшинного пространства, улучшить непосредственные и отдаленные результаты радикального хирургического лечения опухолей с обширной инвазией магистральных вен.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВРЕМЕННОГО ШУНТИРОВАНИЯ МАГИСТРАЛЬНОГО КРОВООБРАЩЕНИЯ ПРИ ОПУХОЛЕВОМ ПОРАЖЕНИИ ЗАБРЮШИННОГО ПРОСТРАНСТВА И ВОВЛЕЧЕНИЕМ НИЖНЕЙ ПОЛОЙ ВЕНЫ | 2006 |
|
RU2317024C1 |
| СПОСОБ ВРЕМЕННОГО СОСУДИСТОГО ШУНТИРОВАНИЯ ПРИ ТРАНСПЛАНТАЦИИ И АУТОТРАНСПЛАНТАЦИИ ПЕЧЕНИ | 2006 |
|
RU2325120C1 |
| СПОСОБ ВРЕМЕННОГО СОСУДИСТОГО ШУНТИРОВАНИЯ ПРИ ТРАНСПЛАНТАЦИИ И АУТОТРАНСПЛАНТАЦИИ ПЕЧЕНИ | 2006 |
|
RU2317010C1 |
| СПОСОБ ВРЕМЕННОГО СОСУДИСТОГО БАЙПАСА ПРИ РЕЗЕКЦИИ МАГИСТРАЛЬНЫХ ВЕН МЕЗЕНТЕРИКО-ПОРТАЛЬНОЙ СИСТЕМЫ | 2006 |
|
RU2321358C1 |
| СПОСОБ ВРЕМЕННОГО СОСУДИСТОГО БАЙПАСА ПРИ РЕЗЕКЦИИ МАГИСТРАЛЬНЫХ ВЕН МЕЗЕНТЕРИКО-ПОРТАЛЬНОЙ СИСТЕМЫ | 2006 |
|
RU2329770C1 |
| СПОСОБ ВРЕМЕННОГО СОСУДИСТОГО БАЙПАСА ПРИ РЕЗЕКЦИИ МАГИСТРАЛЬНЫХ ВЕН МЕЗЕНТЕРИКО-ПОРТАЛЬНОЙ СИСТЕМЫ | 2006 |
|
RU2329771C1 |
| СПОСОБ ВРЕМЕННОГО АРТЕРИАЛЬНОГО СОСУДИСТОГО БАЙПАСА ПРИ РЕЗЕКЦИИ ВИСЦЕРАЛЬНЫХ ВЕТВЕЙ БРЮШНОЙ АОРТЫ | 2006 |
|
RU2321357C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОПУХОЛЕВОЙ ИНВАЗИЕЙ ПЕРЕДНЕЙ СТЕНКИ УСТЬЯ ВОРОТНОЙ ВЕНЫ | 2006 |
|
RU2317019C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОПУХОЛЕВОЙ ИНВАЗИЕЙ ПЕРЕДНЕЙ СТЕНКИ УСТЬЯ ВОРОТНОЙ ВЕНЫ | 2006 |
|
RU2311874C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОБШИРНОЙ ОПУХОЛЕВОЙ ИНВАЗИЕЙ МАГИСТРАЛЬНЫХ ВЕН МЕЗЕНТЕРИКО-ПОРТАЛЬНОЙ СИСТЕМЫ | 2006 |
|
RU2312608C1 |
Изобретение относится к медицине, а именно к хирургии. Выполняют канюляцию правого предсердия и нижней полой вены. При этом правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, нижнюю полую вену - непосредственно над ее бифуркацией. Вовлеченные в опухолевый процесс почечные вены канюлируют проксимальнее их инвазии, при этом канюли почечных вен соединяют с системой нижнекавально-правопредсердного обхода, или устанавливают отдельно в нижнюю полую вену в области расположения канюли системы нижнекавально-правопредсердного обхода. Способ позволяет обеспечить постоянную адекватную работу байпаса на этапе сосудистой реконструкции, дает возможность контролировать проходимость и проводить локальную гепаринизацию системы байпаса. 3 ил.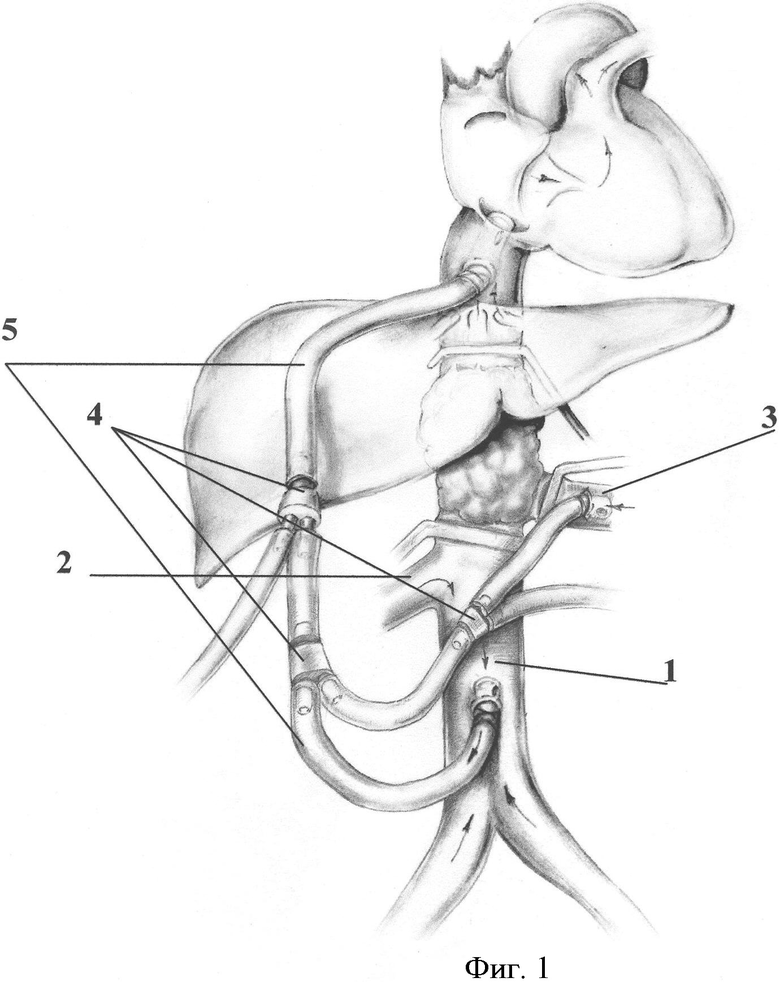
Способ временного шунтирования магистрального кровообращения при обширной резекции нижней полой вены и ее висцеральных ветвей, включающий канюляцию правого предсердия и нижней полой вены, отличающийся тем, что правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, нижнюю полую вену - непосредственно над ее бифуркацией, вовлеченные в опухолевый процесс почечные вены канюлируют проксимальнее их инвазии, при этом канюли почечных вен соединяют с системой нижнекавально-правопредсердного обхода, или устанавливают отдельно в нижнюю полую вену в области расположения канюли системы нижнекавально-правопредсердного обхода.
| Kapasi A., Mullen J.C., Bentley M.J., Moore R.B., Todd G.T | |||
| Resection of renal cell carcinomas with inferior vena caval extension using deep hypothermic circulatory arrest | |||
| Can | |||
| J.Cardiol | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОРГАНОВ МАЛОГО ТАЗА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2154422C1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСТРОЙ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ ПРИ ОБШИРНОЙ РЕЗЕКЦИИ ПЕЧЕНИ | 2002 |
|
RU2222270C2 |
| АРАКЕЛЯН B.C | |||
| и др | |||
| Метод обходного временного шунтирования в хирургии | |||
Авторы
Даты
2008-07-27—Публикация
2006-10-26—Подача