Изобретение относится к медицине и предназначено для диагностики состояния тканей на этапах децеллюляризации и целлюляризации тканевых конструкций в биотехнологии.
В настоящее время основное внимание тканевых инженеров в области кардиохирургии фокусируется на создании функционально идентичной копии здорового клапансодержащего графта. Это относительно новая техника в области тканевого инжиниринга и, может быть скоро, она сможет преодолеть недостатки, связанные с клиническим использованием механических и биологических ксеноклапанов [1, 2, 3, 4]. В настоящее время биотехнологический подход для создания трансплантируемых клапанов заключается в применении ацеллюлярного, натурального биоматрикса. Например, фрагмент клапансодержащего графта может быть обработан для удаления их клеточных составляющих, что уменьшает его иммуногенность и делает возможным повторное заселение клетками реципиента. Этот подход требует техники децеллюляризации, которая заключается в эллиминации клеточных элементов из структуры аорты. Однако децеллюляризация может неблагоприятно влиять на механические свойства биоматрикса и восстановление ткани in vivo [5]. В отличие от полимерных кондуитов. ацеллюлярный биоматрикс сохраняет лиганды и компоненты экстрацеллюлярного матрикса, что более физиологично для процессов восстановления функции клапана. В связи с этим возникает необходимость контроля за состоянием аллографта на этапах децеллюляризации и последующего засевания аутологичными клетками клапансодержащего графта аорты. Системы оценки качества биотехнологических этапов приготовления аутографтов на сегодняшний день нет. Для оценки графта при отработке протокола используется биопсия с последующими исследованиями образцов различными гистологическими, гистохимическими методами, флуоресцентными зондами, включая измерение механического напряжения. Перечисленные методы инвазивны для графта, их проведение требует множества дополнительных и часто длительных процедур, что делает эти методы малопривлекательными для реальной практики. Более того использование всех вышеперечисленных технологий возможно только на этапе подготовки протокола биотехнологии.
Известно, что для определения жизнеспособности тканей может быть использована лазерно-индуцированная флюоресценция (ЛИФ) [6].
Целью изобретения является разработка способа объективной оценки состояния графта на этапах децеллюляризации-целлюляризации, методом лазерноиндуцированной флюоресценции.
Указанная цель достигается путем определения спектров вторичной флюоресценции тканей под воздействием ультрафиолетового импульсного лазерного облучения.
Способ осуществляется следующим образом.
Забор фрагментов клапансодержащих графтов аорты человека производился в областном бюро судебно-медицинской экспертизы города Новосибирска. Проводилась стандартная диссекция аорты вместе с аортальным клапаном согласно протоколам европейского банка тканей. Давность наступления смерти составляла 12-24 часа. Полученные клапансодержащие графты аорты транспортировались в холодном физиологическом растворе и далее велись следующим образом.
Пять фрагментов клапансодержащих графтов аорт размерами 5×1 см после диссекции были сразу же погружены в холодный физиологический раствор и отправлены на анализ ЛИФ, где с каждого кусочка размерами 1×1 см со стороны эндотелия проводили исследование ЛИФ. После этого была произведена фиксация материала в формалине для дальнейшего морфологического исследования. Оставшийся материал клапансодержащих графтов аорт человека в стерильных условиях бокса биологической безопасности подвергался процессу децеллюляризации, затем проводился анализ спектров ЛИФ для оценки степени децеллюляризации во времени. Процесс децеллюляризации заключается в элиминации аутологичных клеток с сохранением структурных особенностей и организации экстрацеллюлярного матрикса, что достигается погружением клапансодержащего фрагмента аорты человека в раствор, содержащий 0,5% трипсин/0,2% ЭДТА на 0,02 М фосфатном буфере, рН=7,4. Образцы оставлены в термостате при 37°С на 40 часов в стерильном сосуде с магнитной мешалкой. Фрагменты аорт забирались на следующих этапах: этап 1-2,5; этап 11-5; этап III-8; этап IV-26; этап V-40 часов после начала процесса децеллюляризации с последующим измерением ЛИФ. После каждого измерения спектров ЛИФ, материал также фиксировался в формалине, для дальнейшего морфологического исследования.
На фиг.1 представлены спектры с аорты (по оси OX - длина волны, по оси OY - интенсивность флюоресценции). Показано, что полный цикл децеллюляции графтов аорт (40 часов) приводит к исчезновению пика в полосе от 420 до 570 нм. Что отражает с одной стороны собственно децеллюляцию, а с другой декальцификацию аорт.
Уточняя феномен исчезновения спектрального пика в полосе 420-570 нм, проведен дополнительный эксперимент с целью изучения морфологических изменений цитоархитектоники ткани аорт и степени деградации ядерного материала. Для этого фрагменты клапансодержащих графтов аорт забирались на различных этапах процесса децеллюляризации Забор образцов производился через 2,5; 5; 8; 24; 40 часов после начала процесса децеллюляризации. Далее материал фиксировался в формалине, и готовились криостатные срезы для последующего окрашивания гематоксилином-эозином, этидиумом бромидом, хлортетрациклином. Выполнялась флюориметрия образцов при температуре 24°C по стандартной схеме.
Выявлено, что стенка аорты в процессе децеллюляризации претерпевает значительные морфологические изменения. Так гистологический анализ показал последовательное уменьшение и полное исчезновения ядросодержащих клеток в стенке аорт на этапах децеллюляции. На фиг.2 отражено начало децеллюляции графта аорты - 2,5 часа в децеллюляризирующем растворе - присутствуют ядросодержащие клетки и полное отсутствие ядросодержащих клеток в стенке аорты через 40 часов после содержания в децеллюлялизирующем растворе, фиг.3.
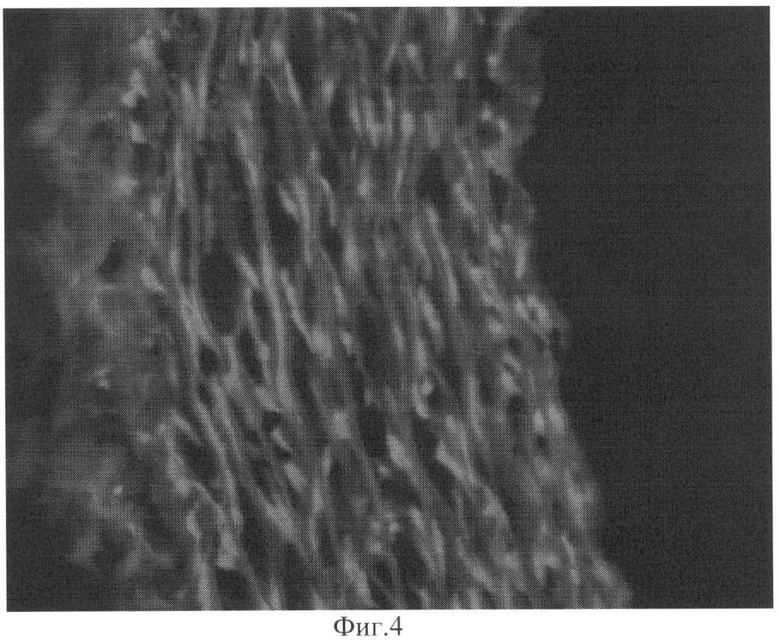
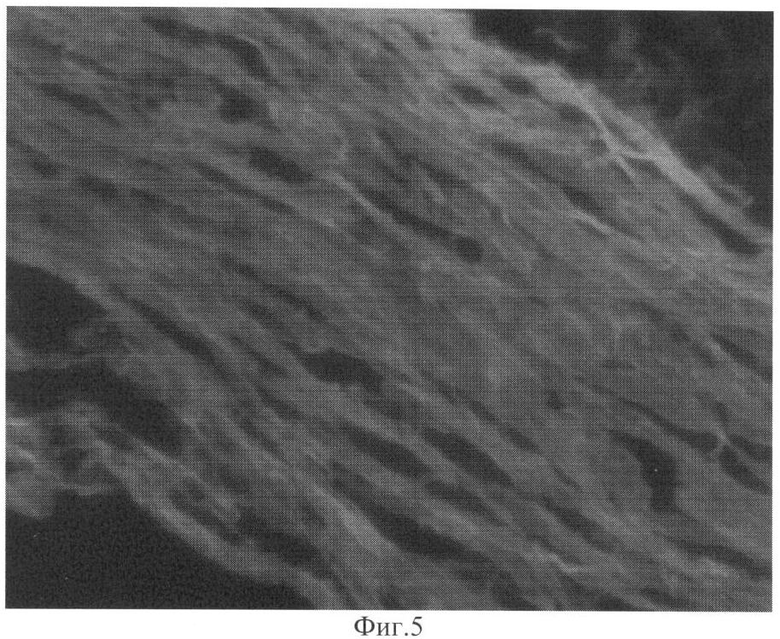
Эти изменения, так же наблюдались при анализе изображений при окрашивании этидиумом бромидом фиг.4 начало децеллюляции - присутствие ядросодержащих клеток, умеренный межволоконный отек, и фиг.5 - конец децеллюляции. Полное отсутствие ядросодержащих клеток, набухание волокон.
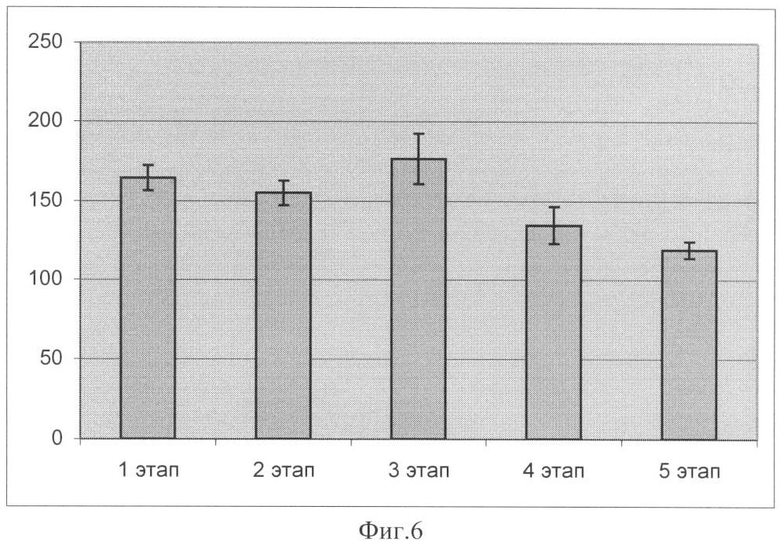
На фиг.6 представлена диаграмма, демонстрирующая изменение интенсивности флюоресценции в процессе децеллюляризации по включению этидиума бромида. Нами получено статистически достоверное различие (р<0,05) по уровню интенсивности суммарной флюоресценции Ethidium bromide аорт на последних двух этапах децеллюляризации - через 24 часа и 40 часов децеллюляризации, где было определено значительное снижение уровня флюоресценции в сравнении с исходным уровнем флюоресценции нативного препарата, а также с предшествовавшими биотехнологическими этапами 2,5 часа, 5, и 8 часов децеллюляризации.
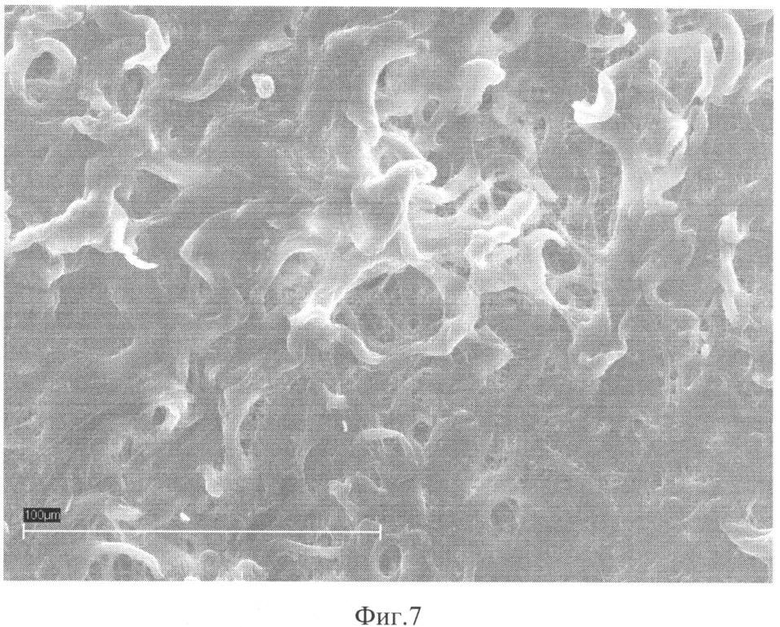
Обзорная сканирующая микроскопия показала, что на последних этапах децеллюляризации происходит тканевая трансформация, которая проявляется выскальзыванием отдельных волокон, нарушением ритмического характера волокнистой организации стенки аорты (фиг.7), а также появлением ячеистых структур при окончании процесса децеллюляризации (фиг.8) в сравнении с контролем, нативной стенкой аорты (фиг.9), отражающим линейно-прерывистый характер ориентации депозитов.
Обзорная сканирующая электронная микроскопия в режиме обратного рассеяния электронов показала ряд характерных черт на этапах получения ацеллюлярного гомографта относительно нативной аорты. Так субэндотелиальные линейно-прерывистые депозиты, ориентированные продольно аорте (по ходу крови), и апатитная минерализация, наблюдаемые во всех нативных аортах и более чем в половине препаратов, определяемые очаговые, глыбчатые депозиты размерами от 1 до 10 микрон не обнаруживались на этапе децеллюляризации 24 и 48 часов. Кроме того, обнаружена характерная трансформация тканей гомографта к поздним этапам децеллюляризации, которую мы охарактеризовали как формирование сетчато-ячеистой структуры. Более того, статистический анализ цифровых данных полученных при рентгеноспектральном изучении образцов тканей аорт, отчетливо продемонстрировал значительное снижение уровня кальция в сочетании с подъемом уровня фосфора. Потеря кальция тканями гомографтов аорт носит комбинированный характер как экстрацеллюлярный, так и внутриклеточный.
Исследование показало, что спектры ЛИФ на этапах децеллюляризации достоверно различаются от спектров тканей до начала этапа децеллюляризации. Более того, исследование показало перспективность использования УФ-лазера с λ=248 нм для диагностики состояния биологических тканей, в частности для определения степени децеллюляризации клапанно-содержащих графтов аорт. Приведенные данные доказывают перспективность применения диагностической лазериндуцированной флюоресценции, возбуждаемой эксимерными лазерами, для идентификации состава биологических тканей, регистрации их состояния и наличия изменений.
Литература
1. Bader A, Schilling Т, Haverich A, et al. Tissue engineering of heart valves-human endothelial cell seeding of detergent acellularized porcine valves. Eur J Cardiothorac Surg. 1998; 14: 279-284.
2. Cebotari S., Mertsching H., et al. Construction of Autologous Human Heart Valves Based on an Acellular Allograft Matrix // Circulation. 2002, 106: 1-63.
3. Elkins RC, Dawson PE, Goldstein S, et al. Decellularized human valve allografts. Ann ThoracSurg. 2001; 71: S428-S432.
4. Hoerstrup S.P., Sodian R., Daebritz S., et al. Functional living trileaflet heart valves grown in vitro. Circulation 2000; 102 (Suppl 3): III44-III49.
5. Steinhoff G, Mertsching H, Haverich A, et al. Tissue engineering of pulmonary heart valves on allogenic acellular matrix conduits: in vivo restoration of valve tissue. Circulation. 2000; 102: III50-5.
6. Ларионов П.М. Лазерно-индуцированная флюоресценция сердечных тканей при поражении кальцинозом. // Журнал Прикладной спектроскопии, 1997, т.64, №4, июль-август, стр.539-541.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОЛОГИЧЕСКОГО СОСУДИСТОГО ПРОТЕЗА | 2021 |
|
RU2781037C1 |
| Способ получения гомографта сердечно-сосудистой системы методом криоконсервации | 2021 |
|
RU2783910C2 |
| АЛЛОГРАФТ (ВАРИАНТЫ), СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПРОВЕДЕНИЯ АОРТАЛЬНОГО ПРОТЕЗИРОВАНИЯ | 2017 |
|
RU2712000C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БЕСКЛЕТОЧНОГО МАТРИКСА ИЗ ПУПОВИНЫ ЧЕЛОВЕКА ДЛЯ СОЗДАНИЯ ВЫСОКОРЕГЕНЕРАТИВНОГО РАНЕВОГО ПОКРЫТИЯ | 2022 |
|
RU2795904C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕРМАЛЬНОГО МАТРИКСА | 2018 |
|
RU2694543C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЗАЩИТЫ МИОКАРДА ПРИ КОРРЕКЦИИ ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА | 2009 |
|
RU2435526C2 |
| СПОСОБ УСКОРЕННОЙ ДЕЦЕЛЛЮЛЯРИЗАЦИИ БИОЛОГИЧЕСКОЙ ТКАНИ ИЛИ ОРГАНА | 2019 |
|
RU2714327C1 |
| ГОМОГРАФТ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ ГОМОГРАФТА, СРЕДА ДЛЯ ВОЗДЕЙСТВИЯ НА ТКАНИ ГОМОГРАФТА (ВАРИАНТЫ) | 2013 |
|
RU2525197C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЦЕЛЛЮЛЯРИЗИРОВАННЫХ МАТРИКСОВ ПАРЕНХИМАТОЗНЫХ ОРГАНОВ ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2016 |
|
RU2653489C2 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ АТРИОВЕНТРИКУЛЯРНОГО КЛАПАНА СЕРДЦА ЛЕГОЧНЫМ АУТОГРАФТОМ | 2009 |
|
RU2392872C1 |




Изобретение относится к области медицины. Способ предназначен для диагностики состояния тканей на этапах децеллюляризации и целлюляризации тканевых конструкций в биотехнологии. Для определения состояния клапаносодержащих графтов аорты человека на этапах децеллюляризации-целлюляризации тканевых биоматериалов и конструкций определяют спектр вторичной флюоресценции тканей под воздействием ультрафиолетового импульсного лазерного облучения. Децеллюляризацию проводят в 5 этапов в течение 2,5, 5, 8, 26, 40 часов. При исчезновении пика в спектральной полосе от 420 нм до 570 нм децеллюляризацию считают завершенной. Способ позволяет проводить идентификацию биологических тканей и определить состояние и наличие в нем изменений. 3 з.п. ф-лы, 9 ил.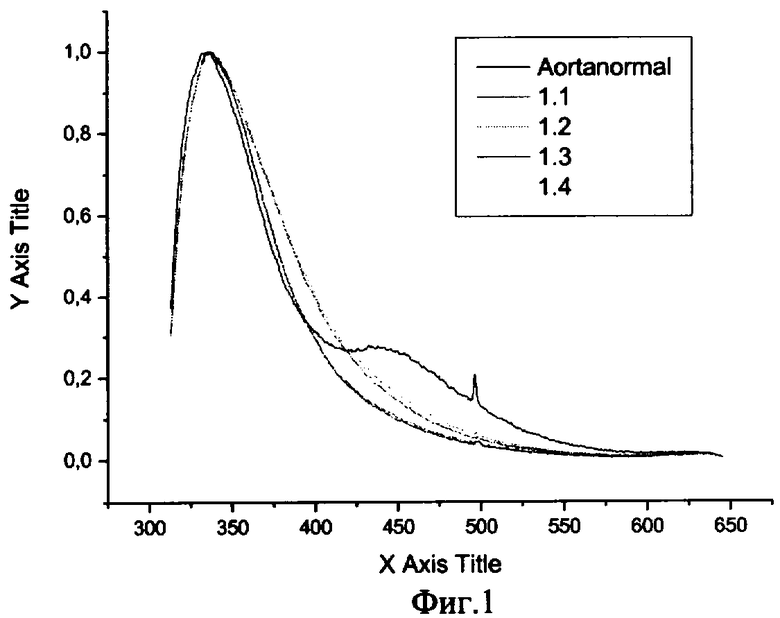
| ЛАРИОНОВ П.М | |||
| и др | |||
| Лазерно-индуцированная флуоресценция сердечных тканей при поражении кальцинозом | |||
| Ж | |||
| прикладной спектроскопии | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| СПОСОБ ОБРАБОТКИ ТКАНЕЙ ТРАНСПЛАНТАТОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2002 |
|
RU2231997C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧИСЛЕННОЙ ПЛОТНОСТИ И ОБЪЕМА ЭЛЕМЕНТОВ МИКРОСКОПИЧЕСКИХ СТРУКТУР В ТКАНЯХ | 1990 |
|
RU2013765C1 |
| US 5993844 A, 30.11.1999 | |||
| LARIONOV PM et al | |||
| Influence of mineral components on laser-induced fluorescence spectra of calcified | |||
Авторы
Даты
2009-01-10—Публикация
2006-08-09—Подача