Настоящее изобретение относится к производным карбоксамидов, к способу их получения, к фармацевтическим композициям, содержащим такие производные, и к их применению в качестве усилителей mGluR1.
Первый объект настоящего изобретения включает соединение формулы I
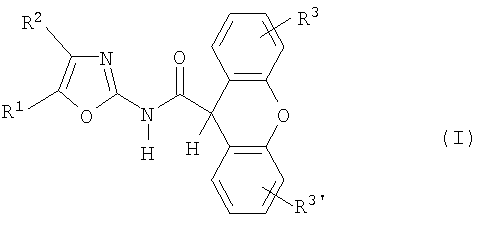
где
один из R1 и R2 означает трифторметил, а другой означает водород;
R3, R3' независимо друг от друга означают водород или галоген;
а также его фармацевтически приемлемые соли.
Соединения формулы I являются новыми. Они в общем виде описаны в опубликованной заявке No. WO 00/63166 (F.Hoffmann-La Roche AG).
Указанные соединения и их соли характеризуются ценными терапевтическими свойствами. Неожиданно было установлено, что соединения общей формулы I являются агонистами рецептора mGlu 1 и положительными аллостерическими модуляторами (усилителями) рецепторов метаботропного глютамата 1 (mGlu1).
В центральной нервной системе (ЦНС) передача нервного испульса происходит при взаимодействии нейромедиатора, который высвобождается из нейрона, с нейрорецептором. В большинстве случаев нейромедиатором в ЦНС является L-глютаминовая кислота, которая играет основную роль во множестве физиологических процессов. Глютамат-зависимые импульсные рецепторы подразделяются на две основные группы. В первую группу включены лиганд-управляемые ионные каналы. Метаботропные глютаматные рецепторы (mGluR) относятся ко второй группе и более того к семейству связанных с G-белком рецепторов. В настоящее время известно восемь различных членов семейства mGluR, причем некоторые из них подразделяются на подтипы. С учетом структурных характеристик, различных сигнальных путей вторичных мессенджеров и различной аффинности в отношении низкомолекулярных соединений указанные восемь рецепторов подразделяются на три подгруппы: рецепторы mGluR1 и mGluR5 относятся к группе I, рецепторы mGluR2 и mGluRS к группе II, а рецепторы mGluR4, mGluR6, mGluR7 и mGluR8 к группе III. Лиганды метаботропных глютаматных рецепторов первой группы можно использовать для лечения или профилактики острых и/или хронических неврологических заболеваний, таких как психоз, шизофрения, болезнь Альцгеймера, нарушение познавательной способности и недостаток памяти, а также хронические и острые боли. К другим показаниям для лечения относятся также ограничение мозговой функции, вызванное шунтированием или трансплантатом, ограниченное кровоснабжение мозга, травмы спинного мозга, травмы головы, гипоксия при беременности, остановка сердца и гипокликемия. Еще один ряд излечиваемых показаний включает хорею Гентингтона, боковой амиотрофический склероз, деменцию, вызванную СПИД, глазные травмы, ретинопатию, идиопатический паркинсонизм или паркинсонизм, вызванный лекарственными средствами, а также состояния, которые приводят к функциям, связанным с недостатком глютамата, таким как мышечные спазмы, судороги, мигрень, недержание мочи, привыкание к никотину, привыкание к опиатам, тревога, рвота, дискинезия и депрессия. Потенциально излечиваемые агонистами mGluR1 показания включают также болезнь Альцгеймера, нарушения познавательного процесса и недостаток памяти, хорею Гентингтона, боковой амиотрофический склероз и деменцию.
Селективными положительными аллостерическими модуляторами (усилителями) рецепторов mGluR1 называются соединения, которые сами по себе напрямую не активируют рецепторы mGlu1, но при связывании этих соединений увеличивается аффинность агониста к глютаматным участкам в его внеклеточном N-концевом участке связывания. Положительная аллостерическая модуляция является перспективным способом повышения степени активации соответствующих физиологических рецепторов, и результаты исследования мозжечковых срезов четко свидетельствуют о способности усилителей mGluR1 модулировать физиологическую активность mGlu1 в мозге (Knoflach et al., Proc. Nat. Acad. Sci. USA 98:13402-13407 (2001)) за счет повышения аффинности агониста к глютаматным участкам в его внеклеточном N-концевом участке связывания. Следовательно, селективные усилители mGluR1 обладают ценным терапевтическим действием и их открытие позволяет осуществлять терапевтическую положительную модуляцию рецепторов mGluR1.
Таким образом, объектом настоящего изобретения является получение соединений, которые обладают перспективными, указанными выше свойствами и следовательно, которые можно использовать для профилактики и лечения указанных выше заболеваний. Установлено, что соединения формулы I и их фармацевтически приемлемые соли проявляют активность усилителей mGluR1. Объектами настоящего изобретения являются также способ получения таких соединений, их применение в качестве фармацевтически активных соединений, лекарственных средств на основе соединений по настоящему изобретению и способ получения таких лекарственных средств.
Предпочтительными соединениями формулы I, включенными в объем настоящего изобретения, являются, например, соединения, в которых R3 и R3' означают водород.
К таким соединениям относятся следующие соединения:
(4-трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты и (5-трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты.
Кроме того, предпочтительными соединениями формулы I являются соединения, в которых R1 означает трифторметил, a R2 означает водород.
Прежде всего предпочтительные соединения означают соединения формулы I, где R1 означает трифторметил, R2 означает водород, и где по крайней мере один из R3 или R3' означает галоген. Более предпочтительно по крайней мере один из R3 или R3' означает фтор. В одном объекте настоящего изобретения R1 означает трифторметил, R2 означает водород, и по крайней мере один из R3 или R3' означает фтор.
Примерами таких соединений являются следующие соединения:
(5-трифторметилоксазол-2-ил)амид 2-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 3-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 4-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты и
(5-трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты.
Кроме того, предпочтительными соединениями формулы I являются соединения, в которых R2 означает трифторметил, а R1 означает водород.
Прежде всего предпочтительные соединения означают соединения формулы I, где R2 означает трифторметил, R1 означает водород, и где по крайней мере один из R3 или R3' означает галоген. Более предпочтительно по крайней мере один из R3 или R3' означает фтор. В одном объекте настоящего изобретения R1 означает водород, R2 означает трифторметил, и по крайней мере один из R3 или R3' означает фтор.
Примерами таких соединений являются следующие соединения:
(4-трифторметилоксазол-2-ил)амид 2-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 3-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 4-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты и
(4-трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты.
Кроме того, предпочтительными соединениями формулы I являются соединения, в которых R2 означает трифторметил, a R1 означает водород, и по крайней мере один из R3 или R3' означает хлор.
Примерами таких соединений являются следующие соединения:
(4-трифторметилоксазол-2-ил)амид 2-хлор-9Н-ксантен-9-карбоновой кислоты и
(4-трифторметилоксазол-2-ил)амид 4-хлор-9Н-ксантен-9-карбоновой кислоты.
В объем изобретения включены также все стереоизомерные формы и рацемические смеси.
Термин «галоген» означает фтор, хлор, бром и иод.
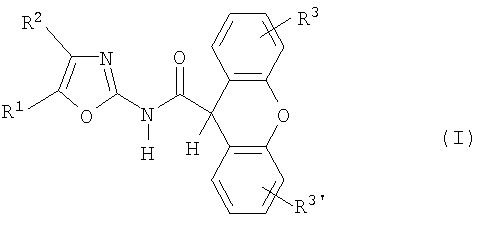
Соединения общей формулы I и их фармацевтически приемлемые соли можно получить способом, который включает взаимодействие соединения формулы II
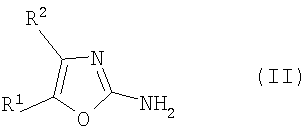
где один из R1 и R2 означает трифторметил, а другой означает водород, с соединением формулы III
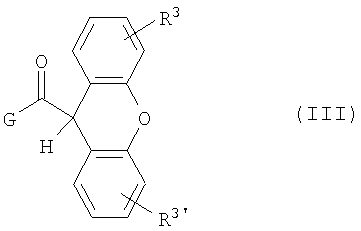
где R3, R3' независимо друг от друга означают водород или галоген, a G означает хлор или гидрокси,
с образованием соединения формулы I

и при необходимости превращение соединения формулы I в фармацевтически приемлемую соль.
Согласно указанному способу соединения формулы I можно получить при взаимодействии оксазол-2-иламина формулы II с хлорангидридом карбоновой кислоты формулы IIIa в присутствии N,N-диметиламинопиридина при температуре 0°С. Предпочтительным растворителем является хлористый метилен (схема 1).
Схема 1

В другом варианте соединения формулы I можно получить при взаимодействии оксазол-2-иламина формулы II с ксантен-9-карбоновой кислотой формулы IIIb. Карбоновую кислоту активируют 1,1'-карбонил-бис(3-метилимидазолий)трифлатом (CBMIT) в нитрометане при температуре 10°С. После нагревания до комнатной температуры к смеси добавляют амин (схема 2).
Схема 2
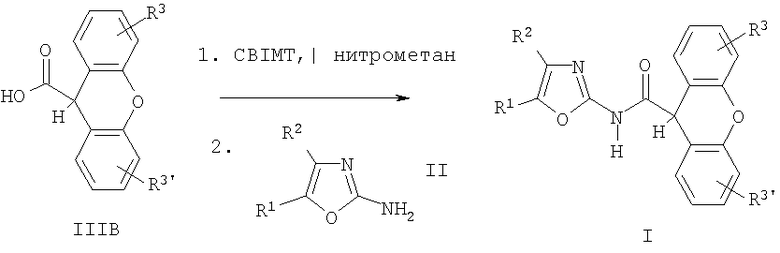
Фармацевтически приемлемые соли можно получить простыми стандартными методами с учетом природы соединения, предназначенного для превращения в соль. Для получения фармацевтически приемлемых солей основных соединений формулы I используют пригодные неорганические или органические кислоты, такие как, например, хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота или лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, пара-толуолсульфоновая кислота и т.п. Для получения фармацевтически приемлемых солей кислотных соединений используют пригодные соединения, содержащие щелочные металлы или щелочноземельные металлы, например, натрий, калий, кальций, магний или т.п., основные амины или основные аминокислоты.
Как указано выше, соединения формулы I и их фармацевтически приемлемые соли являются усилителями mGIuR1 и их можно использовать для лечения или профилактики острых и/или хронических неврологических нарушений, таких как психоз, шизофрения, болезнь Альцгеймера, нарушение познавательной способности и недостаток памяти, а также хронические и острые боли. К другим показаниям для лечения относятся также ограничение мозговой функции, вызванное шунтированием и трансплантатом, ограниченное кровоснабжение мозга, травмы спинного мозга, травмы головы, гипоксия при беременности, остановка сердца и гипокликемия. Еще один ряд излечиваемых показаний включает болезнь Альцгеймера, хорею Гентингтона, боковой амиотрофический склероз, деменцию, вызванную СПИД, глазные травмы, ретинопатию, идиопатический паркинсонизм или паркинсонизм, вызванный лекарственными средствами, а также состояния, которые приводят к функциям, связанным с недостатком глютамата, таким как мышечные спазмы, судороги, мигрень, недержание мочи, привыкание к никотину, привыкание к опиатам, тревога, рвота, дискинезия и депрессия.
Соединения по настоящему изобретению относятся к группе агонистов рецепторов mGlu1. Соединения обладают активностью, определенной описанным ниже методом анализа и составляющей 0,2 мкМ или менее.
Анализ связывания
Препарат кДНК, кодирующий рецептор mGlu 1a крысы, любезно предоставленный проф. S.Nakanishi (Киото, Япония), временно трансфектировали в клетки EBNA с использованием методики, описанной Schlaeger и др., New Dev. New Appl. Anim. Cell Techn., Proc. ESACT Meet., 15, 105-112 and 117-120 (1998). Величину [Са2+]i определяли с использованием трансфектированных mGlu 1a клеток EBNA после инкубации клеток с реагентом Fluo-3 AM (при конечной концентрации 0,5 мкМ) в течение 1 ч при 37°С с последующей четырехкратной промывкой буферным раствором для анализа (среда DMEM, содержащая соль Хенкса и 20 мМ HEPES. Величину [Са2+]i определяли при измерении флуоресценции на флуориметре-ридере для планшет (FLIPR, фирмы Molecular Devices Corporation, La Jolla, СА, США). Для определения антагонистической активности соединения исследовали в присутствии 10 мкМ глютамата в качестве агониста.
Кривые активации (агонисты) получали с использованием логистического уравнения с четырьмя параметрами и рассчитывали величины EC50 и коэффициент Хилла с использованием итеративного нелинейного метода и программного обеспечения Origin (Microcal Software Inc., Northampton, MA, США).
Специфические величины ЕС50 соединений формулы I представлены ниже в таблице:
Соединения формулы I по настоящему изобретению, кроме того, характеризуются высокой метаболической стабильностью. Этот параметр является предпочтительным для обеспечения высокой биодоступности, которая необходима для получения лекарственных средств, обладающих приемлемой активностью in vivo. Метаболическую стабильность определяли следующим методом.
Инкубация в присутствии микросом
Инкубационные смеси содержали микросомы из печени (из ткани крысы: 1,0 мг белка/мл, или из ткани человека: 2,0 мг белка/мл), исследуемое соединение 10 мкМ, MgCl2 (3,3 мМ) и восстановительную систему НАДФН, содержащую глюкозо-6-фосфатдегидрогеназу, НАДФН и глюкозо-6-фосфат (экв. 1 мМ НАДФН) в конечном объеме 1,0 мл 100 мМ калийфосфатного буферного раствора, рН 7,4. Реакцию инициировали добавлением восстановительной системы НАДФН при 37°С. Через 1, 5, 9, 13, 17, 21, 25 и 29 мин из реакционной смеси отбирали пробы по 5 мкл для анализа в системе ЖХВР-МС/МС, влючающей четырехступенчатый насос HP 1100 с дегазатором и спектрометр PE-Sciex API-2000 MS/MS. Для анализа использовали аналитическую колонку фирмы Waters Symmetry Shield RP8 (2,1×50 мм, размер частиц 3,5 мкм). Для элюции использовали нелинейный градиент полярности растворителя от фазы А (МеОН/1% муравьиная кислота, 20:80) до фазы В (МеОН) в течение 2 мин при скорости потока 0,25 мл/мин. Для определения содержания исходного соединения использовали спектрометр PE-Sciex API-2000 MS/MS. Метаболический клиренс in vivo рассчитывали по известной методике (Houston, Biochem. Pharmacol. 47:1469-1479 (1994)). Краткое описание методики: собственный клиренс (см. столбец «клиренс» ниже в таблице) рассчитывали с использованием полупериода, определенного in vitro, с учетом объема инкубационной смеси и микросомального белка, добавленного в инкубационную смесь in vitro. Собственный клиренс выражали в мкл/мин/мг микросомального белка. Для экстраполяции результатов in vivo рассчитывали коэффициент экстракции в печени (Е). В данном случае величина МАВ в % равна 1-Е. МАВ означает величину максимальной биодоступности при данной величине клиренса.
Соединения формулы I и их фармацевтически приемлемые соли можно использовать в качестве лекарственных средств, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить пероральным способом, например, в форме таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако введение можно осуществлять ректальным способом, например, в форме суппозиториев, или парентеральным способом, например, в форме инъекционных растворов.
Соединения формулы I и их фармацевтически приемлемые соли можно перерабатывать в смеси с инертными, неорганическими или органическими носителями для получения фармацевтических препаратов. В качестве таких носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул используют, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и т.п. В качестве пригодных носителей для мягких желатиновых капсул можно использовать, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п., однако, в зависимости от природы активного соединения в случае мягких желатиновых капсул обычно не требуется никаких носителей. Пригодные носители для получения растворов и сиропов включают, например, воду, полиолы, сахарозу, инвертированный сахар, глюкозу и т.п. Для водных инъекционных растворов водорастворимых солей соединений формулы I можно использовать адьюванты, такие как спирты, полиолы, глицерин, растительные масла и т.п., однако, как правило в них нет необходимости. Пригодные носители для суппозиториев включают, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, увлажнители, эмульгаторы, подсластители, красители, ароматизаторы, соли для изменения осмотического давления, буферные вещества, маскирующие агенты или антиоксиданты.
Фармацевтические препараты могут также содержать другие ценные терапевтические вещества.
Как описано выше, объект настоящего изобретения включает лекарственные средства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный эксципиент, а также способ получения таких лекарственных средств, включающий переработку одного или более соединений формулы I или его фармацевтически приемлемых солей и при необходимости одного или более других терапевтически ценных веществ в галеновую лекарственную форму в смеси с одним или более инертных носителей.
Дозировки могут изменяться в широких пределах и зависят от индивидуальных требований в каждом конкретном случае. В основном эффективная доза для перорального или парентерального введения составляет от 0,01 до 20 мг/кг/сут, но для всех описанных показаний предпочтительной является доза от 0,1 до 10 мг/кг/сут. Суточная доза для взрослого человека массой 70 кг соответственно составляет от 0,7 до 1400 мг/сут, предпочтительно от 7 до 700 мг/сут.
И наконец, объектом изобретения, как указано ранее, является также применение соединений формулы I и их фармацевтически приемлемых солей для получения лекарственных средств, прежде всего для подавления развития или профилактики острых и/или хронических неврологических нарушений указанного типа.
В связи с указанным выше в настоящем изобретении предлагается также:
(1) соединение формулы I или его фармацевтически приемлемая соль для использования в качестве агониста mGluR1, например, для применения при лечении любого конкретного из указанных выше заболеваний;
(2) фармацевтическая композиция, включающая соединение или соль по п.(1) в качестве активного ингредиента в смеси с фармацевтически приемлемым разбавителем или носителем, например, для использования при лечении или профилактике заболевания или состояния, которое связано с активацией mGluR1 или при котором такая активация предполагается;
(3) способ лечения любого конкретного показания, указанного выше, у субъекта, нуждающегося в таком лечении, причем способ включает введение эффективного количества соединения или его соли по п.(1);
(4) применение соединения или его соли по п.(1) для получения лекарственного средства, предназначенного для лечения и профилактики заболеваний, связанных с рецептором mGlu 1, например, хронического неврологического нарушения;
(5) способ получения соединения или его соли по п.(1).
Пример 1
(4-Трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты
а) 4-Трифторметилоксазол-2-иламин
4-Трифторметилоксазол-2-иламин получали по методике, описанной в литературе (Crank и Foulis, J. Med. Chem. 14:1075 (1971)).
б) (4-Трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты
К раствору 150 мг (0,99 ммоля, 1,0 экв.) 4-трифторметилоксазол-2-иламина и 6 мг (0,05 ммоля, 0,05 экв.) N,N-диметиламинопиридина в 2 мл сухого пиридина по каплям при 0°С добавляли раствор 245 мг (0,99 ммоля) хлорангидрида 9-ксантенкарбоновой кислоты (CAS: 26454-53-5) в 2 мл хлористого метилена. Смесь перемешивали в течение 1 ч при 0°С, а затем при комнатной температуре в течение ночи. Смесь выливали в тщательно перемешиваемую смесь 30 мл хлористого метилена и 30 мл воды. Органическую фазу отделяли, водную фазу экстрагировали два раза по 30 мл хлористого метилена. Объединенные органические фазы промывали 25 мл воды, сушили над сульфатом магния и концентрировали, при этом получали неочищенный продукт (590 мг в виде твердого вещества желтого цвета), после перекристаллизации которого из этилацетата/гексана получали 250 мг (0,66 ммоля, 66%) (4-трифторметилоксазол-2-ил)амида 9Н-ксантен карбоновой кислоты в виде кристаллов белого цвета, tпл. 222°С, МС: m/e 361,2 (М+Н+).
Пример 2
(5-Трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты
а) 5-Трифторметилоксазол-2-иламин
5-Трифторметилоксазол-2-иламин получали в виде твердого вещества грязно-белого цвета, МС: m/e 152,0 (М+), по следующей методике. К раствору 21,6 мл (39,4 г, 0,2 моля) 97%-ного 3-бром-1,1,1-трифторацетона в 40 мл трет-бутанола добавляли 12,6 г (0,3 моля. 1.5 экв.) цианамида, при этом наблюдаяась незначительная экзотермическая реакция. После перемешивания в течение 10 мин к смеси добавляли 19,7 г (0,24 моля, 1,2 экв.) тонкодисперсного порошкообразного ацетата натрия при интенсивном перемешивании и суспензию нагревали в течение 30 мин при 65°С, кипятили с обратным холодильником в течение 2 ч и охлаждали. Смесь выливали в тщательно перемешиваемую смесь 200 мл этилацетата и 100 мл воды. Величину рН водной фазы доводили до приблизительно 8-9 при добавлении 5% раствора бикарбоната натрия. Органическую фазу отделяли, водную фазу экстрагировали 50 мл этилацетата. Объединенные органические фазы промывали два раза по 20 мл воды и концентрировали в вакууме. Остаток, 40,2 г вязкого масла светло-оранжевого цвета очищали экспресс-хроматографией на силикагеле (элюент: смесь хлористого метилена и этилацетата, 2:1). Фракции, содержащие требуемое соединение (6,08 г масла светло-желтого цвета) и более полярные примеси, концентрировали и повторно очищали экспресс-хроматографией на силикагеле (элюент: смесь хлористого метилена и метанола, 98:2), при этом получали 1,83 г (0,012 моля, 6%) 5-трифторметилоксазол-2-иламина.
б) (5-Трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 218°C, MC: m/e 360,10 (М+), по общей методике, описанной в примере 1б, из 5-трифторметилоксазол-2-иламина и хлорангидрида 9-ксантенкарбоновой кислоты.
Пример 3
(4-Трифторметилоксазол-2-ил)амид (RS)-2-фтор-9Н-ксантен-9-карбоновой кислоты
а) 2-Фтор-9Н-ксантен
К раствору 19,63 г 2-фтор-9-ксантона (CAS: 2839-49-8) в 290 мл ТГФ при комнатной температуре добавляли 21,7 мл комплекса боран-диметилсульфоксид. Смесь кипятили с обратным холодильником в течение 4 ч и охлаждали до 5-10°С, затем по каплям добавляли 200 мл метанола. При этом наблюдалась эксзотермическая реакция с образованием пены и выделением газа. Раствор упаривали досуха, остаток переносили в 200 мл метанола и упаривали досуха. Остаток переносили в 200 мл этилацетата и упаривали досуха. Неочищенный продукт, 18,69 г твердого вещества бежевого цвета, очищали экспресс-хроматографией на силикагеле (элюент: гексан), при этом получали 17,97 г (89,8 ммоля, 98%) 2-фтор-9Н-ксантена в виде твердого вещества белого цвета.
б) Рац. (RS)-2-фтор-9-ксантенкарбоновая кислота
К раствору 17,97 г фтор-9Н-ксантена в 285 мл сухого ТГФ при температуре от -70°С до -65°С добавляли 53,9 мл 2М раствора диизопропиламида лития. Раствор красного цвета перемешивали в течение 20 мин при -70°С, затем к смеси добавляли несколько кусочков сухого льда до температуры -75°С. Красное окрашивание быстро исчезало, смесь нагревали до комнатной температуры и перемешивали в течение 15 мин, затем добавляли 250 мл воды и продолжали перемешивание в течение еще 15 мин. К смеси добавляли эфир (300 мл), органическую фазу экстрагировали два раза по 100 мл 2н. раствора гидроксида натрия и промывали два раза по 50 мл воды. Объединенные водные фазы промывали 25 мл эфира, затем рН доводили до 1-2 при добавлении 27%-ного раствора хлористоводородной кислоты, при этом образовывался осадок белого цвета. Подкисленную водную фазу экстрагировали один раз 300 мл смеси хлористого метилена и метанола, 9:1, и два раза по 300 мл хлористого метилена. Объединенные органические фазы промывали 30 мл воды, сушили над сульфатом натрия и концентрировали в вакууме. Неочищенный продукт (12,87 г твердого вещества бежевого цвета) растирали в эфире, при этом получали 11,78 г (48,2 ммоля, 54%) (RS)-2-фтор-9-ксантенкарбоновой кислоты в виде кристаллов белого цвета, МС (отриц. ион): m/e 198,9 (М-HCO2)-.
в) (4-Фторметилоксазол-2-ил)амид (RS)-2-фтор-9Н-ксантен-9-карбоновой кислоты
К раствору 883 мг (1,80 ммоля, 1,1 экв.) трифтата 1,1'-карбонил-бис-(3-метилимидазолия) (CBMIT, см. Saha и др., J. Am. Chem. Soc. 111:4856 (1989)) в 3 мл нитрометана при 10°С добавляли 400 мг (1,64 ммоля) (RS)-2-фтор-9-ксантенкарбоновой кислоты. Полученную суспензию нагревали до комнатной температуры и перемешивали в течение еще 15 мин. Затем добавляли 4-трифторметилоксазол-2-иламин (274 мг, 1,80 ммоля, 1,1 экв.) и смесь перемешивали при комнатной температуре в течение 16 ч. Полученную вязкую смесь светло-красного цвета экстрагировали смесью 45 мл хлористого метилена, 5 мл метанола и 50 мл воды. Органическую фазу отделяли и водную фазу экстрагировали два раза по 30 мл хлористого метилена/метанола, 9:1.
Объединенные органические фазы промывали 30 мл воды, сушили над сульфатом натрия и концентрировали в вакууме. Неочищенный продукт (630 мг твердого вещества светло-красного цвета) очищали экспресс-хроматографией на силикагеле (элюент: хлористый метилен), при этом после перекристаллизации из этилацетата/гексана получали 233 мг (0,62 ммоля, 38%) (4-трифторметилоксазол-2-ил)амида (RS)-2-фтор-9Н-ксантен-9-карбоновой кислоты, tпл. 241°С, МС: m/e 379,1 (М+Н+).
Пример 4
(5-Трифторметилоксазол-2-ил)амид (RS)-2-фтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества светло-желтого цвета, tпл. 217°С, МС (отриц.ион): m/e 377,1 (М-Н-), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и (RS)-2-фтор-9-ксантенкарбоновой кислоты.
Пример 5
(4-Трифторметилоксазол-2-ил)амид (RS)-3-фтор-9Н-ксантен-9-карбоновой кислоты
а) (RS)-3-Фтор-9-ксантенкарбоновая кислота
Рац. (RS)-3-фтор-9-ксантенкарбоновую кислоту получали в виде твердого вещества белого цвета, МС (отриц.ион): m/e 198,9 (М-HCO2)-), по общей методике, описанной в примерах 3а и 3б, из 3-фторксантона (CAS: 2839-50-1).
б) (4-Трифторметилоксазол-2-ил)амид (RS)-3-фтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества светло-желтого цвета, tпл. 221°С, МС: m/e 379,1 (М+Н+), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и (RS)-3-фтор-9-ксантенкарбоновой кислоты.
Пример 6
(5-Трифтирметилоксазол-2-ил)амид (RS)-3-фтор-9Н-ксантен-9-карбоновой кислоты.
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 250°С, МС (отриц.ион): m/e 377,1 (М-Н-), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и (RS)-3-фтор-9-ксантенкарбоновой кислоты.
Пример 7
(4-Трифторметилоксазол-2-ил)амид (RS)-4-фтор-9Н-ксантен-9-карбоновой кислоты
а) (RS)-4-Фтор-9-ксантенкарбоновая кислота
Рац. (RS)-4-фтор-9-ксантенкарбоновую кислоту получали в виде твердого вещества белого цвета, МС (отриц.ион): m/e 198,9 (М-HCO2)-), по общей методике, описанной в примерах 3а и 3в, из 4-фторксантона (CAS: 2839-51-2).
б) (4-Трифторметилоксазол-2-ил)амид (RS)-4-фтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 233°С, МС: m/e 379,2 (М+Н+), по общей методике, описанной в примере 3в, из 4-трифторметилоксазол-2-иламина и (RS)-4-фтор-9-ксантенкарбоновой кислоты.
Пример 8
(5-Трифторметилоксазол-2-ил)амид (RS)-4-фтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 228°С, МС: m/e 379,2 (M+H+), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и (RS)-4-фтор-9-ксантенкарбоновой кислоты.
Пример 9
(4-Трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой-кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 259°С, МС: m/e 397,1 (М+Н+), по общей методике, описанной в примере 3в, из 4-трифторметилоксазол-2-иламина и 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты (CAS: 188028-26-4).
Пример 10
(5-Трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 232°С, МС (отриц.ион): m/e 395,1 (М-Н-), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты.
Пример 11
(4-Трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 265°С, МС: m/e 397,2 (М+Н+), по общей методике, описанной в примере 3в, из 4-трифторметилоксазол-2-иламина и 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты (CAS:188028-37-7).
Пример 12
(5-Трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 249°С, МС: m/e 379,2 (М+Н+), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты.
Пример 13
(4-Трифторметилоксазол-2-ил)амид (RS)-2-хлор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 235°С, МС: m/e 395,2, 397,2 (М+Н+), по общей методике, описанной в примере 3в, из 4-трифторметилоксазол-2-иламина и (RS)-2-хлор-9Н-ксантен-9-карбоновой кислоты (CAS: 188027-67-0).
Пример 14
(4-Трифторметилоксазол-2-ил)амид (RS)-4-хлор-9Н-ксантен-9-карбоновой кислоты
Указанное в заголовке соединение получали в виде твердого вещества белого цвета, tпл. 212°С, МС: m/e 395,1, 397,1 (М+Н+), по общей методике, описанной в примере 3в, из 5-трифторметилоксазол-2-иламина и (RS)-4-хлор-9Н-ксантен-9-карбоновой кислоты (CAS: 188027-87-4).
Пример А
Таблетки
Таблетки (250 мг) следующего состава получали по стандартной методике.
Пример Б
Таблетки
Таблетки (400 мг) следующего состава получали по стандартной методике.
Пример В Капсулы
Капсулы (масса содержимого 150 мг) следующего состава получали следующим способом:
Активный ингредиент с соответствующим размером частиц, кристаллическую лактозу и микрокристаллическую целлюлозу смешивали до образования гомогенной смеси, просеивали и добавляли тальк и стеарат магния. Полученной смесью наполняли твердые желатиновые капсулы соответствующего размера.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ЭФИРОВ КАРБАМИНОВОЙ КИСЛОТЫ, ИХ ПОЛУЧЕНИЕ (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛИГАНДОВ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ | 2000 |
|
RU2248349C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2001 |
|
RU2251419C2 |
| ПРОИЗВОДНЫЕ ДИГИДРОБЕНЗО[b][1,4]ДИАЗЕПИН-2-ОНА В КАЧЕСТВЕ АНТАГОНИСТОВ I mGluR2 | 2002 |
|
RU2270197C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНА И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ, ОБЛАДАЮЩЕЕ СЕЛЕКТИВНОЙ БЛОКИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ПОДВИДА NMDA-РЕЦЕПТОРОВ | 2002 |
|
RU2303037C2 |
| ПРОИЗВОДНЫЕ ПИРИДИН-2-КАРБОКСАМИДА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR5 | 2006 |
|
RU2411237C2 |
| ПРОИЗВОДНЫЕ ДИГИДРОБЕНЗО[b][1,4]ДИАЗЕПИН-2-ОНА В КАЧЕСТВЕ АНТАГОНИСТОВ MGLUR2 II | 2002 |
|
RU2263112C2 |
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, КОМБИНИРОВАННЫЙ ПРОДУКТ И СПОСОБ ИНГИБИРОВАНИЯ МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2003 |
|
RU2314306C2 |
| ПРОИЗВОДНЫЕ СУЛЬФОНИЛПИРРОЛИДИНА | 2001 |
|
RU2272026C2 |
| ПРОИЗВОДНЫЕ БЕНЗОЦИКЛОАЛКИЛАЗОЛОТИОНА | 1995 |
|
RU2145321C1 |
| ПРОИЗВОДНЫЕ БЕНЗОДИАЗЕПИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2278865C2 |
Настоящее изобретение относится к новым соединениям формулы (I) и их фармацевтически приемлемым солям. Соединения настоящего изобретения обладают свойствами свойствами агонистов рецепторов mGlu 1 и могут найти применение для лечения таких заболеваний, как психоз, шизофрения, болезнь Альцгеймера и т.д. В общей формуле (I)
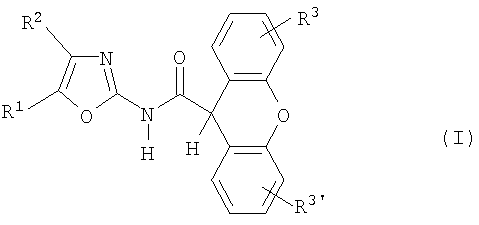
где один из R1 и R2 означает трифторметил, а другой означает водород; R3, R3' независимо друг от друга означают водород или галоген. Изобретение также относится к получению соединений изобретения, применению соединений изобретения для получения лекарственного средства и к лекарственному средству, обладающему свойствами агонистов рецепторов mGlu 1. 4 н. и 3 з.п. ф-лы, 2 табл.
где один из R1 и R2 означает трифторметил, а другой означает водород;
R3, R3' независимо друг от друга означают водород или галоген;
а также его фармацевтически приемлемые соли.
(4-трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 2-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 3-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 4-фтор-9Н-ксантен-9-карбоновой кислоты,
(5-трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты и
(5-трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 2-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 3-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 4-фтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 2,7-дифтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 3,6-дифтор-9Н-ксантен-9-карбоновой кислоты,
(4-трифторметилоксазол-2-ил)амид 2-хлор-9Н-ксантен-9-карбоновой кислоты и
(4-трифторметилоксазол-2-ил)амид 4-хлор-9Н-ксантен-9-карбоновой кислоты.
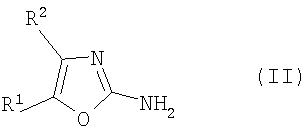
где один из R1 и R2 означает трифторметил, а другой означает водород, с соединением формулы III
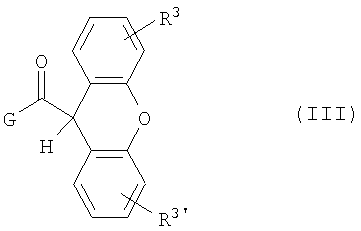
где R3, R3' независимо друг от друга означают водород или галоген, a G означает хлор или гидрокси,
и необязательно превращение полученного соединения формулы I в его фармацевтически приемлемую соль.
| RU 94022743 A1, 10.10.1996 | |||
| ПНЕВМАТИЧЕСКИЙ ГЛУБИННЫЙ НАСОС | 1940 |
|
SU63166A1 |
| ЛЕНТОЧНЫЙ МАГНИТНЫЙ СЕПАРАТОР | 2007 |
|
RU2356631C1 |
Авторы
Даты
2009-01-27—Публикация
2003-12-17—Подача