Ферментный каскад системы ренин-ангиотензин (РАС) включает ряд биохимических реакций и, как хорошо известно, существуют различные подходы, основанные на применении регуляторного вмешательства в этот каскад, которые могут применяться в области терапии, например, для лечения гипертензии.
Ангиотензиноген, т.е. α2-макрогликопротеин, расщепляется ферментом ренином с образованием декапептида ангиотензина I, который сам обладает лишь очень слабой биологической активностью. На следующей стадии каскада (пути превращения) под действием ангиотензинпревращающего фермента (АСЕ), который главным образом связан с эндотелием, отщепляются еще 2 аминокислоты, что приводит к образованию ангиотензина II. Последний, как полагают, является одним из наиболее сильных природных вазоконстрикторов.
Сосудосуживающая активность ангиотензина II обусловлена его действием на клетки гладкой мускулатуры и стимулированием образования адренергических гормонов адреналина и норадреналина, и увеличением активности симпатической нервной системы вследствие образования норадреналина. Кроме того, ангиотензин II воздействует на электролитический баланс, вызывая, например, антинатрийуретические и антидиуретические воздействия на почки, и вследствие этого стимулируя, с одной стороны, высвобождение пептида вазопрессина из гипофиза, и, с другой стороны, альдостерона из гломерулозной области надпочечников. Все эти воздействия играют важную роль в регуляции кровяного давления.
Ангиотензин II взаимодействует со специфическими рецепторами на поверхности клетки-мишени. В настоящее время достигнуты успехи в идентификации подтипов рецепторов, которые, например, обозначают как АТ1-рецепторы и АТ2-рецепторы. В настоящее время значительные усилия предпринимаются для выявления веществ, которые избирательно связываются с AT1-рецептором. Эти действующие вещества называют антагонистами ангиотензина II или блокаторами рецептора ангиотензина II. Вследствие их способности ингибировать АТ2-рецептор эти антагонисты могут, например, применяться в качестве гипотензивных средств или для лечения застойной сердечной недостаточности.
Ишемическая болезнь сердца - острый инфаркт миокарда
Ишемическая болезнь сердца является основной причиной смерти в промышленно развитых странах. Методы борьбы с ишемической болезнью сердца в основном основаны на одной из трех стратегий, которые включают медицинскую терапию, процедуры подкожного внутрипросветного хирургического вмешательства, такие как коронарная ангиопластика и атеректомия, и трансплантация с использованием коронарного артериального шунтирования. Хотя медицинское лечение остается основным средством противоишемической терапии, многие пациенты подвергаются дополнительной инвазивной терапии с целью восстановления коронарного потока крови. Однако продолжается все более интенсивная дискуссия, касающаяся не только достоинств этих терапевтических подходов, но также и момента времени в процессе лечения ишемической болезни сердца, когда они должны применяться, и типа пациента, для которого они пригодны в наибольшей степени.
Острый инфаркт миокарда (МИ) поражает большинство больных без предварительных симптомов и при отсутствии обнаруживаемой в клинических условиях предрасположенности (факторов риска) (Braunwald E., Heart Disease - a Textbook of Cardiovascular Medicine, 1997). Когда пациенты попадают в отделение интенсивной терапии с симптомами острого МИ, для установления диагноза острого МИ требуется, чтобы пациенты имели
(1) увеличенную концентрацию сердечных ферментов в плазме и
(2) или типичный клинический симптом и/или типичные изменения ЭКГ (электрокардиограммы).
Повышение уровня сердечных ферментов может быть обусловлено любым из следующих факторов:
- общий уровень креатинкиназы (КК) по крайней мере в 2 раза превышает верхний предел нормального диапазона, или
- уровень КК-ММ (в мышце - головном мозге) превышает верхний предел нормального диапазона и составляет по крайней мере 5% нормального уровня КК;
Если общий уровень КК или КК-ММ не может быть установлен, то в качестве критерия наличия острого МИ могут быть приняты следующие факторы:
- уровень тропонина Т по крайней мере в 3 раза превышает верхний предел нормального диапазона;
- уровень тропонина I по крайней мере в 3 раза превышает верхний предел нормального диапазона.
Использование тропонина Т в качестве сывороточного маркера МИ описано у Murthy V.V. и Karmen A., J. Clin. Labor. Analys., 11: 125-128 (1997).
Аналитические характеристики и данные о клиническом применении при чувствительном иммуноанализе для определения уровня сердечного тропонина I описаны у Davies E. и др., Clin. Biochem., 30: 479-490 (1997).
Типичные изменения ЭКГ включают развитие ST-сегмента или Т-волны в двух или большем количестве непрерывных ЭКГ-записей, развитие новых патологических Q/QS-волн в двух или большем количестве непрерывных ЭКГ-записей, или развитие новой блокады ножки пучка Гиса.
Таким образом, для таких пациентов основная цель профилактической лекарственной терапии состоит во вторичной профилактике, а именно в применении терапии для дальнейшего лечения последующих коронарных симптомов.
Пациенты, перенесшие острый МИ, подвергаются умеренному риску возникновения повторного инфаркта или смерти от сердечного приступа. Заболеваемость и смертность после МИ могут быть связаны с аритмией, дисфункцией левого желудочка и повторным МИ. Для вторичной профилактики пациентов, перенесших МИ, применяют аспирин. Поскольку аспирин обладает выраженным защитным действием в качестве средства вторичной профилактики сосудистых заболеваний, то также было проведено изучение преимуществ аспирина в качестве средства первичной профилактики. Однако некоторые исследования показали, что терапия с использованием аспирина приносит реальную пользу только ограниченному проценту населения из группы риска. Например, для первичной профилактики применение аспирина может быть рекомендовано только для людей старше 50 лет с неконтролируемыми факторами риска в отношении развития коронарных симптомов (Cairns J.A., Lewis H.D., Mead T.W., Sutton G.S., Theroux P., Antithrombotic agents in coronary arthery disease. Chest 108 (приложение 4): 3805, 1995).
Вторичная профилактика острого инфаркта миокарда
В течение нескольких десятилетий активно проводилось изучение концепции вторичной профилактики повторного инфаркта и предупреждения смерти после восстановления пациентов, перенесших МИ. При доказательстве эффективности различных видов вмешательства существуют проблемы, связанные как с недостаточной эффективностью определенных стратегий, так и с трудностью доказательства того, что улучшились показатели смертности и заболеваемости после перенесенного МИ. Хотя в опытах с использованием лекарств для вторичной профилактики при доказательстве преимущества определенной терапии обычно проводится тестирование одной из форм терапии в сравнении с плацебо, врач должен понимать, что строгий клинический уход за конкретными пациентами является намного более важным, чем механическое применение агента, который оказался эффективным в самых современных испытаниях лекарственного средства.
Первичная и вторичная профилактика - эпидемиологические аспекты
С эпидемиологической точки зрения первичная профилактика представляет собой защиту здоровья с помощью индивидуальных и социальных средств, таких как хорошее состояния питания, физическая подготовленность и эмоциональное состояние. Первичная профилактика включает общее укрепление здоровья и конкретные защитные меры. Она может быть определена как профилактика болезни путем изменения чувствительности или уменьшения воздействия вредных факторов на чувствительных индивидуумов. Трудно определить, как, например, введение антагониста ангиотензина II - лосартана может быть оценено с точки зрения улучшения общего состояния здоровья. Это должно было бы включать введение антагониста ангиотензина II всему населению в целом с целью предупреждения возникновения МИ у части этого населения, что исключительно трудно оценить количественно. С другой стороны, вторичная профилактика включает все средства раннего обнаружения, пригодные для отдельных пациентов и населения в целом, и быстрого и эффективного вмешательства для коррекции отклонений от здорового состояния. В целом, вторичная профилактика предназначена для уменьшения распространенности за счет сокращения продолжительности.
Ингибиторы АСЕ использовали для вторичной профилактики для пациентов, перенесших МИ, т.е. применение ингибиторов АСЕ в тех случаях, когда пациент(ка) страдает от ПЕРВОГО МИ, может предупредить дальнейшие осложнения, связанные с исходным (первоначальным) заболеванием, и таким образом повысить выживаемость.
Разработка антагонистов AT1-рецептора дает в дополнение к ингибиторам АСЕ новое более избирательное фармакологическое средство для ингибирования каскада ренин-ангиотензин. Однако существуют различия в характеристиках антагонистов АТ1-рецептора и ингибиторов АСЕ. Одно из них заключается в том, что ингибиторы АСЕ вызывают усиление продуцирования брадикинина, поскольку киназа II и превращающий фермент представляют собой одно и то же. Связанный с брадикинином механизм, опосредуемый оксидом азота, простагландинами и гиперполяризующим эндотелиальным фактором, может обусловливать различные клинические воздействия ингибиторов АСЕ. Кроме того, в настоящее время не выяснено воздействие АТ2, тогда как известно, что ингибирование AT1-рецептора приводит к увеличению уровня АТ2.
Лечение, с одной стороны, заключается в использовании таких мер, как изменения стиля жизни, применение определенных лекарств, таких как антибиотики, которые могут изменить течение болезни (например, введение ингибиторов ангиотензинпревращающего фермента пациентам с застойной сердечной недостаточностью для повышения их выживаемости) и/или привести к устранению болезни. Если диагностирован острый МИ, то пациента можно лечить с помощью лекарственного средства, которое, как ожидается, понижает смертность пациента(ки) и улучшает кратковременный и долговременный прогноз. Основная причина ЛЕЧЕНИЯ пациентов с острым МИ, например, с помощью антагониста ангиотензина II валсартана основана на предшествующих доклинических научных исследованиях, в которых продемонстрировано, что введение соединения может уменьшать размер МИ, что в результате его воздействия на функцию левого желудочка, является одной их основных. предпосылок выживаемости.
Целью настоящего исследования является разработка терапевтического подхода для лечения острого МИ и для вторичной профилактики острого МИ.
При создании настоящего изобретения неожиданно было установлено, что антагонисты рецептора ангиотензина II могут применяться для лечения острого МИ и для вторичной профилактики острого МИ.
Это благоприятное действие может быть продемонстрировано на основе сравнительного исследования эффективности кратковременного или долговременного введения терапевтически эффективного антагониста ангиотензина II в качестве дополнения к принятой (общепризнанной) терапии, применяемой при указанном заболевании. Соответствующие исследования проводят, например, путем оценки на двух параллельных группах пациентов в рамках перспективного многонационального проводимого в нескольких центрах вслепую в двух повторностях рандомизированного активно контролируемого клинического испытания, результаты которого должны быть статистически достоверными. Первая группа включает людей, имеющих высокую степень риска в отношении чувствительности к острому МИ, например, подвергающихся соответствующим факторам риска, таким как стресс, имеющим диабет, сопровождающийся высоким кровяным давлением, большой вес тела, семейный анамнез и т.д., и их лечат терапевтически эффективным количеством антагониста рецептора ангиотензина II, в то время как вторая группа также включает людей, имеющих высокую степень риска в отношении чувствительности к острому МИ, но их лечат ингибиторами ангиотензинпревращающего фермента, таким как каптоприл. Продолжительность таких исследований варьируется и зависит от достижения заранее определенного количества данных или первичных конечных результатов. Например, продолжительность такого исследования обычно может составлять по крайней мере 4 года, включая период регистрации, составляющий 18 месяцев, однако может быть и короче. Все данные и степень безопасности подвергаются мониторингу независимой группой наблюдателей, которые проводят анализ в определенные моменты времени в течение исследования.
Для того, чтобы удовлетворять критериям острого МИ (см. выше),
(1) все пациенты должны иметь увеличенную концентрацию в плазме сердечных ферментов, таких как общая креатинкиназа (КК), по крайней мере в 2 раза превышающую верхний предел нормального диапазона, или уровень КК-ММ, превышающий верхний предел нормального диапазона и составляющий по крайней мере 5% нормального уровня КК, и
(2) все пациенты должны иметь или типичные клинические симптомы и/или типичные изменения ЭКГ, например, включающие развитие ST-сегмента или изменения Т-волны при двух или большем количестве непрерывных ЭКГ-записей, или иметь развитие новой блокады ножки пучка Гиса.
Таким образом может быть доказано, что долговременное введение антагониста рецептора ангиотензина II может применяться для лечения острого МИ и для вторичной профилактики острого МИ.
Объектом изобретения является фармацевтическая композиция для лечения острого МИ и вторичной профилактики острого МИ, включающая антагонист AT1-рецептора или его фармацевтически приемлемую соль либо индивидуально, либо в сочетании с другими принятыми средствами лечения (действующими веществами) острой и хронической фаз МИ, такими как, например, ингибиторы АСЕ, бета-блокаторы, аспирин и т.д., предназначенная для лечения острого МИ, прежде всего для населения в целом (включая пациентов из группы высокого риска).
Предпочтительные другие принятые средства лечения (действующие вещества) острой и хронической фаз МИ, которые могут применяться в сочетании с антагонистами AT1-рецептора, являются ингибиторы АСЕ, представляющие собой (но не ограничиваясь ими) соединение из группы, включающей алацеприл, беназеприл, беназеприлат, каптоприл, церонаприл, цилазаприл, делаприл, эналаприл, эналаприлат, фосиноприл, имидаприл, лизиноприл, мовелтоприл, периндоприл, хинаприл, рамиприл, спираприл, темокаприл и трандолаприл.
Объектом изобретения является объединенная фармацевтическая композиция для одновременного, раздельного или последовательного введения при лечении острого МИ, а также для вторичной профилактики острого МИ, включающая блокатор АТ1-рецептора и другое принятое средство лечения острой и хронической фаз МИ, которое может применяться для такого лечения, например, выбранное из группы, включающей ингибитор АСЕ, бета-блокатор и аспирин, в каждом случае в виде стандартной дозируемой формы в смеси с фармацевтически приемлемым носителем.
Фармацевтическая композиция для лечения острого МИ и вторичной профилактики острого МИ, включающая блокатор АТ1-рецептора и другое принятое действующее вещество для лечения острой и хронической фаз инфаркта миокарда, например, выбранное из группы, включающей ингибитор АСЕ, бета-блокатор и аспирин или в каждом случае его фармацевтически приемлемую соль, в смеси с фармацевтически приемлемым носителем.
Наиболее неожиданным результатом являются экспериментальные данные о том, что объединенное введение приводит не только к благоприятному, прежде всего комплементарному и синергетическому терапевтическому действию, но также и к дополнительным благоприятным действиям, обусловленным объединенным лечением, таким как неожиданное увеличение длительности действия, более широкое разнообразие терапевтического лечения и неожиданные благоприятные воздействия на симптомы болезней и состояния, связанные с острым МИ.
Другие преимущества заключаются в том, что меньшие дозы отдельных лекарственных средств, которые следует объединять согласно настоящему изобретению, могут использоваться для снижения дозировки, это означает, например, что дозы часто могут быть не только уменьшены, но также и вводиться более редко, или это может использоваться для уменьшения случаев возникновения побочных действий. Это соответствует желаниям и требованиям подлежащих лечению пациентов.
Изобретение также относится к применению антагониста рецептора ангиотензина II или его фармацевтически приемлемой соли индивидуально или в сочетании с другими принятыми средствами лечения острой и хронической фаз МИ, такими как, например, ингибиторы АСЕ, бета-блокаторы и аспирин и т.д., для приготовления лекарственного средства, предназначенного для лечения острого МИ и для вторичной профилактики острого МИ, прежде всего у населения в целом (включая пациентов из группы высокого риска).
Кроме того, изобретение относится к способу лечения острого МИ и вторичной профилактики острого МИ прежде всего у населения в целом (включая пациентов из группы высокого риска), предусматривающему введение теплокровному животному, включая человека, терапевтически эффективного количества антагониста рецептора ангиотензина II или его фармацевтически приемлемой соли индивидуально или в сочетании с другими принятыми средствами лечения острой и хронической фаз МИ, такими как, например, ингибиторы АСЕ, бета-блокаторы и аспирин и т.д.
Изобретение относится также к применению антагониста рецептора ангиотензина II или его фармацевтически приемлемой соли индивидуально или в сочетании с другими принятыми средствами лечения острой и хронической фаз МИ, такими как, например, ингибиторы АСЕ, бета-блокаторы и аспирин и т.д., для лечения острого МИ, прежде всего у населения в целом (включая пациентов из группы высокого риска).
Антагонисты рецептора ангиотензина II включают соединения, имеющие различные структурные характеристики. Можно, например, отметить соединения, перечисленные в заявке на европейский патент №443983 (ЕР 443983), в частности, заявленные соединения, и конечные продукты в примерах получения; сущность данной заявки включена в настоящее описание путем ссылки на эту публикацию.
Предпочтительным является (S)-N-(1-карбокси-2-метилпроп-1-ил)-N-пентаноил-N-[2′(1Н-тетразол-5-ил)бифенил-4-илметил]амин[валсартан] формулы
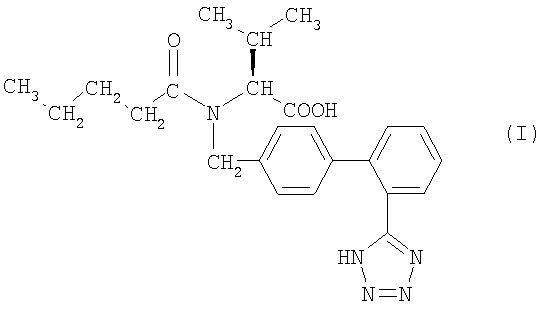
и его фармацевтически приемлемые соли.
Кроме того, соединения, указанные в заявке на европейский патент, опубликованной под номером 253310 (ЕР 253310), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [лосартан] следующей формулы
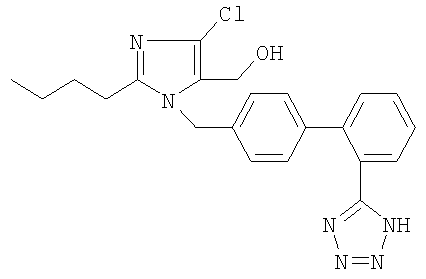
и его фармацевтически приемлемые соли.
Кроме того, следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 403159 (ЕР 403159), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [эпросартан] следующей формулы

и его фармацевтически приемлемые соли.
Также следует отметить соединения, указанные в заявке на патент РСТ, опубликованной под номером WO 91/14679, в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [ирбесартан] следующей формулы

и его фармацевтически приемлемые соли.
Кроме того, следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 420237 (ЕР 420237), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [Е-1477] следующей формулы
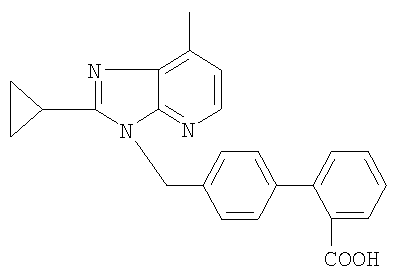
и его фармацевтически приемлемые соли.
Также следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 502314 (ЕР 502314), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [телмисартан] следующей формулы

и его фармацевтически приемлемые соли.
Кроме того, следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 459136 (ЕР 459136), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [кандесартан] следующей формулы

и его фармацевтически приемлемые соли.
Также следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 504888 (ЕР 504888), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [SC-52458] следующей формулы

и его фармацевтически приемлемые соли.
Кроме того, следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 514198 (ЕР 514198), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [саприсартан] следующей формулы

и его фармацевтически приемлемые соли.
Кроме того, следует отметить соединения, указанные в заявке на европейский патент, опубликованной под номером 475206 (ЕР 475206), в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение следующей формулы

и его фармацевтически приемлемые соли.
Также следует отметить соединения, указанные в заявке на патент РСТ, опубликованной под номером WO 93/20816, в частности, заявленные соединения и конечные продукты примеров получения, включенные в настоящее описание в качестве ссылки.
Предпочтительным является соединение [ZD-8731] следующей формулы
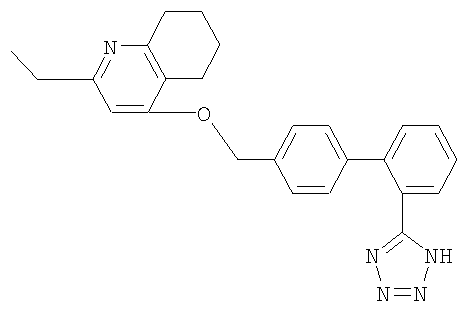
и его фармацевтически приемлемые соли.
Антагонисты рецептора ангиотензина II, которые, например, несут по меньшей мере один основный центр, могут образовывать кислотно-аддитивные соли. Они могут быть получены, например, с сильными неорганическими кислотами, такими как минеральные кислоты, например серная кислота, фосфорная кислота или галогенводородная кислота, с сильными органическими карбоновыми кислотами, такими как С1-С4алканкарбоновые кислоты, которые могут быть не замещены или замещены, например, галогеном, например уксусная кислота, такими как насыщенные или ненасыщенные дикарбоновые кислоты, например щавелевая, малоновая, янтарная, малеиновая, фумаровая, фталевая или терефталевая кислота, такими как гидроксикарбоновые кислоты, например аскорбиновая, гликолевая, молочная, яблочная, винная или лимонная кислота, такими как аминокислоты, например аспарагиновая или глутаминовая кислота, или такой как бензойная кислота, или с использованием органических сульфоновых кислот, таких как С1-С4алкансульфоновые кислоты или арилсульфоновые кислоты, которые могут быть не замещены или замещены, например, галогеном, например метансульфоновая кислота или пара-толуолсульфоновая кислота. Примерами приемлемых солей с основаниями являются соли металлов, например соли щелочных металлов или соли щелочноземельных металлов, например соли натрия, калия или магния, или соли с аммиаком или органическим амином, таким как морфолин, тиоморфолин, пиперидин, пирролидин, моно-, ди- или три(низш.)алкиламин, например этил-, трет-бутил-, диэтил-, диизопропил-, триэтил-, трибутил- или диметилпропиламины, или моно-, ди- или тригидрокси(низш.)алкиламин, например моно-, ди- или триэтаноламин. Кроме того, могут быть получены соответствующие внутренние соли.
Фармацевтические композиции предназначены для энтерального, например перорального, а также ректального или парентерального введения теплокровным животным, причем композиции содержат фармакологически активное соединение либо индивидуально, либо в сочетании с общепринятыми фармацевтическими вспомогательными веществами. Например, фармацевтические композиции содержат от примерно 0,1% до 100%, предпочтительно от примерно 1% до примерно 80% действующего вещества. Фармацевтические композиции для энтерального или парентерального введения, а также для введения в глаз, представляют собой например, стандартные дозы, такие как филмтаблетки, таблетки, капсулы или суппозитории, а также ампулы. Их приготавливают хорошо известными методами, например с помощью обычных процессов смешения, грануляции, нанесения покрытия, солюбилизации или лиофилизации. Так, фармацевтические композиции для перорального введения могут быть приготовлены путем объединения действующего вещества с твердыми эксципиентами, если требуется грануляция полученной смеси и, если целесообразно или необходимо, путем обработки смеси или гранулята после добавления приемлемых вспомогательных веществ с получением таблеток или ядер филмтаблеток.
Доза действующего вещества может зависеть от многочисленных факторов, таких как путь введения, вид теплокровного животного, возраст и/или индивидуальное состояние. Как правило, в случае перорального введения приблизительная суточная доза составляет от примерно 10 мг до примерно 360 мг, например в случае валсартана, для введения пациенту рекомендуется доза примерно 40 мг, 80 мг, 160 мг или 320 мг.
Предпочтительным антагонистом рецептора ангиотензина II является валсартан. Валсартан может вводиться в виде приемлемой стандартной дозы, например капсулы или таблетки, которая включает терапевтически эффективное количество, например от примерно 20 до примерно 320 мг валсартана, и может вводиться пациентам, нуждающимся в таком лечении, для вторичной профилактики состояния после перенесенного МИ. Введение действующего вещества может осуществляться трижды в день, начиная, например, с суточной дозы 20 мг или 40 мг валсартана, которая повышается до 80 мг в сутки, а затем до 160 мг в сутки и вплоть до 320 мг в сутки. Предпочтительно валсартан вводят дважды в день в дозе, каждая из которых составляет 80 мг или 160 мг соответственно. Соответствующие дозы могут вводиться, например, утром, днем или вечером. Предпочтительным является введение дважды в день.
Предпочтительными дозами для фармацевтических композиций являются терапевтически эффективные дозы, особенно те, которые содержатся в поступающих в продажу лекарственных средствах. Особенно предпочтительными являются комбинации с низкими дозами. В случае ингибиторов АСЕ, предпочтительными стандартными дозируемыми формами ингибиторов АСЕ являются, например, таблетки или капсулы, включающие, например, от примерно 5 мг до примерно 20 мг, предпочтительно 5 мг, 10 мг или 20 мг беназеприла; от примерно 6,5 мг до 100 мг, предпочтительно 6,25 мг, 12,5 мг, 25 мг, 50 мг, 75 мг или 100 мг каптоприла; от примерно 2,5 мг до примерно 20 мг, предпочтительно 2,5 мг, 5 мг, 10 мг или 20 мг эналаприла; от примерно 10 мг до примерно 20 мг, предпочтительно 10 мг или 20 мг фосиноприла; от примерно 2,5 мг до примерно 4 мг, предпочтительно 2 мг или 4 мг периндоприла; от примерно 5 мг до примерно 20 мг, предпочтительно 5 мг, 10 мг или 20 мг хинаприла; или от примерно 1,25 мг до примерно 5 мг, предпочтительно 1,25 мг, 2,5 мг или 5 мг рамиприла. Предпочтительным является введение трижды в день.
Приведенные ниже примеры иллюстрируют описанное выше изобретение; однако они никоим образом на направлены на ограничение его объема.
Пример 1 композиции.
Филмтаблетки:
Филмтаблетки изготавливают, например, следующим образом.
Смесь, содержащую валсартан, микрокристаллическую целлюлозу, кросповидон, часть коллоидного безводного диоксида кремния/коллоидного диоксида кремния/Aerosil 200, диоксид кремния и стеарат магния, предварительно смешивают в диффузионном смесителе и затем просеивают через мельницу с ситами. Образовавшуюся смесь вновь предварительно смешивают в диффузионном смесителе, уплотняют в вальцовом уплотнителе и затем просеивают через мельницу с ситами. К образовавшейся смеси добавляют оставшуюся часть коллоидного безводного диоксида кремния/коллоидного диоксида кремния/Aerosil 200 и готовят окончательную смесь в диффузионном смесителе. Всю смесь прессуют на роторной таблетирующей машине и на таблетки наносят пленочное покрытие в перфорированном чане, используя светло-красный краситель Diolack.
Пример 2 композиции.
Филмтаблетки:
Филмтаблетки изготавливают, например, согласно процессу, описанному в примере 1 композиции.
Пример 3 композиции.
Филмтаблетки:
Состав Opadry®:
Филмтаблетки изготавливают, например, согласно процессу, описанному в примере 1 композиции.
Пример 4 композиции.
Капсулы:
Таблетку изготавливают следующим образом:
Грануляция/сушка
Валсартан и микрокристаллическую целлюлозу гранулируют распылением в грануляторе с псевдоожиженным слоем с использованием раствора для грануляции, который содержит повидон и лаурилсульфат натрия, растворенные в очищенной воде. Полученный гранулят сушат в сушилке с псевдоожиженным слоем.
Измельчение/смешение
Высушенный гранулят измельчают вместе с кросповидоном и стеаратом магния. Затем массу перемешивают в коническом смесителе шнекового типа в течение примерно 10 мин.
Капсулирование
Пустые желатиновые капсулы с твердым покрытием заполняют перемешенной порцией гранул при контролируемой температуре и влажности. Заполненные капсулы обеспыливают, визуально обследуют, осуществляют проверку массы и сертифицируют в Департаменте гарантии качества.
Пример 5 композиции.
Капсулы:
Композицию изготавливают, например, согласно процессу, описанному в примере 4 композиции.
Пример 6 композиции.
Желатиновая капсула с твердым покрытием:
Пример 7 композиции.
Желатиновая капсула с твердым покрытием, содержащая в качестве действующего вещества, например, (S)-N-(1-карбокси-2-метилпроп-1-ил)-N-пентаноил-Н-[2′(1Н-тетразол-5-ил)бифенил-4-илметил]амин, может быть приготовлена, например, следующим образом:
Композиция:
Компоненты (1) и (2) гранулируют с раствором компонентов (3) и (4) в воде. Компоненты (5) и (6) добавляют к сухому грануляту и смесью заполняют желатиновые капсулы с твердым покрытием размера 1.
Предложено применение валсартана или его фармацевтически приемлемой соли в комбинации с другим приемлемым действующим веществом, выбранным из группы, включающей алацеприл, беназеприл, беназеприлат, каптоприл, церонаприл, силазаприл, делаприл, эналаприл, эналаприлат, фосиноприл, имидаприл, лизиноприл, мовелтоприл, периндоприл, хинаприл, рамиприл, спираприл, темокаприл и трандолаприл для приготовления лекарственного средства для лечения острого инфаркта миокарда. Показано снижение смертности больных в результате сочетанного применения валсартана с каптоприлом по сравнению с самостоятельным приемом валсартана или каптоприла. 2 з.п. ф-лы, 6 табл.
| Реферат АБД Medline: Di Pasquale P et al Safety, tolerability, and neurohormonal changes of the combination captopril plus losartan in the early postinfarction period: a pilot study | |||
| Cardiovasc Drug Ther | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| реферат из АБД Medline: Taylor К et al Divergent effects of | |||
Авторы
Даты
2009-02-10—Публикация
2006-10-05—Подача