ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к защитному изделию для ран, которое включает в себя вещество, которое препятствует росту бактерий в ранах. Изобретение также относится к способу производства защитного изделия для ран. Изобретение, кроме того, относится к использованию в защитных изделиях для ран вещества, которое ингибирует рост бактерий в ранах. Дополнительно изобретение относится к использованию вещества для получения композиции, которая обладает эффектом, препятствующим росту бактерий в ранах.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Защитные изделия для ран существуют во многих различных формах, таких как мази, пасты, перевязочные материалы, пластыри и бактериостатические агенты.
Процесс заживления ран можно в принципе разделить на три стадии. Сначала рану от всего очищают, после чего ткань регенерируется, далее ткань стабилизируется в течение завершающей стадии созревания и становится менее хрупкой и более эластичной.
В течение стадии регенерации капилляры, фибробласты и эпителий растут в области раны и синтезируют новую ткань. Регенерированная ткань является очень хрупкой и чувствительной к внешним воздействиям. При обработке ран в течение процесса заживления используются перевязочные материалы некоторого типа. Перевязочные материалы, которые используются в течение чувствительной фазы регенерации, должны быть сконструированы так, чтобы они не попадали в рану и были гибкими, и их контактная поверхность с раной должна быть мягкой. Перевязочные материалы также должны быть способны абсорбировать избыток секрета из ран или позволять секрету из ран проходить насквозь в абсорбционную часть, которая располагается над перевязочным материалом или которая включается в перевязочный материал.
Примерами перевязочных материалов, которые используются на ранах на стадии регенерации, являются насыщенные мазями компрессы, составленные из марлевой или нейлоновой ткани, в комбинации, где приемлемо, с адсорбентной основной частью. В то время как эти перевязочные материалы имеют меньшую тенденцию попадать в рану, чем традиционные волокнистые перевязочные материалы, они, тем не менее, имеют ряд недостатков, например они часто попадаются в рану, несмотря на пропитывание, и вызывают повреждение ткани.
Патент ЕР 0261167 В1 описывает перевязочный материал, который является заметно лучшим. Этот патент относится к перевязочному материалу для гнойных ран, который включает в себя гидрофобный слой, который непосредственно контактирует с раной в течение использования и который является проницаемым для жидкости. Этот перевязочный материал отличается тем, что гидрофобный слой состоит из мягкого и эластичного геля, предпочтительно в форме силиконового геля, который нанесен на сетеподобном элементе жесткости, огораживающем все сеточные части, но оставляющем сквозные отверстия. Перевязочный материал этого типа на самом деле устраняет проблему прилипания в ране.
Другая проблема, которая может влиять на заживление ран и делает это невозможным, является присутствие или рост бактерий в области раны. Присутствие обширного ряда бактерий может также привести к запаху, который может составить социальное препятствие и трудноизлечимую болезнь. Поверхность раны может также составлять точку входа для более серьезных системных инфекций, которые требуют госпитализации и относительно длительного периода выздоровления и в некоторых случаях могут привести к смерти.
Некоторые из видов бактерий, которые найдены в ранах, трудно обрабатываются антибиотиками. Обработка еще более затрудняется фактом, что интенсивное и продолжительное воздействие антибиотиков, которому пациенты с раневыми инфекциями часто подвергаются, приводит к стойким штаммам. Эти стойкие ко многим воздействиям раневые бактерии, которые представляют серьезную угрозу в последние годы и приводят к явным клиническим проблемам, включают стойкий к метициллину Staphylococcus aureus (MRSA), стойкий к ванкоцину enterococci (VRE) и полностью стойкий Pseudomonas aeruginosa.
Пациенты, страдающие от диабета, являются группой, которая является очень уязвимой с точки зрения раневых инфекций. Количество больных диабетом постоянно увеличивается, причем это характерно для обширных областей в мире. В целом, заболевание ослабляет способность тела защищать себя от инфекций, и изменения в касательном восприятии и кровообращении приводят к тому, что раны легче возникают. Кроме того, более высокое содержание глюкозы в крови и тканях создает благоприятную основу для большинства бактерий. Бета-гемолитический стрептококк составляет группу бактерий, которые особенно развиваются благодаря хорошему доступу к сахару. Стрептококки генетически очень хорошо приспособлены по отношению к понижающим сахар ферментам и область их обитания, следовательно, располагается во рту, где содержание сахара является самым высоким. Эти бактерии также охотно дают начало инфекциям для диабетиков, которые являются относительно тяжелыми. Это также относится к стрептококкам группы В, которые обычно являются бактериями с относительно низкой вирулентностью для взрослых людей. Хронические раны ступней и ног являются особенной проблемой для диабетиков, причем требуется широкий спектр антибиотиков и относительно длительные периоды времени, чтобы избежать ампутации. Существует большой риск этой группы, требующей способа защиты, способствующего развитию сопротивления и уменьшающего временной интервал после периода антибиотиков. Поэтому для этих пациентов есть очень большая необходимость в альтернативных формах лечения.
Как очевидно из приведенных выше примеров, проблемы, включающие лечение инфекций ран, не уменьшаются, но в некоторой степени усиливаются, несмотря на новые и улучшенные защитные изделия для ран и способы лечения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение приводит и защитному изделию для ран, использование которого значительно улучшает возможность лечения инфицированных ран.
В соответствии с изобретением защитное изделие для ран, которое является изделием типа, упомянутого в начале, и которое включает в себя вещество, которое ингибирует рост бактерий в ранах, отличается тем, что вещество является ксилитом.
В соответствии с одним воплощением изобретение отличается тем, что указанное защитное изделие для ран включает в себя гель, в который вводят ксилит. В соответствии с модифицированным воплощением изобретение отличается в этой связи тем, что указанный гель является силиконовым гелем.
В соответствии с другим воплощением изобретение отличается тем, что защитное изделие для ран состоит или включает в себя слой, который непосредственно контактирует с раной в течение использования и который является непроницаемым для жидкости раны за счет того, что слой состоит из геля и сетеподобного элемента жесткости, при этом гель наносят, окружая все сеточные части, но оставляя сквозные отверстия в слое, образованном гелем и элементом жесткости, и при этом ксилит введен в гель. В соответствии с одним воплощением изобретение отличается в этой связи тем, что указанный слой является гидрофобным и не адгезирует к гнойным ранам. В соответствии с одним воплощением гель является силиконовым гелем.
В соответствии с другим воплощением изобретение отличается тем, что защитное изделие для ран включает в себя перевязочный материал и тем, что ксилит наносят на подложку, которая включается в этот перевязочный материал. В соответствии с одним воплощением указанная подложка является марлей. В соответствии с другим воплощением подложка является нетканой тканью.
В соответствии с другим воплощением подложка является полимерной пеной, обладающей открытыми порами. В соответствии с другим воплощением подложка является водорастворимой полимерной пеной.
В соответствии с другим воплощением указанное защитное изделие для ран представлено в форме перевязочного материала и отличается тем, что указанный перевязочный материал содержит абсорбционный слой для приема выделяемой из раны жидкости.
В соответствии с одним воплощением способа производства защитного изделия для ран изобретение отличается тем, что ксилит наносят на подложку в форме раствора. В соответствии с одним воплощением указанного способа подложку затем высушивают.
Изобретение также относится к применению в защитных изделиях для ран вещества, которое ингибирует рост бактерий в ранах. В соответствии с изобретением это применение принципиально отличается тем, что указанное вещество является ксилитом. В соответствии с одним воплощением применения указанное вещество находится в порошковой форме. В соответствии с другим воплощением использования указанное вещество включается в гель. В соответствии с другим воплощением применения указанное вещество включается в жидкий раствор. В соответствии с другим воплощением применения указанное вещество включается в мазь. В соответствии с еще одним воплощением применения указанное вещество включается в пасту.
Изобретение также относится к перевязочному материалу для ран в форме пластыря, содержащего вещество, ингибирующее рост бактерий в ранах. В этой связи изобретение отличается тем, что указанное вещество является ксилитом.
В соответствии с другим воплощением изобретение состоит в применении ксилита для получения композиции, которая имеет эффект ингибирования роста бактерий в ранах.
В соответствии с одним воплощением это применение отличается тем, что указанная композиция включает в себя жидкий раствор, который содержит ксилит.
В соответствии с одним воплощением защитное изделие для ран является стерильным во всей своей полноте и пакуется стерильным способом.
Как является очевидным из приведенного выше, сущность изобретения заключается в применении ксилита для ингибирования роста бактерий, которые присутствуют в ранах.
Ксилит (березовый сахар) является природным углеводом, который встречается в свободной форме и в небольших количествах, в особенности в растительных частях на деревьях, овощах и фруктах и, в частности, участвует в переходном обмене веществ человека. Ксилит известен в органической химии, по меньшей мере, с 1890 годов. Немецкие и французские исследователи были первыми, кто получил ксилит химическим способом более чем 100 лет назад. Окончательно ксилит был охарактеризован и очищен в течение 1930-х годов. Кроме того, что ксилит имеет относительно длинную историю с химической точки зрения, его рассматривали в течение долгого времени как один из нескольких сладких углеводов. Однако отсутствие сахара в течение второй мировой войны в ряде стран увеличило интерес к ксилиту. Это было до тех пор, пока исследователи не изучили его природу независимости к инсулину, так что его биологические свойства стали понятны, и до 1970-х годов ксилит использовался в ряде стран, как подслащивающее вещество для диабетиков в связи с парентеральным питанием, т.е. питанием, даваемым прямо через кровяные сосуды или в связи с лечением инсулиновой комы. Использование ксилита в связи со стоматологией началось только в течение 1970-х годов, и первую содержащую ксилит жевательную резинку для борьбы с кариесом выпустили в Финляндии в 1975 г.
Ксилит является сахарным пятиатомным спиртом (СН2ОН(СНОН)3СН2ОН), имеющим пять атомов углерода и пять гидроксильных групп. Следовательно, его можно обозначить как пентитол. Ксилит принадлежит к полимерным спиртам (полиолам), которые не являются сахарами в буквальном смысле. Однако биохимически они относятся к сахарам благодаря тому факту, что они производятся их сахаров и могут в них преобразоваться. Кроме того, некоторые химические ссылочные работы определяют сахара как кристаллические сладкие углеводы, которые являются категорией, которая охватывает ксилит.
Никакие мутагенные свойства, т.е. увеличение частоты природной мутации, не обнаружены, когда этот сахарный спирт использовали в бактериологических испытаниях (Batzinger et al.; Saccharin and other sweeteners: mutagenic properties. Science 1977; 198:944-946). Кроме того, ряд национальных и интернациональных крупных специалистов оценили его токсичность настолько низкую, что нет предельного значения для допустимого ежедневного приема внутрь (Mäkinen; Dietary prevention of dental caries by xylitol - clinical effectiveness and safety; J. Appl. Nutr. 1992; 44:16-28).
Бактериальным эффектом, который был первым и в первую очередь изученным и документированным, является зубной эффект, который в большой степени является эффектом структуры этого соединения. Наиболее диетическими полиолами являются гекситолы. С точки зрения эволюции не является, следовательно, преимуществом для бактерий разрушать что-нибудь другое, чем гекситолы. По этой причине большинство бактерий не располагают ферментативным аппаратом для использования пентитолов для их роста.
Поэтому добавление ксилита (1-10%) к питательной среде уменьшает рост бактерий, которые наиболее часто находят в соединении с раневыми инфекциями, т.е. S. aureus (включая MRSA), стрептококками группы А, В, С и G, энтерококками (включая VRE) и Pseudomonas aeruginosa, при коэффициенте до приблизительно 1000, как показано экспериментами авторов, которые описываются более подробно ниже. Эти результаты не зависят от стойкости бактерий к антибиотикам.
Рост альфа-стрептококка в ротовой области сдерживается тем фактом, что ксилит удаляется в виде системы фосфотрансферазы и фруктозы. Сахарный спирт накапливается в бактериях без возможности разрушиться и может быть сразу токсичным (Trahan et al. Transport and phosphorylation of xylitol by a fructose phosphotransferase system in Streptococcus mutans. Caries Res. 1985; 19:53-63); однако если накапливается фруктоза, ситуация нормализуется, т.е. тогда существует сравнительная конкурентоспособность (Tapiainen et al. Effect of xylitol on growth of Streptococcus pneumoniae in presence of fructose and sorbitol). Эта конкурентоспособность не является равно очевидной для самых распространенных раневых бактерий. Следовательно, ксилит может служить препятствием с различными функциями в случае этих микроорганизмов.
Кроме влияния на рост потребление ксилита также влияет на синтез протеина в альфа-стрептококке (Hrimech et al. Xylitol disturbs protein synthesis, including the expression of HSP-70 and HSP-60, in Streptococcus mutans. Oral Microbiol. Immunol. 2000; 15:249-257). Кроме других эффектов видоизменяется получение нагруженных протеинов, которые требуются для способности бактерий приспосабливаться к неблагоприятному окружению. Это увеличивает уязвимость бактерий.
Снижение получения гликокаликса, сахарного вещества, которое увеличивает адгезивную способность бактерий по отношению тканей раны и колонизировать на ней, продемонстрировано на S.aureus (Akiyama et al. Actions of farnesol and xylitol against Staphylococcus aureus. Chemotherapy 2002; 48:122-128). Факт, что ксилит снижает адгезию бактерий, также продемонстрирован в случае интестинальных бактерий, которые вызывают диарею, и бактерий, которые дают начало ушным воспалениям и в случае дрожжевого грибка (Naaber et al. Inhibition of adhesion of Clostridium difficile to Caco-2-cells. FEMS Immunol. Med. Microbiol. 1966; 14:205-209. Kontiokari et al. Antiadhesive effects of xylitol on otopathogenic bacteria. J. Antimicrob. Chemother. 1998; 41:563-565. Pizzo et al. Effect of dietary carbohydrates on the in vitro epithelial adhesion of Candida albicans, Candida tropicalis, and Candida krusei. New Microbiol. 2000; 31:63-71).
Адгезия и колонизация представляют первую фазу для бактерий в процессе инфицирования и, следовательно, имеют большое значение для частоты инфицирования. Клиническое изучение, в котором ксилит уменьшает количество ушных воспалений у детей до 40%, показывает, как важно это может быть (Uhari et al. Xylitol in preventing acute otitis media. Vaccine 2000; 19 Suppl. Pp 144-147).
В то время как интестинальные бактерии обнаружили первыми и самыми главными в связи с хроническими, а не острыми раневыми инфекциями, их значение в раневых инфекциях не является ясным. Некоторые интестинальные бактерии могут разрушать ксилит, в то время как другие должны видоизменяться, чтобы получить это свойство. Мутации часто происходят с определенной жертвой. Или бактерии могут только разрушать ксилит в течение сравнительно короткого периода времени, или бактерии вырастают менее хорошо в своем нормальном окружении, когда удаляется сахарный спирт (Scangos et al. Acquisition of ability to utilize xylitol: disadvantages of a constitutive catabolic pathway in Escherichia coli. J. Bacteriol. 1978; 134:501-505. Inderlied et al. Growth of Klebsiella aerogenes on xylitol: implications for bacterial enzyme evolution. J. Mol. Evol. 1977; 9:181-190).
Однако в случае ротовых бактерий существует риск выбрать стойкие к ксилиту штаммы (Hrimech et al. 2000), когда ксилит используется в течение длительного периода. Однако этот тип бактерий редко включается в раневые инфекции на ногах или стопах.
Ксилит только абсорбируется в очень легкой степени эпительными клетками на коже и если не абсорбируется, он экстрагирует жидкость благодаря своей гиперосмолярной природе. Это не влияет на активность эндогенных веществ, таких как дефенсины, которые обладают антибактериальными свойствами (Zabner et al. The osmolyte xylitol reduces the salt concentration of airway surface liquid and may enhance bacterial killing. Proc. Natl. acad. Sci. USA 2002; 97:11614-11619).
Высокая эндотермичность нагрева ксилита в растворе предоставляет его с охлаждающим восприятием при контакте со слизистыми оболочками или кожей. Ксилит также может образовать комплексы с кальцием и другими поливалентными катионами. Возможно, что эти комплексы вносят вклад в усиление абсорбции кальция и могут внести вклад в реминерализацию в областях некроза костей, осложнение, которое не является совсем необычным в связи с глубокими ранами ног и ступней. Подобно другим сахарным спиртам ксилит обладает эффектом стабилизации протеина в результате предохранения протеинов в водном растворе от денатурации, структурного изменения и другого повреждения, которое, иногда, может быть важным в связи с заживлением ран.
Как очевидно из приведенного выше, с 1970-х годов написано большое количество работ о биологических свойствах ксилита с главным акцентом, приходящимся на дентальный контекст.
Несмотря на все исследования и все, что документировано по отношению к ксилиту за несколько десятилетий, ни одно до настоящего изобретения не объясняет или понимает факт, что ксилит имеет большой потенциал в контексте ран и может составлять мощное средство для борьбы с присутствием и ростом разновидностей бактерий, которые являются наиболее частыми и опасными в связи с инфекциями ран, и что для данной цели можно получить подходящие защитные изделия для ран. В отличие от использования антисептиков и токсичных ионов металлов это происходит без какого-либо риска развития бактерий, которые являются стойкими ко многим антибиотикам, или имеется любой губительный эффект на ткань. Также нет риска экологических нарушений или аллергических реакций, как в случае систематического использования и локального использования соответственно антибиотиков.
Ксилит может успешно применяться во многих ситуациях в связи с инфекциями ран, где ранее известные защитные изделия для ран и способы лечения не имели эффекта или производили неблагоприятный эффект. Как будет очевидно из следующего описания, наши эксперименты показали, что ксилит является эффективным в борьбе с ростом MRSA, VRE и Pseudomonas aeruginosa, бактерии которых вызывают трудноизлечимые инфекции, включающие высокие затраты на медицинское лечение и длительные сроки изоляции. Кроме того, наши эксперименты показывают, что ксилит также является эффективным против бета-гемолитического стрептококка, включая стрептококк группы В, которые ранее являлись частой причиной относительно тяжелых и инвазивных инфекций в связи с диабетическими ранами.
Как упомянуто выше, биологические эффекты ксилита также естественно хорошо документируются без проявления возможных любых негативных эффектов.
ОПИСАНИЕ ФИГУР
Частью, которая следует далее, изобретение будет объясняться со ссылкой на осуществленные испытания, которые показаны на прилагаемых чертежах:
Фиг.1 иллюстрирует в диаграммной форме рост S. Aureus в питательной среде без добавления ксилита и, соответственно, с добавлением его с различным содержанием.
Фиг.2 иллюстрирует в диаграммной форме рост S. Aureus (очень стойкого) в питательной среде без добавления ксилита и, соответственно, с добавлением его с различным содержанием.
Фиг.3 иллюстрирует в диаграммной форме рост стрептококка группы В в питательной среде без добавления ксилита и, соответственно, с добавлением его с различным содержанием.
Фиг.4 иллюстрирует в диаграммной форме рост стрептококка группы G в питательной среде без добавления ксилита и, соответственно, с добавлением его с различным содержанием.
Фиг.5 иллюстрирует в диаграммной форме рост P. Aeruginosa в питательной среде без добавления ксилита и, соответственно, с добавлением его с различным содержанием.
ВОПЛОЩЕНИЯ
Как очевидно из прилагаемых чертежей, выполненные испытания демонстрируют исключительно хороший эффект в отношении ингибирования роста распространенных бактериальных видов, которые найдены в ранах.
Эксперименты проводились следующим образом.
Штаммы бактерий хранили при -70°С. Сразу же перед каждым экспериментом данные штаммы вытаскивали и помещали на чашку с кровью и выдерживали всю ночь при 35°С. Во всех экспериментах использовали тот же самый инкубатор. После этого петлю колоний, которая выросла, выдерживали в сердце-мозговом бульоне (BHI) в течение 18 часов. 100 мкл данного бульона прививали на 3-5 мл свежего бульона BHI с добавлением ксилита или без него. Добавляли различные содержания ксилита. Как очевидно из фиг.1-5, содержания ксилита были 1%, 2,5%, 5% и 10%.
Коэффициент пропускания или полупрозрачность измеряли от часа 0 и далее через каждый час в течение 6 часов на Biolog мутномере от компании Biolog Inc., Hayward, CA, USA. Рост бактерий снижает полупрозрачность, т.е. чем ниже коэффициент пропускания, тем выше рост бактерий.
В начале и через 6 часов 100 мкл бульона культивировали и подсчитывали количество живых бактерий. Затем сравнивали значение коэффициента пропускания и количество бактерий (колониеобразующие единицы/мл) в пробирках с ксилитом и без него.
На графике, показанном на фиг.1, можно видеть, что полупрозрачность бактерий S. Aureus, т.е. которые называются больничными бактериями, в BHI без добавления ксилита постепенно уменьшалась от 100 при времени в точке 0 до 20 при времени в точке 6 часов, показывающем, что бактерии росли очень сильно.
На том же графике можно видеть, что полупрозрачность составляет все еще больше, чем 60%, после 6 часов в питательном растворе, к которому добавили 10% ксилита, что показывает, что рост бактерий очень сильно ослабился по сравнению с раствором без ксилита. Более того, как очевидно из кривой для BHI, содержащей 10% добавленного ксилита, едва ли какой-либо бактериальный рост совсем происходит через 2 часа.
График на фиг.2 показывает кривые, где вариант Staphylococcus aureus использовался с добавлением ксилита или без него. Бактерия, показанная на фиг.2, является штаммом MRSA, проявляющим очень высокую степень стойкости, и где только один или два типа антибиотика являются возможными альтернативами лечения. Данные лекарственные препараты стоят более чем 1000 SEK на день по сравнению с обычными ценами порядка 55-70 SEK на день. Кроме того, сверхустойчивость приводит к тому, что о пациентах, инфицированных MRSA, следует заботиться в отдельных помещениях со специальными гигиеническими распоряжениями и не позволять двигаться самим в госпитале. Это, естественно, очень дорого и мучительно для пациентов.
Как очевидно из фиг.2, добавление ксилита к питательному раствору, содержащему бактерии, приводит к тому, что рост бактерий в растворе ингибируется очень эффективно. Рост сдерживается в увеличивающейся степени по мере того, как увеличивается количество добавляемого ксилита. Через 6 часов полупрозрачность в присутствии 10% добавленного ксилита составляет более чем 70%, в то время как полупрозрачность для раствора без какого-либо добавления ксилита составляет только приблизительно 30%. На фиг.2 не измерялись значения после 2 часов.
Фиг.3 показывает график, соответствующий графикам, показанным на фиг.1 и 2, но в этом случае для стрептококка группы В. Данный тип бактерий обычно находят в тяжелых диабетических ранах, в особенности ранах на ногах и ступнях, которые вызывают риск угрожающих жизни инфекций и некроза костей.
Как можно видеть на фиг.3, рост данных бактерий можно эффективно ингибировать добавлением ксилита.
Соответствующим способом, как и на фиг.1-3, фиг.4 и 5 показывают две дополнительные бактерии, т.е. стрептококк группы G и P. aeruginosa, которые найдены в ранах. Как показывают данные графики, ксилит является также очень эффективным для ингибирования роста данных бактериальных штаммов.
В соответствии с изобретение защитные изделия для ран, включающие в себя ксилит, можно изготовить различными способами.
Один способ заключается в добавлении ксилита в порошковой форме к силиконовому гелю. Данный гель является химически сшитым силиконовым гелем (полидиметилсилоксановым гелем), например двухкомпонентным, дополнительно вулканизуемым при комнатной температуре с платиновым катализатором силиконом (RTV). Примерами гелей, которые можно использовать, являются SiGel от Wacker-Chemie GmbH, Burghausen, Germany и MED-6430 от NuSil Technology, Carpinteria, USA. Примеры самоклеящихся гелей также описываются в GB-A-2192142, GB-A-2226780 и ЕР-А1-0300620. Также возможны другие гидрофобные гели, такие как гидрофобные полиуретановые гели.
В соответствии с одним воплощением ксилит в порошковой форме можно добавлять к жидкому силикону вышеупомянутых типов и смешивать с ним. После чего данную смесь адгезионно вулканизуют для сшивания полимерной сетки при температуре 90-130°С. Силиконовый гель, содержащий ксилит, можно использовать в качестве защитного изделия для ран, особенно в комбинации с внешним перевязочным материалом для ран.
Ксилит является коммерчески доступным в порошковой форме, приблизительно такого же размера частиц, как гранулированный сахар. В соответствии с одним воплощением порошковый ксилит можно размолоть так, чтобы получить порошок с более мелкими частицами, обладающими более высокой удельной поверхностью. Смешивание с силиконом приводит к увеличению действующей поверхности и это увеличит выделение ксилита из силиконового геля, содержащего ксилит, по сравнению с тем же силиконовым гелем и ксилитом, обладающим более крупным размером частиц. Размер частиц ксилита можно таким образом использовать для изменения скорости выделения из силиконового геля, содержащего ксилит.
Альтернативно ксилит можно сначала растворить в воде; после чего получают суспензию силикона и раствора ксилита с последующей вулканизацией суспензии.
Силиконовый гель, содержащий ксилит в форме частиц или добавленный в раствор, можно использовать для получения защитного изделия для ран, которое включает в себя слой, который контактирует с раной непосредственно в период использования, который является проницаемым для жидкости раны и который включает указанный силиконовый гель, содержащий ксилит и сетеподобный элемент жесткости. Наносят гель так, чтобы он закрыл все части сетки, но оставил сквозные отверстия на слое, образованном гелем и элементом жесткости. Перевязочный материал, который является материалом данного типа, но который не содержит ксилит, описывается в патенте авторов ЕР 0261167В1, полное содержание которого включено в качестве ссылки в данное описание.
Изобретение не ограничивается описанными выше воплощениями и возможен ряд модификаций в рамках объема притязаний последующей формулы изобретения.
Например, перевязочный материал может содержать ксилит в растворе или в форме частиц, который наносят или вводят в подложку, такую как полимерная пена, обладающая открытыми порами. Примером является полиуретановая пена типа Hypol® от Hampshire Chemical Corporation, Lexington, Massachusetts, USA.
Другими примерами подложек являются марля, термоплавкий адгезив и нетканая ткань.
Защитное изделие для ран полностью стерилизуют и упаковывают стерильным образом.
Изобретение относится к медицине. Описано защитное изделие для ран, которое включает в себя вещество, которое ингибирует рост бактерий в ранах. Изобретение характеризуется тем, что вещество является ксилитом. Изобретение также относится к применению ксилита в защитных изделиях для ран и к применению ксилита для получения композиции, которая обладает эффектом ингибирования роста бактерий в ранах. Изобретение, кроме того, относится к способу производства защитных изделий для ран, которые содержат ксилит. Изделие для ран значительно улучшает возможность лечения инфицированных ран. 5 н. и 33 з.п. ф-лы, 5 ил.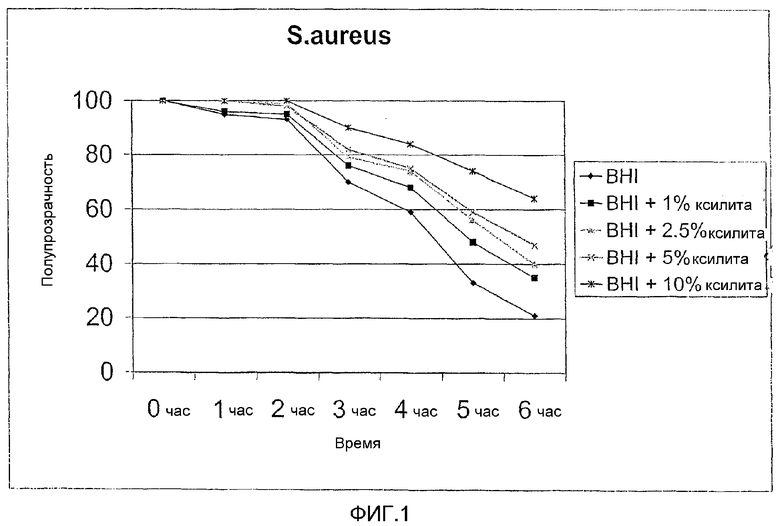
1. Защитное изделие для ран, включающее в себя вещество, которое ингибирует рост бактерий в ранах, отличающееся тем, что вещество является ксилитом.
2. Защитное изделие для ран по п.1, отличающееся тем, что указанное защитное изделие для ран включает в себя мазь, которая содержит ксилит.
3. Защитное изделие для ран по п.1, отличающееся тем, что указанное защитное изделие для ран включает в себя порошок, который содержит ксилит.
4. Защитное изделие для ран по п.1, отличающееся тем, что указанное защитное изделие для ран включает в себя гель, в который ввели ксилит.
5. Защитное изделие для ран по п.4, отличающееся тем, что указанный гель является силиконовым гелем.
6. Защитное изделие для ран по любому из пп.4 и 5, отличающееся тем, что ксилит введен в гель в кристаллической форме.
7. Защитное изделие для ран по п.1, отличающееся тем, что указанное защитное изделие для ран содержит полимерную пену, в которую ксилит введен в водном растворе, в соединении с которым образована полимерная пена.
8. Защитное изделие для ран по п.1, отличающееся тем, что указанное защитное изделие для ран содержит полимерную пену, в которую ксилит введен в кристаллической форме, в соединении с которым образована полимерная пена.
9. Защитное изделие для ран по п.7 или 8, отличающееся тем, что указанная полимерная пена содержит водорастворимый полимер.
10. Защитное изделие для ран по п.1, отличающееся тем, что защитное изделие для ран состоит из слоя или включает в себя слой, который непосредственно контактирует с раной в период использования и который является проницаемым для жидкости раны, при этом слой включает в себя гель и сетеподобный элемент жесткости, а гель наносят так, что он покрывает все части сетки, но оставляет сквозные отверстия на слое, образованном гелем и элементом жесткости и при этом ксилит введен в гель.
11. Защитное изделие для ран по п.10, отличающееся тем, что указанный сетеподобный элемент жесткости является эластичным, и гель является мягким и эластичным.
12. Защитное изделие для ран по п.10, отличающееся тем, что указанный слой является гидрофобным и не приклеивается к гнойным ранам.
13. Защитное изделие для ран по п.10, отличающееся тем, что указанный гель является силиконовым гелем.
14. Защитное изделие для ран по одному из пп.10-13, отличающееся тем, что элемент жесткости включает в себя мягкую, гибкую и эластично растягиваемую сетку текстильного материала.
15. Защитное изделие для ран по п.1, отличающееся тем, что защитное изделие для ран включает в себя перевязочный материал и тем, что ксилит нанесен на подложку, которая включена в данный перевязочный материал.
16. Защитное изделие для ран по п.15, отличающееся тем, что подложка является марлей.
17. Защитное изделие для ран по п.15, отличающееся тем, что подложка является нетканой тканью.
18. Защитное изделие для ран по п.15, отличающееся тем, что подложка является полимерной пеной, обладающей открытыми порами.
19. Защитное изделие для ран по п.15, отличающееся тем, что подложка является водорастворимой полимерной пеной.
20. Защитное изделие для ран по любому из пп.1-5 в форме перевязочного материала, отличающееся тем, что указанный перевязочный материал содержит абсорбентный слой для приема выделяемой из ран жидкости.
21. Защитное изделие для ран по любому из пп.1-5, отличающееся тем, что защитное изделие для ран является стерильным в целом и пакуется стерильным способом.
22. Способ производства защитного изделия для ран по любому из пп.15-19, отличающийся тем, что ксилит наносят на подложку в форме раствора.
23. Способ по п.22, отличающийся тем, что подложку затем высушивают.
24. Способ по п.22, отличающийся тем, что защитное изделие для ран и приложенную упаковку стерилизуют.
25. Применение вещества в защитных изделиях для ран, которое ингибирует рост бактерий в ранах, отличающееся тем, что указанное вещество является ксилитом.
26. Применение по п.25, отличающееся тем, что указанное вещество находится в порошковой форме.
27. Применение по п.25, отличающееся тем, что указанное вещество включено в гель.
28. Применение по п.25, отличающееся тем, что указанное вещество включено в жидкий раствор.
29. Применение по п.25, отличающееся тем, что указанное вещество включено в мазь.
30. Применение по п.25, отличающееся тем, что указанное вещество включено в пасту.
31. Применение по любому из пп.26-30, отличающееся тем, что защитное изделие для ран является стерильным в целом и упаковано стерильным способом.
32. Перевязочный материал для ран в форме пластыря, содержащий вещество для ингибирования роста бактерий в ранах, отличающийся тем, что указанное вещество является ксилитом.
33. Перевязочный материал для ран по п.32, отличающийся тем, что перевязочный материал для ран является полностью стерильным и упакован стерильным способом.
34. Применение ксилита для получения композиции, которая обладает эффектом ингибирования роста бактерий в ранах.
35. Применение по п.34, отличающееся тем, что указанная композиция включает в себя жидкий раствор, который содержит ксилит.
36. Применение по п.34, отличающееся тем, что указанная композиция включает в себя гель, в который введен ксилит.
37. Применение по п.36, отличающееся тем, что указанный гель включает в себя гидрофобный гель, предпочтительно силиконовый гель.
38. Применение по любому из пп.34-37, отличающееся тем, что указанная композиция является стерильной и упакована стерильным способом.
| RU 2000133217 A, 10.11.2002 | |||
| УСТРОЙСТВО ДЛЯ ДОСТАВКИ ВЕЩЕСТВА ДЛЯ УХОДА ЗА РОТОВОЙ ПОЛОСТЬЮ С ИСПОЛЬЗОВАНИЕМ ПОЛОСКИ МАТЕРИАЛА, ИМЕЮЩЕГО НИЗКУЮ ЖЕСТКОСТЬ ПРИ ИЗГИБЕ | 1998 |
|
RU2192202C2 |
| Jannesson L, Renvert S, Birkhed D., Effect of xylitol in an enzyme-containing dentifrice without sodium lauryl sulfate on mutans streptococci in vivo., Acta Odontol Scand | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| RU 2001126402 A, 27.06.2003 | |||
| RU 2000133213 A, 10.11.2002. | |||
Авторы
Даты
2009-05-10—Публикация
2004-12-16—Подача