Изобретение относится к области обработки природных вод при их использовании для выработки электроэнергии, теплоснабжения, а также в различных отраслях промышленности и в сельском хозяйстве.
Известны способы предотвращения карбонатных отложений с помощью введения в обрабатываемую воду кристаллической затравки с добавлением поверхностно-активных веществ [1].
Недостатками их являются загрязнение водоемов поверхностно-активными веществами, а также необходимость расходования химических реагентов.
Наиболее близким к описываемому изобретению по технической сущности и достигаемому результату является способ предотвращения карбонатных отложений в геотермальной воде, заключающийся в ее дегазации с последующим использованием образовавшихся кристаллов карбоната кальция в качестве затравки [2].
Недостаток данного изобретения заключается в невысокой эффективности очистки воды от карбоната кальция. Это связано с недостаточной степенью удаления углекислого газа из обрабатываемой воды после дегазации и невысоким значением перепада парциального давления углекислого газа в воде от равновесного до конечного значения.
Техническим решением предлагаемого изобретения является повышение эффективности стабилизационной обработки воды, заключающееся в более глубокой очистке ее от растворенного в ней карбоната кальция.
Техническое решение достигается тем, что в способе стабилизационной обработки геотермальной воды, заключающейся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, перед дегазацией при сохранении исходного давления в воде парциальное давление углекислого газа в ней доводят до равновесного значения путем замещения части растворенного углекислого газа азотом.
Схема реализации предлагаемого способа стабилизационной обработки воды дается на примере геотермальной воды скважины №3Т г.Кизляра Республики Дагестан. Вода скважины содержит ионы, мг/л: Na+ - 2260; Са2+ - 160; Mg2+ - 40; Cl- - 3550; HCO3 - - 390; SO4 2- - 150. Газосодержание - 1,2 м3/м3, в процентном отношении - СО2 - 18%, N2+СН4 - 82%. pH 6,55.
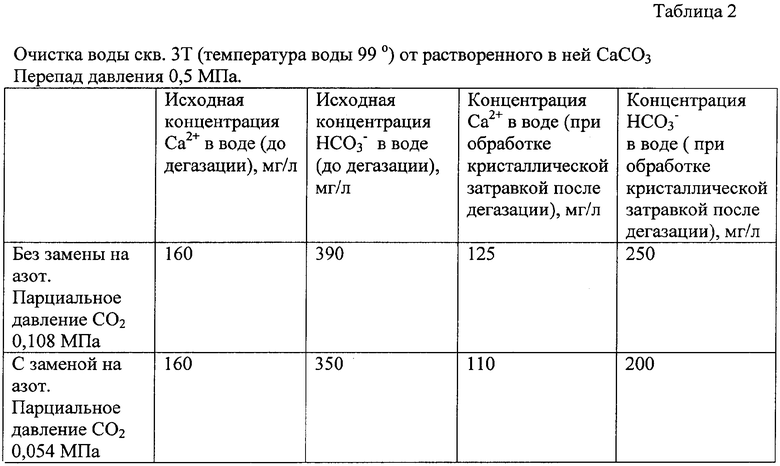
На фиг.1 - блок-схема реализации способа, на фиг.2 - кривые, соответствующие реальным (1) и возможным (2) значениям равновесного давления и температуры воды скважины 3Т, при которых вода стабильна.
Геотермальная вода из скважины 1 поступает в конвертор 2 с исходным давлением Рo; где осуществляется замена части углекислого газа, растворенного в воде, на азот с таким расчетом, что парциальное давление углекислого газа на выходе из конвертора 2 устанавливается на величине, близкой к равновесному, то есть из воды еще не выделяется твердая фаза карбоната кальция. При этом исходное давление Рo в воде сохраняется. Далее вода с давлением Рo поступает в кристаллизатор-отстойник 3, где происходит ее дегазация при резком падении давления от исходного Рo до конечного Pt значения. Нарушается карбонатно-кальциевое равновесие и в толще воды выделяется большое количество твердой фазы карбоната кальция. Образовавшийся осадок из нижней части кристаллизатора-отстойника 3 выводится наружу по линии 4, а часть его по линии 5 подается обратно в кристаллизатор-отстойник 3 в качестве затравки. Выделившиеся при дегазации пар и газ по линии 6 поступают к соответствующему потребителю, а обработанная (стабильная) вода подается по линии 7 для нужд горячего тепловодоснабжения.
Обычно на практике при осуществлении дегазации (фиг.2) перепад давления ΔР от исходного Рo до конечного Pt значения состоит из двух составляющих:
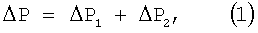
где ΔР1=Po-Ps - перепад давления от исходного Рo до равновесного Ps значения, при котором еще не выделяется твердая фаза карбоната кальция; ΔР2=Ps-Pt - перепад давления от равновесного Ps до конечного Рt значения. При замещении части углекислого газа в воде на азот значение Ps смещается в сторону исходного давления Рo и перепад давления
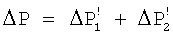 ,
,
где 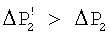 .
.
При этом скорость кристаллизации карбоната кальция в присутствии кристаллической затравки определяется согласно исследованиям [3-5]:
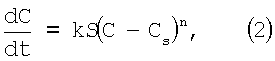
где k - коэффициент пропорциональности; n - константа поверхностной реакции (n=1÷2); S - площадь поверхности кристаллической затравки; С-Cs - пересыщение раствора воды по карбонату кальция. Как видно из (2), чем больше С-Cs, тем больше скорость кристаллизации, а пересыщение раствора С-Cs, в свою очередь, прямо пропорционально второй составляющей ΔР2 (или 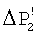 ). Поэтому, чем больше ΔР2 (или
). Поэтому, чем больше ΔР2 (или 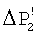 ) при дегазации, тем эффективнее идет процесс кристаллизации карбоната кальция на затравке. На фиг.2 показана разница в величинах ΔР2 и
) при дегазации, тем эффективнее идет процесс кристаллизации карбоната кальция на затравке. На фиг.2 показана разница в величинах ΔР2 и 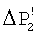 при подаче воды на дегазацию без замещения СО2 на азот (кривая 1) и с замещением (кривая 2) соответственно.
при подаче воды на дегазацию без замещения СО2 на азот (кривая 1) и с замещением (кривая 2) соответственно.
В работе [6] показано образование твердой фазы карбоната кальция в воде скважины 3Т в виде частиц взвеси сразу после дегазации ее при различных перепадах давления в системе (см. табл.1). При большом перепаде 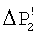 и большой поверхности, образующейся при этом, кристаллической затравки скорость кристаллизации карбоната кальция из раствора возрастает, то есть имеет место так называемое явление массовой кристаллизации. А многократное использование кристаллической затравки для обработки воды приводит к более глубокой очистке воды от растворенного в ней карбоната кальция. Результаты опытов по очистке геотермальной воды скв. №3Т г.Кизляра от растворенного в ней карбоната кальция при замене части углекислого газа на азот и использовании кристаллической затравки для ее обработки показаны в таблице 2. Как видно из таблицы 2, при замене 50% углекислого газа на азот перед дегазацией концентрация ионов Са2+ в воде после дегазации и обработки ее кристаллической затравкой снижается до уровня 110 мг/л против 125 мг/л без замены СО2 на азот, что свидетельствует о более глубокой очистке воды от растворенного в ней карбоната кальция.
и большой поверхности, образующейся при этом, кристаллической затравки скорость кристаллизации карбоната кальция из раствора возрастает, то есть имеет место так называемое явление массовой кристаллизации. А многократное использование кристаллической затравки для обработки воды приводит к более глубокой очистке воды от растворенного в ней карбоната кальция. Результаты опытов по очистке геотермальной воды скв. №3Т г.Кизляра от растворенного в ней карбоната кальция при замене части углекислого газа на азот и использовании кристаллической затравки для ее обработки показаны в таблице 2. Как видно из таблицы 2, при замене 50% углекислого газа на азот перед дегазацией концентрация ионов Са2+ в воде после дегазации и обработки ее кристаллической затравкой снижается до уровня 110 мг/л против 125 мг/л без замены СО2 на азот, что свидетельствует о более глубокой очистке воды от растворенного в ней карбоната кальция.
Технически замена СО2 на азот была осуществлена следующим образом. В емкости из нержавеющей стали объемом 1,2 м3 исходное давление Рo=0,6 МПа. Парциальное давление СО2 при этом составляло 0,18×0,6 МПа = 0,108 МПа. Снизили Рo до 0,3 МПа. Это - давление, при котором еще не выделяется твердая фаза карбоната кальция из раствора воды скв. 3Т. Далее с помощью насоса закачали в емкость воздух (в воздухе 78% азота и 21% О2) до достижения исходного значения Рo=0,6 МПа. Парциальное давление СО2 при этом составило 0,09×0,6 МПа = 0,054 МПа.
Таким образом, в способе стабилизационной обработки геотермальной воды, заключающейся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, замещение части углекислого газа на азот с сохранением исходного давления в воде перед ее дегазацией позволяет повысить эффективность стабилизационной обработки воды, заключающейся в более глубокой очистке ее от растворенного в ней карбоната кальция.
Источники информации
1. Авторское свидетельство СССР №307070, кл. С02В 5/00, 1971.
2. Авторское свидетельство СССР №810615, кл. C02F 5/00, 1981.
3. Nivlt J., Karpinski P. Determination of individual rate constans of reaction and diffusion steps from over - oll cristall growth coefficient // Kristall und Technik. 1977. Vol.12. P.1233-1241.
4. Васина Л.Г., Богловский А.Б., Календарев P.H. Изучение кинетики образования карбоната кальция в закрытой системе.// Тр. МЭИ, 1980, Вып.466, С.51-56.
5. Новиков Б.Е., Ахмедов Г.Я. Кинетика кристаллизации карбоната кальция из геотермальных вод в присутствии затравочных кристаллов. // Материалы III-го международного симпозиума по гидротермальным реакциям, Фрунзе, Киргизия. 1989. С.28.
6. Ахмедов Г.Я. Исследование процессов кристаллизации карбоната кальция при использовании геотермальных вод. // Материалы научно-практической конференции «Геоэкологические проблемы освоения и охраны ресурсов подземных вод Восточного Предкавказья», 22-26 сентября 2003 г., Махачкала: РАН, Дагестанский научный центр, 2003, С.162-165.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ предотвращения карбонатных отложений в испарителе и устройство для его осуществления | 1987 |
|
SU1532723A1 |
| СПОСОБ ОЧИСТКИ ТЕПЛООБМЕННИКА ОТ КАРБОНАТНЫХ ОТЛОЖЕНИЙ | 2013 |
|
RU2528776C1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ | 2007 |
|
RU2345958C1 |
| Способ обработки воды | 1985 |
|
SU1330075A1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ | 2012 |
|
RU2522602C1 |
| УСТАНОВКА ДЛЯ ОБРАБОТКИ ВОДЫ | 1998 |
|
RU2145939C1 |
| СПОСОБ ПРЕДОТВРАЩЕНИЯ СОЛЕОТЛОЖЕНИЯ ПРИ УТИЛИЗАЦИИ ЭНЕРГИИ ГЕОТЕРМАЛЬНЫХ ВОД | 2008 |
|
RU2372564C1 |
| Аппарат для дегазации и умягчения вод | 1985 |
|
SU1310340A1 |
| Композиция неуглеводородной смеси газов и способ эксплуатации подземного хранилища природного газа | 2021 |
|
RU2768850C1 |
| Способ предотвращения карбонат-НыХ ОТлОжЕНий | 1976 |
|
SU810615A1 |
Изобретение относится к области очистки природных вод, преимущественно геотермальных, и может быть использовано, например, в теплоэнергетике и теплоснабжении. Способ стабилизационной обработки геотермальной воды заключается в ее дегазации с последующим использованием образовавшихся кристаллов карбоната кальция в качестве затравки. Перед дегазацией парциальное давление углекислого газа в обрабатываемой воде доводят до равновесного значения путем замещения на другой газ - азот. При этом исходное давление в воде перед ее дегазацией сохраняют. Способ обеспечивает повышение эффективности стабилизационной обработки воды за счет более глубокой очистки ее от растворенного в ней карбоната кальция. 2 ил., 1 табл.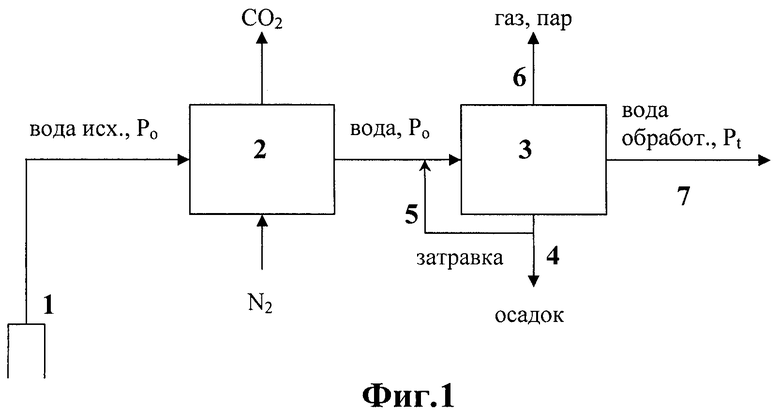
Способ стабилизационной обработки геотермальной воды, заключающийся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, отличающийся тем, что перед дегазацией при сохранении исходного давления в воде парциальное давление углекислого газа в ней доводят до равновесного значения путем замещения части растворенного углекислого газа азотом.
| Способ предотвращения карбонат-НыХ ОТлОжЕНий | 1976 |
|
SU810615A1 |
| SU 13300075 А1, 15.08.1987 | |||
| СПОСОБ ТЕРМОУМЯГЧЕНИЯ И ОБЕЗЖЕЛЕЗИВАНИЯ ВОДЫ | 2001 |
|
RU2225848C2 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| JP 2001129305 А, 15.05.2001. | |||
Авторы
Даты
2009-06-10—Публикация
2007-11-21—Подача