Изобретение относится к медицине, а именно к травматологии и ортопедии, и может быть использовано для лечения многооскольчатых и множественных переломов длинных трубчатых костей различных локализаций с абсолютными и относительными дефектами кости.
Проблема оптимизации репаративной регенерации кости после тяжелой механической травмы является одной из наиболее актуальных проблем травматологии, несмотря на все достижения медицины и смежных наук, совершенствование методов остеосинтеза и конструкций для фиксации костных отломков. Процесс восстановления целостности кости после травмы является сложным биологическим процессом и зависит от многих факторов, которые можно разделить на общие (возраст, сопутствующие заболевания, эндокринные, уровень обмена веществ, алиментарные нарушения и др.) и местные (характер перелома, качество репозиции и иммобилизации, объем повреждений окружающих тканей и нарушение кровоснабжения отломков и др.). При использовании традиционных методов лечения при множественных переломах замедление консолидации или несращение переломов с образованием ложных суставов встречается в 4,8-45% случаев.
Отмечается большое количество (до 51,6%) неудовлетворительных результатов лечения. Так, по данным центральной медико-социальной экспертной комиссии г.Москвы за период с 2001 по 2005 год в структуре осложнений, приводящих к инвалидизации лиц с изолированными повреждениями нижних конечностей, нарушение репаративной регенерации костной ткани занимает первое место (65,4%), а при множественных переломах костей голени или бедренных костей первичная инвалидность достигает 76,4%.
Таким образом, одной из главных задач лечения любого перелома является создание оптимальных условий для репаративного остеогенеза. Но, даже, несмотря на проводимые лечебные мероприятия, особенно у пострадавших с множественными и многооскольчатыми переломами длинных трубчатых костей, часто наблюдается замедление сращения переломов и формирование ложных суставов, что приводит к нарушению функции конечности и инвалидизации. Трубчатые кости (большие кости): большеберцовая, бедренная, плечевая, лучевая, локтевая обладают определенным анатомическим строением, определенным кровоснабжением, чем обуславливается процесс регенерации. Для предотвращения нежелательных осложнений используют разные методы.
Лечение перечисленных переломов может быть как консервативное, так и оперативное. В разное время применялись различные консервативные методы для стимуляции образования костной мозоли (Травматология и ортопедия. Т.1. Под ред. Ю.Г.Шапошникова, Москва, 1997):
1) Введение между отломками 10-20 мл аутокрови, 5-10 мл аутологичного красного костного мозга.
2) Применение застойной гиперемии.
3) Физиотерапия, УВЧ, электрофорез солей кальция, анаболических гормонов (метандростенолон, ретаболил и др.).
4) Электростимуляция слабыми токами.
5) Механотерапия - метод Турнера (поколачивание области перелома деревянным молоточком).
Существует ряд оперативных методов, направленных на коррекцию репаративного остеогенеза при выявлении наличия признаков замедления сращения и при формировании ложных суставов. К ним относятся свободная костная пластика, микрокомпрессия - микродистракция в аппаратах внешней фиксации, использование кровоснабжаемых трансплантатов (васкуляризованного или реваскуляризованного), использование клеточных технологий, в частности мезенхимальных стволовых клеток (МСК).
Известно, что в экспериментах на крысах на свежих повреждениях плоских костей (теменная кость) испытывали биотрансплантаты с недифференцированными МСК, в результате чего подобрали оптимальную для лечения плотность МСК на 1 см3 трансплантата (Кругляков П.В., Соколова И.Б. и др. Влияние сингенных МСК на восстановление костной ткани при имплантации деминерализованного костного матрикса. // Цитология. - 2005, Т.47 (№6). - С.466-477).
Известен патент РФ №2240135, по которому восстановление целостности кости осуществляют с помощью клеток-предшественников остеогенеза. Но по известному способу лечения клетки наносят на трехмерный аллогенный костный матрикс или губку. Вводили аутологичные МСК (АМСК) в аутологичной сыворотке крови, причем полученные по известному патенту клетки обработаны каким-либо индуктором остеогенеза (инсулином, дексаметазоном, глицерофосфатом), что часто используют в практике остеосинтеза. Авторы известного способа утверждают, что привнесение клеток в зону дефекта без фиксации не позволит создать концентрацию клеток, необходимую для регенерации кости, из-за вымывания их из зоны дефекта.
Известен патент РФ №230167, защищающий биотрансплантат для восстановления хрящевой ткани (одна из стадий остеосинтеза). Биотрансплантат состоит из МСК и клеточных культур, а также трехмерной матрицы-носителя, т.е. необходима операция для образования полости, куда вносят биотрансплантат. Метод лечения травматичен.
Лечение больных с помощью инъекционного введения АМСК применяли в случае образования ложных суставов. /Современные методы лечения больных с травмами и их осложнениями. Материалы конференции, Курган, 2006, с.207-209/. В методе указывают на то, что необходима поверхность, обладающая высокоадгезивными свойствами. Так как речь идет уже о лечении сформировавшегося ложного сустава, то время после перелома составляет длительный срок и процессы остеосинтеза проходят в иных условиях, чем сразу после перелома.
Известна работа «Влияние аутотрансплантации мезенхимальных стволовых клеток на дистракционный остеогенез» (Клеточные и нанотехнологии в биологии и медицине. Курган, 2007, с.149-150).
Она направлена на оптимизацию дистракционного остеогенеза с помощью МСК. В этой работе лечение осуществляли 4-х кратным инъекционным введением МСК под контролем рентгенографии и компьютерной томографии.
В описанном методе лечение было проведено на уже сформированных костях, чтобы их удлинить или чтобы заместить образовавшиеся дефекты в «спокойной» кости. Авторами был изучен темп формирования регенерата при ежемесячном введении клеток.
Широко распространены при лечении многооскольчатых и множественных переломов, которые всегда считались сложными (вне зависимости, являются ли они открытыми или закрытыми), оперативные методы, в частности метод внутрикостной фиксации. К нему обращаются при переломах длинных трубчатых костей со значительным и трудноустранимым смещением отломков (А.В.Каплан. Техника лечения переломов костей. М., 1948). Если при множественных переломах удается сопоставить отломки бескровным путем, то лечение стараются проводить путем прочной фиксации.
При лечении многооскольчатых и множественных переломов применяются различные методы накостного и интрамедуллярного металлоостеосинтеза. Одним из основных принципов оперативного (хирургического) вмешательства является малотравматичность - максимальное сохранение окружающих мягких тканей, надкостницы, сосудов и нервов, костного мозга. С этой целью широко применяется туннельный метод постановки пластины без вскрытия зоны перелома и, соответственно, без нарушения питания и иннервации отломков и осколков (Методические рекомендации Минздрава РФ).
После того как проведена иммобилизация отломков, сращение происходит за счет мобилизации репаративных факторов организма пациента.
Целью предлагаемого изобретения является стимуляция процессов репаративного остеогенеза на ранних стадиях лечения сложных переломов и предотвращение замедленного сращения и формирования ложных суставов. Такие осложнения возникают в тех случаях, когда имеются факторы, способствующие замедлению консолидации, например такие, как: множественный характер переломов, многооскольчатые переломы с абсолютными и относительными дефектами, когда в организме в результате тяжелой травмы возникает дефицит стволовых клеток (снижение их количества в 10000-100000 раз). Стволовые клетки - плюрипотентные клетки являются предшественниками остеобластов - клеток, участвующих в остеогенезе. Стимуляцию остеогенеза необходимо осуществлять в этих трудных случаях малотравматичным методом лечения.
Задача решена с помощью дополнительного к основному хирургическому лечению введения в зону перелома (дефект кости) однородных на 87-99,9% по клеточным маркерам CD 34-; CD 45-; CD 44+; CD 90+; CD 105+; CD 106+ аутологичных мезенхимальных стволовых клеток (АМСК) в аутосыворотке больного в количестве 25-50 млн в зависимости от объема повреждения и дефекта костной ткани. Причем такое введение осуществляют одноразовым малотравматичным инъекционным способом. АМСК вводят не сразу после перелома, а после завершения фазы экссудативного воспаления, сопровождающего травму. Время для введения АМСК определяют, проводя контроль показателей клинического анализа крови. Количество имплантируемых АМСК определяют по площади дефекта кортикального слоя кости по рентгенограммам в 2 перпендикулярных проекциях.
Введение АМСК для получения лечебного эффекта необходимо осуществлять на определенной стадии восстановления кости. Время введения АМСК выбирают по биохимическим показателям крови пациента. Авторами было установлено, что не только качественное сращение, но и ускорение процесса сращения зависит от момента введения АМСК в зону повреждения. Ускорение образования костной мозоли за счет введения АМСК на определенной стадии процесса консолидации было обнаружено случайно, после чего авторы начали подбирать оптимальные сроки, когда после травмы необходимо вводить АМСК. Введение АМСК осуществляли без использования трехмерных матриц.
Во всех последних работах, связанных с восстановлением целостности костей с помощью МСК, использовали матрицы, инициирующие дифференцировку МСК в остеобласты. В заявляемом изобретении такими матрицами могут выступать осколки длинных трубчатых костей. И хотя такая фиксация клеток в зоне перелома на отломках и осколках костей не определялась, именно при множественных и многооскольчатых переломах длинных трубчатых костей положительный эффект получают уже от одноразового инъекционного введения клеток.
Первоначально было замечено, что введение АМСК в зону перелома после постановки пластины для фиксации кости после репозиции улучшает качество костной мозоли, на сроки сращения внимание не обратили. Сравнивая сроки сращения у пациентов с переломом костей 2-х нижних конечностей, обратили внимание на то, что сроки сращения зависят от момента введения АМСК, причем рентгенологически четко видно, что в конечности, дополнительно леченой АМСК, восстановление целостности кости наступает в 1,5-2 раза быстрее, чем там, куда АМСК не вводили. При наличии множественных и многооскольчатых переломов длинных трубчатых костей важны биохимические характеристики крови, по которым устанавливают сроки для введения АМСК. Течение болезни у разных пациентов идет по-разному, поэтому очень важны цифровые характеристики биохимических показателей крови для принятия решения, на каком сроке лечения необходимо осуществлять введение АМСК, чтобы получить лучший результат лечения, чтобы восстановление целостности кости прошло быстрее.
Применение в лечении АМСК в аутологичной сыворотке приводит как к быстрому образованию первичной костной мозоли, так и полноценному восстановлению структуры кости с восстановлением костномозгового канала. Вводили АМСК в аутологичной сыворотке крови, причем АМСК были получены способом по патенту РФ №2303632, при осуществлении которого клетки не обрабатывают каким-либо индуктором остеогенеза (инсулином, дексаметазоном, β-глицерофосфатом), что часто используют в практике остеосинтеза, например, известной из патента РФ №2240135.
Популяция АМСК, полученных способом по патенту РФ №2303632, обладает преимуществом в сроках накопления in vitro массы клеток для проведения лечения. Это связано со способом выделения посевного материала из костного мозга пациента и способом их культивирования, благодаря чему популяцию живых, однородных на 87-99,9% по фенотипу, т.е. по клеточным маркерам CD 34-; CD 45-; CD 44+; CD 90+; CD 105+; CD 106+, клеток (АМСК) получают с высокой степенью однородности.
До введения АМСК проводят хирургическое лечение.
Для предотвращения нежелательных осложнений авторами предлагается следующая последовательность действий.
1) Производится закрытая репозиция - сопоставление отломков на скелетном вытяжении на дооперационном этапе (выполняется рентгеноконтроль на вытяжении) или ручная репозиция отломков во время операции. Основной задачей такой репозиции является восстановление правильной оси конечности (устранение смещения по ширине) и восстановление длины кости без точного сопоставления мелких осколков. Таким образом, зона перелома либо не вскрывается, либо выполняется небольшой разрез 2.0-3.0 см для сопоставления отломков, мелкие осколки остаются в различной степени смещенными. Надкостница не отделяется от отломков и осколков и, соответственно, не нарушается их питание.
2) На следующем этапе через небольшие разрезы (3.0 см) в области проксимального или дистального отломков под мягкими тканями по кости туннельно проводится моделированная металлическая пластина и фиксируется винтами к кости через разрезы по 0,5-1,0 см в проекции отверстий пластины под рентгеноконтролем. Дополнительная фиксация прооперированного сегмента гипсовыми лангетами осуществляется по необходимости в зависимости от характера перелома и достигнутой с помощью остеосинтеза стабильности.
Для получения АМСК для трансплантации у пациента до или во время операции остеосинтеза производят забор костного мозга путем пункции, чаще - из подвздошной кости. Гепаринизированный пунктат в среде ДМЕМ центрифугировали с фиколлом с выделением фракции однородных по фенотипу МСК, которые затем пассировали неоднократно в среде ДМЕМ с добавлением 15-22% FBS in vitro до накопления массы клеток в соответствии с площадью подлежащей лечению травмы.
В послеоперационном периоде, на 10-16 день после операции, после стихания фазы экссудативного воспаления, что определяется по показателям клинического анализа крови (лейкоцитоз, сдвиг лейкоцитарной формулы, СОЭ) и оценки локального статуса (заживление послеоперационной раны, отек, гиперемия и др.) вводят инъекционно АМСК.
Показатели клинического анализа крови, определяющие время для инъекционного введения АМСК, характеризуются цифрами: лейкоциты - 4-10*109/л, СОЭ - 2-20 мм/ч, палочкоядерные нейтрофилы - 1-8% (см. Таблицу ).
АМСК в аутологичной сыворотке имплантируют в зону перелома путем инъекции под ЭОП-контролем. Учитывают при лечении также средние сроки формирования костной мозоли, их изменения в зависимости от влияния перечисленных выше общих и местных факторов. Сращение переломов у большинства пострадавших происходит по хондробластическому типу, в котором выделяют 4 стадии:
1) 1 стадия катаболизма (7-10 дней).
2) 2 стадия дифференциации и пролиферации (7-14 день).
3) 3 стадия - формирование первичной костной мозоли (2-6 неделя).
4) 4 стадия - минерализация костной мозоли (2-4 месяц).
АМСК имплантируют в зону перелома во 2 - начале 3 стадии образования костной мозоли (10-16 сутки после операции), когда в зоне перелома стихают воспалительные процессы, уменьшается ферментативная активность и создаются оптимальные условия для пролиферации и дифференцировки полипотентных стволовых клеток, начинается формирование хрящевой мозоли, выполняющей роль матрицы для клеток.
После введения в место перелома АМСК в зоне имплантации общих реакций организма и местных патологических процессов в зоне имплантации не наблюдалось. У пострадавших с множественными переломами (перелом обеих бедренных или большеберцовых костей) АМСК в аутологичной сыворотке вводили в зону более тяжелого и неблагоприятного в отношении сращения перелома.
По описанной методике прошли лечение 10 пациентов, 4 пострадавших с множественными переломами и 6 с изолированными многооскольчатыми переломами длинных трубчатых костей. Для оценки результатов применялись рентгенологический метод, компьютерная томография, клинические исследования. Во всех случаях применения АМСК достигнуто сращение переломов без замедления сращения и без формирования ложных суставов. У больных с множественными сходными повреждениями, в лечении которых использовались одинаковые методы остеосинтеза, в один из поврежденных сегментов имплантировались АМСК. Было отмечено, что введение стволовых клеток способствует опережению восстановления кости по сравнению с другим сегментом - без применения АМСК - в 1.5-2 раза, что выражалось в формировании выраженной костной мозоли.
Также было отмечено опережение в 1,5-2 раза средних сроков сращения переломов и заполнения дефектов кости при введении АМСК в зону перелома при лечении изолированных оскольчатых переломов костей голени и бедра.
Средние сроки сращения переломов:
Примеры лечения больных
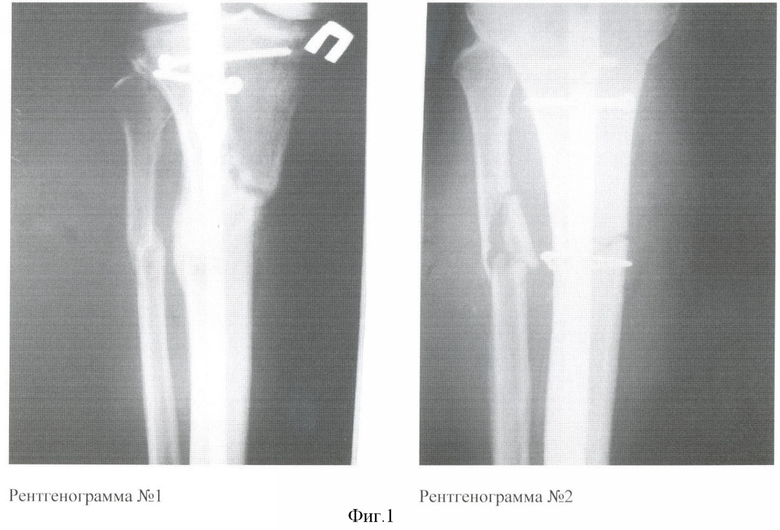
1) Больной К. 45 лет поступил в клинику в первые сутки после травмы с диагнозом: Автотравма. Закрытый оскольчатый перелом обеих костей в/3 правой голени со смещением. При поступлении больному было выполнено скелетное вытяжение правой голени. Клинический анализ крови при поступлении: гемоглобин - 140 г/л, эритроциты - 3.8*1012/л, лейкоциты - 5.3*109/л, палочкоядерные нейтрофилы - 2%, СОЭ - 8 мм/ч. Учитывая сохранение смещения отломков на скелетном вытяжении после рентгеноконтроля и многооскольчатый характер перелома, через 4 суток после поступления было выполнено оперативное вмешательство - блокируемый интрамедуллярный остеосинтез большеберцовой кости. В ходе операции зона перелома не вскрывалась. На 2 сутки после поступления у больного был выполнен забор 40 мл костного мозга из гребня подвздошной кости для культивирования АМСК. Послеоперационный период протекал без осложнений, послеоперационные раны зажили первичным натяжением. Клинический анализ крови на 9-е сутки после операции: гемоглобин - 125 г/л, эритроциты - 3.1*1012/л, лейкоциты - 7.4*109/л, палочкоядерные нейтрофилы - 4%, СОЭ - 15 мм/ч, данные показатели указывают на отсутствие воспалительного процесса в области послеоперационной раны. Через 10 дней после проведения операции больному были введены 50 млн АМСК в зону перелома (в зону наибольшего относительного дефекта кости) под рентгеноконтролем. После введения АМСК местных и общих патологических реакций организма не наблюдалось.
Данные лечения представлены на фиг.1 Рентгенограмма №1 - с применением АМСК. Оскольчатый перелом обеих костей в/3 голени со смещением, 8 недель после операции (интрамедуллярный металлоостеосинтез большеберцовой кости). На снимке видна выраженная периостальная мозоль в зоне имплантации АМСК и интермедиальная мозоль, сращение оскольчатого перелома в/3 малоберцовой кости. Рентгенограмма №2 - лечение аналогичной травмы без применения АМСК. Оскольчатый перелом обеих костей в/3 голени со смещением, 8 недель после операции (интрамедуллярный МОС б/берцовой кости с дополнительной фиксацией осколков проволочным серкляжем). На снимке отсутствуют отчетливые признаки сращения, щель между отломками не заполнена костной тканью, начальные признаки интермедиальной мозоли. Отсутствуют признаки сращения м/берцовой кости.
При выписке больному (лечение с АМСК) были даны стандартные рекомендации после подобных операций. Через 8 недель после операции был выполнен рентгеноконтроль правой голени. На рентгенограмме (фиг.1, №1) отмечались выраженная периостальная мозоль в зоне имплантации АМСК и интермедиальная мозоль, сращение оскольчатого перелома в/3 малоберцовой кости.
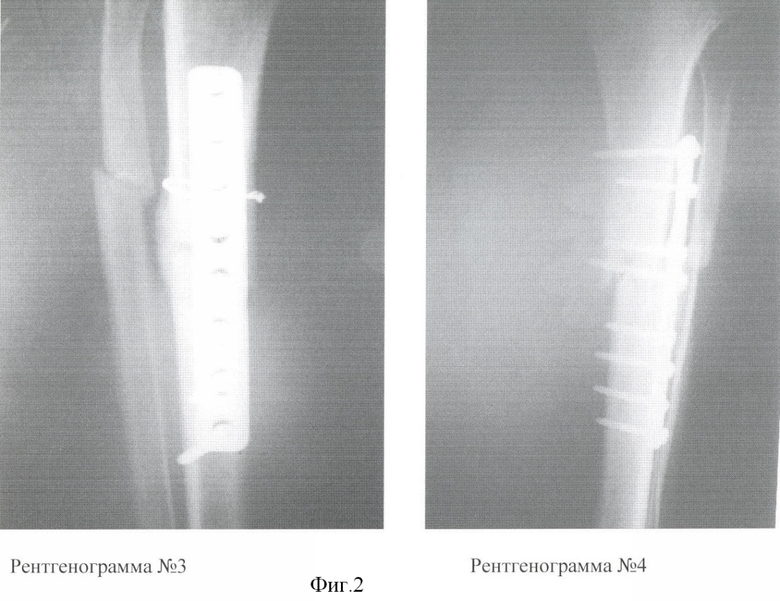
2) Больная Б. 38 лет поступила в клинику в первые сутки после травмы с диагнозом: Автотравма. Закрытый оскольчатый перелом костей обеих голеней в ср/3 со смещением. При поступлении больной было выполнено скелетное вытяжение обеих голеней. Клинический анализ крови при поступлении: гемоглобин - 116 г/л, эритроциты - 2.8*1012/л, лейкоциты - 7.3*109/л, палочкоядерные нейтрофилы - 3%, СОЭ - 10 мм/ч. Учитывая множественный и многооскольчатый характер переломов, сохранение смещения отломков на скелетном вытяжении после рентгеноконтроля, через 3 суток после поступления было выполнено оперативное вмешательство - накостный остеосинтез большеберцовых костей обеих голеней. В ходе операции зоны переломов вскрывались в связи с невозможностью закрытой репозиции. На 2 сутки после поступления у больной был выполнен забор 40 мл костного мозга из гребня подвздошной кости для культивирования АМСК. Послеоперационный период протекал без осложнений, послеоперационные раны зажили первичным натяжением. Клинический анализ крови на 11-е сутки после операции: гемоглобин - 110 г/л, эритроциты - 2.7*1012/л, лейкоциты - 7.6*109/л, палочкоядерные нейтрофилы - 5%, СОЭ - 13 мм/ч. Через 12 дней после операции больной были введены 50 млн АМСК в зону перелома левой большеберцовой кости (в зону наибольшего относительного дефекта кости по сравнению с правой конечностью) под рентгеноконтролем. После введения АМСК местных и общих патологических реакций организма не наблюдалось. Результаты лечения представлены на фиг.2.
Фиг. 2
- Рентгенограмма №3 - лечение с применением АМСК. Оскольчатый перелом обеих костей ср/3 левой голени со смещением. 8 недель после операции (накостный МОС б/берцовой кости с дополнительной фиксацией проволочным серкляжем). На снимке видна выраженная периостальная мозоль в зоне имплантации АМСК.
- Рентгенограмма №4 - лечение без применения АМСК. Оскольчатый перелом обеих костей ср/3 правой голени со смещением. 8 недель после операции (накостный МОС б/берцовой кости). На снимке отсутствуют признаки сращения б/берцовой и м/берцовой костей.
При выписке больной были даны стандартные рекомендации - постельный режим, передвижение на коляске, исключение осевой нагрузки на обе ноги. Через 8 недель после операций был выполнен рентгеноконтроль обеих голеней, на рентгенограммах отмечалось выраженная периостальная мозоль в зоне имплантации АМСК в левую голень. Лечение без применения АМСК: через 8 недель отсутствовали признаки сращения б/берцовой и м/берцовой костей правой голени - фиг. 2, рентг. №4). Полная консолидация костей левой голени была констатирована через 3 мес после операции, в то время как в правой голени сращение большеберцовой кости не наступило, а через 12 мес после операции там сформировался ложный сустав.
При резком дефиците МСК, который фиксируется при таких переломах, можно было предположить, что одноразового введения клеток будет недостаточно для регенерации кости. Однако строение длинных трубчатых костей, их структура и, следовательно, структура их отломков и множественных осколков в зоне перелома создают условия для того, чтобы не происходило вымывание АМСК. Происходит восстановление кости, причем именно за счет введенных в аутологичной сыворотке АМСК, подтверждением чему являются сроки восстановления одноименных конечностей у одного и того же пациента, когда одну конечность лечили с помощью АМСК, а другую - без. Регенеративная способность организма здесь одна и та же, но условия для консолидации кости разные.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ЗАМЕДЛЕННО СРАСТАЮЩИХСЯ ПЕРЕЛОМОВ ПУТЕМ ТРАНСПЛАНТАЦИИ АУТОЛОГИЧНЫХ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК | 2008 |
|
RU2375981C1 |
| РОЛЬ ГЕМАТОМЫ ПРИ ПЕРЕЛОМАХ КОСТЕЙ | 2017 |
|
RU2696765C2 |
| СПОСОБ ЛЕЧЕНИЯ ЛОЖНЫХ СУСТАВОВ ПУТЕМ ТРАНСПЛАНТАЦИИ АУТОЛОГИЧНЫХ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК, БИОТРАНСПЛАНТАТ ДЛЯ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2309756C1 |
| СПОСОБ ОПТИМИЗАЦИИ УСЛОВИЙ СРАЩЕНИЯ ПЕРЕЛОМОВ КОСТЕЙ КОНЕЧНОСТЕЙ И ИХ ПОСЛЕДСТВИЙ В УСЛОВИЯХ ИХ ОБЕЗДВИЖИВАНИЯ | 2010 |
|
RU2454962C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСКОЛЬЧАТЫХ ПЕРЕЛОМОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2003 |
|
RU2253393C1 |
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2006 |
|
RU2315580C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ОСТЕОМИЕЛИТА С ДЕФЕКТОМ КОСТИ | 2008 |
|
RU2389442C1 |
| УСТРОЙСТВО ДЛЯ СТИМУЛЯЦИИ ОСТЕОГЕНЕЗА ПРИ ЛЕЧЕНИИ ОСКОЛЬЧАТЫХ ПЕРЕЛОМОВ ГОЛЕНИ В АППАРАТЕ ИЛИЗАРОВА | 2002 |
|
RU2264182C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ТЯЖЕЛОЙ ПОЛИТРАВМОЙ И СЛОЖНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2005 |
|
RU2294168C1 |
| СПОСОБ ЛЕЧЕНИЯ ТУГОГО ЛОЖНОГО СУСТАВА ГОЛЕНИ | 2008 |
|
RU2363410C1 |
Изобретение относится к медицине, а именно к травматологии и ортопедии, и предназначено для лечения многооскольчатых и множественных переломов длинных трубчатых костей. Проводят репозицию отломков кости и фиксацию их с помощью накостного или интрамедуллярного остеосинтеза. На 10-16 сутки после операции в зону перелома дополнительно вводят инъекционно аутологичные мезенхимальные стволовые клетки в аутологичной сыворотке в количестве 25-50 млн клеток, причем инъекцию осуществляют при следующих показателях клинического анализа крови: лейкоциты - 4-10·109/л, СОЭ - 2-20 мм/ч, палочкоядерные нейтрофилы - 1-8%. Аутологичные мезенхимальные стволовые клетки являются популяцией живых однородных на 87-99,9% по клеточным маркерам CD 34-; CD 45-; CD 44+; CD 90+; CD 105+; CD 106+ клеток, которые выделены из костного мозга пациента и накоплены in vitro. Способ обеспечивает создание оптимальных условий для репаративного остеогенеза, стимуляцию процессов репаративного остеогенеза на ранних стадиях лечения сложных переломов и предотвращение замедленного сращения и формирования ложных суставов, снижение травматичности. 1 з.п. ф-лы., 1 табл., 2 ил.
1. Способ лечения многооскольчатых и множественных переломов длинных трубчатых костей хирургическим путем, включающий репозицию отломков кости и фиксацию их с помощью накостного или интрамедуллярного остеосинтеза, отличающийся тем, что на 10-16 сутки после операции в зону перелома дополнительно вводят инъекционно аутологичные мезенхимальные стволовые клетки в аутологичной сыворотке в количестве 25-50 млн. клеток, причем инъекцию осуществляют при следующих показателях клинического анализа крови: лейкоциты 4-10·109/л, СОЭ 2-20 мм/ч, палочкоядерные нейтрофилы 1-8%.
2. Способ лечения по п.1, отличающийся тем, что аутологичные мезенхимальные стволовые клетки являются популяцией живых однородных на 87-99,9% по клеточным маркерам CD 34-; CD 45-; CD 44+; CD 90+; CD 105+; CD 106+ клеток, которые выделены из костного мозга пациента и накоплены in vitro.
| МЮЛЛЕР М.Е | |||
| и др | |||
| Руководство по внутреннему остеосинтезу Springer-Verlag, 1996, с.28-29 | |||
| СПОСОБ ЛЕЧЕНИЯ ЛОЖНЫХ СУСТАВОВ ПУТЕМ ТРАНСПЛАНТАЦИИ АУТОЛОГИЧНЫХ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК, БИОТРАНСПЛАНТАТ ДЛЯ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2309756C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК ИЗ КОСТНОГО МОЗГА МЛЕКОПИТАЮЩИХ И ПОПУЛЯЦИЯ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК, ПОЛУЧЕННАЯ ЭТИМ СПОСОБОМ | 2006 |
|
RU2303632C1 |
| Под ред | |||
| ШЕВЦОВА В.И | |||
| и др | |||
| Клеточные и нанотехнологии в биологии и медицине Курган, 2007, с.149-150 | |||
| ZACHOS T | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2009-10-20—Публикация
2008-03-20—Подача