Изобретение относится к области медицины, а именно к средствам, обладающим гранулоцитопоэзстимулирующим, радиопротекторным и иммуностимулирующим свойствами.
Известно, что в онкологии используется ряд лекарственных средств, способствующих восстановлению кроветворения после применения радио- и химиотерапии, таких как: макрофагальный колониестимулирующий фактор (М-КСФ), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), гранулоцитарный колониестимулирующий фактор (ГКСФ) (Richards D. Prevention of oral mucositis in cancer patients treated with chemotherapy or radiotherapy. Evid Based Dent. 2006; 7 (4): 106; Peoples GE, Holmes JP, Hueman MT, Mittendorf EA, Amin A, Khoo S, Dehqanzada ZA, Gurney JM, Woll MM, Ryan GB, Storrer CE, Craig D, Ioannides CG, Ponniah S. Combined clinical trial results of a HER2/neu (E75) vaccine for the prevention of recurrence in high-risk breast cancer patients: U.S. Military Cancer Institute Clinical Trials Group Study I-01 and I-02. Clin Cancer Res. 2008 Feb 1; 14 (3): 797-803).
Наиболее близким по назначению к заявляемому средству (прототипом) является гранулоцитарный колониестимулирующий фактор (ГКСФ) (Xiao BG, Lu CZ, Link H. Cell biology and clinical promise of G-CSF: immunomodulation and neuroprotection. J Cell Mol Med. 2007; 11 (6): 1272-90). Известно, что ГКСФ индуцирует дифференцировку стволовых элементов костного мозга в нейтрофилы (гранулоциты), мобилизует их выход в периферическую кровь, увеличивая их продукцию. ГКСФ поляризует Т-клеточную дифференцировку от Т-хелперов 1-го типа к хелперам 2-го типа (Pan L, Delmonte JJ, Jalonen CK, Ferrara JL. Pretreatment of donor mice with granulocyte colony-stimulating factor polarizes donor Т lymphocytes toward type-2 cytokine production and reduces severity of experimental graft-versus-host disease. Blood 1995; 86: 4422-9). Применение ГКСФ способствует генерации супрессорных Т-клеток (CD4+25+) и супрессорных цитокинов (IL-10, TGF-β) (Morris ES, MacDonald KP, Rowe V, Johnson DH, Banovic T, Clouston AD, Hill GR. Donor treatment with pegylated G-CSF augments the generation of IL-10-producing regulatory T cells and promotes transplantation tolerance. Blood 2004; 103 3573-81). Кроме того, ГКСФ является радиопротектором (Bertho JM, Frick J, Prat M, Demarquay С, Dudoignon N, Trompier F, Gorin NC, Thierry D, Gourmelon P. Comparison of autologous cell therapy and granulocyte-colony stimulating factor (G-CSF) injection vs. G-CSF injection alone for the treatment of acute radiation syndrome in a non-human primate model. Int J Radiat Oncol Biol Phys. 2005 Nov 1; 63 (3): 911-20., Streeter PR, Dudley LZ, Fleming WH. Activation of the G-CSF and Flt-3 receptors protects hematopoietic stem cells from lethal irradiation. Exp. Hematol. 2003 Nov; 31 (11): 1119-25).
Задачей изобретения является расширение ассортимента средств,
обладающих стимулирующим гранулоцитопоэз, радиопротекторным и иммуностимулируюшим действием.
Циклофилин А - белок с молекулярной массой 18 кД, обладающий цистрансизомеразной активностью (G. Fischer, H. Bang, C. Mech С. Determination of enzymatic catalysis for the cis-trans-isomerization of peptide binding in proline-containing peptides. Biomed. Biochim. Acta. 43. 1984. P.1101-11). Циклофилин А является лигандом для связывания циклоспорина А, чем и обусловлено иммуносупрессорное действие последнего (D.A.Fruman, S.J.Burakoff, B.E.Bierer. Immunophilins in protein folding and immunosuppression. FASEB J. 8. 1994. 391-400). Циклофилин А принимает активное участие в аутоиммунных заболеваниях, обусловливая воспалительные процессы на периферии (P.Zhu, J.Ding, J.Zhou et.al., Expression of CD147 on monocytes/macrophages in rheumatoid arthritis: its potential role in monocyte accumulation and matrix metalloproteinase production. Arthritis Research & Therapy. 7. 2005. P.1023-33, A.Billich, G.Winkler, H.Aschauer, A.Rot, P.Peichl. J Exp Med. 185. 1997. P.975-80). Активированные макрофаги способны секретировать циклофилин А во внешнюю среду (B.Sherry, N.Yarlett, A.Strupp. Identification of cyclophilin A as a proinflammatory secretory product of lipopolysaccharide-activated macrophages. Proc.Natl. Acad. Aci. 89 (1992) 3511-15). Циклофилин А обладает хемотаксическим действием, регулируя миграцию зрелых моноцитов, нейтрофилов, эозинофилов и Т-лимфоцитов, формируя таким образом зону воспаления (Q.Xu, M.C.Leiva, SA.Fischkoff, R.E.Handschumacher, C.R.Lyttle. Leukocyte chemotactic activity of cyclophilin. J Biol.Chem. 267.1992. P.1168-71). Циклофилин А не используется в качестве лекарственного средства. Основные усилия исследователей направлены на поиски веществ антагонистов (различные формы циклоспорина А), нейтрализующих действие циклофилина А при воспалительных и других процессах (Shuai Chen, Xuemei Zhao, Jinzhi Tan, et.al. Structure-based identification of small molecule compounds targeting cell cyclophilin A with anti-HIV-1 activity. European Journal of Pharmacology 565. 2007. P.54-59).
Для выполнения поставленной задачи проводили оценку влияния циклофилина А на миграцию стволовых клеток костного мозга in vivo на сублетально облученных мышах по методу Till J.E., McCullough E.A (J.E.Till, Е.А.McCullough. A direct measurment of the radiation sensitivity of normal mouse bone marrow cells. Rad Res. 14 (1961) 213-22). Нативный циклофилин А получали из культуральной жидкости клеток мышиной тимомы EL-4 путем биохимической очистки до конечной чистоты белка не менее 95%. Для облучения использовали 35-50 взрослых мышей самок (C57BL/6x CBA) F1 в возрасте 12-14 недель, весом 20-22 г, которых разделили на пять групп по 7-10 животных в каждой группе. Мыши были облучены при помощи Cо60 гамма- терапевтического аппарата "Агат-Р" (Россия) с начальной мощностью 1,9×1014 Бк дозой 4,5 Gy. Эксперимент повторялся трижды.
Циклофилин А вводили мышам в хвостовую вену в дозе 30 мкг/мышь через 24 часа после облучения. В качестве контроля вводили буфер, используемый при очистке циклофилина А. Через семь дней после облучения мышей забивали методом цервикальной дислокации. Селезенку извлекали и помещали в фиксирующую жидкость, состоящую из ледяной уксусной кислоты и абсолютного спирта в соотношении 1:3. Визуальный подсчет эндогенных колоний в каждой селезенке проводили через 4 часа.
Выявлено, что количество колоний стволовых клеток, образующихся в селезенке исследуемых мышей, увеличивалось в 2-3 раза по сравнению с контрольными животными.
Далее был проведен детальный анализ клеток-мишеней циклофилина А в костном мозге. Клетки костного мозга получали путем промывания культуральной средой RPMI 1640 бедренной и большой берцовой костей мыши. Суспензию клеток получали, пропуская их через иглу шприца, и осаждали на центрифуге. Эритроциты удаляли 0,85% раствором NH4Cl, после чего отмывали раствором Эрла. Затем клетки разводили средой RPMI 1640 и использовали в концентрации 5×106%.
При оценке поверхностных маркеров мигрировавших клеток костного мозга использовали трансвеллы с величиной пор 5 микрон (Costar). Буфер, содержащий циклофилин А, помещали на дно 24-луночного планшета в количестве 600 мкл. Клетки костного мозга мышей (5×106/мл) помещали над мембраной в объеме 100 мкл и культивировали в течение 90 минут при 37°C и 5% CO2. В контрольный буфер (элюат с колонки) и буфер, содержащий циклофилин А, а также к клеткам костного мозга добавляли бычий сывороточный альбумин до конечной концентрации 0,5%. По истечении времени культивирования мембрану убирали и количество мигрировавших клеток на дне лунки подсчитывали при помощи микроскопа.
Для определения клеточного фенотипа был использован метод проточной цитофлуорометрии (FaxCalibur, Beckon Dickenson Cell Quest program). Идентификацию клеточных маркеров проводили при помощи флюоресцентномеченых моноклональных антител (Pharmingene), используя антитела к молекулам: CD31 (РЕ), Gr-l(CD97) (FITC), SCA-1 (FITC),CD3 (FITC), B220 (РЕ), CD19 (FITC),.CDllb(PE), CDllc (FITC). Погибшие клетки определяли добавлением пропидия йодида и исключали их из исследования.
Для определения мишеней, чувствительных к присутствию циклофилина А, проанализирован фенотип клеток костного мозга, мигрировавших in vitro под его влиянием.
SCA-1 маркер характеризует популяцию низкодифференцированных гемопоэтических стволовых клеток костного мозга. Влияние циклофилина А на миграцию стволовых SCA+ клеток представлено на Фиг.1А, при этом выявлено незначительное повышение количества клеток, несущих этот маркер. Влиянию циклофилина А подвержены клетки более поздней дифференцировки, утратившие молекулу SCA-1 на своей поверхности.
Молекула GR-1 (CD97) - маркер гранулоцитов различного уровня дифференцировки и зрелых нейтрофилов. Молекула адгезии CD31 присутствует на низкодифференцированных гранулоцитах (GR-1+ клетках) и ее количество снижается в процессе клеточного созревания (A.Solowiej, P.Biswas, D.Graesser, J.A.Madri. Lack of platelet endothelial cell adhesion molecule-1 attenuates foreign body inflammation because of decreased angiogenesis. American J. of Pathology. V.162. 2003. P.953-62). Незрелые предшественники гранулоцитов GR-1+CD31+, несущие обе анализируемые молекулы на своей поверхности, проявляют выраженную способность к миграции под влиянием циклофилина А. Влияние циклофилина А на миграцию предшественников гранулоцитов показано на Фиг.1В. Также наблюдалось увеличение миграции незрелых CD31+, не относящихся к гранулоцитарным предшественникам.
CD3+- маркер Т-клеточной популяции. В костном мозге имеются Т-клетки различной степени дифференцировки. Влияние циклофилина А на миграцию Т-клеток костного мозга представлено на Фиг.1C. Проведенный анализ показал, что Т-клетки высоко чувствительны к присутствию циклофилина А. Количество клеток, мигрировавших в присутствии циклофилина А, увеличилось более чем в 10 раз по сравнению с контролем.
При анализе B220+CD19+маркеров показано, что предшественники В-клеток также подвержены хемоаттрактивному действию циклофилина А, что отражено на Фиг.1D. Циклофилин А оказывает влияние на миграцию предшественников В-клеток разной степени дифференцировки (менее зрелых - B220+ и более зрелых B220+CD19+).
Циклофилин А стимулирует также миграцию предшественников дендритных клеток с фенотипом CDllb+CDllc+ и CDllc+, что представлено на Фиг.1Е. В то же время предшественники макрофагов с фенотипом CDllb+CDllc- не чувствительны к присутствию циклофилина А, что отличает их от зрелых моноцитов.
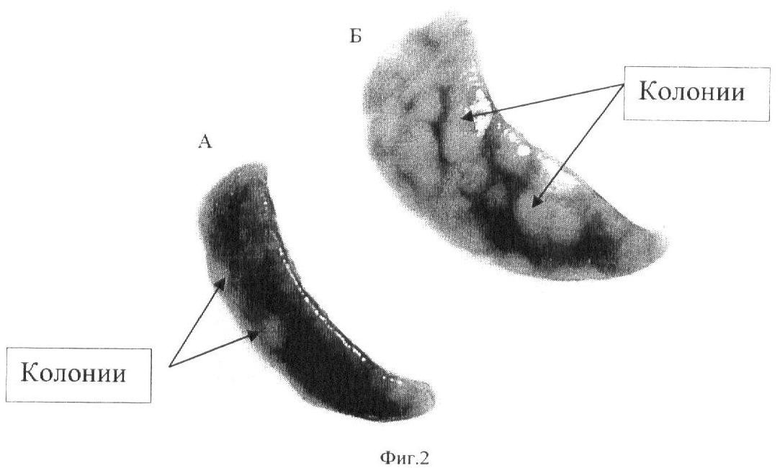
Оценка биологического действия рекомбинантного циклофилина А человека. Вследствие практически полной гомологичности (разница в одну аминокислоту) циклофилин А мыши и человека проявляет видовую неспецифическую активность. Влияние рекомбинантного циклофилина А человека, полученного из трансфецированных геном циклофилина А человека клеток E-coli, на образование селезеночных колоний стволовых клеток у сублетально облученных мышей представлено в таблице 1 и на Фиг.2 (А, Б). На Фиг.2А представлена селезенка мыши, обработанной буфером, на Фиг.2Б - селезенка мыши, обработанной 50 мкг циклофилина А. Как видно, циклофилин А значительно увеличивает миграцию стволовых клеток, образующих колонии в селезенке.
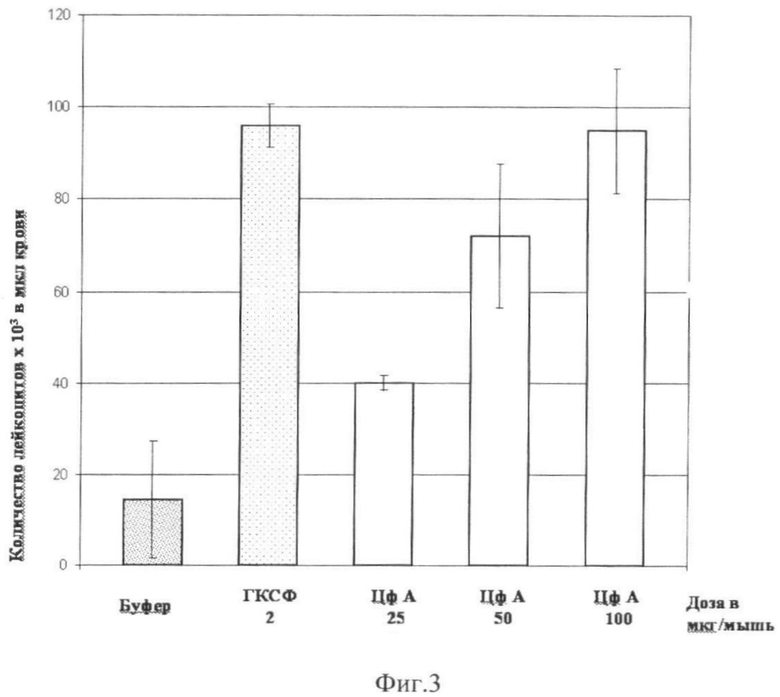
Для оценки способности циклофилина А восстанавливать кроветворение проводили сравнительный анализ его активности с ГКСФ на модели определения активности ГКСФ (Morrison SJ, Wright DE, Weissman IL. Cyclophosphamide/granulocyte colony-stimulating factor induces hematopoietic stem cells to proliferate prior to mobilization. Proc. Natl. Acad. Sci. USA Vol.94, pp.1908-1913, 1997). Мышей CBA (H-2к) обрабатывали циклофосфамидом, который вводили внутрибрюшинно в дозе 150 мг/кг веса. Через сутки мышам подкожно вводили циклофилин А (25, 50 и 100 мкг/мышь) или ГКСФ (2 мкг/мышь). В качестве контроля вводили буфер, используемый при очистке циклофилин А. Инъекции проводили в течение четырех дней, после чего кровь животных исследовали на содержание количества лейкоцитов, лимфоцитов, гранулоцитов и моноцитов.
Забор крови осуществляли из надреза хвостовой вены в объеме 5 микролитров и разводили ее в 95 микролитрах 3% уксусной кислоты. Мазки крови готовили на стекле, подсушивали, обрабатывали 96% этиловым спиртом в течение 1-2 с, повторно подсушивали и обрабатывали краской азур-эозином по Романовскому в течение 30-45 мин. Стекла промывали в воде, подсушивали и проводили микроскопическое исследование.
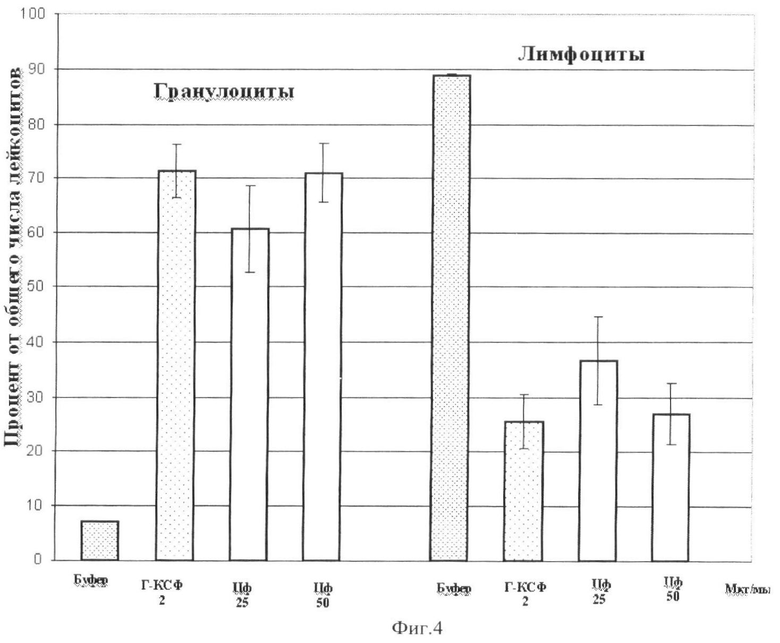
Полученные результаты выявили сопоставимое воздействие циклофилина А и ГКСФ на восстановление количества лейкоцитов периферической крови мышей, обработанных циклофосфамидом (в 103 на микролитр крови) (Фиг.3 и Табл.1). Циклофилин А так же как ГКСФ является средством, способствующим дифференцировке стволовых клеток костного мозга в гранулоциты, и мобилизует их выход в кровяное русло (Фиг.4, Табл.2).
Технический результат изобретения:
- Циклофилин А усиливает миграцию стволовых элементов из костного мозга на периферию у сублетально облученных животных.
- Стимулирует образование предшественников гранулоцитов и выход их из костного мозга в кровоток при применении химиотерапии.
- Стимулирует миграцию дендритных клеток и предшественников Т- и В-лимфоцитов.
Циклофилин А может быть использован как стимулятор гранулоцитопоэза, радиопротектор и иммуностимулятор.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ИНДУЦИРУЮЩЕЕ ДИФФЕРЕНЦИРОВКУ СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТОК В ТРОМБОЦИТЫ | 2012 |
|
RU2482870C1 |
| ИЗОЛИРОВАННЫЕ ПОПУЛЯЦИИ МИЕЛОИДОПОДОБНЫХ КЛЕТОК КОСТНОГО МОЗГА И СПОСОБЫ ЛЕЧЕНИЯ С НИМИ | 2006 |
|
RU2418856C2 |
| ПОПУЛЯЦИЯ СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТОК И ЕЕ ПРИМЕНЕНИЕ | 2003 |
|
RU2331669C2 |
| ВЫДЕЛЕННЫЕ ПОПУЛЯЦИИ МИЕЛОПОДОБНЫХ КЛЕТОК И СПОСОБЫ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ ТАКИХ ПОПУЛЯЦИЙ | 2007 |
|
RU2473686C2 |
| СПОСОБ РАЗМНОЖЕНИЯ КРОВЕТВОРНЫХ СТВОЛОВЫХ КЛЕТОК | 2002 |
|
RU2297451C2 |
| СПОСОБ ПОЛУЧЕНИЯ РЕЗИДЕНТНЫХ СТВОЛОВЫХ КЛЕТОК СЕРДЦА МЛЕКОПИТАЮЩЕГО ИЗ ОБРАЗЦОВ МИОКАРДА | 2012 |
|
RU2505602C1 |
| ГУМАНИЗИРОВАННЫЕ IL-6 И РЕЦЕПТОР IL-6 | 2012 |
|
RU2751240C2 |
| ГЕМАТОПОЭТИЧЕСКИЕ СТВОЛОВЫЕ КЛЕТКИ И СПОСОБЫ ЛЕЧЕНИЯ НЕОВАСКУЛЯРНЫХ ЗАБОЛЕВАНИЙ ГЛАЗ С ИХ ПОМОЩЬЮ | 2006 |
|
RU2389497C2 |
| ГЕМАТОПОЭТИЧЕСКИЕ СТВОЛОВЫЕ КЛЕТКИ И СПОСОБЫ ЛЕЧЕНИЯ НЕОВАСКУЛЯРНЫХ ЗАБОЛЕВАНИЙ ГЛАЗ С ИХ ПОМОЩЬЮ | 2004 |
|
RU2345780C2 |
| СПОСОБ ЛЕЧЕНИЯ РЕТИНОПАТИИ ПРИ НЕДОНОШЕННОСТИ И РОДСТВЕННЫХ РЕТИНОПАТИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2403906C2 |

Изобретение относится к медицине, в частности к стимулирующим гранулоцитопоэз, радиопротекторным и иммуностимулирующим средствам. При воздействии цитостатиков циклофилин А усиливает выход предшественников гранулоцитов из костного мозга и является веществом, стимулирующим гранулоцитопоэз. При сублетальном облучении циклофилин А стимулирует миграцию стволовых элементов костного мозга и участвует в восстановлении клеток крови, иммунной системы и обладает радиопротекторными свойствами. 4 ил., 2 табл.
Циклофилин А - стимулятор гранулоцитопоэза, радиопротектор и иммуностимулятор.
| KHROMYKH L.M | |||
| et al | |||
| Cyclophilin A produced by thymocytes regulates the migration of murine bone marrow cells | |||
| Cell Immunol | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ЯРИЛИН А.А | |||
| Основы иммунологии: учебник | |||
| - М.: Медицина, 1999 | |||
| Большой словарь медицинских терминов | |||
| Сост | |||
| Федотов В.Д | |||
| - М.: ЗАО Центрполиграф, 2007, с.254 | |||
| Большая медицинская энциклопедия, 1983, | |||
Авторы
Даты
2009-10-20—Публикация
2008-04-21—Подача