Изобретение относится к комплексам оксалата димеди(I), стабилизированным нейтральными основаниями Льюиса, такими, как алкены или алкины, и применению комплексов оксалатов димеди(I) в качестве исходных продуктов для осаждения металлической меди, при которых в качестве нейтрального основания Льюиса применяются алкины, алкены, триарилфосфины, СО и изонитрилы.
1. Уровень техники и задача изобретения
Для осаждения тонких слоев меди на субстраты известны многие медноорганические исходные вещества. При этом в качестве многообещающих веществ проявили себя медьсодержащие соединения со степенью окисления +1, которые содержат лиганды β-дикетоната и нейтральное основание Льюиса L, такое, как, например, алкен или алкин. Подобные комплексы и их применение в качестве исходных продуктов в процессе CVD (процесс химического осаждения из паровой фазы) описаны, например, в источниках US 5220044, WO 00/71550, WO 00/17278, US 6130345 или Chem. Mater. 2001, 13, 3993; Inorg. Chem. 2001, 40, 6167; Chem. Mater. 1992, 4, 365; Organometallics 2001, 20, 4001. Предпочтительно применяются фторсодержащие лиганды β-дикетоната, такие, как, например, гексафторацетилацетонат, так как соответствующие комплексы меди(I) имеют намного более высокую химическую стабильность и более высокую летучесть, чем их свободные от фтора аналоги. Свободные от фтора комплексы β-дикетонатов меди(I), такие, как, например, стабилизированные алкином ацетилацетонаты меди(I), являются крайне чувствительными к кислороду, разлагаются уже при 0°С (см. публикацию Chem. Ber. 1995, 128, 525) и таким образом не пригодны в качестве исходного продукта для процесса CVD. Осаждение слоя меди происходит термически индуцированным диспропорционированием согласно следующему уравнению:
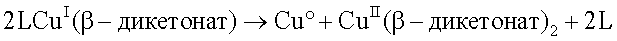
Полученный CuII(β-дикетонат)2 и основание Льюиса L при применяемых в процессе условиях являются летучими и поэтому могут быть удалены из системы.
Остается в идеальном случае высокочистый медный слой. В этой реакции в медь(0) могут превращаться только 50% примененного исходного продукта меди(I), остальные 50% приходятся на соответствующий CuII(β-дикетонат)2. Тот же результат получают при применении сложного β-кетоэфира вместо β-дикетонов, как, например, описано в WO 00/08225 или в US 5441766. Недостатком при применении фторсодержащего исходного продукта меди(I) является то, что адгезия тонкого медного слоя к различным поверхностям субстратов не является оптимальной, что возможно является следствием Ван-дер-ваальсовых сил атомов фтора в молекуле исходного продукта и соответственно отталкивающим взаимодействием. К тому же имеется опасность загрязнения подложки, в частности кремния, фтором, что приводит к непригодности подложки.
Полная конверсия меди достигается стабилизированными основаниями Льюиса алкоксидами меди(I) формулы LCuIOR (EP 0468396) и стабилизированными основаниями Льюиса циклопентадиенилами меди(I) формулы LCuI(η5-C5R5), описанными в EP 0297348 и DE 4124686. Частично примеры в названных патентах являются даже свободными от фтора и стабильными при 25°С. В связи с тем, что термические реакции разложения в этих случаях протекают неопределенно, в реакциях разложения образуются радикальные реагенты, которые, к сожалению, приводят к загрязненным медным слоям (кислорода прибл. 5%, углерода прибл. 1%) (см. MRS Bulletin/August 1994, 41; Chem. Mater. 1992, 4, 577).
Задача настоящего изобретения поэтому заключается в разработке свободных от фтора, простых и изготавливаемых недорогими методами исходных продуктов меди(I) для осаждения металлической меди, которые термически стабильны и по возможности светостабильны и которые могут быть термически полностью превращены в металлические медные тонкие слои в реакции разложения в температурном интервале прибл. 50-400°С с образованием определенных молекулярных, свободных от меди, неядовитых и, по возможности, газообразных побочных продуктов. Другая задача предлагаемого изобретения заключается в разработке наряду с простым и недорогим способом получения исходных веществ согласно изобретению пригодного способа получения тонких высокочистых медных пленок или слоев с помощью этих исходных продуктов и таким образом улучшенных высокочистых тонких слоев меди.
Согласно изобретению для получения высокочистых тонких медных металлических слоев применяют соединения общей формулы (II)
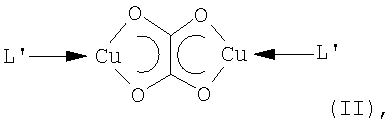
где медь имеется со степенью окисления +1 и
L' означает ненасыщенный углеводород с, по меньшей мере, одной олефиновой или ацетиленовой группой или СО, Р(арил)3 или изонитрил RN≡C,
где R означает А, арил или алкиларил,
А означает неразветвленный или разветвленный С1-С30-алкил, С3-С30-циклоалкил, неразветвленный или разветвленный С2-С30-алкенил, неразветвленный или разветвленный С3-С30-циклоалкенил,
арил означает С6-С10-арилы,
алкиларил С7-С18-алкиларилы.
Хороший результат получают с соединениями общей формулы (II), при которых
LII означает ненасыщенный углеводород, выбранный из группы, включающей нециклические С2-С30 алкены или циклические С4-С30 алкены, нециклические С2-С30 алкины или циклические С10-С30 алкины, СО, Р(арил)3 или RN≡C,
где R означает А,
арил означает фенил и
А означает неразветвленный или разветвленный С1-С30-алкил, С3-С30-циклоалкил.
Особенно хорошие результаты достигают соединениями общей формулы (II), в которых
L' означает ненасыщенный углеводород из ряда нециклических С2-С15 алкенов или циклических С4-С15 алкенов, нециклических С2-С15 алкинов или циклических С10-С15 алкинов или СО, Р(С6Н5)3 или RN≡C,
где R означает А,
А означает неразветвленный или разветвленный С1-С8-алкил, С3-С10-циклоалкил.
Из этой группы особенно предпочтительны соединения, при которых нециклический С2-С15 алкен означает этен, пропен, изомеры бутена, пентена, гексена, гептена, октена, нонена или децена, и/или циклический С4-С15 алкен означает циклобутен, циклопентен, циклогексен, циклогептен, циклооктен, циклопентадиен, циклогексадиен, циклооктадиен, норборнен, норборнадиен, которые могут быть замещены углеводородом, и/или нециклический С2-С15 алкин означает ацетилен, пропин, изомеры бутина, пентина, гексина, гептина, октина, нонина, децина или дифенилацетилена, и/или циклический С10-С15 алкин означает циклодецин, циклодекадиин, циклододецин или циклододекадиин, которые могут быть замещены углеводородом. В одинаковой степени предпочтительны соединения, при которых L' означает изонитрилы, циклогексилизонитрил или фенилизонитрил.
Поставленная задача изобретения решается предпочтительно соединениями общей формулы (I)
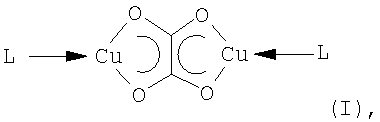
где медь имеется со степенью окисления +1 и
L означает углеводород из ряда нециклического алкина формулы R-C≡C-R' или циклического С10-С20 алкина или нециклического внутреннего алкена формулы R″HC=CHR′′′ или циклического С4-С20 алкена,
где R, R' означают Н, А, алкиларил или алкинил,
R″, R′′′ означают А, арил, алкиларил или алкинил,
причем L, R, R', R″ и R′′′ каждый независимо друг от друга в различных положениях молекулы может принимать различные или одинаковые значения, и
А означает неразветвленный или разветвленный С1-С30-алкил, С3-С30-циклоалкил, неразветвленный или разветвленный С2-С30-алкенил, неразветвленный или разветвленный С3-С30-циклоалкенил,
арил означает С6-С10-арилы,
алкиларил означает С7-С18-алкиларилы,
алкил означает неразветвленный или разветвленный С2-С30-алкинил.
Эти новые соединения являются при этом другим объектом настоящего изобретения.
Соединениями согласно изобретению являются предпочтительно также и соединения общей формулы (I),
где А означает неразветвленный или разветвленный С1-С9-алкил, неразветвленный или разветвленный С3-С9-циклоалкил, неразветвленный или разветвленный С2-С9-алкенил, неразветвленный или разветвленный С3-С9-циклоалкенил,
арил означает фенил, нафтил,
алкиларил означает толуил или мезитил,
алкинил означает неразветвленные или разветвленные С2-С9-алкинилы
и L, R, R', R″ и R′′′ каждый независимо друг от друга в различных положениях молекулы может принимать различные или одинаковые значения.
Другие предпочтительные подгруппы образуют соединения общей формулы (I),
где
I.
А означает неразветвленные или разветвленные С1-С4-алкилы, выбранные из группы, включающей метил, этил, н- и изопропил или н-, изо- и трет-бутил, С3-С6-циклоалкилы из группы, включающей циклопропил, циклобутил, цикпопентил и циклогексил, неразветвленный или разветвленный С2-С6-алкенил из группы, включающей винил, пропенил, бутенил, пентенил или гексенил, С3-С6-цикпоалкенилы из группы, включающей циклопропенил, циклобутенил, циклопентенил, циклопентадиенил и метилциклопентадиенил,
арил означает фенил,
алкиларил означает толуил или мезитил,
алкинил означает неразветвленные или разветвленные С2-С6-алкинилы из группы, включающей этинил, пропинил, бутинил, пентинил или гексинил,
и R, R', R″ и R′′′ каждый независимо друг от друга в различных положениях молекулы может принимать различные или одинаковые значения,
или
II.
где L означает нециклический алкин, выбранный из группы, включающей
Me-C≡C-Me, Et-C≡C-Et, Pr-C≡C-Pr или Bu-C≡C-Bu,
или
III.
где L означает циклический алкин, выбранный из группы, включающей циклодецин, циклодекадиин, циклододецин, циклододекадиин,
или
IV.
где L означает нециклический внутренний алкен, выбранный из группы, включающей HR″C=CHR′′′, где R″, R′′′ означают независимо друг от друга СН3, С2Н5, С3Н7, С4Н9,
или
V.
где L означает циклический алкен, выбранный из группы, включающей циклобутен, циклопентен, циклопентадиен, циклогексен, циклогексадиен, циклогептен, циклогептадиен, циклооктен, циклооктадиен, норборнен или норборнадиен.
Особенно предпочтительно задача изобретения решается новыми соединениями общей формулы (I):
оксалатом ди[(3-гексин)медь(I)] и
оксалатом ди[(норборнен)медь(I)].
Соединения согласно изобретению, соответственно, применяемые согласно изобретению соединения могут быть получены способом, при котором Cu2O подвергают взаимодействию с щавелевой кислотой и основанием Льюиса L в инертном растворителе и выделяют полученный продукт. Этот способ является также объектом настоящего изобретения.
Получение высокочистых тонких металлических медных слоев осуществляют способом, для проведения которого соединения общей формулы (II) нагревают, вследствие чего основание Льюиса L' отщепляется и металлическая медь осаждается декарбоксилированием. Также и этот способ получения является объектом настоящего изобретения.
Отщепление основания Льюиса L' осуществляют в температурном интервале от прибл. 50 до прибл. 200°С. Следующее как вторая реакция декарбоксилирование при образовании металлической меди и диоксида углерода заканчивают предпочтительно в температурном интервале прибл. от 150 до 350°С.
Отщепленное основание Льюиса L' предпочтительно регенерируют и снова возвращают в способ получения соединений общей формулы (II) и применяют для получения высокочистых металлических медных слоев.
Таким образом, поставленная задача изобретения решается высокочистыми тонкими металлическими медными слоями с улучшенными свойствами при применении соединения общей формулы (II) в способе согласно изобретению.
2. Подробное описание изобретения
Настоящим изобретением получают соединения общей формулы (I)

где независимо от положения в комплексе и независимо друг от друга
L означает нециклический алкин R-C≡C-R' или циклический алкин или нециклический алкен R″HC=CHR′′′ или циклический алкен. Степень окисления меди составляет +1.
R и R' могут независимо друг от друга означать Н или углеводород из группы, включающей алкил, циклоалкил, алкенил, циклоалкенил, алкиларил или алкинил.
R″ и R′′′ могут независимо друг от друга означать углеводород из группы, включающей алкил, циклоалкил, алкенил, циклоалкенил, арил, алкиларил или алкинил.
Получение соединения общей формулы (I) осуществляют взаимодействием Cu2O, щавелевой кислоты и нейтрального лиганда L или двух различных нейтральных лигандов в инертном апротонном органическом растворителе. Соединения общей формулы (I) могут быть чисто выделены как термостабильные вещества I. К тому же полученные вещества отличаются неожиданно и необычно высокой стойкостью к окислению, они могут без проблем применяться на воздухе, что намного облегчает дальнейшее применение веществ в качестве исходных продуктов для осаждения металлической меди.
Если нагревают соединения общей формулы (II)
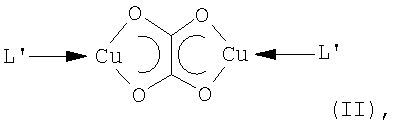
где медь имеет степень окисления +1 и
L' означает ненасыщенный углеводород с, по меньшей мере, одной олефиновой или ацетиленовой группой или СО, Р(арил)3 или изонитрил RN≡C,
причем R означает алкил, циклоалкил, алкенил, циклоалкенил, арил, алкиларил или алкинил, то остается высокочистый слой меди; все побочные продукты являются летучими и могут очень просто удаляться из реакции. Термическое разложение происходит согласно уравнению:
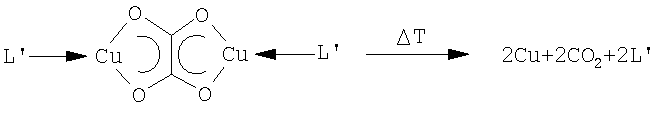
В качестве продуктов реакции образуются наряду с металлической медью только диоксиды углерода и основание Льюиса L', которые могут регенерироваться и повторно применяться.
Соединения общей формулы (II) в качестве исходного продукта для осаждения металлической меди.
Осаждение может осуществляться из газовой фазы или из раствора, содержащего исходный продукт и подходящий растворитель или из исходного продукта в твердом состоянии посредством контакта исходного продукта с нагретым субстратом. По сравнению с уровнем техники дает преимущества то, что сначала получают исходные продукты меди (I), которыми может количественно осаждаться металлическая медь в свободной от радикалов реакции разложения с образованием высокочистого тонкого слоя меди. Этим можно повышать выход осажденной металлической меди с 50 до 100% по сравнению с уровнем техники. Высокая стойкость и нечувствительность соединений, в особенности высокая стойкость к окислению, упрощает обращение с соединениями в способе осаждения металлической меди и положительно отражается на стоимости процесса осаждения.
Таким образом, преимуществами соединений общей формулы (II) по сравнению с применяемыми в уровне техники веществами (CupraSelect®) являются следующие: лучшие физические свойства, такие, как более высокая термическая стойкость, лучшие химические свойства, такие, как более высокая стойкость к окислению, упрощенное обращение, связанный с низкими затратами синтез вследствие недорогого исходного вещества (щавелевой кислоты) по сравнению с гексафторацетилацетоном, вдвое более высокий выход металлической меди в процессе осаждения, несодержащие медь и неядовитые побочные продукты, меньшее количество побочных продуктов и таким образом более низкая нагрузка для окружающей среды. К тому же в соединениях не содержатся атомы фтора, которые могут приводить к загрязнению фтором и этим к невозможности использования подложки.
В общем синтез исходных продуктов меди(I) упрощается и удешевляется по сравнению с имеющимися на рынке исходными продуктами меди(I) CupraSelect®, причем здесь речь идет о (триметилвинилсилан)медь(I)гексафторацетилацетоне. Одновременно исходные продукты согласно изобретению способствуют повышению качества слоев меди и обеспечивают безопасный для окружающей среды способ осаждения.
Соединения согласно изобретению общей формулы (I) содержат один дианион оксалата, два медных центра в степени окисления +1 и, по меньшей мере, два нейтральных лиганда L, причем дианион оксалата в качестве мостика в µ-1,2,3,4-модусе связан с обоими центрами меди(I). Конструкция оксалата димеди(I) CuO2C2O2Cu стабилизируется координацией, по меньшей мере, двух нейтральных лигандов L к обоим центрам меди(I), предпочтительно двух одинаковых лигандов L, так что оба центра меди(I) имеют, по меньшей мере, одно псевдо-тригонально-плоское, в случае необходимости, тетраэдрическое окружение. Содержащиеся в комплексе атомы меди могут быть присоединены к двум различным лигандам L. Ниже для упрощения в общем речь будет идти об одном лиганде или основании Льюиса L, хотя под этим можно понимать также два различных лиганда или основания Льюиса L.
L означает нециклический алкин R-C≡C-R' или циклический С10-С20 алкин или нециклический алкен R″HC=CHR′′′ или циклический С4-С20 алкен. R и R' могут независимо друг от друга означать Н, алкил, циклоалкил, алкенил, циклоалкенил, алкиларил или алкинил. R″ и R′′′ могут независимо друг от друга означать алкил, циклоалкил, алкенил, циклоалкенил, арил, алкиларил или алкинил.
Циклические С10-С20-алкины могут быть неразветвленными или разветвленными С10-С20 циклоалкинами, предпочтительно неразветвленными или разветвленными С10-С15 циклоалкинами, особенно предпочтительно С10-С12 циклоалкинами из группы, включающей циклодецин, циклодекадиин, циклододецин, циклододекадиин.
Циклические С4-С20-алкены могут быть неразветвленными или разветвленными С4-С20-циклоалкенами, предпочтительно неразветвленными или разветвленными С4-С15-циклоалкенами, особенно предпочтительно С4-С8-циклоалкенами из группы, включающей циклобутен, циклопентен, циклопентадиен, циклогексен, циклогексадиен, циклогептен, циклогептадиен, циклооктен, циклооктадиен, норборнен или норборнадиен.
Алкильные группы могут быть неразветвленными или разветвленными С1-С30-алкилами, предпочтительно неразветвленными или разветвленными С1-С9-алкилами, особенно предпочтительно неразветвленными или разветвленными С1-С4-алкилами из группы, включающей метил, этил, н- и изопропил или н-, изо- и трет-бутил. Циклоалкильные группы могут быть неразветвленными или разветвленными С3-С30-циклоалкилами, предпочтительно С3-С9-циклоалкилами, особенно предпочтительно С3-С6-циклоалкилами из группы, включающей циклопропил, циклобутил, циклопентил и циклогексил.
Алкенильные группы могут быть неразветвленными или разветвленными С2-С30-алкенилами, предпочтительно неразветвленными или разветвленными С2-С9-алкенилами, особенно предпочтительно неразветвленными или разветвленными С2-С6-алкенилами из группы, включающей винил, пропенил, бутенил, пентенил или гексенил. Циклоалкенильные группы могут быть неразветвленными или разветвленными С3-С30-циклоалкенилами, предпочтительно С3-С9-циклоалкенилами, особенно предпочтительно С3-С6-циклоалкенилами из группы, включающей циклопропенил, циклобутенил, циклопентенил, циклопентадиен ил и метилциклопентадиенил.
Арильные группы могут быть С6-С10-арилами, предпочтительно фенилом или нафтилом. Алкиларилы могут быть С7-С18-алкиларилами, предпочтительно толуилом или мезитилом.
Алкинильные группы могут быть неразветвленными или разветвленными С2-С30-алкинилами, предпочтительно неразветвленными или разветвленными С2-С9-алкинилами, особенно предпочтительно неразветвленными или разветвленными С2-С6-алкинилами из группы, включающей этинил, пропинил, бутинил, пентинил или гексинил.
В качестве нейтральных оснований Льюиса особенно хорошо пригодны нециклические алкины формулы R-C≡C-R', циклические алкины, нециклические алкены формулы R′′HC=CHR′′′ и циклические алкены. Предпочтительно применяют нециклические алкины из группы R-C≡C-R' и особенно хорошие результаты получают с алкинами R-C≡C-R' (R, R'=СН3, С2Н6, С3Н7, С4Н9). Предпочтительно применяют нециклические алкены из группы R′′HC=CHR′′′ (R′′, R′′′=СН3, C2H5, С3Н7, С4Н9) и циклические алкены, и особенно хорошие свойства достигают применением циклических алкенов (циклогексен и норборнен). Особенно хорошие результаты получают с алкином Et-C≡C-Et и алкеном норборненом.
Получение соединений общей формулы (I) осуществляют предпочтительно взаимодействием Cu2O, щавелевой кислоты и основания Льюиса L под атмосферой защитного газа в инертном апротонном органическом растворителе. В качестве основания L могут применяться два различных основания Льюиса L в эквимолярном соотношении. Последовательность подачи компонентов может быть любой. Если в качестве основания Льюиса L должна применяться смесь из двух различных соединений, то предпочтительно оба соединения подаются в реакцию одновременно или перед подачей смешиваются друг с другом. Исходные соединения могут быть предварительно растворены, соответственно, суспендированы в подходящем растворителе или могут подаваться без растворителя в виде твердого вещества, соответственно, жидкости. В качестве пригодных растворителей для проведения реакции могут применяться инертные апротонные растворители, такие, как нециклические или циклические алифатические и ароматические углеводороды, которые могут быть частично галогенированы, или простые эфиры и циклические эфиры. Особенно предпочтительно применение таких растворителей, как пентан, гексан, гептан, циклогексан, толуол, метиленхлорид, трихлорметан, хлорбензол, диэтиловый эфир или тетрагидрофуран. В качестве защитной атмосферы может служить азот или аргон. Стехиометрическое соотношение исходных продуктов Cu2O, щавелевой кислоты и основания Льюиса L составляет между 1:1:2 и 1:1:4, предпочтительно между 1:1:2 и 1:1:3 и особенно предпочтительно 1:1:2. Основание Льюиса L не следует добавлять в пониженном относительно щавелевой кислоты Cu2O количестве. Реакцию можно осуществлять в температурном интервале от -30 до +100°С, предпочтительно от 0 до 50°С и особенно предпочтительно от 20 до 40°С. Самый высокий выход получают при комнатной температуре. Время реакции составляет от одного часа до 24 часов, предпочтительно от 2 до 8 часов и особенно предпочтительно от 3 до 6 часов.
Реакционный раствор изменяется, начиная от красной суспензии и до бесцветного или коричневатого раствора или суспензии в зависимости от вида получаемого комплекса. Нерастворимые компоненты отделяют. Это может осуществляться фильтрацией, центрифугированием или другими, известными специалисту в данной области методами. Получают прозрачный бесцветный, желтый или красный раствор в зависимости от вида применяемого основания Льюиса L. В заключение соединения общей формулы (I) выделяют. Это может осуществляться после удаления растворителя известным специалисту методом. В случае необходимости, производят дальнейшую очистку. Вместо механического отделения твердого вещества из реакционной смеси фильтрацией или другими методами можно осуществлять также и экстракцию для отделения образовавшегося продукта. Соединения общей формулы (I) являются, как указано выше, неожиданным образом чрезвычайно термостабильными и могут хорошо выделяться в качестве чистых веществ и затем аналитически и спектроскопически охарактеризовываться.
Соединения согласно изобретению общей формулы (II)

могут применяться для получения высокочистых тонких слоев металлической меди.
L' означает нециклический алкин R-C≡C-R', циклический алкин, нециклический алкен RHC=CHR', циклический алкен, СО, Р(арил)3 или изонитрил RN≡C. R и R' могут независимо друг от друга означать Н, алкил, циклоалкил, алкенил, циклоалкенил, арил, алкиларил или алкинил.
Значения для алкила, циклоалкила, алкенила, циклоалкенила, арила, алкиларила или алкинила соответствуют значениям в соединениях общей формулы (I).
Циклоалкины могут быть неразветвленными или разветвленными С10-С20-циклоалкинами, предпочтительно неразветвленными или разветвленными С10-С15-циклоалкинами, особенно предпочтительно С10-С12-циклоалкинами из группы, включающей циклодецин, циклодекадиин, циклоундецин, циклоундекадиин, циклододецин, циклододекадиин.
Циклоалкены могут быть неразветвленными или разветвленными С4-C2O-циклоалкенами, предпочтительно неразветвленными или разветвленными С4-С15 циклоалкенами, особенно предпочтительно С4-С8-циклоалкенами из группы, включающей циклобутен, циклопентен, циклопентадиен, циклогексен, циклогексадиен, циклогептен, циклогептадиен, циклооктен, циклооктадиен, норборнен или норборнадиен.
В качестве нейтральных оснований Льюиса L' особенно хорошо пригодны нециклические алкины формулы R-C≡C-R', циклические алкины, нециклические алкены формулы RHC=CHR', циклические алкены, СО, Р(арил)3 и RN≡C. Предпочтительно применяют нециклические алкины из группы, включающей R-C≡C-R', нециклические алкены формулы RHC=CHR', циклические алкены, СО и RN≡C. Особенно хорошие результаты достигаются с такими основаниями, как алкины R-C≡C-R' (R, R'=СН3, С2Н5, С3Н7 С4Н9), нециклические алкены RHC=CHR' (R, R'=СН3, С2Н5, С3Н7, С4Н9), циклические алкены (циклогексен и норборнен), с СО и RN≡C (R=трет-C4H9, С6Н11, С6Н5). Предпочтительно применяют нециклические алкены из группы, включающей RHC=CHR' (R, R'=СН3, С2Н5, С3Н7, С4Н9), циклические алкены (циклогексен и норборнен), СО и C6H11N≡С и особенно хорошие результаты получают при применении таких оснований, как нециклический алкин Et-C≡C-Et, циклический алкен, норборнен, СО и C6H11N≡С. Более хорошие результаты получают при применении алкина Et-C≡C-Et и алкена норборнена.
Термические свойства соединений может быть исследованы с помощью TGA (термогравиметрический анализ) и DSC (дифференциальная сканирующая колориметрия). Проведенные исследования показывают, что разложение соединений согласно изобретению происходит за 2 главные стадии:

Сначала основание Льюиса L' отщепляется от комплекса меди(I). Это отщепление может происходить в зависимости от соединения ступенчато и может устанавливаться термогравиметрическим анализом. На второй стадии вследствие внутренней окислительно-восстановительной реакции оставшегося фрагмента CuO2C2O2Cu происходит декарбоксилирование при образовании металлической меди и диоксида углерода. Первая стадия происходит в зависимости от исходного продукта в температурном интервале от прибл. 50 до прибл. 200°С, вторая стадия от прибл. 150°С и заканчивается при прибл. 350°С. При этом отщепление оснований Льюиса и реакция декарбоксилирования при переходе к более высоким температурам могут протекать параллельно. Остаточное содержание соответствует точно доле меди в соответствующем исходном продукте меди(I), так что выход металлической меди при соединениях общей формулы (II) составляет 100% и таким образом вдвойне выше, чем в известном уровне техники.
Вследствие эффективной реакции разложения соединений общей формулы (II) образуется меньше побочных продуктов по сравнению с уровнем техники. В процессе осаждения образуется свободное основание Льюиса L', которое может улавливаться соответствующими устройствами, такими, как, например, охлаждающие уловители в отводимом газе, и снова использоваться; в качестве второго побочного продукта образуется диоксид углерода. Побочные продукты, таким образом, по сравнению с уровнем техники, при котором в качестве побочных продуктов образуется гексафторацетилацетонат меди(II) и основание Льюиса (триметилвинилсилан), не содержат меди, нетоксичны и поэтому безопасны. Таким образом, нагрузка окружающей среды значительно меньше, чем при применении соединений из уровня техники.
В качестве термически стабильного и особенно мало чувствительного к окислению проявил себя (норборнен)2Cu2O4C2. Соединение стабильно до 100°С и может продолжительное время быть на воздухе. По сравнению с уровнем техники это является огромным преимуществом, так как CupraSelect® уже, начиная от прибл. 50°С, медленно разлагается и соединение окисляется быстрее на воздухе до меди(II). Это позволяет намного более простое обращение не только при синтезе, но также и в процессе осаждения.
Соединения общей формулы (II) могут применяться в качестве исходных продуктов для осаждения металлической меди. Осаждение слоев металлической меди может происходить из газовой фазы, или из раствора исходных продуктов в пригодном растворителе, или из твердого исходного продукта контактированием исходного продукта с нагретым субстратом.
Для наглядности и для лучшего понимания настоящего изобретения ниже приведены примеры. Эти примеры вследствие общего действия описанного принципа изобретения не пригодны для ограничения объема защиты настоящего изобретения только этими примерами. Далее содержание цитируемых патентных заявок следует рассматривать как часть раскрытия настоящего изобретения, лежащего в основе описания.
3. Примеры
Пример 1
Оксалат ди[(3-гексин)медь(I)]
К суспензии из 1,8 г Cu2O в 30 мл метиленхлорида в атмосфере инертного газа добавляют 3 мл EtC≡CEt и 1,1 г щавелевой кислоты и реакционную смесь перемешивают в течение 4 часов при комнатной температуре. Для отделения нерастворимых остатков раствор подают на пористый стеклянный фильтр с силикагелем и остаток на фильтре промывают два раза метиленхлоридом. Бесцветный раствор концентрируют и при -30°С получают бесцветные кристаллы (EtC≡CEt)2Cu2O4C2.
C14H20Cu2O4 (379,40 г/моль). Анализ [%]: рассчитано: С 44,3, Н 5,3; получено: С 44,7, Н 4,9. IR (KBr) [см-1]: νC≡C 2053, 2020 (w), νCO2 1645 (vs), 1355 (w), 1314 (m). 1H-ЯМР (CDCl3): δ 1,22 (t, 12Н, 3J=7,3 Hz, СН3), 2,49 (q, 8Н, 3J=7,4 Hz, CH2). 13С{1H}ЯМР (CDCl3): δ 14,4 (СН3), 15,5 (CH2), 87,6 (С≡С), 171,4 (COO). MS (m/z (%)): 525 (7) [M+Cu(EtC≡CEt)+, 443 (7) [M+Cu]+, 227 (100) [M-CuO4C2]+, 145 (96) [M-(EtC≡CEt)CuO4C2]+. TG (30-1000°С, 5°С/мин): разложение в три стадии.
Стадия 1: температурный интервал 60-120°С, снижение веса 22% (EtC≡CEt).
Стадия 2: температурный интервал 120-150°С, снижение веса 19% (EtC≡CEt).
Стадия 3: температурный интервал 200-310°С, снижение веса 24% (2 CO2), остаточное количество 35% (2 Cu).
На фиг.1 показано разложение полученного оксалата ди[(3-гексин)медь(I)] в зависимости от температуры при осаждении тонкого слоя меди на субстрат.
Пример 2
Оксалат ди[(норборнен)медь(I)]
К суспензии из 1,8 г Cu2O в 50 мл метиленхлорида в инертной газовой атмосфере добавляют 2,4 г норборнена и 1,1 г щавелевой кислоты и перемешивают при комнатной температуре в течение 5 часов. Для отделения нерастворимых остатков раствор подают на пористый стеклянный фильтр с силикагелем и остаток два раза промывают метиленхлоридом. Бесцветный раствор конденсируют и при -30°С получают бесцветные кристаллы (норборнена)2Cu2O4C2.
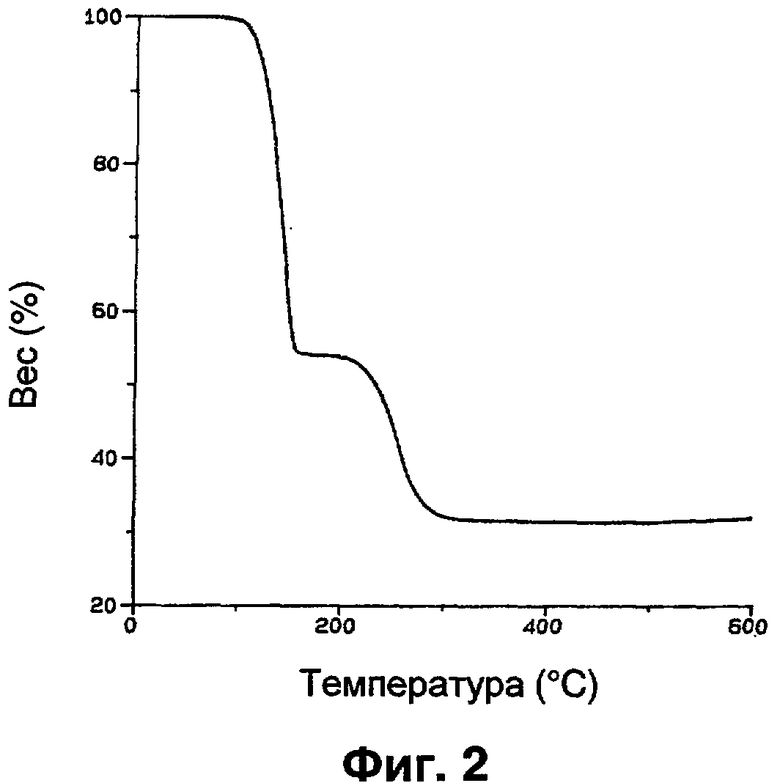
C16H20Cu2O4 (403,43 г/моль). IR (KBr) [см-1]: νC=C 1473 (w); νCO2 1644 (m), 1362 (m), 1303 (vs). 1Н-ЯМР (CDCl3) [ч/млн]: 1,00 (d, 2J=7,8 Hz, 2H, Hendo), 1,03 (d, 2J=9,5 Hz, 1H, Hanti), 1,28 (d, 2J=9,6 Hz, 1H, Hsyn), 1,59 (d, 2J=7,7 Hz, 2H, Hexo), 3,08 (s, 2H, CH), 5,25 (s, 2H,=CH). 13С{1H}ЯМР (CDCl3) [ч/млн]: 24,4 (CH2CH2), 42,7 (СНСН2), 45,7 (CHCH2CH), 109,2 (=СН), 171,4 (COO). TG (30-1000°C, 5°С/мин): разложение в две стадии, стадия 1: температурный диапазон 100-150°С, снижение веса 46% (2 норборнен), стадия 2: температурный диапазон 200-300°С, снижение веса 23% (2 CO2), остаток 31% (2 Cu).
На фиг.2 представлено разложение полученного оксалата ди[(норборнен)медь(I)] в зависимости от температуры при осаждении на субстрат тонкого слоя меди.
Перечень чертежей
На фиг.1 показано разложение полученного согласно примеру 1 оксалата ди[(3-гексин)медь(I)] в зависимости от температуры при осаждении тонкого слоя меди на субстрат (измерение согласно термогравиметрическому анализу TGA).
На фиг.2 представлено разложение полученного согласно примеру 2 оксалата ди[(норборнен)медь(I)] в зависимости от температуры при осаждении тонкого слоя меди на субстрат (измерение согласно термогравиметрическому анализу TGA).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСЫ ОКСАЛАТА ДИМЕДИ (I) В КАЧЕСТВЕ ВЕЩЕСТВ-ПРЕДШЕСТВЕННИКОВ ДЛЯ НАНЕСЕНИЯ МЕТАЛЛИЧЕСКОЙ МЕДИ | 2003 |
|
RU2322447C2 |
| СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 2006 |
|
RU2392283C2 |
| ГИДРОФОБНЫЕ ФУНКЦИОНАЛИЗИРОВАННЫЕ ЧАСТИЦЫ | 2011 |
|
RU2571758C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ СТИМУЛЯЦИИ РОСТА НЕВРИТОВ | 1996 |
|
RU2197240C2 |
| КОМПОНЕНТ КАТАЛИЗАТОРА, КАТАЛИЗАТОР И КАТАЛИЗАТОР ПРЕПОЛИМЕРИЗАЦИИ, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПОЛИМЕРИЗАЦИИ ОЛЕФИНА, И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНА | 2018 |
|
RU2776708C2 |
| ФОТОРЕЗИСТНАЯ КОМПОЗИЦИЯ И ПОЛИМЕР | 1997 |
|
RU2194295C2 |
| СОЕДИНЕНИЯ И СПОСОБЫ ИНГИБИРОВАНИЯ ВЗАИМОДЕЙСТВИЯ БЕЛКОВ BCL С КОМПОНЕНТАМИ СВЯЗЫВАНИЯ | 2006 |
|
RU2424230C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОЙ ИЗОЛЯЦИОННОЙ КОМПОЗИЦИИ (ВАРИАНТЫ), КОМПОЗИЦИЯ, ИСПОЛЬЗУЕМАЯ ДЛЯ ПОЛУЧЕНИЯ ПОРИСТОГО ИЗОЛЯЦИОННОГО МАТЕРИАЛА (ВАРИАНТЫ), И ПОЛУПРОВОДНИКОВОЕ УСТРОЙСТВО | 1999 |
|
RU2195050C2 |
| ПРОЗРАЧНЫЕ ПОЛИПРОПИЛЕНОВЫЕ КОНТЕЙНЕРЫ ДЛЯ УПАКОВКИ ОБУВИ | 2004 |
|
RU2378169C9 |
| ФОТОРЕЗИСТНАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2199773C2 |

Изобретение относится к комплексам оксалата димеди(I), стабилизированным нейтральным основанием Льюиса, таким как алкины, и к применению комплексов оксалата димеди(I) в качестве исходных продуктов для осаждения металлической меди, при котором в качестве нейтрального основания Льюиса применяют нециклические алкины. 3 н. и 5 з.п. ф-лы, 2 ил.
1. Соединения общей формулы (I)
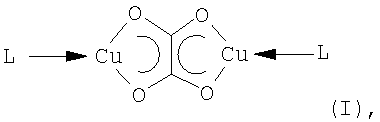
где медь имеет степень окисления +1 и
L означает нециклический алкин формулы R-C≡C-R′, где R, R′ означают А, где А означает алкил с 1-6 атомами углерода или циклоалкенил с 3-30 атомами углерода,
причем L, R, и R′ каждый независимо друг от друга в различных положениях молекулы может принимать одинаковые или различные значения.
2. Соединения общей формулы (I) по п.1, где R и R′ означают А, где А означает алкил с 1-6 атомами углерода или циклоалкенил с 3-9 атомами углерода, причем
L, R и R′ каждый независимо друг от друга в различных положениях молекулы может принимать одинаковые или различные значения.
3. Соединения общей формулы (I) по п.1, где R и R′ означают А, где
А означает алкил с 1-4 атомами углерода из группы, включающей метил, этил, н- и изопропил или н-, изо- и трет-бутил, или циклоалкенил с 3-6 атомами углерода, из группы, включающей циклопропенил, циклобутенил, циклопентенил, циклопентадиенил и метилциклопентадиенил,
причем L, R и R′ каждый независимо друг от друга в различных положениях молекулы может принимать одинаковые или различные значения.
4. Соединения общей формулы (I) по п.1, где L означает нециклический алкин, выбранный из группы, включающей Ме-С≡С-Ме, Et-C≡C-Et, Pr-С≡С-Pr или Bu-C≡C-Bu, где Me означает метил, Et означает этил, Pr означает пропил, а Bu означает бутил.
5. Соединения общей формулы (I) по п.1, отличающиеся тем, что представляют собой оксалат ди[(3-гексин)медь(I)] и/или оксалат ди[(норборнен)медь(I)].
6. Способ получения высокочистых тонких слоев металлической меди, отличающийся тем, что соединения общей формулы (I) по одному из пп.1-5 нагревают, отщепляют основание Льюиса L при температуре от 50 до приблизительно 200°С и затем осаждают металлическую медь путем декарбоксилирования при температуре в интервале от 150 до 350°С.
7. Способ по п.6, отличающийся тем, что отщепленное основание Льюиса L регенерируют и снова используют в способе по п.6.
8. Применение соединений общей формулы (I) для получения тонких слоев высокочистой металлической меди.
| БЕЗМЕН | 1928 |
|
SU8225A1 |
| US 4387055 А, 07.06.1983. | |||
Авторы
Даты
2010-02-20—Публикация
2004-03-29—Подача