Данное изобретение относится к лечению угрей и конкретно к применению производных 5-аминолевулиновой кислоты (5-АЛК) в способе лечения угрей, например обыкновенных угрей. Конкретнее данное изобретение относится к применению эфиров 5-АЛК для лечения таких состояний.
Угри представляют собой одно из самых распространенных кожных расстройств во всем мире. Несмотря на то, что угри являются особенно превалирующими на протяжении периода полового созревания, они могут сохраняться в течение многих лет. В Великобритании угри поражают приблизительно 83-95% шестнадцатилетних подростков обоих полов, и примерно 20% пострадавших обращаются за помощью к врачу. В некоторых случаях они могут вызвать образование постоянных рубцов и часто являются источником значительного эмоционального расстройства.
В более умеренных формах угри являются поверхностным расстройством, которое сопровождается незначительными точечными раздражениями. Однако при более воспалительных типах угрей происходит бактериальная инвазия сальных желез волос или близлежащих участков, приводящая к образованию пустул, инфицированных кист и так далее. Эти поражения могут становиться обширными и часто оставляют постоянные обезображивающие рубцы.
Точная причина угрей не является полностью понятной, хотя полагают, что закупорка канала сальной железы является первичным фактором. Это может быть вызвано избыточным образованием кожного сала, повышенным обменом веществ эпителиальных клеток и/или размножением бактерий (например, Propionibacterium acnes). Считают, например, что избыточное образование кожного сала и повышенный обмен веществ эпителиальных клеток могут вызвать закупорку или блокирование пор кожи и приводить к образованию комедонов (черных угрей) и белых угрей. Если в комбинации с этими факторами присутствуют определенные бактерии, могут образоваться воспалительные поражения, такие как папулы, пустулы и кисты.
Черные угри, белые угри, папулы, пустулы и кисты обычно называют «прыщами». У любого пострадавшего от угрей каждый тип прыщей может присутствовать в различной степени, и чаще всего обнаруживают целый ряд различных типов. Прыщи обычно появляются на лице и на спине, особенно на участках кожи лица (например, на подбородке, на носу и на лбу), где сальные железы являются наибольшими, наиболее превалирующими и наиболее активными.
Признанные способы лечения угрей разработаны таким образом, чтобы предупредить образование новых поражений и облегчить лечение существующих поражений. Традиционные способы лечения включают, например, системное или местное введение антибиотиков, целью которого является уменьшение бактериальной популяции сальных желез волос, и местное нанесение пероксидов, например бензоилпероксида, который является и антибактериальным, и, в умеренной степени, противоугревым средством. Аналоги витамина А, такие как ретиноиды, являются противоугревыми, и их также с некоторой степенью успеха используют в композициях для местного лечения угрей.
Однако существуют проблемы, возникающие при таких традиционных способах лечения. Например, пероксиды, такие как бензоилпероксид, часто являются нестабильными и, следовательно, имеют ограниченный срок хранения. Их эффективность также имеет тенденцию снижаться со временем. Устойчивость Propionibacterium acnes к антибиотикам также увеличивается, и это серьезно снижает эффективность. Ретиноидные лекарственные средства (например, изотретиноин), хотя и являются эффективными, часто вызывают неприятные и иногда серьезные побочные эффекты, и противопоказания часто ограничивают их приемлемость и применение. Следовательно, существует необходимость в разработке альтернативных способов лечения угрей.
Одним способом, который недавно предложили для лечения угрей, является фотодинамическая терапия (ФДТ) с использованием фотосенсибилизирующих агентов. Фотодинамическая терапия (ФДТ) является относительно новой методикой, которую использовали при лечении различных ненормальных состояний или расстройств кожи или других эпителиальных органов или слизистых оболочек, особенно раковых или предраковых поражений, а также определенных незлокачественных поражений, таких как псориаз. ФДТ включает введение фотосенсибилизирующих агентов с последующим воздействием фотоактивирующего света для того, чтобы активировать фотосенсибилизирующие агенты и превратить их в цитотоксическую форму, приводящую к разрушению клеток и, таким образом, к лечению заболевания. Несколько фотосенсибилизирующих агентов известно и описано в литературе, например, различные порфирины, псоралены, хлорины, фталоцианины, а также 5-аминолевулиновая кислота (5-АЛК) и ее определенные производные, например, эфиры 5-АЛК.
Несмотря на то что ФДТ прежде всего направлена на лечение рака и предраковых стадий, существует несколько сообщений, относящихся к применению ФДТ в лечении угрей. Однако такие способы имели только ограниченный успех. Например, и Itoh, Y. et al. (Brit. J. Dermatology, 2001, 144, 575-579) и Hongcharau, W. et al. (J. Invest. Dermatology, 2000, 115, 183-192) описали испытания по лечению угрей посредством ФДТ с использованием 5-АЛК в качестве фотосенсибилизатора. В обоих исследованиях сделан вывод, что АЛК-ФДТ может быть эффективной для лечения угрей, но отмечено, что с данным лечением связаны значительные неблагоприятные эффекты. Они включают дискомфорт, жжение, зуд и острую боль на протяжении облучения, отечную эритему и отслоение эпидермиса вскоре после ФДТ и длительное раздражение и гиперчувствительность к физической стимуляции в течение вплоть до 10 суток после лечения. В целом ряде случаев также сообщали о пигментации, и требовалось до месяца для возвращения кожи пациента к нормальному состоянию.
Дополнительной проблемой, связанной с применением 5-АЛК в терапии (например, в ФДТ), является то, что она крайне нестабильна и имеет тенденцию подвергаться множеству реакций разложения. В результате нестабильности 5-АЛК обычно присутствует в виде кислой композиции (она наиболее стабильна при рН менее 5), но это, в свою очередь, дополнительно снижает ее приемлемость в качестве терапевтического вещества. 5-АЛК также имеет относительно низкую биодоступность, что означает, что она часто должна быть использована в высоких дозах, усугубляя, таким образом, проблемы, связанные с кислотностью многих композиций 5-АЛК.
Следовательно, все еще существует необходимость в альтернативных способах лечения и/или предупреждения угрей. Несмотря на различные проблемы, освещенные в литературе в связи с лечением угрей с использованием ФДТ и 5-АЛК, авторы данного изобретения теперь неожиданно обнаружили, что производные 5-АЛК (например, эфиры 5-АЛК, особенно возможно замещенные бензиловые эфиры АЛК) можно эффективно использовать в фотодинамическом лечении угрей.
Таким образом, в одном аспекте согласно данному изобретению предложено применение фотосенсибилизатора, который представляет собой производное (например, эфир) 5-аминолевулиновой кислоты (5-АЛК) или его фармацевтически приемлемую соль, в изготовлении лекарственного средства для применения в предупреждении или лечении угрей.
В другом аспекте согласно данному изобретению предложен способ лечения или предупреждения угрей, включающий введение (например, местное нанесение) фотосенсибилизатора, который представляет собой производное (например, эфир) 5-аминолевулиновой кислоты (5-АЛК) или его фармацевтически приемлемую соль, в участок кожи (например, на пораженный участок кожи) на теле и фотоактивацию указанного фотосенсибилизатора.
В частности, согласно данному изобретению предложен способ лечения или предупреждения угрей, включающий стадии:
(а) введения (например, местного нанесения) фотосенсибилизатора, который представляет собой производное (например, эфир) 5-аминолевулиновой кислоты (5-АЛК) или его фармацевтически приемлемую соль, в участок кожи (например, на пораженный участок кожи) на указанном теле;
(б) возможно, ожидания в течение периода времени, необходимого для достижения фотосенсибилизатором эффективной концентрации в ткани в желательном (например, пораженном) месте; и
(в) фотоактивации фотосенсибилизатора в желательном (например, пораженном) месте.
Применение производных 5-АЛК (5-амино-4-оксо-пентановой кислоты, иначе известной как 5-аминолевулиновая кислота) в ФДТ хорошо известно в научной и патентной литературе (см., например, J.C. Kennedy et al., J. Clin. Laser Med. Surg. (1996) 14: 289-304, US-A-5079262, US-A-5211938, US-A-5234940, US-A-5422093, US-A-6034267, WO 91/01727 и WO 96/28412, содержание которых включено в данное описание изобретения посредством ссылки). Все такие производные 5-АЛК и их фармацевтически приемлемые соли являются подходящими для применения в способах, описанных здесь.
Производыми 5-АЛК, полезными согласно данному изобретению, могут быть любые производные 5-АЛК, способные образовать протопорфирин IX (PplX) или любой другой фотосенсибилизатор (например, производное PplX) in vivo. Обычно такие производные будут предшественником PplX или производного PplX (например, сложного эфира PplX) в пути биосинтеза гема и которые, следовательно, способны индуцировать накопление PplX в месте угрей после введения in vivo. Подходящие предшественники PplX или производных PplX включают пролекарства 5-АЛК, которые могут иметь способность образовывать 5-АЛК in vivo в качестве промежуточного соединения в биосинтезе PplX или которые могут быть превращены (например, ферментативно) в порфирины без образования 5-АЛК в качестве промежуточного соединения. Эфиры 5-АЛК находятся среди предпочтительных соединений для применения в описанных здесь способах.
Эфиры 5-аминолевулиновой кислоты и их N-замещенные производные являются предпочтительными фотосенсибилизаторами для применения в данном изобретении. Те соединения, в которых 5-аминогруппа является незамещенной (то есть эфиры АЛК) являются особенно предпочтительными. Такие соединения обычно известны и описаны в литературе (см., например, WO 96/28412 и WO 02/10120 (PhotoCure ASA), содержание которых включено в данное описание изобретения посредством ссылки).
Эфиры 5-аминолевулиновой кислоты с замещенными или незамещенными, предпочтительно замещенными, алканолами, то есть алкиловые эфиры или, более предпочтительно, замещенные алкиловые эфиры, являются особенно предпочтительными фотосенсибилизаторами для применения в данном изобретении. Примеры таких соединения включают соединения общей формулы I:
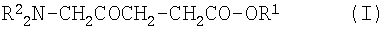
где R1 представляет собой замещенную или незамещенную, предпочтительно замещенную, алкильную группу с прямой цепью, разветвленную или циклическую (например замещенную алкильную группу с прямой цепью) и каждый R2 независимо представляет собой атом водорода или возможно замещенную алкильную группу, (например, группу R1), и их фармацевтически приемлемые соли.
Термин «алкил», в том виде, как он здесь используется, если не указано иначе, включает любую длинно- или короткоцепочечную, циклическую, с прямой цепью или разветвленную алифатическую насыщенную или ненасыщенную углеводородную группу. Данные ненасыщенные алкильные группы могут быть моно- или полиненасыщенными и включают как алкенильные, так и алкинильные группы. Если не указано иначе, такие группы могут содержать вплоть до 40 атомов. Однако алкильные группы, содержащие вплоть до 30, предпочтительно вплоть до 10, особенно предпочтительно вплоть до 8, особенно предпочтительно вплоть до 6, например, вплоть до 4 атомов углерода, являются предпочтительными.
Замещенные алкильные группы R1 и R2 могут быть моно- или полизамещенными. Подходящие заместители могут быть выбраны из групп гидрокси, алкокси, ацилокси, алкоксикарбонилокси, амино, арил, нитро, оксо, фторо, -SR3, -NR3 2 и -PR3 2, и каждая алкильная группа возможно может быть прервана одной или более чем одной группой -O-, -NR3-, -S- или -PR3-, в которой R3 представляет собой атом водорода или C1-6алкильную группу.
Предпочтительные замещенные алкильные группы R1 включают группы, несущие одну или более чем одну оксогруппу, предпочтительно С4-12алкильные (например С8-10алкильные) группы с прямой цепью, замещенные одной, двумя или тремя (предпочтительно двумя или тремя) оксогруппами. Примеры таких групп включают 3,6-диокса-1-октильную и 3,6,9-триокса-1-децильную группы.
Особенно предпочтительными для применения в данном изобретении являются те соединения формулы I, в которых по меньшей мере один R2 представляет собой атом водорода. В особенно предпочтительных соединениях каждый R2 представляет собой атом водорода.
Соединения формулы I, в которых R1 представляет собой незамещенную алкильную группу (предпочтительно C1-6алкильную, например C1-8алкильную) или более предпочтительно алкильную группу (например, С1-2алкильную, особенно С1алкильную), замещенную заместителем, как определено здесь выше (например, арильной группой, такой как фенильная, или алкоксигруппой, такой как метокси), также являются предпочтительными.
Незамещенные алкильные группы, которые можно использовать в данном изобретении, включают как разветвленные углеводородные группы, так и углеводородные группы с прямой цепью. Предпочтительными являются соединения формулы I, в которых R1 представляет собой С4-8, предпочтительно С5-8алкильную группу с прямой цепью, которая разветвляется одной или более чем одной C1-6 (например, С1-2алкильной) группой. Показательные примеры подходящих незамещенных разветвленных алкильных групп включают 2-метилпентильную, 4-метилпентильную, 1-этилбутильную и 3,3-диметил-1-бутильную. 4-Метилпентил является особенно предпочтительным.
Соединения формулы I, в которых R1 представляет собой C1-10алкильную группу с прямой цепью, также являются предпочтительными. Показательные примеры подходящих незамещенных алкильных групп включают метильную, этильную, пропильную, бутильную, пентильную, гексильную и октильную (например н-пропильную, н-бутильную, н-пентильную, н-гексильную и н-октильную). Гексил, особенно н-гексил, является особенно предпочтительной группой. Метил также является особенно предпочтительным.
Особенно предпочтительными для применения в данном изобретении являются те соединения формулы I, в которых R1 представляет собой C1-2алкильную группу (предпочтительно С1алкильную группу), возможно замещенную арильной группой.
Другими предпочтительными для применения в данном изобретении являются те соединения формулы I, в которых R1 представляет собой алкильную группу (например, С1-2алкильную, особенно С1алкильную), замещенную арильной группой (например, фенильной). Предпочтительные замещенные алкильные группы R1, которые могут присутствовать в соединениях формулы I, включают C1-6алкильную, предпочтительно C1-4алкильную, особенно предпочтительно C1 или С2алкильную (например, С1алкильную), замещенную (предпочтительно замещенную на конце) возможно замещенной арильной группой.
Под «арильной группой» подразумевают группу, которая является ароматической. Предпочтительные арильные группы включают вплоть до 20 атомов углерода, более предпочтительно вплоть до 12 атомов углерода, например, 10 или 6 атомов углерода.
Арильные группы, которые могут присутствовать в соединениях по данному изобретению, могут быть гетероароматическими (например, 5-7-членными гетероароматическими), но предпочтительно являются негетероароматическими. Под «негетероароматической» подразумевают арильную группу, имеющую ароматическую систему, включающую электроны, происходящие исключительно от атомов углерода. Предпочтительные арильные группы включают фенильную и нафтильную, особенно фенильную. В предпочтительных соединениях для применения в данном изобретении могут присутствовать одна или две арильные группы, предпочтительно одна.
В предпочтительном аспекте данного изобретения предложено применение фотосенсибилизатора, который представляет собой соединение формулы I, где R1 представляет собой С1-4алкильную группу (предпочтительно C1-2, например С1), замещенную арилом, предпочтительно где указанная арильная группа содержит вплоть до 20 атомов углерода (например, вплоть до 12 атомов углерода, особенно 6 атомов углерода) и сама является возможно замещенной, и каждый R2 является таким, как определено выше (например, каждый R2 представляет собой атом водорода), или его фармацевтически приемлемую соль, в изготовлении лекарственного средства для применения в предупреждении или лечении угрей.
Арильные группы, которые могут присутствовать в соединениях по изобретению, возможно могут быть замещены одной или более чем одной (например, от 1 до 5), более предпочтительно одной или двумя группами (например, одной группой). Предпочтительно данная арильная группа замещена по мета- или параположению, наиболее предпочтительно по параположению. Подходящие группы заместителей могут включать галогеноалкил (например, трифторметил), алкокси (то есть -OR группы, где R предпочтительно представляет собой C1-6алкильную группу), галогено (например, йодо, бромо, особенно хлоро или фторо), нитро и С1-6алкил (предпочтительно С1-4алкил). Предпочтительные С1-6алкильные группы включают метильную, изопропильную и трет-бутильную, особенно метильную, группы. Особенно предпочтительные группы заместителей включают хлоро и нитро. Наиболее предпочтительно арильная группа является незамещенной.
Предпочтительные соединения для применения в данном изобретении включают метиловый эфир АЛК, этиловый эфир АЛК, пропиловый эфир АЛК, бутиловый эфир АЛК, пентиловый эфир АЛК, гексиловый эфир АЛК, октиловый эфир АЛК, 2-метоксиэтиловый эфир АЛК, 2-метилпентиловый эфир АЛК, 4-метилпентиловый эфир АЛК, 1-этилбутиловый эфир АЛК, 3,3-диметил-1-бутиловый эфир АЛК, бензиловый эфир АЛК, 4-изопропилбензиловый эфир АЛК, 4-метилбензиловый эфир АЛК, 2-метилбензиловый эфир АЛК, 3-метилбензиловый эфир АЛК, 4-[трет-бутил]бензиловый эфир АЛК, 4-[трифторметил]бензиловый эфир АЛК, 4-метоксибензиловый эфир АЛК, 3,4-[дихлор]бензиловый эфир АЛК, 4-хлорбензиловый эфир АЛК, 4-фторбензиловый эфир АЛК, 2-фторбензиловый эфир АЛК, 3-фторбензиловый эфир АЛК, 2,3,4,5,6-пентафторбензиловый эфир АЛК, 3-нитробензиловый эфир АЛК, 4-нитробензиловый эфир АЛК, 2-фенилэтиловый эфир АЛК, 4-фенилбутиловый эфир АЛК, 3-пиридинил-метиловый эфир АЛК, 4-дифенил-метиловый эфир АЛК и бензил-5-[(1-ацетилоксиэтокси)-карбонил]аминолевулинат.
Другие предпочтительные соединения для применения в данном изобретении включают метиловый эфир АЛК, этиловый эфир АЛК, 2-метоксиэтиловый эфир АЛК, бензиловый эфир АЛК, 4-изопропилбензиловый эфир АЛК, 4-метилбензиловый эфир АЛК, 2-метилбензиловый эфир АЛК, 3-метилбензиловый эфир АЛК, 4-[трет-бутил]бензиловый эфир АЛК, 4-[трифторметил]бензиловый эфир АЛК, 4-метоксибензиловый эфир АЛК, 3,4-[дихлор]бензиловый эфир АЛК, 4-хлорбензиловый эфир АЛК, 4-фторбензиловый эфир АЛК, 2-фторбензиловый эфир АЛК, 3-фторбензиловый эфир АЛК, 2,3,4,5,6-пентафторбензиловый эфир АЛК, 3-нитробензиловый эфир АЛК, 4-нитробензиловый эфир АЛК, 2-фенилэтиловый эфир АЛК, 4-фенилбутиловый эфир АЛК, 3-пиридинил-метиловый эфир АЛК, 4-дифенил-метиловый эфир АЛК и бензил-5-[(1-ацетилоксиэтокси)-карбонил]аминолевулинат.
Особенно предпочтительные соединения для применения в данном изобретении включают бензиловый эфир АЛК, 4-изопропилбензиловый эфир АЛК, 4-метилбензиловый эфир АЛК, 2-метилбензиловый эфир АЛК, 3-метилбензиловый эфир АЛК, 4-[трет-бутил]бензиловый эфир АЛК, 4-[трифторметил]бензиловый эфир АЛК, 4-метоксибензиловый эфир АЛК, 3,4-[дихлор]бензиловый эфир АЛК, 4-хлорбензиловый эфир АЛК, 4-фторбензиловый эфир АЛК, 2-фторбензиловый эфир АЛК, 3-фторбензиловый эфир АЛК, 2,3,4,5,6-пентафторбензиловый эфир АЛК, 3-нитробензиловый эфир АЛК, 4-нитробензиловый эфир АЛК, 2-фенилэтиловый эфир АЛК, 4-фенилбутиловый эфир АЛК, 3-пиридинил-метиловый эфир АЛК, 4-дифенил-метиловый эфир АЛК и бензил-5-[(1-ацетилоксиэтокси)-карбонил]аминолевулинат.
Особенно предпочтительные соединения для применения в описанных здесь способах включают бензиловый эфир АЛК, 4-изопропилбензиловый эфир АЛК и 4-метилбензиловый эфир АЛК, особенно бензиловый эфир АЛК. 4-Нитробензиловый эфир АЛК, 4-хлорбензиловый эфир АЛК и бензиловый эфир АЛК являются особенно предпочтительными.
Соединения для применения в данном изобретении можно получить любым традиционным способом, доступным в данной области (например, как описано в WO 02/10120 (PhotoCure ASA)). Например, эфиры 5-АЛК можно получить путем взаимодействия 5-АЛК с подходящим спиртом в присутствии основания. В качестве альтернативы, соединения для применения в данном изобретении могут иметься в продаже (например, от PhotoCure ASA, Норвегия).
Соединения для применения согласно способу по изобретению могут находиться в виде свободного амина (например -NH2, -NHR2 или -NR2R2) или предпочтительно в виде физиологически приемлемой соли. Такие соли предпочтительно представляют собой соли присоединения кислоты с физиологически приемлемыми органическими или неорганическими кислотами. Подходящие кислоты включают, например, соляную, азотную, бромоводородную, фосфорную, серную, сульфоновую и производные сульфоновой кислоты. Особенно предпочтительными солями являются соли присоединения сульфоновой кислоты или производных сульфоновой кислоты, как описано в WO 2005/092838 (PhotoCure ASA), полное содержание которой включено в данное описание изобретения посредством ссылки. Способы получения солей являются традиционными в данной области.
В способе по изобретению в лечении или предупреждении угрей один фотосенсибилизатор (то есть производное 5-АЛК) можно использовать отдельно. В качестве альтернативы, можно использовать комбинацию двух или более чем двух, предпочтительно двух, фотосенсибилизаторов, где по меньшей мере один из фотосенсибилизаторов представляет собой производное 5-АЛК или его фармацевтически приемлемую соль.
Другие фотосенсибилизаторы, которые можно приготовить в виде препаратов с производным 5-АЛК (например, с эфиром 5-АЛК) или ввести совместно согласно данному изобретению включают:
Производное гематопорфирина (HpD);
Гематопорфирины, такие как Photofrin® (Quadra Logic Technologies Inc., Vancouver, Canada) и гематопорфирин IX (HplX);
Photosan III (Seehof Laboratorium GmbH, Seehof, Wesselburenerkoog, Germany);
Хлорины, такие как тетра(м-гидроксифенил)хлорины (m-ТНРС) и их бактериохлорины (Scotia Pharmaceuticals Ltd, Surrey, UK), моно-L-аспартилхлорин е6 (NPe6) (Nippon Petrochemical Co., CA, USA), хлорин е6 (Porphyrin Products Inc.), бензопорфирины (Quadra Logic Technologies Inc., Vancouver, Canada) (например, бензопорфириновое производное монокислота кольца A, BPD-MA) и пурпурины (PDT Pharmaceuticals Inc., CA, USA) (например, олово-этил-этиопурпурин, SnET2);
Фталоцианины (например, цинк-(Quadra Logic Technologies Inc., Vancouver, Canada), некоторые алюминий- или кремний-фталоцианины, которые могут быть сульфонированными, конкретно сульфонированные фталоцианины, такие как алюминий-фталоцианина дисульфонат (AlPcS2a) или алюминий-фталоцианина тетрасульфонат (AIPcS4));
Порфицены;
Гипокреллины;
Протопорфирин IX (PplX);
Гематопорфирина диэфиры;
Уропорфирины;
Копропорфирины;
Дейтеропорфирин;
Полигематопорфирин (РНР) и его предшественники и производные; и антибиотики, такие как тетрациклин (например, Topicycline®, Shire).
Предпочтительно вторым фотосенсибилизатором будет гематопорфирин (например, Photofrin®), хлорин (конкретно м-ТНРС или хлорин е6) или сульфонированный фталоцианин (конкретно алюминий-фталоцианина дисульфонат или алюминий-фталоцианина тетрасульфонат).
В другом аспекте согласно данному изобретению, таким образом, предложено применение первого фотосенсибилизатора, который представляет собой производное 5-АЛК, как определено здесь выше, или его фармацевтически приемлемую соль, совместно со вторым фотосенсибилизатором в изготовлении лекарственного средства для применения в предупреждении или лечении угрей.
В еще одном другом аспекте согласно данному изобретению предложено применение первого фотосенсибилизатора, который представляет собой производное 5-АЛК, как определено здесь выше, или его фармацевтически приемлемую соль, совместно со вторым фотосенсибилизатором в изготовлении лекарственных средств для одновременного, раздельного или последовательного применения в способе лечения или предупреждения угрей.
В еще одном аспекте согласно данному изобретению предложен набор или упаковка, содержащие первый фотосенсибилизатор, который представляет собой производное 5-АЛК, как определено здесь выше, или его фармацевтически приемлемую соль, и отдельно второй фотосенсибилизатор для одновременного, раздельного или последовательного применения в способе лечения или предупреждения угрей.
Термин «предупреждение» угрей, в том виде, как он здесь используется, означает профилактическое лечение угрей. Таким образом, соединения, описанные здесь, можно использовать согласно данному изобретению для лечения участков кожи, которые необязательно содержат во время лечения развившиеся угри, но которые склонны к угрям. Предпочтительно соединения для применения согласно данному изобретению предназначены для лечения угрей, как только они появляются, конкретно для лечения воспалительных угрей.
Термин «угри» в том виде, как он здесь используется, включает как воспалительные, так и невоспалительные заболевания сальных желез волос. Прежде всего, однако, описанные здесь способы будут использовать для лечения более воспалительных типов угрей, где произошла бактериальная инвазия в сальную единицу или железу волоса. Как было отмечено ранее, точная причина угрей является неизвестной, несмотря на то, что их обычно связывают с повышенным образованием кожного сала (липидов, секретируемых сальными железами, чувствительными к андрогенам), размножением бактерий, таких как Propionibacterium (например Р. acnes, P. granulosum и Р. avidum), повышенным обменом эпителиальных клеток и/или развитием воспаления (например краснота, припухлость и/или гной). Соединения, описанные здесь, предпочтительно используют для лечения или предупреждения (предпочтительно для лечения) угрей, связанных с Propionibacterium acnes.
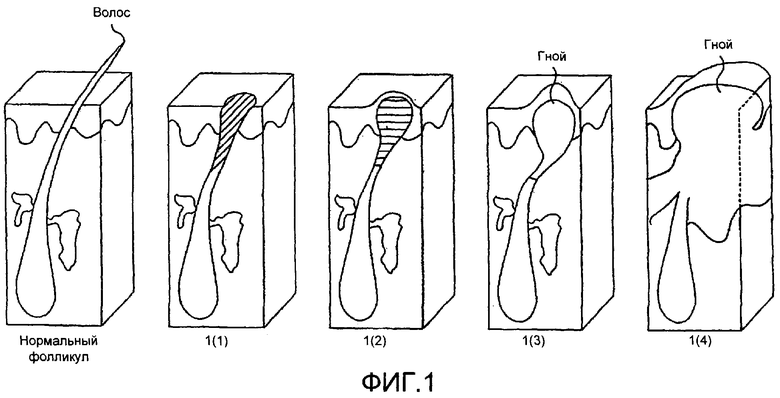
Угри могут проявлять себя целым рядом различных способов (см. приложенную Фиг.1). Обычные характерные признаки угрей включают черные угри (комедоны) и белые угри. Они вызваны тем, что поры становятся закупоренными (например, кожным салом и/или мертвыми клетками). Если поры остаются открытыми, образуются черные угри (Фиг.1(1)), тогда как если поры закрываются и выпячиваются наружу, образуются белые угри (Фиг.1(2)). Считается, что папулы, пустулы и кисты образуются, если стенка поры становится поврежденной, и бактерии инфицируют данную пору. В папуле гной лежит довольно близко к поверхности кожи (Фиг.1(3)), тогда как в пустуле гной находится глубже внутри поры (Фиг.1(4)). Кисты обычно больше и глубже, чем пустулы, и содержат большие количества гноя. Соединения, описанные здесь, можно использовать для лечения или предупреждения одного или более чем одного из следующего: черных угрей, белых угрей, папул, пустул и кист.
Угри классифицируют на различные формы в зависимости, например, от природы, серьезности и/или расположения черных угрей, белых угрей, папул, пустул и/или кист. Показательные типы угрей, которые можно лечить согласно данному изобретению, включают обыкновенные угри, розовые угри, шаровидные угри, папулезные угри и предменструальные угри, предпочтительно обыкновенные угри, которые представляют собой хроническое воспалительное заболевание аппарата сальных желез волос. Угри могут встречаться на спине, груди, плечах и/или на лице; соединения, описанные здесь, можно использовать для лечения любого из этих участков тела, особенно лица.
Определенные более умеренные формы угрей (например, черные угри и/или белые угри) не всегда могут рассматриваться как «заболевание», и их лечение можно проводить исключительно по косметическим причинам. Это может быть так, например, когда угри являются относительно нечастыми и/или не являются широко распространенными (например, встречается несколько прыщей).
Таким образом, в другом аспекте согласно данному изобретению предложен способ косметического лечения угрей (например, на лице), включающий введение (например, местное нанесение) фотосенсибилизатора, который представляет собой производное (например, эфир) 5-аминолевулиновой кислоты (5-АЛК), как определено здесь выше, или его фармацевтически приемлемую соль, в пораженный участок и фотоактивацию указанного фотосенсибилизатора в пораженном участке.
Соединения для применения согласно данному изобретению можно приготовить в виде препаратов любым традиционным способом с одним или более чем одним физиологически приемлемым носителем или эксципиентом согласно методикам, хорошо известным в данной области.
Композиции можно вводить системно (например, перорально или парентерально) или более предпочтительно местно (например, путем инъекции или более предпочтительно местно) в пораженный участок или около него. Путь введения будет зависеть от серьезности и природы угрей, которые нужно лечить, расположения угрей и от используемого фотосенсибилизатора (или комбинации фотосенсибилизаторов). Обычно, однако, местное введение, все же более предпочтительно местное нанесение, будет предпочтительным.
Предпочтительные композиции включают гели, кремы, мази, спреи, лосьоны, бальзамы, палочки, мыла, порошки, аэрозоли, капли, растворы и любые другие традиционные в данной области фармацевтические формы. Гели, кремы и мази обычно являются предпочтительными.
Мази, гели и кремы, например, могут быть приготовлены с водной или масляной основой с добавлением подходящих загустителей и/или гелеобразующих агентов. Лосьоны могут быть приготовлены с водной или масляной основой и, в общем, также содержат один или более чем один эмульгирующий, диспергирующий, суспендирующий агент, загуститель или краситель. Порошки можно получить с помощью любой подходящей порошковой основы. Капли и растворы можно приготовить с водной или неводной основой, также содержащей один или более чем один диспергирующий, солюбилизирующий или суспендирующий агент. Аэрозольные спреи удобно доставляют из упаковок под давлением с применением подходящего пропеллента.
Данные композиции могут дополнительно включать смазывающие агенты, увлажняющие агенты, эмульгирующие агенты, суспендирующие агенты, консерванты, корригенты, усилители аромата и/или усилители поглощения, например, агенты, способствующие проникновению через поверхность, как упомянуто ниже, и тому подобное. Композиции для применения в способе по изобретению можно приготовить так, чтобы обеспечить быстрое, непрерывное или замедленное высвобождение активного ингредиента после введения пациенту путем применения методик, хорошо известных в данной области. Также можно использовать солюбилизирующие и/или стабилизирующие агенты, например, циклодекстрины (CD) α, β, γ и НР-циклодекстрин. Композиции могут находиться в любой подходящей лекарственной форме, например, в виде эмульсии или в липосомах, ниосомах, микросферах, наночастицах или тому подобном. Соединение для применения в данном изобретении затем может абсорбироваться, включаться или связываться с этими формами.
Обычно композиции для лечения угрей ФДТ будут находиться в виде готовых для применения композиций, таких как крем, или в виде набора, состоящего из двухкомпонентной системы (например, содержащей два фотосенсибилизирующих агента).
рН в конечной композиции предпочтительно находится в интервале от 2,5 до 7,4. Слабокислый рН, например рН 5-7, является предпочтительным, если данная композиция представляет собой готовую для применения композицию.
Концентрация соединений 5-АЛК, описанных здесь, в конечной композиции для лечения угрей будет варьировать в зависимости от нескольких факторов, включая химическую природу соединения, химический состав, способ введения и природу угрей, которые нужно лечить. Обычно, однако, подходящими являются интервалы концентрации от 0,01 до 30% (мас./мас.). Наиболее предпочтительные концентрации для лечения угрей местным введением находятся в интервале от 0,02 до 25% (мас./мас.), например, примерно 5% (мас./мас.).
После введения фармацевтической композиции, содержащей фотосенсибилизатор(ы), участок, который нужно лечить, облучают светом для достижения желательного фотосенсибилизирующего эффекта. Продолжительность времени после введения, когда имеет место облучение светом, будет зависеть от природы композиции, состояния, которое нужно лечить, и от формы введения. Обычно необходимым является то, что фотосенсибилизатор должен достигать эффективной концентрации в ткани в участке с угрями перед фотоактивацией. Это обычно может занимать время приблизительно от 0,5 до 24 часов (например, от 1 до 3 часов).
В предпочтительной методике лечения фотосенсибилизатор(ы) наносят на пораженный сайт с последующим облучением (например, после промежутка времени примерно 3 часа). Если необходимо, эту процедуру можно повторить, например, вплоть до еще 3 раз с интервалами вплоть до 14 суток (например 7-14 суток). В тех случаях, когда эта процедура не приводит к удовлетворительному уменьшению или полному излечению угрей, можно провести дополнительное лечение несколькими месяцами позднее.
Способы облучения различных участков тела, например, лампами или лазерами, являются хорошо известными в данной области (см., например, Van den Bergh, Chemistry in Britain, May 1986, p.430-439). В общем будут применять облучение с уровнем дозы от 40 до 200 Дж/см2, например 100 Дж/см2.
Длину волны света, используемого для облучения, можно выбрать для достижения более эффективного фотосенсибилизирующего эффекта. Наиболее эффективным светом является свет в интервале длины волны 300-800 нм, обычно 400-700 нм.
Согласно другому аспекту данного изобретения, таким образом, предложен способ лечения угрей у человека, включающий введение фотосенсибилизатора, который представляет собой производное 5-АЛК или композицию, как определено выше, в пораженный участок и облучение указанной поверхности светом, предпочтительно светом с длиной волны в интервале 300-800 нм, например 400-700 нм.
Как описано выше, соединения для применения в данном изобретении можно приготовить в виде препарата и/или ввести с другими фотосенсибилизирующими агентами, например, с 5-АЛК или другим производным 5-АЛК, или с производным порфирина, таким как Photofrin®. В качестве альтернативы, соединения для применения согласно данному изобретению можно приготовить в виде препарата и/или ввести с другими активными компонентами, которые способны повышать фотосенсибилизирующий эффект и, таким образом, улучшать лечение угрей. Например, хелатирующие агенты можно с пользой включать и/или совместно вводить для того, чтобы усилить накопление Рр; хелатирование железа хелатирующим агентом предотвращает его включение в Рр с образованием гема действием фермента феррохелатазы, приводя, таким образом, к накоплению Рр. Фотосенсибилизирующий эффект, таким образом, усиливается.
Подходящие хелатирующие агенты включают аминополикарбоновые кислоты, включая любые хелаторы, описанные в литературе, для детоксикации металлов или для хелатирования ионов парамагнитных металлов в контрастных агентах для магнитно-резонансной визуализации.
Можно особо упомянуть EDTA (этилендиаминтетрауксусная кислота), CDTA (циклогександиаминтетрауксусная кислота), DTPA и DOTA и их хорошо известные производные/аналоги. EDTA и DTPA являются особенно предпочтительными. Для достижения эффекта хелатирования железа также можно использовать десферриоксамин и другие сидерофоры, например, в сочетании с хелатирующими агентами на основе аминополикарбоновых кислот, такими как EDTA.
Хелатирующий агент, когда он присутствует, можно с удобством использовать в концентрации от 0,05 до 20%, например, от 0,1 до 10% (мас./мас.).
Агенты, способствующие проникновению внутрь, также могут иметь полезный эффект в усилении фотосенсибилизирующего эффекта соединений для применения в данном изобретении. Агенты, содействующие проникновению через поверхность, особенно диалкилсульфоксиды, такие как диметилсульфоксид (DMSO), следовательно, также можно включать в композиции для применения в данном изобретении и/или вводить совместно. Агентом, содействующим проникновению через поверхность, могут быть любые агенты, содействующие проникновению через кожу, описанные в фармацевтической литературе, например, хелаторы (например EDTA), поверхностно-активные вещества (например, додецилсульфат натрия), вещества, не являющиеся поверхностно-активными, соли желчи (например, дезоксихолат натрия) и жирные кислоты (например, олеиновая кислота). Примеры подходящих агентов, содействующих проникновению через поверхность, включают изопропанол, НРЕ-101 (имеющийся в продаже от Hisamitsu), DMSO и другие диалкилсульфоксиды, конкретно н-децилметил-сульфоксид (NDMS), диметилсульфацетамид, диметилформамид (DMFA), диметилацетамид, гликоли, различные производные пирролидона (Woodford et al., J. Toxicol. Cut & Ocular Toxicology, 1986, 5: 167-177), Azone® (Stoughton et al., Drug Dpv. Ind. Pharm. 1983, 9: 725-744) или их смеси.
Агент, способствующий проникновению через поверхность, можно с удобством обеспечить в интервале концентраций от 0,2 до 50% (мас./мас.), например, около 10% (мас./мас.).
В другом аспекте согласно данному изобретению, таким образом, предложено применение фотосенсибилизатора, который является производным 5-АЛК (например, эфиром 5-АЛК) или его фармацевтически приемлемой солью, совместно с по меньшей мере одним агентом, содействующим проникновению через поверхность, и, возможно, с одним или более чем одним хелатирующим агентом, в изготовлении лекарственного средства или лекарственных средств для применения в лечении или предупреждении угрей.
Соединения для применения в данном изобретении можно дополнительно использовать в комбинации с другими нефотосенсибилизирующими агентами, которые улучшают лечение или предупреждение угрей. Такие агенты включают один или более чем один традиционный агент для лечения угрей. Показательные примеры таких агентов включают:
Ретиноиды, такие как ацитретин, изотретинион (например, Isotrex®, Steifel и Roaccutane®, Roche), третинион (например, Retin-A®, Janssen-Cilag) и тазаротен;
Пероксиды, такие как бензоилпероксид (например, PanOxyl®, Stiefel);
Антибиотики, такие как тетрациклин (например, Topicycline®, Shire), клиндамицин (например, Dalacin Т®, Pharmacia), эритромицин (например, Stiemycin®, Stiefel), доксициклин, окситетрациклин, миноциклин, триметоприм и метронидазол;
Гормоны, такие как ко-циприндиол (ципротерона ацетат с этинилэстрадиолом), например, Dianette®, Schering Health;
Азелаиновая кислота (например, Skinoren®, Schering Health) и ее производные, такие, как описано в WO 03/045893 (PhotoCure ASA);
Адапален (например, Differin®, Galderma);
Никотинамид (например, Nican®, Dermal) и
Салициловая кислота (например, Acnisal®, DermaPharm).
Несмотря на то, что эти агенты для лечения угрей могут присутствовать в виде части композиции, обычно их будут использовать как отдельный способ лечения для введения одновременно, раздельно или последовательно. Введение любого дополнительного агента следует проводить в показателях пути, концентрации и композиции согласно известным способам применения этих агентов. Эти дополнительные агенты можно вводить перед, на протяжении или после ФДТ, в зависимости от их функции.
В другом аспекте согласно данному изобретению, таким образом, предложен продукт или набор для применения в способе лечения или предупреждения угрей, содержащий:
(а) первый контейнер, содержащий фотосенсибилизатор, который представляет собой производное (например, эфир) 5-АЛК или его фармацевтически приемлемую соль; и
(б) второй контейнер, содержащий нефотосенсибилизирующий агент для лечения угрей.
Также могут быть предложены дополнительные компоненты данного набора, такие как второй фотосенсибилизирующий агент, агент, содействующий проникновению через поверхность, или хелатирующий агент, как здесь описано.
В другом аспекте согласно данному изобретению, таким образом, предложено применение фотосенсибилизатора, который является производным 5-АЛК (например, эфиром 5-АЛК) или его фармацевтически приемлемой солью, совместно с нефотосенсибилизирующим агентом для лечения угрей в изготовлении лекарственного средства или лекарственных средств для применения в предупреждении или лечении угрей.
В еще одном аспекте данного изобретения предложено применение фотосенсибилизатора, который является производным 5-АЛК (например, эфиром 5-АЛК) или его фармацевтически приемлемой солью, совместно с нефотосенсибилизирующим агентом для лечения угрей в изготовлении лекарственных средств для одновременного, раздельного или последовательного применения в способе лечения или предупреждения угрей.
В зависимости от природы угрей, которые нужно лечить, и природы любого дополнительного активного агента или агентов, которые следует использовать в способе по изобретению, его можно совместно вводить с производным 5-АЛК, например, в одной композиции, или его можно вводить последовательно или раздельно. Обычно в тех случаях, когда используют агент, содействующий проникновению через поверхность, его будут вводить на отдельной стадии перед введением соединений для применения в данном изобретении. Когда агент, содействующий проникновению через поверхность, используют в предварительной обработке, его можно использовать в высоких концентрациях, например, вплоть до 100% (мас./мас.). Если применяют такую стадию предварительной обработки, фотосенсибилизирующий агент затем можно вводить через промежуток времени вплоть до нескольких часов после предварительной обработки, например, с интервалом 5-60 минут после предварительной обработки.
Данное изобретение теперь будет описано более подробно посредством следующих неограничивающих примеров и со ссылкой на сопровождающие графические материалы, в которых:
на Фиг.1 показаны различные стадии угрей;
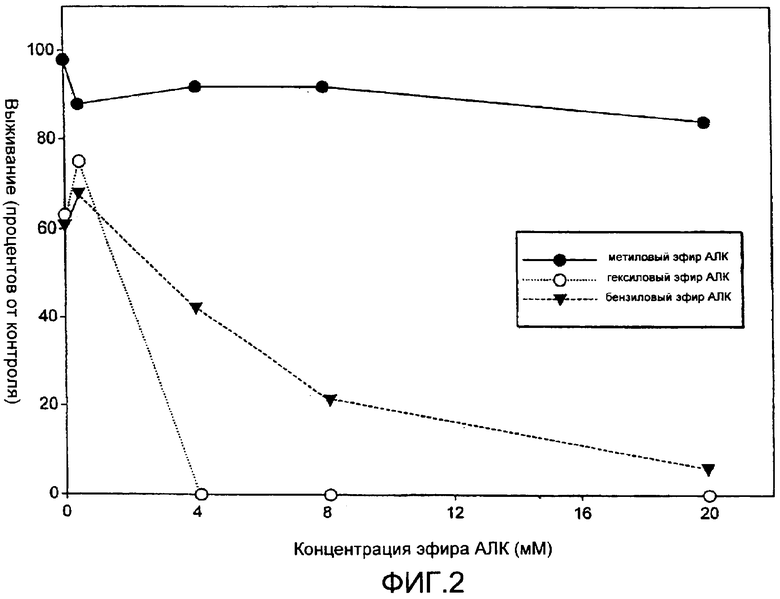
на Фиг.2 показаны результаты токсичности в темноте для метилового эфира АЛК, гексилового эфира АЛК и бензилового эфира АЛК;
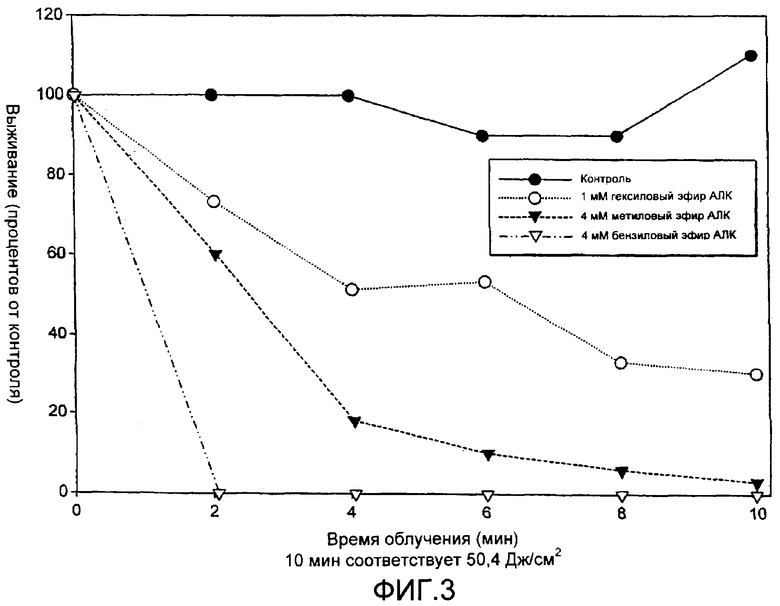
на Фиг.3 показаны фотодинамические эффекты у бактерий Р. acnes, инкубируемых с метиловым эфиром АЛК, гексиловым эфиром АЛК и бензиловым эфиром АЛК;
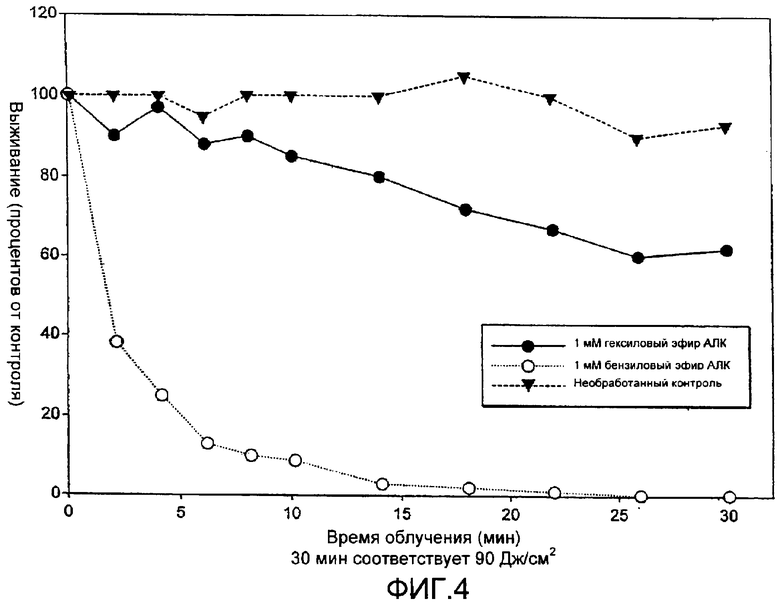
на Фиг.4 показаны фотодинамические эффекты у бактерий, инкубируемых с гексиловым эфиром АЛК и бензиловым эфиром АЛК;
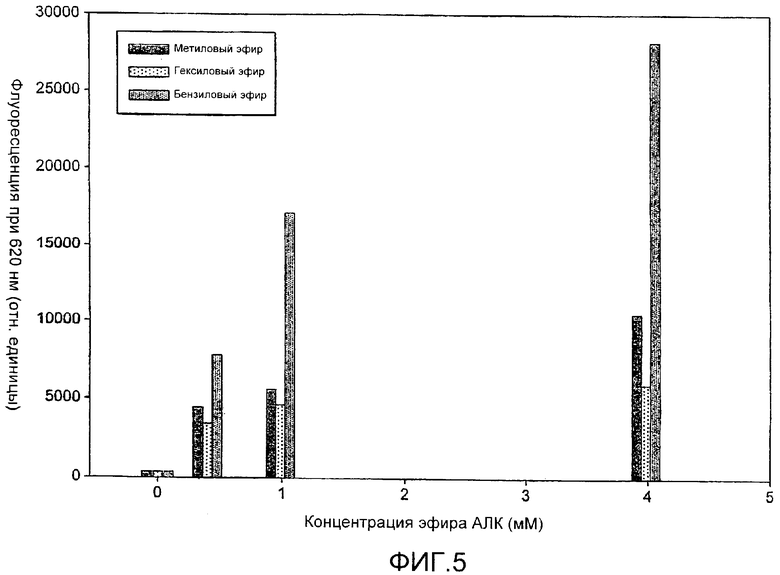
на Фиг.5 показано образование порфирина у Р. acnes после инкубации с различными концентрациями эфиров АЛК;
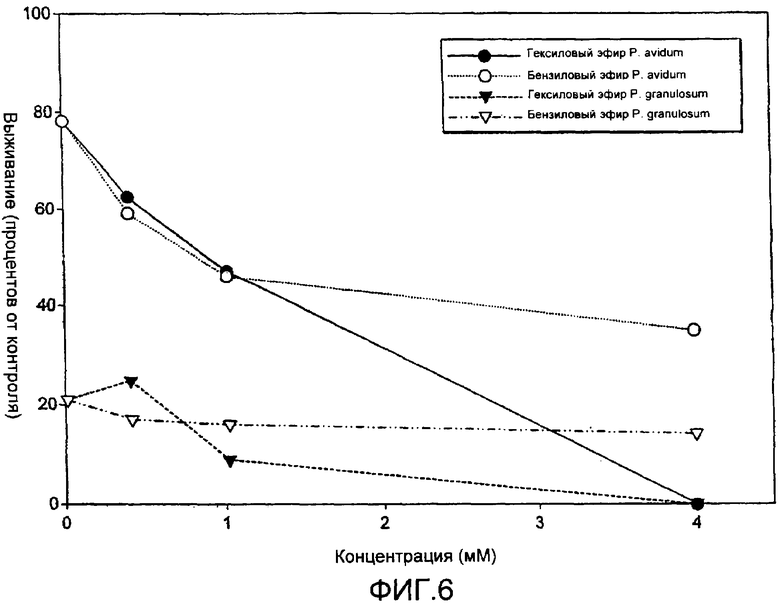
на Фиг.6 показана токсичность в темноте гексилового эфира АЛК и бензилового эфира АЛК (выживание приведено по отношению к необработанному контролю, то есть к контролю, который не инкубировали в течение 4 часов в инкубационном буфере);
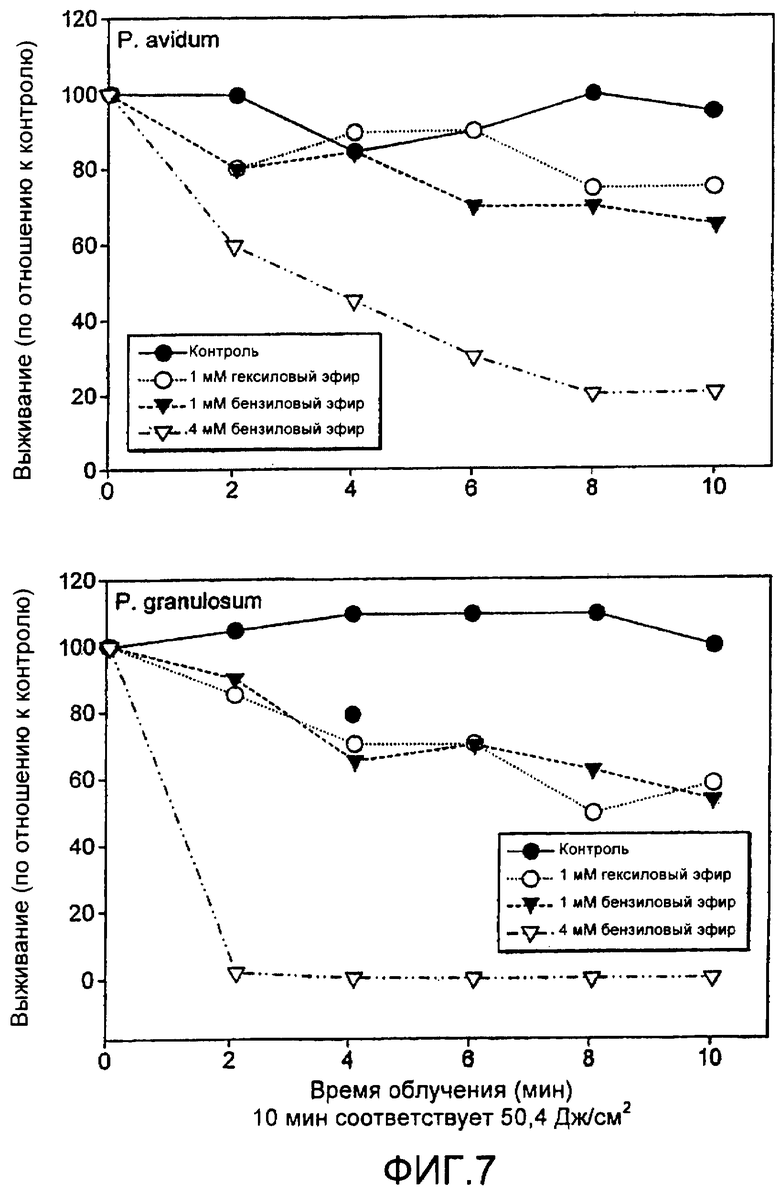
на Фиг.7 показаны фотодинамические эффекты у бактерий Р. granulosum и Р. avidum, инкубируемых с гексиловым эфиром АЛК и бензиловым эфиром АЛК;
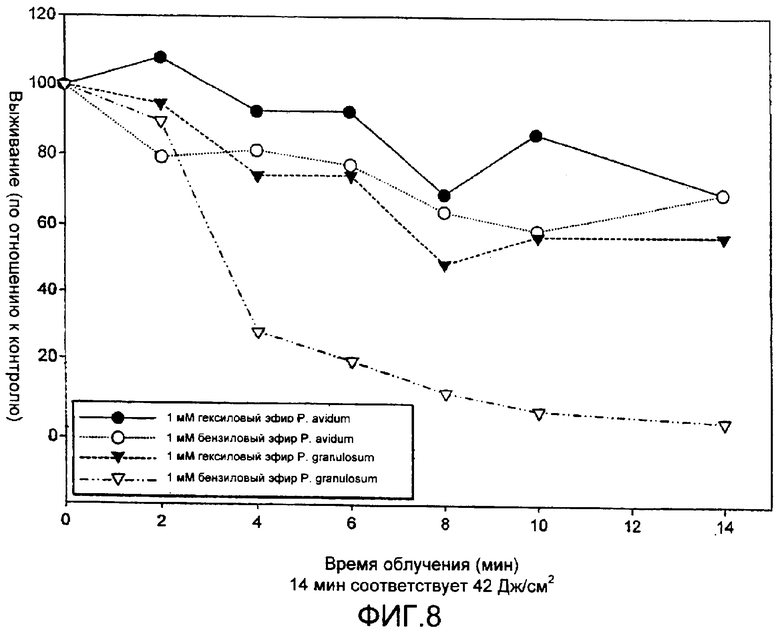
на Фиг.8 показаны фотодинамические эффекты у Р. granulosum и Р. avidum при использовании лампы CureLight LED (которая продается под торговым наименованием Aktilite 128 PhotoCure ASA) после инкубации с гексиловым эфиром АЛК и бензиловым эфиром АЛК;
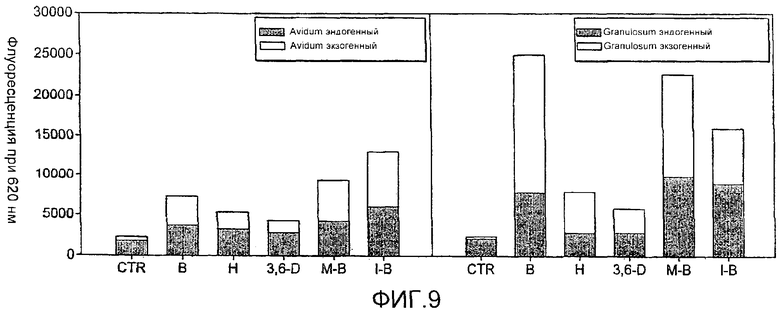
на Фиг.9 показано образование порфирина у Р. avidum и Р. granulosum после инкубации с 1 мМ бензиловым (В), гексиловым (Н), 3,6-диокса-1-октиловым (3,6-D), 4-метилбензиловым (М-В) и 4-изопропилбензиловым (I-B) эфирами АЛК;
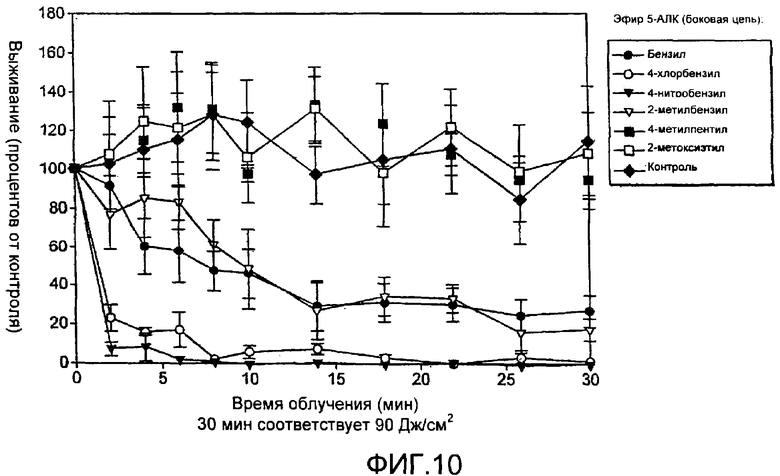
на Фиг.10 показаны фотодинамические эффекты у бактерий Р. acnes, инкубируемых с бензиловым эфиром АЛК, 4-хлорбензиловым эфиром АЛК, 4-нитробензиловым эфиром АЛК, 2-метилбензиловым эфиром АЛК, 4-метилпентиловым эфиром АЛК и 2-метоксиэтиловым эфиром АЛК;
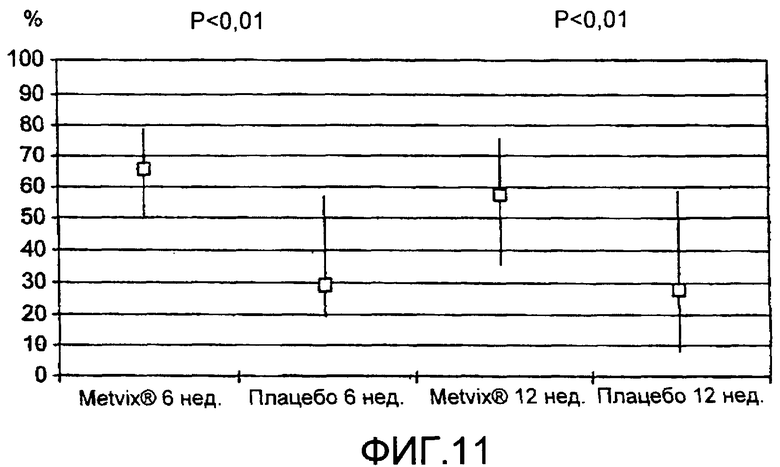
на Фиг.11 показано уменьшение воспалительных поражений после лечения Metvix® и ФДТ или кремом с плацебо и ФДТ в моменты времени 6 и 12 недель после лечения.
Общие способы
Культуры бактерий:
Propionibacterium acnes (P. acnes) получали из Американской коллекции типовых культур (АТСС) (АТСС №6919) и выращивали бактерии анаэробно в темноте на чашках с кровяным агаром при 37°С.
Ссылки: Skerman VB et al., Int. J. Syst. Bacteriol. 30: 225-420, 1980; Goodsell ME et al., Curr. Microbiol. 22: 225-230, 1991; Zierdt CH et al., Int. J. Syst. Bacteriol. 18: 33-47, 1968; Douglas HD and Gunter SE, J. Bacteriol. 52: 15-23, 1946; Johnson JL and Cummins CS, J. Bacteriol. 109: 1047-1066, 1972; Wang RF et al., Appl. Environ. Microbiol. 62: 1242-1247, 1996.
Propionibacterium granulosum (P. granulosum) получали из Американской коллекции типовых культур (АТСС №25564).
Ссылки: Johnson JL, et al., J. Bacteriol. 109(3): 1047-1066, 1972; Skerman VB et al., Int. J. Syst. Bacteriol. 30: 225-420, 1980.
Propionibacterium avidum (P. avidum) получали из АТСС (АТСС №25577).
Ссылки: Goodsell ME, et al., Curr. Microbiol. 22(4): 225-230, 1991; Skerman VB, et al., Int. J. Syst. Bacteriol. 30: 225-420, 1980.
Инкубация с эфирами АЛК
К каждой чашке Петри с кровяным агаром добавляли PIPES буфер (приблизительно 1 мл) и переносили раствор бактерий в 20 мл пробирку при помощи стерильной стеклянной палочки и пипетки Пастера. Данную суспензию затем разбавляли PIPES буфером до достижения оптической плотности (ОП) 1,00±0,01 при 550 нм, измеренной спектрофотометром. При этой ОП плотность бактерий составляет приблизительно 5×108 клеток на мл.
Отбирали пробу бактерий (100 мкл суспензии, содержащей приблизительно 5×108 бактерий на мл) и использовали ее в качестве контроля t=0. Аликвоты суспензии бактерий смешивали с подходящими объемами исходных растворов эфиров 5-АЛК (содержащих 100 мМ эфир АЛК) с получением подходящих концентраций и инкубировали в течение 4 часов при 37°С в темноте. Если не проводили облучение, то анализировали выживание, как описано ниже.
Облучение
В некоторых случаях облучение проводили на суспензиях бактерий, обработанных эфирами АЛК. Точные условия описаны в Примерах, приведенных ниже. После облучения выживание анализировали, как описано ниже.
Анализ выживания
После обработки эфирами АЛК (с облучением или без него) обработанные пробы бактерий (а также необработанные контроли) собирали и далее разбавляли PIPES буфером до плотности 1×104 бактерий на мл. Затем переносили 20 мл аликвоты этой суспензии на чашки Петри с бактоагаром (Bactoagar) (Futsaether et at., Can. J. Microbiol., 39(2): 180-186, 1993) и инкубировали в течение 3-5 суток при 37°С в темноте. Колонии, образующиеся на чашках Петри с бактоагаром, подсчитывали, используя счетчик колоний. Выживание клеток после инкубации с различными концентрациями эфиров 5-АЛК приведено по отношению к контрольным пробам (то есть пробам, отобранным в t=0 ч, и пробе, отобранной после 4 ч инкубации без эфира 5-АЛК), и дано как процент выживания:
Выживание=[Собработанных/Сконтрольных]×100%,
где С = число колоний.
Пример 1 - Токсичность в темноте
Для того чтобы найти подходящие условия для исследования фотодинамического эффекта у Р. acnes после инкубации с эфирами АЛК, провели исследование по анализу токсичности данных эфиров. Это было сделано в темноте для того, чтобы избежать любого эффекта ФДТ, вызванного посторонним светом. Инкубации и выживание анализировали, как описано в общем разделе, приведенном выше, и результаты приведены в прилагающейся Фиг.2.
Из Фиг.2 можно увидеть, что метиловый эфир по существу был нетоксичным для концентраций вплоть до 20 мМ, тогда как гексиловый эфир АЛК был очень токсичным. Бензиловый эфир АЛК показывал промежуточную токсичность.
Пример 2 - ФДТ с лампой широкого диапазона длин волн Curelight
Суспензии бактерий (Р. acnes) обрабатывали 4 мМ метиловым эфиром АЛК, 4 мМ бензиловым эфиром и 1 мМ гексиловым эфиром (вследствие результатов по высокой токсичности этого эфира в темноте), как описано в общем разделе, приведенном выше, разбавляли и облучали, используя лампу широкого диапазона длин волн Curelight (имеющуюся в продаже от PhotoCure ASA, Norway, красный свет с длиной волны 580-740 нм и плотностью потока, меньшей или равной 840 Вт/м2) в условиях с контролируемой температурой (например, при температуре окружающей среды). Во время облучения каждую вторую минуту отбирали аликвоты 2×20 мкл в целом в течение 10 минут и анализировали их на выживание, как описано в общем разделе, приведенном выше. Относительное выживание после облучения рассчитывали по отношению к контрольной пробе без облучения красным светом. Результаты показаны на Фиг.3.
На Фиг.3 можно увидеть, что бензиловый эфир АЛК был наиболее эффективным для умерщвления бактерий, тогда как метиловый эфир АЛК был наименее эффективным. При использовании 4 мМ бензилового эфира АЛК доза света приблизительно 10 Дж/см2 была достаточной для получения 100%-ного умерщвления. Гексиловый эфир АЛК также был довольно эффективным, но этот эфир использовали в более низкой концентрации (1 мМ) вследствие его высокой токсичности в темноте.
Пример 3 - ФДТ с лампой Curelight LED (которая продается PhotoCure ASA под торговым наименованием Aktilite)
Для того чтобы сравнить гексиловый эфир АЛК и бензиловый эфир АЛК в той же самой концентрации (1 мМ) и также протестировать другой источник света, проводили другой эксперимент, включающий использование красного света с узким диапазоном длин волн (лампа CureLight LED 128, которая продается PhotoCure ASA, Norway, под торговым наименованием Aktilite). Эта лампа состоит из 128 светоизлучающих диодов (LED) и имеет пиковую длину волны 634±3 нм. Спектр испускания данной лампы имеет полную ширину на полумаксимуме (FWHM) 18 нм. Плотность потока на расстоянии 50 мм составляет приблизительно 50 мВт/см2 (максимальное изменение плотности потока на намеченной площади составляет ±10%).
После инкубации с эфирами АЛК 10 мл бактериальных суспензий облучали в 5,5 см пластиковой чашке Петри (см. общий раздел, приведенный выше). Данные чашки Петри помещали на подложку, лежащую в большом резервуаре с водой при температуре окружающей среды, для того чтобы избежать температурных эффектов. Во время облучения каждую вторую минуту отбирали аликвоты 2×20 мкл в целом в течение 10 минут и переносили их на чашки Петри с бактоагаром. Через 3-5 суток инкубации (при 37°С в темноте) определяли выживание, как описано в общем разделе, и приводили его по отношению к необлученной контрольной пробе. Данные результаты показаны на Фиг.4.
На Фиг.4 можно увидеть, что 1 мМ бензиловый эфир АЛК давал значительно лучший фотодинамический эффект, чем 1 мМ гексиловый эфир АЛК. На самом деле, 26 минут облучения (соответствующих плотности потока 78 Дж/см2) убивало все бактерии, инкубируемые с 1 мМ бензиловым эфиром АЛК, но только 40% бактерий, инкубируемых с 1 мМ гексиловым эфиром АЛК.
Пример 4 - Внутриклеточное образование порфирина
Для исследования внутриклеточного образования порфирина после инкубации с эфирами АЛК бактерии (5×108 клеток на мл, 10 мл) инкубировали с эфирами АЛК при 37°С в темноте в течение четырех часов. Образование порфиринов отслеживали путем изучения эмиссионных спектров флуоресценции (порфирины показывают характерные пики). Процедура была следующей.
Для анализа количества эндогенно удерживаемых порфиринов 8 мл бактерий, инкубируемых в эфире 5-АЛК, добавляли в пластиковые пробирки и инкубировали при 2-3°С в холодильнике для того, чтобы остановить дальнейшее поглощение эфира 5-АЛК и/или образование порфирина. Затем данные клетки осаждали центрифугированием (5000 г, 5 мин, 2-3°С), супернатант отбрасывали, клетки ресуспендировали в свежем буфере (8 мл) и хорошо перемешивали. Аликвоты из 2 мл бактериальной суспензии переносили в стандартные имеющиеся в распоряжении пластиковые кюветы и определяли эмиссионные спектры флуоресценции суспензий клеток в флуоресцентном спектрометре Perkin Elmer LS 50 В, используя следующие установки:
Довольно широкий диапазон измеренных длин волн объяснялся необходимостью иметь контроль автофлуоресценции от бактерий, которая легче всего различается при более низких или более высоких длинах волн.
Данные результаты показаны на Фиг.5, из которой очевидно, что гексиловый эфир АЛК был наименее эффективным в индукции образования порфирина у Р. acnes, возможно из-за высокой токсичности в темноте. Метиловый эфир АЛК давал слегка более высокие уровни порфирина, но бензиловый эфир АЛК был наиболее эффективным индуктором биосинтеза порфирина в бактериях.
Пример 5 - Токсичность в темноте
Для того чтобы найти подходящие условия для исследования фотодинамического эффекта у двух других штаммов «бактерий, ассоциированных с угрями», выполнили исследование для анализа токсичности гексилового эфира АЛК и бензилового эфира АЛК у Р. granulosum и Р. avidum. Это сделали, как описано в Примере 1, и результаты приведены на Фиг.6.
Из Фиг.6 очевидно, что гексиловый эфир АЛК был значительно более токсичным, чем бензиловый эфир АЛК, и что гексиловый эфир в концентрации 4 мМ убивал 100% обоих штаммов. Также можно увидеть, что штамм Р. granulosum не слишком хорошо переносил условия инкубации.
Пример 6 - ФДТ с лампой с широким диапазоном длин волн Curelight
Суспензии бактерий (Р. granulosum и Р. avidum) обрабатывали 4 мМ метиловым эфиром АЛК, 4 мМ бензиловым эфиром и 1 мМ гексиловым эфиром (из-за высокой токсичности этого эфира в темноте), как описано в общем разделе, приведенном выше, разбавляли и облучали, используя лампу с широким диапазоном длин волн Curelight (имеющуюся в продаже от PhotoCure ASA, Norway - красный свет с длиной волны 580-740 нм и плотностью потока, меньшей или равной 840 Вт/м2) в условиях с контролируемой температурой (например, при температуре окружающей среды).
Используя способ, описанный в Примере 2, наблюдали эффекты ФДТ у Р. granulosum и Р. avidum после инкубации с гексиловым эфиром АЛК и бензиловым эфиром АЛК, используя лампу с широким диапазоном длин волн Curelight (PhotoCure ASA, Norway - красный свет с длиной волны 580-740 нм и плотностью потока, меньшей или равной 840 Вт/м2) в условиях с контролируемой температурой (например, при температуре окружающей среды). Результаты показаны на Фиг.7.
Пример 7 - Эффекты ФДТ с LED лампой
Эффекты ФДТ у Р. granulosum и Р. avidum после инкубации с гексиловым эфиром АЛК и бензиловым эфиром АЛК (1 мМ) наблюдали с использованием лампы Curelight LED 128 (которая продается PhotoCure ASA, Norway, под торговым наименованием Aktilite), как описано в Примере 3. Данный эксперимент выполняли, как описано в Примере 3, и результаты показаны на Фиг.8.
Пример 8 - Образование порфирина
Этот эксперимент проводили на Р. granulosum и Р. avidum, и он включал следующие эфиры АЛК: гексил-5-аминолевулинат, бензил-5-аминолевулинат, 3,6-диокса-1-октил-5-аминолевулинат, 4-изопропилбензил-5-аминолевулинат и 4-метилбензил-5-аминолевулинат.
Концентрация 1 мМ для этого эксперимента была выбрана, поскольку гексиловый эфир показывал высокую токсичность в темноте при концентрации 4 мМ (см. Пример 5). Данный эксперимент проводили, как описано в Примере 4, и количество эндогенно удерживаемых порфиринов, а также количество экзогенных порфиринов определяли флуоресцентной спектроскопией.
Результаты показаны на Фиг.9, где для количественной оценки использовали флуоресценцию при 620 нм. Несмотря на то, что имело место значительное отличие между двумя штаммами бактерий в отношении образования порфирина, из данной Фиг.9 очевидно, что бензиловые эфиры имели наибольшую способность индуцировать образование порфирина, за ними следовали гексиловый и 3,6-диокса-1-октиловый эфир.
Пример 9 - Токсичность в темноте
Для того чтобы найти подходящие условия для исследования фотодинамического эффекта у Р. acnes после инкубации с бензил-, 4-хлорбензил-, 4-нитробензил-, 2-метилбензил-, 4-метилпентил- и 2-метоксиэтил-5-аминолевулинатом, провели исследование для анализа токсичности этих соединений. Это сделали в темноте, как и в Примере 1, для того, чтобы избежать любого эффекта ФДТ, вызванного посторонним светом. Инкубации и выживание анализировали, как описано в общем разделе, приведенном выше, и результаты представлены в Таблице 1 ниже.
метилбензил
n=5
n=5
4
20
1,2
0,0
0,8
-
Данные вещества показывали довольно разные токсичности. 4-Нитробензиловый и 2-метоксиэтиловый эфиры АЛК практически не показывали токсичности при концентрациях вплоть до 20 мМ, тогда как 4-хлорбензиловый и 2-метилбензиловый эфиры АЛК показывали значительную токсичность при 4 мМ. При тестировании в концентрации 0,4 мМ наблюдали низкую токсичность для всех веществ, поэтому данную концентрацию выбрали для последующих экспериментов с ФДТ.
Пример 10 - Эффекты ФДТ с LED лампой
Исследовали фотодинамическую инактивацию Р. acnes после инкубации с эфирами 5-АЛК, перечисленными в Примере 9 (в концентрации 0,4 мМ), после облучения лампой Aktilite® 128. Данная лампа и экспериментальные подробности описаны в Примере 3, и результаты показаны на Фиг.10.
На Фиг.10 можно увидеть, что 4-хлорбензиловый и 4-нитробензиловый эфиры АЛК были наиболее эффективными. Действительно, требовалось только 10 минут облучения для получения практически 100%-ного умерщвления после инкубации с концентрациями 0,4 мМ этих эфиров. В этой концентрации бензиловый и 2-метилбензиловый эфиры АЛК показывали хорошие способности убивать бактерии (10-минутное облучение давало приблизительно 50-процентное умерщвление). Более слабый эффект ФДТ получали с 4-метилпентиловым и 2-метоксиэтиловым эфирами АЛК.
Пример 11 - Приготовление геля
К воде (10 мл) добавляют гидроксиэтилцеллюлозу (ГЭЦ) (150 мг, мол. масса 720000), данную смесь перемешивают и нагревают до 70°С. ГЭЦ растворяется и образует гель. Данную смесь охлаждают до 50°С и добавляют к гелю при перемешивании бензиловый эфир 5-АЛК HCl (300 мг) и бензиловый спирт (150 мг). Смесь перемешивают в течение 5 минут и наполняют ею 10 мл тюбик.
Данный гель содержит 3%-ный бензиловый эфир 5-АЛК HCl и является готовым к применению.
Пример 12 - Приготовление крема
Изопропилбензиловый эфир 5-АЛК HCl (500 мг) перемешивают в Ung. Merck (10 г) с использованием ступки и пестика. Образующимся кремом наполняют флакон.
Данный крем содержит 5%-ный изопропилбензиловый эфир 5-АЛК HCl и является готовым к применению.
Пример 13 - Клиническое применение метилового эфира АЛК
Целью этого клинического исследования было изучение эффективности и переносимости фотодинамической терапии (ФДТ) после местного нанесения метилового эфира АЛК для лечения умеренных воспалительных угрей на лице.
Тридцать пациентов в возрасте 15-28 лет с угрями от умеренных до тяжелых включали в слепое ожидаемое рандомизированное многоцентровое исследование с контролем в виде плацебо. Для каждой стороны лица каждого пациента случайным образом назначали обработку кремом, содержащим 160 мг/г метиламинолевулината гидрохлорида (который продается PhotoCure ASA, Norway, под торговым наименованием Metvix®), или кремом с плацебо и покрывали ее адгезивной окклюзионной повязкой (Tegaderm®, 3М или Opsite®, Smith and Nephew). С использованием канюли (1-2 мм) получали узелковые или кистозные повреждения для облегчения проникновения крема. Через 3 часа аккуратно стирали крем с обеих сторон лица непосредственно перед облучением некогерентным красным светом с использованием лампы Aktilite® CL 128 (PhotoCure ASA, средняя длина волны 635 нм, доза света 37 Дж·см-2). Затем повторяли облучение для другой стороны лица. Сторона лица, не получающая облучения, была покрыта, когда другую сторону облучали.
Вторую обработку делали через 2 недели. В каждом случае пациенты анализировали интенсивность боли, используя 10 см визуальную аналоговую шкалу. Поражения воспалительными и невоспалительными угрями подсчитывали в исходный момент времени (то есть перед началом обработки) и через 4 и 10 недель после последней обработки ФДТ. Исследователь анализировал общую тяжесть (см. Таблицу 2) угрей в исходный момент времени (семь пациентов имели серьезные угри по меньшей мере на одной стороне лица) и во время каждого визита для исследования, используя 6-точечную шкалу оценок. Данные анализировали на основе "заживления при лечении" (intention-to-treat), включая всех 30 пациентов.
Результаты данного исследования показаны на Фиг.11, где результаты для каждой группы представлены как среднее (квадрат) и 50%-ный процентиль (полоса) всех наблюдений. Это значит, что для каждой группы 25% наблюдений находится ниже и 25% находится выше полосы.
Имело место статистически значимое большее снижение общего индекса воспалительного поражения при использовании ФДТ с Metvix® по сравнению с ФДТ с плацебо на неделю 12 (среднее снижение 54% [95% CI35% - 64%] по отношению к 20% [95% Cl 8% - 50%], р=0,0006). ФДТ с Metvix® была связана с большей болью, чем ФДТ с плацебо, хотя ее интенсивность варьировала по отношению к центрам и была снижена при повторной обработке. Местные неблагоприятные события согласовались с этим способом лечения. Можно заключить, что ФДТ с Metvix® является эффективной в лечении умеренных-тяжелых воспалительных угрей на лице.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ 5-АМИНОЛЕВУЛИНОВОЙ КИСЛОТЫ И ЕЕ ПРОИЗВОДНЫХ В ТВЕРДОЙ ФОРМЕ ДЛЯ ФОТОДИНАМИЧЕСКОГО ЛЕЧЕНИЯ И ДИАГНОСТИКИ | 2008 |
|
RU2521228C2 |
| ЭФИРЫ 5-АМИНОЛЕВУЛИНОВОЙ КИСЛОТЫ КАК ФОТОЧУВСТВИТЕЛЬНЫЕ АГЕНТЫ В ФОТОХИМИОТЕРАПИИ | 2001 |
|
RU2246483C2 |
| НИЗКОМОЛЕКУЛЯРНЫЕ ПРОИЗВОДНЫЕ КАРБОКСАМИДНЫХ ГАЛОГЕНИРОВАННЫХ ПОРФИРИНОВ, А ИМЕННО ХЛОРИНОВ И БАКТЕРИОХЛОРИНОВ, И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2718923C2 |
| СОЛИ ПРИСОЕДИНЕНИЯ КИСЛОТЫ 5-АМИНОЛЕВУЛИНОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2005 |
|
RU2392266C2 |
| СОЕДИНЕНИЯ | 2013 |
|
RU2635563C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИНОВ И ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2009 |
|
RU2513483C2 |
| УСТРОЙСТВО ОБЛУЧЕНИЯ | 2009 |
|
RU2487740C2 |
| ПОЛУТВЕРДЫЕ КОМПОЗИЦИИ И ФАРМАЦЕВТИЧЕСКИЕ ПРОДУКТЫ | 2010 |
|
RU2526803C2 |
| Устройство облучения | 2012 |
|
RU2615870C2 |
| Устройство облучения | 2009 |
|
RU2619790C2 |
Изобретение относится к косметологии и дерматологии и представляет собой применение фотосенсибилизатора, выбранного из метилового эфира АЛК (аминолевулиновой кислоты), бензилового эфира АЛК или замещенного бензилового эфира АЛК или их фармацевтически приемлемой соли, в изготовлении лекарственного средства для применения в предупреждении или лечении угрей, ассоциированных с Propionibacterium. Изобретение обеспечивает эффективное лечение угрей на лице с помощью производных 5-аминолевулоновой кислоты (5-АЛК), применение которых позволяет избежать таких неблагоприятных эффектов, как дискомфорт, жжение, зуд, острую боль на протяжении облучения, отечную эритему, длительное раздражение и гиперчувствительность. 4 н. и 9 з.п. ф-лы, 2 табл., 11 ил.
1. Применение фотосенсибилизатора, выбранного из метилового эфира АЛК (аминолевулиновой кислоты), бензилового эфира АЛК или замещенного бензилового эфира АЛК, или их фармацевтически приемлемой соли, в изготовлении лекарственного средства для применения в предупреждении или лечении угрей, ассоциированных с Propionibacterium.
2. Применение по п.1, где указанный фотосенсибилизатор представляет собой метиловый эфир АЛК.
3. Применение по п.1, где указанный фотосенсибилизатор представляет собой бензиловый эфир АЛК.
4. Применение по п.1, где указанный фотосенсибилизатор представляет собой замещенный бензиловый эфир АЛК.
5. Применение по п.4, где указанный замещенный бензиловый эфир АЛК выбран из 2-метилбензилового эфира АЛК, 4-хлорбензилового эфира АЛК и 4-нитробензилового эфира АЛК.
6. Применение по любому из пп.1-5, где указанные угри ассоциированы с Propionibacterium acnes, Propionibacterium avidum или Propionibacterium granulosum.
7. Применение по любому из пп.1-5, где указанные угри выбраны из обыкновенных угрей, розовых угрей, шаровидных угрей, папулезных угрей и предменструальных угрей, предпочтительно из обыкновенных угрей.
8. Способ косметического лечения угрей, включающий местное нанесение фотосенсибилизатора, как определено в любом из пп.1-5, или его фармацевтически приемлемой соли на пораженный участок на теле и фотоактивацию указанного фотосенсибилизатора в пораженном участке.
9. Способ по п.8 для лечения угрей на лице.
10. Способ лечения или предупреждения угрей, включающий местное нанесение фотосенсибилизатора, как определено в любом из пп.1-5, или его фармацевтически приемлемой соли на участок кожи на теле и фотоактивацию указанного фотосенсибилизатора.
11. Способ лечения или предупреждения угрей, включающий стадии:
(а) местного нанесения фотосенсибилизатора, как определено в любом из пп.1-5, или его фармацевтически приемлемой соли на участок кожи на теле;
(б) ожидания в течение периода времени, необходимого для достижения фотосенсибилизатором эффективной концентрации в ткани в желательном месте; и
(в) фотоактивации фотосенсибилизатора в желательном месте.
12. Способ по п.11, при котором стадию (б) пропускают.
13. Способ по любому из пп.10-12, при котором указанный фотосенсибилизатор наносят местно на пораженный участок кожи.
| WO 9628412 A1, 19.09.1996 | |||
| СПОСОБ ОЧИСТКИ ВЫСШИХ ЖИРНЫХ СПИРТОВ, ПОЛУЧЕННЫХ ГИДРОЛИЗОМ БОРНОКИСЛЫХ ЭФИРОВ | 0 |
|
SU213788A1 |
| КОМПОЗИЦИЯ ПРОТИВ УГРЕЙ С ОДНОВРЕМЕННЫМ ЛЕЧЕНИЕМ ПОВЕРХНОСТНЫХ И ГЛУБОКИХ СЛОЕВ КОЖИ И ЕЕ ПРИМЕНЕНИЕ | 1994 |
|
RU2128506C1 |
Авторы
Даты
2010-04-10—Публикация
2005-11-04—Подача