Изобретение относится к области медицины, а именно неврологии, и может быть использовано у пациентов в остром периоде нетравматических внутричерепных кровоизлияний (НВЧК) для оценки реактивности вегетативной нервной системы (ВНС), в том числе и у больных с выраженной очаговой неврологической симптоматикой, различной степенью нарушения сознания и лечебном наркозе.
Способом объективной оценки функционального состояния ВНС является анализ вариабельности сердечного ритма (ВСР).
Известен способ оценки реактивности ВНС с помощью дыхательной пробы при записи кардиоциклов (Бабунц И.В., Мириджанян Э.М., Машаех Ю.А. Азбука вариабельности сердечного ритма. - Ставрополь, 2002. - С.49-50). По результатам пробы определяют реактивность парасимпатического отдела ВНС. Применяют два метода оценки результатов - расчет дыхательного коэффициента и спектральный анализ. В норме дыхательный коэффициент более 1,2. Значение коэффициента менее 1,2 отражает снижение реактивности парасимпатического отдела ВНС. При спектральном анализе дыхательной пробы в норме происходит повышение мощности волн высокой частоты (HF), а значение коэффициента вагосимпатического взаимодействия (LF/HF) существенно снижается. При незначительном уменьшении значения коэффициента LF/HF, либо в случае, если коэффициент не изменяется наблюдают недостаточную реактивность парасимпатического отдела ВНС. Парадоксальной считают реакцию, в которой происходит усиление симпатических влияний.
Недостатки способа:
- оценка реактивности только парасимпатического отдела ВНС;
- невозможность использования у пациентов с различной степенью нарушения сознания, грубой очаговой неврологической симптоматикой (например, при афазии) и в лечебном наркозе.
Наиболее близким к заявляемому является способ оценки реактивности ВНС при помощи активной ортостатической пробы (АОП) (Бабунц И.В., Мириджанян Э.М., Машаех Ю.А. Азбука вариабельности сердечного ритма. - Ставрополь, 2002. - С.43-46), принятый за прототип.
Пробу проводят в три этапа после предварительной адаптации к условиям исследования (отдых 10-15 минут):
1-й этап: непрерывная фоновая запись электрокардиограммы (ЭКГ) в горизонтальном положении, дыхание спокойное;
2-й этап: пациенту предлагают встать, запись при этом не прекращают и временные интервалы между R-зубцами ЭКГ (интервалы RR), записываются в вертикальном положении, дыхание спокойное;
3-й этап: после проведения пробы запись кардиоинтервалов в горизонтальном положении, дыхание спокойное.
Анализируют АОП на основании характера переходного процесса между первым и вторым этапом.
Для оценки реактивности парасимпатического отдела ВНС высчитывают коэффициент 30/15 (К 30/15), равный отношению максимального RR интервала в диапазоне 30 сек к минимальному RR интервалу в диапазоне 15 сек. При значении коэффициента менее 1.35 реактивность парасимпатического отдела ВНС расценивают как сниженную.
Для оценки реактивности симпатического отдела ВНС производят спектральный анализ участка записи кардиоинтервалограммы в вертикальном положении после исключения из обработки переходного периода. Критерием недостаточной реактивности симпатического отдела ВНС при проведении АОП считают увеличение относительной мощности медленных волн (LF) при нагрузке по сравнению с фоном менее 10%. Значение коэффициента LF/HF во время АОП более 16,5 оценивают как избыточную реактивность симпатического отдела ВНС.
Недостатки прототипа:
- недостаточно полная оценка реактивности ВНС, так как оценивают только симпатический и парасимпатический отделы ВНС;
- невозможность использования у пациентов в остром периоде НВЧК из-за постельного режима больного, наличия грубой очаговой неврологической симптоматики, различной степени нарушения сознания и у пациентов, находящихся в лечебном наркозе.
Изобретение направлено на создание способа оценки реактивности ВНС в остром периоде внутричерепных кровоизлияний, обеспечивающего повышение точности за счет оценки влияний надсегментарных центров на реактивность ВНС, в том числе и у больных, находящихся на постельном режиме, с выраженной общемозговой симптоматикой (различная степень нарушение сознания, наличие гипертензионного синдрома), грубой очаговой симптоматикой (афазии, парезы, атаксия), либо в лечебном наркозе.
Указанный технический результат при осуществлении изобретения достигается тем, что в известном способе оценки реактивности ВНС в остром периоде внутричерепных кровоизлияний, включающем проведение анализа ВСР в покое, во время пробы и при восстановлении после пробы, используя временной анализ кардиоинтервалов, вариационную пульсометрию, анализ волновой структуры ритма и суммарную оценку регуляторных систем, особенность заключается в том, что запись проводят на фоне люмбальной пункции с измерением давления цереброспинальной жидкости (ЦСЖ); снижение напряжения высших вегетативных центров (НВВЦ), оцениваемое по вкладу очень медленных волн (VLF) после люмбальной пункции, расценивают как адекватную реактивность ВНС, таким образом, при адекватной реактивности ВНС и отсутствии внутричерепной гипертензии напряженная ваготония фона во время пункции переходит в напряженный баланс, а при восстановлении после пробы в баланс без напряжения, напряженный баланс с уменьшением вклада VLF, либо в напряженную ваготонию; переход напряженного баланса в фоне и во время пункции в баланс без напряжения в восстановительном периоде; переход баланса при фоновой записи в напряженную ваготонию во время пункции с последующим восстановлением в баланс без НВВЦ; при сохранении НВВЦ или нарастании его во время и после пункции реактивность ВНС оценивают как неадекватную: недостаточную или истощение, причем при недостаточной реактивности ВНС напряженный баланс в покое переходит в напряженную симпатикотонию во время пункции, а затем в напряженный баланс или напряженную симпатикотонию с уменьшением НВВЦ в восстановительном периоде; напряженная симпатикотония в покое переходит в напряженную симпатикотонию с уменьшением НВВЦ и VLF<50%, а при наличии внутричерепной гипертензии и истощение реактивности ВНС напряженная симпатикотония или ваготония при VLF>50% в покое не меняется во время и после пункции, либо происходит нарастание НВВЦ.
Способ осуществляют следующим образом. Регистрируют ЭКГ-сигнал в одном из стандартных (I, II, III) или грудных отведениях.
1-й этап: в горизонтальном положении при спокойном дыхании производят фоновую запись в течение 5-10 минут;
2-й этап: в этом же положении по стандартной методике производят люмбальную пункцию с выведением ЦСЖ и измерением давления ликвора, на фоне чего записывают кардиоинтервалограмму продолжительностью 5-10 минут в зависимости от длительности выведения ликвора;
3-й этап: восстановление после пункции продолжительностью 5-10 минут.
Анализ нескольких последовательных записей по 5 минут подтверждает условия стабильности физиологического статуса.
Оценивают ВСР, для чего используют методы временного анализа кардиоинтервалов (статистические и геометрические), вариационную пульсометрию по Баевскому P.M., анализ волновой структуры ритма и методы комплексной оценки регуляторных систем.
Анализируют:
1. Статистические показатели: SDNN (среднее квадратичное отклонение величин нормальных RR интервалов); CV (коэффициент вариации).
2. Геометрические показатели: ΔX - разница значений максимального и минимального RR интервала (указывает на максимальную амплитуду колебаний RR интервалов); ТИ (триангулярный индекс).
3. Вариационную пульсометрию по P.M.Баевскому: ИН (индекс напряжения регуляторных систем, стресс-индекс).
Оценивают общую мощность спектра (TP), абсолютные значения (VLF, LF, HF) в мс^2 и относительные (VLF%, LF%, HF% от TP) значения каждого частотного диапазона. Рассчитывают: LF/HF; ИЦ (индекс централизации).
В качестве нормативных данных используют стандарты для ручного и автоматизированного анализа ВСР, принятые рабочей группой Европейского кардиологического общества и Северо-Американского общества стимуляции и электрофизиологии на совместном заседании в 1996 году, а также методические рекомендации Комиссии по клинико-диагностическим приборам и аппаратам Комитета по новой медицинской технике Минздрава России (протокол №4 от 11 апреля 2000 г.).
Для определения уровня адаптационно-приспособительных возможностей проводят интегральную оценку состояния регуляторных систем по показателю СОРС (суммарная оценка регуляторных систем), вычисляемого в баллах с помощью алгоритма (Бабунц И.В., Мириджанян Э.М., Машаех Ю.А. Азбука вариабельности сердечного ритма. - Ставрополь, 2002. - С.36-37).
Анализируют реактивность ВНС.
Регулирующие влияния высших вегетативных центров оценивают по вкладу VLF в ТР. Снижение НВВЦ (уменьшение VLF) или его полный регресс во время и после люмбальной пункции оценивают как адекватную реактивность ВНС, при сохранении НВВЦ или его нарастании - как неадекватную реактивность.
По степени изменения НВВЦ можно выделить:
1) незначительное НВВЦ - VLF=30-40%;
2) умеренное НВВЦ - VLF=40-50%;
3) выраженное НВВЦ - VLF>50%.
Типы реактивности ВНС в зависимости от степени НВВЦ и наличия внутричерепной гипертензии в остром периоде внутричерепных кровоизлияний представлены в табл.1.
На фоне лечебного наркоза и благоприятном течении заболевания с отсутствием внутричерепной гипертензии у пациентов регистрируют ригидный ритм при СОРС от +3 до -3, характерный для первых двух типов реактивности ВНС.
Напряженная симпатикотония или напряженная ваготония при люмбальной пункции на фоне ригидного ритма с СОРС от +10 до +12 является предиктором летального исхода в ближайшем периоде с TP≤10 (мс2), а при ТР=1(мс2) можно констатировать смерть мозга, что соответствует третьему типу реактивности ВНС - истощению.
Заявленный способ разработан в РНХИ им. проф. А.Л.Поленова и прошел клинические испытания при обследовании 12 больных в остром периоде НВЧК.
Приводим примеры - выписки из истории болезни.
Пример 1. Пациентка Н., 28 лет, история болезни №618, и поступила в РНХИ на 3-и сутки после первого кровоизлияния, развившегося на фоне физической нагрузки, когда во время занятий в спортзале появилась резкая боль в области шеи и в голове, после чего присоединилась тошнота и рвота на фоне подъема АД до 140 мм рт.ст. По «Скорой помощи» госпитализирована в городскую больницу с диагнозом шейный остеохондроз. На КТ АГ головного мозга - признаки САК, мешотчатая аневризма параклиноидного отдела правой ВСА, в связи с чем для дальнейшего обследования и лечения поступила в РНХИ. На 3-й сутки от кровоизлияния клиническая картина заболевания была представлена общемозговой симптоматикой в виде головной боли гипертензионного характера, слабоположительным менингеальным синдром, рефлексами орального автоматизма, пирамидной недостаточностью с 2-х сторон, больше слева. Интраоперационно произошло повторное ЦСАК с формированием в/мозговой гематомы медиобазальных отделов правой лобной доли, выявлены признаки вазоспазма III ст., в связи с чем пациентка на протяжении нескольких дней находилась в лечебном наркозе. На 15-е сутки острого периода произведен анализ ВСР на фоне АД 127/77 мм рт.ст., давления ЦСЖ=180 мм вод. ст. (нормотензия). Показатели кардиоритмограммы приведены в табл.2.
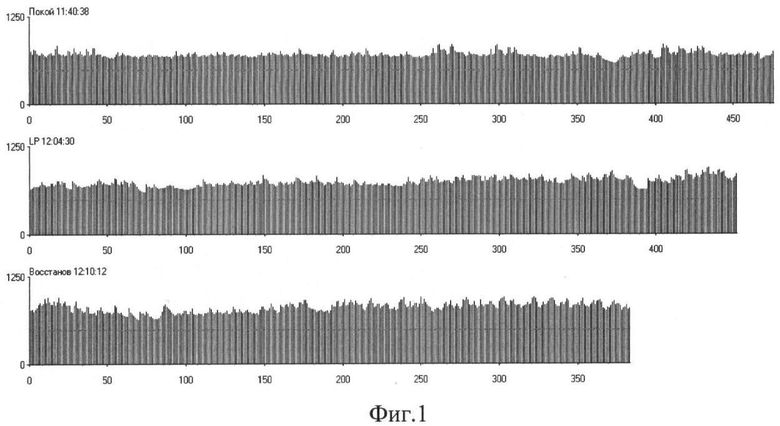
На Фиг.1 представлена ритмограмма в покое, при люмбальной пункции и восстановлении после пробы.
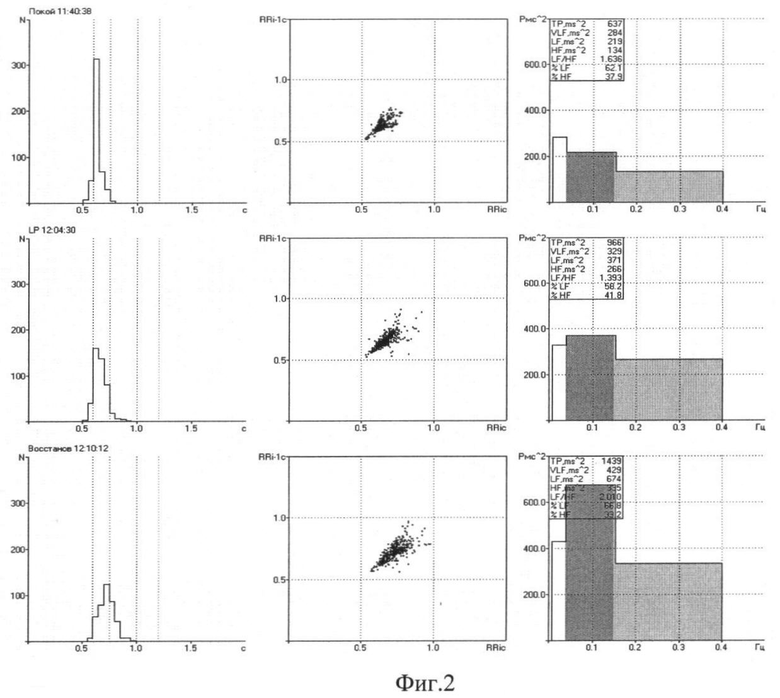
На Фиг.2 - гистограммы, скатерграммы и спектры мощности в покое, во время и после пробы.
Заключение: в покое у пациентки наблюдают напряженный баланс с умеренным НВВЦ (40%<VLF<50%, 0,5<LF/HF<2,5), во время люмбальной пункции - напряженный баланс с уменьшением напряжения (30%<VLF<40%, 0,5<LF/HF<2,5), в восстановительном периоде - баланс с некоторым нарастанием вклада симпатических волн, но без НВВЦ (VLF=30%, 0,5<LF/HF<2,5 при 40%<LF<50%). СОРС=+4 (состояние функционального напряжения). Адекватная реактивность ВНС.
После выхода из острого периода кровоизлияния пациентка была выписана в компенсированном состоянии с легким левосторонним гемипарезом до 4 баллов и левосторонней гемигипалгезией без гипертензионно-гидроцефального синдрома.
Пример 2. Пациентка Ш., 41 года, история болезни №2799, в 2006 г. перенесла ЦСАК, при поступлении в институт больная перенесла повторное САК аневризматической этиологии из мешотчатой аневризмы параклиноидного отдела правой ВСА, выполнена окклюзия аневризмы отделяемыми спиралями. При осмотре в первые трое суток от кровоизлияния в неврологическом статусе отмечалась умеренно выраженная общемозговая симптоматика в виде головной боли гипертензионного характера, микроочаговая симптоматика в виде положительных рефлексов орального автоматизма, пирамидной недостаточности в виде оживления рефлексов и появления патологических знаков с двух сторон, больше слева. На вторые сутки острого периода САК выполнена запись ВСР до, во время и после люмбальной пункции на фоне АД=100/70 мм рт.ст., давления ЦСЖ=200 мм вод. ст. (пограничное давление). Показатели кардиоритмограммы представлены в табл.3.
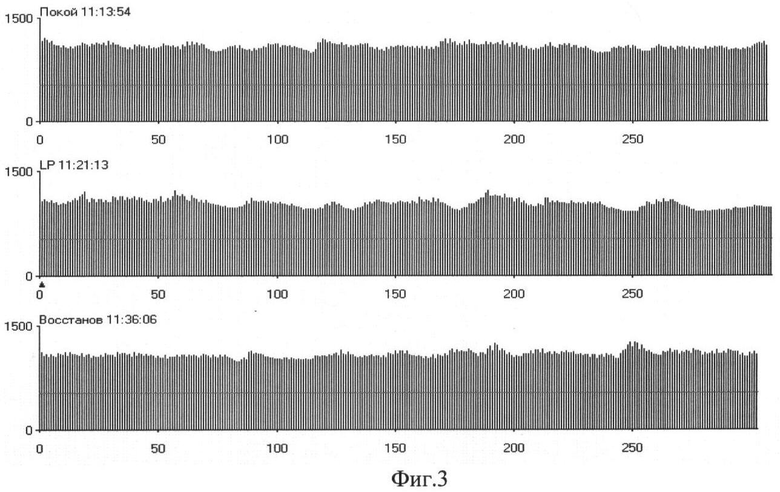
На Фиг.3 представлена интервалокардиограмма в покое, при люмбальной пункции и в восстановительном периоде после пробы.
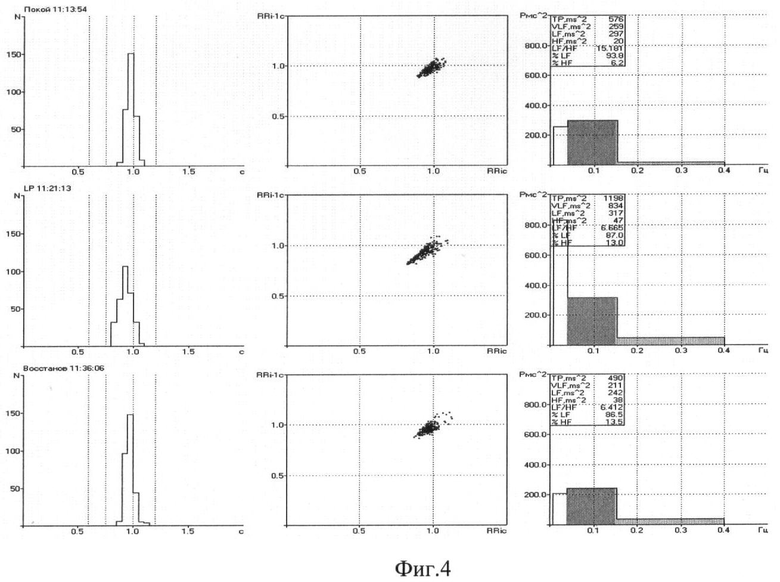
На Фиг.4 - гистограммы, скатерграммы и спектры мощности в покое, во время и после пробы.
Заключение: в покое наблюдают напряженную симпатикотонию, при люмбальной пункции - напряженную симпатикотонию с некоторым нарастанием НВВЦ, а после пробы - напряженную симпатикотонию с уменьшением НВВЦ до умеренного, при VLF<50% и уменьшением симпатических влияний. Данное состояние при СОРС=+7. Недостаточная реактивность ВНС.
По окончанию острого периода (после 21-х суток) пациентка была выписана в компенсированном состоянии без гипертензионно-гидроцефального синдрома и грубой очаговой симптоматики.
Пример 3. Пациентка К., 61 г., и/б №120, поступила в РНХИ на 4-е сутки вентрикулярного кровоизлияния. При поступлении состояние тяжелое, компенсированное по витальным функциям. Неврологически выраженный гипертензионный и менингеальным синдромы, двусторонняя пирамидная недостаточность, больше справа. При дообследовании с помощью КТ АГ данных за АА, АВМ не получено, этиология кровоизлияния была расценена как гипертоническая и атеросклеротическая. За время нахождения в стационаре состояние больной было нестабильным, наблюдались признаки диэнцефально-катаболического синдрома (гипертензия, гипертермия до фебрильных цифр), стволовая симптоматика (неполный синдром Парино, дисфония, дизартрия, дисфагия) с последующим регрессом. На 21-е сутки острого периода пациентке была выполнена люмбальная пункция на фоне записи интервалокардиограммы при АД=140/90 мм рт.ст., давлении ЦСЖ=230 мм вод.ст. (гипертензия). Показатели кардиоритмограммы представлены в табл.4.
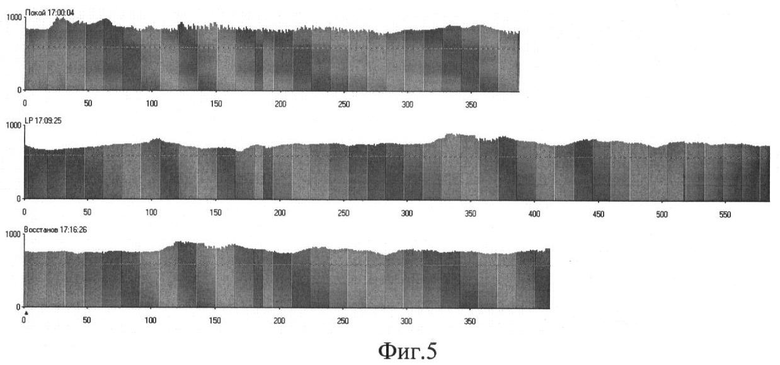
На Фиг.5 представлена интервалокардиограмма в покое, при люмбальной пункции и в восстановительном периоде после пробы.
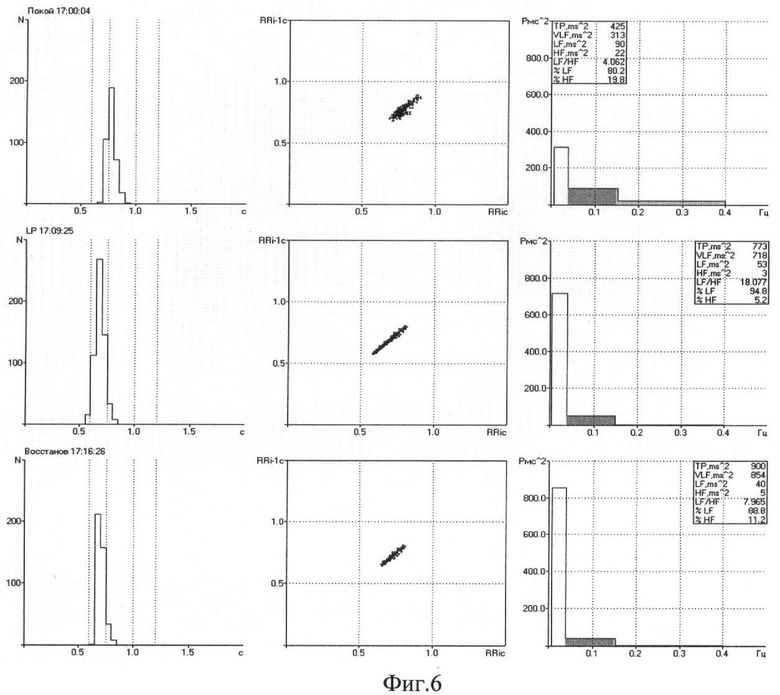
На Фиг.6 - гистограммы, скатерграммы и спектры мощности в покое, во время и после пробы.
Заключение: в покое наблюдают напряженную симпатикотонию, которая сохраняется как во время люмбальной пункции, так и в восстановительном периоде после пробы с выраженным НВВЦ (VLF>50%, LF/HF>2,5), при СОРС=+7 (состояние перенапряжения). Неадекватная реактивность ВНС - истощение.
В связи с развитием гипертензионно-гидроцефального синдрома пациентке выполнено вентрикулоперитонеальное шунтирование (ВПШ). После ВПШ отмечалась положительная динамика, пациентка была выписана, однако в восстановительном периоде - на 4-м месяце после кровоизлияния пациентка скончалась от острого инфаркта миокарда.
Использование заявленного способа обеспечивает возможность оценки реактивности ВНС у пациентов в остром периоде НВЧК с различной степенью выраженности общемозговой и очаговой симптоматики, находящихся в лечебном наркозе, а также повышение точности выявления адаптивных возможностей организма с определением варианта течения заболевания и позволяет выявлять корреляцию степени напряжения надсегментарных центров с наличием гипертензионно-гидроцефального синдрома.
Оценка патогенетических механизмов степени НВВЦ по вкладу очень медленных волн у пациентов с внутричерепной гипертензией в зависимости от латерализации и типа кровоизлияния при анализе вариабельности сердечного ритма до, во время и после люмбальной пункции, производимой по показаниям, является наиболее ранним критерием прогноза течения заболевания и эффективности лечения (медикаментозного и хирургического), обеспечивающее повышение точности диагностики отклонений, возникающих в регулирующих системах, предшествующих грубым гемодинамическим, метаболическим и энергетическим нарушениям.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОРРЕКЦИИ ВЕГЕТАТИВНОГО БАЛАНСА ОРГАНИЗМА СПОРТСМЕНОВ | 2008 |
|
RU2373975C1 |
| СПОСОБ ДИАГНОСТИКИ СМЕРТИ МОЗГА | 2009 |
|
RU2389432C1 |
| СПОСОБ ОЦЕНКИ ВЕГЕТАТИВНОГО ТОНУСА | 2007 |
|
RU2361508C2 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ ПОДРОСТКОВ | 2004 |
|
RU2266703C1 |
| СПОСОБ ЛЕЧЕНИЯ ВЕГЕТАТИВНОЙ ДИСФУНКЦИИ ПРИ ФИБРОЗНО-КИСТОЗНОЙ БОЛЕЗНИ МОЛОЧНЫХ ЖЕЛЕЗ У ЖЕНЩИН РЕПРОДУКТИВНОГО ВОЗРАСТА | 2011 |
|
RU2471494C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ БИСОПРОЛОЛОМ ПАЦИЕНТОВ, ПЕРЕНЕСШИХ ИНФАРКТ МИОКАРДА, ПРИ НАЛИЧИИ СИНУСОВОГО РИТМА | 2015 |
|
RU2615730C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ У ДЕТЕЙ, БОЛЬНЫХ ТУБЕРКУЛЕЗОМ | 2010 |
|
RU2459575C2 |
| СПОСОБ КУРОРТНОГО ЛЕЧЕНИЯ ВЕГЕТО-СОСУДИСТОЙ ДИСТОНИИ У РАБОТНИКОВ ОПАСНОГО ХИМИЧЕСКОГО ПРОИЗВОДСТВА | 2013 |
|
RU2551302C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ДИСФУНКЦИИ И ТИПА ДИСФУНКЦИИ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ У ДЕТЕЙ И ПОДРОСТКОВ | 2007 |
|
RU2338459C1 |
| ЭЛЕКТРОФИЗИЧЕСКИЙ СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ СИСТЕМЫ РЕГУЛЯЦИИ МОЗГОВОГО КРОВООБРАЩЕНИЯ | 2005 |
|
RU2301085C2 |
Изобретение относится к области медицины, а именно неврологии. Регистрируют кардиоинтервалограмму в покое, во время пробы и в период восстановления после пробы. Проводят временной анализ кардиоциклов, волновой структуры ритма и осуществляют комплексную оценку регуляторных систем. При этом в качестве пробы используют люмбальную пункцию с измерением давления цереброспинальной жидкости. При отсутствии внутричерепной гипертензии и уменьшении вклада очень медленных волн (VLF) после пробы, если напряженная ваготония покоя во время пункции переходит в напряженный баланс, а в восстановительном периоде в напряженную ваготонию, напряженный баланс или баланс без напряжения, либо, если напряженный баланс покоя сохраняется во время проведения пункции и переходит в баланс без напряжения в восстановительном периоде, либо, если баланс в покое переходит в напряженную ваготонию и в баланс в восстановительном периоде - реактивность ВНС оценивают адекватной. При наличии внутричерепной гипертензии или ее отсутствии и при VLF более 30% после пробы, если напряженный баланс покоя при пункции переходит в напряженную симпатикотонию, а затем в восстановительном периоде в напряженный баланс или напряженную симпатикотонию, или напряженная симпатикотония покоя переходит в напряженную симпатикотонию в восстановительном периоде с уменьшением VLF - реактивность ВНС оценивают, как неадекватную недостаточную. При наличии внутричерепной гипертензии, если ваготония во время пункции и в восстановительном периоде переходит в напряженную ваготонию, или симпатикотония в напряженную симпатикотонию, или напряженная ваготония и напряженная симпатикотония покоя не меняется во время и после пробы, либо происходит нарастание вклада VLF более 50% - реактивность ВНС оценивают, как неадекватную истощенную. Способ обеспечивает повышение точности за счет оценки влияний надсегментарных центров на реактивность ВНС. 6 ил., 4 табл.
Способ оценки реактивности вегетативной нервной системы (ВНС) в остром периоде внутричерепных кровоизлияний, включающий регистрацию кардиоинтервалограммы в покое, во время пробы и в период восстановления после пробы, а также проведение временного анализа кардиоциклов, волновой структуры ритма и комплексной оценки регуляторных систем, отличающийся тем, что в качестве пробы используют люмбальную пункцию с измерением давления цереброспинальной жидкости и при отсутствии внутричерепной гипертензии и уменьшении вклада очень медленных волн (VLF) после пробы, если напряженная ваготония покоя во время пункции переходит в напряженный баланс, а в восстановительном периоде в напряженную ваготонию, напряженный баланс или баланс без напряжения, либо, если напряженный баланс покоя сохраняется во время проведения пункции и переходит в баланс без напряжения в восстановительном периоде, либо, если баланс в покое переходит в напряженную ваготонию и в баланс в восстановительном периоде - реактивность ВНС оценивают адекватной; при наличии внутричерепной гипертензии или ее отсутствии и при VLF более 30% после пробы, если напряженный баланс покоя при пункции переходит в напряженную симпатикотонию, а затем в восстановительном периоде в напряженный баланс или напряженную симпатикотонию, или напряженная симпатикотония покоя переходит в напряженную симпатикотонию в восстановительном периоде с уменьшением VLF - реактивность ВНС оценивают как неадекватную недостаточную, при наличии внутричерепной гипертензии, если ваготония во время пункции и в восстановительном периоде переходит в напряженную ваготонию, или симпатикотония в напряженную симпатикотонию, или напряженная ваготония и напряженная симпатикотония покоя не меняется во время и после пробы, либо происходит нарастание вклада VLF более 50% - реактивность ВНС оценивают как неадекватную истощенную.
| БАБУНЦ И.В | |||
| и др | |||
| Азбука вариабельности сердечного ритма | |||
| - Ставрополь, 2002, с.36-37 | |||
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ ЦЕНТРАЛЬНОЙ НЕЙРОГОРМОНАЛЬНОЙ РЕГУЛЯЦИИ | 2002 |
|
RU2233616C2 |
| СПОСОБ КУРМЫШКИНЫХ ОЦЕНКИ РЕАКТИВНОСТИ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ | 1990 |
|
RU2016542C1 |
| US 2008058662 A1, 06.03.2008 | |||
| БАБУНЦ И.В | |||
| Оптимизация методов исследования вегетативного статуса у лиц молодого возраста: Автореф | |||
| дис | |||
| - Краснодар, 2007, с.5-20 | |||
| VUKSANOVIC V | |||
| et al | |||
| Heart rate variability in mental stress aloud | |||
| Med | |||
| Eng | |||
| Phys | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2010-04-27—Публикация
2008-07-23—Подача