Настоящее изобретение относится к соединениям общей формулы
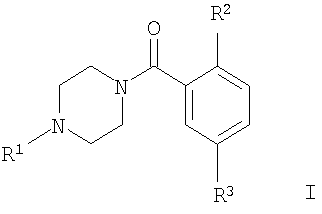
где
R1 представляет собой группу
 или
или  или
или
 или
или 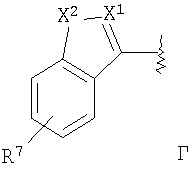 ;
;
R2 представляет собой неароматический гетероцикл или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или
-(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2, CN или SO2R';
R4 представляет собой водород, гидрокси, галоген, NO2, низший алкил, низший алкил, замещенный галогеном, низший алкокси, SO2R' или C(O)OR'';
R5/R6/R7 представляют собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
X1/X1' представляют собой СН или N при условии, что X1/X1' одновременно не являются СН;
X2 представляет собой О, S, NH или N(низший алкил);
n представляет собой 0, 1 или 2;
и к фармацевтически активным кислотно-аддитивным солям.
Настоящее изобретение относится к соединениям общей формулы I, к способам получения этих соединений, к фармацевтической композиции, содержащей их, и к их применению при лечении неврологических и психоневрологических заболеваний.
Неожиданно было установлено, что соединения общей формулы 1 являются хорошими ингибиторами переносчика глицина 1 (GlyT-1) и что они обладают высокой селективностью к ингибиторам переносчика глицина 2 (GlyT-2).
Настоящее изобретение включает следующие соединения формул IA, IБ, IB и IГ:
Соединение формулы
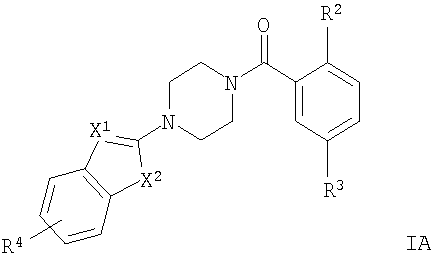
где
R2 представляет собой неароматический гетероцикл или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или
-(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2, CN или SO2R';
R4 представляет собой водород, гидрокси, галоген, NO2, низший алкил, низший алкил, замещенный галогеном, низший алкокси, SO2R' или C(O)OR'';
X1 представляет собой СН или N;
X2 представляет собой О, S, NH или N(низший алкил);
n представляет собой 0, 1 или 2;
и фармацевтически активные кислотно-аддитивные соли.
Соединение формулы

где
R2 представляет собой неароматический гетероцикл или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(CH2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2, CN или SO2R';
R5 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
X1 представляет собой СН или N;
X2 представляет собой О, S, NH или N(низший алкил);
n представляет собой 0, 1 или 2;
и фармацевтически активные кислотно-аддитивные соли.
Соединение формулы

где
R2 представляет собой неароматический гетероцикл или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или
-(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2, CN или SO2R';
R6 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
X1/X1' представляют собой СН или N при условии, что X1/X1' одновременно не являются СН;
n представляет собой 0, 1 или 2;
и фармацевтически активные кислотно-аддитивные соли.
Соединение формулы

где
R2 представляет собой неароматический гетероцикл или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или
-(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2, CN или SO2R';
R7 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
X1 представляет собой СН или N;
X2 представляет собой О, S, NH или N(низший алкил);
n представляет собой 0, 1 или 2;
и фармацевтически активные кислотно-аддитивные соли.
Неожиданно было установлено, что соединения общей формулы I являются хорошими ингибиторами переносчика глицина 1 (GlyT-1) и что они обладают высокой селективностью к ингибиторам переносчика глицина 2 (GlyT-2).
Шизофрения представляет собой прогрессирующее и разрушающее неврологическое заболевание, характеризующееся периодическими положительными симптомами, такими как бред, галлюцинации, психические расстройства и психоз, и постоянными отрицательными симптомами, такими как притупленный аффект, нарушенное внимание и социальная самоизоляция, и когнитивными ухудшениями (Lewis DA and Lieberman JA, Neuron, 2000, 28: 325-33). В течение десятилетий исследование сосредотачивалось на гипотезе "дофаминергической гиперактивности", которая привела к терапевтическим воздействиям, включающим блокаду дофаминергической системы (Vandenberg RJ and Aubrey KR., Exp.Opin. Ther. Targets, 2001, 5(4): 507-518; Nakazato A and Okuyama S, et al., 2000, Exp.Opin. Ther. Patents, 10(1): 75-98). Этот фармакологический подход плохо согласуется с отрицательными и когнитивными симптомами, которые являются лучшими показателями функционального результата (Sharma Т., Br.J. Psychiatry, 1999, 174 (suppl. 28): 44-51).
Комплементарная модель шизофрении, предложенная в середине 1960-х годов, основывалась на психотомиметическом действии, вызванном блокадой глутаматной системы соединениями подобными фенциклидину (РСР) и родственным агентам (кетамину), которые являются неконкурентными антагонистами NMDA рецептора. Интересно, что у здоровых волонтеров РСР-индуцированное психотомиметическое действие объединяет как положительные и отрицательные симптомы, так и когнитивную дисфункцию, таким образом, сильно напоминая шизофрению у пациентов (Javitt DC et al., 1999, Biol. Psychiatry, 45: 668-679 и ссыл. здесь). Кроме того, трансгенные мыши, экспрессирующие пониженные уровни NMDAR1 субъединицы, проявляют поведенческие нарушения, подобные тем, которые наблюдаются у фармакологически индуцированных моделей шизофрении, подтверждая модель, в которой пониженная активность NMDA рецептора приводит к поведению, подобному шизофрении (Mohn AR et al., 1999, Cell, 98: 427-236).
Глутаматная нейротрансмиссия, в особенности активность NMDA рецептора, играет определяющую роль в синаптической пластичности, обучении и памяти, так как считается, что NMDA рецепторы служат в качестве дифференцированного переключателя для синхронизации предела синаптической пластичности и формирования памяти (Hebb DO, 1949, The organization of behavior, Wiley, NY; Bliss TV and Collingridge GL, 1993, Nature, 361: 31-39). Трансгенные мыши, сверхэкспрессирующие NMDA NR2B субъединицу, проявляют повышенную синаптическую пластичность и значительную способность к обучению и памяти (Tang JP et al., 1999, Nature: 401: 63-69).
Таким образом, если патофизиология шизофрении включает недостаток глутамата, можно предсказать, что повышенная глутаматная трансмиссия, в особенности посредством активации NMDA рецептора, вызовет как антипсихотические эффекты, так и эффекты повышения когнитивной функции.
Известно, что аминокислота глицин выполняет по меньшей мере две важные функции в ЦНС. Действует как тормозящая аминокислота, связывая чувствительные к стрихнину глициновые рецепторы, и также влияет на возбудительную активность, действуя как основной коагонист с глутаматом для функции рецептора N-метил-О-аспартата (NMDA). Когда глутамат выделяется из синаптических окончаний зависимым от активности способом, глицин, несомненно, присутствует на более постоянном уровне, и считается, что модулирует/контролирует рецептор для его отклика на глутамат.
Один из самых эффективных способов контроля синаптических концентраций нейротрансмиттера состоит в том, чтобы влиять на их повторное поглощение в синапсах. Переносчики нейротрансмиттера, удаляя нейротрансмиттеры из внеклеточной области, могут контролировать их внеклеточное время жизни и, следовательно, модулировать величину синаптической трансмиссии (Gainetdinov RR et al, 2002, Trends in Pharm. Sci., 23(8): 367-373).
Переносчики глицина, которые являются частью натриевого и хлоридного семейства переносчиков нейротрансмиттера, играют важную роль в завершении постсинаптических глицинергических действий и поддержании низкой внеклеточной концентрации глицина в ходе повторного поглощения глицина в пресинаптических нервных окончаниях и окружающих точных глиальных процессов.
Два разных гена переносчиков глицина были клонированы (GlyT-1 и GlyT-2) из мозга млекопитающих, они дают начало двум переносчикам с гомологией последовательностей аминокислот ~50%. GlyT-1 присутствует в четырех изоформах, являющихся результатом альтернативного сплайсинга и альтернативного использования промотора (1а, 1b, 1с и 1d). Только две из этих изоформ были найдены в мозге грызунов (GlyT-1а и GlyT-1b). GlyT-2 также показывает некоторую степень гетерогенности. Две GlyT-2 изоформы (2а и 2b) были идентифицированы в мозге грызунов. Известно, что GlyT-1 располагается в ЦНС и периферических тканях, тогда как GlyT-2 является характерным для ЦНС. GlyT-1 обладает преимущественно глиальным распределением и обнаружен не только в областях, соответствующих чувствительным к стрихнину глициновым рецепторам, но также за пределами этих областей, где, как считается, участвует в модуляции функции NMDA рецептора (Lopez-Corcuera В et al., 2001, Mol. Mem. Biol., 18: 13-20). Таким образом, один метод повышения активности NMDA рецептора состоит в том, чтобы увеличить концентрацию глицина в локальном микроокружении синаптических NMDA рецепторов в ходе ингибирования переносчика GlyT-1 (Bergereon R. Et al., 1998, Proc. Natl. Acad. Sci. USA, 95: 15730-15734; Chen L et al., 2003, J. Neurophysiol., 89 (2): 691-703).
Ингибиторы переносчиков глицина подходят для лечения неврологических и психоневрологических заболеваний. Большинство подразумеваемых болезненных состояний представляет собой психоз, шизофрению (Armer RE and Miller DJ, 2001, Exp. Opin. Ther. Patents, 11 (4): 563-572), психотические расстройства настроения, такие как тяжелое большое депрессивное расстройство, расстройства настроения, связанные с психотическими расстройствами, такими как острый маниакальный синдром или депрессия, связанная с биполярными расстройствами, и расстройства настроения, связанные с шизофренией (Pralong ET et al., 2002, Prog. Neurobiol., 67: 173-202), аутистические заболевания (Carlsson ML, 1998, J. Neural Transm. 105: 525-535), когнитивные расстройства, такие как слабоумие, включая возрастное слабоумие и старческое слабоумие по типу Альцгеймера, нарушения памяти у млекопитающих, включая человека, синдромы дефицита внимания и боль (Armer RE and Miller DJ, 2001, Exp. Opin. Ther. Patents, 11 (4): 563-572).
Таким образом, увеличенная активация NMDA рецепторов посредством ингибирования GlyT-1 может приводить к агентам, которые лечат психоз, шизофрению, слабоумие и другие заболевания, при которых нарушены когнитивные процессы, такие как синдромы дефицита внимания или болезнь Альцгеймера.
Предметами настоящего изобретения являются соединения формулы I как таковые, применение соединений формулы I и их фрамацевтически приемлемых солей для изготовления лекарств для лечения заболеваний, относящихся к активации NMDA рецепторов посредством ингибирования GlyT-1, их изготовление, лекарства, основанные на соединении согласно этому изобретению, и их производство, а также применение соединений формулы I для лечения или предотвращения болезней, таких как психоз, дисфункция памяти и обучения, шизофрения, слабоумие и другие заболевания, при которых нарушены когнитивные процессы, такие как синдромы дефицита внимания или болезнь Альцгеймера.
Предпочтительными показаниями применения соединений настоящего изобретения являются шизофрения, когнитивное нарушение и болезнь Альцгеймера.
Кроме того, изобретение включает все рацемические смеси, все их соответствующие энантиомеры и/или оптические изомеры.
Используемый здесь термин «низший алкил» означает насыщенную неразветвленную или разветвленную группу, содержащую от 1 до 7 атомов углерода, например метил, этил, пропил, изо-пропил, н-бутил, изо-бутил, 2-бутил, трет-бутил и т.п. Предпочтительными алкильными группами являются группы с 1-4 атомами углерода.
Используемый здесь термин «низший алкокси» означает насыщенную неразветвленную или разветвленную группу, содержащую от 1 до 7 атомов углерода, как определено выше, и которая присоединяется через атом кислорода.
Используемый здесь термин «циклоалкил» означает насыщенное углеродное кольцо, содержащее от 3 до 7 атомов углерода, например циклопропил, циклопентил или циклогексил.
Используемый здесь термин «неароматический гетероцикл» означает пяти- или шестичленное гетероциклическое кольцо, содержащее один или два гетероатома, выбранных из группы, состоящей из О, N или S. Предпочтительными кольцами являются 1-пирролидин, 1-пиперидин, 1-пиперазин или 1-морфолин.
Термин «галоген» означает хлор, йод, фтор и бром.
Используемый здесь термин «низший алкил, замещенный галогеном» означает алкильную группу, как определено выше, где по меньшей мере один атом водорода замещен галогеном, например CF3, CHF2, CH2F, CH2CF3 и т.п.
Термин «фармацевтически приемлемые кислотно-аддитивные соли» включает соли с неорганическими и органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п.
Наиболее предпочтительными соединениями формулы I являются соединения формул IA и IB.
Предпочтительными соединениями формулы IA являются следующие:
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-морфолин-4-ил-5-нитро-фенил)-метанон,
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
(4-бензоксазол-2-ил-пиперазин-1-ил)-(2-циклопентилокси-5-метансульфонил-фенил)-метанон,
(4-бензоксазол-2-ил-пиперазин-1-ил)-(2-изобутокси-5-метансульфонил-фенил)-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(6-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(6-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(4-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(4-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
[4-(4-гидрокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(5-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(6-этокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-циклопропилметокси-5-метансульфонил-фенил)-метанон или
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанон.
Предпочтительные соединения формулы IB представляют собой
(2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-2-ил-пиперазин-1-ил)-метанон,
[4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-циклопентилокси-5-метансульфонил-фенил)-метанон,
(2-изобутокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-изопропокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-циклопентилокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанон или
(2-циклопентилокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанон.
Предпочтительным соединением формулы IБ является
(2-изобутокси-5-метансульфонил-фенил)-[4-(2-метил-бензотиазол-5-ил)-пиперазин-1-ил]-метанон.
Предпочтительные соединения формулы IГ представляют собой
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-изопропокси-5-метансульфонил-фенил)-метанон,
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-циклопропилметокси-5-метансульфонил-фенил)-метанон или
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанон.
Данные соединения формулы I и их фармацевтически приемлемые соли можно получить известными из предшествующего уровня техники методами, например описанными ниже способами, при которых
а) соединение формулы
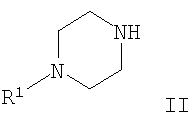
подвергают взаимодействию с соединением формулы

в присутствии активирующего агента, такого как TBTU,
с получением соединения формулы
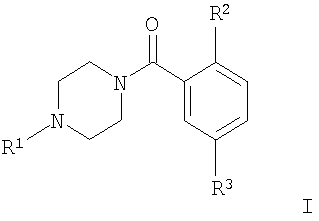
где заместители являются такими, как определено выше, или
б) соединение формулы

подвергают взаимодействию с соединением формулы

в присутствии основания, подобного карбонату калия, или при добавлении катализатора, подобного Cu(I)I
с получением соединения формулы
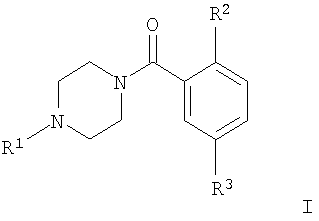
где заместители R1, R2 и R3 являются такими, как определено выше, и Х представляет собой галоген, или
в) соединение формулы
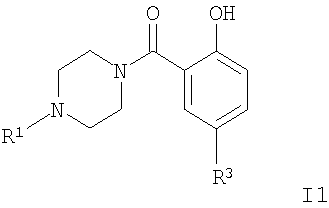
подвергают взаимодействию с соединением формулы

с получением соединения формулы
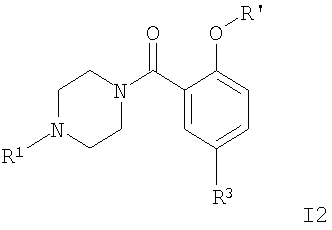
где заместители R1 и R3 являются такими, как определено выше, и R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n- циклоалкил, и Х представляет собой галоген, или
г) соединение формулы

подвергают взаимодействию с соединением формулы

при условиях реакции Мицунобу
с получением соединения формулы

где заместители R1 и R3 являются такими, как определено выше, и R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n- циклоалкил, и
при желании переводят полученные соединения в фармацевтически приемлемые кислотно-аддитивные соли.
Соединения формулы I можно получить согласно вариантам способов а), б), в) или г) и по следующим схемам 1, 2, 3 и 4. Все исходные вещества являются или коммерчески доступными, описанными в литературе, или их можно получить хорошо известными из предшествующего уровня техники способами.
Следующее сокращение используется:
TBTU = (2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилуронийтетрафторборат)
Схема 1
Получение соединений формул II и I:

где R1, R2 и R3 являются такими, как описано выше, R12 представляет собой водород или защитную группу, такую как трет-бутилоксикарбонил или бензилоксикарбонил, и Х представляет собой галоген, мезилат или трифлат.
Когда Х является активированной уходящей группой (например, в орто-положении к атому азота), соединения формулы Х получают, нагревая соединение формулы VIII в присутствии соединения формулы IX и основания, подобного карбонату калия или натрия, в подходящем растворителе, таком как спирт, ацетон или ацетонитрил.
Когда Х является неактивированной уходящей группой, соединения Х получают известными реакциями сочетания, катализируемыми Pd или Cu, между соединениями формул VIII и IX (см. пример S.L.Buchwald еа., Org. Lett. 4, 581 (2002) или J.F.Hartwig ea., JOC 67, 6479 (2002)).
Когда R12 является защитной группой, снятие защитной группы известными из предшествующего уровня техники способами дает соединения формулы II. Затем соединение формулы II обрабатывают соединением формулы III в присутствии TBTU и основания, такого как N-этилдиизопропиламин, с получением соединения формулы I.
Схема 2
Получение соединений формулы III:

где R2 и R3 являются такими, как описано выше, и гал означает галоген.
Соединения формулы III можно получить обычным способом. Если H-R2 является неароматическим гетероциклом, например морфолином, реакцию проводят при комнатной температуре в течение приблизительно 2 часов.
Если R2 является OR', где R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(CH2)n-циклоалкил, реакцию проводят с соответствующим спиртом формулы V по реакции со смесью соединения формулы XI и Cu(I)Br в триэтиламине.
Схема 3
Получение соединений формулы I:

где R1, R2 и R3 являются такими, как описано выше, и Х представляет собой галоген.
Х можно заменить R2 обычным способом в присутствии основания, такого как триэтиламин, или при добавлении катализатора, подобного Cu(I)Br.
Схема 4
Получение соединений формулы I2:

где R', R1 и R3 являются такими, как описано выше, и Х представляет собой галоген.
Кислотно-аддитивные соли основных соединений формулы I можно превратить в соответствующие свободные основания при обработке по меньшей мере стехиометрическим эквивалентом подходящего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и т.п.
Соединения формулы I и их фармацевтически приемлемые соли присоединения обладают ценными фармакологическими свойствами. А именно, было установлено, что соединения настоящего изобретения представляют собой хорошие ингибиторы переносчика глицина I (GlyT-1).
Соединения исследовали согласно тесту, приведенному далее.
Растворы и материалы
Полная среда DMEM: питательная смесь F-12 (Gibco life technologies), эмбриональная телячья сыворотка (FBS) 5% (Gibco life technologies), пенициллин/стрептомицин 1% (Gibco life technologies), гигромицин 0,6 мг/мл (Gibco life technologies), глутамин 1 мМ (Gibco life technologies).
Буфер поглощения (БП): 150 мМ NaCl, 10 мМ Hepes-Tris, pH 7,4, 1 мМ CaCl2, 2,5 мМ KCl, 2,5 мМ MgSO4, 10 мМ (+) D-глюкоза.
Клетки Flp-in™-CHO (Invitrogen, Кат №R758-07), стабильно трансфицированные кДНК mGlyT1b.
Анализ ингибирования поглощения глицина (mGlyT-1b)
В первый день клетки млекопитающих (Flp-in™-CHO), трансфицированные mGlyT-1b кДНК, высевали при плотности 40000 клеток/лунка в полной среде F-12 без гигромицина на 96-луночных культуральных планшетах. На второй день среду отсасывали и клетки дважды промывали буфером поглощения (БП). Затем клетки инкубировали в течение 20 минут при 22°С (i) в отсутствие потенциального конкурента, (ii) с 10 мМ нерадиоактивного глицина, (iii) с некоторой концентрацией потенциального ингибитора. Использовали диапазон концентраций потенциального ингибитора, чтобы сформировать данные для вычисления концентрации ингибитора, приводящей к 50% эффекту (например, ИК50, концентрации конкурента, ингибирующей поглощение глицина на 50%). Затем непосредственно добавляли раствор, содержащий 60 нМ (11-16 Ки/ммоль) [3H]-глицина и 25 мкМ нерадиоактивного глицина. Планшеты инкубировали при слабом встряхивании и реакцию останавливали отсасыванием смеси и промыванием (три раза) с ледяным БП. Клетки подвергали лизису со сцинтилляционной жидкостью, встряхивали 3 часа и радиоактивность в клетках подсчитывали, используя сцинтилляционный счетчик.
Предпочтительные соединения показывают ИК50(мкМ) при GlyT-1<0,5.
Соединения формулы I и фармацевтически приемлемые соли соединений формулы I можно использовать в качестве лекарств, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить перорально, например, в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным также может быть ректальное введение, например в форме суппозиториев, или парентеральное, например в форме растворов для инъекций.
Соединения формулы I можно переработать с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических препаратов. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. можно использовать, например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Однако в зависимости от природы активного вещества для мягких желатиновых капсул носители обычно не требуются. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, глицерин, растительные масла и т.п. Подходящими носителями для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, ароматизаторы, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Также они могут содержать другие терапевтически ценные вещества.
Лекарства, содержащие соединение формулы 1 или его фармацевтически приемлемую соль и терапевтически инертный носитель, также являются предметом настоящего изобретения, как и способ их изготовления, при котором одно или более соединений формулы 1 и/или фармацевтически приемлемых кислотно-аддитивных солей и, если требуется, одно или более других терапевтически ценных веществ превращают в галеновою лекарственную форму вместе с одним или более терапевтически инертным носителем.
Наиболее предпочтительными показаниями согласно настоящему изобретению являются те, которые включают заболевания центральной нервной системы, например лечение или предотвращение шизофрении, когнитивного нарушения и болезни Альцгеймера.
Дозировка может варьировать в широких пределах и, конечно, должна быть подобрана по индивидуальным потребностям в каждом конкретном случае. В случае перорального введения дозировка для взрослых может варьировать от приблизительно 0,01 мг до приблизительно 1000 мг в день соединения общей формулы I или соответствующего количества его фармацевтически приемлемой соли. Суточную дозировку можно вводить в виде однократной дозы или разделенными дозами, и, кроме того, верхний предел можно превысить, когда установлено, что это необходимо.
Процедура изготовления
1. Смешивают 1, 2, 3 и 4 и гранулируют с очищенной водой.
2. Высушивают гранулы при 50°С.
3. Пропускают гранулы через подходящее помольное оборудование.
4. Добавляют 5 и перемешивают в течение трех минут; прессуют под соответствующим прессом.
Процедура изготовления
1. Смешивают 1, 2 и 3 в подходящей мешалке в течение 30 минут.
2. Добавляют 4 и 5 и перемешивают в течение 3 минут.
3. Заполняют подходящую капсулу.
Следующие примеры иллюстрируют настоящее изобретение, не ограничивая его. Все температуры приведены в градусах Цельсия.
Все исходные вещества являются или коммерчески доступными, описанными в литературе (приведены СА номера), или их можно получить хорошо известными из предшествующего уровня техники способами.
Пример 1.1
Получение [4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-морфолин-4-ил-5-нитро-фенил)-метанона
а) 6-Хлор-2-пиперазин-1-ил-бензотиазол
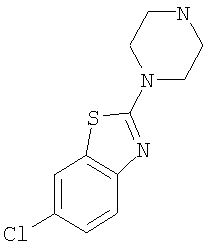
Смесь 10 ммоль 2,6-дихлорбензотиазола, 12,3 ммоль пиперазина и 20 ммоль карбоната калия в 50 мл ацетонитрила нагревали с обратным холодильником в течение 3 часов. Реакционную смесь концентрировали и обрабатывали 25 мл воды. Экстракция этилацетатом, сушка над сульфатом магния и выпаривание растворителя давали указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 254,7 (MH+).
б) [4-(6-Хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-морфолин-4-ил-5-нитро-фенил)-метанон

К раствору 0,25 ммоль 2-морфолин-4-ил-5-нитро-бензойной кислоты (пример 2.1) в 0,7 мл диметилформамида последовательно добавляли 0,26 ммоль TBTU, 1,6 ммоль N-этилдиизопропиламина и 0,25 ммоль 6-хлор-2-пиперазин-1-ил-бензотиазола. Реакционную смесь затем перемешивали при комнатной температуре в течение двух часов, концентрировали в вакууме и обрабатывали 5 мл воды. Твердое вещество отфильтровывали и перекристаллизовывали из метанола с получением указанного в заголовке соединения в виде желтого твердого вещества. MS (m/e): 488,1 (M+H+).
Пример 1.2
Получение [4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и 6-хлор-2-пиперазин-1-ил-бензотиазола. Неочищенный материал очищали с помощью хроматографии (SiO2, CH2Cl2/МеОН = 95/5) с получением указанного в заголовке соединения в виде желтоватого твердого вещества. MS (m/e): 552,3 (М+СН3СООН+).
Пример 1.3
Получение (4-бензоксазол-2-ил-пиперазин-1-ил)-(2-изопропокси-5-метансульфонил-фенил)-метанона
а) Трет-бутиловый эфир 4-бензоксазол-2-ил-пиперазин-1-карбоновой кислоты
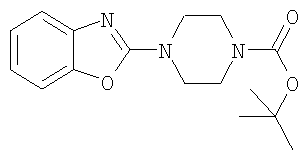
Смесь 52,5 ммоль 2-хлорбензоксазола, 53,6 ммоль трет-бутилового эфира пиперазин-1-карбоновой кислоты и 63 ммоль карбоната калия в 60 мл ацетонитрила нагревали с обратным холодильником в течение 16 часов. Реакционную смесь концентрировали, разбавляли водой и экстрагировали этилацетатом. Органическую фазу высушивали и концентрировали с получением указанного в заголовке соединения в виде бледно-оранжевого твердого вещества. MS (m/e): 304,2 (M+H+).
б) Гидрохлорид 2-пиперазин-1-ил-бензоксазола
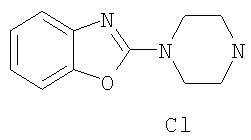
10,8 ммоль трет-бутилового эфира 4-бензоксазол-2-ил-пиперазин-1-карбоновой кислоты обрабатывали 30 мл диоксана, насыщенного газообразной соляной кислотой. Гетерогенную смесь перемешивали при комнатной температуре в течение 1 часа перед выпариванием растворителя. Получали указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 204,1 (M+H+).
в) (4-Бензоксазол-2-ил-пиперазин-1-ил)-(2-изопропокси-5-метансульфонил-фенил)-метанон

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида 2-пиперазин-1-ил-бензоксазола. Неочищенный материал растирали с диэтиловым эфиром с получением указанного в заголовке соединения в виде бесцветного твердого вещества. MS (m/e): 444,1 (M+H+).
Пример 1.4
Получение (4-бензоксазол-2-ил-пиперазин-1-ил)-(2-циклопентилокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-циклопентилокси-5-метансульфонил-бензойной кислоты (пример 2.3) и гидрохлорида 2-пиперазин-1-ил-бензоксазола. Неочищенный материал очищали с помощью хроматографии (SiO2, этилацетат) с получением указанного в заголовке соединения в виде бесцветного твердого вещества. MS (m/e): 470,1 (М+Н+).
Пример 1.5
Получение (4-бензоксазол-2-ил-пиперазин-1-ил)-(2-изобутокси-5-метансульфонил-фенил)-метанона
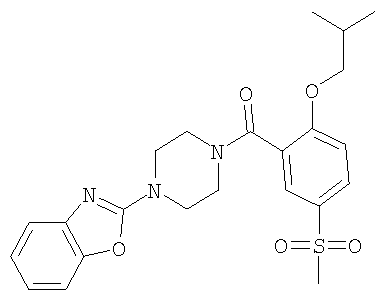
Получали по аналогии с примером 1.1 б) из 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) и гидрохлорида 2-пиперазин-1-ил-бензоксазола. Неочищенный материал очищали с помощью хроматографии (SiO2, этилацетат) с получением указанного в заголовке соединения в виде бледно-желтого твердого вещества. MS (m/e): 458,1 (M+H+).
Пример 1.6
Получение (2-циклопентилокси-5-метансульфонил-фенил)-[4-(5-этансульфонил-бензоксазол-2-ил)-пиперазин-1-ил]-метанона
а) 5-Этансульфонил-бензоксазол-2-тиол
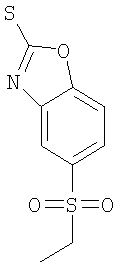
100 ммоль 1-амино-5-этилсульфонил-2-гидроксибензола растворяли в 200 мл этанола и 150 мл сероуглерода. Добавляли 120 ммоль гидроксида калия и смесь нагревали с обратным холодильником в течение ночи. Растворитель выпаривали, остаток обрабатывали 1 М соляной кислотой, экстрагировали этилацетатом и высушивали. Выпаривание давало неочищенный продукт, который перекристаллизовывали из этилацетата с получением указанного в заголовке соединения в виде желтоватого твердого вещества. MS (m/e): 242,4 (М-Н).
б) 2-Хлор-5-этансульфонил-бензоксазол

8 ммоль 5-этансульфонил-бензоксазол-2-тиола растворяли в 10 мл тионилхлорида. Добавляли 1 каплю N,N-диметилформамида и реакционную смесь держали при 65°С в течение 45 минут. Выпаривание растворителя давало указанное в заголовке соединение в виде коричневатого твердого вещества. MS (m/e): 262,9 (M+NH4 +).
в) Трет-бутиловый эфир 4-(5-этансульфонил-бензоксазол-2-ил)-пиперазин-1-карбоновой кислоты

Смесь 8,1 ммоль 2-хлор-5-этансульфонил-бензоксазола, 8,3 ммоль трет-бутилового эфира пиперазин-1-карбоновой кислоты и 9,8 ммоль карбоната калия в 20 мл ацетонитрила нагревали с обратным холодильником в течение 16 часов. Реакционную смесь охлаждали, концентрировали в вакууме и обрабатывали 50 мл воды. Экстракция этилацетатом и перекристаллизация из концентрированного раствора этилацетата давали указанное в заголовке соединение в виде коричневатого твердого вещества. MS (m/e): 454,4 (М+СН3СОО).
г) Гидрохлорид 5-этансульфонил-2-пиперазин-1-ил-бензоксазола
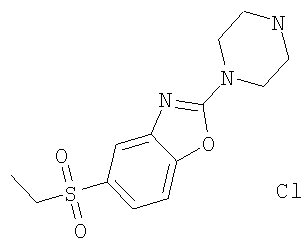
10,8 ммоль трет-бутилового эфира 4-(5-этансульфонил-бензоксазол-2-ил)-пиперазин-1-карбоновой кислоты обрабатывали 256 мл диоксана, насыщенного газообразной соляной кислотой. Гетерогенную смесь перемешивали всю ночь при комнатной температуре. Выпаривание растворителя давало указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 296,4 (M+H+).
д) (2-Циклопентилокси-5-метансульфонил-фенил)-[4-(5-этансульфонил-бензоксазол-2-ил)-пиперазин-1-ил]-метанон

Получали по аналогии с примером 1.1 б) из 2-циклопентилокси-5-метансульфонил-бензойной кислоты (пример 2.3) и гидрохлорида 5-этансульфонил-2-пиперазин-1-ил-бензоксазола. Неочищенный материал очищали с помощью хроматографии (SiO2, этилацетат) с получением указанного в заголовке соединения в виде бесцветного твердого вещества. MS (m/e): 562,3 (M+H+).
Пример 1.7
Получение [4-(5-этансульфонил-бензоксазол-2-ил)-пиперазин-1-ил]-(2-изобутокси-5-метансульфонил-фенил)-метанона
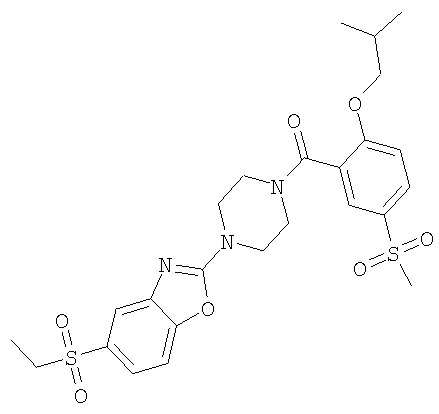
Получали по аналогии с примером 1.1 б) из 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) и гидрохлорида 5-этансульфонил-2-пиперазин-1-ил-бензоксазола. Неочищенный материал очищали с помощью хроматографии (SiO2, этилацетат) с получением указанного в заголовке соединения в виде бесцветного твердого вещества. MS (m/e): 550,2 (М+Н+).
Пример 1.8
Получение (2-изопропокси-5-метансульфонил-фенил)-[4-(6-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанона
а) 6-Метокси-2-пиперазин-1-ил-бензотиазол
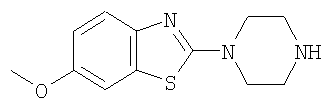
Смесь 1,50 ммоль 2-хлор-6-метоксибензотиазола (СА=[2605-14-3]), 4,51 ммоль пиперазина и 4,51 ммоль триэтиламина в 5 мл тетрагидрофурана в закрытом сосуде нагревали при 160°С в течение 5 минут в условиях микроволнового излучения. Реакционную смесь концентрировали и остаток очищали с помощью хроматографии (SiO2, метанол/дихлорметан) с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 250,3 (M+H+).
б) (2-Изопропокси-5-метансульфонил-фенил)-[4-(6-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанон

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и 6-метокси-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) с получением указанного в заголовке соединения в виде белой пены. MS (m/e): 490,3 (M+H+).
Пример 1.9
Получение (2-изопропокси-5-метансульфонил-фенил)-[4-(6-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанона
а) 6-Нитро-2-пиперазин-1-ил-бензотиазол

Смесь 1,40 ммоль 2-хлор-6-нитробензотиазола (СА=[2407-11-6]), 4,19 ммоль пиперазина и 4,19 ммоль триэтиламина в 5 мл тетрагидрофурана в закрытом сосуде нагревали при 160°С в течение 10 минут в условиях микроволнового излучения. Реакционную смесь концентрировали и остаток очищали с помощью хроматографии (SiO2, метанол/дихлорметан) с получением указанного в заголовке соединения в виде желтого твердого вещества. MS (m/e): 264,9 (M+H+).
б) (2-Изопропокси-5-метансульфонил-фенил)-[4-(6-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанон

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и 6-нитро-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде желтого твердого вещества. MS (m/e): 505,3 (M+H+).
Пример 1.10
Получение метилового эфира (2-[4-(2-изопропокси-5-метансульфонил-бензоил)-пиперазин-1-ил]-бензотиазол-4-карбоновой кислоты

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида метилового эфира 2-пиперазин-1-ил-бензотиазол-4-карбоновой кислоты в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 518,5 (М+Н+).
Пример 1.11
Получение (2-изопропокси-5-метансульфонил-фенил)-[4-(4-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанона

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида 4-метокси-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 490,5 (M+H+).
Пример 1.12
Получение (2-изопропокси-5-метансульфонил-фенил)-[4-(4-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанона
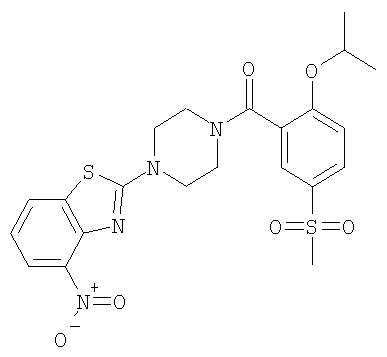
Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида 4-нитро-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 505,3 (М+Н+).
Пример 1.13
Получение [4-(4-гидрокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида 2-пиперазин-1-ил-бензотиазол-4-ола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 476,0 (М+Н+).
Пример 1.14
Получение [4-(5-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанона
а) 5-Хлор-2-пиперазин-1-ил-бензотиазол

Смесь 0,49 ммоль 2,5-дихлорбензотиазола (СА=[2941-48-2]), 1,47 ммоль пиперазина и 1,47 ммоль триэтиламина в 5 мл тетрагидрофурана в закрытом сосуде нагревали при 160°С в течение 5 минут в условиях микроволнового излучения. Реакционную смесь концентрировали и остаток очищали с помощью хроматографии (SiO2, метанол/дихлорметан) с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 254,1 ({35Cl}M+H+), 256,2 ({37Cl}M+H+).
б) [4-(5-Хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и 5-хлор-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 494,3
({35Cl}М+Н+), 496,2 ({37Cl}М+Н+).
Пример 1.15
Получение [4-(6-этокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанона
а) 6-Этокси-2-пиперазин-1-ил-бензотиазол
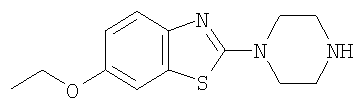
Смесь 1,36 ммоль 2-хлор-6-этокси-бензотиазола (СА=[79071-17-3]), 3,00 ммоль пиперазина и 3,00 ммоль триэтиламина в 5 мл тетрагидрофурана в закрытом сосуде нагревали при 160°С в течение 5 минут в условиях микроволнового излучения. Реакционную смесь концентрировали и остаток очищали с помощью хроматографии (SiO2, метанол/дихлорметан) с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 264,3 (M+H+).
б) [4-(6-Этокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и 6-Этокси-2-пиперазин-1-ил-бензотиазола в тетрагидрофуране. Неочищенный материал очищали с помощью хроматографии (SiO2, гептан/этилацетат) и затем остаток растирали в эфире с получением указанного в заголовке соединения в виде белого твердого вещества. MS (m/e): 504,1 (М+Н+).
Пример 1.16
Получение (2-изопропокси-5-метансульфонил-фенил)-[4-(2-метил-бензотиазол-5-ил)-пиперазин-1-ил]-метанона
а) Трет-бутиловый эфир 4-(2-метил-бензотиазол-5-ил)-пиперазин-1-карбоновой кислоты

К смеси 1,3 ммоль 5-бром-2-метилбензотиазола, 1,4 ммоль пиперазин-1-карбоновой кислоты, 2,0 ммоль гидроксида калия, 0,01 ммоль бис(три-трет-бутилфосфин)палладия и 0,01 ммоль цетилтриметиламмоний бромида в 1 мл толуола добавляли 1 каплю воды. Реакционную смесь нагревали всю ночь в атмосфере аргона при 90°С. Добавление воды и экстракция этилацетатом давали коричневатое масло, которое очищали с помощью хроматографии (SiO2, циклогексан/этилацетат, 7:3) с получением указанного в заголовке соединения в виде желтоватого твердого вещества. MS (m/e): 334,4 (M+H+).
б) Гидрохлорид 2-метил-5-пиперазин-1-ил-бензотиазола
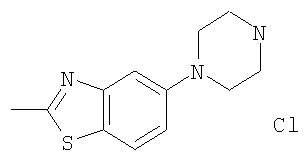
Получали по аналогии с примером 1.6 г) из трет-бутилового эфира 4-(2-метил-бензотиазол-5-ил)-пиперазин-1-карбоновой кислоты и диоксана, насыщенного газообразной соляной кислотой. MS (m/e): 234,1 (М+Н+).
в) (2-Изопропокси-5-метансульфонил-фенил)-[4-(2-метил-бензотиазол-5-ил)-пиперазин-1-ил]-метанон
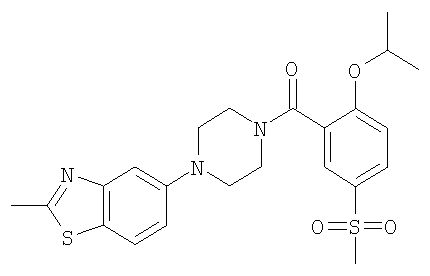
Получали по аналогии с примером 1.1 б) из гидрохлорида 2-метил-5-пиперазин-1-ил-бензотиазола и 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) в ацетонитриле. Растирание в диэтиловом эфире давало указанное в заголовке соединение в виде желтоватого твердого вещества. MS (m/e): 474,1 (M+H+).
Пример 1.17
Получение (2-изобутокси-5-метансульфонил-фенил)-[4-(2-метил-бензотиазол-5-ил)-пиперазин-1-ил]-метанона
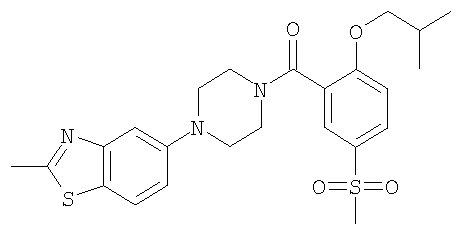
Получали по аналогии с примером 1.1 б) из гидрохлорида 2-метил-5-пиперазин-1-ил-бензотиазола и 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде коричневатого твердого вещества. MS (m/e): 488,4 (M+H+).
Пример 1.18
Получение (2-изопропокси-5-метансульфонил-фенил)-(4-хинолин-2-ил-пиперазин-1-ил)-метанона
а) Трет-бутиловый эфир 4-хинолин-2-ил-пиперазин-1-карбоновой кислоты

Смесь 6,1 ммоль 2-хлорхинолина, 6,7 ммоль трет-бутилового эфира пиперазин-1-карбоновой кислоты и 12,2 ммоль карбоната калия в 15 мл ацетонитрила нагревали с обратным холодильником всю ночь. Реакционную смесь концентрировали, добавляли воду и соединение экстрагировали этилацетатом. Хроматография (SiO2, циклогексан/этилацетат, 9/1) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 314,3 (M+H+).
б) Гидрохлорид 2-пиперазин-1-ил-хинолина
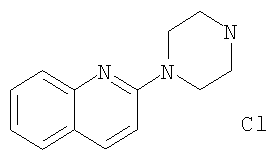
Получали по аналогии с примером 1.6 г) из трет-бутилового эфира 4-хинолин-2-ил-пиперазин-1-карбоновой кислоты и диоксана, насыщенного газообразной соляной кислотой. MS (m/e): 214,4 (M+H+).
в) (2-Изопропокси-5-метансульфонил-фенил)-(4-хинолин-2-ил-пиперазин-1-ил)-метанон
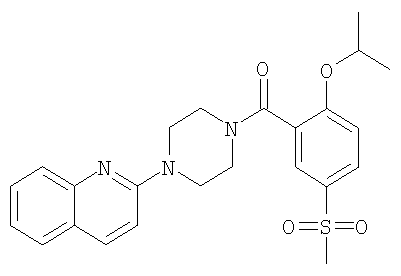
Получали по аналогии с примером 1.1 б) из гидрохлорида 2-пиперазин-1-ил-хинолина и 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) в ацетонитриле. Растирание в диэтиловом эфире давало указанное в заголовке соединение в виде желтоватой пены. MS (m/e): 454,4 (М+Н+).
Пример 1.19
Получение (2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-2-ил-пиперазин-1-ил)-метанона
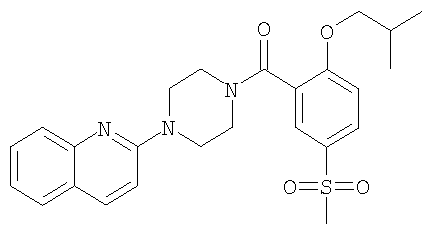
Получали по аналогии с примером 1.1 б) из гидрохлорида 2-пиперазин-1-ил-хинолина и 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде желтоватого твердого вещества. MS (m/e): 468,4 (M+H+).
Пример 1.20
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанона
а) Трет-бутиловый эфир 4-(6-хлор-хинолин-2-ил)-пиперазин-1-карбоновой кислоты
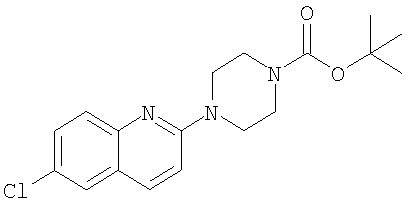
Получали по аналогии с примером 1.18 а) из 2,6-дихлорхинолина и трет-бутилового эфира пиперазин-1-карбоновой кислоты. Кристаллизация из метанола давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 348,5 (М+Н+).
б) Гидрохлорид 6-хлор-2-пиперазин-1-ил-хинолина
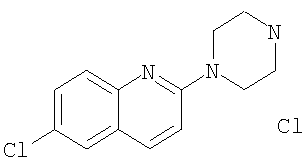
Получали по аналогии с примером 1.6 г) из трет-бутилового эфира 4-(6-хлор-хинолин-2-ил)-пиперазин-1-карбоновой кислоты и диоксана, насыщенного газообразной соляной кислотой. MS (m/e): 248,1 (M+H+).
в) [4-(6-Хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон

Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина и 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде желтоватой пены. MS (m/e): 488,1 (M+H+).
Пример 1.21
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-изобутокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина и 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 503,1 (М+H+).
Пример 1.22
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-циклопентилокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина и 2-циклопентилокси-5-метансульфонил-бензойной кислоты (пример 2.3) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 515,1 (M+H+).
Пример 1.23
Получение (2-изобутокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанона
а) Трет-бутиловый эфир 4-хиноксалин-2-ил-пиперазин-1-карбоновой кислоты
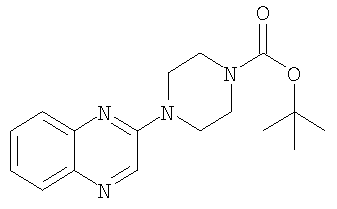
Смесь 9,1 ммоль 2-хлорхиноксалина, 10,0 ммоль трет-бутилового эфира пиперазин-1-карбоновой кислоты, 22,8 ммоль карбоната калия и 2,1 ммоль иодида калия в 20 мл толуола нагревали с обратным холодильником всю ночь. Реакционную смесь охлаждали, наливали воду и экстрагировали 3 раза этилацетатом. Органическую фазу высушивали, выпаривали, и указанное в заголовке соединение кристаллизовалось из метанола. Желтоватое твердое вещество. MS (m/e): 315,0 (M+H+).
б) Гидрохлорид 2-пиперазин-1-ил-хиноксалина
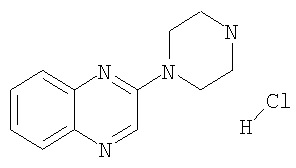
Получали по аналогии с примером 1.6 г) из трет-бутилового эфира 4-хиноксалин-2-ил-пиперазин-1-карбоновой кислоты и диоксана, насыщенного газообразной соляной кислотой. MS (m/e): 215,4 (М+Н+).
в) (2-Изобутокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон

Получали по аналогии с примером 1.1 б) из гидрохлорида 2-пиперазин-1-ил-хиноксалина и 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде желтоватой пены. MS (m/e): 527,3 (М+СН3СОО).
Пример 1.24
Получение (2-изопропокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 2-пиперазин-1-ил-хиноксалина и 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде желтоватой пены. MS (m/e): 455,5 (М+H+).
Пример 1.25
Получение (2-циклопентилокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 2-пиперазин-1-ил-хиноксалина и 2-циклопентилокси-5-метансульфонил-бензойной кислоты (пример 2.3) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде желтоватой пены. MS (m/e): 481,5 (M+H+).
Пример 1.26
Получение (2-изопропокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанона
а) Трет-бутиловый эфир 4-хинолин-3-ил-пиперазин-1-карбоновой кислоты

Получали по аналогии с примером 1.18 а) из 3-бромхинолина и трет-бутилового эфира пиперазин-1-карбоновой кислоты. Хроматография (SiO2, циклогексан/этилацетат, 1/1) после кристаллизации из диэтилового эфира/циклогексана давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 314,2 (M+H+).
б) Гидрохлорид 3-пиперазин-1-ил-хинолина
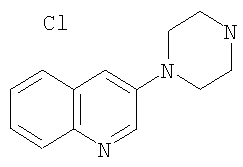
Получали по аналогии с примером 1.6 г) из трет-бутилового эфира 4-хинолин-3-ил-пиперазин-1-карбоновой кислоты и диоксана, насыщенного газообразной соляной кислотой. Желтое твердое вещество. MS (m/e): 214,4 (М+H+).
в) (2-Изопропокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанон

Получали по аналогии с примером 1.1 б) из гидрохлорида 3-пиперазин-1-ил-хинолина и 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветной пены. MS (m/e): 454,5 (М+Н+).
Пример 1.27
Получение (2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанона
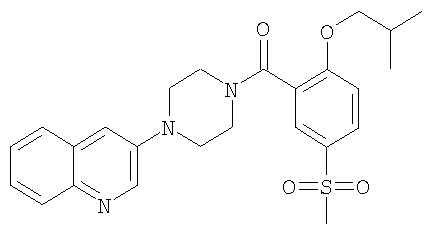
Получали по аналогии с примером 1.1 б) из гидрохлорида 3-пиперазин-1-ил-хинолина и 2-изобутокси-5-метансульфонил-бензойной кислоты (пример 2.4) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 468,3 (М+Н+).
Пример 1.28
Получение (2-циклопентилокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 3-пиперазин-1-ил-хинолина и 2-циклопентилокси-5-метансульфонил-бензойной кислоты (пример 2.3) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 480,3 (M+H+).
Пример 1.29
Получение (4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-изопропокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-изопропокси-5-метансульфонил-бензойной кислоты (пример 2.2) и гидрохлорида 3-пиперазин-1-ил-бензо[d]изотиазола (СА=87691-88-1) в диметилформамиде. Неочищенный материал очищали с помощью ВЭЖХ (Zorbax XDB, обращенная фаза, вода/ацетонитрил) с получением указанного в заголовке соединения в виде белой пены. MS (m/e): 460,3 (M+H+).
Пример 1.30
Получение (4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-диэтиламино-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-диэтиламино-5-метансульфонил-бензойной кислоты (пример 2.5) и гидрохлорида 3-пиперазин-1-ил-бензо[d]изотиазола (СА=87691-88-1) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 473,4 (M+H+; 100%).
Пример 1.31
Получение (4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-морфолин-4-ил-5-нитро-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-морфолин-4-ил-5-нитро-бензойной кислоты (пример 2.1) и гидрохлорида 3-пиперазин-1-ил-бензо[d]изотиазола (СА=87691-88-1) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 454,2 (M+H+; 100%).
Пример 1.32
Получение (4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-циклопропилметокси-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из 2-циклопропилметокси-5-метансульфонил-бензойной кислоты (пример 2.6) и гидрохлорида 3-пиперазин-1-ил-бензо[d]изотиазола (СА=87691-88-1) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 472,1 (М+H+; 100%).
Пример 1.33
Получение (4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанона

Получали по аналогии с примером 1.1 б) из 5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-бензойной кислоты (пример 2.7) и гидрохлорида 3-пиперазин-1-ил-бензо[d]изотиазола (СА=87691-88-1) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 514,1 (M+H+; 37%).
Пример 1.34
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-диэтиламино-5-метансульфонил-фенил)-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина (пример 1.20б) и 2-диэтиламино-5-метансульфонил-бензойной кислоты (пример 2.5) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 501,4 (M+H+; 100%).
Пример 1.35
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-морфолин-4-ил-5-нитро-фенил)-метанона
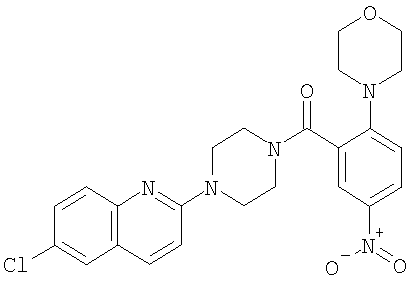
Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина (пример 1.20б) и 2-морфолин-4-ил-5-нитро-бензойной кислоты (пример 2.1) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 482,2 (M+H+; 100%).
Пример 1.36
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанона

Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина (пример 1.20б) и 5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-бензойной кислоты (пример 2.7) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 542,3 (M+H+; 100%).
Пример 1.37
Получение [4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-циклопропилметокси-5-метансульфонил-фенил)-метанона
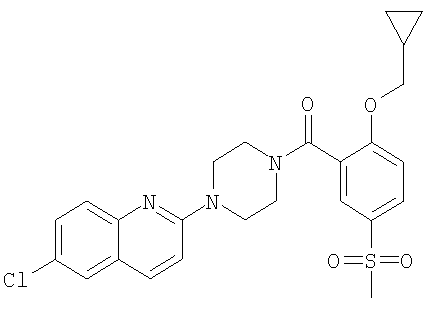
Получали по аналогии с примером 1.1 б) из гидрохлорида 6-хлор-2-пиперазин-1-ил-хинолина (пример 1.20б) и 2-циклопропилметокси-5-метансульфонил-бензойной кислоты (пример 2.6) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 500,3 (M+H+; 100%).
Пример 1.38
Получение [4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-диэтиламино-5-метансульфонил-фенил)-метанона
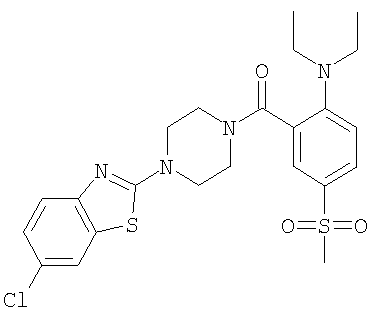
Получали по аналогии с примером 1.1 б) из 5-хлор-2-пиперазин-1-ил-бензотиазола (пример 1.14а) и 2-диэтиламино-5-метансульфонил-бензойной кислоты (пример 2.5) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 507,5 (М+Н+; 100%).
Пример 1.39
Получение [4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-циклопропилметокси-5-метансульфонил-фенил)-метанона
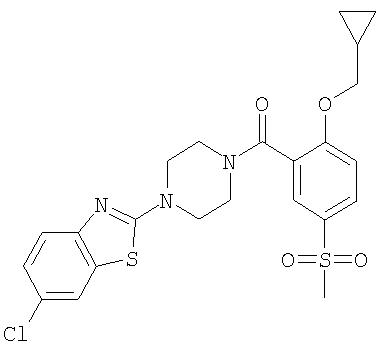
Получали по аналогии с примером 1.1 б) из 5-хлор-2-пиперазин-1-ил-бензотиазола (пример 1.14а) и 2-циклопропилметокси-5-метансульфонил-бензойной кислоты (пример 2.6) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 506,3 (М+H+; 100%).
Пример 1.40
Получение [4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанона
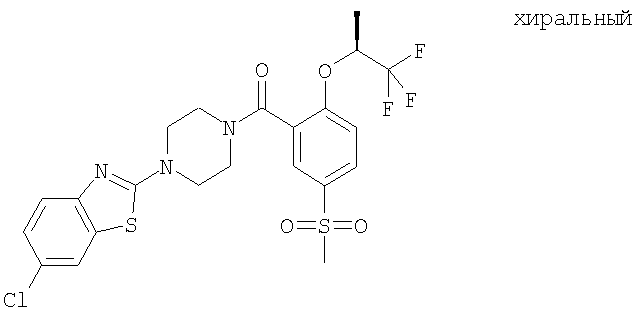
Получали по аналогии с примером 1.1 б) из 5-хлор-2-пиперазин-1-ил-бензотиазола (пример 1.14а) и 5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-бензойной кислоты (пример 2.7) в ацетонитриле. Хроматография (SiO2, этилацетат) давала указанное в заголовке соединение в виде бесцветного твердого вещества. MS (m/e): 548,2 (М+H+; 100%).
Пример 2.1
Получение 2-морфолин-4-ил-5-нитро-бензойной кислоты

К раствору 2-фтор-5-нитробензойной кислоты (4,86 г, 26,2 ммоль) в диоксане (50 мл) добавляли морфолин (11,5 мл). Смесь перемешивали при комнатной температуре в течение 2 часов. Растворитель удаляли в вакууме. Остаток растворяли в воде и смесь подкисляли 2 н. HCl. Твердое вещество фильтровали, промывали водой и высушивали с получением указанного в заголовке соединения (6,2 г, 93%) в виде желтого твердого вещества. MS (m/e): 251,2 (М-Н; 100%).
Пример 2.2 Получение 2-изопропокси-5-метансульфонил-бензойной кислоты
а) 2-Хлор-5-метансульфонил-бензойная кислота

К 99 ммоль 2-хлор-5-(метилтио)бензойной кислоты в 400 мл метанола при 0°С добавляли 296 ммоль Оксона® и смесь перемешивали при комнатной температуре в течение 3,5 часов. Осадок отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток экстрагировали 3 раза 400 мл этилацетата и объединенные органические фазы промывали 2 раза 300 мл 1 н. HCl и 300 мл насыщенного водного раствора NaCl и высушивали с MgSO4. Выпаривание при пониженном давлении давало указанное в заголовке соединение.
б) 2-Изопропокси-5-метансульфонил-бензойная кислота
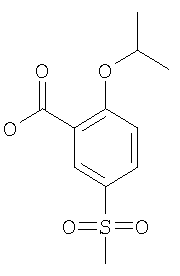
Смесь 2,13 ммоль 2-хлор-5-метансульфонил-бензойной кислоты, 0,64 ммоль Cu(I)Br в 5 мл NEt3 и 25 мл изопропанола нагревали до 120°С в течение 16 часов в закрытом сосуде. Летучие компоненты удаляли в вакууме и остаток помещали в 70 мл 1 н. HCl. Экстракция этилацетатом, сушка объединенных органических фракций и выпаривание давали остаток, который очищали с помощью обращенно-фазовой препаративной ВЭЖХ, элюируя градиентом ацетонитрил/вода. Выпаривание фракций продукта давало указанное в заголовке соединение. MS (m/e): 257,0 (МН-; 100%).
Пример 2.3 Получение 2-циклопентилокси-5-метансульфонил-бензойной кислоты
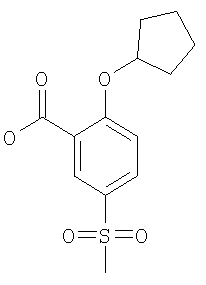
Получали по аналогии с примером 2.2 б) из 2-хлор-5-метансульфонил-бензойной кислоты и циклопентанола. MS (m/e): 282,9 (MH-; 100%).
Пример 2.4 Получение 2-изобутокси-5-метансульфонил-бензойной кислоты
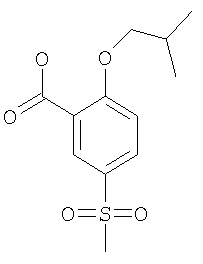
Получали по аналогии с примером 2.2 б) из 2-хлор-5-метансульфонил-бензойной кислоты и изобутанола. MS (m/e): 271,1 (МН-; 100%).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ [4-(ГЕТЕРОАРИЛ)ПИПЕРАЗИН-1-ИЛ]-(2,5-ЗАМЕЩЕННЫЙ ФЕНИЛ)МЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ПЕРЕНОСЧИКА ГЛИЦИНА-1 (GLYT-1) ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ И ПСИХОНЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2005 |
|
RU2396270C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ФЕНИЛМЕТАНОНА | 2007 |
|
RU2437872C2 |
| 4-ФЕНОКСИ-НИКОТИНАМИДЫ ИЛИ 4-ФЕНОКСИ-ПИРИМИДИН-5-КАРБОКСАМИДЫ | 2011 |
|
RU2565077C2 |
| НОВЫЕ ФЕНИЛАМИДНЫЕ ИЛИ ПИРИДИЛАМИДНЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТОВ GPBAR1 | 2009 |
|
RU2533887C2 |
| ПРОИЗВОДНЫЕ (3-МЕТИЛПИРРОЛИДИН-3-ИЛ)-МЕТИЛ ПИРИДИНИЛОВОГО ЭФИРА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ РЕЦЕПТОРА NK-3 | 2011 |
|
RU2625798C2 |
| НОВЫЕ БЕНЗОДИОКСОЛЫ | 2003 |
|
RU2304580C2 |
| ХИНОЛИН В КАЧЕСТВЕ АЛЛОСТЕРИЧЕСКОГО ЭНХАНСЕРА РЕЦЕПТОРОВ ГАМК-В | 2005 |
|
RU2378256C2 |
| МЕЧЕННЫЕ РАДИОАКТИВНОЙ МЕТКОЙ ИНГИБИТОРЫ ПЕРЕНОСЧИКА ГЛИЦИНА 1 | 2009 |
|
RU2512529C2 |
| 1-ГИДРОКСИИМИНО-3-ФЕНИЛ-ПРОПАНЫ | 2011 |
|
RU2579114C9 |
| АМИНОМЕТИЛХИНОЛОНЫ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ JNK-ОПОСРЕДОВАННОГО РАССТРОЙСТВА | 2012 |
|
RU2629111C2 |
Изобретение относится к новым соединениям общей формулы

где R1 представляет собой группу
 или
или 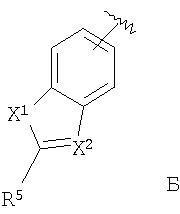 или
или
 или
или 
R2 представляет собой морфолин или представляет собой OR' или N(R'')2; R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n-циклоалкил; R'' представляет собой низший алкил; R3 представляет собой NO2 или SO2R'; R4 представляет собой водород, гидрокси, галоген, NO2, низший алкокси, SO2R' или C(O)OR''; R5/R6/R7 представляют собой водород, галоген, низший алкил; Х1/Х1' представляют собой СН или N при условии, что Х1/Х1' одновременно не являются СН; X2 представляет собой О или S; n представляет собой 0 или 1; и к их фармацевтически активным кислотно-аддитивным солям. Изобретение также относится к лекарству. Технический результат - получение новых биологически активных соединений, обладающих активностью в качестве ингибиторов переносчика глицина 1. 2 н. и 9 з.п. ф-лы, 1 табл.
1. Соединения общей формулы

где R1 представляет собой группу
 или
или 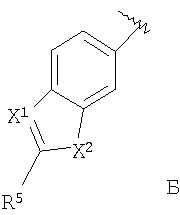 или
или
 или
или  ;
;
или R2 представляет собой морфолин или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2 или SO2R';
R4 представляет собой водород, гидрокси, галоген, NO2, низший алкокси, SO2R' или C(O)OR'';
R5/R6/R7 представляют собой водород, галоген, низший алкил;
X1/Xl' представляют собой СН или N при условии, что X1/X1' одновременно не являются СН;
X2 представляет собой О или S;
n представляет собой 0 или 1;
и фармацевтически активные кислотно-аддитивные соли.
2. Соединение формулы IA по п.1, где R1 представляет собой группу А,

где R2 представляет собой морфолин или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2 или SO2R';
R4 представляет собой водород, гидрокси, галоген, NO2, низший алкокси, SO2R' или C(O)OR'';
X1 представляет собой СН или N;
X2 представляет собой О или S;
n представляет собой 0 или 1;
и фармацевтически активные кислотно-аддитивные соли.
3. Соединение формулы IБ по п.1, где R1 представляет собой группу Б,

где R2 представляет собой морфонил или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(CH2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2 или SO2R';
R5 представляет собой водород, галоген, низший алкил;
X1 представляет собой СН или N;
X2 представляет собой О или S;
n представляет собой 0 или 1;
и фармацевтически активные кислотно-аддитивные соли.
4. Соединение формулы IB по п.1, где R1 представляет собой группу В,

где R2 представляет собой морфолин или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(СН2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2 или SO2R';
R6 представляет собой водород, галоген, низший алкил;
Х1/Х1' представляют собой СН или N при условии, что X1/Х1' одновременно не являются СН;
n представляет собой 0 или 1;
и фармацевтически активные кислотно-аддитивные соли.
5. Соединение формулы IГ по п.1, где R1 представляет собой группу Г,

где R2 представляет собой морфолин или представляет собой OR' или N(R'')2;
R' представляет собой низший алкил, низший алкил, замещенный галогеном, или -(CH2)n-циклоалкил;
R'' представляет собой низший алкил;
R3 представляет собой NO2 или SO2R';
R7 представляет собой водород, галоген, низший алкил;
X1 представляет собой СН или N;
X2 представляет собой О или S;
n представляет собой 0 или 1;
и фармацевтически активные кислотно-аддитивные соли.
6. Соединения формулы IA по п.2, которые представляют собой
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-морфолин-4-ил-5-нитро-фенил)-метанон,
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
(4-бензоксазол-2-ил-пиперазин-1-ил)-(2-циклопентилокси-5-метансульфонил-фенил)-метанон,
(4-бензоксазол-2-ил-пиперазин-1-ил)-(2-изобутокси-5-метансульфонил-фенил)-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(6-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(6-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(4-метокси-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
(2-изопропокси-5-метансульфонил-фенил)-[4-(4-нитро-бензотиазол-2-ил)-пиперазин-1-ил]-метанон,
[4-(4-гидрокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(5-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(6-этокси-бензотиазол-2-ил)-пиперазин-1-ил]-(2-изопропокси-5-метансульфонил-фенил)-метанон,
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-(2-циклопропилметокси-5-метансульфонил-фенил)-метанон или
[4-(6-хлор-бензотиазол-2-ил)-пиперазин-1-ил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанон.
7. Соединения формулы IБ по п.3, одно из которых представляет собой
(2-изобутокси-5-метансульфонил-фенил)-[4-(2-метил-бензотиазол-5-ил)-пиперазин-1-ил]-метанон.
8. Соединения формулы IB по п.4, которые представляют собой
(2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-2-ил-пиперазин-1-ил)-метанон,
[4-(6-хлор-хинолин-2-ил)-пиперазин-1-ил]-(2-циклопентилокси-5-метансульфонил-фенил)-метанон,
(2-изобутокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-изопропокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-циклопентилокси-5-метансульфонил-фенил)-(4-хиноксалин-2-ил-пиперазин-1-ил)-метанон,
(2-изобутокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанон или
(2-циклопентилокси-5-метансульфонил-фенил)-(4-хинолин-3-ил-пиперазин-1-ил)-метанон.
9. Соединения формулы IГ по п.5, которые представляют собой
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-изопропокси-5-метансульфонил-фенил)-метанон,
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-(2-циклопропилметокси-5-метансульфонил-фенил)-метанон или
(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанон.
10. Лекарство, обладающее активностью в качестве ингибиторов переносчика глицина 1, содержащее одно или более соединений по любому из пп.1-9 и фармацевтически приемлемые эксципиенты.
11. Лекарство по п.10 для лечения болезни Альцгеймера.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| НОВЫЕ 4-АРИЛПИПЕРАЗИНЫ И 4-АРИЛПИПЕРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ ДОПАМИН-2-РЕЦЕПТОРОВ | 1992 |
|
RU2139867C1 |
Авторы
Даты
2010-07-27—Публикация
2005-12-01—Подача