Все цитируемые в настоящем описании документы включены в него во всей полноте посредством ссылки.
Область техники изобретения
Настоящее изобретение относится к области анализа и контроля качества вакцин, содержащих бактериальные капсульные сахариды, и, в частности, вакцин, в которых сахариды конъюгированы с носителем.
Предшествующий уровень техники изобретения
Иммуногены, содержащие капсульные сахаридные антигены, конъюгированные с белками-носителями, хорошо известны в данной области техники. Конъюгирование превращает Т-независимые антигены в Т-зависимые антигены, тем самым усиливая реакции с созданием памяти и позволяя формироваться защитному иммунитету, и прототипной конъюгированной вакциной являлась вакцина против Haemophilus influenzae типа b (Hib) [см., например, главу 14 ссылки 1]. После создания вакцины против Hib были разработаны конъюгированные сахаридные вакцины для защиты от Neisseria meningitidis (менингококка) и Streptococcus pneumoniae (пневмококка). Другие микроорганизмы, создание вакцины против которых представляет интерес, представляют собой Streptococcus agalactiae (стрептококк группы В) [2], Pseudomonas aeruginosa [3] и Staphylococcus aureus [4].
Помимо использования полноразмерных капсульных сахаридов, после гидролитической обработки можно отобрать олигосахаридные фрагменты желаемого размера [например, ссылка 5], и были опубликованы сообщения о том, что конъюгаты, образованные олигосахаридами с промежуточной длиной цепи, характеризуются повышенной иммуногенностью [например, ссылки 6 и 7]. Из трех конъюгированных вакцин против N. meningitidis серогруппы С, одобренных для использования у человека, Menjugate™ [8] и Meningitec™ основаны на олигосахаридах, тогда как в NeisVac-C™ использован полноразмерный полисахарид. Таким образом, измерение длины олигосахарида (например, путем измерения степени полимеризации, или DP, т.е. количества повторяющихся звеньев в цепи) может быть использовано для косвенной оценки иммуногенности.
Если в состав вакцины входят олигосахаридные фрагменты, контроль качества производства и выпуска должен гарантировать, что олигосахариды имеют определенную длину и что эта длина постоянна от партии к партии. Таким образом, оценка DP также применима в контроле качества, и в структуру Европейского управления по качеству лекарственных средств (the European Directorate for Quality of Medicines, EDQM) входит Официальное ведомство по контролю качества выпускаемых партий (Official Control Authority Batch Release, OCABR), которое для вакцин против Hib особо требует представлять сведения, относящиеся к DP и распределению размеров молекул сахаридов, используемых в производстве.
Оценка DP также может быть использована для мониторинга стабильности вакцины. Сахаридные антигены могут легко деполимеризовываться при температурах окружающей среды [9, 10], что приводит к снижению иммуногенности и повышению гетерогенности вакцины. Такие изменения могут отслеживаться путем определения DP с течением времени хранения.
Среднее значение DP в пуле олигосахаридов может быть измерено в соответствии с рядом методик, и в некоторых случаях выбор метода зависит от анализируемого сахарида. Для анализа олигосахаридов oligosaccharides Hib и менингококков серогрупп А и С были описаны такие методики как колориметрический и/или ферментный анализы [5, 11, 12], но авторы настоящего изобретения обнаружили, что гликозидные связи в сахаридах менингококков серогрупп W135 и Y ('MenW135' и 'MenY') делают невозможным использование этих методик.
Хотя ранее были описаны способы измерения DP сахаридов МеnА и МеnС для конъюгированных вакцин [например, ссылки 5 и 13], существует потребность в способах, которые были бы применимы для анализа сахаридов серогрупп W135 и Y. Таким образом, целью изобретения является обеспечение усовершенствований способов оценки DP сахаридов и, в частности, разработка способов, которые могут быть использованы для измерения DP сахаридов менингококков серогрупп W135 и Y.
Раскрытие изобретения
Авторы изобретения разработали способ, который может быть использован для измерения DP капсульных сахаридов менингококков серогрупп W135 и Y. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида, отличающемуся тем, что сахарид относится к менингококкам серогруппы W135 или серогруппы Y. Способ легко осуществляется путем включения стадии хроматографического разделения. Для композиции, содержащей популяцию капсульных сахаридов различных размеров, изобретение относится к способу измерения среднего значения DP.
Способ, как правило, предусматривает гидролиз сахаридов с высвобождением составляющих моносахаридов, причем анализ проводится по моносахаридам. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида менингококка серогруппы W135 или серогруппы Y, причем способ предусматривает следующие стадии: (i) гидролиз сахарида с получением гидролизата сахарида, содержащего моносахаридные звенья; (ii) определения количества моносахаридных звеньев в гидролизате, причем количественные результаты определения на стадии (ii) используют для расчета степени полимеризации.
Перед гидролизом способ, как правило, предусматривает химическое модифицирование концевого остатка (либо по восстанавливающему концу, либо по невосстанавливающему концу) сахарида таким образом, что после гидролиза до моносахаридов концевой остаток можно отличить от неконцевых остатков. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида менингококка серогруппы W135 или серогруппы Y, причем способ предусматривает следующие стадии: (i) модификация концевого моносахаридного звена сахарида с получением модифицированного концевого моносахарида; (ii) гидролиз сахарида с получением гидролизата сахарида, содержащего моносахаридные звенья, включая модифицированный концевой моносахарид; (iii) определение количества моносахаридных звеньев в гидролизате; (iv) определение количества модифицированного концевого моносахарида в гидролизате; и (v) использование количественных результатов определения на стадиях (iii) и (iv) для расчета степени полимеризации.
В более общем смысле, способ применим к любому сахариду, содержащему два или более различных типов моносахаридных звеньев и содержащему концевой остаток сиаловой кислоты. Предпочтительно, способ обеспечивает получение информации о DP на основании только определения количества остатков сиаловой кислоты в сахариде без необходимости анализа какого-либо иного типа моносахарида. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида, в котором (а) сахарид содержит моносахаридные звенья сиаловой кислоты или отличные от сиаловой кислоты моносахаридные звенья; (b) сахарид содержит концевое моносахаридное звено сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) модификация концевого звена сахарида в виде сиаловой кислоты с получением модифицированного концевого звена сиаловой кислоты; (ii) гидролиз сахарида с получением гидролизата сахарида, содержащего звенья сиаловой кислоты, включая модифицированные концевые звенья сиаловой кислоты; (iii) определение количества звеньев сиаловой кислоты в гидролизате, включая модифицированные концевые звенья сиаловой кислоты; и (iv) использование количественных результатов определения на стадии (iii) для расчета степени полимеризации.
Предпочтительный способ по изобретению основан на восстановлении концевых остатков сиаловой кислоты на сахаридах с последующим расчетом DP путем сравнения молярного отношения общего количества сиаловой кислоты к количеству восстановленной сиаловой кислоты. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида, в котором (а) сахарид содержит моносахаридные звенья сиаловой кислоты или отличные от сиаловой кислоты моносахаридные звенья; (b) сахарид содержит концевое моносахаридное звено сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) восстановление концевого моносахаридного звена сиаловой кислоты с получением восстановленного моносахаридного звена сиаловой кислоты; (ii) гидролиз сахарида с получением гидролизата, содержащего моносахаридные звенья; (iii) определение отношения общего количества сиаловой кислоты (т.е. восстановленной и невосстановленной) к количеству восстановленной сиаловой кислоты в гидролизате.
Применительно к композиции, содержащей популяцию капсульных сахаридов различных размеров, изобретение относится к способу измерения среднего значения степени полимеризации сахаридов, в котором (а) сахариды содержат моносахаридные звенья сиаловой кислоты или отличные от сиаловой кислоты моносахаридные звенья; (b) сахариды содержат концевые моносахаридные звенья сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) восстановление концевых моносахаридных звеньев сиаловой кислоты с получением восстановленных моносахаридных звеньев сиаловой кислоты; (ii) гидролиз сахаридов с получением гидролизата сахаридов, содержащего моносахаридные звенья; (iii) определение отношения общего количества сиаловой кислоты (т.е. восстановленной и невосстановленной) к количеству восстановленной сиаловой кислоты в гидролизате. Композиция может содержать сахариды, не содержащие концевые моносахаридные звенья сиаловой кислоты.
Был описан способ анализа длины и состава сахаридов на основе полисиаловой кислоты [14], в котором концевые остатки окисляли и/или восстанавливали, после чего сахарид расщепляли ферментом нейраминидазой с высвобождением его моносахаридных звеньев сиаловой кислоты. Однако этот известный из предшествующего уровня техники способ был описан только для сахаридов, состоящих исключительно из сиаловых кислот (включая N-ацетилнейраминовую кислоту, N-гликолилнейраминовую кислоту и дезаминированную сиаловую кислоту), и был технически ограничен сахаридами, которые могут быть ферментативно расщеплены на моносахариды. Напротив, способ по изобретению может быть осуществлен с использованием сахаридов, содержащих отличные от сиаловых кислот моносахариды, и не требует (но и не исключает) использования ферментативного гидролиза.
Авторы настоящего изобретения также открыли способ, который может быть использован для измерения DP для капсульных сахаридов менингококков серогруппы С. Способ, опять же, основан на восстановлении концевых остатков сиаловой кислоты, причем значение DP рассчитывают тем же способом. Способ находит более общее применение к любому сахариду, содержащему остатки сиаловой кислоты, которые связаны α 2 9. Предпочтительно, способ не предусматривает ферментативную деполимеризацию. Таким образом, изобретение относится к способу измерения степени полимеризации капсульного сахарида, в котором (а) сахарид содержит моносахаридные звенья сиаловой кислоты, которые связаны α 2 9; (b) сахарид содержит концевое моносахаридное звено сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) восстановление концевого моносахаридного звена сиаловой кислоты с получением восстановленного моносахаридного звена сиаловой кислоты; (ii) гидролиз сахарида с получением гидролизата, содержащего моносахаридные звенья; (iii) определение отношения общего количества сиаловой кислоты (т.е. восстановленной и невосстановленной) к количеству восстановленной сиаловой кислоты в гидролизате.
Применительно к композиции, содержащей популяцию капсульных сахаридов различных размеров, изобретение относится к способу измерения среднего значения степени полимеризации сахаридов, в котором (а) сахариды содержат моносахаридные звенья сиаловой кислоты, которые связаны α 2 9; (b) сахариды содержат концевые моносахаридные звенья сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) восстановление концевых моносахаридных звеньев сиаловой кислоты с получением восстановленных моносахаридных звеньев сиаловой кислоты; (ii) гидролиз сахаридов с получением гидролизата, содержащего моносахаридные звенья; (iii) определение отношения общего количества сиаловой кислоты (т.е. восстановленной и невосстановленной) к количеству восстановленной сиаловой кислоты в гидролизате.
Был описан способ анализа длины и состава сахаридов на основе полисиаловой кислоты [14], в котором концевые остатки окисляли и/или восстанавливали, после чего сахарид расщепляли ферментом нейраминидазой с высвобождением его моносахаридных звеньев сиаловой кислоты. Однако этот известный из предшествующего уровня техники способ был описан только для сахаридов, состоящих из α 2 8-связанных сиаловых кислот, и был технически ограничен сахаридами, которые могут быть ферментативно расщеплены на моносахариды. Напротив, способ по изобретению предусматривает использование α 2 9-связанных сиаловых кислот и предпочтительно предусматривает использование неферментативного гидролиза, как правило, химического (т.е. кислотного) гидролиза.
Известен способ определения длины сахарида серогруппы С [5], в котором значение DP определяли путем сравнения отношения между общим количеством сиаловой кислоты и формальдегида, образующегося в результате обработки сахарида МеnС перйодатом. Этот известный из предшествующего уровня техники способ предусматривает модификацию невосстанавливающего конца полимера и не предусматривает образование сиалитола.
Капсульные сахариды, содержащие остатки сиаловой кислоты и отличные от сиаловой кислоты остатки
В некоторых вариантах выполнения изобретение относится к способу анализа сахаридов, содержащих как моносахаридные звенья сиаловой кислоты, так и отличные от сиаловой кислоты моносахаридные звенья. Более конкретно, сахариды предпочтительно состоят из повторяющихся звеньев, а повторяющиеся звенья состоят из моносахаридных звеньев сиаловой кислоты и отличных от сиаловой кислоты моносахаридных звеньев.
Два особенно интересующих сахарида представляют собой капсульные сахариды Neisseria meningitidis серогрупп W135 и Y. Эти сахариды естественно содержат остаток сиаловой кислоты на восстанавливающем конце и либо глюкозу, либо галактозу на невосстанавливающем конце. Сиаловая кислота в составе нативных сахаридов этих серогрупп представляет собой N-ацетилнейраминовую кислоту или 'NeuNAc'.
Сахарид серогруппы W135 представляет собой полимер, состоящий из дисахаридных звеньев сиаловая кислота-галактоза. Он характеризуется изменчивым O-ацетилированием по положениям 7 и 9 сиаловой кислоты [15]. Структура показана на фиг.1 и записывается как 4)-D-Neup5Ac(7/90Ac)-α-(2 6)-D-Gal-α-(1.
Сахарид серогруппы Y схож с сахаридом серогруппы W135 за исключением того, что дисахаридное повторяющееся звено содержит глюкозу вместо галактозы (см. фиг.3). Он характеризуется изменчивым O-ацетилированием по положениям 7 и 9 сиаловой кислоты [15]. Структура сахарида серогруппы Y показана на фиг.2 и записывается как 4)-D-Neup5Ac(7/90Ac)-α-(2 6)-D-Glc-α-(1.
В других вариантах выполнения изобретение относится к способам анализа сахаридов, содержащих (α 2 9)-связанные сиаловые кислоты. Капсульный сахарид серогруппы С представляет собой гомополимер (α 2 9)-связанной сиаловой кислоты, характеризующийся изменчивым O-ацетилированием по положениям 7 и/или 8.
Капсулы менингококков серогрупп С, W135 и Y отличаются от таковой менингококка серогруппы А, содержащей гомополимер (α1→6)-связанного N-ацетил-D-маннозамин-1-фосфата, и от таковой менингококка серогруппы В, содержащей гомополимер (α 2 8)-связанной сиаловой кислоты.
Степень полимеризации
Степень полимеризации сахарида определяется как число повторяющихся звеньев в этом сахариде. Таким образом, для гомополимера степень полимеризации представляет собой то же, что и число моносахаридных звеньев. Однако для гетерополимера степень полимеризации равна числу моносахаридных звеньев во всей цепи, деленному на число моносахаридных звеньев в минимальном повторяющемся звене, например DP (Glc-Gal)10 равна 10, а не 20, a DP (Glc-Gal-Neu)10 равна 10, а не 30.
В смеси сахаридов, характеризующихся одинаковой основной повторяющейся структурой, но различной длиной (например, в частичном гидролизате длинного полисахарида), обычно измеряют среднее значение DP отдельных молекул. Если интервал размеров слишком велик, настолько, что среднее значение не имеет смысла, существует возможность измерения DP для отдельных фракций смеси после разделения (например, после разделения по размеру). Вообще, изобретение применимо для измерения среднего значения DP в композициях, содержащих сахариды переменной длины.
Восстановление концевого моносахаридного звена сиаловой кислоты
Изобретение применимо для анализа сахаридов, содержащих концевые остатки сиаловой кислоты. В частности, оно применимо для анализа сахаридов, содержащих остатки сиаловой кислоты на восстанавливающем конце.
Для восстановления концевого остатка сиаловой кислоты может быть использована любая химическая методика, предусматривающая, как правило, инкубирование сахарида с восстановителем. Подходящие для каждого данного восстановителя и каждого данного сахарида условия могут быть определены в соответствии с рутинным анализом.
Предпочтительным восстановителем является боргидрид натрия (NaBH4), который восстанавливает концевые остатки сиаловой кислоты [14] в щелочных условиях. Продукт такого восстановления иногда называют сиалитолом [16]. Как правило, достаточным является инкубирование с NaBH4 в течение 2 часов при 37°С. После восстановления в щелочных условиях композицию предпочтительно нейтрализуют, например, путем добавления умеренно кислого ацетата аммония.
Гидролиз сахарида с получением гидролизата сахарида
После восстановления концевого остатка сиаловой кислоты сахарид расщепляют на составляющие моносахаридные звенья. Вообще говоря, деполимеризация сахаридов с получением моносахаридов может быть проведена химически и ферментативно. Однако, если фермента для осуществления данной реакции расщепления не существует, то следует использовать химический способ.
Химический гидролиз сахаридов, как правило, предусматривает обработку либо кислотой, либо основанием в стандартных для данной области техники условиях. Условия деполимеризации капсульных сахаридов на составляющие моносахариды известны в данной области техники. Для сахаридов серогрупп W135 и Y предпочтительным является кислотный гидролиз. Для гидролиза каждого из сахаридов серогрупп С, W135 и Y может быть использован кислотный гидролиз с помощью ТФУ (трифторуксусной кислоты) с предпочтительным использованием слегка более низкой температуры инкубации для сахаридов серогруппы С во избежание разрушения их сиаловых кислот (90°С вместо 100°С). Типичная обработка ТФУ предусматривает добавление ТФУ до конечной концентрации 2 М с последующим нагреванием до 90-100°С в течение 90 минут. Для проведения анализа общего содержания сахарида сахарид серогруппы С может быть гидролизован путем обработки 100 мМ HCI при 80°С в течение 2 часов [17]. Другие типичные условия гидролиза предусматривают использование миллимолярных концентраций слабой кислоты (например, уксусной кислоты) при повышенных температурах (например, 70-80°С).
Доступны ферменты для расщепления связей α 2 9, обнаруженных в сахаридах серогруппы С, и они могут быть использованы в соответствии с изобретением. Однако для ферментативной обработки, как правило, требуется, чтобы сахариды были дез-O-ацетилированы перед гидролизом, так что если желательным является сохранение O-ацетилирования [15], то предпочтительно гидролизовать сахарид химически. Химический гидролиз также может быть предпочтительным, если ферментативный гидролиз протекает медленно. Ферменты для расщепления сахаридов серогрупп W135 и Y, как правило, недоступны.
Хотя выше изобретение раскрыто применительно к получению и анализу гидролизата, содержащего моносахаридные звенья, изобретение также применимо к гидролизатам, содержащим дисахаридные, трисахаридные, тетрасахаридные и т.д. фрагменты капсульного сахарида, но гидролизат в виде моносахаридов является более легким в получении. Условия гидролиза, обеспечивающие получение настолько гомогенной популяции ди-, три-, тетра- и т.д. сахаридов, что количественному анализу подвергается единственное соединение, гораздо сложнее контролировать, чем таковые, просто позволяющие протекать деполимеризации до конца, т.е. с получением моносахаридов.
После деполимеризации гидролизаты сахаридов могут быть высушены, например, с помощью вакуумной сушки.
Определение отношения общего количества сиаловой кислоты к количеству восстановленной сиаловой кислоты
Гидролиз позволяет получить гидролизат сахарида, содержащий моносахаридные звенья исходного сахарида. В вариантах выполнения, в которых сахариды содержат как звенья сиаловой кислоты, так и отличные от сиаловой кислоты звенья, гидролизат содержит сиаловую кислоту и отличные от сиаловой кислоты моносахариды; в вариантах выполнения, в которых сахариды представляют собой гомополимеры сиаловой кислоты, гидролизат содержит только сиаловую кислоту; в обоих случаях фракция моносахаридов сиаловой кислоты находится в модифицированной форме (например, в восстановленной форме). Эта фракция может быть использована для определения значения DP исходного сахарида. Например, если в смеси модифицирован один из десяти остатков сиаловой кислоты, а минимальное повторяющееся звено сахарида содержит единственный остаток сиаловой кислоты, то значение DP исходного сахарида равно 10.
Количества отдельных моносахаридов могут быть определены в виде количества (т.е. молей) молекул, масс, отношений или концентраций. Обычно для облегчения расчета отношений работают с мольными значениями, особенно если составляющие моносахариды имеют различные молекулярные массы, но для определения содержания моносахаридов в смеси могут быть использованы и взаимозаменяемы любые из этих величин. Для измерения количества результаты анализа могут быть сравнены со стандартом, характеризующимся известным содержанием конкретного сахарида.
Деполимеризованная смесь предпочтительно гидролизована полностью до моносахаридов. Авторы настоящего изобретения обнаружили, что иногда происходит неполный гидролиз с получением смесей, в которых присутствуют дисахаридные фрагменты (т.е. Gal-NeuNAc в MenW135 и Glc-NeuNAc в MenY). Например, существуют наблюдения, что обработка сахаридов MenW135 или MenY 2M ТФУ при 90°С позволяла получить смесь моносахаридов и дисахаридов, тогда как повышение температуры гидролиза до 100°С позволяло получить по существу только моносахариды. Неполный гидролиз не ожидался даже при 90°С, но, как показали наблюдения, специалист в данной области техники способен при необходимости модифицировать любую конкретную методику гидролиза для обеспечения полного гидролиза, например, путем повышения температуры и т.д.
Способы определения количества моносахаридов сиаловой кислоты хорошо известны в данной области техники. Способы могут быть прямыми и непрямыми (например, они могут предусматривать дериватизацию моносахаридов с последующим анализом, результаты которого коррелируют с исходным содержанием моносахаридов). Предпочтительные способы позволяют анализировать содержание сиаловой кислоты в присутствии других моносахаридов, так что их не требуется отделять друг от друга перед анализом. Кроме того, способы могут быть использованы для анализа конъюгированных сахаридов, в которых после деконъюгирования нет необходимости разделения носителя и сахарида. Один такой способ представляет собой анионообменную хроматографию и, в частности, высокоэффективную анионообменную хроматографию (НРАЕС), обычно с импульсным амперометрическим обнаружением (PAD) [18, 19]. Системы HPAEC-PAD поставляются Dionex™ Corporation (Sunnyvale, CA), например система BioLC™, в которой используется такая колонка как РА1 [диаметр 10 мкм, полистирольный субстрат, сшитый 2% дивинилбензола, аггломерированный с 500 нм функционализированным четвертичным аммонием латексом MicroBead (сшитым на 5%)] или РА10 [диаметр 10 мкм, этилвинилбензольный субстрат, сшитый 55% дивинилбензола, аггломерированный с 460 нм дифункционализированным ионом четвертичного аммония MicroBead (сшитым на 5%)]. Эти системы позволяют проводить количественный анализ отдельных сахаридов в смесях без необходимости дериватизации или разделения перед анализом. Для анализа сахаридов может быть желательно отфильтровать другие соединения перед нанесением на колонку, и Dionex™ производит для этих целей предколонки и ловушки, например аминоуловитель для удаления аминокислот, боратный уловитель и т.д.
Альтернативным способом определения количества моносахаридов сиаловой кислоты в деполимеризованной смеси является ядерный магнитный резонанс (ЯМР). Однако для легкости использования и высокой чувствительности предпочтительны хроматографические методики по изобретению. Однако какой бы способ не был выбран, в некоторых вариантах выполнения изобретения важно отличить восстановленную сиаловую кислоту от невосстановленной сиаловой кислоты. Это может предусматривать получение от каждой из них уникальных сигналов или может предусматривать получение одного уникального сигнала и одного объединенного сигнала, причем различие между двумя данными сигналами предоставляет необходимую информацию.
Другим способом определения количества моносахаридов сиаловой кислоты является колориметрический анализ [80]. Этот способ особенно применим для определения количества невосстановленной сиаловой кислоты после гидролиза в ТФУ.
Определив относительные количества модифицированной и немодифицированной (например, восстановленной и невосстановленной) сиаловой кислоты, легко установить значение DP исходного сахарида.
Помимо определения количества сиаловых кислот в гидролизате, способы по изобретению могут предусматривать определение количества других моносахаридов (например, глюкозы или галактозы), которые могут быть производными того же сахарида, что и сиаловые кислоты, или других сахаридов. Эти измерения могут быть использованы для определения параметров, отличных от DP, или могут быть использованы как часть определения значения DP, например в качестве подтверждения или вместо измерения общего количества сиаловой кислоты, особенно если мольные количества сиаловой кислоты и другого моносахарида такие же, как и сахариды W135 и Y.
Способ по изобретению, как правило, является деструктивным. Более типично взять образец интересующей композиции и затем проводить анализ образца, чем осуществлять способ на всей композиции.
Конъюгаты
Изобретение применимо для анализа содержания сахарида в вакцинах и, в частности, в вакцинах, содержащих конъюгированный сахарид. Ковалентное конъюгирование применяют для повышения иммуногенности сахаридов благодаря их переходу из разряда Т-независимых антигенов в разряд Т-зависимых антигенов, обеспечивая таким образом прайминг с созданием иммунной памяти. Конъюгирование особенно применимо для создания педиатрических вакцин и представляет собой хорошо известный метод [обзор приводится, например, в ссылках 20-29]. Сахариды могут быть связаны с носителями непосредственно [30, 31], но, как правило, используют линкер, например адипиновую кислоту, β-пропионамидо [32], нитрофенилэтиламин [33], галогенацилгалогениды [34], гликозидные связи [35], 6-аминокапроновую кислоту [36], ADH [37], радикалы C4-C-12 [38] и т.д.
Типичными белками-носителями для использования в конъюгатах являются бактериальные токсины или анатоксины, такие как дифтерийный анатоксин или столбнячный анатоксин. В Menjugate™ и Meningitec™ белком-носителем является производное дифтерийного токсина CRM197 [39-41], тогда как в составе NeisVac™ использован столбнячный анатоксин. В Menactra™ в качестве носителя используют дифтерийный анатоксин. Другие подходящие белки-носители включают в себя белок внешней мембраны N. meningitidis [42], синтетические пептиды [43, 44], белки теплового шока [45, 46], белки возбудителя коклюша [47, 48], цитокины [49], лимфокины [49], гормоны [49], факторы роста [49], искусственные белки, содержащие множественные эпитопы человеческих CD4+ Т-клеток из антигенов различных патогенов [50], белок D Н. influenzae [51, 52], поверхностный белок PspA пневмококков [53], железосвязывающие белки [54], токсин А или В С.difficile [55] и т.д. В составе композиций может быть использовано более одного белка-носителя, например для снижения риска возникновения супрессии носителем, а один белок-носитель может нести более одного сахаридного антигена [56]. Конъюгаты, как правило, характеризуются отношением сахарид:белок (по массе) от 1:5 (т.е. избытка белка) до 5:1 (т.е. избытка сахарида). Помимо конъюгатов композиции могут содержать свободный белок-носитель [57].
Изобретение особенно применимо перед конъюгированием на стадии, на которой необходимо обеспечить, что для получения конъюгата отобраны сахаридные цепи нужного размера.
Изобретение обеспечивает подлежащее контролю или мониторингу протекание фрагментации полноразмерного полисахарида перед конъюгированием. Если желательно получение олигосахаридов конкретной длины (интервала длин), то важно, чтобы фрагментация полисахарида не была настолько полной, что деполимеризация проходила желаемую точку (например, как максимум с получением моносахаридов). Изобретение обеспечивает мониторинг протекания этой частичной деполимеризации путем измерения средней длины цепи во времени. Таким образом, изобретение относится к способу измерения степени полимеризации сахарида(ов) в композиции, предусматривающему следующие стадии: (а) начало деполимеризации сахарида(ов) в композиции; и в одной или нескольких временных точках после этого (b) измерение значения DP сахарида(ов), как описано выше. При первоначальном проведении экспериментов обычно измеряют значение DP в нескольких временных точках для определения хода процесса во времени, а после того как стандартные условия определены, обычно измеряют значение DP в определенной временной точке для подтверждения. Когда DP достигает желаемого значения, способ может предусматривать следующую стадию: (с) остановки деполимеризации, например, путем промывания, разделения, охлаждения и т.д. Способ также может предусматривать дополнительную стадию конъюгирования деполимеризованного сахарида с белком-носителем после химической активации при необходимости.
Изобретение также позволяет проводить отбор олигосахаридных цепей желаемой длины после фрагментации. Таким образом, изобретение относится к способу отбора сахаридов для использования в получении гликоконъюгата, предусматривающему следующие стадии: (а) приготовление композиции, содержащей смесь различных полисахаридных фрагментов, характеризующихся различными степенями полимеризации; (b) разделение смеси на подсмеси; (с) определение значения DP одной или нескольких подсмесей в соответствии со способом, описанным выше; и (d) использование результатов стадии (с) для отбора одной или нескольких подсмесей для использования в конъюгировании. Способ может предусматривать фрагментацию полисахарида перед стадией (а) или может начинаться с использования заранее приготовленной смеси. Фрагменты могут представлять собой фрагменты одного и того же полисахарида, например сахарида той же серогруппы. После стадии (d) способ может предусматривать стадию конъюгирования с белком-носителем после химической активации при необходимости.
Для сахарида перед конъюгированием вполне обычной является химическая активация с целью введения функциональной группы, способной реагировать с носителем. Условия активации сахарида могут вызвать гидролиз, и, соответственно, после активации полезно проверить значение DP. Термин "сахарид" следует, где уместно, понимать как охватывающий эти активированные сахариды. Более того, изобретение относится к способу получения активированного сахарида для использования в получении гликоконъюгата, предусматривающему следующие стадии: (а) получение сахарида; (b) химическая активация сахарида с целью введения функциональной группы, способной реагировать с белком-носителем; и (с) измерение значения DP продукта стадии (b), описанного выше. Способ может предусматривать дополнительную стадию (d) реакции активированного сахарида с белком-носителем (который сам может быть активирован) с получением гликоконъюгата. Способ может предусматривать фрагментацию полисахарида перед стадией (а) или может начинаться с использования заранее приготовленной смеси.
Изобретение также может быть использовано после конъюгирования. После конъюгирования композиции могут быть проанализированы с помощью изобретения тремя способами: во-первых, может быть измерено общее значение DP сахаридов композиции, например, перед смешиванием различных конъюгатов или перед выпуском вакцины (в целях соблюдения регламента или контроля качества); во-вторых, может быть измерено значение DP свободного неконъюгированного сахарида в композиции, например, для контроля неполного конъюгирования или для слежения за гидролизом конъюгатов путем мониторинга повышения содержания свободного сахарида с течением времени; в-третьих, для тех же целей может быть измерено значение DP конъюгированного сахарида в композиции. Для первого и третьего способов требуется, чтобы сахарид высвобождался из состава конъюгата до проведения анализа. Однако в ситуациях, в которых конъюгирование сахарида предусматривает такие реакцию или модификацию остатка сиаловой кислоты на его восстанавливающем конце, что остаток теряет способность к восстановлению, изобретение может быть применимо только к тем сахаридам, концевая сиаловая кислота которых может быть регенерирована (или в которых восстановленная концевая сиаловая кислота может быть получена прямо).
Для раздельной оценки конъюгированных и неконъюгированных сахаридов они должны быть разделены. Свободный (т.е. неконъюгированный) сахарид в водной композиции может быть отделен от конъюгированного сахарида различными способами. Реакция конъюгирования изменяет различные химические и физические параметры сахарида, и различия могут быть использованы для разделения. Например, для разделения свободного или конъюгированного сахаридов может быть использовано разделение по размеру, поскольку конъюгированное вещество характеризуется более высокой массой благодаря наличию белка-носителя. Предпочтительным методом разделения по размеру является ультрафильтрация. В качестве дополнительной альтернативы, если конъюгаты адсорбированы на адъюванте, то центрифугирование позволяет разделить адсорбированный конъюгат (в осадке) от свободного сахарида (в супернатанте), который десорбируется после гидролиза.
Изобретение относится к способу анализа гликоконъюгата, предусматривающему следующие стадии: (а) обработка гликоконъюгата для высвобождения сахарида с носителя; и (b) измерение значения DP высвобожденного сахарида, как описано выше. Изобретение относится к способу анализа композиции гликоконъюгата, предусматривающему следующие стадии: (а) отделение неконъюгированного сахарида в составе композиции от конъюгированного сахарида; и (b) измерение значения DP неконъюгированного и/или конъюгированного сахарида, как описано выше.
Изобретение также относится к способу выпуска вакцины для клинического применения, предусматривающему следующие стадии: (а) производство вакцины, содержащей конъюгат капсульного сахарида, причем сахарид содержит моносахаридные звенья сиаловой кислоты и отличные от сиаловой кислоты моносахаридные звенья; (b) анализ DP сахарида в составе вакцины, как описано выше; и, если результаты стадии (b) свидетельствуют о приемлемом для клинического применения значении DP, (с) выпуск вакцины для клинического применения. Стадия (b) может быть осуществлена на упакованной вакцине или на неупакованной вакцине перед упаковкой.
Смешанные сахариды
Изобретение позволяет проводить анализ DP в композициях, содержащих менингококковые капсульные сахариды, содержащие сиаловую кислоту. Композиции также могут содержать дополнительные капсульные сахариды (например, капсульные сахариды N. meningitidis серогруппы А, капсульный сахарид Н. influenzae b и т.д.) при условии, что эти сахариды не содержат сиаловые кислоты, которые могли бы помешать проведению итогового анализа. Если остатки сиаловой кислоты в композиции содержат более одного сахарида, то для различения отдельных сахаридов могут быть использованы принципы, описанные в ссылке 58.
Капсульный сахарид менингококка серогруппы А представляет собой гомополимер (α1→6)-связанного N-ацетил-D-маннозамин-1-фосфата с частичным O-ацетилированием по положениям С3 и С4. Ацетильные группы могут быть заменены блокирующими группами во избежание гидролиза [10], и для целей настоящего изобретения такие модифицированные сахариды остаются сахаридами серогруппы А.
Капсульный сахарид Hib представляет собой полимер рибозы, рибитола и фосфата. Сахарид известен как 'PRP' (поли-3-β-D-рибозо-(1,1)-D-рибитол-5-фосфат).
Отличные от капсульных сахаридов сахаридные компоненты
Предпочтительно, чтобы композиции, анализируемые в соответствии с изобретением, не содержали сиаловую кислоту в свободной форме (помимо каких-либо фоновых моносахаридов, образующихся в результате гидролиза капсульных сахаридов). Однако, если присутствует свободная сиаловая кислота, существует два основных способа минимизации или устранения помех для анализа. Во-первых, исходное содержание свободной сиаловой кислоты может быть измерено, а затем вычтено из содержания, измеренного в деполимеризованной смеси. Во-вторых, свободная сиаловая кислота может быть удалена из композиции до проведения анализа, например путем фильтрования или диализа. Для удаления низкомолекулярных компонентов могут быть использованы ультрафильтрационные мембраны.
Несахаридные компоненты
Помимо анализа сахаридов в составе композиции способ может предусматривать анализ других компонентов или свойств, например, осмоляльности, рН, степени полимеризации отдельных сахаридов или конъюгатов, содержания белка (особенно белков-носителей), содержания алюминия, содержания поверхностно-активных веществ, содержания консервантов и т.д.
Изобретение относится к способу приготовления вакцинной композиции, предусматривающему стадию анализа DP сахарида по изобретению и стадию измерения рН композиции с последующей необязательной стадией доведения рН композиции до желаемого значения, например от 6 до 8 или около 7.
Изобретение также относится к способу приготовления вакцинной композиции, предусматривающему следующие стадии: (а) проведение анализа DP капсульного сахарида, как описано выше; (b) конъюгирование прошедшего анализ DP сахарида с одним или несколькими белками-носителями; (с) при необходимости анализ рН и/или других свойств нерасфасованной вакцины и, если результаты стадии (с) свидетельствуют о приемлемости нерасфасованной вакцины для клинического применения, (d) приготовление и упаковка вакцины для использования у человека из нерасфасованной партии. Стадия (с) может предусматривать оценку минимальной концентрации сахарида, оценки отношения "неконъюгированный:конъюгированный сахарид" и т.д. Стадия (d) может предусматривать упаковку в разовую дозированную форму или многократную дозированную форму, например в ампулы или в шприцы. Объем типичной дозы для инъекции человеку составляет 0,5 мл.
Изобретение также относится к способу приготовления вакцинной композиции, предусматривающему следующие стадии: (а) получение прошедшего анализ DP капсульного сахарида серогрупп W135 и/или Y, как описано выше; (b) конъюгирование прошедшего анализ DP сахарида с одним или несколькими белками-носителями с получением конъюгированного сахарида; и (с) смешивание конъюгированного сахарида с одним или несколькими дополнительными антигенами, например, с
- капсульным сахаридным антигеном N. meningitidis серогруппы С;
- капсульным сахаридным антигеном N. meningitidis серогруппы А;
- белковым антигеном N. meningitidis серогруппы В;
- препаратами микровезикул N. meningitidis серогруппы В [59], "нативных OMV" [60], пузырьков или везикул внешней мембраны [например, ссылки 61-66 и т.д.];
- сахаридным антигеном Haemophilus influenzae типа b;
- антигеном Streptococcus pneumoniae, таким как поливалентные конъюгированные сахаридные антигены [например, ссылки 67-69];
- антигеном вируса гепатита А, таким как инактивированный вирус [например, 70, 71];
- антигеном вируса гепатита В, таким как поверхностный и/или коровий антигены [например, 71, 72];
- антигеном Bordetella pertussis, таким как голотоксин возбудителя коклюша (РТ) и волокнистый гемагглютинин (FHA) В. pertussis, при необходимости также в сочетании с пертактином и/или агглютиногенами 2 и 3 [например, ссылки 73 и 74]. Могут быть использованы клеточные антигены возбудителя коклюша;
- дифтерийным антигеном, таким как дифтерийный анатоксин [например, глава 3 ссылки 75], например мутант CRM197 [например, ссылка 76];
- столбнячным антигеном, таким как столбнячный анатоксин [например, глава 4 ссылки 75];
- антигеном(ами) полиовируса [например, 77, 78], таким(и) как IPV.
Такие антигены могут быть адсорбированы на адъювант на основе солей алюминия (например, гидроксида или фосфата). Любые дополнительные сахаридные антигены предпочтительно включают в состав в виде конъюгатов.
Однородность между партиями
При производстве вакцин для человека конъюгированные сахариды должны проходить контроль качества перед конъюгированием (например, сахарида и белка-носителя), после конъюгирования, после составления и после смешивания. Известные из предшествующего уровня техники способы измерения DP не относятся к сахаридам серогрупп W135 и Y. Однако с созданием настоящего изобретения измерение DP сахаридов этих двух серогрупп стало возможным и может быть объединено со способами измерения DP сахаридов серогрупп А и С [5]. Более того, способы по изобретению дают надежные и однородные результаты и, таким образом, позволяют проводить достоверные сравнения различных партий смешанных конъюгатов A/C/W135/Y, что было невозможно в соответствии с известными из предшествующего уровня техники способами. Таким образом, различные партии смешанных конъюгированных вакцин могут быть приготовлены, проанализированы, и однородные между собой партии могут быть отобраны для выпуска и использования, тогда как отклоняющиеся партии могут быть отброшены.
Изобретение относится к двум партиям вакцины, причем (а) обе партии вакцины содержат (i) конъюгат капсульного сахарида Neisseria meningitidis cepoгруппы A; (ii) конъюгат капсульного сахарида Neisseria meningitidis серогруппы С; (iii) конъюгат капсульного сахарида Neisseria meningitidis серогруппы W135; (iv) конъюгат капсульного сахарида Neisseria meningitidis серогруппы Y; (b) значение DP сахарида серогруппы А в первой партии составляет A1, a значение DP сахарида серогруппы А во второй партии составляет А2; (с) значение DP сахарида серогруппы С в первой партии составляет C1, а значение DP сахарида серогруппы С во второй партии составляет С2; (d) значение DP сахарида серогруппы W135 в первой партии составляет W1, а значение DP сахарида серогруппы W135 во второй партии составляет W2; (е) значение DP сахарида серогруппы Y в первой партии составляет Y1, а значение DP сахарида серогруппы Y во второй партии составляет Y2; (f) каждое из отношений A1/А2, C1/C2, W1/W2 и Y1/Y2 составляет от 0,90 до 1,10, а предпочтительно составляет от 0,95 до 1,05.
Значения отношений, указанные в (f), могут быть основаны на единственном образце из каждой сравниваемой партии, но, как правило, основаны на средних значениях (например, средних) множества образцов из каждой партии. Таким образом, из двух партий могут быть взяты множественные образцы, и каждый образец может быть подвергнут множественным измерениям A1, А2, C1, С2, W1, W2, Y1 и Y2 с последующим расчетом средних значений для каждой партии и использованием средних значений для расчета необходимых отношений.
Каждая партия (или серия) вакцины изготавливается отдельно. Например, две различные партии могут быть получены путем раздельных смешиваний одних и тех же нерасфасованных отдельных конъюгатов или путем смешивания нерасфасованных отдельных конъюгатов, полученных раздельно. Различные образцы одной нерасфасованной смеси не являются различными партиями, поскольку эти образцы не подвержены вариациям между партиями, которые появляются благодаря различиям, возникающим при приготовлении смесей различных конъюгатов.
Помимо характеристик (а)-(f), указанных выше, две партии могут быть дополнительно охарактеризованы следующими параметрами: (g) значение концентрации неконъюгированного сахарида серогруппы А в первой партии составляет А3, (h) значение концентрации неконъюгированного сахарида серогруппы А во второй партии составляет А4, (i) значение концентрации неконъюгированного сахарида серогруппы С в первой партии составляет С3; (j) значение концентрации неконъюгированного сахарида серогруппы С во второй партии составляет C4; (k) значение концентрации неконъюгированного сахарида серогруппы W135 в первой партии составляет W3, если подходит, (I) значение концентрации неконъюгированного сахарида серогруппы W135 во второй партии составляет W4, (m) значение концентрации неконъюгированного сахарида серогруппы Y в первой партии составляет Y3; (n) значение концентрации неконъюгированного сахарида серогруппы Y во второй партии составляет Y4; (о) каждое из значений отношений А3/А4, С3/С4, W3//W4 и Y3/Y4 составляет от 0,90 до 1,10, а предпочтительно составляет от 0,95 до 1,05.
Общие определения
Термин "содержащий" охватывает термин "включающий в себя", равно как и "состоящий из", например композиция, "содержащая" Х может состоять исключительно из Х или может включать в себя что-либо отличное, например X+Y.
Словосочетание "по существу" не исключает значения "полностью" или "абсолютно", например композиция, "по существу не содержащая" Y, может абсолютно не содержать Y. При необходимости словосочетание "по существу" может быть опущено из определения по изобретению.
Термин "около" применительно к численному значению х означает, например, х±10%.
Очевидно, что циклические молекулы сахаров могут находиться в открытой и замкнутой форме, и что хотя в приведенных здесь структурных формулах показаны замкнутые формы, открытые формы также подпадают под объем изобретения.
Краткое описание чертежей
На фиг.1 и 2 показаны структурные формулы капсульных сахаридов менингококков серогрупп W135 (11) и Y (2). На фиг.3 показано различие между сахаридами серогрупп W135 и Y.
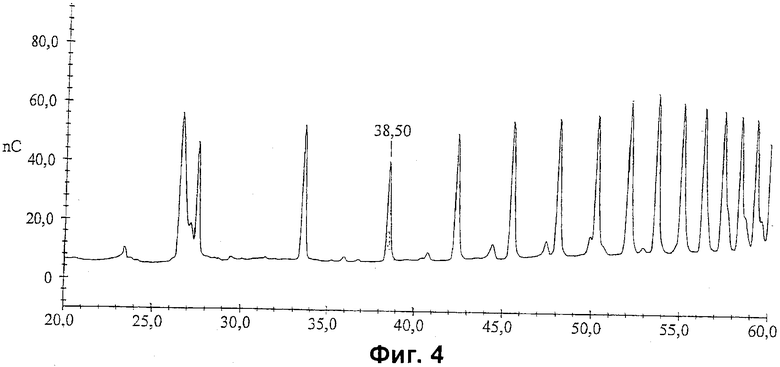
На фиг.4 и 5 показаны хроматограммы сахаридов MenY до (4) и после (5) разделения по размеру.
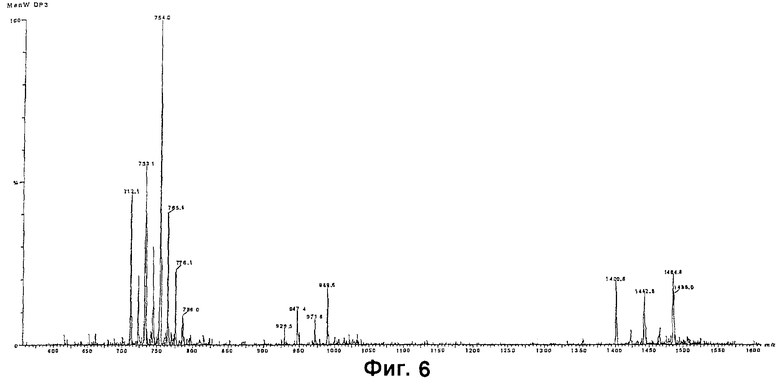
На фиг.6 и 7 показаны спектры ESI для сахаридов MenW135 (6) и MenY (7).
На фиг.8 показана структура сахарида MenW135 с DP3 над его спектром 1Н-ЯМР. На фиг.9 показано то же для сахарида MenY с DP4.
На фиг.10-12 показаны профили изократической элюции стандартных растворов сиаловой кислоты.
На фиг.13 показан профиль градиентной элюции олигосахарида MenY.
На фиг.14 показана стандартная кривая для сиалитола.
На фиг.15 показано снижение DP MenW135 () и MenY () при деполимеризации по данным HPAEC-PAD. На фиг.16 и 17 показан рост количества короткоцепочечных олигосахаридов при том же процессе для MenW135 (16) и MenY (17) со сравнением нулевого момента времени (А) с конечными смесями (В).
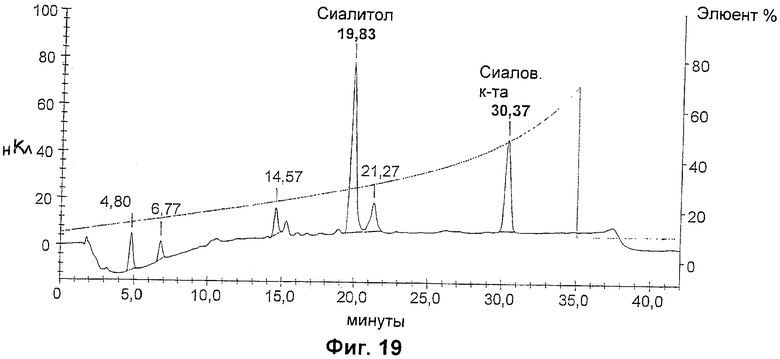
На фиг.18 показан спектр ESI МеnС с DP5, а на фиг.19 проиллюстрирован его анализ НРАЕС.
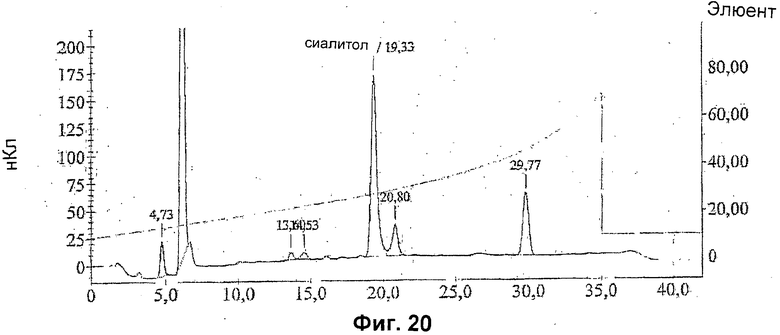
На фиг.20 приведен профиль градиентной элюции олигосахарида MenW135. По левой оси отложены результаты амперометрического обнаружения в нКл; на правой оси отложен % элюента (100 мМ ацетат Na+20 мМ NaOH).
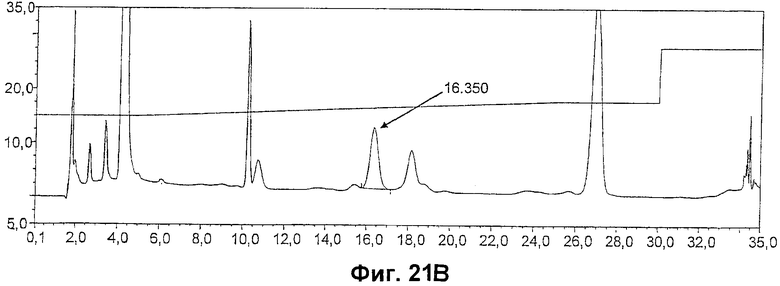
На фиг.21 приведен еще один профиль градиентной элюции олигосахарида MenW135. На фиг.21 А показаны результаты на стандартном образце, а на фиг.21В показаны результаты на MenW135.
Способы осуществления изобретения
Приготовление стандартных растворов олигосахаридов
Очищенные капсульные полисахариды (CPS) серогрупп W135 и Y получали в соответствии со способами, описанными в ссылке 79. Их получали в виде 10 мг/мл раствора в 0,01 М уксусной кислоте. Для гидролиза CPS их нагревали до 70-80°С в течение продолжительного периода времени. В ходе гидролиза образцы получали из подлежащих анализу растворов, охлаждали и нейтрализовали после экстракции. Фрагменты, полученные в результате гидролиза, содержат конечные остатки сиаловой кислоты, а не конечные остатки глюкозы или галактозы. Олигосахариды затем очищали по методу ионообменной хроматографии на колонке с Q-сефарозой, разделение в которой происходит по размеру и заряду. Для первоначальной нормализации содержание сиаловой кислоты измеряли по модифицированному методу Свеннерхольма [80], в соответствии с которым поглощение измеряли при 564 нм. Отдельные фракции выделяли и анализировали по методу ЯМР, масс-спектрометрии с электрораспылением и НРАЕС.
Для проведения анализа НРАЕС олигосахаридов использовали либо колонку CarpoPac PA100, либо колонку lonPac AS11 (обе 4×250 мм) в хроматографической системе Dionex DX-500, оборудованной насосом GP40, детектором ED40 и автодозатором AS3500. Разделение проводили при комнатной температуре при скорости потока 1,0 мл/мин.
Для колонки PA100 использовали следующие элюенты: А) ацетат натрия 500 мМ + гидроксид натрия 100 мМ и В) гидроксид натрия 100 мМ. Первоначальная изократическая элюция 10% А (15 мин) сменялась элюцией по линейному градиенту от 10% до 100% А в течение 50 мин. Для колонки AS11 использовали следующие элюенты: А) гидроксид натрия 100 мМ и В) вода с элюцией по линейному градиенту от 5% до 100% А в течение 50 мин.
Мониторинг элюатов проводили с помощью импульсного электрохимического детектора (ED40) в импульсном амперометрическом режиме с золотым рабочим электродом и Ag/AgCl контрольным электродом. Применяли серии из трех потенциалов со следующими параметрами: Е1=0,05 В, t1=400 мс; Е2=0,75 В, t2=200 мс; Е3=0,15 В, t3=400 мс. Интеграция имела место от 200 мс до 400 мс приложения Е1. Полученные хроматографические данные сводили и обрабатывали с помощью программного обеспечения для преобразования данных Peak Net (Dionex).
НРАЕС на CarboPac PA100 позволяла получать профиль для олигосахаридов MenW135 и MenY. Калибровку спектров проводили путем сравнения хроматограмм очищенных и объединенных олигосахаридов с параллельным определением параметров олигосахаридов по методу ESI-MS для выявления корреляции между значением пика хроматограммы и значением DP элюируемых олигосахаридов.
Масс-спектрометрию с ESI проводили с помощью масс-анализатора Micromass ZQ-4000, оборудованного источником электрораспыления ионов. Прибор калибровали с помощью йодида натрия (2 г/л) и йодида цезия (50 мг/л), растворенных в изопропиловом спирте/воде 50/50 (по объему). Разность потенциалов в капилляре составляла 3 кВ, разность потенциалов на конусе составляла 60 В. Образцы растворяли в 50% (по объему) водном ацетонитриле + 0,1% муравьиная кислота и вводили со скоростью потока 10 мкл/мин. Спектры регистрировали в режиме положительных ионов с интервалом сканирования от 200 до 2000 m/z.
На фиг.4 и 5 показаны НРАЕС-хроматограммы (колонка РА100) смеси олигосахаридов MenY до (фиг.4) и после (фиг.5) разделения на Q-сефарозе. Анализ с ESI пика во временной точке -38 минут подтвердил наличие олигосахарида MenY, характеризующегося значением DP, равным 4 (фиг.7). Сходные эксперименты были проведены для MenW135, а на фиг.6 показан спектр анализа с ESI для олигосахарида с DP 3.
В анализе с ESI в спектре может наблюдаться множество молекулярных ионов одного вида молекулы, соответствующих исходной молекуле с варьирующими числами O-ацетильных заместителей и ионов аддуктов натрия. Ионы аддуктов натрия могут возникать благодаря присутствию некоторых количеств натрия при анализе образцов и обычно наблюдаются в масс-спектрах олигосахаридов. Кроме того, исходная молекула может характеризоваться различным числом положительных зарядов, и, таким образом, молекула олигосахарида способна производить множество различных положительных ионов в зависимости от наличия O-ацетильных заместителей, аддуктов натрия и числа положительного заряда. Таким образом, спектры, приведенные на фиг.6 и 7, свидетельствуют о большом количестве положительных ионов.
На фиг.6 пики между 700-800 и 1400-1526 m/z соответствуют ионам с двойным и одинарным зарядом соответственно, возникающим в результате добавления катионов натрия и O-ацетильных групп. Они были отнесены к следующим моноизотопным массам, соответствующим таковым тримерного олигосахарида (MenW135 с DP 3):
b число O-ацетильных заместителей
с число противоионов натрия
На фиг.7 пики между 900-1100 и 1800-2000 m/z соответствуют ионам с двойным и одинарным зарядом соответственно, возникающим в результате добавления катионов натрия и O-ацетильных групп. Они были отнесены к следующим моноизотопным массам, приведенным в таблице 2 и соответствующим таковым тетрамерного олигосахарида (MenY с DP 4):
Образцы для ЯМР-анализа готовили путем растворения лиофилизированных олигосахаридов в 750 мкл 99,9% D2O (Aldrich™) с получением 10-15 мМ концентрированных растворов. Для каждого эксперимента использовали 5 мм ампулы для ЯМР Wilmad™. ЯМР-спектры регистрировали при 298 К с помощью ЯМР-спектрометра Bruker™ Avance DRX 600 MHz, оборудованного 5 мм гетероядерным зондом тройного резонанса TBI и блоком BGU. Для регистрации и обработки данных использовали программное обеспечение Bruker XWINNMR 3.0. Условия регистрации 1H-стандартного спектра предусматривают получение 32 тыс. точек в спектральном окне 6000 Гц с 4 сканированиями и задержкой релаксации 10 с. Спектры 1Н-ЯМР подвергались преобразованию Фурье после применения расширяющей линии 0,1 Гц функции и относили к контролю в виде монодейтерированной воды при 4,79 м.д. Эксперименты по снятию 13С и двухмерного ЯМР-спектров (COSY и HSQC с двухквантовым фильтром) проводили для получения 1H-спектров олигосахаридов.
Протонные ЯМР-спектры менингококковых олигосахаридов W135 и Y сопоставляли путем сравнения с опубликованными данными [81] и с помощью корреляционных спектров двухмерной протон-протонной COSY и протон-углеродной HSQC. Наряду с протонными химическими сдвигами, много структурной информации дают константы гомоядерной и гетероядерной связей. В ЯМР-спектрах высокого разрешения олигосахаридов W135 (фиг.8) и MenY (фиг.9) наблюдались относительно четкие сигналы, которые позволяли провести особенно определенное сопоставление пиков аномерного протона радикалов Gal/Glc и H3eq/axNeuNAc радикалов NeuNAc. Эти пики расположены в областях спектра, где отсутствует наложение других сигналов, которое могло бы осложнить линейное разрешение. Продолжая спектр, можно определить протонные химические сдвиги сигналов:
1H ЯМР-спектры подтвердили молекулярную структуру, идентичность и целостность сахаридных цепей и показали, что значения DP образцов составляли: DPMenW135=3; DPMenY=4.
Таким образом, колонка с Q-сефарозой позволила разделить олигосахариды по DP, а анализы ESI и ЯМР подтвердили, что олигосахаридные стандарты представляли собой MenW135 с DP 3 и MenY с DP 4. Эти стандарты анализировали в соответствии со способами по изобретению.
Хроматографический анализ DP
Содержание сиаловой кислоты в образцах олигосахаридов объемом 100 мкл доводили до 0,5 мг/мл. Эти образцы обрабатывали 100 мкл 40 мМ раствора NaBH4 в 10 мМ NaOH. Образцы нагревали при 37°С в течение 2 часов в закрытой пробирке с завинчивающейся крышкой. Для остановки реакции образцы затем обрабатывали 10 мкл 5 М ацетата аммония, рН 6,0 и выдерживали при комнатной температуре в течение 30 минут. Добавляли 200 мкл метанола и образцы затем сушили в вакууме в течение 1 часа с помощью концентрирующей установки Speed Vac, оборудованной охлаждаемой конденсатной ловушкой (Savant SC110).
Образцы восстанавливали 100 мкл воды Milli-Q и 100 мкл 4 М ТФУ (в конечной концентрации 2 М) и нагревали при 100°С в течение 90 минут. Гидролизаты затем сушили с помощью концентрирующей установки Speed Vac, оборудованной двумя охлаждаемыми конденсатными ловушками (Savant SC110).
Для анализа HPAEC-PAD образцы растворяли в 1,0 мл дегазированной воды Milli-Q и затем фильтровали (0,22 мкм). Анализ продуктов гидролиза проводили на той же системе Dionex, но используя колонку Carbopac PA1 (4×250 мм) с предколонкой для улавливания боратов. Эти колонка и предколонка лучше подходят для анализа моносахаридов, чем колонки PA100 и AS11. В некоторых экспериментах использовали изократическую элюцию 50 мМ ацетатом натрия и 20 мМ гидроксидом натрия, а в других экспериментах использовали градиентную элюцию следующими элюентами: А) 100 мМ ацетат натрия и 20 мМ гидроксид натрия и В) 20 мМ гидроксид натрия и градиент от 10% до 70% А (кривая 7). Элюаты анализировали, как описано выше.
Эта установка позволяет отличать сиаловую кислоту от сиалитола и получить количественные результаты для каждого из них. Для расчета значения DP исходных олигосахаридов использовали отношение общего содержания (т.е. восстановленной и невосстановленной) сиаловой кислоты к содержанию восстановленной сиаловой кислоты.
Для первоначального тестирования стандартный раствор чистой сиаловой кислоты (Sigma, Steinheim, Germany) готовили в концентрации 2,0 мкг/мл и восстанавливали NaBH4, как описано выше. Образцы анализировали в различных временных точках по методу НРАЕС с изократической элюцией. Было определено, что обработка 0,04 М NaBH4 в течение 2 часов при 37°С обеспечивала полное восстановление сиаловой кислоты в стандарте. На фиг.10 показаны результаты анализа образца в нулевой момент времени, а на фиг.11 показаны результаты анализа образца через 2 часа с уменьшением времени удерживания с 8,5 до 4,7-5,0.
Двойной пик на фиг.11 образовался благодаря неразрешенным диастереоизомерам сиалитола [14]. Обработка стандарта сиаловой кислоты 2 М ТФУ в течение 90 минут при 100°С обеспечивала устранение двойного пика (фиг.12), оставляя таким образом единственный пик для количественного анализа сиалитола. Известно, что гидролиз ТФУ применим для расщепления сахаридов как по причине эффективности, так и благодаря простоте удаления [82-84], и его использовали для анализа нескольких вакцин на основе сахаридов [82]. Таким образом, использование ТФУ для кислотного гидролиза сахаридов оправдано тремя целями - эффективным гидролизом, эффективным удалением и устранением расщепления пика сиалитола.
Образец олигосахарида MenY с ожидаемым значением DP в интервале от 3 до 5 обрабатывали, как описано, но изократические условия хроматографической элюции не обеспечивали удовлетворительного разделения пика сиалитола. Поэтому вместо указанных условий использовали градиент элюции, что позволило получить хроматограмму, показанную на фиг.13. Сиалитол и сиаловая кислота характеризовались значениями времени удерживания соответственно 19,3 и 29,8 минут. В соответствии с той же методикой анализировали образец олигосахарида MenW135 с ожидаемым значением DP в интервале от 3 до 5 (фиг.20). Элюцию сиалитола отмечали через 19,33 минут, а элюцию сиаловой кислоты отмечали через 29,77 минут.
Для обеспечения количественного анализа хроматограмм, приведенных на фиг.13 и фиг; 20, строили стандартные кривые на основе известных концентраций сиаловой кислоты и сиалитола. Для построения стандартной кривой использовали концентрации сиаловой кислоты или сиалитола 0,5, 1,0, 2,0, 4,0 и 6,0 мкг/мл. Линейный ответ детектора показан на фиг.14.
Количества сиалитола и сиаловой кислоты могут быть определены в образцах MenW135 и MenY путем сравнения с этими стандартными кривыми. Например, по расчетам площадь под пиком на 19,33 минутах в кривой элюции MenW135 (фиг.20) составляла 44914068. Путем расчета методом сравнения со стандартной кривой концентрация сиалитола была установлена на уровне 7,96 мкг/мл. В параллельном эксперименте наблюдалась концентрация 8,05 мкг/мл. Среднее значение результатов двух анализов составляло 8,005 мкг/мл. Поскольку перед анализом образцы разбавляли в 10 раз, исходная средняя концентрация сиалитола составляла 80,05 мкг/мл. Колориметрическое определение общего содержания сиаловой кислоты показало концентрацию 241,09 мкг/мл. Принимая во внимание небольшое различие масс между сиаловой кислотой и сиалитолом, эти концентрации переводили в молярные концентрации (на самом деле, различие масс столь мало, что превосходное приближение достигается и без перевода в моли), и рассчитанное мольное отношение составляло 3 (т.е. DP=3). Отношения, рассчитанные по результатам двух различных параллельных анализов, принимали следующие значения:
(мкг/мл)
(мкг/мл)
Воспроизводимость методики измерения содержания сиалитола оценивали путем анализа одного образца MenW135 в 4 воспроизведениях с использованием трех различных улавливающих бораты предколонок. Были получены следующие результаты:
Таким образом, результаты свидетельствовали о хорошей воспроизводимости (CV%<2%).
Раствор 10 мг/мл полноразмерного CPS MenY или MenW135 в 0,01 М уксусной кислоте нагревали до 70-80°С. Во время гидролиза для определения среднего значения DP с целью слежения за ходом реакции вплоть до временной точки 6 часов отбирали образцы. Образцы быстро замораживали и содержали при -20°С до повторного анализа с использованием колонки lon-Рас AS11. Были получены следующие результаты:
Таким образом, измерения DP свидетельствовали о постепенном снижении значения DP с течением времени (фиг.15). Подтверждение деполимеризации было получено с помощью хроматографического анализа lonPac AS11, который свидетельствовал о том, как росло содержание низкомолекулярных олигосахаридов с течением времени при кислотном гидролизе, как показано на фиг.16 (MenW315) и 17 (MenY), причем 16А/17А относятся к нулевой временной точке, а 16 В/17 В относятся к временной точке 6 часов.
Образец сахарида серогруппы W135
Получали капсульный сахарид серогруппы W135. При получении измеряли его DP в соответствии с описанными здесь методиками. Хроматограмма 100-кратного разведения этого вещества приведена на фиг.21 В, а хроматограмма стандарта в концентрации 6 мкг/мл приведена на фиг.21А. Для элюции в обоих случаях использовали 100 мМ ацетат натрия и 20 мМ NaOH, и результаты показаны для элюции с линейным ростом объема элюирующего буфера с 10% до 30% в течение 30 минут с финальным скачком объема элюирующего буфера до 100% в течение 10 минут.
Было показано, что при анализе стандарта сиалитол элюируется через 16,383 минут; в образце пик наблюдался через 16,350 минут.
Результаты двух раздельных анализов одного образца и пяти стандартных образцов приведены ниже вместе с расчетной концентрацией сиалитола:
Судя по среднему значению результатов анализов (а) и (b) в образце содержалось 3,339 мкг/мл сиалитола. Учитывая первоначальное разведение, исходная концентрация сиалитола составляла 333,9 мкг/мл. Измеренное значение общего содержания сиаловой кислоты составляло 5732,6 мкг/мл, что давало значение DP 17,2.
Анализ сахарида серогруппы С
Очищенный олигосахарид МеnС с DP 5 получали, как описано ранее [5]. Анализ ESI MS проводили в режиме определения положительных ионов. Масс-спектр приведен на фиг.18, где видны три основные группы ионов. Подробное изучение пиков наибольшей интенсивности (856-941 m/z) свидетельствовало о том, что они соответствовали пентасахаридам с двойным зарядом, тогда как пики в интервале 1733-1826 m/z соответствовали пентасахаридам с одинарным зарядом, отличающимся друг от друга количеством O-ацетильных заместителей и натрия в качестве противоионов.
Значение DP олигосахаридов МеnС с DP 5 определяли в соответствии со способами по изобретению, а хроматограмма, полученная в результате анализа, приведена на фиг.19. Были проведены четыре раздельных анализа олигосахаридов, и были получены следующие результаты:
Заключение
Размер молекул сахаридов представлял собой важную проблему в разработке известных из уровня техники конъюгированных вакцин [6, 7], причем олигосахариды со средней длиной цепи проявляли лучшую иммуногенность. Были проведены получение, выделение и определение свойств промежуточных олигосахаридов MenW135 и MenY, причем первоначальную деполимеризацию капсульного полисахарида вызывает кислотный гидролиз [79]. Изобретение относится к новому хроматографическому способу определения степени полимеризации этих олигосахаридов, и способ характеризуется высокой точностью и достоверностью, подтвержденными результатами анализа ЯМР и ESI-MS. Более того, способ может быть также использован для определения значения DP олигосахаридов серогруппы С.
С дополнительными подробностями проведения экспериментов можно ознакомиться в ссылке 85.
Следует понимать, что изобретение описано исключительно в иллюстративных целях и могут быть сделаны модификации, подпадающие под объем и сущность изобретения.
Ссылки
(содержание которых включено в настоящее описание посредством ссылки)
[1] Vaccines (eds. Plotkin et al.) 4th edition, ISBN: 0721696880.
[2] Baker et al. (2003) J Infect Dis 188:66-73.
[3] Theilacker et al. (2003) Infect Immun 71:3875-84.
[4] Анонимное сообщение (2003) Drugs R D 4:383-5.
[5] Ravenscroft et al. (1999) Vaccine 17:2802-2816.
[6] Paoletti et al. (1992) J Clin Invest 89:203-9.
[7] Anderson et al. (1986) J Immunol 137:1181-6.
[8] Jones (2001) Curr Opin Investig Drugs 2:47-49.
[9] Corbel (1996) Dev Biol Stand 87:113-124.
[10] WO 03/080678.
[11] Costantino etal. (1999) Vaccine 17:1251-63.
[12] D'Ambra et al. (1997) Anal Biochem 250:228-36.
[13] Ravenscroft et al. (2000) Dev Biol (Basel) 103:35-47.
[14] Ashwell et al. (1994) Anal Biochem 222:495-502.
[15]WO 2005/033148.
[16] Hallenbeck et al. (1987) J Biol Chem 262(8):3553-61.
[17] Jumel et al. (2002) Biotechnol Appi Biochem 36:219-226.
[18] Hardy et al. (1988) Anal Biochem 170:54-62.
[19] Wang et al. (1990) Anal Biochem 190:182-187.
[20] Ramsay et al. (2001) Lancet 357(9251): 195-196.
[21] Lindberg (1999) Vaccine 17 Suppi 2:S28-36.
[22] Buttery & Moxon (2000) JR Coil Physicians Lond 34:163-168.
[23] Ahmad & Chapnick (1999) Infect Dis Clin North Am 13:113-133, vii.
[24] Goldblatt (1998) J. Med. Microbiol. 47:563-567.
[25] Европейский патент №0477508.
[26] Патент США №5306492.
[27] WO 98/42721.
[28] Conjugate Vaccines (eds. Cruse et al.) ISBN 3805549326, particularly vol. 10:48-114.
[29] Hermanson (1996) Bioconjugate Techniques ISBN: 0123423368 or 012342335X.
[30] Патент США №4761283.
[31] Патент США №4356170.
[32] WO 00/10599.
[33] Gever et al. Med. Microbiol. Immunol, 165: 171-288 (1979).
[34] Патент США №4057685.
[35] Патенты США №№4673574; 4761283; 4808700.
[36] Патент США №4459286.
[37] Патент США №4965338.
[38] Патент США №4663160.
[39] Анонимное сообщение (Jan 2002) Research Disclosure, 453077.
[40] Anderson (1983) Infect Immun 39(1):233-238.
[41] Anderson et al. (1985) J Clin Invest 76(1):52-59.
[42] EP-A-0372501.
[43] EP-A-0378881.
[44] EP-A-0427347.
[45] WO 93/17712.
[46] WO 94/03208.
[47] WO 98/58668.
[48]EP-A-0471177.
[49] WO 91/01146.
[50] Falugi et al. (2001) Eur J Immunol 31:3816-3824.
[51] EP-A-0594610.
[52] WO 00/56360.
[53] WO 02/091998.
[54] WO 01/72337.
[55]WO 00/61761.
[56] WO 99/42130.
[57] WO 96/40242.
[58] PCT/IB2005/000987.
[59] WO 02/09643.
[60] Katial et al. (2002) Infect Immun 70:702-707.
[61] WO 001/52885.
[62] Европейский патент №0301992.
[63] Bjune et al. (1991) Lancet 338(8775): 1093-1096.
[64] Fukasawa et al. (1999) Vaccine 17:2951-2958.
[65] WO 02/09746.
[66] Rosenqvist et al. (1998) Dev. Biol. Stand. 92:323-333.
[67] Watson (2000) Pediatr Infect Dis J 19:331-332.
[68] Rubin (2000) Pediatr dm North Am 47:269-285, v.
[69] Jedrzejas (2001) Microbiol Mol Biol Rev 65:187-207.
[70] Bell (2000) Pediatr Infect Dis J 19:1187-1188.
[71] Iwarson (1995) APMIS 103:321-326.
[72] Gerlich et al. (1990) Vaccine 8 Suppl:S63-68 & 79-80.
[73] Gustafsson et al. (1996) N. Engl. J. Med. 334:349-355.
[74] Rappuoli et al. (1991) TIBTECH 9:232-238.
[75] Vaccines (1988) eds. Plotkin & Mortimer. ISBN 0-7216-1946-0.
[76] Del Guidice et al. (1998) Molecular Aspects of Medicine 19:1-70.
[77] Sutter et al. (2000) Pediatr Clin North Am 47:287-308.
[78] Zimmerman & Spann (1999) Am Fam Physician 59:113-118, 125-126.
[79] WO 03/007985.
[80] Svennerholm (1957) Biochem Biophys Acta 24:604-11.
[81] Lemercinier & Jones(1996) Carbohydr Res 296:83-96.
[82] Ip et al. (1992) Anal Biochem 201:343-349.
[83] Neeser & Schweizer (1984) Anal Biochem 142:58-67.
[84] Bierman. Hydrolysis and other cleavages of glycosidic bonds. In: Analysis of Carbohydrates by GLC and MS (Eds Bierman & McGinnis) CRC Press Inc., Boca Raton, Florida, 1989, pp.27-41.
[85] Bardotti et al. (2005) Vaccine 23:1887-99.



















Изобретение относится к способу измерения степени полимеризации капсульных полисахаридов, содержащих сиаловую кислоту. Способ предусматривает стадии восстановление концевого моносахаридного звена сиаловой кислоты с получением восстановленного моносахаридного звена сиаловой кислоты, гидролиз сахарида с получением гидролизата, содержащего моносахаридные звенья. Причем сахарид содержит моносахаридные звенья сиаловой кислоты, которые связаны α 2→9, и концевое моносахаридное звено сиаловой кислоты. Далее определяют отношение общего количества сиаловой кислоты к количеству восстановленной сиаловой кислоты в гидролизате. Изобретение позволяет измерять величину степени полимеризации сахаридов и проводить оценку качества вакцин, в состав которых входят сахариды, новым способом, характеризующимся высокой точностью и достоверностью. 5 н. и 8 з.п. ф-лы, 21 ил., 8 табл.
1. Способ измерения степени полимеризации капсульного сахарида, в котором (а) сахарид содержит моносахаридные звенья сиаловой кислоты, которые связаны α 2→9; (b) сахарид содержит концевое моносахаридное звено сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) восстановление концевого моносахаридного звена сиаловой кислоты с получением восстановленного моносахаридного звена сиаловой кислоты; (ii) гидролиз сахарида с получением гидролизата, содержащего моносахаридные звенья; (iii) определение отношения общего количества сиаловой кислоты к количеству восстановленной сиаловой кислоты в гидролизате.
2. Способ по п.1, в котором концевой остаток сиаловой кислоты восстанавливают путем инкубации сахарида с восстановителем.
3. Способ по п.2, в котором восстановитель представляет собой боргидрид натрия.
4. Способ по п.1, в котором стадию гидролиза проводят химически или ферментативно.
5. Способ по п.4, в котором используют кислотный гидролиз.
6. Способ по любому из предшествующих пунктов, в котором капсульный полисахарид представляет собой популяцию капсульных сахаридов различных размеров, и способ относится к средней степени полимеризации сахаридов.
7. Способ измерения степени полимеризации капсульного сахарида, в котором (а) сахарид содержит моносахаридные звенья сиаловой кислоты и отличные от сиаловой кислоты моносахаридные звенья; (b) сахарид содержит концевое моносахаридное звено сиаловой кислоты; и (с) способ предусматривает следующие стадии: (i) модификация концевого звена сахарида в виде сиаловой кислоты с получением модифицированного концевого звена сиаловой кислоты; (ii) гидролиз сахарида с получением гидролизата сахарида, содержащего звенья сиаловой кислоты, включая модифицированные концевые звенья сиаловой кислоты; (iii) определение количества звеньев сиаловой кислоты в гидролизате, включая модифицированные концевые звенья сиаловой кислоты; и (iv) использование количественных результатов определения на стадии (iii) для расчета степени полимеризации.
8. Способ измерения степени полимеризации сахарида(ов) в композиции, предусматривающий следующие стадии: (а) начало деполимеризации сахарида(ов) в композиции; и в одной или нескольких временных точках после этого (b) измерение значения DP сахарида(ов) в соответствии со способом по любому из предшествующих пунктов.
9. Способ по п.8, дополнительно предусматривающий стадию конъюгирования деполимеризованного сахарида с белком-носителем после химической активации при необходимости.
10. Способ по п.7, отличающийся тем, что сахарид относится к менингококкам серогруппы W135 или серогруппы Y.
11. Способ по п.10, в котором модификация на стадии (i) представляет собой восстановление концевого остатка сиаловой кислоты, в котором значение DP рассчитывают путем сравнения отношения общего количества сиаловой кислоты, определенного на стадии (iii), к количеству восстановленной сиаловой кислоты.
12. Способ анализа гликоконъюгата, содержащего сахарид и носитель, предусматривающий следующие стадии: (а) обработка гликоконъюгата для высвобождения сахарида с носителя; и (b) измерение значения DP высвобожденного сахарида в соответствии со способом по любому из предшествующих пунктов.
13. Способ приготовления вакцинной композиции, предусматривающий следующие стадии: (а) проведение анализа DP капсульного сахарида в соответствии со способом по любому из пп.1-11; (b) конъюгирование прошедшего анализ DP сахарида с одним или несколькими белками-носителями; (с) при необходимости анализ рН и/или других свойств нерасфасованной вакцины; и, если результаты стадии (с) свидетельствуют о приемлемости нерасфасованной вакцины для клинического применения, (d) приготовление из нерасфасованной партии и упаковка вакцины для использования у человека.
| RAVENSCROFT N ВТ AL: "Size determination of bacterial capsular oligosaccharides used to prepare conjugate vaccines", Vaccine, Butterworth Scientific, Guilford, GB, vol.17, no.22, 16.07.1999, pages 2802-2816 | |||
| WO 0308678 A1, 02.10.2003 | |||
| WO 03007985 A2, 30.01.2003. |
Авторы
Даты
2010-10-10—Публикация
2005-05-23—Подача