Изобретение относится к микробиологической промышленности и касается получения органических растворителей - бутанола, ацетона и этанола путем биосинтеза углеводсодержащих материалов.
Наиболее ценным из перечисленных растворителей является бутанол.
Бутанол - это дорогостоящий органический растворитель, широко применяется при изготовлении нитролаков и масляных лаков, в производстве сложных растворителей, синтетической резины и шелка, при экстрагировании фармацевтических препаратов, служит сырьем для производства практически всех пластмасс и их растворителей, поэтому на рынке химических реактивов и веществ имеет постоянно большой спрос.
Органические растворители могут быть использованы также и в качестве биотоплива.
При этом бутанол обладает целым рядом преимуществ перед этанолом. По сравнению с этанолом бутанол может быть смешан в более высоких пропорциях с бензином и может использоваться в существующих двигателях автомобилей без модификации системы формирования воздушно-топливной смеси. Бутанол выделяет чистой энергии на рабочий цикл больше, чем этанол или метанол, и примерно на 10% больше, чем бензин.
Бутиловый спирт (бутанол) С4Н9OН - бесцветная жидкость с характерным запахом сивушного масла. Известны нормальный первичный бутиловый спирт СН3(СН2)3ОН, нормальный вторичный бутиловый спирт СН3СН2СН2(ОН)СН3, изобутиловый спирт (СН3)2СНСН2OН, триметилкарбинол (СН3)3СОН.
В промышленности бутанол получают оксосинтезом из пропилена с использованием никель-кобальтовых катализаторов при 130-150°С и давлении 20-35 МПа.
В настоящее время в связи с появлением новых экономичных технологий производства резко возрос интерес к получаемому микробиологическим путем бутанолу и его использованию в качестве биотоплива.
Основными направлениями исследований сейчас в области получения органических растворителей и биотоплива в Великобритании, США, Германии, Китае и Японии являются конструирование новых штаммов ацетонобутиловых бактерий методами генной инженерии, повышение продуктивности процесса биосинтеза и разработка новых технологических приемов выделения конечных целевых продуктов (US 2007259411 2007-11-08, US 2007259410 2007-11-08, WO 2007050671 2007-05-03).
Усовершенствования известных отечественных технологий в ацетоно-бутиловом производстве касались, как правило, создания новых штаммов, обеспечивающих повышение выхода целевых продуктов, главным образом, бутанола, как наиболее ценного из них (RU 2080382 1997.05.27).
Бутанол начал производиться в 10-х годах XX века микробиологическим путем с использованием бактерии вида Clostridium acetobutylicum. Сырьем для производства была глюкоза сахарного тростника, свеклы, кукурузы, пшеницы, маниоки, т.е. пищевое сырье.
Известно, что бактерии вида Clostridium acetobutylicum при сбраживании различных углеводов синтезируют одновременно три целевых продукта: бутанол, ацетон и этанол, процентное соотношение которых примерно 60:30:10 (соответственно). Это соотношение не является строго постоянным и может незначительно изменяться в сторону увеличения выхода того или иного продукта в зависимости от условий брожения или состава сырья, используемого для брожения.
Так, при культивировании на мучных средах различные штаммы Clostridium acetobutylicum синтезируют общее количество растворителей, составляющие 18-19 г/л (Корнеева О.С., Жеребцов Н.А. и др. Роль амилолитических ферментов Clostridium acetobutylicum в биосинтезе растворителей. Биотехнология, 1986 г. №3, стр.133-136).
Известен способ повышения продуктивности процесса при периодическом культивировании бактерий вида Clostridium acetobutylicum на мучных средах за счет предварительного разжижения крахмала рециркулируемой бражкой, содержащей активные амилолитические ферменты. При этом общий выход растворителей повышается, а время брожения сокращается (а.с. SU 160485, 21.12.88).
Вышеописанные способы обладают всеми недостатками периодических процессов, а главное не предполагают возможности использования непищевых возобновляемых источников сырья, таких как солома, отходы деревообрабатывающих производств и т.п.
Целлюлоза самый распространенный углевод в биосфере, она составляет основную часть всей растительной биомассы, ее гидролиз играет главную роль в обмене углерода в атмосфере. Несмотря на простой химический состав, целлюлоза имеет множество топологий: кристаллические, аморфные и переходные. Ее нерастворимость в воде и гетерогенность определяет низкую возможность воздействия кислых катализаторов и делает целлюлозу устойчивой к ферментативному гидролизу, несмотря на ее гомогенный химический состав. В настоящее время принято считать гидролиз кристаллической целлюлозы нерешенной биохимической задачей.
При этом установлено, что примерно три четверти от миллионов тонн биомассы, получаемой на культивированных землях и пастбищах и в процессе переработки древесины, превращается в отходы. Эти отходы давно стремились использовать для создания альтернативных источников горючего, химических продуктов и других полезных веществ. Однако опыты по гидролизу целлюлозы до сих пор не привели к созданию экономически эффективного способа производства сахаров в больших количествах, что главным образом определено высокой степенью кристаллизации структуры целлюлозы и наличием в ней лигнина.
Процессы гидролиза целлюлозы включают биологические и небиологические способы деполимеризации. В биологических способах используются ферменты целлюлозы. Среди небиологических способов традиционным и наиболее известным в производстве сахаров из целлюлозы является гидролиз в среде кислоты.
Известен способ сбраживания сахаров для получения органических соединений, например этанола, включающий измельчение рисовой соломы до частиц размером от 3 до 7 мм, декристаллизацию получаемых материалов путем смешивания их с раствором, содержащим 25-90% серной кислоты по весу, отделение жидкости, полученной в результате гидролиза, путем пропускания через слой катионообменной смолы, при этом сахар адсорбируют на слое смолы, а кислоту выводят в виде потока жидкости с содержанием сахара менее 2%; ферментацию сахаров с использованием микроорганизмов в течение от 3 до 5 дней, удаление испаряющихся продуктов брожения путем рециркуляции двуокиси углерода через охлаждаемую колонну-конденсатор, отделение микроорганизмов от оставшихся продуктов брожения и дистилляцию продуктов брожения.
При этом в качестве микроорганизмов могут быть выбраны дрожжи, выбранные из группы, состоящей из Candida kefyr, Dichia stipitis, штаммов с респираторной недостаточностью Saccharonujces cerevisiae, Hansenula anomala, Hansenula jadinii, Hansenula fabianii u Pachysolen tannophilus или бактерии, выбранные из группы, включающей виды Clostridium, виды Acetobacter, виды Lactobacillus, виды Aspergillus, виды Propionibacteria u Zymomonas mobilis (RU 2144087 25.03.94).
Основным недостатком известного способа является необходимость использования в процессе гидролиза серной кислоты, которая требует в дальнейшем обработки щелочью для нейтрализации и удаления образующегося осадка. Кроме того, процесс гидролиза проходит при высокой температуре, что ведет к разложению сахаров, с образованием фурфурола и других нежелательных побочных продуктов. Эти соединения препятствуют брожению и некоторые из них являются токсичными. В результате этого выход глюкозы очень низок. Кроме того, возникает необходимость в оборудовании, кислотостойком при высоких температурах.
Известно, что в процессе биосинтеза органических растворителей по мере накопления бутанола, этанола и ацетона происходит снижение активности биосинтезирующих микроорганизмов, т.к. органические растворители по мере их накопления в ферментере ингибируют процесс биосинтеза. С целью исключения подобного бутанол и другие органические растворители выводят из процесса.
Известен ферментационный способ получения бутанола и других органических растворителей, включающий сбраживание раствора сахаров в ферментере на питательной среде с использованием двух различных штаммов бактерий, отвод органических растворителей и газов, образующихся в процессе сбраживания и выделение целевых продуктов. Процесс подготовки сырья к сбраживанию в данном способе не описан.
Изобретение описывает процесс получения растворителей, протекающий в две стадии, за каждую из которых ответственны разные микроорганизмы. Первая стадия - производство масляной кислоты из раствора углеводов первым микроорганизмом, вторая стадия - производство бутанола из масляной кислоты вторым микроорганизмом.
Для первой стадии могут быть использованы штаммы анаэробных бактерий, таких как, например, Clostridium tyrobutyricum, С.thermobutyricum, для второй стадии чаще всего используются штаммы таких микроорганизмов, как, например, Clostridium acetobutylicum, С.beijerinkii.
Бутанол и другие органические соединения извлекаются из второго реактора активированными сорбентами или с помощью мембран (US 5753474, 1988 г.).
Известен способ получения бутанола и других органических растворителей, включающий сбраживание углеводсодержащих сред с помощью бактерий, продуцирующих бутанол, ацетон, этанол и/или изопропанол, отвод органических растворителей и газов, образующихся в процессе сбраживания и выделение целевых продуктов. В процессе сбраживания на первой стадии в основном происходит непрерывное размножение бактерий, а на второй, проводимой непрерывно или периодически, образуется целевой продукт. Образующиеся на второй стадии продукты отводят из среды путем диффузионного испарения, используя для этой цели перфузионную мембрану, в частности из силиконового каучука. Процесс подготовки сырья к сбраживанию в данном способе также не описан (RU 2044773, 1989 г.).
Основные недостатки описанных выше способов связаны со сложностями выделения органических растворителей из культуральной среды, поскольку это наиболее энергоемкое и дорогостоящее звено в технологии их получения. Сегодня известно немало способов выделения спиртов из гетерогенной среды:
- дистилляция - перегонка через паровую фазу см. «Касаткин А.Г., Основные процессы и аппараты химической технологии, 8 изд., М., 1971»;
- разделение на мембранах см. «Хванг С.-Т., Каммермайер К. Мембранные процессы разделения. М.: Химия, 1981» или «Шапошник В.А. Мембранная электрохимия // Соросовский Образовательный Журнал. 1999. №2. С.71-77»;
- сепарация с помощью сорбентов «Zolotov Yu.A., Kuz'min N.M. Preconcentraion in Inorganic Analysis. Amsterdam: Elsevier, 1990»;
- вымораживание «Пап Л., Концентрирование вымораживанием, М., 1982».
Недостатками всех известных способов выделения спиртов является высокая энергоемкость и необходимость относительно частой замены или восстановления исходных свойств функциональных элементов - мембран или твердых сорбентов.
Примером производства органических растворителей с использованием ферментов целлюлозы может служить способ, включающий подготовку растительного сырья, ферментолиз подготовленного сырья до получения раствора сахаров путем обработки его ферментами, сбраживание раствора сахаров в ферментере на питательной среде с помощью бактерий, продуцирующих бутанол, ацетон и этанол, отгонку органических растворителей и газов, образующихся в процессе сбраживания, подпитку растворами углеводов и минеральных солей во время сбраживания и выделение целевых продуктов (US 2005233423 2005-10-20).
Там же описана установка для производства органических растворителей, содержащая устройство для грубого помола углеводсодержащего сырья, устройство для ферментолиза полученной суспензии, ферментер для сбраживания раствора сахаров и устройство для отгонки органических растворителей и газов, образующихся в процессе сбраживания.
Продукт, полученный известным способом, на известной установке, имеет соотношение растворителей 30:60:10.
В известном способе и установке ферментолиз подготовленного сырья осуществляют без учета его полисахаридного состава, в данном источнике не описана возможность использования в качестве сырья отходов деревоперерабатывающей промышленности, и в частности, щепы хвойных пород деревьев с высоким содержанием смолы; в качестве предварительной обработки растительного сырья упомянут «паровой взрыв», требующий повышения температуры до 240°С, что приводит к разложению сахаров, выделению фурфурола и т.п. продуктов; время обработки сырья длительное, до 120 часов.
Технической задачей настоящего изобретения является создание способа получения органических растворителей, лишенного недостатков вышеописанных способов и обеспечивающего возможность создания непрерывного процесса с использованием непищевого возобновляемого растительного сырья, в частности отходов деревоперерабатывающей промышленности, уменьшение времени подготовки сырья, увеличение продуктивности процесса при одновременном снижении энергопотребления на стадии выделения целевых продуктов, получение продукта в соответствии с описанным способом, а также создание установки, реализующей указанный способ.
Для решения этой задачи предложен способ получения органических растворителей, включающий подготовку растительного сырья, ферментолиз подготовленного сырья до получения раствора сахаров путем обработки его ферментами, сбраживание раствора сахаров в ферментере на питательной среде с помощью бактерий Clostridium acetobutylicum, продуцирующих бутанол, ацетон и этанол, отгонку органических растворителей и газов, образующихся в процессе сбраживания, подпитку растворами углеводов и минеральных солей во время сбраживания и выделение целевого продукта, при этом подготовка растительного сырья включает в себя грубый помол сырья и последующий тонкий помол, при ферментолизе используют комплекс ферментов, соответствующий полисахаридному составу используемого сырья, а процесс сбраживания ведут с преимущественным синтезом бутанола посредством периодического понижения давления в ферментере с одновременной отгонкой образующихся растворителей.
Грубый помол растительного сырья осуществляют до размеров частиц 1-2 мм на пригодных для такого процесса мельницах, например шаровых, предпочтительно одновременно с сушкой, путем продувки воздухом с температурой 120-130°С, что позволяет удалить влагу из сырья и подготовить его к тонкому помолу.
Тонкий помол растительного сырья осуществляют до размеров частиц 1-5 мкм, до изменения его агрегатного состояния, близкого к аморфному, что позволяет улучшить перемешивание с водой, используя соотношение 1:6, а не 1:10, как того требует необработанное сырье, и увеличить таким образом биодоступность растительного сырья на стадии ферментолиза.
Предпочтительно осуществлять тонкий помол растительного сырья в вибрационных, струйных и коллоидных мельницах, обеспечивающих усилие сдвига при помоле, что, как показали исследования авторов, обеспечивает механоактивацию сырья.
Хотя в предлагаемом способе могут быть использованы любые возобновляемые источники растительного сырья, такие, например, как солома, травяные растительные отходы и т.п., но преимуществом предлагаемого способа является возможность использования отходов деревоперерабатывающей промышленности - древесных опилок.
В качестве опилок возможно использование наиболее трудно ферментализуемых опилок деревьев хвойных пород.
Перед тонким помолом древесных опилок из них предпочтительно удаляют смолу, что дает возможность осуществить полный ферментолиз целлюлозы, поскольку в противном случае в силу гидрофобности часть ферментов садится на смолу и не участвует в процессе ферментолиза.
Удаление смолы предпочтительно осуществляют экстракцией органическими растворителями, ацетоном и/или этанолом с модулем 1:7-1:10.
В качестве комплекса ферментов при получении раствора сахаров предпочтительно использовать комплекс ферментов целлюлазы, ксиланазы и целлобиазы, соответствующий полисахаридному составу сырья.
При этом в качестве ферментного препарата предпочтительно использовать культуральную жидкость, полученную культивированием грибов Penicillium verruculosum, а процесс предпочтительно вести при рН=4,0-6,0 и Т=50-55°С, что позволяет исключить процесс разложения сахаров.
Использование данного комплекса ферментов позволяет почти полностью разложить сахара древесины.
Перед сбраживанием от раствора сахаров отделяют лигнин, а раствор сахаров концентрируют до 25-40%, с целью предотвращения контаминации.
Поскольку наиболее ценным среди органических растворителей является бутанол, существует множество патентов, описывающих способы получения органических растворителей, целью которых является повышение выхода бутанола. Продуктивность процесса - выход бутанола из углеводов (вес продукта на единицу веса углеводов) в известных способах получения органических растворителей составляет примерно 22-23 г/л, тогда, как продуктивность процесса в предлагаемом способе доходит до 27 г/л.
Многочисленные исследования, проводимые авторами, подтвердили, что возможно в процессе биосинтеза органических растворителей изменять соотношение растворителей в получаемой смеси в сторону увеличения бутанола за счет его преимущественного синтеза.
Возможным объяснением вышеописанного является эффект воздействия переменного давления на биологические системы, что влечет за собой изменение микроокружения клеточных мембран, приводящее к нарушению процессов переноса веществ через мембраны, изменению скоростей ферментативных процессов в клетке, возникновению и развитию репаративных реакций, сопровождаемых новыми синтезами. (Акопян В.Б., Коржевенко Г.Н., Шангин-Березовский Г.Н., Скрытый резерв роста и развития живых систем. Вестник сельскохозяйственной науки, 1988, №4, (380), с.96-105).
Как показали исследования авторов, предпочтительно начинать понижение давления в процессе сбраживания при достижении уровня концентрации бутанола в ферментере, приближающейся к токсической для продуцирующей культуры, а более конкретно, по достижению уровня концентрации бутанола в культуральной среде - 0,6-1,2%.
Процесс понижения давления в ферментере предпочтительно продолжать до достижения уровня концентрации бутанола в культуральной среде - 0,5-0,2%.
Давление в ферментере во время отгонки предпочтительно поддерживать в интервале - 0,90-0,94 кг/см2.
Интервал между понижениями давления по исследованиям авторов составляет 0,5-10 часов.
Интересным является тот факт, что соотношение образующихся растворителей, зафиксированное во время понижения давления (и соответственно при повышенной скорости синтеза - наибольший выход бутанола), сохраняется таковым и в течение последующих 20 часов после предыдущего понижения давления, а это значит, что усиление процесса биосинтеза растворителей с повышенным содержанием бутанола во время понижения давления не прекращается и после его нормализации.
Бактерией, продуцирующей бутанол, ацетон и этанол в описываемом способе, является бактерия вида Clostridium acetobutylicum, а в качестве питательной среды возможно использование, например, картофельно-глюкозной среды, имеющей следующий состав, г/л: картофель - 37, глюкоза - 0,75, СаСО3 - 0,3, (NR4)2SO4 - 0,225.
Дальнейшее разделение целевых продуктов допустимо осуществлять одним из известных и применимых в данном случае способов, например, ректификацией.
Для решения вышеуказанной технической задачи и реализации описанного способа предложена установка, содержащая устройство для грубого помола углеводсодержащего сырья, экстрактор для отделения смолы, устройство для тонкого помола сырья, смеситель для смешивания измельченного сырья с водой, устройство для ферментолиза полученной суспензии, ферментер для сбраживания раствора сахаров, вакуум-насос, концентратор, дображиватель и устройство для разделения целевых продуктов.
Предпочтительно, устройство для грубого помола углеводсодержащего сырья выполнять в виде шаровой мельницы с продувкой воздухом с температурой 120-130°С.
Предпочтительно, устройство для тонкого помола сырья выполнять в виде вибрационной или струйной или коллоидной мельницы.
Предпочтительно, устройство для разделения целевых продуктов выполнять в виде ректификационной колонны.
Заявитель защищает также продукт, полученный способом по п.1.
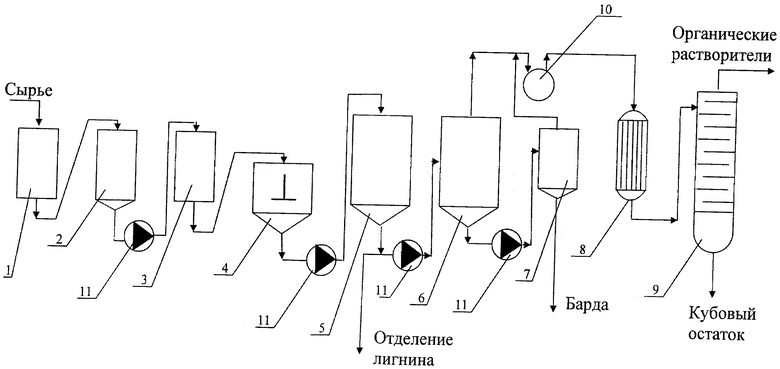
Схематично предлагаемая установка изображена на чертеже и содержит последовательно установленные устройство для грубого помола углеводсодержащего сырья 1, экстрактор для отделения смолы 2, устройство для тонкого помола сырья 3, смеситель для смешивания измельченного сырья с водой 4, устройство для ферментолиза полученной суспензии 5, ферментер для сбраживания раствора сахаров 6, дображиватель 7, концентратор 8, устройство для разделения целевых продуктов 9, вакуум-насос 10 и насосы 11.
Предлагаемый способ получения органических растворителей с помощью описываемой установки осуществляют следующим образом.
Углеводсодержащее сырье, предпочтительно древесные опилки, предварительно подвергают грубому помолу до размеров 1-2 мм в устройстве для грубого помола 1, экстрагируют и отделяют смолу в экстракторе 2, опилки подвергают дальнейшему тонкому измельчению с механоактивацией до размеров частиц 1-5 мкм в устройстве для тонкого помола 3, смешивают полученную пыль с водой в смесителе 4, осуществляют ферментолиз полученной суспензии для трансформации целлюлозы в сахара в устройстве для ферментолиза 5, отделяют образующийся лигнин, а раствор сахаров направляют в ферментер 6, где сахара подвергаются биотрансформации в ацетон-бутанол-этанольную смесь, а также в выделяющиеся при этом газы СО2 и Н2. В ферментер 6 вносят подготовленную стандартным способом углеводо-минеральную смесь (раствор минеральных солей, необходимый набор витаминов и один из следующих источников углерода: глюкозу, маннозу, ксилозу, галактозу или их смесь; или ферментолизат непищевых полисахаридов растений), в концентрации 2-4%; затем вносят инокулят бактерий, например, Clostridium acetobutylicum, BKM B-2531D с плотностью клеток 1-109 кл/мл. Через 30 мин после засева начинается интенсивное выделение газов брожения, через 5-6 часов - синтез органических кислот и на 10-12 часах - начинается синтез органических растворителей, скорость которого достигает максимума к 28-36 часу. В это время концентрация клеток бактерий в ферментере 6 также максимальна - 3·109 кл./мл суспензии. В это же время начинают понижение давления в ферментере 6 с помощью вакуум-насоса 10 и отгонку органических растворителей из культуральной среды до содержания бутанола 0,5-0,2% и одновременную подачу в ферментер раствора углеводов и минеральных солей, поддерживая необходимую концентрацию углеводов ферментере 6 и периодически, по достижению содержания бутанола - 0,6-1,2%, удаляя растворители из ферментера 6 и часть суспензии, чтобы скорость протока была в пределах 0,025-0,035 час-1. Процесс продолжают в непрерывном режиме в течение 500 часов, хотя ограничений по времени культивирования и синтезу растворителей практически нет; полученный целевой продукт направляют в дображиватель 7, концентратор 8, и органические растворители окончательно разделяют с помощью ректификационной колонны 9. Для передачи текучих сред по установке используют насосы 11.
Изобретение поясняется примерами, которые не носят ограничивающего характера.
Пример 1. Известный способ осуществления процесса биосинтеза органических растворителей.
120 г предварительно измельченного зерна (обойная мука) смешивают с 2,4 л воды, стерилизуют и вносят в предварительно стерилизованный ферментер с рабочим объемом 3 л. Туда же вносят 300 мл инокулята, содержащего бактерии Clostridium acetobutylicum СК 425, регистрационный номер ВКПМ В-4786 с плотностью 1-2 млрд/мл. Осуществляют ацетон-бутанол-этаноловое брожение при температуре 37°С. Ферментацию продолжают в течение 72 часов. После 72 часов процесс ферментации прекращают и конденсацией отогнанных паров получают в среднем 250 мл раствора, содержащего 5% бутанола, 1,5% ацетона и 0,5% этанола с соотношением растворителей 30:60:10. Продуктивность процесса в среднем - 3 г/л/день.
Пример 2. 120 г предварительно измельченного зерна (обойная мука) смешивают с 2,4 л воды, стерилизуют и вносят в предварительно стерилизованный ферментер с рабочим объемом 3 л. Туда же вносят 300 мл инокулята, содержащего бактерии Clostridium acetobutylicum BKM B-2531D с плотностью 1-2 млрд/мл. Осуществляют ацетон-бутанол-этаноловое брожение при температуре 37°С.
При концентрации бутанола в среде 0,6%, снижают давление в ферментере на 0,5 часа до -0,94 кг/см2, что приводит к изменению соотношения ацетон-бутанол-этанол 30:60:10 (соотношение растворителей 15:80:5). Как только концентрация бутанола в среде достигает 0,2%, давление в ферментере повышают до атмосферного. Через 8 часов осуществляют повторное понижение давления на 0,5 часа до -0,94 кг/см2, что приводит к изменению соотношения ацетон-бутанол-этанол 90:9:1.
Конденсацией отогнанных паров во время всей ферментации получают в среднем 250 мл раствора, содержащего 6,5% бутанола, 2% ацетона и 0,75% этанола (соотношение растворителей 80:15:5).
После удаления бутанола и сопутствующих газов вводят в ферментер питательную среду с содержанием 50 г глюкозы. Продолжительность процесса 48-52 часа. Продуктивность процесса в среднем 8,5 г/л/ день.
Пример 3. Древесную щепу измельчают на шаровой мельнице до 1-2 мм и сушат в потоке горячего воздуха до влажности не более 10%. Полученные опилки измельчают на вибрационной мельнице, ВТсМ-5 (Институт химии твердого тела и механохимии СО РАН, Новосибирск), до размера 1-5 мкм. Полученную пыль суспендируют в воде и к полученной суспензии в соотношении 2,5 г/кг пыли добавляют комплекс гидролитических ферментов, представляющий собой лиофильно высушенную культуральную жидкость, полученную культивированием штамма Penicillium verruculosum BKM F-3984D (целлобиогидролазная активность сухого комплекса составляет 900-920 ед/г, эндоглюканазная активность - 14500-14900 ед/г, β-глюкозидазная активность - 1200-1250 ед/г, целлобиазная активность - 600-670 ед/г, ксиланазная активность - 23000-24000 ед/г, ксилоглюканазная активность - 7500-8200 ед/г). Процесс ферментолиза проходит при температуре 50°С и рН 5 и заканчивается через 12 часов, когда 40% сахаров переходит в раствор. Образующийся лигнин отделяют от раствора сахаров центрифугированием.
В предварительно стерилизованный ферментер с рабочим объемом 3 л вводят 2,5 л 4% раствора полученных сахаров и 300 мл инокулята, состоящего из муки (40 г/л), воды и бактерий Clostridium beijerinckii, регистрационный номер КМ МГУ №101 с плотностью 1-2 млрд/мл. Осуществляют непрерывное ацетон-бутанол-этаноловое брожение при температуре 37°С.
При концентрации бутанола в среде 1,0%, снижают давление в ферментере на 1 час до -0,90 кг/см2, что приводит к изменению соотношения ацетон-бутанол-этанол 30:60:10 (на соотношение растворителей 21:70:9). Понижение давления в ферментере обеспечивает испарение органических растворителей из ферментационной среды. Как только концентрация бутанола в среде достигает 0,4%, давление в ферментере повышают до атмосферного. Через 6 часов осуществляют повторное понижение давления на 1,0 час до -0,90 кг/см2, что приводит к повторному изменению соотношения ацетон-бутанол-этанол. Конденсацией отогнанных паров во время всей ферментации получают в среднем 250 мл раствора, содержащего 6,5% бутанола, 2% ацетона и 0,75% этанола (соотношение растворителей 90:9:1).
Процедуру снижения давления повторяют каждый раз при достижении концентрации бутанола в 1,0%. После удаления бутанола и сопутствующих газов вводят в ферментер питательную среду с содержанием 50 г глюкозы. Раз в три дня в питательную среду добавляют 28 г дрожжевого автолизата. Продуктивность процесса в среднем 10,0 г/л/ день.
Пример 4. Древесную щепу хвойных пород измельчают на шаровой мельнице до 1-2 мм и сушат в потоке горячего воздуха до влажности не более 10%. Из полученных опилок удаляют смолу экстракцией этанолом с модулем 1:10. Опилки отделяют от экстрагента на центрифуге, остатки экстрагента удаляют продувкой сухим паром.
Обессмоленные опилки с влажностью 3-4% измельчают на активационной, коллоидной мельнице, например ОГО-3, Новосибирск, до размера 1-5 мкм. Полученную пыль суспендируют в воде и к полученной суспензии в соотношении 2,5 г/кг пыли добавляют комплекс гидролитических ферментов, представляющий собой лиофильно высушенную культуральную жидкость, полученную культивированием штамма Penicillium verruculosum BKM F-3984D. Процесс ферментолиза проходит при температуре 50°С и рН 5 и заканчивается через 12 часов, когда 40% сахаров переходит в раствор. Образующийся лигнин отделяют от раствора сахаров центрифугированием.
В предварительно стерилизованный ферментер с рабочим объемом 3 л вводят 2,5 л 4% раствора полученных сахаров и 300 мл инокулята, состоящего из муки (40 г/л), воды и бактерий Clostridium acetobutylicum BKM B-2531D с плотностью 1-2 млрд/мл. Осуществляют непрерывное ацетон-бутанол-этаноловое брожение при температуре 37°С.
При концентрации бутанола в среде 1,2% снижают давление в ферментере на 0,8 часа до -0,90 кг/см2, что приводит к изменению соотношения ацетон-бутанол-этанол 30:60:10 на (соотношение растворителей 21:70:9). Понижение давления в ферментере обеспечивает испарение органических растворителей из ферментационной среды. Как только концентрация бутанола в среде достигает 0,5%, давление в ферментере повышают до атмосферного. Через 8 часов осуществляют повторное понижение давления на 0,8 часа до -0,90 кг/см2, что приводит к изменению соотношения ацетон-бутанол-этанол. Конденсацией отогнанных паров во время всей ферментации получают в среднем 250 мл раствора, содержащего 6,5% бутанола, 2% ацетона и 0,75% этанола (соотношение растворителей 90:9:1).
Процедуру снижения давления повторяют каждый раз при достижении концентрации бутанола в 0,8%. После удаления бутанола и сопутствующих газов вводят в ферментер питательную среду, с содержанием 50 г глюкозы. Раз в три дня в питательную среду добавляют 28 г дрожжевого автолизата. Продуктивность процесса в среднем 10,0 г/л/ день.
Преимущества предложенного способа, устройства для его осуществления и продукта, полученного описанным способом, состоят в следующем:
- возможность использования пищевых и непищевые источников сырья, особенно трудно гидролизуемых отходов древесины;
- возможность организации непрерывного процесса получения органических растворителей;
- сокращение времени обработки сырья на подготовительных стадиях;
- увеличение выхода сахаров в процессе ферментолиза;
- отсутствие гидролиза серной кислотой;
- уменьшение энергозатрат на стадии выделения целевых продуктов;
- уменьшение числа аппаратов и их габаритов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 2009 |
|
RU2405828C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 2009 |
|
RU2405827C2 |
| СПОСОБ ПОЛУЧЕНИЯ БУТАНОЛА | 2008 |
|
RU2404247C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ, ПРЕИМУЩЕСТВЕННО БУТАНОЛА | 2008 |
|
RU2375454C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 2009 |
|
RU2405829C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 2009 |
|
RU2405830C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ ИЗ ФЕРМЕНТАЦИОННЫХ СРЕД | 2009 |
|
RU2405831C2 |
| ШТАММ БАКТЕРИЙ Clostridium acetobutylicum - ПРОДУЦЕНТ БУТАНОЛА, АЦЕТОНА И ЭТАНОЛА | 2008 |
|
RU2381270C1 |
| ШТАММ БАКТЕРИЙ CLOSTRIDIUM ACETOBUTYLICUM-ПРОДУЦЕНТ Н-БУТИЛОВОГО СПИРТА И АЦЕТОНА | 1995 |
|
RU2080382C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ ИЗ НЕПИЩЕВОГО ВОЗОБНОВЛЯЕМОГО РАСТИТЕЛЬНОГО СЫРЬЯ | 2012 |
|
RU2539094C2 |
Способ получения органических растворителей предусматривает грубый помол растительного сырья и последующий тонкий помол. Осуществляют обработку подготовленного сырья комплексом ферментов, соответствующим полисахаридному составу используемого сырья, до получения раствора сахаров. Сбраживают раствор сахаров в ферментере на питательной среде с помощью бактерий, продуцирующих бутанол, ацетон и этанол. Осуществляют отгонку органических растворителей и газов, образующихся в процессе сбраживания. Во время сбраживания осуществляют подпитку растворами углеводов и минеральных солей. При этом процесс сбраживания ведут с преимущественным синтезом бутанола путем периодического понижения давления в ферментере с одновременной отгонкой образующихся растворителей. Проводят выделение целевого продукта. Также предложены установка для осуществления способа и продукт, полученный описанным способом. Изобретение позволяет использовать непищевое возобновляемое растительное сырье, уменьшить время подготовки сырья, увеличить продуктивность процесса. Продуктивность процесса составляет в среднем 8,5-10,0 г/л/день. 3 н. и 19 з.п. ф-лы, 1 ил.
1. Способ получения органических растворителей, включающий подготовку растительного сырья, ферментолиз подготовленного сырья до получения раствора сахаров путем обработки его ферментами, сбраживание раствора сахаров в ферментере на питательной среде с помощью бактерий, продуцирующих бутанол, ацетон и этанол, отгонку органических растворителей и газов, образующихся в процессе сбраживания, подпитку растворами углеводов и минеральных солей во время сбраживания и выделение целевого продукта, отличающийся тем, что подготовка растительного сырья включает в себя грубый помол сырья и последующий тонкий помол, при ферментолизе используют комплекс ферментов, соответствующий полисахаридному составу используемого сырья, а процесс сбраживания ведут с преимущественным синтезом бутанола посредством периодического понижения давления в ферментере с одновременной отгонкой образующихся растворителей.
2. Способ по п.1, отличающийся тем, что грубый помол растительного сырья осуществляют до размеров частиц 1-2 мм одновременно с сушкой путем продувки воздухом с температурой 120-130°С.
3. Способ по п.1, отличающийся тем, что тонкий помол растительного сырья осуществляют до размеров частиц 1-5 мкм.
4. Способ по п.1, отличающийся тем, что тонкий помол растительного сырья осуществляют в вибрационной, или струйной, или коллоидной мельнице.
5. Способ по п.1, отличающийся тем, что в качестве сырья используют древесные опилки.
6. Способ по п.5, отличающийся тем, что в качестве древесных опилок используют опилки деревьев хвойных пород.
7. Способ по п.6, отличающийся тем, что перед тонким помолом древесных опилок из них удаляют смолу.
8. Способ по п.7, отличающийся тем, что удаление смолы осуществляют экстракцией органическими растворителями, предпочтительно ацетоном и/или этанолом с модулем 1:7-1:10.
9. Способ по п.1, отличающийся тем, что в качестве комплекса ферментов при получении раствора сахаров используют комплекс ферментов целлюлазы, ксиланазы и целлобиазы, а процесс ведут при рН 4,5-6,0 и Т=50-55°С.
10. Способ по п.1, отличающийся тем, что перед сбраживанием от раствора сахаров отделяют лигнин.
11. Способ по п.1, отличающийся тем, что раствор сахаров концентрируют до 25-40%.
12. Способ по п.1, отличающийся тем, что понижение давления в процессе сбраживания начинают при достижении уровня концентрации бутанола в ферментере, приближающейся к токсической для продуцирующей культуры.
13. Способ по п.12, отличающийся тем, что понижение давления в ферментере начинают по достижению уровня концентрации бутанола в культуральной среде 0,6-1,2%.
14. Способ по п.1, отличающийся тем, что понижение давления в ферментере продолжают до достижения уровня концентрации бутанола в культуральной среде 0,5-0,2%.
15. Способ по п.1, отличающийся тем, что давление в ферментере во время отгонки поддерживают в интервале 0,90-0,94 кг/см2.
16. Способ по п.1, отличающийся тем, что бактерией, продуцирующей бутанол, ацетон и этанол, является бактерия вида Clostridium acetobutylicum.
17. Способ по п.1, отличающийся тем, что разделение целевых продуктов осуществляют ректификацией.
18. Установка для осуществления способа по п.1, содержащая устройство для грубого помола углеводсодержащего сырья, экстрактор для отделения смолы, устройство для тонкого помола сырья, смеситель для смешивания измельченного сырья с водой, устройство для ферментолиза полученной суспензии, ферментер для сбраживания раствора сахаров, вакуум-насос, дображиватель, концентратор и устройство для разделения целевых продуктов.
19. Установка по п.18, отличающаяся тем, что устройство для грубого помола углеводсодержащего сырья выполнено в виде шаровой мельницы с продувкой воздухом с температурой 120-130°С.
20. Установка по п.18, отличающаяся тем, что устройство для тонкого помола сырья выполнено в виде вибрационной, или струйной, или коллоидной мельницы.
21. Установка по п.18, отличающаяся тем, что устройство для разделения целевых продуктов выполнено в виде ректификационной колонны.
22. Продукт, полученный способом по п.1.
| US 2005233423 A1, 20.10.2005 | |||
| US 5753474 A, 19.05.1998 | |||
| СПОСОБ СБРАЖИВАНИЯ УГЛЕВОДСОДЕРЖАЩИХ СРЕД С ПОМОЩЬЮ БАКТЕРИЙ, ПРОДУЦИРУЮЩИХ БУТАНОЛ, АЦЕТОН, ЭТАНОЛ И/ИЛИ ИЗОПРОПАНОЛ, И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1989 |
|
RU2044773C1 |
Авторы
Даты
2010-12-10—Публикация
2008-12-29—Подача