Изобретение относится к медицине, конкретно к медицинской технике травматологии, ортопедии и нейрохирургии.
Травматические повреждения позвоночника - опорной основы организма - влекут за собой шлейф патологических последствий, включая тяжелые, судьбоносные для больного. Поэтому пристальное внимание ученых и клиницистов к этому разделу медицины оправдано и актуально.
Один из видов травматических повреждений позвоночника - компрессионный перелом тела позвонка, когда разнохарактерная дезинтеграция тела позвонка сопровождается снижением его высоты. В задачу хирурга входит восстановление целостности, формы и размеров позвонка в усложненных условиях высоких механических нагрузок органа и близости спинного мозга.
Известные решения пластики тела сломанного позвонка базируются на скреплении фрагментов после их репозиции с помощью различных технических средств, сколько-нибудь биосовместимых и прочностно надежных. Наиболее доступные и привычные в хирургической медицине металлические крепежные элементы (титан, нержавеющая сталь) - винты, штифты - по указанным характеристикам далеко не удовлетворяют требованиям.
Известен способ пластики тела сломанного позвонка (сокр. вертебропластики), включающий дистракцию позвонка, репозицию отломков, создание транспедикулярных (как правило, цилиндрических) глухих каналов, ориентированных поперек поверхностей разлома, и заполнение их самотвердеющим костным цементом [Leferink V.J., Zimmerman K.W., et al Thoracolumbar spinal fractures: radiological results of transpedicular fixation combined with transpedicular cancellous bone graft and posterior fusion in 183 patients // Eur Spine J. 2001 Dec; 10(6): 517-523].
Недостаток способа обусловлен низкой биосовместимостью костного цемента. При затвердевании он инкапсулируется. Не имея возможности интегрироваться с костной тканью, цемент малоадгезивен и в отдаленных сроках функционально ненадежен. При наличии микротрещин средней опорной колонны существует опасность проникновения неотвердевшего костного цемента в позвоночный канал и повреждения спинного мозга; при проникновении в диск развиваются асептические дисциты с выраженным болевым синдромом.
Известен способ вертебропластики с применением в качестве материала - заполнителя транспедикулярных каналов костной стружки [Мюллер М.Е., Альговер М., Шнайдер Р., Виллигер X. Руководство по внутреннему остеосинтезу (методика, рекомендованная группой АО) // Springer - Verlag, Москва, 1996]. Недостаток костной стружки в указанной функции - склонность к резорбции в отдаленные сроки, что также приводит к низкой надежности фиксации костных отломков, к снижению состоятельности операции, как главной характеристики способа. Недостаток усугублен для случаев использования способа при восстановлении поврежденных позвонков на фоне остеопороза.
По наибольшему сходству данного аналога с предлагаемым решением он выбран в качестве прототипа.
Технический результат предлагаемого изобретения - повышение состоятельности операции за счет повышения надежности скрепления отломков тела позвонка больного, страдающего остеопорозом.
Указанный технический результат достигается тем, что в способе пластики тела сломанного позвонка, включающем дистракцию позвонка, репозицию и скрепление отломков путем создания транспедикулярных глухих каналов, ориентированных поперек поверхностей разломов, и заполнения их гранулами биосовместимого остеообразующего материала для синтеза скрепляющих элементов, в качестве биосовместимого остеообразующего материала используют проницаемо-пористый никелид титана. Заполнение транспедикулярных каналов осуществляют последовательно, порционно от дистального (глухого) конца канала к его устью и механически утрамбовывают каждую порцию гранул мануальными усилиями оператора. При этом преимущественный размер гранул проницаемо-пористого никелида титана выбирают из интервала 0.5÷5.0 мм.
На участке транспедикулярного канала в зоне разлома тела позвонка предпочтительно трамбовать внедренный объем гранул мануальными усилиями, увеличенными на 20÷50% по сравнению с ординарными.
Предпочтительно пропитывать объем гранулированного проницаемо-пористого никелида титана до его внедрения в транспедикулярные каналы раствором антибиотика.
Предпочтительно заполнять каждый канал гранулами проницаемо-пористого никелида титана через воронку-концентратор с цилиндрическим наконечником длиной 1.5÷2.0 см и внешним диаметром, сопряженным с диаметром транспедикулярного канала для беззазорного и свободного перемещения.
Работоспособность способа обеспечивается всем комплексом хирургических действий и использованием проницаемо-пористого никелида титана в качестве матрикса при образовании остеоникелидтитанового композита. Процесс остеоинтеграции протекает следующим образом: после заполнения транспедикулярного канала уплотненным объемом гранул проницаемо-пористого никелида титана последний, как гигроскопический материал, энергично пропитывается физиологическими жидкостями организма, переносящими питательные вещества и метаболиты. Осуществляется питание костных клеток, мигрирующих из прилежащих костных тканей в пространство между гранулами и в их поры. Эти клетки колонизируются и впоследствии формируют костную ткань, армированную гранулами никелида титана. Синтезированный композит прочен и органически эластичен. Образованные им штифтообразные крепежные элементы надежно фиксируют отломки, не отторгаются и не резорбируют, не требуют их удаления в постоперационный период.
Достижимость технического результата, доминантой которого является состоятельность лечения травмированного позвонка на фоне остеопороза, обусловлена, главным образом, высокой биосовместимостью использованного материала. Никелид титана благодаря своим деформационным и химическим свойствам бесконфликтно взаимодействует с окружающими и вновь генерируемыми тканями. Высокая биосовместимость материала особенно важна для остеопорозных тканей, прочность которых ослаблена, а физиологические процессы аномальны. Под оптимальные условия взаимодействия имплантата с травмированной и остеопорозной тканью экспериментально подобраны режимы заполнения транспедикулярных каналов и размер гранул. При последовательном порционном заполнении каналов гранулами и мануальной трамбовке каждой порции достигается однородность создаваемого крепежного элемента и кратчайшие сроки остеоинтеграции. Воронка с цилиндрическим наконечником облегчает заполнение каналов гранулами, сокращает длительность операции в целом, что также способствует повышению ее состоятельности. Размеры наконечника воронки усреднены для типичных размеров позвонков и продиктованы методикой последовательного высвобождения наконечника из транспедикулярного канала по мере его заполнения гранулами.
Экспериментально определенные рациональные размеры гранул соответствуют максимальной прочности синтезированных скрепляющих элементов. При меньших размерах скрепляющие элементы охрупчиваются, заметно увеличивается их вес; большие размеры хуже вписываются в цилиндрическую форму транспедикулярного канала и не проходят через просвет воронки. Повышение усилий трамбовки на участке разлома предпочтительно для компрессионного внедрения гранул в зазор разлома для образования костной мозоли, как дополнительного элемента скрепления отломков.
Предварительное, до внедрения в каналы, пропитывание гранул никелида титана антибиотиком снижает возможность постоперационных осложнений.
Комплекс мероприятий, выраженных признаками формулы, повышает состоятельность предлагаемого способа по сравнению с прототипом, что особенно заметно для случаев осложнения травмы остеопорозом. Кроме того, обнаружено дополнительное позитивное действие указанных крепежных элементов, приводящее к расправлению поврежденного позвонка. Восстанавливается до нормы высота тела позвонка, снижаемая в результате компрессионного перелома в экстремальных случаях до одной трети.
Совокупность действий способа оригинальна для обозримого уровня техники, а логика их причинно-следственной связи выявлена в процессе исследований и для простого проектирования не очевидна. Эти факторы свидетельствуют о соответствии предложения критерию патентоспособности «изобретательский уровень».
На иллюстрациях представлено:
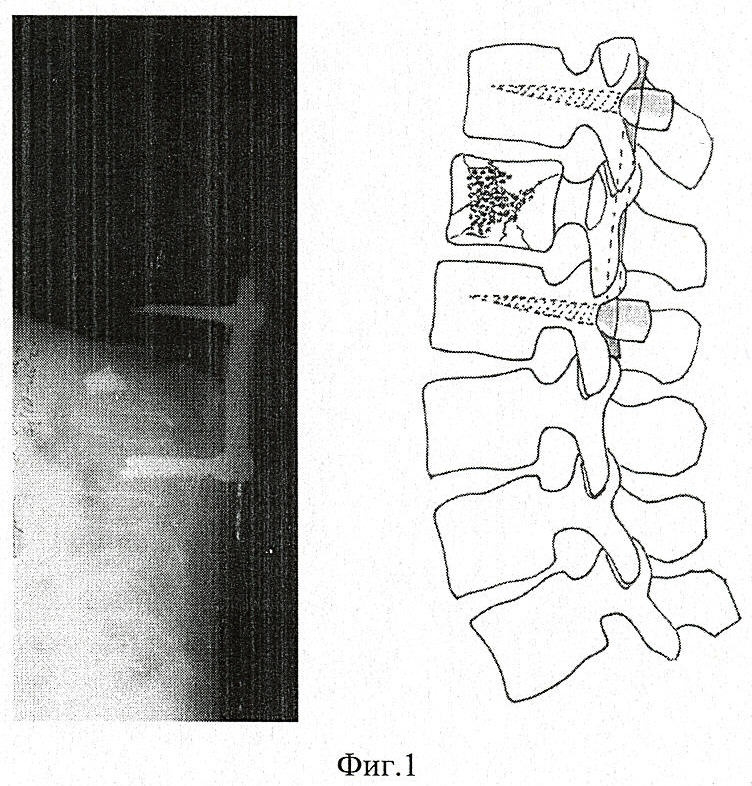
Фиг.1. Рентгенограмма позвоночника после внутренней транспедикулярной фиксации.
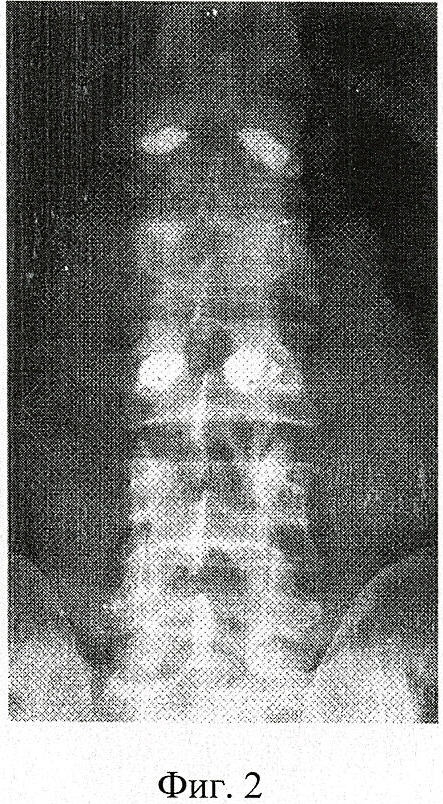
Фиг.2. Рентгенограмма позвоночника после удаления системы внутренней транспедикулярной фиксации.
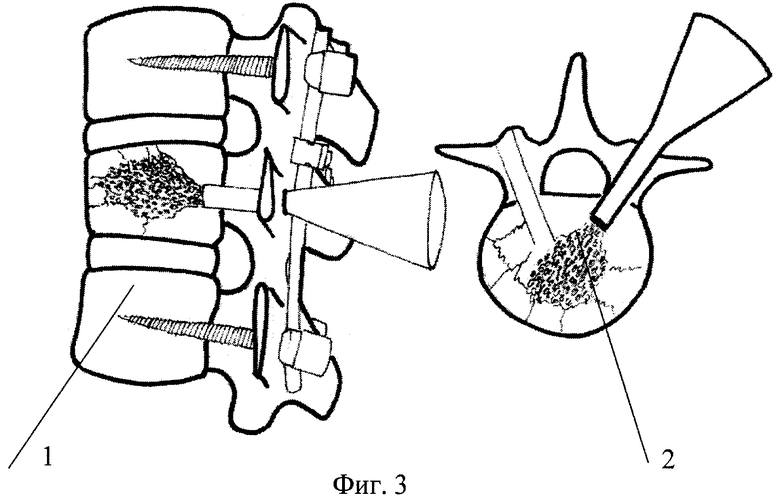
Фиг.3. Схема заполнения транспедикулярных каналов сломанного позвонка.
1 - боковая проекция, 2 - вид в разрезе.
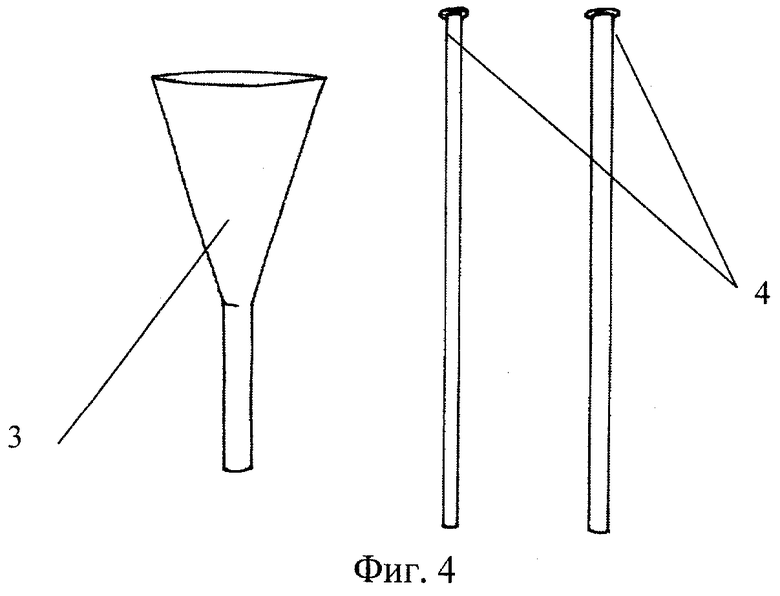
Фиг.4. Инструментарий для заполнения каналов и трамбовки внедренных объемов гранулированного никелида титана.
3 - воронка, 4 - трамбовочные стержни.
Достижимость технического результата после экспериментального лабораторного исследования на макетах проверена и подтверждена клиническими примерами лечения больных с переломами позвонков.
Пример 1
Больной Л., 68 лет, поступил в клинику с диагнозом «Закрытый компрессионный нестабильный неосложненный перелом тела и остистого отростка позвонка L1 2-й степени, перелом суставных отростков позвонка Th12, разрыв межостной связки позвонков L1-L2, в условиях остеопорозного снижения минеральной плотности костной ткани».
Больному проведена восстановительная операция в соответствии с методикой предлагаемого способа. В состав операции вошли: внутренняя транспедикулярная фиксация позвоночника на уровне позвонков Th12-L2, устранение кифотической деформации позвоночника путем создания лордоза на операционном столе, лигаментотаксис и дистракция поврежденного позвонка. Пластика сломанного позвонка проведена следующим образом.
Поперек поверхностей разлома тела позвонка с заходом от корней дужек выполнены глухие транспедикулярные каналы диаметром 5 мм и глубиной 25 мм с помощью подрезной и корончатой фрез. Через воронку 3 (фиг.4) каналы заполнены гранулами проницаемо-пористого никелида титана с распределением их поперечных размеров в интервале 0.5÷5.0 и преимущественным размером около 3 мм. Заполнение произведено последовательно, начиная с дистального (глухого) конца канала (фиг.3) к его устью, с трамбовкой каждой порции мануальными усилиями с помощью трамбовочных стержней 4 (фиг.4) легкими ударами молотка. На участке разлома (фиг.3) трамбовочные усилия увеличены по субъективным ощущениям и усадочной реакции объема гранул, внедряемых в зазор разлома. Процесс заполнения транспедикулярных каналов сопровождается визуально ощутимым расправлением позвонка, т.е. восстановлением его нормальной высоты. Устья каналов тампонированы гемостатической губкой. Общий объем внедренного в каналы материала составил около 4 г.
После операции больной активизирован в корсете на 6-е сутки. Послеоперационное рентгенологическое обследование свидетельствует о полном устранении кифотической деформации участка позвоночника и восстановлении высоты поврежденного позвонка.
Пример 2
Больной Е., 45 лет. Посттравматический диагноз с последствиями предыдущих хирургических вмешательств: закрытая черепно-мозговая травма - вдавленный перелом теменной кости слева, ушиб головного мозга средней степени, удаление вдавленного перелома (2006 г.), пластика дефекта черепа протакрилом (2007 г.); закрытый неосложненный компрессионный нестабильный вертикальный проникающий перелом тела позвонка L2, внутренняя транспедикулярная фиксация L1-L3 (2006 г.); закрытый оскольчатый перелом левой ключицы, остеосинтез ключицы спицей (2006 г.), удаление спицы (2007 г.). Сочетанная травматизация, осложненная снижением минеральной плотности костной ткани позвоночника до уровня остеопороза.
С целью профилактики кифотической деформации позвоночника после перечисленного комплекса хирургических вмешательств больному выполнена пластика поврежденного позвонка L2 по предлагаемому способу. Для этого после внутренней транспедикулярной фиксации и дистракции поврежденного участка позвоночника (фиг.1) удалены транпедикулярные винты (фиг.2). Штихт-каналы удаленных транспедикулярных винтов сломанного позвонка доработаны до формы регулярных цилиндрических транспедикулярных каналов, которые подобно примеру 1 заполнены гранулированным никелидом титана для синтеза скрепляющих элементов (фиг.3).
Благополучный исход операции в отдаленные постоперационные сроки, обеспечивающий удовлетворительное качество жизни больного, свидетельствует, в том числе, о достижимости технического результата предлагаемого способа, а подкрепление его солидной положительной статистикой подобных операций - о соответствии предложения критерию «промышленная применимость».
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРАНСКУТАННОЙ ПЛАСТИКИ ТЕЛА ПОЗВОНКА | 2014 |
|
RU2573101C1 |
| ПРОТЕЗ МЕЖПОЗВОНКОВОГО ДИСКА | 1998 |
|
RU2140229C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЧРЕСКОСТНЫХ РАЗРЫВОВ СУХОЖИЛИЙ РОТАТОРНЫХ МЫШЦ ПЛЕЧА | 2003 |
|
RU2244522C2 |
| УСТРОЙСТВО ДЛЯ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ ПОЗВОНОЧНИКА | 1999 |
|
RU2173117C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОВЕРХНОСТНЫХ РАНЕНИЙ СЕЛЕЗЕНКИ | 2007 |
|
RU2337632C1 |
| СПОСОБ СТАБИЛИЗАЦИИ ТЕЛ ПОЗВОНКОВ ПУТЕМ ВВЕДЕНИЯ ИМПЛАНТА | 2020 |
|
RU2743364C1 |
Изобретение относится к медицине, а именно к вертебрологии. Для скрепления и расправления тела позвонка, поврежденного в результате компрессионного перелома, после дистракции участка позвоночника и репозиции отломков выполняют глухие транспедикулярные каналы, ориентированные в направлении и поперек разлома. Созданные каналы заполняют порционно гранулами проницаемо-пористого никелида титана размерами от 0,5 до 5 мм с трамбовочным уплотнением каждой порции. Высокая биосовместимость никелида титана обеспечивает постоянное функционирование скрепляющих элементов без их отторжения и резорбции. 3 з.п. ф-лы, 4 ил.
1. Способ пластики тела сломанного позвонка, включающий дистракцию позвонка, репозицию и скрепление отломков путем создания транспедикулярных глухих каналов, ориентированных поперек поверхностей разлома, и заполнения их гранулами биосовместимого остеообразующего материала для синтеза скрепляющих элементов, отличающийся тем, что в качестве биосовместимого остеообразующего материала используют проницаемо-пористый никелид титана, заполнение транспедикулярных каналов осуществляют последовательно, порционно, от заглушенного конца к устью, с механической трамбовкой каждой порции гранул мануальными усилиями оператора, причем преимущественный размер гранул проницаемо-пористого никелида титана выбирают из интервала 0,5÷5 мм.
2. Способ по п.1, отличающийся тем, что на участке транспедикулярного канала в зоне разлома тела позвонка мануальные усилия механической трамбовки объема гранул увеличивают на 20÷50%.
3. Способ по п.1, отличающийся тем, что объем гранулированного проницаемо-пористого никелида титана до его внедрения в транспедикулярные каналы пропитывают раствором антибиотика.
4. Способ по п.1, отличающийся тем, что заполнение каждого транспедикулярного канала осуществляют через воронку с цилиндрическим наконечником длиной 1,5÷2,0 см и внешним диаметром, сопряженным с диаметром транспедикулярного канала при условии беззазорного свободного перемещения.
| МЮЛЛЕР М.Е | |||
| и др | |||
| Руководство по внутреннему остеосинтезу Springer-Verlag | |||
| - М., 1996, 750 | |||
| СПОСОБ ПЛАСТИКИ ИМПРЕССИОННЫХ ДЕФЕКТОВ ГОЛОВКИ ПЛЕЧЕВОЙ КОСТИ | 2005 |
|
RU2290122C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ СЕДЛОВИДНОЙ ДЕФОРМАЦИИ НОСА | 2002 |
|
RU2226369C1 |
| LEFERINK V.J | |||
| et | |||
| al Thoracolumbar spinal fractures | |||
| Eur | |||
| Spine J | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2011-02-10—Публикация
2009-07-06—Подача