Изобретение относится к серии новых биологически активных соединений сульфонных производных 2-нитро-2-(3-арил-1,2,4-оксадиазол-5-ил)этана общей формулы Iа-ж
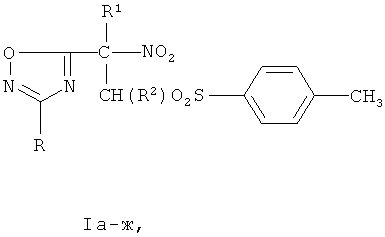
Ia R=3-NO2C6H4, R1=NO2, R2=H; б R=3-NO2C6H4, R1=NO2, R2=CH3; в R=4-CH3OC6H4, R1=NO2, R2=H; г R=4-CH3OC6H4, R1=NO2, R2=CH3; д R=4-CH3OC6H4, R1=CO2Et, R2=H; e R=4-CH3OC6H4, R1=CO2Et, R2=CH3; ж R=4-CH3C6H4,, R1=CO2Et, R2=H,
проявляющих противолепрозную и противотуберкулезную активность.
Известный структурный аналог сульфонилиминное производное 5-(4-метоксифенил)-1,2,4-оксадиазола относится к противотуберкулезному препарату и самостоятельно не применяется из-за быстрого развития к нему устойчивости микобактерий туберкулеза [E.D.Bergmann, Н.Bendas, U.Avilla. J.Org. Chem. 1953, v.18(1), р.64-66].
Аналоги по свойствам диафенилсульфон (дапсон) и диуцифон проявляют только противолепрозную активность [Машковский М.Д. Лекарственные средства, 2006, М., Новая волна, с.872-873].
Целью изобретения является исследование у новых сульфонных производных 2-нитро-2-(3-арил-1,2,4-оксадиазол-5-ил)этана противолепрозной и противотуберкулезной активности.
Технический результат достигается соединениями формулы Iа-ж, обладающими высокой противолепрозной и противотуберкулезной активностью.
Указанные соединения получают реакцией нуклеофильного замещения терминального хлора в 5-нитрохлороэтильных производных 1,2,4-оксадиазола [заявка №2009117364 от 06.5.2009 г.].
Токсичность соединений была определена по методу Миллера и Тейнтера в условиях in vivo на белых беспородных мышах весом 20-25 г при внутрибрюшинном введении в 3-х дозах и составила более 1100 мг/кг (таблица 1).
Сущность изобретения иллюстрируется следующим примером.
Пример 1. Определение противолепрозной и противотуберкулезной активности.
Минимальные ингибирующие концентрации (МИК) сульфонов в мкг/мл определялись на синхронизированных холодом (+4°C) музейных культурах M.lufu, которые используются для предварительного отбора веществ с антилепрозной активностью и М.tuberculosis (штамм H37RV) с добавлением 10% бычьей сыворотки и 20 ед/мл пенициллина в условиях in vitro методом серийных разведений в среде Школьниковой. Минимальные бактерицидные концентрации (МБК) в мкг/мл определялись по подавлению роста микобактерий на 50%. Препаратами сравнения во всех сериях экспериментов служили дапсон и изониазид. Исследование состояло из 5 серий экспериментов, ряды пробирок, содержащих разведения каждого соединения в димексиде от 256 мкг/мл до 1 мкг/мл, засевались по 1·106 культурами M.lufu или M.tuberculosis. Посевы инкубировались в термостате при 37±1°C в течение 12 дней. По прошествии этого срока пробирки извлекали из термостата и 0,1 мл образовавшейся взвеси микобактерий пересевали на плотную среду Левенштейна-Иенсена. Посевы повторно инкубировали в термостате при 37±1°C в течение 12 дней. После этого подсчитывали количество колоний, выросших на косяке Левенштейна-Йенсена. Результаты исследований подвергались статистической обработке с использованием t-критерия Стьюдента и сведены в таблице.
Анализ данных таблицы показывает, что соединения Iж, Iд по сравнению с дапсоном и изониазидом оказывают более выраженное противолепрозное и противотуберкулезное действие.
Таким образом, заявляемые соединения обладают комплексом полезных свойств: малотоксичны, проявляют хорошую ингибирующую и бактерицидную активность на микобактерии M.lufu и M.tuberculosis.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОННЫХ ПРОИЗВОДНЫХ 2-НИТРО-2-(3-АРИЛ-1,2,4-ОКСАДИАЗОЛ-5-ИЛ)ЭТАНА | 2009 |
|
RU2404170C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАЗОНОВ НИТРО-ТЕТРАЗОЛ-5-КАРБАЛЬДЕГИДА | 2012 |
|
RU2522437C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ГЕТАРИЛ-2-НИТРО-2-(3-ФЕНИЛ-1,2,4-ОКСАДИАЗОЛ-5-ИЛ) ЭТАНОВ | 2009 |
|
RU2415140C1 |
| ГИДРАЗОНЫ НИТРО ТЕТРАЗОЛ-5-КАРБАЛЬДЕГИДА, ОБЛАДАЮЩИЕ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2594983C1 |
| ПИРИДИНОИЛГИДРАЗОНЫ ДИАЛКИЛ(2-МЕТИЛ-4-ОКСОПЕНТ-2-ИЛ) ФОСФИНОКСИДОВ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2498990C1 |
| ПРИМЕНЕНИЕ 1-ГЕТАРИЛ-2-НИТРО-2-(3-ФЕНИЛ-1,2,4-ОКСАДИАЗОЛ-5-ИЛ) ЭТАНОВ В КАЧЕСТВЕ ПСИХОТРОПНЫХ ВЕЩЕСТВ | 2009 |
|
RU2420521C1 |
| СОЕДИНЕНИЯ ИМИДАЗО[1,2-а] ПИРИДИНА, ИХ СИНТЕЗ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2608611C2 |
| ПРОИЗВОДНЫЕ 5-ОКСО-5Н-[1]-БЕНЗОПИРАНО-[5,6-B]4-ОКСО-4Н-[1,2]-ПИРИМИДО-1,4,5,6-ТЕТРАГИД РО-1,3-ТИАЗИНА | 1997 |
|
RU2169732C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ N-(АРИЛ)-1,2,4-ТРИАЗОЛОПИРИМИДИН-2-СУЛЬФАМИДОВ | 1992 |
|
RU2061692C1 |
| ПРОИЗВОДНЫЕ ФЕНОТИАЗИНА И ИХ ПРИМЕНЕНИЕ ПРОТИВ ТУБЕРКУЛЕЗА | 2013 |
|
RU2663289C2 |
Изобретение относится к сульфонным производным 2-нитро-2-(3-арил-1,2,4-оксадиазол-5-ил)этана формулы I а-ж

Ia R=3-NO2C6H4, R1=NO2, R2=H; б R=3-NO2C6H4, R1=NO2, R2=CH3; в R=4-CH3OC6H4, R1=NO2, R2=H; г R=4-CH3OC6H4, R1=NO2, R2=CH3; д R=4-CH3OC6H4, R1=CO2Et, R2=H; e R=4-CH3OC6H4, R1=CO2Et, R2=CH3; ж R=4-CH3C6H4,, R1=CO2Et, R2=H, обладающим противолепрозной и противотуберкулезной активностью. 1 табл.
Сульфонные производные 2-нитро-2-(3-арил-1,2,4-оксадиазол-5-ил)этана формулы I а-ж
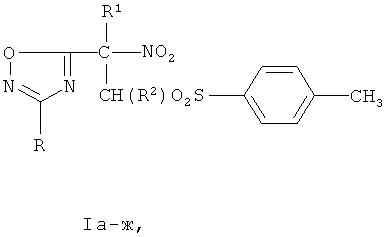
Ia R=3-NO2C6H4, R1=NO2, R2=H; б R=3-NO2C6H4, R1=NO2, R2=CH3; в R=4-CH3OC6H4, R1=NO2, R2=H; г R=4-CH3OC6H4, R1=NO2, R2=CH3; д R=4-CH3OC6H4, R1=CO2Et, R2=H; e R=4-CH3OC6H4, R1=CO2Et, R2=CH3; ж R=4-CH3C6H4, R1=CO2Et, R2=H,
обладающие противолепрозной и противотуберкулезной активностью.
| BERGMANN E.D., et al | |||
| J.Org | |||
| Chem., v.18, no.1, 1953, p.64-66 | |||
| МАШКОВСКИЙ М.Д., Лекарственные средства | |||
| - М.: Новая волна, 2006, с.872-873 | |||
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, ИХ СОДЕРЖАЩЕЕ, И СПОСОБ ЛЕЧЕНИЯ | 2001 |
|
RU2275371C2 |
Авторы
Даты
2011-04-10—Публикация
2009-10-14—Подача