Область изобретения
Данное изобретение относится к композиции, содержащей пробиотики и пребиотические питательные компоненты, которая может быть соответствующим образом использована в качестве детского питания. Композиция снижает вероятность инфекции.
Уровень техники
Композиция для детей обычно предназначается для воспроизведения композиционных свойств и (защитных) эффектов грудного молока человека. Одним важным шагом в направлении этой разработки является включение пребиотического волокна в состав для детей. Пребиотическое волокно также присутствует в грудном молоке человека и стимулирует здоровое развитие кишечной флоры. В последнее время было также обнаружено, что пероральный прием внутрь пребиотических волокон детьми стимулирует развитие здоровой иммунной системы. Дополнительной недавней разработкой является включение в состав для детей пробиотических бактерий. Многие исследования подтверждают полезные эффекты перорального введения пробиотических бактерий.
Значительная исследовательская работа проводится в настоящее время для изыскания оптимальных комбинаций пробиотических бактерий и пребиотического волокна (синбиотических композиций). WO 2004/089115 описывает композицию, содержащую штамм Lactobacillus и неусваиваемый олигосахарид. WO 2004/00340 также описывает синбиотические композиции.
Сущность изобретения
В одном аспекте данное изобретение относится к способу восстановления желудочно-кишечной флоры, поддерживающей жизнедеятельность желудочно-кишечного тракта и предотвращающей, например, инфекции. Найдено, что олигосахариды уроновой кислоты и пробиотические бактерии синергически улучшают кишечную флору, особенно у субъектов, имеющих нарушенную кишечную флору или кишечную флору, которая находится в процессе развития. Такая несбалансированная кишечная флора особенно часто встречается у детей и пациентов, которые подвергались, например, хирургии или лечению антибиотиками.
Пероральный прием внутрь короткоцепочечных олигосахаридов уроновой кислоты уменьшает прилипание патогенных бактерий к эпителию кишечного тракта и, тем самым, уменьшает возможность инфекции. Пероральный прием внутрь указанных олигосахаридов особенно полезен для субъектов, которые подвержены инфекциям патогенами, например, для субъектов с болезненным физиологическим состоянием или с развивающейся кишечной флорой.
Однако, как только прилипание патогенных бактерий уменьшается, патогенные бактерии могут оставаться и колонизировать кишечный тракт. Следовательно, предпочтительно, чтобы уменьшенное прилипание совмещалось с восстановлением кишечной флоры и пониженной возможностью колонизации кишечного тракта патогенными бактериями (т.е. повышением резистентности к колонизации). Резистентность к колонизации патогенными бактериями может быть повышена введением пробиотических бактерий. Пробиотические бактерии уменьшают наличие питательных веществ, снижая, тем самым, скорость роста патогенных бактерий, и занимают в кишечнике места прилипания патогенных бактерий.
Кроме того, было обнаружено, что и пробиотические бактерии, и олигосахариды уроновой кислоты стимулируют системную иммунную систему.
Поэтому данное изобретение относится к композиции олигосахарида уроновой кислоты и пробиотических бактерий, которая может быть соответствующим образом использована для поддержания и восстановления жизнедеятельности желудочно-кишечного тракта, может быть соответственно использована для предотвращения инфекции у субъектов, страдающих различными заболеваниями, когда имеется дисбаланс желудочно-кишечной флоры, и которая особенно применима для субъектов с развивающейся желудочно-кишечной флорой, таких как дети.
Поэтому в одном аспекте данное изобретение относится к детскому питанию, которое поддерживает здоровое развитие кишечной флоры ребенка.
В дополнительном аспекте данное изобретение относится к композиции, которая может быть соответствующим образом использована для лечения и/или профилактики инфекции у пациентов, страдающих от аллергии, аллергического ринита, пищевой гиперчувствительности, атопического дерматита, экземы, астмы, диареи, инфекционной или ассоциированной с антибиотиками диареи, запора, кишечных спазмов, колик, синдрома приобретенного иммунодефицита, рака, диабета, кистозного фиброза, у пациентов, подвергающихся хирургии, пациентов, подвергающихся противораковой терапии, и/или пациентов, страдающих от повреждений, вызванных теплом, трением, электричеством, радиацией или химикатами.
Данное изобретение дополнительно усовершенствовано объединением олигосахаридов уроновой кислоты и пробиотических бактерий с пребиотическим олигосахаридом. Пребиотический олигосахарид дополнительно усиливает комбинацию пробиотических бактерий и олигосахаридов уроновой кислоты, стимулируя рост желательной хорошей врожденной флоры, особенно Lactobacilli и Bifidobacteria, и помогает выживанию и обеспечивает питательные вещества для принятых пробиотических бактерий. Пребиотические олигосахариды, таким образом, специфически стимулируют преобладание хороших кишечных бактерий.
Подробное описание предпочтительных вариантов воплощения
Данное изобретение относится к композиции, содержащей пробиотические бактерии и от 25 до 100 мас.% олигосахарида уроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в композиции.
Пробиотический материал
Данная композиция содержит пробиотические бактерии. Пробиотические бактерии представлены в виде моно- или смешанной культуры живых микроорганизмов, которые при применении человеку или животному благоприятно влияют на хозяина, улучшая свойства кишечной флоры. Предпочтительно, данная композиция содержит от 102 до 1012, более предпочтительно от 104 до 1011, наиболее предпочтительно от 107 до 5×1010, колониеобразующих единиц (cfu) пробиотических бактерий на грамм олигосахарида уроновой кислоты с DP между 2 и 250, предпочтительно DP между 2 и 100. Данная композиция предпочтительно содержит от 102 до 1013 колониеобразующих единиц (cfu) пробиотических бактерий на грамм сухой массы данной композиции, предпочтительно от 102 до 1012, более предпочтительно от 105 до 1010, наиболее предпочтительно от 104 до 1×109 cfu. Дозировка пробиотической бактерии по данному изобретению предпочтительно находится между 102 и 1013, более предпочтительно от 105 до 1011, наиболее предпочтительно от 108 до 5×1010 колониеобразующих единиц (cfu) в сутки.
Предпочтительно, данная композиция содержит бактерии рода Lactobacillus или Bifidobacterium или данная композиция содержит бактерии рода Lactobacillus и Bifidobacterium. Предпочтительно композиция содержит Bifidobacterium, выбранные из группы, состоящей из B.longum, B.breve, B.infantis, B.animalis, B.lactis и B.bifidum, наиболее предпочтительно B.breve. Предпочтительно данная композиция содержит Lactobacillus, выбранные из группы, состоящей из L.casei, L.paracasei, L.rhamnosus, L.acidophilus, L.fermentum и L.plantarum. Наиболее предпочтительно данная композиция содержит Bifidobacterium breve и/или Lactobacillus paracasei, потому что было обнаружено, что рост указанных бактерий ослаблен в кишечнике детей, вскармливаемых составом, по сравнению с детьми, вскармливаемыми грудным молоком.
Bifidobacterium breve представляют собой грамположительные анаэробные палочковидные бактерии. Данные B.breve предпочтительно имеют по меньшей мере 95% идентичность последовательности 16 S рРНК при сравнении с типовым штаммом B.breve ATCC 15700, более предпочтительно по меньшей мере 97% идентичность, как определено в Stackebrandt & Goebel, 1994, Int. J. Syst. Bacteriol. 44:846-849. Идентичность последовательности нуклеиновых кислот предпочтительно рассчитывают для двух нуклеотидных последовательностей, когда они оптимально выровнены, применяя программы GAP или BESTFIT, использующие значения параметров по умолчанию. Значения параметров по умолчанию GAP используют с пенальти создания интервала=50 (нуклеотидов)/8 (протеинов) и пенальти удлинения интервала=3 (нуклеотида)/2 (протеина). Для нуклеотидов используемой матрицей для количественной оценки по умолчанию является nwsgapdna (Henikoff & Henikoff, 1992, PNAS 89, 915-919). Очевидно, что, когда последовательности РНК называют по существу подобными или имеющими конкретную степень идентичности последовательности с последовательностями ДНК, тимин (T) в последовательности ДНК считают равным урацилу (U) в последовательности РНК. Выверки последовательностей и метки для процентной идентичности последовательности могут быть определены с помощью компьютерных программ, таких как GCG Wisconsin Package, Version 10.3, доступная от Accelrys Inc., 9685 Scranton Road, San Diego, CA 92121-3752, USA или EMBOSSwin v. 2.10.0.
Bifidobacterium, используемые в данном изобретении, предпочтительно дают сигнал при использовании метода анализа с 5' нуклеазой, который описан в находящейся одновременно на рассмотрении международной патентной заявке PCT/NL 2004/000748 и европейской патентной заявке 05075486.0 данного заявителя. Согласно предпочтительному варианту воплощения данная композиция содержит по меньшей мере одну разновидность B.breve, выбранную из группы, состоящей из B.breve Bb-03 (Rhodia), B.breve M16-V (Morinaga), B.breve R0070 (Institute Rosell, Lallemand), DSM 20091 и LMG 11613. Наиболее предпочтительно, B.breve является B.breve M-16V (Morinaga).
В предпочтительном варианте воплощения данная композиция содержит Lactobacillus paracasei. Предпочтительно данный штамм L.paracasei имеет по меньшей мере 95, более предпочтительно по меньшей мере 97% идентичность последовательности 16S рРНК, когда его сравнивают с типовым штаммом L.paracasei ATCC 25032, как определено выше. Lactobacillus, используемые в данном изобретении, предпочтительно дают сигнал при использовании метода анализа с 5' нуклеазой, который описан в находящейся одновременно на рассмотрении европейской патентной заявке данного заявителя с номером заявки 05075486.0. Согласно предпочтительному варианту воплощения данная композиция содержит по меньшей мере L.paracasei, выбранные из группы, состоящей из L.paracasei F19 (Aria, Sweden), L.paracasei LAFTI L26 (DSM Food Specialties, the Netherlands) и L.paracasei CRL 431 (Chr. Hansen, Denmark), LMG 12165 и LMG 11407.
Олигосахарид уроновой кислоты
Данная композиция содержит между 25 и 100 мас.%, предпочтительно между 50 и 100 мас.% олигосахарида уроновой кислоты со степенью полимеризации (DP) от 2 до 250 на основе общей массы уроновой кислоты в композиции. Предпочтительно данная композиция содержит между 25 и 100 мас.%, предпочтительно между 50 и 100 мас.% олигосахарида уроновой кислоты со степенью полимеризации (DP) от 2 до 100 на основе общей массы уроновой кислоты в композиции. Более предпочтительно, данная композиция содержит между 25 и 100 мас.% олигосахарида галактуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в композиции, более предпочтительно между 25 и 100 мас.% олигосахарида галактуроновой кислоты с DP от 2 до 100 на основе общей массы уроновой кислоты в композиции, еще более предпочтительно между 25 и 100 мас.% олигосахарида галактуроновой кислоты с DP от 2 до 50 на основе общей массы уроновой кислоты в композиции.
Термин олигосахарид уроновой кислоты, используемый в данном изобретении, относится к олигосахариду, где по меньшей мере 50% остатков выбраны из группы, состоящей из гулуроновой кислоты, маннуроновой кислоты, галактуроновой кислоты и глюкуроновой кислоты. В предпочтительном варианте воплощения олигосахарид уроновой кислоты содержит по меньшей мере 50% галактуроновой кислоты на основе всех остатков уроновых кислот в олигосахариде уроновой кислоты. Более предпочтительно, данный олигосахарид уроновой кислоты является гидролизованным пектином, предпочтительно полигалактуроновой кислотой, еще более предпочтительно, полученным гидролизом пектина яблока, цитруса и/или сахарной свеклы.
В предпочтительном варианте воплощения олигосахариды уроновой кислоты по данному изобретению содержат между 25 и 100 мас.% галактуроновых олигосахаридов с DP между 2 и 100 на основе общей массы галактуроновой кислоты, более предпочтительно между 50 и 100 мас.%, еще более предпочтительно между 75 и 100 мас.%. Предпочтительно композиция содержит между 25 и 100 мас.% галактуроновых олигосахаридов с DP между 2 и 50 на основе общей массы галактуроновой кислоты, более предпочтительно между 50 и 100 мас.%, еще более предпочтительно между 75 и 100 мас.%.
Олигосахариды галактуроновой кислоты предпочтительно получают ферментативным перевариванием пектина пектинлизазой, пектинлиазой, эндополигалактуроназой и/или пектиназой. Данный олигосахарид уроновой кислоты предпочтительно может быть получен ферментативным перевариванием пектина пектинлизазой, пектинлиазой, эндополигалактуроназой и/или пектиназой.
Олигосахарид уроновой кислоты может быть метоксилирован и/или амидирован. Олигосахарид уроновой кислоты является предпочтительно неусваиваемым в верхнем отделе кишечного тракта человека и растворимым в воде.
В предпочтительном варианте воплощения по меньшей мере одно из концевых звеньев гексозы олигосахарида уроновой кислоты имеет двойную связь, которая предпочтительно находится между положением C4 и C5 концевого звена гексозы. Двойная связь обеспечивает эффективную защиту против прикрепления патогенных бактерий к эпителию. Предпочтительно одно из концевых звеньев гексозы содержит двойную связь. Двойная связь при концевом звене гексозы может быть, например, получена ферментативным гидролизом пектина лиазой.
Предпочтительно олигосахарид уроновой кислоты имеет структуру I ниже, где концевая гексоза (левая) предпочтительно содержит двойную связь. Звенья гексозы, иные чем концевое звено (звенья) гексозы, являются предпочтительно звеньями уроновой кислоты, предпочтительно звеньями галактуроновой кислоты. Группы карбоновой кислоты на указанных звеньях могут быть свободными или (частично) этерифицированными и предпочтительно по меньшей мере 10% метилированы (см. ниже).
Структура I: Полимерный олигосахарид кислоты
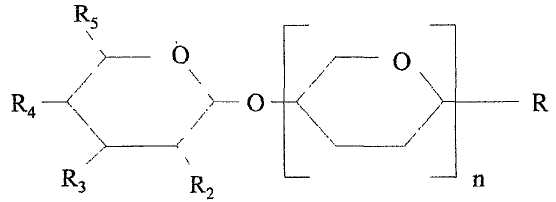
где:
R предпочтительно выбран из группы, состоящей из водорода, гидрокси или кислотной группы, предпочтительно гидрокси; и
по меньшей мере один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет группу N-ацетилнеураминовой кислоты, N-гликолоилнеураминовой кислоты, свободной или этерифицированной карбоновой кислоты, группу серной кислоты или фосфорной кислоты, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород. Предпочтительно один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет группу N-ацетилнеураминовой кислоты, N-гликолоилнеураминовой кислоты, свободной или этерифицированной карбоновой кислоты, группу серной кислоты или фосфорной кислоты, предпочтительно свободной или этерифицированной карбоновой кислоты, и остальные представляют гидрокси и/или водород. Еще более предпочтительно, один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет свободную или этерифицированную карбоновую кислоту, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород; и
n означает целое число и относится к числу звеньев гексозы (см. также Степень полимеризации, ниже), которыми может быть любое звено гексозы. Соответственно n означает целое число между 1-249, предпочтительно между 1 и 99, более предпочтительно между 1 и 49. Предпочтительно звено (звенья) гексозы является звеном уроновой кислоты.
Наиболее предпочтительно R, R2 и R3 представляют гидрокси, R4 представляет водород, R5 представляет карбоновую кислоту, n означает любое число между 1 и 99, предпочтительно между 1 и 50, наиболее предпочтительно между 1 и 10, и звено гексозы является предпочтительно галактуроновой кислотой.
Более предпочтительно, данный олигосахарид уроновой кислоты имеет структуру согласно фиг.2.
Фиг.2: Предпочтительная концевая группа гексуроновой кислоты
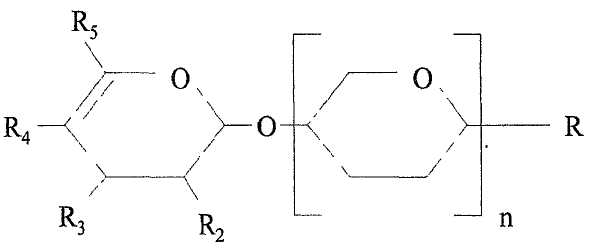
где:
R предпочтительно выбран из группы, состоящей из водорода, гидрокси или кислотной группы, предпочтительно гидрокси (см. выше); и
по меньшей мере один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет группу N-ацетилнеураминовой кислоты, N-гликолоилнеураминовой кислоты, свободной или этерифицированной карбоновой кислоты, группу серной кислоты и фосфорной кислоты, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород. Предпочтительно один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет группу N-ацетилнеураминовой кислоты, N-гликолоилнеураминовой кислоты, свободной или этерифицированной карбоновой кислоты, группу серной кислоты и фосфорной кислоты, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород. Еще более предпочтительно, один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет свободную или этерифицированную карбоновую кислоту, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород; и n означает целое число и относится к числу звеньев гексозы (см. также Степень полимеризации, ниже), которыми может быть любое звено гексозы. Соответственно n означает целое число между 1-249 (предпочтительно между 1 и 99, еще более предпочтительно 1-49), представляя число звеньев гексозы, предпочтительно являющихся звеньями уроновой кислоты, еще более предпочтительно звеньями галактуроновой кислоты. Группы карбоновой кислоты на указанных звеньях могут быть свободными или этерифицированными и предпочтительно являются по меньшей мере частично метилированными.
Наиболее предпочтительно, R2 и R3 представляют гидрокси, R4 представляет водород и R5 представляет свободную или этерифицированную карбоновую кислоту.
В дополнительном варианте воплощения используют смесь олигосахаридов уроновой кислоты, которые имеют различную DP, и/или содержит как ненасыщенное, так и насыщенное концевое звено гексозы. Предпочтительно по меньшей мере 5%, более предпочтительно по меньшей мере 10%, еще более предпочтительно по меньшей мере 25% концевых гексуроновых звеньев представляют ненасыщенные гексуроновые звенья олигосахарида уроновой кислоты (см., например, фиг.2). Так как каждый отдельный олигосахарид уроновой кислоты предпочтительно содержит только одно ненасыщенное концевое гексуроновое звено, предпочтительно менее чем 50% концевых гексуроновых звеньев являются ненасыщенными гексуроновыми звеньями (т.е. содержат двойную связь).
Смесь олигосахаридов уроновой кислоты предпочтительно содержит между 2 и 50% ненасыщенных гексуроновых звеньев на основе общего количества гексуроновых звеньев, предпочтительно между 10 и 40%.
Олигосахарид уроновой кислоты может быть дериватизирован. В одном варианте воплощения олигосахариды уроновой кислоты характеризуются степенью метоксилирования около 20%, предпочтительно около 50%, еще более предпочтительно около 70%. Используемое здесь выражение «степень метоксилирования» (упоминается также как DE или «степень этерификации») предназначается для обозначения пределов, до которых группы свободной корбоновой кислоты, содержащиеся в цепи полигалактуроновой кислоты, этерифицированы (например, метилированием). В другом варианте воплощения олигосахариды уроновой кислоты имеют степень метилирования около 20%, предпочтительно около 50%, еще более предпочтительно около 70%.
Концентрация олигосахаридов уроновой кислоты
Данная композиция является предпочтительно питательной композицией, содержащей жир, усваиваемый углевод и белок. Данная питательная композиция предпочтительно содержит между 0,01 и 5 грамм олигосахарида уроновой кислоты с DP от 2 до 250 на 100 грамм сухой массы питательной композиции, более предпочтительно между 0,05 и 2 грамм на 100 грамм сухой массы. Данная питательная композиция предпочтительно содержит между 0,01 и 5 грамм олигосахарида галактуроновой кислоты с DP от 2 до 250 (предпочтительно DP 2-100) на 100 грамм сухой массы питательной композиции, более предпочтительно между 0,05 и 2 грамм на 100 грамм сухой массы.
Данный способ предпочтительно включает введение между 0,05 и 10 грамм олигосахарида уроновой кислоты с DP от 2 до 100 в сутки, еще более предпочтительно между 0,1 и 5 грамм олигосахаридов уроновой кислоты в сутки.
Пребиотическое волокно
В дополнение к олигосахариду уроновой кислоты и пробиотическим бактериям данная композиция предпочтительно содержит пребиотическое волокно, которое стимулирует рост кишечных пробиотических бактерий, особенно Bifidobacteria и/или Lactobacilli. Преимущественно, пребиотическими волокнами являются по меньшей мере 50% растворимых в воде олигосахаридов (L. Prosky et al, J. Assoc. Anal. Chem 71:1017-1023, 1988) со степенью полимеризации (DP) 2-100, которые предпочтительно не содержат уроновой кислоты. Олигосахариды, лишенные звеньев уроновой кислоты, упоминаются здесь далее как «неусваиваемый олигосахарид». Неусваиваемый олигосахарид не переваривается или только частично переваривается в кишечнике под действием кислот или пищеварительных ферментов, присутствующих в верхнем отделе пищеварительного тракта человека (тонкая кишка и желудок) и ферментируются кишечной флорой человека. Например, глюкоза, фруктоза, галактоза, сукроза, лактоза, мальтоза и мальтодекстрины рассматриваются как легко усваиваемые.
Неусваиваемым олигосахаридом является предпочтительно смесь неперевариваемых сахаридов. Это является общей практикой, потому что применение неусваиваемых олигосахаридов, например, с одной длиной цепи очень распространено. Предпочтительными примерами коммерчески доступных смесей неусваиваемых олигосахаридов являются инулин, фруктоолигосахарид и галактоолигосахарид. Когда неусваиваемым олигосахаридом являются смеси сахаридов, средние значения соответствующих параметров используют для определения данного изобретения. Например, если сахарид A является смесью отдельных сахаридов 25 мас.% Glu-Gal-Gal-Gal, 25 мас.% Glu-Gal-Gal и 50 мас.% Gal-Gal, усредненный состав моносахаридов представляет собой 85,4% Gal и 14,6% Glu. Средняя степень полимеризации (DP) составляет 2,75.
Степень полимеризации неусваиваемого олигосахарида предпочтительно ниже 60, более предпочтительно ниже 40, еще более предпочтительно ниже 20, наиболее предпочтительно ниже 10. Олигосахарид предпочтительно содержит по меньшей мере 60%, более предпочтительно по меньшей мере 95% звеньев гексозы, выбранных из группы, состоящей из фруктозы, галактозы и глюкозы.
Предпочтительно, неусваиваемый олигосахарид выбран из группы, состоящей из таких как: целлобиоза (4-O-β-D-глюкопиранозил-D-глюкоза), целлодекстрины ((4-O-β-D-глюкопиранозил)n-D-глюкоза), B-циклодекстрины (циклические молекулы α-1-4-связанной D-глюкозы; α-циклодекстрин-гексамера, β-циклодекстрин-гептамера и γ-циклодекстрин-октамера), неусваиваемый декстрин, гентиоолигосахариды (смесь β-1-6-связанных остатков глюкозы, некоторые 1-4 связи), глюкоолигосахариды (смесь α-D-глюкозы), изомальтоолигосахариды (линейные α-1-6 связанные остатки глюкозы с некоторыми 1-4 связями), изомальтоза (6-O-α-D-глюкопиранозил-D-глюкоза); изомальтриоза (6-O-α-D-глюкопиранозил-(1-6)-α-D-глюкопиранозил-D-глюкоза), паноза (6-O-α-D-глюкопиранозил-(1-6)-α-D-глюкопиранозил-(1-4)-D-глюкоза), лейкроза (5-O-α-D-глюкопиранозил-D-фруктопиранозид), палатиноза или изомальтулоза (6-O-α-D-глюкопиранозил-D-фруктоза), теандероза (О-α-D-глюкопиранозил-(1-6)-О-α-D-глюкопиранозил-(1-2)-β-D-фруктофуранозид), D-агатоза, D-lyxo-гексулоза, лактосукроза (О-β-D-галактoпиранозил-(1-4)-О-α-D-глюкопиранозил-(1-2)-β-D-фруктофуранозид), α-галактоолигосахариды, включая раффинозу, стахиозу и другие соевые олигосахариды (O-α-D-галактoпиранозил-(1-6)-α-D-глюкопиранозил-β-D-фруктофуранозид), β-галактoолигосахариды или трансгалактoолигосахариды (β-D-галактoпиранозил-(1-6)-[β-D-глюкопиранозил]n-(1-4)-α-D-глюкоза), лактулоза (4-O-β-D-галактoпиранозил-D-фруктоза), 4'-галактозиллактоза (О-D-галактoпиранозил-(1-4)-О-β-D-глюкопиранозил-(1-4)-D-глюкопираноза), синтетический галактoолигосахарид (неогалактoбиоза, изогалактoбиоза, галсукроза, изолактоза I, II и III), фруктаны - типа левана (β-D-(2→6)-фруктофуранозил)n-α-D-глюкопиранозид), фруктаны - типа инулина (β-D-((2→1)-фруктофуранозил)n-α-D-глюкопиранозид), 1f-β-фруктофуранозилнистоза (β-D-((2→1)-фруктофуранозил)n-β-D-фруктофуранозид), ксилоолигосахариды (β-D-((1→4)-ксилоза)n, лафиноза, лактосукроза, арабиноолигосахариды и их смеси.
Согласно дополнительному предпочтительному варианту воплощения неусваиваемый олигосахарид выбран из группы, состоящей из фруктанов, фруктоолигосахаридов, неусваиваемых декстринов, галактoолигосахаридов (включая трансгалактoолигосахариды), ксилоолигосахаридов, олигосахаридов соевых бобов, арабиноолигосахаридов, глюкоолигосахаридов, манноолигосахаридов, фукоолигосахаридов и их смесей.
Подходящие неусваиваемые олигосахариды и способы их получения дополнительно описаны у Laere KJM (Laere, KJM, Degradation of structurally different non-digestible oligosaccharides by intestinal bacteria: glycosylhydrolases of Bi. adolescentis. PhD-thesis, June 2000, Wageningen Agricultural University, Wageningen, The Netherlands), полное содержание этой публикации включено в описание в виде ссылки.
Данное изобретение предпочтительно относится к композиции с двумя различными неусваиваемыми олигосахаридами, например, неусваиваемым олигосахаридом A и неусваиваемым олигосахаридом B, упоминаемыми здесь далее как сахарид A и сахарид B соответственно. Сахарид A и сахарид B являются предпочтительно различными сахаридами и имеют различные гликозидные связи, степень полимеризации и/или состав моносахаридов.
Предпочтительно по меньшей мере 98% всех звеньев моносахаридов сахарида A и B являются моносахаридами, выбранными из группы, состоящей из моносахаридов галактoзы (gal), фруктозы (fru) и глюкозы (glu). Согласно предпочтительному варианту воплощения данного изобретения процентная доля по меньшей мере одного моносахарида, выбранного из группы, состоящей из глюкозы, фруктозы и галактoзы, в сахариде A по меньшей мере на 40% выше, чем процентная доля того же моносахарида в сахариде B, предпочтительно по меньшей мере на 50%, более предпочтительно по меньшей мере на 75%, еще более предпочтительно по меньшей мере на 90%. Повышенное несходство моносахаридов стимулирует более широкую популяцию полезных кишечных бактерий.
Процентную долю моносахарида в сахариде можно легко рассчитать делением количества звеньев соответствующего моносахарида (например, глюкозы) в сахариде на общее число моносахаридных звеньев в сахариде и умножением на 100. Когда сахарид является смесью сахаридов, вклад каждого отдельного сахарида в смесь сахаридов необходимо принимать во внимание. Процентное отношение сахаридной смеси может быть просто определено путем полного гидролиза смеси и определения молярного процентного отношения для каждого моносахарида.
Предпочтительно сахарид A содержит по меньшей мере 40% галактoзы, более предпочтительно по меньшей мере 67% галактoзы, более предпочтительно по меньшей мере 75 мол.% галактoзы. Предпочтительно сахарид B содержит по меньшей мере 30% фруктозы, более предпочтительно по меньшей мере 67% фруктозы, еще более предпочтительно по меньшей мере 80 мас.% фруктозы.
Например, в случае, когда сахарид A представляет смесь glu-(gal)n=2-7 (n является, следовательно, целым числом, выбранным из 2-7) с усредненным составом моносахаридов 20% глюкозы и 80% галактoзы, и сахарид B представляет смесь glu-(fru)n=2-7 и (fru)n=2-7 с усредненным составом моносахаридов 10% глюкозы и 90% фруктозы, разница составляет в a) глюкозе 10%; b) фруктозе 90% и c) галактoзе 80%. В этом примере и фруктоза, и галактoза отвечают критерию, что процентная доля по меньшей мере одного моносахарида, выбранного из группы, состоящей из глюкозы, фруктозы и галактoзы, в сахариде A по меньшей мере на 40% выше, чем процентная доля того же моносахарида в сахариде B.
Степень полимеризации
Сахариды A и B имеют степень полимеризации (DP) от 2 до 100. Предпочтительно по меньшей мере 80 мас.%, более предпочтительно по меньшей мере 95 мас.%, наиболее предпочтительно по меньшей мере 98 мас.% общей массы сахарида A и B имеют степень полимеризации (DP) ниже 60, более предпочтительно ниже 40, наиболее предпочтительно ниже 20. Более низкая DP преимущественно уменьшает вязкость и увеличивает способность к ферментации неусваиваемых сахаридов. Предпочтительно по меньшей мере 50 мас.%, предпочтительно по меньшей мере 75 мас.% общей массы сахаридов A и B составляют неусваиваемые сахариды с DP 2-8. Путем использования смеси с высокой процентной долей малых сахаридов может быть усилена способность к ферментации и эффект стимуляции роста молочно-кислых бактерий и Bifidobacteria.
Согласно предпочтительному варианту воплощения данного изобретения DP сахарида A по меньшей мере на 5 моносахаридных звеньев ниже, чем степень полимеризации сахарида B, предпочтительно по меньшей мере на 10, еще более предпочтительно по меньшей мере на 15. Включение сахарида с повышенной степенью полимеризации снижает осмотическую нагрузку, что является благоприятным для детского питания и также улучшает пребиотическую стимуляцию кишечной флоры в более дистальных частях толстой кишки.
Предпочтительно, сахарид A имеет DP 2-15, более предпочтительно 2-8. Предпочтительно сахарид B имеет DP 8-100. Сахариды A и B с различными DP могут иметь одинаковый или слегка отличающийся моносахаридный состав. Когда сахариды A и B имеют различную DP и сходный моносахаридный состав, тогда разница в усредненной DP между сахаридом A и сахаридом B предпочтительно по меньшей мере 5, более предпочтительно по меньшей мере 10, еще более предпочтительно по меньшей мере 15. Предпочтительно, сахариды A и B имеют различный моносахаридный состав (см. выше) и различные DP.
Например, если сахарид A представляет смесь glu-(fru)m=2-7 и (fru)m=2-6 с усредненной DP 3,5 моносахаридных звена и сахарид B представляет glu-(fru)m=12-100 с усредненной DP 25 моносахаридных звеньев, тогда разница в усредненных DP (25-3,5)=21,5.
В другом предпочтительном варианте воплощения данного изобретения процентная доля по меньшей мере одной гликозидной связи сахарида A на основе всех гликозидных связей сахарида A по меньшей мере на 40% выше процентной доли той же гликозидной связи в сахариде B, предпочтительно по меньшей мере на 50%, еще более предпочтительно по меньшей мере на 75%. Термин «гликозидная связь», используемый в данном изобретении, относится к связи C-О-C, образованной между кольцами двух циклических моносахаридов путем удаления воды. Повышенная несхожесть в гликозидных связях стимулирует более широкий диапазон полезных бактерий.
Гликозидные связи отличаются тем, что они ковалентно связывают атомы углерода в моносахаридных звеньях при различно пронумерованных положениях и/или тем, что они образуют α или β связи. Примерами различных гликозидных связей, встречающихся в неусваиваемых сахаридах, являются β(1,3), α(1,4), β(2,1), α(1,2) и β(1,4) связи.
Предпочтительно гликозидные связи в сахариде A содержат по меньшей мере 40% β(1,4) и/или β(1,6) гликозидных связей, более предпочтительно по меньшей мере 75%. Гликозидные связи в сахариде B предпочтительно содержат по меньшей мере 40% β(2,1) гликозидных связей, более предпочтительно по меньшей мере 75%.
Сахаридом A является предпочтительно сахарид, выбранный из группы, состоящей из β-галактoолигосахаридов, α-галактoолигосахаридов и галактанов. Согласно более предпочтительному варианту воплощения сахаридом A является β-галактoолигосахарид, более предпочтительно трансгалактoолигосахарид. Предпочтительно сахарид содержит β-галактoолигосахариды с β(1,4) и/или β(1,6) гликозидными связями и концевой глюкозой. Трансгалактoолигосахарид, например, коммерчески доступен под торговым названием Vivinal®GOS (Borculo Domo Ingredients, Zwolle, Netherlands).
Сахаридом B предпочтительно является сахарид, выбранный из группы, состоящей из фруктополисахаридов и фруктоолигосахаридов. Термины фруктополисахариды, полифруктоза, полифруктан и фруктан являются взаимозаменяемыми и относятся к полисахаридам, содержащим β-связанные звенья фруктозы, которые предпочтительно связаны β(2,1) и/или β(2,6) гликозидными связями. Предпочтительно, фруктополисахарид содержит концевую глюкозу с β(2,l) гликозидной связью. Предпочтительно, фруктополисахарид содержит по меньшей мере 7 β-связанных звеньев фруктозы. В дополнительном предпочтительном варианте воплощения инулин используют в качестве сахарида B. Инулин является типом фруктополисахарида, где по меньшей мере 75% гликозидных связей представлено β(2,1) связями. Обычно инулин имеет среднюю длину цепи от 8 до 60 моносахаридных звеньев. Подходящий фруктополисахарид для применения в композициях по данному изобретению коммерчески доступен под торговым названием Raftiline®HP (Orafti).
В дополнительном предпочтительном варианте воплощения сахаридом B является фруктоолигосахарид. Фруктоолигосахарид является сахаридом, содержащим β-связанные звенья фруктозы, которые предпочтительно связаны β(2,1) и/или β(2,6) гликозидными связями. Фруктоолигосахарид предпочтительно содержит глюкозу с β(2,1) гликозидной связью на редуцирующем конце. Предпочтительно, фруктоолигосахарид содержит от 2 до 6 β-связанных звеньев фруктозы. Подходящим источником фруктоолигосахарида является Raftilose® (Orafti) или Actilight (Beghin-Meiji).
Концентрация неусваиваемых олигосахаридов
Данная композиция предпочтительно содержит по меньшей мере 5 мг неусваиваемого олигосахарида на 100 грамм сухой массы данной композиции, более предпочтительно по меньшей мере 50 мг, еще более предпочтительно по меньшей мере 0,1 г, наиболее предпочтительно по меньшей мере 0,5 г. Предпочтительно данная композиция не содержит более чем 10 г неусваиваемого олигосахарида на 100 г сухой массы данной композиции, предпочтительно не более чем 2,0 г.
Неусваиваемые олигосахариды по данному изобретению предпочтительно вводят в суточной дозе от 0,1 до 30 г, более предпочтительно от 0,5 до 15 г, более предпочтительно от 3 до 10 г.
Если композиция содержит сахарид A и сахарид B, массовое отношение сахарид A/сахарид B предпочтительно составляет между 0,01 и 100, более предпочтительно между 0,5 и 100, еще более предпочтительно между 4 и 100, наиболее предпочтительно между 24 и 100. Высокое массовое отношение особенно благоприятно, когда сахарид A имеет низкую DP и сахарид B имеет относительно высокую DP. Это обеспечивает оптимальное равновесие между осмоляльностью и способностью к ферментации.
Сахарид A и сахарид B предпочтительно составляют от 5 до 100 мас.% на основе общей массы неусваиваемых сахаридов в данной композиции, более предпочтительно от 50 до 100 мас.%.
Питательные макроэлементы
Данная композиция, когда она приготовлена как питательная композиция, предпочтительно содержит от 5 до 16 en% белка, от 35 до 60 en% жира и от 25 до 75 en% углеводов, предпочтительно от 5 до 12,0 en% белка, от 39 до 50 en% жира и от 40 до 55 en% углеводов (en% является сокращением для процента энергии и представляет относительное количество, которое каждый компонент вносит в общую калорийность препарата). Питательная композиция является особенно подходящей для кормления детей, так как она обеспечивает ребенка необходимыми питательными веществами.
Данная композиция может быть также добавлена к грудному молоку. Продукты, добавляемые в настоящее время к грудному молоку, часто относятся к усилителям грудного молока. Поэтому в дополнительном аспекте данное изобретение относится к составу, содержащему грудное молоко и данную композицию. В еще одном дополнительном аспекте данное изобретение относится к способу приготовления питательной композиции, содержащей смесь грудного молока и данной композиции.
Предпочтительно, данная композиция содержит от 5 до 20 en.% белка, более предпочтительно от 8 до 12 en.%. Предпочтительно данная композиция содержит белок, выбранный из группы, состоящей из казеина, сыворотки, снятого молока, соевого белка, горохового белка, коллагена, рисового белка и/или кукурузного белка. Предпочтительно по меньшей мере 25 мас.% всего белка данной композиции представлено гидролизованным белком и/или свободной аминокислотой. Применение гидролизата белка и/или свободных аминокислот уменьшает побочные эффекты, такие как аллергия, которые особенно нежелательны для детей с субоптимальной кишечной флорой.
Предпочтительно, данная композиция содержит цинк (Zn). Цинк защищает кишечную барьерную функцию в присутствии патогенов (Roselli et al, 2003 J Nutr. 133:4077) и играет важную роль в пролиферации энтероцитов. Данная композиция предпочтительно содержит по меньшей мере 10 мкг цинка на г сухой массы композиции, более предпочтительно по меньшей мере 30 мкг, наиболее предпочтительно по меньшей мере 50 мкг Zn. Предпочтительно, данная композиция содержит менее чем 0,3 мг, более предпочтительно не более чем 0,2 мг цинка на г сухой массы данной композиции. Предпочтительно цинк добавляют в композицию в форме сульфата цинка, ацетата цинка, хлорида цинка, лактата цинка, цитрата цинка, глюконата цинка и/или оксида цинка.
Данную композицию предпочтительно вводят в жидком виде. Нарушения нормального стула (например, твердый стул, недостаточный объем стула, диарея) являются главной проблемой у детей с субоптимальной кишечной флорой. Поэтому данная композиция предпочтительно имеет осмоляльность между 50 и 500 мОсм/кг, более предпочтительно между 100 и 400 мОсм/кг. С такой осмоляльностью данная композиция является особенно подходящей для лечения и/или предотвращения диареи. Правильная осмоляльность в сочетании с олигосахаридами уроновой кислоты и пробиотиками уменьшает время, в течение которого нормальный стул восстанавливается.
По некоторым причинам также важно, что данная композиция не имеет избыточной удельной калорийности, обеспечивая, однако, достаточно калорий для питания субъекта. Поэтому жидкое питание предпочтительно имеет удельную калорийность между 0,1 и 2,5 ккал/мл, еще более предпочтительно удельную калорийность между 0,5 и 1,5 ккал/мл, наиболее предпочтительно между 0,6 и 0,9 ккал/мл. Оптимальная удельная калорийность также вносит свой вклад в снижение вероятности диареи.
Данные композиции предпочтительно содержат минеральные вещества, микроэлементы и витамины, холин, таурин, карнитин, миоинозит и/или их смеси.
Области применения
Данная композиция особенно применима для питания детей. Поэтому данное изобретение относится также к применению данной композиции для получения питательного состава для вскармливания детей. Предпочтительно дети имеют возраст 0-36 месяцев, предпочтительно возраст от 0 до 18 месяцев.
Композиция по данному изобретению, как было обнаружено, особенно применима в качестве детского питания. Также композиция является особенно подходящей для нормализации популяции Bifidobacterium и/или Lactobacillus соответственно распределению разновидностей у детей, вскармливаемых грудным молоком, в желудочно-кишечном тракте детей, вскармливаемых только частично грудным молоком или вообще без него, в частности, тех, которые являются преждевременно рожденными детьми, доношенными детьми, а также детей, которые находятся в периоде адаптации к твердой пище. Поэтому данное изобретение относится к способу обеспечения питанием ребенка человека, указанный способ включает введение ребенку данной композиции.
Таким образом, дополнительный аспект данного изобретения относится к пищевому препарату, содержащему композицию, которая определена выше. В одном варианте воплощения пищевой препарат является детским питанием.
Кишечная флора оказывает важное воздействие на нарушения, такие как желудочно-кишечные расстройства, иммунные расстройства и/или эндокринные расстройства. Поэтому в дополнительном аспекте данное изобретение относится к способу, данная композиция может быть использована в производстве медикамента для применения в способе предотвращения и/или лечения желудочно-кишечного расстройства, иммунного расстройства и/или эндокринных расстройств. В частности, аллергия, аллергический ринит, гиперчувствительность к пище, атопический дерматит, экзема, астма, диарея, инфекционная и ассоциированная с антибиотиками диарея, кишечное воспаление, инфекция, запор, кишечные спазмы, колики, синдром приобретенного иммунодефицита, рак, кистозный фиброз и/или диабет могут быть соответственно излечены и/или предупреждены данной композицией. В предпочтительном варианте воплощения данное изобретение относится к способу лечения и/или предупреждения аллергии и/или инфекции. В предпочтительном варианте воплощения данное изобретение относится к способу лечения и/или предупреждения синдрома приобретенного иммунодефицита.
В дополнительном предпочтительном варианте воплощения данную композицию применяют в способе лечения и/или предотвращения инфекции у пациентов, страдающих от аллергии, аллергического ринита, пищевой гиперчувствительности, атопического дерматита, экземы, астмы, диареи, инфекционной или ассоциированной с антибиотиками диареи, запора, кишечных спазмов, колик, синдрома приобретенного иммунодефицита, рака, диабета, кистозного фиброза, пациентов, подвергающихся хирургии, пациентов, подвергающихся противораковой терапии, и пациентов, страдающих от повреждений, вызванных теплом, трением, электричеством, радиацией или химикатами. Пониженная вероятность возникновения или интенсивность указанных болезней являются результатом оптимизированной кишечной флоры, особенно оптимизированной популяции вида Bifidobacterium и/или оптимизированной популяции вида Lactobacillus и уменьшенного прилипания патогенных бактерий.
В другом варианте воплощения данное изобретение относится к способу предупреждения вагинальных инфекций, указанный способ включает местное применение данной композиции в подходящей для введения форме.
ПРИМЕРЫ
Пример 1: Композиция с гидролизатом пектина, пребиотическим волокном и пробиотическими бактериями
Детское питание, содержащее на 12,6 грамма порошка: 1,6 грамма белка, 3,6 грамма жира, 6,4 грамма легко усваиваемых углеводов (в основном лактозы), 0,8 грамма неусваиваемых углеводов, из которых 0,60 грамм трансгалактoолигосахаридов, 0,07 грамма инулина (Raftilin HP, Orafti), 0,12 грамма гидролизованного лиазой пектина со средней степенью полимеризации 4 и 1×109 cfu Bifidobacterium breve M-16V (Moringa) и 1×109 cfu Lactobacillus paracasei LAFTIL26 (DSM Food Specialties, the Netherlands).
Изобретение относится к фармакологии и медицине и представляет собой применение композиции, содержащей пробиотические бактерии рода Lactobacillus или Bifidobacterium или обоих и от 25 до 100 мас.% олигосахарида уроновой кислоты, в котором, по меньшей мере, 50% остатков выбраны из труппы, состоящей из гулуроновой кислоты, маннуроновой кислоты, галактуроновой и глюкуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в композиции, для изготовления питательной композиции, для лечения и/или предотвращения инфекции патогеном у субъекта. Изобретение обеспечивает синергетическое ингибирование патогенов. 3 н. и 14 з.п. ф-лы.
1. Применение композиции, содержащей пробиотические бактерии рода Lactobacillus или Bifidobacterium или обоих и от 25 до 100 мас.% олигосахарида уроновой кислоты, в котором, по меньшей мере, 50% остатков выбраны из группы, состоящей из гулуроновой кислоты, маннуроновой кислоты, галактуроновой и глюкуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в композиции, для изготовления питательной композиции, для лечения и/или предотвращения инфекции патогеном у субъекта.
2. Применение по п.1, где указанный олигосахарид уроновой кислоты является гидролизованным пектином.
3. Применение по п.1 или 2, где питательная композиция дополнительно содержит пребиотическое волокно, которое стимулирует рост кишечных пробиотических бактерий, выбранное из группы, состоящей из фруктанов, фруктоолигосахаридов, неусваиваемых декстринов, галактоолигосахаридов (включая трансгалактоолигосахариды), ксилоолигосахаридов, олигосахаридов соевых бобов, арабиноолигосахаридов, глюкоолигосахаридов, манноолигосахаридов, фукоолигосахаридов и их смесей.
4. Применение по п.1 или 2, где указанным субъектом является ребенок или пациент, который подвергается хирургии или лечению антибиотиками.
5. Композиция детского питания, пригодного для кормления ребенка, содержащая
a. пробиотические бактерии рода Lactobacillus или Bifidobacterium или обоих; и
b. от 25 до 100 мас.% олигосахарида уроновой кислоты, в котором, по меньшей мере, 50% остатков выбраны из группы, состоящей из гулуроновой кислоты, маннуроновой кислоты, галактуроновой и глюкуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в композиции.
6. Композиция детского питания по п.5, содержащая от 25 до 100 мас.% олигосахарида галактуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты в детском питании.
7. Композиция детского питания по п.5 или 6, содержащая Bifidobacterium и дополнительно содержащая неусваиваемый олигосахарид, выбранный из группы, состоящей из фруктанов, фруктоолигосахаридов, неусваиваемых декстринов, галактоолигосахаридов (включая трансгалактоолигосахариды), ксилоолигосахаридов, олигосахаридов соевых бобов, арабиноолигосахаридов, глюкоолигосахаридов, манноолигосахаридов, фукоолигосахаридов и их смесей.
8. Композиция детского питания по п.5 или 6, где олигосахарид уроновой кислоты получают ферментативным перевариванием пектина пектин-лиазой, пектиновой лиазой, эндополигалактуроназой и/или пектиназой.
9. Композиция детского питания по п.5 или 6, где олигосахарид уроновой кислоты имеет следующую структуру:
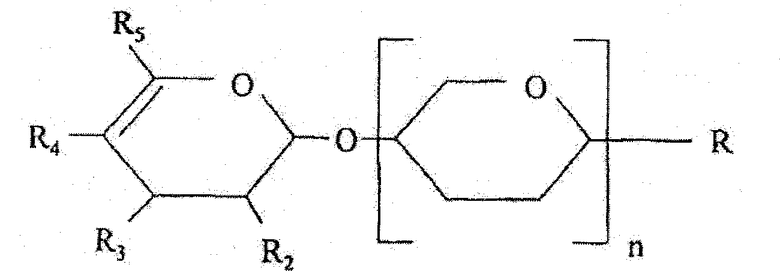
где R выбран из группы, состоящей из водорода, гидрокси или кислотной группы, и по меньшей мере один радикал, выбранный из группы, состоящей из R2, R3, R4 и R5, представляет группу N-ацетилнейраминовой кислоты, N-гликолоилнейраминовой кислоты, свободной или этерифицированной карбоновой кислоты, группу серной кислоты и/или группу фосфорной кислоты, и остальные R2, R3, R4 и R5 представляют гидрокси и/или водород, и n означает целое число 1-99.
10. Композиция детского питания по п.5 или 6, содержащая Bifidobacterium.
11. Композиция детского питания по п.5 или 6, содержащая Lactobacillus.
12. Композиция детского питания по п.5 или 6, содержащая Lactobacillus и Bifidobacterium.
13. Композиция детского питания по п.5 или 6, содержащая неусваиваемые олигосахариды, свободные от уроновой кислоты.
14. Композиция обогатителя грудного молока, включающая
a. пробиотические бактерии рода Lactobacillus или Bifidobacterium или обоих; и
b. от 25 до 100 мас.% олигосахарида уроновой кислоты, в котором, по меньшей мере, 50% остатков выбраны из группы, состоящей из гулуроновой кислоты, маннуроновой кислоты, галактуроновой и глюкуроновой кислоты с DP от 2 до 250 на основе общей массы уроновой кислоты.
15. Применение композиции, определенной в любом из пп.5-14, для изготовления питательной композиции для применения в питании детей.
16. Применение по любому из пп.1-4, где указанная композиция определена в любом из пп.5-14.
17. Применение по п.1, где питательная композиция предназначена для лечения и/или предупреждения инфекции у пациента, страдающего от аллергии, аллергического ринита, пищевой гиперчувствительности, атопического дерматита, экземы, астмы, диареи, инфекционной и ассоциированной с антибиотиками диареи, запора, кишечных спазмов, колик, синдрома приобретенного иммунодефицита, рака, диабета, кистозного фиброза, пациентов, подвергающихся хирургии, пациентов, подвергающихся противораковой терапии и пациентов, страдающих от повреждений, вызванных теплом, трением, электричеством, радиацией или химикатами.
| WO 2004000340 A2, 31.12.2003 | |||
| JP 2004182609 A, 02.07.2004 | |||
| ДИЕТИЧЕСКАЯ АБСОРБИРУЕМАЯ КОМПОЗИЦИЯ, СПОСОБНАЯ УЛУЧШАТЬ БИОЛОГИЧЕСКОЕ РАВНОВЕСИЕ ФЛОРЫ КИШЕЧНОГО ТРАКТА | 1996 |
|
RU2152792C1 |
Авторы
Даты
2011-05-27—Публикация
2006-04-18—Подача