Настоящее изобретение относится к способу пивоварения, предусматривающему добавление каталазной композиции, не содержащей или по существу не содержащей глюкозооксидазу, с целью улучшения вкуса и/или стабильности вкуса готового пива.
Известно применение в процессах пивоварения ферментных композиций, содержащих каталазу и глюкозооксидазу, улучшающих стабильность вкуса пива. Однако результаты, полученные при использовании композиций каталазы-глюкозооксидазы, были не вполне успешны, и было сделано предположение, что глюкозооксидаза и сульфит могут оказаться привлекательной альтернативой (Blockmans et al. ASBC Journal 1987, vol.45, 85-90). Таким образом, существует потребность в дальнейших способах улучшения стабильности вкуса пива.
Авторы настоящего изобретения установили, что эффективность ферментной обработки может быть значительно повышена путем применения каталазной композиции без глюкозооксидазы. Таким образом, настоящее изобретение обеспечивает способ пивоварения, предусматривающий добавление каталазной композиции (E.C. 1.11.1.6), не содержащей или по существу не содержащей глюкозооксидазу, к суслу, бродящему суслу или сбродившему пиву для улучшения вкуса и/или стабильности вкуса готового пива.
Процесс пивоварения хорошо известен специалисту, квалифицированному в данной области техники. Стандартный метод может быть проведен следующим образом: исходным материалом является осоложенный (то есть смоченный, проросший и затем высушенный) ячмень и/или неосоложенные добавки, называемые зерном для размола. В процессе затирания солода, когда зерно размалывают и смешивают с водой, нагревают и перемешивают, углеводы расщепляются до сбраживаемых сахаров при помощи ферментов, естественно присутствующих в солоде. После затирания солода необходимо отделить жидкий экстракт (сусло) от твердых частиц (частицы шелухи и добавки), чтобы получить прозрачное сусло. Важна фильтрация сусла, так как твердые частицы содержат большие количества белка, слабомодифицированного крахмала, жирового материала, силикатов и полифенолов (танинов) и белков. После добавки хмеля сусло кипятят. В результате происходит осаждение полифенолов. После охлаждения и удаления осадка готовое пивное сусло (суслa) аэрируют, после чего добавляют дрожжи. После основного брожения, которое обычно продолжается 5-10 дней, большую часть дрожжей удаляют и так называемое зеленое пиво (b) хранят при низкой температуре, обычно при 0-5°C, от одной до 12 недель. В течение данного периода оставшиеся дрожжи выпадают вместе с полифенолами. Для удаления остатка излишних полифенолов проводят фильтрацию. Сбродившее пиво (c) можно теперь газировать перед розливом в бутылки. Диоксид углерода не только способствует восприятию "полноты" или насыщенности вкуса и усиливает вкус, но он также усиливает потенциал пенообразования и играет важную роль в повышении срока годности продукта.
Не связываясь с конкретной теорией, предполагается, что процессы окисления в процессе соложения и затирания солода являются основной причиной возникновения посторонних привкусов и нестабильности вкуса в бутылочном пиве. Основными продуктами окисления являются ДМС (диметилсульфид) и транс-2-ноненаль (T2N). ДМС и T2N являются одними из основных источников посторонних привкусов в пиве. Окисление и образование активного кислорода обусловлено присутствием липоксигеназы, образующейся в процессе соложения, а также неферментативным окислением, вызываемым активной медью (Cu+) и железом, что приводит к образованию свободных радикалов и перекиси водорода. Нативная каталаза солода уменьшает уровень кислородных радикалов в солоде. Однако нативная каталаза легко инактивируется в процессе соложения и на первой стадии затирания солода. Применение каталазы в процессах пивоварения известно из уровня техники (EP 1122303). Однако применения предшествующего уровня техники включают применение ферментных композиций, содержащих глюкозооксидазу и каталазу. При использовании ферментных композиций, содержащих каталазу и не содержащих или по существу не содержащих глюкозооксидазу, в отношении вкуса и/или стабильности вкуса производится улучшенный положительный эффект. Не связываясь с конкретной теорией, предполагается, что улучшение стабильности вкуса, достигнутое способом по изобретению, можно объяснить уменьшением количества продуктов окисления, обусловленных присутствием H2O2, образовавшейся в результате действия глюкозооксидазы.
В контексте настоящего изобретения понятие "по существу не содержащий глюкозооксидазу" следует понимать так, что отношение активности глюкозооксидазы к активности каталазы GODU/CIU в ферментной композиции составляет менее 1, предпочтительно менее 0,75, например менее 0,50, менее 0,25, менее 0,10, менее 0,50, менее 0,25, менее 0,10, менее 0,05, менее 0,01, менее 0,001, менее 0,0001, и наиболее предпочтительно менее 0,00001. Предпочтительно активность глюкозооксидазы ниже предела обнаружения.
Согласно настоящему изобретению, ферментную композицию, содержащую каталазу, добавляют во время пивоваренного процесса. Ферментная композиция не содержит или по существу не содержит глюкозооксидазу. Ферментная композиция, содержащая каталазу, может быть добавлена на любой стадии во время процесса, например, к суслу, пивному суслу, молодому пиву и/или сбродившему пиву. Предпочтительно ферментная композиция, содержащая каталазу, добавляется перед и/или во время стадии затирки солода. Ферментная композиция, содержащая каталазу, предпочтительно добавляется к смеси зерна и воды, суслу. Каталаза может быть добавлена в количестве 0,02-200 мг активного белка (ЕР)/кг сусла, предпочтительно 0,2-20 мг активного белка (ЕР)/кг сусла, более предпочтительно 1-10 мг активного белка (ЕР)/кг сусла. Каталаза может быть добавлена в количестве от 1 CIU до 10 милл. CIU/кг сусла, предпочтительно от 10 CIU до 1 милл. CIU/кг сусла, более предпочтительно от 100 CIU до 0,1 милл. CIU/кг сусла и наиболее предпочтительно от 1000 CIU до 1000 милл. CIU/кг сусла.
Предпочтительно каталаза представляет собой микробную каталазу, например каталазу, выделенную из грибов или бактерий. Предпочтительно каталаза получена из штамма Scytalidium sp., предпочтительно S.thermophilum, штамма Aspergillus sp., предпочтительно A.niger, штамма Micrococcus sp., предпочтительно M.luteus.
Предпочтительно ферментная композиция, содержащая каталазу, не содержащая или по существу не содержащая глюкозооксидазу, является однокомпонентной композицией, полученной в результате очистки ферментной композиции, полученной из нерекомбинантного штамма-продуцента. Способы очистки полипептидов, включая ферменты, хорошо известны квалифицированному специалисту.
Более предпочтительно ферментную композицию, содержащую каталазу, получают с помощью рекомбинантных технологий. С помощью рекомбинантных технологий может быть получена ферментная композиция, содержащая особо чистую каталазу, например композицию, не содержащую или по существу не содержащую глюкозооксидазу. Способы получения рекомбинантных полипептидов, включая ферменты, хорошо известны квалифицированному специалисту.
Предпочтительная коммерческая ферментная композиция, полученная с помощью рекомбинантных технологий, поставляется фирмой Novozymes A/S под маркой Terminox Ultra™ и фирмой Genencor Int. под маркой Fercolase. Предпочтительная коммерческая однокомпонентная ферментная композиция, полученная из Aspergillus niger, поставляется фирмой Novozymes A/S под маркой Catazyme. В предпочтительном варианте осуществления ферментная композиция также содержит лакказу.
Пиво, приготовленное способом по изобретению, может быть любым типом пива. Предпочтительные типы пива включают эли, крепкие эли, стауты, портеры, лагеры, горькое пиво, экспортное пиво, солодовые напитки, хаппошу, крепкое пиво, легкое пиво, низкокалорийное пиво или светлое пиво.
Способы по изобретению могут предусматривать добавление гидрогеля диоксида кремния, кизельгура и/или поливинилполипирролидона (PVPP) к сброженному суслу и фильтрацию с целью придания пиву прозрачности.
Каталаза, применяемая в способах по изобретению, вызывает снижение концентрации основных соединений, обуславливающих посторонний привкус. Предпочтительно концентрация ДМС в сусле и/или пиве уменьшается по сравнению с уровнем ДМС в сусле или пиве, произведенном в соответствии со стандартным способом затирания солода, например, по меньшей мере, на 10%, по меньшей мере, на 20%, по меньшей мере, на 30%, по меньшей мере, на 40%, по меньшей мере, на 50% или, по меньшей мере, на 60% соответственно, по отношению к уровню в сусле или пиве, произведенном согласно конгрессному способу затирания солода. Предпочтительно концентрация T2N в сусле или пиве уменьшается, соответственно по сравнению с уровнем T2N в сусле или пиве, произведенном в соответствии с обычным способом, например, по меньшей мере, на 10%, по меньшей мере, на 20%, по меньшей мере, на 30%, по меньшей мере, на 40%, по меньшей мере, на 50% или, по меньшей мере, на 60%.
Активность каталазы
Активность каталазы может быть измерена в CIU. Каталаза катализирует реакцию первого порядка:
2H 2 O 2 → 2H 2 O + O 2
Расщепление перекиси водорода измеряют с помощью спектрофотометрии при 240 нм. Время, затраченное на определенное уменьшение поглощения при определенной концентрации H2O2, является выражением активности каталазы. Одна CIU определяется как активность фермента, при которой расщепляется один мкМ H2O2 в минуту при pH 7,0 и 25°C, а концентрация H2O2 снижается от с 10,3 до 9,2 мМ.
Условия реакции:
Детектирование:
Подробное описание стандартной методики CIU (EB-SM-0250,02/01) доступно по запросу от Novozymes A/S.
Активность глюкозооксидазы
Единица глюкозооксидазы (GODU) представляет собой количество фермента, который окисляет 1 мкМ бета-D-глюкозы в минуту. Глюкозооксидаза (бета-D-глюкоза:кислород-1-оксидоредуктаза, EC 1.1.3.4.) окисляет бета-D-глюкозу в присутствии кислорода до дельта-глюконолактона и перекиси водорода. Образовавшаяся перекись водорода окисляет ABTS-R (2,2-азино-ди-(3-этилбензтиазолин)-6-сульфонат) в присутствии пероксидазы (POD). В результате развивается зеленовато-синее окрашивание, которое фотометрически измеряется при 405 нм.
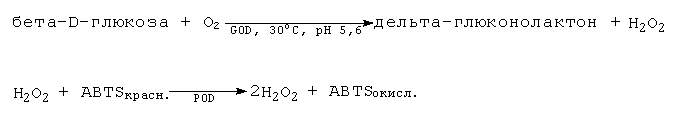
Условия реакции
Подробное описание стандартной методики GODU (EB-SM-0244.02) доступно по запросу от Novozymes A/S.
МАТЕРИАЛЫ И МЕТОДЫ
ESR-cпектроскопия (ESR - электронный спиновый резонанс)
В течение последних нескольких лет для прогноза стабильности вкуса пива использовали спектроскопию электронного спинового резонанса (ESR-спектроскопию), с помощью которой определяют так называемое время задержки пива в ускоренной выдержке пива при повышенных температурах (60°С). Значение времени задержки, определенное данным способом, рассматривается как критерий эндогенного антиоксидантного потенциала пива, который прежде всего обусловлен восстанавливающими соединениями (например, SO2, аскорбиновой кислотой), и само по себе непосредственно связано с устойчивостью пива к окислению.
Измерение времени задержки с помощью ESR-спектроскопии основано на косвенном обнаружении образования радикалов в пиве во время ускоренной выдержки пива. Образующиеся короткоживущие активные радикалы можно обнаружить, улавливая их спиновыми ловушками и детектируя долгоживущие спиновые аддукты, используя ESR-спектроскопию.
В течение определенного промежутка времени образование радикалов может задерживаться или предотвращаться благодаря эндогенной антиоксидантной активности пива (фаза задержки). После фазы задержки количество радикалов начинает быстро увеличиваться с течением временем.
Эндогенный Антиоксидантный Потенциал (ЭАП) отражает естественную способность образца пива подавлять образование радикалов при нагреве до 63°C и контакте с атмосферным кислородом. Чем дольше фаза задержки в сигнале ESR, тем выше ЭАП пива. После фазы задержки, согласно данной точке зрения, радикалы в пиве будут образовываться естественно. Чтобы сравнить различное пиво, общий ESR (T300-700) сигнал за установленное время считают эквивалентным количеству радикалов, образованных на определенный момент времени, при 63°C и контакте с атмосферным воздухом. Чем ниже сигнал, тем меньше радикалов образуется в образце пива.
Антиоксидантный Показатель Напитка (АПН), определяемый как АПН(обр.)=ЭАП-значение/ΔSO2-содержание [мин*л/мг], измеряет влияние внесенного в пиво SO2, а также взаимодействие с естественно присутствующими в пиве антиоксидантами.
Высокое значение ЭАП, так же, как и высокое значение АПН, соотносится с лучшей стабильностью пива при хранении (Uchida et al. 1996, J.Am.Brew.Chem. 54 205-211, Andersen et al. 1998. J. Agric. Food Chem. 1998, Т.46, стр.1272-1275, Andersen et. al. 2000. J. Agric. Food Chem. 2000, Т.48, стр.3106-3111).
Пример 1
Пивное сусло было приготовлено из зерна, содержащего 35% солода (Esperanza Riego), 15% неосоложенного ячменя и 50% кукурузной крупы. Зерно затерли с 0 м.д. каталазы (контроль), 2 м.д. каталазы (как мг/кг DS) и 10 м.д. контроль. Использовалась высокоочищенная каталаза из Aspergillus niger, имеющая активность 132000 CIU/мл и не имеющая обнаруживаемой активности глюкозооксидазы. Сусло сбраживалось пивными дрожжами до лагерного пива. При отправке на выдержку после брожения к молодому пиву были добавлены следующие добавки: 34 г/гл Britesorb и 2 г/гл эриторбата натрия.
Сусло и пиво были исследованы, соответствующие результаты приведены в таблицах 1 и 2.
Анализ сусла из зерна, затертого с 0 м.д. каталазы (контроль), 2 м.д. каталазы (как мг/кг DS) и 10 м.д. контроль
Анализ пива из зерна, затертого с 0 м.д. каталазы (контроль), 2 м.д. каталазы (как мг/кг DS) и 10 м.д. контроль
Пиво было подвергнуто органолептическому анализу, выполненному подготовленной группой экспертов. Методика интенсивного теста на стабильность при перемешивании была следующей: 24 часа при перемешивании и 3 дня при 38°C. Принятая шкала стабильности вкуса - от 1 до 7. 1 показывает, что привкус окисления отсутствует, а 7 показывает, что пиво имеет высокую степень окисления. Результаты приведены в таблице 3.
Стабильность вкуса. Шкала стабильности вкуса от 1 до 7, где значение 1 показывает, что привкус окисления отсутствует, а 7 показывает, что пиво имеет высокую степень окисления
Пример 2
С использованием 100% ячменного пльзенского солода было сварено классическое немецкое пиво пльзенского типа. Ферменты были добавлены во время стадии затирания солода с последующей варкой сусла, созреванием и хранением в бутылках. Используемые ферменты представляли собой композицию каталазы A. niger, содержащую побочную активность глюкозооксидазы (Catazyme®), и композицию каталазы Scytalidium thermophilum без побочной активности глюкозооксидазы (Terminox Ultra®).
Бутылочное пиво хранилось при 20°C и было исследовано через 4 и 12 недель.
Эндогенный Антиоксидантный Потенциал (мин) и общий ESR (общий сигнал) после 4 недель хранения и после 12 недель хранения при 20°C
Пример 3
С использованием ячменного пльзенского солода, а также кукурузного крахмала в качестве добавки было сварено пиво пльзенского типа. Ферменты были добавлены во время стадии затирания солода с последующей варкой сусла, созреванием и хранением в бутылках. Используемые ферменты представляли собой композицию каталазы A.niger, содержащую побочную активность глюкозооксидазы (Catazyme®), очищенный образец каталазной композиции A.niger без побочной активности глюкозооксидазы и композицию каталазы Scytalidium thermophilum без побочной активности глюкозооксидазы (Terminox Ultra®).
Бутылочное пиво хранилось при 20°C и было исследовано через 120 дней.
Антиоксидантный Показатель Напитка (мин*л/мг SO
2
) и общий ESR (общий сигнал) после 120 дней хранения при 20°C
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МАЛЬТОБИОНАТА | 2008 |
|
RU2495130C2 |
| СПОСОБ ПИВОВАРЕНИЯ | 2008 |
|
RU2475526C2 |
| СПОСОБ ПИВОВАРЕНИЯ | 2009 |
|
RU2524118C2 |
| ПИТАТЕЛЬНЫЙ НАПИТОК И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2531436C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУСЛА | 2007 |
|
RU2426775C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИВНОГО СУСЛА | 2012 |
|
RU2600885C2 |
| АРАБИНОКСИЛООЛИГОСАХАРИДЫ В ПИВЕ | 2008 |
|
RU2444565C2 |
| СПОСОБ ПИВОВАРЕНИЯ | 2010 |
|
RU2531522C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИВА "ВОЛЖАНИН" | 1999 |
|
RU2173701C2 |
| СПОСОБ ЗАТИРАНИЯ | 2004 |
|
RU2376347C2 |
Настоящее изобретение относится к способу пивоварения, предусматривающему добавление каталазной композиции к суслу. Причем указанная каталазная композиция имеет отношение глюкозооксидазной активности к каталазной активности GODU/CIU менее 0,001. Это позволяет достичь улучшения вкуса и/или стабильности вкуса готового пива. 6 з.п. ф-лы, 5 табл.
1. Способ производства пива, включающий добавление каталазной композиции к суслу для улучшения вкуса и/или стабильности вкуса готового пива, причем указанная каталазная композиция имеет отношение глюкозооксидазной активности к каталазной активности GODU/CIU менее 0,001.
2. Способ по п.1, в котором каталазную композицию добавляют к суслу в количестве 0,02-200 мг ферментного белка на 1 кг сусла.
3. Способ по п.1, в котором каталаза происходит из микроорганизма, являющегося бактерией или грибком.
4. Способ по п.3, в котором каталаза происходит из микроорганизма рода Scytalidium sp., Aspergillus sp или Micrococcus sp.
5. Способ по п.4, в котором каталаза происходит из микроорганизма вида Scytalidium thermophilum, Aspergillus niger или Micrococcus luteus.
6. Способ по п.1, в котором каталаза получена рекомбинантной технологией.
7. Способ по п.3, в котором ферментная композиция дополнительно содержит лакказу.
| Операционный зажим | 1983 |
|
SU1122303A1 |
| JP 60083579 А, 11.05.1985 | |||
| Ограничитель перенапряжений | 1984 |
|
SU1294184A1 |
Авторы
Даты
2011-06-27—Публикация
2007-03-06—Подача