Настоящее изобретение относится к использованию стеклообразных веществ для стабилизации биологических материалов.
Известно, что из некоторых материалов, в частности из некоторых сахаров, может образовываться стекло, то есть некристаллическое твердое вещество, которое обеспечивает стабилизацию биологического материала, распределенного в нем в форме суспензии или твердого раствора. Примерами таких биологических материалов являются, например, вакцины и инсулин. Иногда биологический материал должен быть в жидкой форме, например при осуществлении инъекции пациенту. Для этой цели было предложено формировать стеклообразный материал в форме частиц, взвешенных в инертной нетоксичной жидкости.
В этом случае основной проблемой является выбор подходящей жидкости. Традиционными жидкими носителями, используемыми для инъекций лекарственных средств, являются масла, плотность которых меньше, чем плотность сахарных стекол, обычно используемых для целей стабилизации, и поэтому частицы сахарного стекла опускаются в жидкости в нижнюю часть резервуара. Осаждающиеся частицы со временем могут уплотняться на дне резервуара. Хотя резервуар можно встряхивать для перемешивания препарата с целью восстановления суспензии перед введением препарата пациенту, однако такое перемешивание должно быть очень энергичным и продолжительным, чтобы можно было получить необходимый результат. Существует неприемлемая вероятность того, что такое перемешивание не будет выполнено должным образом, в результате чего эффективность лекарственного средства будет неудовлетворительной.
В последнее время было предложено в качестве жидкого носителя использовать перфторуглероды. Эти соединения имеют высокую плотность, и в этом случае можно регулировать плотность частиц путем добавления в стекло более плотного материала, например фосфата кальция, чтобы плотности носителя и частиц были примерно одинаковыми. Практика показала действенность такой технологии для экстренных случаев или при ее использовании в малых масштабах, однако использование перфторуглеродов в промышленных масштабах связано с нежелательным воздействием на верхнюю часть земной атмосферы. Такие материалы необычайно устойчивы даже при воздействии интенсивных потоков ультрафиолетового излучения и могут накапливаться в стратосфере в течение многих лет, создавая условия для глобального потепления.
В настоящем изобретением предлагается композиция, содержащая тело, состоящее из биологического материала и из стеклообразного материала, обеспечивающего стабилизацию биологического материала, причем тело содержит по меньшей мере одну полость, заполненную газом.
Предпочтительно используется большое количество таких "тел", каждое из которых является частицей порошка. При использовании подходящего управления производственным процессом можно уменьшать плотность таких частиц вплоть до низкой плотности жидкости, например, масла, используемого в качестве жидкого носителя. В этом случае можно предположить, что будет получена устойчивая суспензия с использованием традиционных жидкостей, полная безопасность которых уже была подтверждена практикой.
Для каждой частицы можно использовать только одну полость, так что получается нечто вроде надутого шарика, или же получают структуры в форме пены или сот, которые содержат много полостей. В качестве альтернативного варианта могут использоваться структуры, являющиеся промежуточными между указанными крайними случаями, то есть в одной частице может быть несколько полостей.
Стеклообразные частицы могут быть сформированы путем использования раствора стеклообразующего материала, смешанного с биологическим материалом. Затем эта смесь нагревается в сухой среде для выпаривания растворителя (обычно это вода) в условиях, необходимых для получения некристаллической твердой фазы, то есть стекла. Если при проведении такого процесса известна температура, при которой смесь находится в переходном состоянии между жидкой и твердой фазами, то можно подобрать подходящую добавку, которая при указанной температуре образует газ, причем стеклообразование происходит таким образом, что газ захватывается стеклом, в результате чего формируются газовые полости, представляющие существенную часть изобретения.
В соответствии со вторым вариантом осуществления изобретения предлагается способ получения стеклообразного продукта, который состоит из следующих стадий:
i) смешивание первого жидкого материала, способного образовывать стекло, со вторым материалом, из которого можно получать газ; и
ii) проведение процесса, при котором из первого материала образуется стекло, и в то же время из второго материала образуется газ;
в результате чего формируется стеклообразная структура, содержащая газонаполненное стекло.
Существует огромное многообразие стеклообразных материалов, которые могут использоваться для целей изобретения. К подходящим материалам относятся сахара, такие как, например, рафиноза и трегалоза, палатинит (смесь глюкопиранозил-сорбита и глюкопиранозил-маннита), глюкопиранозил-сорбит, глюкопиранозил-маннит, лактит и моносахаридные спирты.
Проблема, связанная с использованием сахарных стекол для стабилизации биологических материалов, заключается в том, что для достижения необходимого эффекта стабилизации необходимо удалить из стекла почти всю воду. Для достижения этой цели могут потребоваться условия (например, высокая температура), которые несовместимы с условиями, необходимыми для получения стеклообразного состояния и для предотвращения повреждения активного биологического материала. Однако мы обнаружили, что указанная проблема может быть разрешена путем использования вместо сахаров глютаминовой кислоты или ее соли, например глютамата мононатрия (далее - ГМН) в качестве компонента стеклообразующего материала.
ГМН ранее был известен как вещество, обладающее стабилизирующими свойствами при его смешивании с другими стеклообразующими веществами, как описано, например, в патенте США №6872357 и в статье "Выделение микробов после высушивания в глютамате и других веществах", D.I.Annear, опубликованной в августовском выпуске журнала "J. exp. Biol. Med. Sci", 1964, 42, стр.717-722. Однако мы обнаружили, что ГМН может иметь более 3% остаточной влажности, причем он практически не размягчается при содержании влаги до примерно 5% и сохраняет свои стабилизирующие свойства при температурах до примерно 70°С. Кроме того, мы обнаружили, что при переходе в стеклообразное состояние ГМН проявляет ярко выраженное переходное состояние, в котором он находится в форме тягучей сиропообразной полутвердой фазы. Это свойство особенно эффективно для захвата пузырьков газа по мере их формирования.
Обнаружение того обстоятельства, что ГМН и аналогичные соединения могут использоваться в качестве стабилизаторов даже при сравнительно высоком содержании влаги, можно считать обладающим новизной, и таким образом в соответствии с другим вариантом настоящего изобретения предлагается композиция, в которой биологический материал стабилизируется стеклообразным веществом, содержащим глютаминовую кислоту или ее соль, причем стеклообразное вещество в композиции содержит более 3% вес. воды, причем предпочтительным диапазоном величины содержания воды является 4-5%.
Было обнаружено, что при использовании глютаминовой кислоты или ее соли, например ГМН, активный материал (особенно если он содержит адъювант в форме микрочастиц) может вызывать кристаллизацию. Эта проблема может быть разрешена добавлением ингибитора кристаллизации, такого как, например, аспартовая кислота или ее соль. Этот ингибитор кристаллизации предпочтительно сам по себе является стеклообразующим материалом, например аспартат мононатрия (далее - АМН), и два компонента предпочтительно имеют сходную молярную концентрацию (между 4:6 и 6:4) для обеспечения оптимального замедления процесса кристаллизации.
При проведении процесса высушивания раствора стеклообразующего материала с использованием тепла, особенно если осуществляется высушивание материала в форме капелек, повышение температуры капелек сдерживается высокой скоростью испарения с их поверхности, при котором происходит охлаждение. По мере того как раствор становится все более густым и тягучим, подвижность молекул воды относительно поверхности капелек снижается из-за повышения вязкости, и температура капелек повышается по мере того как снижается охлаждение в результате испарения. Таким образом, температура высушиваемых густых капелек быстро повышается по мере того как они начинают затвердевать, образуя стекло.
Газ предпочтительно вводится в стекло путем смешивания стеклообразующего материала (и биологического материала) с химическим реагентом, который разлагается при условиях проведения процесса с выделением газа; однако также может использоваться материал, который становится газообразным без осуществления химических изменений. В любом случае добавка предпочтительно выбирается таким образом, чтобы газ выделялся, когда температура поднимется до такого уровня, при котором стеклообразующий материал находится в густом переходном состоянии между жидкой и твердой фазами. Подходящей добавкой оказался бикарбонат аммония, поскольку при его разложении выделяется газообразный аммиак, углекислый газ и водяные пары примерно при той же температура, порядка 60°С, при которой происходит увеличение вязкости.
Таким образом, использование ГМН является особенно подходящим, поскольку вода в качестве побочного продукта не оказывает неблагоприятного влияния на его стабилизирующие свойства. Однако также можно использовать и другие стеклообразующие материалы, такие как, например, сахара, в частности рафиноза и трегалоза. Использование фосфата кальция представляет особый интерес ввиду его физической прочности. Предполагается, что таким образом мог бы быть сформирован твердый компонент, имеющий сотовую структуру, для формирования конструктивной части, особенно если он будет иметь замкнутую внешнюю поверхность. В этом случае компонент будет иметь высокую прочность и сравнительно малый вес, подобно костям животных организмов. Возможно, такое вещество можно было бы использовать для целей восстановления или замены костей.
В вышеприведенном описании предполагается, что необходимо выбрать добавку, которая имеет присущие ей свойства, обеспечивающие выделение газа в тот момент, когда стеклообразующее вещество находится в полутвердой фазе, то есть оно достаточно густое для захвата газа. Однако имеется альтернативная возможность использования внешнего воздействия для запуска процесса выделения газа точно в требуемый момент времени. Это может быть осуществлено путем воздействия на материал радиации или других стимулирующих факторов, в результате чего происходят физические или химические изменения материала, необходимые для обеспечения выделения газа.
Описание осуществления изобретения будет приведено ниже на примере одного из его вариантов со ссылками на прилагаемые чертежи, на которых показано:
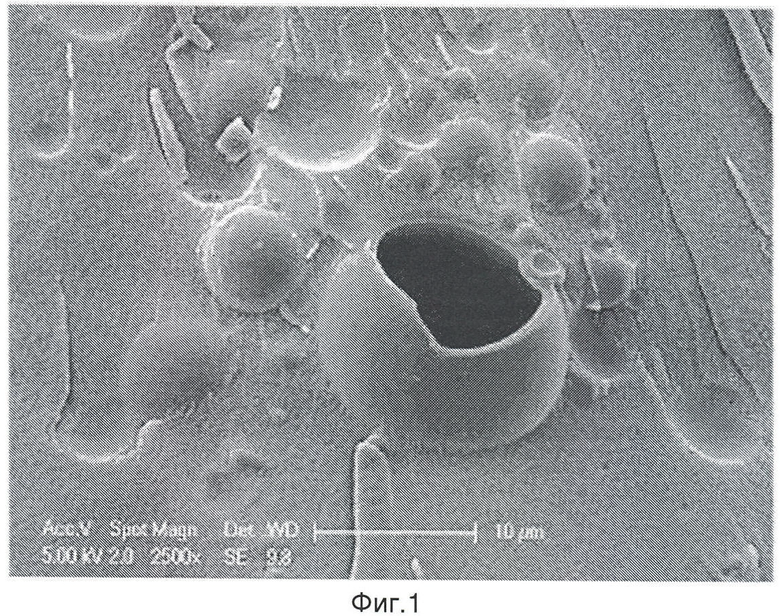
Фигура 1 - вид частиц стекла, полученных из ГМН с использованием предлагаемого в изобретении способа (фотография получена с помощью растрового электронного микроскопа).
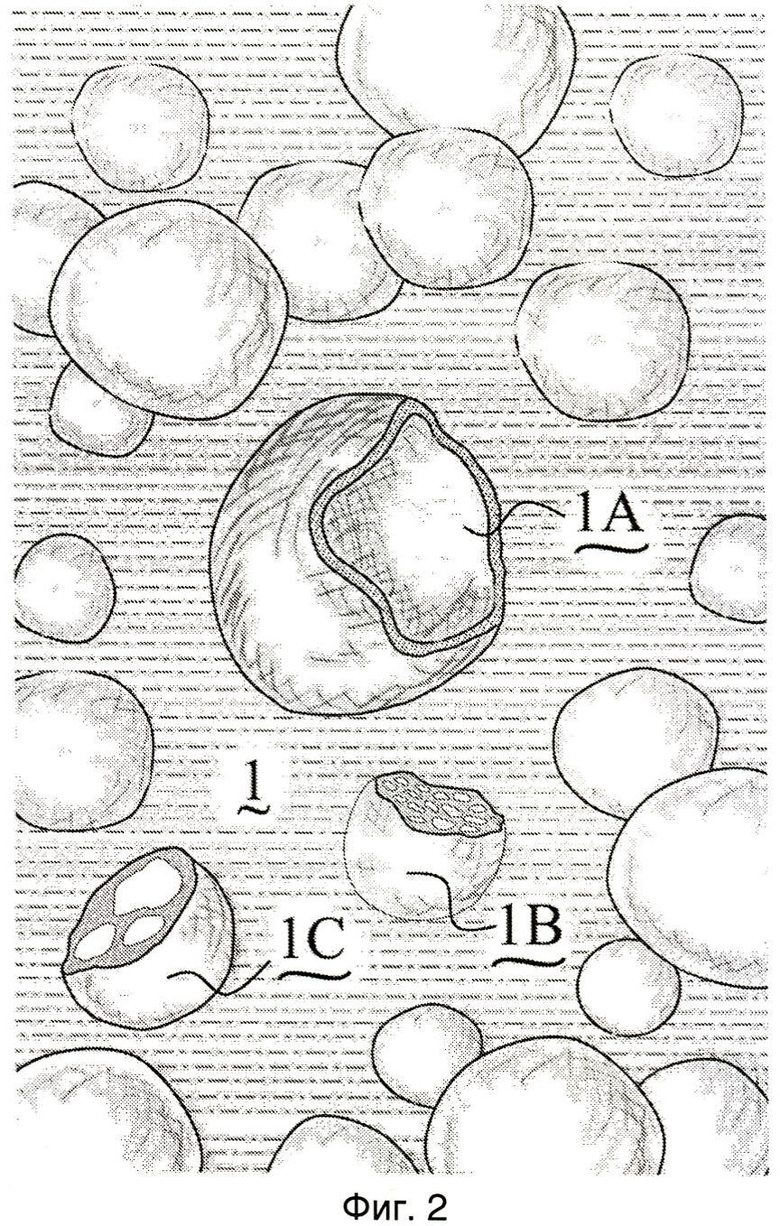
Фигура 2 - схематический вид, иллюстрирующий частицы, представленные на фигуре 1, взвешенные в нетоксичной неводной биологически совместимой жидкости, для формирования устойчивой суспензии, подходящей для введения пациенту с помощью шприца для подкожных инъекций.
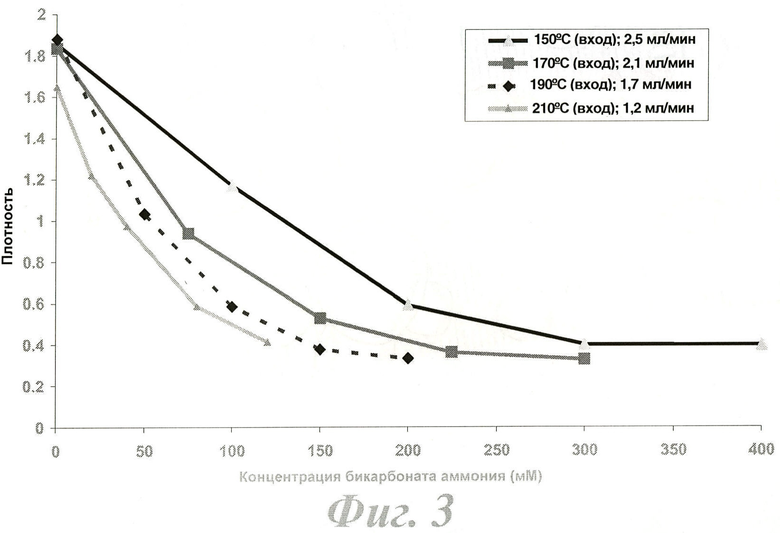
Фигура 3 - графики, содержащие результаты экспериментов, на которых видно как плотность частиц изменяется при изменении концентрации бикарбоната аммония для различных входных температур и расходов сушильного газа распылительной сушилки.
На первой стадии необходимо получить водный раствор, содержащий стеклообразующий агент и газообразующий агент (далее - порообразователь). В этом примере в качестве стеклообразующего агента используется ГМН, а в качестве порообразователя используется бикарбонат аммония. Концентрация ГМН составляет 200 мг/мл, а концентрация бикарбоната аммония составляет 17,4 мг/мл. Затем в раствор добавляется биологический материал. При этом вышеуказанные концентрации изменяются незначительно.
Параметры работы распылительной мини-сушилки Buchi В290 задаются таким образом, что газ поступает в ее сушильную камеру при температуре 150°С и выходит при температуре примерно 95°С. Расход сушильного газа, поступающего в сушильную камеру, установлен на уровне 600 л/час.
Водный раствор подается в сушильную камеру в форме мелкораспыленной струи через форсунку диаметром 0,7 мм. В течение 1-1,5 с водный раствор высушивается и получается порошок, который затем собирается. Порошок отделяется от сушильного газа в циклоне, установленном на выходе из сушильной камеры, и под действием силы тяжести он поступает вниз в бутыль, прикрепленную к нижней части циклона. При этом температура частиц увеличивается от комнатной температуры (порядка 21°С) до теоретического максимума, находящегося в диапазоне 95-120°С (выходная температура). На практике сухие стеклянные частицы выдерживаются при выходной температуре лишь непродолжительное время, поскольку в течение нескольких секунд они отделяются в циклоне от горячих выходных газов и собираются вместе в бутыли, имеющей пониженную температуру.
По мере прохождения частиц через сушильную камеру их температура растет сначала сравнительно медленно, поскольку тепло, поглощаемое частицами, идет на испарение растворителя (воды). Затем при испарении растворителя частицы превращаются в стекло, проходя через промежуточную стадию, на которой они уже не являются жидкими, однако еще не превратились в стекло. В условиях вышеописанного процесса в начале этой промежуточной стадии частицы имеют температуру порядка 60°С. Продолжающийся нагрев обеспечивает удаление большей части остающейся воды, так что продолжается отверждение композиции в результате испарения растворителя, и, наконец, формируется стекло.
На фигуре 1 приведен вид высушенных частиц стекла, полученных с использованием вышеописанного способа (фотография получена с помощью растрового электронного микроскопа). Для анализа внутренней структуры шариков они были смешаны с жидким носителем, который затем был заморожен и расколот в соответствии со стандартной методикой замораживание - скалывание, используемой в микроскопии. Поверхность раскола замороженного носителя образует фон изображения. Можно видеть, что частицы имеют примерно сферическую форму, и их диаметр варьируется от примерно 2 мкм до примерно 15 мкм, то есть они достаточно малы, чтобы могли пройти через иглу шприца для подкожных инъекций. Вышеуказанный размер частиц необходимо сравнивать со средним размером частиц порядка 3-5 мкм, которые получают, используя аналогичный способ, но без бикарбоната аммония.
На фигуре 1 одна из самых больших сфер расколота и видно, что она в целом полая, и толщина стенок составляет примерно 1 мкм. Возможно, что сферы меньших размеров имеют аналогичную или более сложные структуры, которые иллюстрируются на фигуре 2.
На фигуре 2 жидкость Crodamol GTCC указана ссылочным обозначением 1 и в ней взвешены частицы 1А, 1В, 1С, средняя плотность которых равна плотности жидкости. Частица 1А, изображенная без удаленной части для иллюстрации ее внутренней структуры, аналогична частице, расколотой на фигуре 1. Частица 1В, также изображенная без удаленной части, содержит большое количество пустот, заполненных газом, то есть формируется структура, похожая на губку или соты, и частица 1С, представляющая собой промежуточный вариант между частицами 1А и 1В, имеет всего лишь несколько пустот. Плотности этих различных структур будут немного различаться, но все они находятся в диапазоне, обеспечивающем поддержание постоянного взвешенного состояния частиц в результате термодинамических процессов, происходящих при нормальной температуре.
В альтернативном процессе в соответствии с изобретением вместо чистого ГМН используется смесь ГМН и АМН в равных молярных концентрациях (0,5 М), полученная добавлением 0,935 г ГМН и 0,865 г АМН (общее количество 1,8 г) к 10 мл дистиллированной воды. В качестве подходящих материалов могут использоваться мононатрия L-глютамат-моногидрат и мононатрия L-аспарат-моногидрат производства компании Ajinomoto.
Полученный раствор добавляется к материалу вакцины, который содержит 2 мг антигена гепатита В и 160 мг адъюванта (гидроокись алюминия), так что получается отношение количества стабилизатора (в данном случае ГМН и АМН) к количеству адъюванта, равное 10,7:1 (1,8 г:0,16 г). Затем добавляется количество бикарбоната аммония, которое находится в диапазоне, указанном на фигуре 3.
Затем для получения порошка, имеющего низкую плотность, используется вышеупомянутая распылительная мини-сушилка Buchi В290.
В обоих описанных процессах по мере формирования стекла из растворимых в воде стеклообразующих материалов получаемый порошок может быть при необходимости регидрирован с использованием нужного количества стерилизованной воды.
Необходимо понимать, что вышеописанные процессы являются всего лишь примерами использования изобретения. Плотность частиц может точно регулироваться путем добавления выбранного количества бикарбоната аммония, так чтобы эта плотность соответствовала плотности любой возможной жидкости, в которой эти частицы должны быть взвешены. Эксперименты показали, что можно вводить до 1,0 М (79 мг/мл) бикарбоната аммония, и при этой концентрации могут быть получены высушенные сферы, имеющие средний диаметр порядка 20 мкм и плотность порядка 0,64. Другие исследования, результаты которых приведены на фигуре 3, показали, что путем изменения концентрации бикарбоната аммония, расхода жидкости, поступающей в распылительную сушилку, и температуры сушильного газа, подаваемого в сушильную установку, можно точно регулировать плотность получаемых микросфер.
Хотя в качестве агента, используемого для создания полостей в частицах, был указан бикарбонат аммония, необходимо отметить, что для достижения аналогичного результата могут использоваться многие другие материалы, причем наиболее существенным требованием является то, что газ должен выделяться в тот момент, когда стеклообразующий материал находится в густой полутвердой или полужидкой фазе, так что газовые пузырьки могут быть захвачены материалом. Хотя воздействие теплом является обычным способом, обеспечивающим выделение газа из порообразующего агента, могут использоваться и другие альтернативные механизмы, такие как, например, излучение микроволн или ультразвука, для достижения аналогичного результата независимо от температуры. Кроме того, хотя в вышеописанном примере для образования газа используется химическая реакция, газообразование может быть получено просто переходом подходящей добавки из твердой или жидкой фазы в газообразную.
Хотя в качестве стеклообразующих материалов были указаны конкретные сахара и аминокислоты, однако существуют многие другие известные альтернативные материалы, способные обеспечить необходимый эффект стабилизации биологических материалов путем формирования стеклообразной среды.
Необходимо также отметить, что хотя в вышеописанном конкретном примере газ выделяется, когда стекло формируется при испарении растворителя, аналогичного результата можно достичь путем использования стекол, температура фазового перехода которых соответствует температуре газообразующего материала (порообразователя). В таком варианте стекло, смешанное с порообразующим агентом, должно быть нагрето так, чтобы оно размягчилось, и при этом должен выделяться газ для образования необходимых полостей. Последующее охлаждение завершает процесс.
Вышеописанная технология обеспечивает многообещающий способ регулирования плотности частиц, так чтобы она соответствовала плотности жидкости, в которой они должны быть взвешены. Однако выше уже отмечалось, что частицы, получаемые в соответствии с изобретением, могут иметь такую низкую плотность, что они легко будут взвешены в газообразной среде, и поэтому изобретение потенциально применимо для лекарственных средств, предназначенных для введения путем ингаляции. Также было отмечено, что частицы благодаря большой площади их поверхности (включая поверхности внутренних полостей) способны быстро растворяться в водных жидкостях и поэтому могут быть полезны в ситуациях, когда необходимо хранить стабилизированные биологические материалы в твердой устойчивой форме и растворять их непосредственно перед использованием.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТВЕРДЫЕ СИСТЕМЫ ДОСТАВКИ ДЛЯ КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ ВКЛЮЧЕННЫХ В НИХ МОЛЕКУЛ И СПОСОБЫ ИХ ПРИГОТОВЛЕНИЯ | 1995 |
|
RU2177785C2 |
| СУХАЯ СТЕКЛОВИДНАЯ КОМПОЗИЦИЯ ДЛЯ СТАБИЛИЗАЦИИ И ЗАЩИТЫ БИОЛОГИЧЕСКИ АКТИВНОГО МАТЕРИАЛА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2535869C2 |
| КОМПОЗИЦИЯ ДЛЯ ДОСТАВКИ СТАБИЛЬНЫХ ИНЪЕЦИРУЕМЫХ ЖИДКОСТЕЙ И СПОСОБ ДОСТАВКИ | 2000 |
|
RU2259817C2 |
| СТАБИЛИЗИРУЮЩАЯ КОМПОЗИЦИЯ ДЛЯ СУХОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ (ВАРИАНТЫ) | 2011 |
|
RU2573324C2 |
| СТАБИЛИЗИРУЮЩАЯ КОМПОЗИЦИЯ ДЛЯ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ | 2013 |
|
RU2666601C2 |
| СТЕКЛЯННЫЕ ИЗДЕЛИЯ СО СПЕЦИАЛЬНО РАЗРАБОТАННЫМИ ПРОФИЛЯМИ СОСТАВА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2739535C2 |
| СЫРЬЕВАЯ СМЕСЬ ДЛЯ ПОЛУЧЕНИЯ ПЕНОСТЕКЛА | 2009 |
|
RU2445280C2 |
| НАПРАВЛЕННАЯ ДОСТАВКА ВЫСУШЕННЫХ РАСПЫЛЕНИЕМ КОМПОЗИЦИЙ В ЛЕГКИЕ | 2016 |
|
RU2731212C2 |
| Способ получения однофазового стеклообразного материала вещества нестехиометрического состава | 2002 |
|
RU2224725C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУХИХ АМОРФНЫХ ПРОДУКТОВ И СУХИЕ АМОРФНЫЕ ПРОДУКТЫ | 1998 |
|
RU2233105C2 |
Изобретение относится к получению композиции для стабилизации биологического материала, такие как, например, вакцины могут стабилизироваться в некоторых стеклообразных материалах, растворимых в воде. Стеклообразные материалы формируют в виде порошка, взвешенного в неводной жидкости для инъекции пациенту. Возникает проблема поддержания частиц во взвешенном состоянии, поскольку они имеют тенденцию опускаться на дно резервуара. Указанная проблема разрешается добавлением порообразующего агента в раствор, из которого формируется стекло. Порообразующий агент разлагается при испарении раствора, в результате чего формируются полости в полученной стеклообразной структуре, которые снижают ее плотность таким образом, чтобы эта плотность соответствовала плотности жидкости, в которой должна быть суспендирована эта структура. Другие использования изобретения охватывают композиции, предназначенные для ингаляций и для быстрого растворения в водных растворах непосредственно перед их использованием. 2 н. и 22 з.п. ф-лы, 3 ил.
1. Композиция, содержащая частицу, включающую биологический материал и стеклообразный материал для стабилизации биологического материала, причем частица содержит по меньшей мере одну газообразную полость, образованную газообразующей добавкой.
2. Композиция по п.1, отличающаяся тем, что стеклообразный материал содержит стеклообразующий сахар, или глутаминовую кислоту, или ее соль.
3. Композиция по п.2, отличающаяся тем, что соль глутаминовой кислоты представляет собой глутамат натрия.
4. Композиция по п.2, отличающаяся тем, что стеклообразующий сахар выбран из раффинозы, трегалозы, палатинита (смеси сорбитол глюкопиранозила и маннитол глюкопиранозила), сорбитол глюкопиранозила, маннитол глюкопиранозила, лактитола и моносахаридного спирта.
5. Композиция по п.2, отличающаяся тем, что стеклообразный материал содержит более чем от 3% (мас.) воды.
6. Композиция по п.1, отличающаяся тем, что стеклообразный материал содержит более чем от 4 до 5% (мас.) воды.
7. Композиция по п.1, отличающаяся тем, что представляет собой препарат вакцины.
8. Композиция по п.1, в которой множество частиц взвешено в жидкости.
9. Композиция по п.1, отличающаяся тем, что частица содержит множество полостей, причем стеклообразный материал определяет пенистую или сотовую структуру.
10. Композиция по п.1, отличающаяся тем, что стеклообразный материал находится в форме полых частиц, имеющих твердую внешнюю оболочку и полую внутреннюю часть.
11. Композиция по п.1, отличающаяся тем, что стеклообразный материал дополнительно содержит ингибитор кристаллизации.
12. Композиция по п.11, отличающаяся тем, что ингибитор кристаллизации представляет собой стеклообразующий материал.
13. Композиция по п.11 или 12, отличающаяся тем, что ингибитор кристаллизации включает аспартовую кислоту или ее соль.
14. Композиция по п.1, отличающаяся тем, что стеклообразный материал дополнительно содержит фосфат кальция.
15. Композиция по п.1, отличающаяся тем, что стеклообразный материал дополнительно содержит мононатрий аспартат.
16. Композиция по п.1, отличающаяся тем, что по меньшей мере одна полость содержит аммиак, двуокись углерода и/или воду, полученные при разложении бикарбоната аммония.
17. Способ получения композиции, содержащей частицу, включающую биологический материал и стеклообразный материал для стабилизации биологического материала по п.1, включающий следующие стадии:
(i) смешивание первого жидкого материала, способного образовывать стекло, со вторым материалом, из которого при нагреве образуется газ; и
(ii) проведение процесса, при котором из первого материала образуется стекло и одновременно из второго материала образуется газ,
в результате чего формируется стеклообразная структура, содержащая стекло, заполненное газом, и первый материал содержит биологический материал.
18. Способ по п.17, отличающийся тем, что стеклообразный материал выбран из стеклообразующего сахара, или глутаминовой кислоты, или ее соли.
19. Способ по п.18, отличающийся тем, что стеклообразующий сахар выбран из раффинозы, трегалозы, палатинита (смеси сорбитол глюкопиранозила и маннитол глюкопиранозила), сорбитол глюкопиранозила, маннитол глюкопиранозила, лактитола и моносахаридного спирта.
20. Способ по п.17, отличающийся тем, что стекло содержит фосфат кальция.
21. Способ по п.17, отличающийся тем, что второй материал разлагается в то время, как первый материал находится в переходном состоянии между жидкой фазой и стеклообразной фазой.
22. Способ по п.17, отличающийся тем, что второй материал образует газ при нагреве бикарбоната аммония.
23. Способ по п.17, отличающийся тем, что частицы формируются в распылительной сушилке.
24. Способ по п.17, содержащий дополнительную стадию суспендирования частиц в нетоксичной жидкости.
| US 6630169 B1, 07.10.2003 | |||
| EP 0913178 A1, 06.05.1999 | |||
| BARTHOMEUF С et al | |||
| Stabilization of Octastain, a somatostatin analogue: comparative accelerated stability studies of two formulations for freeze-dried products | |||
| Pharm Acta Helv., 1996, 71(2), p 161-6, РМID: 8810582, найдено в PubMed. |
Авторы
Даты
2011-09-27—Публикация
2006-08-31—Подача