Настоящее изобретение относится, в целом, к твердым системам доставки для хранения, распределения и контролируемого высвобождения молекул и, более конкретно, к твердым дозируемым системам доставки, содержащим стеклообразный носитель и переносимые вещества. Также предусматриваются способы получения систем доставки и способы их использования.
Твердые системы доставки являются полезными в большом наборе применений, таких как контролируемое высвобождение лабильных молекул, в частности биологически активных материалов, таких как фармацевтические агенты, ферменты, вакцины и агенты биологического контроля, такие как фертилизаторы, пестициды и феромоны.
Доставка биологически активных материалов в виде твердой дозы к биологическим тканям, таким как мукозальная, дермальная, окулярная, подкожная, интрадермальная и пульмонарная, дает некоторые преимущества по сравнению с известными ранее способами, такими как местные нанесения жидкостей, трансдермальное введение через так называемые "пластыри" и гиподермическая инъекция. Доставка твердой дозы может быть осуществлена с помощью прямой трансдермальной доставки твердой дозы, которая уменьшает риск инфицирования путем устранения использования обычных иголок и шприцов, обеспечивает более аккуратную дозировку, чем многодозовые флаконы и сводит до минимума или устраняет тот дискомфорт, который часто сопровождает гиподермическую инъекцию. Разработаны несколько твердых дозирующих систем доставки, включая такие системы, использующие средства для трансдермальной и баллистической доставки.
Местная доставка используется для разнообразных биологически активных материалов, таких как антибиотики, для заживления ран. Эти местные примочки, гели, кремы и так далее должны наноситься многократно через малые промежутки времени для поддержания их эффективности. Это является особенно сложным в случае ожоговых ран и язв.
Средства, используемые для введения лекарств трансдермально, обычно включают ламинатные композиты со слоем резервуаром лекарства и с композитом, приклеенным к коже, то есть трансдермальным пластырем, таким как описанный в патенте США 4906463. Однако многие лекарства являются непригодными для трансдермальной доставки и не имеют скоростей трансдермального высвобождения лекарства, для которых способность такой доставки является безупречной.
Субдермальные имплантируемые терапевтические системы также приготавливают для медленного высвобождения определенных фармацевтических агентов в течение длительного периода времени, такого как месяцы или годы. Хорошо известным примером является Norplant® для доставки стероидных гормонов.
При доставке лекарства через проницаемую мембрану лекарство инкапсулируют внутри резервуара, который окружен полимерной мембраной, лимитирующей скорость высвобождения. Резервуар лекарства может содержать либо частицы лекарства, либо дисперсию (или раствор) твердого лекарства в жидкости или в дисперсионной среде типа матрицы. Полимерная мембрана может быть изготовлена из гомогенного или гетерогенного непористого полимерного материала или микропористой или полупроницаемой мембраны. Инкапсуляция резервуара лекарства внутри полимерной мембраны может достигаться путем заливки, инкапсуляции, микроинкапсуляции и других методик. Имплантанты высвобождают лекарства путем растворения лекарства во внутреннем ядре и медленной диффузии через внешнюю матрицу. Высвобождение лекарства из этого типа имплантируемой терапевтической системы должно быть относительно постоянным и является сильно зависящим от скорости растворения лекарства в полимерной мембране или скорости диффузии через микропористую или полупроницаемую мембрану. Внутреннее ядро может, в основном, раствориться через некоторое время, однако в используемых в настоящее время средствах внешняя матрица не растворяется.
Имплантанты размещают подкожно путем надреза кожи и силового введения имплантантов между кожей и мышцей. В конце их использования, если они не растворились, эти имплантанты удаляют хирургически. Патент США 4244949 описывает имплантант, который имеет наружную матрицу из инертного пластика, такого как политетрафторэтилен. Примерами этого типа имплантируемых терапевтических систем являются Progestasert IUD и Ocusert system.
Другие имплантируемые терапевтические системы включают доставку лекарства, контролируемую диффузией в матрице. Резервуар лекарства образуется путем гомогенного диспергирования частиц лекарства в липофильной или гидрофильной полимерной матрице. Диспергирование частиц лекарства в полимерной матрице может быть достигнуто путем смешивания лекарства с вязким жидким полимером или полутвердым полимером при комнатной температуре с последующим поперечным сшиванием полимера или путем смешивания частиц лекарства с расплавленным полимером при повышенной температуре. Он также может быть получен путем растворения частиц лекарства и/или полимера в органическом растворителе с последующим смешиванием и выпариванием растворителя в форме при повышенной температуре или в вакууме. Скорость высвобождения лекарства из устройства доставки этого типа не является постоянной. Примерами этого типа имплантируемой терапевтической системы являются противозачаточное вагинальное кольцо и имплантант Compudose. PCT/GB 90/00497 описывает системы на основе стекла с медленным высвобождением для образования имплантируемых средств. Описанные имплантанты являются биологически адсорбируемыми и не требуют хирургического удаления. Однако введение осуществляют с помощью хирургических средств. Кроме того, эти устройства являются строго ограниченными относительно типа биологически активного материала, который может быть включен, поскольку они должны быть стабильными по отношению к нагреву и/или растворителю, чтобы сделать возможным включение в средство доставки.
При доставке лекарств, контролируемой растворением микрорезервуара, резервуар лекарства, который является суспензией частиц лекарства в водном растворе смешиваемого с водой полимера, образует гомогенную дисперсию множества дискретных, не выщелачивающихся микроскопических резервуаров лекарства в полимерной матрице. Микродисперсия может быть получена путем использования высокоэффективного диспергирования. Высвобождение лекарства из этого типа средства доставки лекарств следует либо за междуфазным распределением, либо за процессом контролируемой диффузии в матрице. Примером этого типа средств доставки лекарств является Syncro-Mate-C Implant.
В случае литых полимерных имплантантов биологически активные материалы, которые не могут противостоять органическим растворителям, не являются пригодными. В случае систем на основе экструдированного полимера биологически активные материалы, которые не могут противостоять повышенным температурам, необходимым для формирования имплантантов, являются непригодными для использования. Во всех случаях биологически активные материалы, которые являются нестабильными при температуре тела, особенно в течение длительных периодов времени, являются непригодными для использования.
Большой набор препаратов разработан для введения в форме аэрозолей на слизистые оболочки, в частности "путем ингаляции" (назо-фарингеальной и пульмонарной). Композиции для фармацевтического введения путем ингаляции обычно включают жидкий препарат фармацевтического агента и средства для доставки жидкости в форме аэрозоля. Патент США 5011678 описывает соответствующие композиции, содержащие фармацевтически активное вещество, биологически совместимый амфифильный стероид и биологически совместимый угле(водород/фтор)-пропеллант. Патент США 5006343 описывает соответствующие композиции, содержащие липосомы, фармацевтически активные вещества и определенное количество альвеолярного поверхностно-активного белка, эффективно усиливающего транспорт липосом через пульмонарную поверхность.
Одним из недостатков использования препаратов в виде аэрозолей является то, что содержание фармацевтических агентов в водных суспензиях или растворах может вести к агрегации и к потере активности и биодоступности. Потеря активности может частично быть предотвращена путем замораживания, однако это ограничивает применение этих препаратов. Это относится, в частности, к пептидам и гормонам. Например, синтетические аналоги гормонов высвобождения гонадотропина (GnRH), такие как агонист нафарелина или антагонист ганирелекса, сконструированы для сильнодействия, повышенной гидрофобности и связывания с мембраной. Соединения имеют достаточно гидрофобный характер для агрегирования в водном растворе и для формирования упорядоченной структуры, что увеличивает вязкость со временем. Поэтому биологическая доступность в назальных и пульмонарных препаратах может быть очень низкой. Использование порошкообразных препаратов преодолевает многие из этих недостатков. Требуемый размер частиц в таких порошках составляет 0,5-5 микрон для достижения глубокого альвеолярного осаждения при пульмонарной доставке. К сожалению, порошки с таким размером частиц имеют тенденцию адсорбировать воду и слипаться, таким образом уменьшая осаждение порошка в глубине пространства альвеол. Хотя порошки с большим размером частиц являются пригодными для доставки в назо-фарингеальную область, тенденция порошков к слипанию уменьшает доступную площадь поверхности частицы для контакта и адсорбции через эти мембраны. Устройства, которые разрушают агрегаты, образованные вследствие электростатических взаимодействий, используются в настоящее время (например, TurbohalerТМ); однако они не разрушают агрегаты, вызванные влажностью. Было бы преимуществом иметь порошки, которые не поглощают влажность и не слипаются, увеличивая таким образом пульмонарную концентрацию лекарства.
Также разработаны твердые носители дозируемой доставки для баллистического трансдермального введения. Например, в патенте США 3948263 баллистический имплантант для животных, состоящий из внешней полимерной оболочки, окружающей биологически активный материал, описан для ветеринарного использования. Подобно этому в патенте США 4326524 описана "баллистическая пуля" для твердой дозировки, включающая биологически активный материал и инертное связующее без внешней оболочки. Доставка осуществляется с помощью сжатого газа или путем взрыва. Покрытые желатином транквилизирующие вещества для имплантанта, которые несут баллистические пули, также описаны в патенте США 979993. Эти баллистические средства, однако, являются подходящими только для ветеринарного применения на крупных животных из-за относительно большого размера доставляемой дозы, обычно порядка миллиметров.
Баллистическая доставка на клеточном уровне также была успешно решена. Общим принципом баллистического введения является использование волнового фронта сверхзвуковой волны, образующейся путем высвобождения сжатого газа, для разгона частиц, содержащихся в присоединенной камере. Например, нуклеиновые кислоты, адсорбированные на вольфрамовых частицах - "микропулях" были успешно доставлены в живые эпидермальные клетки растений. Смотри Klein (1987) Nature 327: 70-73. Лучшим контролирующим устройством является пистолет для доставки частиц (PIG). Vain et al. (1993) Plant Cell. Tissue and Organ Culture 33: 237-246.
Описаны устройства, которые выстреливают ампулы, содержащие лекарства, используя давление газа. Патент США 4790824; и PCT/GB 94/00753. Также описаны несколько устройств, которые инжектируют жидкости, патенты США 5312335 и 4680027. Имеется несколько существующих препаратов, пригодных для баллистической доставки. Однако порошковые препараты или медикаменты в их существующей форме являются непригодными для баллистического введения. Частицы доступных порошковых форм являются обычно иррегулярными, с разбросом по размеру, форме и плотности. Это отсутствие однородности ведет к осаждению и потерям порошка на поверхности кожи во время введения, а также к проблемам с контролем и разбросом глубины доставки в подкожные и интрадермальные ткани.
Таким образом, для баллистической доставки являлось бы выгодным создание твердых систем доставки лекарств с заданным размером, формой, плотностью и скоростью растворения для обеспечения более однородного распределения. Дополнительные преимущества были бы достигнуты, если бы форма носителя была контролируемой для облегчения или контроля проникновения через эпидермис и твердые слои кожи. Малый размер системы доставки, предпочтительно связанный с высоким импульсом доставки, также увеличивал бы комфорт введения и уменьшал (сводил к минимуму) повреждения тканей. Производство такой твердой дозированной системы доставки должно быть таким, чтобы как носитель доставки, так и переносимое вещество при доставке не были бы повреждены или не уменьшилась бы их эффективность. Кроме того, переносимое вещество должно оставаться стабильным, когда оно загружается с носителем или без него, так чтобы могла быть достигнута эффективность введения и облегчено хранение загруженной системы доставки. Производство твердого носителя для дозированной доставки, его загрузка содержащимся материалом для получения твердой дозируемой системы доставки и введение системы также должны быть относительно простыми и экономичными.
Все ссылки, цитируемые здесь, тем самым являются включаемыми путем упоминания.
Настоящее изобретение включает твердые стеклообразные носители для доставки, пригодные для загрузки широким набором веществ или "переносимых веществ" для получения твердых систем доставки. Выбор стеклообразных носителей для доставки определяется природой заряжаемых веществ и желаемой скоростью доставки заряжаемого вещества. Обеспечивается широкое разнообразие типов и скоростей доставки. Также предусматриваются предпочтительные переносимые вещества, буферы, вспомогательные вещества и дополнительные стабилизаторы. Системы доставки могут иметь размеры и формы, соответствующие разнообразным способам введения.
Изобретение касается быстрорастворимых твердых дозируемых систем доставки, содержащих стабилизирующий полиол (СП) и переносимое вещество. Эти системы доставки могут быть приготовлены в виде порошков с гомогенным размером частиц и более в имплантируемых формах.
Изобретение далее касается новых стеклообразных носителей, образованных из гидрофобных производных углеводов (ГПУ). Эти ГПУ являются нетоксичными, и высвобождение переносимых веществ из этих систем является в высшей степени контролируемым по отношению к высвобождению переносимых веществ в течение продолжительных периодов времени. Высвобождение из систем доставки на основе ГПУ может подвергаться влиянию расстекловывания, растворения и/или гидролиза. Системы доставки на основе ГПУ являются уникально приспособленными для доставки гидрофобных переносимых веществ, таких как пестициды, феромоны, стероидные гормоны, пептиды, миметики пептидов, антибиотики и другие органические медикаменты, такие как синтетические кортикостероиды, бронходилаторы, и иммуномодуляторы и иммуносупрессанты, подобные циклоспорину А (ЦСА).
Изобретение далее касается со-препаратов различных стеклообразных носителей для создания новых комбинированных систем доставки. Комбинированные системы доставки включают ГПУ, объединенные с СП и/или другими стеклообразными материалами, медленно растворяющимися в воде, такими как карбоксилатные, нитратные и фосфатные стекла, для получения твердых дозируемых систем доставки с широким набором новых свойств.
Изобретение касается твердых дозированных систем доставки для многофазной доставки, включающие наружную часть, содержащую ГПУ, медленно растворяющийся в водном растворе, имеющую внутри полое отделение, и внутреннюю часть, размещенную в отделении, внутренняя часть включает хотя бы одно СП и терапевтически эффективное количество хотя бы одного переносимого вещества.
Изобретение также касается способов доставки биологически активных материалов для создания твердых дозированных систем доставки, описанных выше, и введения системы в биологическую ткань. Введение может быть мукозальным, оральным, местным, подкожным, интрадермальным, внутримышечным, внутривенным или путем ингаляции.
Изобретение далее касается способов получения твердых дозированных систем доставки. СП и/или ГПУ, переносимые вещества и любые другие компоненты смешивают и обрабатывают с помощью широкого набора способов, включая растворение в расплаве и последующее гашение, сушку распылением, сушку замораживанием, сушку на воздухе, вакуумную сушку, сушку в ожиженном слое, соосаждение и испарение сверхкритической жидкости. Полученное в результате стекло может быть нагрето до размягчения и может затем быть экструдировано, продавлено или вытянуто в сплошные или полые волокна. Высушенные компоненты могут также быть смешаны в водных или органических растворах и высушены, например, путем сушки распылением, сушки вымораживанием, сушки на воздухе, вакуумной сушки, сушки в ожиженном слое, соосаждения и выпаривания сверхкритической жидкости.
Настоящее изобретение далее касается способов получения систем доставки, пригодных для медленного высвобождения переносимых веществ или их высвобождения с переменной скоростью. Способы включают объединение переносимых веществ в твердых растворах стабилизирующих стеклообразующих полиолов, и/или ГПУ, и/или других стеклообразующих веществ со скоростями растворения или разложения, меньшими, чем таковые у СП, и обработку компонентов, как описано выше. Отношение материалов может контролироваться, чтобы обеспечить широкий диапазон значений точно определенных скоростей высвобождения. Со-препараты СП и/или ГПУ и других водорастворимых и/или биологически разлагаемых стекол, пластиков и модификаторов стекла, получаемых таким образом, также относятся к настоящему изобретению.
Твердые дозированные системы и способы согласно изобретения также касаются твердых дозированных форм, которые включают волокна, сферы, таблетки, диски, частицы и иголки с относительно гомогенным распределением по размерам. Носители могут быть либо микроскопическими, либо макроскопическими.
Широкое разнообразие переносимых веществ является пригодными для использования в соответствии с настоящим изобретением, включая, но не ограничиваясь ими, диагностические, терапевтические, профилактические и другие активные агенты. Системы доставки и способы их использования предусматриваются для разнообразных схем дозировки для доставки переносимых веществ и являются пригодными для широкого диапазона использования, включая агрономическое, ветеринарные и медицинские применения.
Краткое описание фигур
Фигура 1 представляет собой график, представляющий типичное распределение частиц по размерам микронного порошка трегалозного стекла, пригодного для введения путем ингаляции. Фигура 1 описана в примере 2.
Фигура 2А представляет собой график, представляющий узкое распределение частиц по размерам для порошка стекла трегалоза/буферная соль - молекулярный водяной насос (МВН).
Фигура 2В представляет собой график, представляющий адсорбцию воды различных порошков стекла трегалоза, МВН и трегалоза, хлорид после хранения при температуре окружающей среды и различных относительных влажностях.
Фигура 2В представляет 51% относительную влажность и МВН (▪), 80% относительную влажность и МВН (I), 51% относительную влажность и хлорид (□), и 80% относительную влажность и хлорид (X). Фигура 2 описывается в примере 2.
Фигура 3 представляет собой график, представляющий узкое распределение частиц по размерам для порошка трегалозного стекла, полученного сушкой распылением в сушке-распылителе Lab-Plant-spray. Фигура 3 описывается в примере 2.
Фигура 4 представляет собой график, представляющий сравнение формы распределения частиц по размерам для порошков трегалозного стекла (0,5М трегалоза/0,5М лактат кальция), полученных на двух различных сушилках-распылителях (Lab-Plant (□), и Buchi (вертикальная черно-белая стрелка, направленная вверх), как показано). Фигура 4 описывается в примере 2.
Фигура 5А представляет собой график, представляющий устойчивость пероксидазы хрена по отношению к ацетону, осуществляемой путем сушки фермента с трегалозой. Средние величины представлены для ситуаций: без растворителя плюс трегалоза (°), без растворителя минус трегалоза (•), ацетон плюс трегалоза (квадрат, открытый снизу) и ацетон минус трегалоза (квадрат, открытый сверху).
Фигура 5В представляет собой график, представляющий устойчивость щелочной фосфатазы по отношению к ацетону, осуществляющейся при сушке фермента с трегалозой. На фигуре 5В светлые кружки представляют экспозицию без растворителя плюс трегалоза, темные кружки представляют экспозицию без растворителя минус трегалоза, квадраты (открытые снизу) представляют средний ацетон плюс трегалоза, и квадраты (открытые сверху) представляют средний ацетон минус трегалоза. Фигура 5 описывается в примере 3.
Фигура 6 представляет собой график, представляющий высвобождение МВ9 из выбранных пленок металлкарбоксилатного стекла. Квадраты представляют пленку гексаноата алюминия (100-200 микрон), где высвобождение предваряет растворение пленки. Кружки представляют пленку неодеканоата кальция (1-2 мм), где высвобождение следует за растворением пленки. Фигура 6 описывается в примере 7.
Фигура 7 представляет собой график, представляющий скорость высвобождения инкапсулированного красителя Кислотный Синий 129 из диска α-D-глюкозапентаацетатного стекла α-ГПАЦ). Фигура 7 обсуждается в примере 8.
Фигура 8 представляет собой график, представляющий высвобождение МВ9 из диска трегалозаоктаацетатного стекла (ТОАЦ) (6 мм • 2,5 мм) в растворе PBS. Фигура 8 обсуждается в примере 9.
Фигура 9 представляет собой график, представляющий высвобождение МВ9 из ТОАЦ/РУДА (треагалозаоктаацетат/раффинозаундецацетат) матриц в деионизированную воду. Различные представленные концентрации представляют собой: 95% ТОАЦ, 0,61% весового красителя (□); 75% ТОАЦ, 1,17 весового красителя (°); 50% ТОАЦ, 2,09% весовых красителя (вертикальная черно-белая стрелка, направленная вверх); чистый ТОАЦ, 1,39% весовых красителя  и чистый РУДА, 4% весовых красителя (вертикальная черно-белая стрелка, направленная вниз). Фигура 9 описывается в примере 9.
и чистый РУДА, 4% весовых красителя (вертикальная черно-белая стрелка, направленная вниз). Фигура 9 описывается в примере 9.
Фигура 10 представляет собой график, представляющий изменение Тg в зависимости от молярного процента ТОАЦ в со-препаратах двух ГПУ. Квадраты представляют трегалозаоктаацетат/сорбитгексаацетат (ТОАЦ/СГАЦ) стекло. Кружки представляют ТОАЦ/РУДА стекло. Треугольники представляют трегалозаоктаацетат/α-глюкозапентаацетат (ТОАЦ/α-ГПАЦ) стекло. Фигура 10 описывается в примере 9.
Фигура 11 представляет собой график, представляющий средний процент высвобождения МВ9 в PBS из выбранных стеклянных сфер ТОАЦ/РУДА (n= 4). Квадраты представляют 10% РУДА. Кружки представляют 50% РУДА. Треугольники представляют чистый РУДА. Фигура 11 описывается в примере 9.
Фигура 12 представляет собой график, представляющий высвобождение МР9 (1% весовой) из со-препаратов ТОАЦ плюс 25% СОАЦ (▪) и 25% ЦОАЦ (•) (n= 5). Фигура 12 описывается в примере 9.
Фигура 13 представляет собой график, представляющий высвобождение МВ9 (1% весовой) из ТОАЦ/α-ГПАЦ в следующих отношениях: 90: 10 (▪), 75: 25 (•), 50: 50 (вертикальная черно-белая стрелка, направленная вверх) и 25: 75 (вертикальная черно-белая стрелка, направленная вниз) (n= 4). Фигура 13 описывается в примере 9.
Фигура 14 представляет собой график, представляющий высвобождение МВ9 из ТОАЦ (▪) и ТОАЦ/ТОПР (25% весовых) (•) (n= 5). Фигура 14 описывается в примере 9.
Фигура 15 представляет собой график, представляющий высвобождение МВ9 (1% весовой) из чистого ТОАЦ (▪) и ТОАЦ плюс XPDO (5%) (•) (n= 5). Фигура 15 описывается в примере 9.
Фигура 16 является микрофотографией тонкой пленки со-препарата стекла, содержащей 10% трегалозы в ТОАЦ, высушенном от диметилформамида (ДМФ). Фигура 16 описывается в примере 10.
Фигура 17 является микрофотографией со-препарата фигуры 16 при более высоком увеличении. Фигура 17 описывается в примере 10.
Фигура 18 является микрофотографией со-препарата стекла, содержащего 10 трегалозы в ТОАЦ, с Метиловым Зеленым и Масляным Красным О, осушенным от ДМФ. Фигура 18 описывается в примере 10.
Настоящее изобретение включает дозированные твердые системы доставки, содержащее носители доставки твердой дозы и переносимые вещества. Системы доставки приготавливают для обеспечения точно задаваемых скоростей доставки переносимых веществ, включенных в них. Системы доставки являются, в частности, пригодными для доставки биологически активных молекул животным, включая людей.
Также изобретение включает способы доставки терапевтических агентов, включающие но не ограничивающиеся ими, мукозальное, оральное, наружное, подкожное и интрадермальное, внутримышечное, внутривенное введение и введение путем ингаляции.
Изобретение также указывает способы получения систем доставки.
"Твердая доза", как здесь используется, обозначает, что переносимое вещество, включенное в носителе, находится скорее в жидкой форме и твердая форма является формой, используемой для доставки. Переносимые вещества представляют собой такие молекулы, макромолекулы и совокупность макромолекул, синтетические и натуральные, и клеточные фракции, живые и мертвые клетки, бактерии и вирусы и другие активные вещества, включенные в носитель; широкое разнообразие переносимых веществ являются пригодными для использования в них и являются описанными ниже. Под "эффективным количеством" переносимого вещества подразумевается количество, необходимое для оказания желаемого воздействия. Например, у биологически активного материала, эффективным количеством является такое, которое вызывает желаемую физиологическую реакцию. Носитель находится в твердой форме и является аморфным или стеклообразным по природе. Другие добавки, буферы, красители и тому подобное могут быть включены в системы доставки. Как он здесь используется, термин "носитель" включает все стеклообразующие вещества, воплощенные в заявляемом изобретении. Термин "система(ы) доставки" включает твердые формы дозировки, содержащие носители и переносимые вещества. Системы доставки, образуемые из конкретных носителей, как указано, получают различные названия, если не указывается другого, термин система доставки определяет каждую из них.
В одном из воплощений изобретение относится к системам твердых доз с высокими скоростями высвобождения переносимых веществ. В этом воплощении носитель представляет собой СП. В настоящее время обнаружено, что СП могут быть обработаны для получения порошков с гомогенным распределением размеров частиц в форме либо микросфер, либо иголок. СП также могут быть обработаны для получения макроскопических форм доставки, пригодных для приготовления имплантируемых средств. Здесь описывается большое разнообразие форм дозировки и способов получения форм дозировки. Как обнаружено, эти СП являются, в частности, пригодными для использования там, где в противоположном случае денатурирующие условия сделали бы невозможным приготовление твердых форм дозировки биологически активных материалов. В частности, такие условия включают повышенные температуры (такие, выше которых биологически активный материал в противном случае денатурируется) и присутствие органических растворителей.
В другом воплощении изобретение относится к твердым системам дозировки с задаваемыми по-новому и контролируемыми скоростями высвобождения переносимых веществ. В этом воплощении носитель является органическим карбоксилатным стеклом. Как обнаружено в настоящее время, органические карбоксилаты образуют стабильные аморфные носители с помощью выпаривания растворителя. Эти органические стекла высвобождают включенные переносимые вещества при прецизионно определяемых скоростях, зависящих от состава используемых карбоксилатного аниона и катиона металла. Подобно носителям, содержащим СП, эти стекла могут быть обработаны либо сами по себе, либо другими органическими карбоксилатами, и/или СП, и/или ГПУ для получения порошков с гомогенным распределением частиц по размерам в форме микросфер, иголок и/или имплантируемых средств для получения широкого разнообразия макроскопических форм доставки.
В дальнейшем воплощении изобретение относится к твердым системам дозировки с задаваемыми по-новому и контролируемыми скоростями высвобождения переносимых веществ. В этом воплощении носитель является гидрофобным производным углевода (ГПУ). Как обнаружено в настоящее время, ГПУ образуют стабильные стеклообразные носители, которые выпускают переносимые вещества в водных условиях при точно определяемых скоростях высвобождения, зависящих от углевода, гидрофобного фрагмента (гидрофобных фрагментов), используемых для получения производных углевода, и степени разветвленности. Подобно носителям, содержащим СП, носители, содержащие ГПУ, могут быть обработаны для получения порошков с гомогенным распределением частиц по размерам в форме либо микросфер, либо иголок. ГПУ также могут быть обработаны для получения широкого разнообразия микроскопических форм доставки.
Здесь описаны формы дозировок и способы получения форм дозировок. Эти системы доставки, как обнаружено, являются, в частности, полезными там, где природа переносимого вещества делала бы невозможным приготовление форм твердой дозировки, поскольку они предусматривают системы доставки для гидрофобных переносимых веществ, которые являются сложными либо для приготовления в форме дозировки, либо для получения эффективных физиологических концентраций из-за нерастворимости в водных растворителях.
Системы доставки существуют в виде твердых растворов, эмульсий, суспензий или коацерватов переносимого вещества в твердом носителе. Переносимое вещество является устойчивым при более высоких температурах внутри носителя, чем само по себе. Конкретная температурная устойчивость зависит от используемого носителя. Таким образом, компоненты систем доставки могут поддерживаться в форме расплавов в течение коротких периодов без повреждения переносимых веществ во время обработки. Системы доставки могут быть далее обработаны тем же самым способом, и они являются устойчивыми к разрушению во время совместного плавления с нитратом, и/или карбоксилатом, и/или ГПУ, и/или другими стеклообразующими веществами.
Изобретение далее определяет со-препараты различных носителей для доставки и систем доставки для создания широкого разнообразия объединенных носителей доставки.
Настоящее изобретение определяет композиции и способы получения композиций. Хотя могут использоваться единичные формы, могут быть представлены более чем один носитель, более чем одно переносимое вещество и более чем одна добавка. Определение эффективных количеств этих соединений является результатом опыта специалистов в данной области.
Системы доставки, стабилизированные полиолом
Изобретение включает твердые дозированные системы доставки, в которых носитель доставки содержит стабилизирующий полиол. Они определяются как "СП системы доставки". Как обнаружено в настоящее время, СП системы доставки могут быть обработаны для получения широкого разнообразия форм твердой дозировки, пригодных для использования, в частности для терапевтического введения переносимых веществ.
СП включают, но не ограничиваются ими, углеводороды. Используемый здесь термин "углеводы" включает, но не ограничивается ими, моносахариды, дисахариды, трисахариды, олигосахариды и соответствующие спирты этих сахаров, полисахариды и химически модифицированные углеводы, такие как гидроксиэтилкрахмал и сополимеры сахаров (Ficoll). Для использования здесь пригодны как натуральные, так и синтетические углеводороды. Синтетические углеводы включают, но не ограничиваются ими, такие углеводы, которые имеют гликозидную связь, замещенную тиольной или углеродной связью. Могут быть использованы как D, так и L формы углеводов. Углеводы могут быть невосстанавливающие или восстанавливающие. Соответствующие носители являются такими носителями, в которых переносимое вещество может быть высушено и хранится без значительных потерь активности из-за денатурации, агрегации или других механизмов. Предотвращение потерь активности может быть усилено путем добавления различных добавок, таких как ингибиторы реакции Маллара, как описано ниже. Добавление этих ингибиторов является особенно предпочтительным в соединении с восстанавливающими углеводами.
Восстанавливающие углеводы, пригодные для использования в настоящем изобретении, являются углеводами, известными в данной области, и включают, но не ограничиваются ими, глюкозу, мальтозу, лактозу, фруктозу, галактозу, маннозу, мальтулозу, изомальтулозу и лактулозу.
Невосстанавливающие углеводы включают, но не ограничиваются ими, трегалозу, раффинозу, стахиозу, сахарозу и декстран. Другие полезные углеводы включают невосстанавливающие гликозиды полигидроксисоединений, выбираемых из спиртов сахаров и других полиспиртов с прямой цепью. Гликозиды сахарных спиртов являются предпочтительно моногликозидами, в частности соединениями, полученными путем восстановления дисахаридов, таких как лактоза, мальтоза, лактулоза и мальтулоза. Гликозидная группа является предпочтительно глюкозидом или галактозидом, и сахарный спирт является предпочтительно сорбитом (глюцитол). Особенно предпочтительными углеводами являются мальтитол (4-О-β-D-глюкопиранозил-D-глюцитол), лактитол (4-О-β-D-галактопиранозил-D-глюцитол), палатинит (смесь GPS, α-D-глюкопиранозил-1-->6-сорбита и GPM, α-D-глюкопиранозил-1-->6-маннитола) и его конкретные сахарные спирты, компоненты GPS и GPM.
Предпочтительно СП является углеводом, который существует как гидрат, включая трегалозу, лактитол и палатинит. Наиболее предпочтительно СП является трегалозой. В настоящее время неожиданно обнаружено, что твердые дозированные системы доставки, содержащие определенные гидраты сахаров, подобно трегалозе, лишены "липкости" или "прикрепляемости" твердых форм дозировки, содержащих другие углеводы. Таким образом, для производства, упаковки и введения, трегалоза является предпочтительным СП.
Трегалоза, (α-D-глюкопиранозил-α-D-глюкопиранозид), является невосстанавливающим дисахаридом природного происхождения, который, как первоначально обнаружено, связан с предотвращением повреждений в отсутствии влаги у определенных растений и животных, которые могут высыхать без повреждения и могут оживать, когда присоединяют воду. Трегалоза, как показано, является полезной при предотвращении денатурации протеинов, вирусов и пищевых продуктов при высыхании. Смотри патенты 4891319; 5149653; 5026566; Blakeley et al. (1990) lancet 336: 854-855; Roser (July 1991) Trends in Food Sci. and Tech. 166-169; Colaco et al. (1992) Biotechnol. Internant, 345-350; Roser (1991) Biopharm. 4: 47-53; Colaco et al. (1992) Bio/Tech. 10: 1007-1011; and Roser et al. (May 1993) New Scientist, pp. 25-28.
Другие СП, пригодные для использования здесь, описаны, например, в WO 91/18091, 87/00196 и патентах США 4891319 и 5098893, которые описывают использование полиолов в качестве стекол для стабилизации молекул во время сушки и хранения для восстановления перед использованием. Твердые формы дозировки, определяемые настоящим изобретением, как обнаружено в настоящее время, являются пригодными для непосредственного использования в качестве систем доставки для контролируемого высвобождения включенных переносимых веществ. Кроме того, эти полиолы могут быть использованы в комбинации с другими аморфными матрицами для получения систем доставки, которые как обнаружено в настоящее время, имеют широкий диапазон скоростей высвобождения и характеристики, которые легко и аккуратно контролируются, для производства уникальных твердых систем дозировки.
В настоящее время также обнаружено, что переносимые вещества, предпочтительно растворимые в органических растворителях, могут быть высушены в трегалозе из смеси органических/водных растворителей с получением со-препаратов, которые в настоящее время легко восстанавливаются в водных растворителях. Настоящее изобретение определяет твердые системы дозировки, полученные таким способом. Настоящим изобретением предусматриваются способы получения высушенного материала и композиции, получаемые при этом. Переносимое вещество растворяется в органическом, водном растворителе в комбинации с эффективным количеством трегалозы, а затем высушивается. Это дает твердый раствор, эмульсию, суспензию или коацерват переносимого вещества в трегалозном стекле, которое затем легко растворяется в водном растворе, давая мелкодисперсную суспензию нерастворимого переносимого вещества. В настоящее время показано, что иммуносуппрессант ЦСА (который плохо растворяется в воде и обычно вводится в виде масляной эмульсии) в растворе трегалозы в смеси этанол: вода 1: 1 может быть высушен до получения прозрачного стекла трегалозы, содержащего ЦСА. Это стекло может быть размолото для получения свободно пересыпающегося порошка, который может быть также таблетирован, который при добавлении в воду непосредственно растворяется, давая мелкодисперсную суспензию ЦСА в воде.
ГПУ Системы доставки
Изобретение далее определяет системы доставки твердой дозы, в которых носитель содержит хотя бы один ГПУ. Они определяются как "ГПУ системы доставки". ГПУ образуют отдельную группу нетоксичных производных углеводородов, пригодных для использования при формировании носителя твердой дозы. Хотя были синтезированы многие ГПУ, преимущества легкого образования ими стекла не сообщались ранее. Таким образом, изобретение определяет стеклообразную форму этих ГПУ, которые также упоминаются как аморфная матрицеобразующая композиция. ГПУ системы доставки являются особенно пригодными для использования при контролируемом, переменном или замедленном высвобождении переносимых веществ. Любое из переносимых веществ, описанных здесь, может быть включено в ГПУ системы доставки.
Как показано здесь, ГПУ легко образуют стекла либо из погашенного расплава, либо из выпаренного органического растворителя. ГПУ могут быть также обработаны с помощью способов, описанных для СП.
Используемый здесь термин ГПУ относится к широкому разнообразию гидрофобных производных углеводов, где хотя бы одна гидроксильная группа замещена гидрофобным фрагментом, включая, но не ограничиваясь ими, простые и сложные эфиры. Многочисленные примеры соответствующих ГПУ и их синтезов описаны в Developments in Food Carbohydrate 2 ed. С. К. Lee, Applied Science Publishers, London (1980). Другие синтезы описаны, например, в Akoh et al. (1987) J. Food Sci. 52: 1570; Khan et al. (1993) Tetra. Letts 34: 7767; Khan (1984) Pure & Appl. Chem. 56: 833-844; and Khan et al. (1990) Carb. Res. 198: 275-283. Конкретные примеры ГПУ включают, но не ограничиваются ими, сорбитгексаацетат (СГАЦ), α-глюкоза-пентаацетат (α-ГПАЦ), β-глюкозапентаацетат (β-ГПАЦ), 1-О-октил-β-D-глюкозатетраацетат (ОГТА), трегалозаоктаацетат (ТОАЦ), трегалозаоктапропаноат (ТОПР), сахарозаоктаацетат (СОАЦ), целлобиозаоктаацетат(ЦОАЦ), раффинозаундецацетат (РУДА), сахарозаоктапропаноат, целлобиозаоктапропаноат, раффинозаундецпропаноат, тетра-О-метилтрегалоза и ди-О-метилгекса-О-ацетилсахароза. Примером соответствующего ГПУ, где углеводородом является трегалоза, является:
формула 1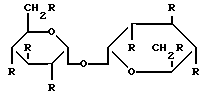
В формуле 1 R представляет гидроксильную группу или ее низшее гидрофильное производное, такое как простой или сложный эфир, или любые их функциональные модификации, где хотя бы один R является не гидроксилом, а гидрофобным производным. Соответствующие функциональные модификации включают, но не ограничиваются ими, такие, где атом кислорода замещен гетероатомом, таким как N или S. Степень замещения также может варьироваться и может представлять собой смесь различных производных. Полное замещение гидроксильных групп не является необходимым и предоставляет возможность изменения физических свойств (таких как растворимость) носителя. R может иметь любую длину цепи, начиная с С2, и может быть линейным, разветвленным, циклическим или модифицированным. Хотя формула 1 изображает дисахаридтрегалозу, любой из углеводов, обсуждаемых здесь, может быть углеводной основной цепью, а положение гликозидной связи и длина цепи сахарида могут быть различными. Обычно практическим диапазоном в терминах стоимости и эффективности синтеза является пентасахарид; однако изобретение не ограничивается сахаридами конкретного типа с конкретной гликозидной связью или длиной цепи. Различные другие аспекты ГПУ не являются ограничивающими. Например, компоненты сахаридов в каждом ГПУ также могут варьироваться, положение и природа гликозидной связи между сахаридами могут быть изменены, и тип замещения может варьироваться внутри ГПУ. Представительным примером ГПУ со смешанным замещением простыми и сложными эфирами является 1-о-октил-β-D-глюкопиранозид 2,3,4,5-тетраацетат:
формула 2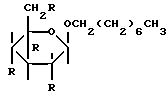
где R представляет собой О2ССН3.
Способность к модификации свойств ГПУ путем небольших изменений в составе делает их уникальными в качестве носителей твердой дозы, особенно по сравнению с полимерными системами, которые часто в зависимости от регионов кристалличности изменяют их свойства, в частности биологическую эрозию. ГПУ системы доставки могут быть сконструированы так, чтобы иметь определенные (четкие) свойства, такие как скорости высвобождения переносимых веществ. Такое конструирование может происходить путем варьирования модификаций конкретного углевода или путем объединения набора различных ГПУ.
Чистые стекла на основе единственного ГПУ, как обнаружено, являются стабильными при температурах окружающей среды и при влажности по крайней мере до 60%. Смеси ГПУ стекол, включающие определенные переносимые вещества, являются, однако, неожиданно стабильными при температурах окружающей среды и при влажности вплоть до 95%. Замечательно, что включение даже 10% (вес/объем) исключительно гигроскопичных переносимых веществ, таких как синтетический кортикостероид 6α, 9α-дифтор-11β,21-дигидрокси-16α, 17α-пропил метилен диокси-4-прегнен-3,20-дион (XPDO), дает ГПУ стекла, которые являются стабильными, когда подвергаются воздействию относительных влажностей вплоть до 95% при комнатной температуре в течение более чем одного месяца, еще непосредственно выпуская переносимые вещества в течение 5-10 минут при добавлении в жидкую воду. Идентичное воздействие на стабильность ГПУ стекла было обнаружено у ТОАЦ стекол, содержащих 10% (вес/объем) ЦСА, включенного в качестве переносимого вещества.
Мы также обнаружили в настоящее время, что добавление других ГПУ при тех же самых уровнях также дает смешанные ГПУ стекла, которые являются в той же степени устойчивыми к расстекловыванию при 95% относительной влажности. Таким образом, ТОАЦ стекла, содержащие 10% (вес/объем) либо ГПАЦ, либо ТОПР, демонстрируют полную устойчивость к расстекловыванию при 95% относительной влажности. Интересно, что эти композитные стекла ведут себя по-разному в жидкой воде, ГПАЦ/ТОАЦ стекло расстекловывается с поверхности гораздо быстрее, чем ТОПР/ТОАЦ стекло. Смотри фигуры 13, 14. Эта способность задавать скорости растворения композитных ГПУ стекол делает их особенно полезными в качестве носителей доставки с контролируемым высвобождением.
ГПУ стекла могут быть сформированы либо путем выпаривания растворителя, либо путем гашения ГПУ расплава. Из-за низких температур размягчения определенных ГПУ стекол, термически лабильные переносимые вещества, такие как лекарства и биологические молекулы, могут быть включены в расплав ГПУ во время обработки системы доставки без разложения. Неожиданно, эти переносимые вещества демонстрируют кинетику высвобождения нулевого порядка, когда композиции, образующие аморфную матрицу, подвергаются эрозии в водном растворе. Высвобождение следует за процессом расстекловывания поверхности. ГПУ системы доставки могут быть легко моделированы в любую форму, такую как те, которые здесь описаны. Такое моделирование может осуществляться путем экструзии, литья и так далее, с помощью любого способа, известного в данной области. ГПУ носители доставки являются нетоксичными и инертными по отношению к любым веществам, которые могут быть включены в них.
Эти ГПУ системы доставки, когда они приготовлены в виде матриц и/или покрытий, подвергаются гетерогенной поверхностной эрозии, когда они помещаются в водное окружение. Хотя и не привязываясь к какой-либо теории, один из возможных механизмов их разложения начинается с начального расстекловывания поверхности, поскольку на границе раздела осуществляются сверхнасыщение с последующей эрозией и/или растворением поверхностных слоев с меньшей скоростью. Матрицы могут быть модифицированы путем аккуратного выбора компонентов для получения желаемых скоростей расстекловывания и, следовательно, требуемых скоростей высвобождения переносимого вещества, поскольку расстекловавшаяся матрица не обеспечивает никакого барьера для высвобождения переносимого вещества.
Расплавы ГПУ являются превосходными растворителями для многих органических молекул. Это делает их особенно пригодными для использования при доставке биологически активных материалов, которые другим способом сложно включать в препарат. Более чем 20% весовых органических молекул могут быть включены в ГПУ системы доставки. Замечательно, что ГПУ являются инертными и не проявляют никакой реакционной активности по отношению к растворенным молекулам или переносимым веществам, включенным в них. Как описано более подробно ниже, ГПУ являются пригодными для формирования мелкодисперсной суспензии СП системы доставки для получения сложных композитных систем доставки.
Многокомпонентные ГПУ синтезируют с высокой чистотой, используя установившиеся принципы химического или ферментативного синтеза. ГПУ и переносимые вещества могут быть тщательно смешаны вместе в соответствующих молярных отношениях и расплавлены до прозрачности. Соответствующие условия плавления включают, но не ограничиваются ими, плавления в открытых стеклянных колбах при температуре между 100 и 150oС в течение 1-2 минут. Это дает в результате жидкий расплав, которому можно дать слегка остыть сначала, растворяя переносимое вещество в расплаве, если необходимо, перед гашением до стекла, например путем выливания на бронзовую пластинку или в металлическую форму для формованных носителей доставки. Другим способом можно осторожно контролировать температуру расплава, и переносимые вещества могут быть включены либо в препарат ГПУ перед плавлением, либо размешаны в остывающем расплаве ГПУ перед гашением.
Расплавы ГПУ являются термически стабильными и дают возможность включения органических молекул без денатурации или суспендирования основных частиц, без изменения их физической природы. Расплавы стекла также могут быть использованы для покрытия частиц микронного размера, это является особенно важным при приготовлении негигроскопичных порошков, содержащих гигроскопичные агенты, для введения путем ингаляции терапевтических агентов.
Альтернативно, стеклообразные носители доставки могут быть образованы путем выпаривания ГПУ и переносимого вещества, которое необходимо включать в раствор в растворителе или в смеси растворителей. Многокомпонентные ГПУ легко растворяются во многих органических растворителях. Соответствующие растворители включают, но не ограничиваются ими, дихлорметан, хлороформ, диметилсульфоксид (ДМСО), диметилформамид (ДМФ) и высшие спирты. Природа растворителя не является важной, поскольку он полностью удаляется при образовании системы доставки. Предпочтительно, чтобы как компонент ГПУ, так и переносимое вещество являлись растворимыми в растворителе. Однако растворитель может растворять ГПУ и давать возможность суспендирования переносимого вещества. При концентрировании растворителя, при использовании более пригодных ГПУ, кристаллизация не осуществляется. Вместо этого образуется аморфный твердый продукт, который по свойствам подобен гашеному стеклу. Опять же, переносимые вещества могут быть легко включены либо из раствора, либо в виде суспензии частиц.
Температуры стеклования ГПУ (Тg) являются низкими, обычно меньшими, чем 70oС, и, неожиданно, не являются предсказуемыми по температурам плавления. Как правило, тенденция к кристаллизации из охлаждающегося расплава или с восстанавливающим растворителем является низкой. Как расстекловывание, так и текучесть расплава при температурах, близких к Тg, могут контролироваться с помощью модификаторов, таких как другие производные сахара и определенные органические активные агенты. Таблицы 1 и 2, полученные, как описано в примерах, представленных ниже, содержат данные по Тg и температуре плавления для ряда ГПУ, пригодных для использования либо по одиночке, либо в композитном стекле.
Изобретение далее определяет носители доставки, содержащие комбинации различных ГПУ, которые, как обнаружено в настоящее время, дают возможность создания новых носителей доставки с хорошо контролируемой Тg и другими физико-химическими свойствами, такими как вязкость и устойчивость по отношению к водному разложению.
Комбинированные системы доставки
Изобретение также указывает системы доставки твердой дозы, содержащие ГПУ и СП, и/или другие стекообразующие вещества в со-препаратах и других комбинациях. Они определяются как "объединенные системы доставки".
По крайней мере две комбинированные системы доставки получают путем совместного приготовления ГПУ и СП носителей для получения систем доставки. В одном случае микросферы СП системы доставки суспендируют в ГПУ системе доставки. Во втором случае микросферы ГПУ системы доставки суспендируют в СП системе доставки. Эти комбинированные системы доставки дают возможность высвобождения по крайней мере двух различных переносимых веществ, одного гидрофобного и одного гидрофильного, при не менее чем двух различных скоростях высвобождения.
Другие комбинированные системы доставки образуют путем покрытия одной системы доставки другой. Например, СП система доставки в имплантируемой форме могла бы быть покрыта слоем ГПУ или ГПУ системой доставки для обеспечения замедленного высвобождения переносимого вещества в СП системе доставки или последовательного высвобождения различных переносимых веществ. Легко себе представить разнообразие таких форм. Число покрытий является теоретически неограниченным и может быть определено специалистом в данной области.
Комбинированные системы доставки могут также быть сформированы путем экструдирования полого цилиндрического носителя, имеющего просвет, из носителя или системы доставки (СП, ГПУ или комбинация) и заполнения просвета другой системой доставки. Эти композиции являются особенно пригодными для формирования средств для инъекции или имплантации.
Другие компоненты в системах доставки
Другие стекла
Как обсуждается ниже, системы доставки могут далее содержать хотя бы одно физиологически приемлемое стекло. Соответствующие стекла включают, но не ограничиваются ими, карбоксилатное, фосфатное, нитратное, сульфатное, бисульфатное, ГПУ и их комбинации. Карбоксилаты ранее использовались там, где требовались стекла, медленно растворяющиеся в воде, поскольку многие из них растворяются в воде довольно плохо. Такие пригодные стекла включают, но не ограничиваются ими, те, которые описаны в PCT/GB 90/00497. Однако образование этих карбоксилатных стекол ранее производилось только путем гашения расплава. Повышенная температура, необходимая для плавления карбоксилатов, строго ограничивает карбоксилаты, которые могут быть использованы для формирования стеклообразных носителей доставки, особенно в случае биологически активных материалов, которые имеют тенденцию к термолабильности. Авторы неожиданно обнаружили в настоящее время, что карбоксилатные стекла могут быть легко образованы путем выпаривания растворителя, содержащего стеклообразующий карбоксилат металла и переносимое вещество, которое должно быть включено. Изобретение, таким образом, определяет способы получения носителей и систем твердой дозы, включающие растворение карбоксилатного компонента в подходящем для этого растворителе и выпаривание растворителя для получения стекловидного стекла. Смеси карбоксилатов могут быть использованы в качестве "упаковочных" смесей других стеклообразующих компонентов для получения новых систем доставки, которые определяются с помощью настоящего изобретения.
Системы доставки также могут быть покрыты одним или более слоями физиологически приемлемого стекла, имеющего заданную скорость растворения. Это является особенно эффективным для высвобождения переносимых веществ с переменной скоростью. Далее, композиция может включать другие водорастворимые и биологически разлагаемые стеклообразующие вещества. Соответствующие стеклообразующие вещества включают, но не ограничиваются ими, лактидные полимеры и лактид/гликолидные сополимеры, глюкуронидные полимеры и другие полиэфиры, полиортоэфиры и полиангидриды.
Переносимые вещества
Примеры типов переносимых веществ, которые могут быть использованы в носителе и в способах настоящего изобретения, включают промышленные химикалии, такие как красители и ароматизаторы, и медицинские или сельскохозяйственные биологически активные материалы, пригодные для использования in vivo и in vitro. Соответствующие биологически активные материалы включают, но не являются ограниченными ими, фармацевтически агенты, терапевтические и профилактические агенты и агрохимикалии, такие как пестициды и феромоны.
Соответствующие фармацевтически агенты включают, но не являются ограниченными ими, противовоспалительные лекарства, анальгетики, противоартритные лекарства, антиспазмодики, антидепрессанты, антипсихотики, транквилизаторы, лекарства для снятия беспокойства, антагонисты наркотиков, лекарства против болезни Паркинсона, холинэргические агонисты, химиотерапевтические лекарства, иммуносупрессивные агенты, противовирусные агенты, антибиотические агенты, суппрессанты аппетита, противорвотные лекарства, антихолинэргики, антигистаминные агенты, противомигреневые агенты, коронарные, церебральные или периферические вазодилаторы, гормональные агенты, контрацептивы, антитромботические агенты, диуретики, противогипертонические агенты, сосудисто-сердечные лекарства, опиоиды и тому подобное.
Соответствующие терапевтические и профилактические агенты включают, но не являются ограниченными ими, любой терапевтически эффективный биологический модификатор. Такие модификаторы включают, но не являются ограниченными ими, субклеточные композиции, клетки, бактерии, вирусы и молекулы, включающие, но не ограниченные ими, липиды, органику, белки и пептиды (синтетические и природные), миметики пептидов, гормоны (пептидные, стероидные и кортикостероидные), D и L полимеры аминокислот, олигосахариды, полисахариды, нуклеотиды, олигонуклеотиды и нуклеиновые кислоты, включая ДНК и РНК, гибриды белок - нуклеиновая кислота, малые молекулы и их физиологически активные аналоги. Далее, модификаторы могут быть получены из природных источников или произведены с помощью рекомбинантных или синтетических средств и включать аналоги агонисты и гомологи.
Используемый здесь термин "белок" относится также к пептидам и полипептидам. Такие белки включают, но не являются ограниченными ими, ферменты, биофармацевтические препараты, гормоны роста, факторы роста, инсулин, моноклональные антитела, интерфероны, интерлейкины и цитокины.
Органика включает, но не является ограниченной ими, фармацевтически активные химикалии. Например, представленная органика включает, но не является ограниченной ими, витамины, нейротрансмитторы, противомикробные средства, противогистаминные средства, анальгетики и иммуносупрессанты.
Соответствующие стероидные гормоны включают, но не являются ограниченными ими, кортикостероиды, эстроген, прогестерон, тестостерон и их физиологически активные аналоги. Многочисленные аналоги стероидных гормонов являются известными в данной области и включают, но не являются ограниченными ими, эстрадиол, SH-135 и тамоксифен. Многие стероидные гормоны, такие как прогестерон, тестостерон и их аналоги, являются особенно пригодными для использования в настоящем изобретении, поскольку они не адсорбируются трансдермально и за исключением немногих аналогов разрушаются при оральном приеме по так называемому механизму первого прохождения через печень.
Используемый здесь термин "нуклеиновые кислоты" включает любые терапевтически эффективные нуклеиновые кислоты, известные в данной области, включая но не ограничиваясь ими, ДНК, РНК и их физиологически активные аналоги. Нуклеотиды могут кодировать единичные гены или могут быть любым вектором рекомбинантной ДНК, известным в данной области, включая, но не ограничиваясь ими, плазмиды, ретровирусы и аденоассоциированные вирусы. Предпочтительно, нуклеотиды вводятся в порошковой форме твердой системы дозировки.
Композиции, составляющие твердую дозированную системы доставки, содержащие профилактические биологически активные материалы и их носители, определяются далее с помощью настоящего изобретения. Предпочтительные композиции включают иммуногены, такие как для использования в вакцинах. Предпочтительно, композиции включают иммуногенное количество иммуногена, эффективного либо для иммунизации, либо для стимулирующей инокуляции.
Соответствующие иммуногены включают, но не являются ограниченными ими, живые и ослабленные вирусы, векторы нуклеотидов, кодирующие антигены, бактерии, антигены, антигены плюс вспомогательные вещества и гаптены, связанные с носителями. Особенно предпочтительными являются иммуногены, эффективные при вызове иммунного ответа против дифтерии, тетануса, коклюша, ботулизма, холеры, лихорадки Денге, гепатита А, С и D, гемоглобинофинные бактерии гриппа В, вируса герпеса, Helicobacterium pylori, гриппа, японского энцефалита, менингококков А, В и С, кори, свинки, вируса папилломы, пневмококка, полиомиелита, краснухи, ротавируса, респираторного синцитиального вируса, шигелла, туберкулеза, желтой лихорадки и их комбинаций.
Иммуногены также могут быть получены с помощью методик молекулярной биологии для получения рекомбинантных пептидов или белков слияния, содержащих одну или несколько частей белка, полученного от патогена. Например, белки слияния, содержащие антиген, представляющий интерес, и В-субъединица токсина холеры, как показано, индуцируют иммунный ответ на представляющий интерес антиген. Sanchez et al. (1989) Proc. Natl. Acad. Sci. USA 86: 481-485.
Предпочтительно иммуногенная композиция содержит определенное количество вспомогательного вещества, достаточное для усиления иммунного ответа на иммуноген. Соответствующие вспомогательные вещества включают, но не являются ограниченными ими, соли алюминия, скваленовые смеси (SAF-1), мурамилпептид, сапониновые производные, препараты клеточных стенок микобактерий, монофосфориллипид А, производные миколовой кислоты, поверхностно-активные вещества на основе неионных блок-сополимеров, Quil А, В-субъединицу токсина холеры, полифосфазен и производные и иммуностимулирующие комплексы (ИСКОМ), такие как те, которые описаны Takahashi et al. (1990) Nature 344: 873-875. Для ветеринарного использования и производства антител у животных могут быть использованы митогенные компоненты вспомогательного вещества Фройнда.
Как происходит со всеми иммуногенными композициями, иммунологически эффективные количества иммуногенов должны определяться эмпирически. Факторы, которые должны быть учтены, включают иммуногенность, будет ли иммуноген комплексно или ковалентно связан со вспомогательным веществом или несущим белком или другим носителем или нет, от способа введения и от числа иммунизирующих доз, которые необходимо принять. Такие факторы являются известными в области вакцинирования, и у иммунологов имеется достаточный опыт проведения таких определений без излишних экспериментов.
Предпочтительно, если переносимое вещество и/или носитель содержат карбоксильную и амино-, имино- или гуанидиногруппы, системы доставки, кроме того, содержат хотя бы один физиологически приемлемый ингибитор реакции Маллара в количестве, эффективном для того, чтобы в основном предотвратить конденсацию аминогрупп и реакционноактивных карбонильных групп в композиции.
Ингибитором реакции Маллара может быть любой из таких ингибиторов, известных в данной области. Ингибитор присутствует в количестве, достаточном, чтобы предотвратить или в основном предотвратить конденсацию аминогрупп и реакционноактивных карбонильных групп. Обычно аминогруппы присутствуют на биологически активном материале, а карбонильные группы присутствуют на углеводороде или наоборот. Однако амино и карбонильные группы могут быть внутримолекулярными, внутри либо биологического вещества, либо углеводорода. Различные классы соединений являются известными как проявляющие ингибирующее воздействие на реакцию Маллара и поэтому пригодные для использования в композициях, описанных здесь. Эти соединения являются обычно либо конкурентными, либо неконкурентными ингибиторами. Конкурентные ингибиторы включают, но не являются ограниченными ими, аминокислотные остатки (как D, так и L), комбинации аминокислотных остатков и пептидов. Особенно предпочтительными являются лизин, аргинин, гистидин и триптофан. Лизин и аргинин являются наиболее эффективными. Существует множество известных неконкурентных ингибиторов. Они включают, но не являются ограниченными ими, аминогуанидин и производные, являются производными 4-гидрокси-5,8-диоксохинолина и соответствующими ингибиторами Маллара, такими как ингибиторы, описанные в ЕР-А-О-433679.
Формы дозировки
В дополнение к формам дозировки, описанным выше, множество других форм дозировки, которые являются пригодным для различного использования, предусматриваются здесь.
Изобретение определяет системы доставки, которые имеют размер и форму, предназначенные для проникновения через эпидермис и являются пригодными для баллистической доставки. Соответствующий размер носителя составляет, таким образом, порядка микрон, предпочтительно в диапазоне 1-5 микрон в диаметре и 5-150 микрон длиной, что делает возможным проникновение и доставку через эпидермис к подкожным и интрадермальным, внутримышечным, внутривенным тканям. Понятно, что при этом размере система доставки может макроскопически казаться находящейся в форме порошка независимо от ее конфигурации на микроскопическом уровне.
Предпочтительными конфигурациями баллистических систем доставки являются микроиголки и микроволокна. Производство микроволокон является относительно простым и экономичным и дает в результате стабильные системы доставки, состоящие из носителя в стеклообразной форме и переносимого вещества. Дополнительные стабилизаторы, буферы, стекла и полимеры могут также быть добавлены во время обработки, как здесь описано. Многие из наиболее лабильных биомолекул могут противостоять высоким температурам (например, 60-100oС) после стабилизации путем сушки в трегалозе, обеспечивая контакт большей части их поверхности с носителем. Температуры в 70oС могут выдерживаться в течение более чем месяца (Colaco et al. (1992) Bio/Technology 10: 1007-1011), а более высокие температуры - в течение более коротких периодов. Результаты, представленные здесь, показывают, что флуоресцентный белок пикоэритрин, высушенный в трегалозе, может храниться при 100oС в течение не менее одного месяца без заметных потерь функциональной активности. Другие носители дают защиту при более низких температурах, чем трегалоза. Максимальная температура защиты должна определяться эмпирически с помощью опыта, накопленного в данной области, и без излишних экспериментов.
Микроволокна, полученные в соответствии с принципами настоящего изобретения, имеют относительно высокое отношение размеров, то есть длины к диаметру, предпочтительно в диапазоне 1-5 микрон в диаметре и 5-150 микрон длиной. Это высокое отношение размеров обеспечивает усиленное проникновение "насквозь" при баллистической доставке из-за тенденции микроволокон выстраиваться параллельно стволу баллистического микроинжектора, как описано более подробно ниже. Более длинные макроволокна могут впрыскиваться с использованием обычных импульсных баллистических устройств или с помощью троакара. Альтернативно, макроскопические стеклянные иголки с достаточной собственной длиной могут быть непосредственно введены через кожу для подкожного, интрадермального или интрамускулярного введения переносимого вещества.
Альтернативные предпочтительные воплощения систем доставки включают однородные микросферы, предпочтительно с узким распределением по размерам. Эта конфигурация является особенно полезной, когда желательным является повышенный контроль глубины проникновения системы доставки. Такой контроль был бы полезен, например, для интрадермальной, внутримышечной, внутривенной доставки вакцин к базальному слою эпидермиса, чтобы ввести антиген вблизи клеток кожи Лангерганса для индуцирования оптимальных иммунных ответов.
Изобретение также определяет полые волокна для доставки переносимых веществ. Путем продавливания полой заготовки через зонную печь, которая вызывает локальное размягчение стеклянного носителя, могут быть сформированы тонкие пустые иголки. Эти иголки могут быть наполнены стабилизированным соединением в виде тонкого порошка путем введения тонкого порошка во время процесса плавления и продавливания. Полое волокно также может быть получено из термопластика, органического полимера, и/или углеводорода, и/или ГПУ, который сам по себе может быть быстро или медленно растворимым в воде и/или биологически разлагаемым.
Альтернативное воплощение носителя доставки в изобретении содержит полый носитель, состоящий из плохо растворимого в воде стекла или пластика, который заполняет и необязательно покрывает описанные здесь системы доставки.
В другом воплощении изобретения включенными являются со-препараты носителей и других плохо растворимых в воде материалов. Например, со-препараты носителей с водорастворимыми стеклами, такими как фосфатные, нитратные или карбоксилатные стекла, или биологически разлагаемыми пластиками, такими как лактидные полимеры или лактид/гликолидные сополимеры, будут давать более медленно разрушающийся носитель для замедленного высвобождения биологически активного материала.
Способы получения систем доставки
Изобретение далее указывает способы получения твердых систем дозировки. Предусматривая, что время выдержки является ограниченным, переносимые вещества, смешанные с сухими носителями, могут быть нагреты для размягчения стекла, которое затем может продавливаться или протягиваться, как волокно, без повреждения продукта. Волокна могут либо быть выдавлены из заготовки, охлаждены до их отверждения, а затем намотаны на барабан, либо они могут быть протянуты через тонкие отверстия в быстро вращающемся цилиндре, который нагрет до температуры, превышающей температуру плавления носителя. Будучи изначально хрупкими, эти волокна могут быть легко разрезаны, разломаны или посечены на короткие отрезки для образования длинных цилиндрических стержней или иголок. Путем варьирования диаметра получаемых волокон могут быть сформированы иголки, которые изменяются от микро- до макроиголок, то есть от толщин в несколько микрон до долей миллиметра. Было обнаружено, что машины для изготовления сахарной ваты являются пригодными для использования микроволокон меньшего диаметра. Хотя оптимальные условия для каждого носителя должны подбираться эмпирически, такие определения вполне доступны специалистам в данной области.
Для получения микросфер настоящего изобретения могут быть использованы несколько способов в зависимости от желаемого применения носителей доставки. Соответствующие способы включают, но не являются ограниченными ими, сушку распылением, сушку вымораживанием, сушку на воздухе, сушку в вакууме, сушку в ожиженном слое, помол, соосаждение и испарение сверхкритической жидкости. В случае сушки распылением, сушки вымораживанием, сушки на воздухе, сушке в вакууме, сушки в ожиженном слое и испарения сверхкритической жидкости, компоненты (СП, и/или ГПУ, и/или другое стеклообразующее вещество, переносимые вещества, буферы и тому подобное) сначала растворяют или суспендируют в соответствующих растворителях. В случае помола стекла, сформированные из компонентов либо путем выпаривания растворителя, либо путем гашения расплава, перемалывают в высушенной форме и обрабатывают с помощью способа, известного в данной области. В случае соосаждения компоненты смешивают в органических условиях и обрабатывают, как описано ниже.
Сушка распылением может быть использована для загрузки носителя переносимым веществом. Компоненты смешивают при условиях соответствующего растворителя и сушат, используя точные сопла, получая в сушильной камере исключительно однородные капли. Соответствующие машины для сушки распылением включают, но не являются ограниченными ими, сушилки-распылители Buchi, NIRO и Lab-plant, используемые согласно инструкциям изготовителей. Ряд углеводородов являются непригодными для использования при сушке распылением, поскольку температуры плавления углеводородов являются слишком низкими, вызывая прилипания высушенных аморфных материалов к стенкам сушильной камеры. Обычно углеводороды с температурой плавления, меньшей, чем рабочая температура камеры для сушки распылением, являются непригодными для использования при сушке распылением. Например, палатинит и лактитол являются непригодными для использования при сушке распылением в обычных условиях. Определение пригодных углеводородов, таким образом, может быть проделано по известным температурам плавления или определены эмпирически. Такие определения вполне доступны для специалиста в данной области.
Альтернативный способ для получения микросфер в качестве носителей доставки в соответствии с настоящим изобретением представляет собой приготовление однородной эмульсии водная/органическая фаза переносимого вещества в растворе носителя, как в водной фазе, и стеклообразующего вещества в органической фазе, или наоборот. За этим следует сушка капель эмульсии для формирования твердого раствора переносимого вещества и носителя в аморфной матрице стеклообразующего вещества. В одной из модификаций этого способа эмульсия может быть сформирована из переносимого вещества в твердом растворе в носителе и двух различных стеклообразующих веществах и/или полимерах, растворенных вместе в одном растворителе или растворенных в двух отдельных растворителях. Затем растворитель (растворители) удаляют путем выпаривания, получая двух- или многостенные микросферы. Соответствующие способы получения многостенных микросфер описаны, например, Pekarek et al. (1994) Nature 367: 258-260 и в патенте США 4861627.
Система доставки также может быть высушена из органического раствора СП и гидрофобного переносимого вещества для образования стекла, содержащего однородно распределенное переносимое вещество в твердом растворе или мелкодисперсной суспензии в полиоловом стекле. Эти стекла могут затем быть перемолоты и/или измельчены до микронного размера для получения микрочастиц с однородным заданным распределением по размерам.
Переносимое вещество и носитель могут также быть соосаждены для получения порошков высокого качества. Соосаждение производится путем распыления, например, с помощью аэрозольного баллончика, различных компонентов и/или полимерных стеклообразующих веществ в жидкости, в которой ни один из них не растворяется, такой как ацетон на льду.
Изобретение также определяет полые волокна для доставки переносимых веществ. Путем продавливания нагретой полой заготовки могут быть сформированы тонкие полые иголки. Они могут быть сделаны так, чтобы содержать стабилизированное соединение в виде тонкого порошка, с помощью введения тонкого порошка во время процесса плавления и продавливания. Полое волокно также может быть сделано из термопластика, органического полимера, и/или углевода, и/или ГПУ стекла, которые сами по себе могут быть медленно или быстро растворятся в воде и/или биологически разлагаться.
Альтернативное воплощение системы доставки в настоящем изобретении включает полый носитель, состоящий из плохо растворимого в воде стекла или пластика, который заполнен и необязательно покрыт СП и/или ГПУ стеклом и переносимым веществом. Тонкие полые волокна из медленно растворяющихся в воде неорганических или органических стекол могут быть выдавлены из полой заготовки, и измельченная в тонкий порошок СП система доставки может быть включена в просвет заготовки и, следовательно, волокна, во время процесса.
В другом воплощении настоящего изобретения являются включенными со-препараты носителей и других водорастворимых материалов. Например, со-препараты носителей с водорастворимыми стеклами, такими как фосфатные стекла (Pilkington Glass Company), или биологически разлагаемыми пластиками, такими как лактидые полимеры или лактид/гликолидные сополимеры, будут давать более медленно разрушающийся носитель для замедленного высвобождения переносимого вещества. Для получения со-препаратов стекло в виде тонкого порошка, содержащее переносимое вещество, может быть тщательно смешано с карбоксилатным стеклом в виде тонкого порошка и спечено. Альтернативно, если металлкарбоксилатное стекло имеет более низкую температуру плавления, чем система доставки, последняя может быть гомогенно взвешена в виде инкапсулята в карбоксилатном стекле при гашении полученного расплава. Он может быть размолот для получения тонкого порошка с растворимостями, промежуточными между относительно быстрой растворимостью носителя и медленной растворимостью карбоксилатного стекла.
Альтернативные со-препараты включают использование гомогенной суспензии тонкого порошка стеклообразной системы доставки, включенной в карбоксилатном стекле путем сушки из органического растворителя, в котором карбоксилат является растворимым, но аморфный порошок - нет, для образования карбоксилатного стекла. Оно может быть перемолото для получения тонкого порошка, который имел бы относительно быстро растворяющуюся систему доставки, захваченную внутри медленно растворяющегося карбоксилатного стекла (то есть сравнимую с обычной системой с медленным высвобождением). Высвобождение с переменной скоростью может быть достигнуто либо с помощью повторяющихся циклов инкапсуляции, используя стекла с различными скоростями растворения, либо путем смешивания порошков ряда со-препаратов с желаемым диапазоном характеристик высвобождения. Заметьте, что это стекло также может быть выдавлено или протянуто для получения микроволокон, которые могли бы быть имплантантами с низкими скоростями высвобождения. Будет очевидным, что любой препарат системы доставки должен быть таким, чтобы он был способен выпускать переносимое вещество при введении, и не должен отрицательно влиять на стабильность материала, который вводиться.
Как обсуждалось выше, пригодными для использования здесь являются также стекла производных углеводов. Соответствующие производные углеводы включают, но не являются ограниченными ими, сложные и простые эфиры углеводов, имиды, плохо растворимые в воде производные и полимеры.
Носитель доставки может быть загружен переносимым веществом путем сушки раствора переносимого вещества, содержащего достаточное количество носителя для образования стекла при сушке. Эта сушка достигается способами, известными в данной области, включая но не ограничиваясь ими, сушку вымораживанием, вакуумную сушку, сушку распылением, конвейерную сушку, воздушную сушку или сушку в ожиженном слое. Высушенный материал может быть перемолот в тонкий порошок перед дальнейшей обработкой материала с полиоловым стеклом или со-препаратом.
В зависимости от используемого носителя доставки также могут быть достигнуты различные схемы дозировки. Носитель доставки настоящего изобретения может быть предусмотрен для быстрого высвобождения текущей дозы переносимого вещества после введения, где система доставки является легко растворимой. Со-препараты носителей с медленно растворяющимися в воде стеклами и пластиками, такими так как фосфатное, нитратное или карбоксилатное стекла, и лактид/гликолидными, глюкуронидными или полигидроксибутиратными пластиками и полиэфирами, могут обеспечить более медленно растворяющиеся носители для более медленного высвобождения и пролонгированного действия дозировки. Начальное и ускоряющее действие также может быть реализовано путем применения полого медленно растворяющегося в воде носителя, заполненного и покрытого быстро растворяющимся СП и/или ГПУ стеклом, нагруженным переносимым веществом. Стеклянное покрытие, нагруженное переносимым веществом, будет растворяться быстро, давая эффект начальной дозировки. Когда часть носителя, расположенного на наружной стенке, растворится, не будет никакого дозирующего действия, но за начальной инициирующей дозой последует усиливающая доза из внутреннего наполнения, когда наружная стенка истончится из-за растворения. Такой режим высвобождения с переменной скоростью является особенно полезным для доставки иммуногенных композиций. Если является желательным многократный эффект доставки с переменной скоростью, могут быть сконструированы носители доставки с любой комбинацией слоев "ненагруженных" носителей и носителей, нагруженных переносимыми веществами.
Доставка более чем одного переносимого вещества также может быть достигнута при использовании системы доставки, состоящей из многих покрытий или слоев носителя, нагруженных различными материалами или их смесями. Введение систем доставки твердых доз настоящего изобретения может быть использовано вместе с другими обычными способами терапии, или оно проводится совместно с другими терапевтическими, профилактическими или диагностическими веществами.
Способы доставки
Изобретение далее определяет способы доставки твердых систем дозировки.
Соответствующие способы доставки переносимых веществ включают, но не являются ограниченными ими, местный, трансдермальный, трансмукозальный, оральный, желудочно-кишечный, подкожный, окулярный, внутримышечный, внутривенный способы и введение путем ингаляции (назо-фарингеальное и пульмонарное, включая трансбронхиальное и трансальвеолярное). Местное введение осуществляется, например, путем повязки или бандажа, имеющих внутри диспергированную систему доставки, или путем прямого введения системы доставки в разрезы или открытые раны. Кремы или мази, имеющие диспергированные в них шарики или микросферы системы доставки с медленным выходом, являются пригодными для использования, например, в качестве наружных мазей или агентов, заполняющих раны.
Композиции для трансдермального введения являются предпочтительно порошками систем доставки в форме микроиголок или микрошариков одинакового размера. Макроскопические формы иголок и шариков большего размера для систем доставки также предусмотрены для подкожной инплантации и растянутой по времени доставки лекарств. Размеры частиц должны быть достаточно малыми, чтобы они вызывали только минимальное повреждение кожи при введении. Порошковые формы систем доставки могут быть микроиголками примерно 10-1000 микрон длиной и 1-150 микрон диаметром. Порошки могут быть предварительно упакованы в однодозовых, герметичных, стерильных упаковках.
Соответствующие способы трансдермального введения включают, но являются не ограниченными ими, доставку с помощью непосредственного втыкания, баллистическую, доставку с помощью троакара и струи жидкости. Для доставки с помощью непосредственного втыкания макроиголки могут быть точно сформированы с помощью способов, хорошо известных в области формования неорганического стекла, таких как те, которые используются при производстве оптического волокна. Эти иголки могут содержаться в точно сформированном закрытом подогнанном пластиковом стволе и внедряться непосредственно через кожу с помощью плунжера. Баллистическое введения является предпочтительным, поскольку оно является относительно безболезненным. Обычно система доставки ускоряется в ударной волне гелия или другого газа и выстреливается в эпидермис. Соответствующее устройство для баллистической доставки описано в PCT/GB 94/00753. Соответствующее устройство для доставки в струе жидкости представляет собой Medi-ject device (Diabetes Care (1993) 1b, 1479-1484). Такие устройства с жидкой струей являются особенно полезными для систем доставки с макроиглами больших размеров, которые могут также быть доставлены с помощью использования обычных импульсных баллистических устройств или с помощью троакара.
При трансдермальном введении степень проникновения систем доставки может контролироваться до определенной степени не только с помощью баллистического микроинжектора, описанного ниже, но также с помощью формы и размера частиц порошка. Например, когда желательной является относительная однородность и меньшая степень проникновения, микросферы могут быть более соответствующими для практики настоящего изобретения. Когда желательной является большая степень проникновения, конфигурация микроиголок может быть предпочтительной.
Поскольку отношение размеров (то есть отношение длины к диаметру) микроигл является высоким, они имеют большие массы, чем сферические частицы с подобным диаметром. Если им придается импульс для проникновения кожи "насквозь", их более высокая масса придаст им больший импульс при той же самой скорости и они будут, таким образом, проникать глубже в ткани. Когда беспорядочно ориентированные микроиголки помещают в ламинарный поток газа, они сами по себе будут выстраиваться в направлении потока воздуха, и в баллистическом инжекторе, приводимым в движение газом, это будет обеспечивать их проникновение в кожу под прямым углом для обеспечения проникновения.
Системы доставки, пригодные для трансмукозальной доставки, включают, но не являются ограниченными ими, мукоадгезивные облатки, пленки или порошки, лепешки для орального приема, пессарии и кольца и другие устройства для вагинальной или шеечной доставки.
Композиции, пригодные для желудочно-кишечного введения, включают, но не являются ограниченными ими, фармацевтически приемлемые порошки, таблетки, капсулы и пилюли для проглатывания и суппозитории для ректального введения.
Композиции, пригодные для подкожного введения, включают, но не являются ограниченными ими, различные имплантанты. Предпочтительно имплантанты являются частицами дискоидной, сферической или цилиндрической формы для простоты введения и могут обеспечивать либо быстрое, либо медленное высвобождение. Поскольку весь имплантант растворяется в телесных жидкостях, удаление имплантанта не является необходимым. Кроме того, имплантанты не содержат синтетических полимеров и являются биологически разлагаемыми.
Композиции, пригодные для окулярного введения, включают, но не являются ограниченными ими, препараты микросфер и макросфер и капли на основе солевого раствора, кремы и мази, содержащие их, и стержни округлой формы, которые с комфортом подгоняются к нижнему коньюктивальному своду за нижним веком.
Композиции, пригодные для введения путем ингаляции, включают, но не являются ограниченными ими, порошковые формы систем доставки. Предпочтительно порошки имеют размер частиц от 0,1 до 10 микрон. Более предпочтительно размер частиц составляет от 0,5 до 5 микрон. Наиболее предпочтительно размер частиц составляет от 1 до 4 микрон. В частности, для пульмонарного введения предпочтительный размер частиц составляет 2,5-3 микрона.
Предпочтительно порошки СП носителей доставки также содержат эффективное количество физиологически приемлемого буфера - молекулярного водяного насоса (МВН). МВН представляет собой физиологически приемлемую соль, которая вызывает потерю воды из композиции, так что при влажности окружающей среды давление паров воды кристаллизации составляет не менее 14 мм рт. ст. (2000 Па) при 20oС и не мешает стеклообразованию в носителе. Эффективное количество МВН является таким, которое для предотвращения заметного слипания существенно уменьшает гигроскопичность, например, это 50% молярная доля сульфата калия. Сульфат натрия и лактат кальция являются предпочтительными солями, с сульфатом калия, являющимся наиболее предпочтительным.
Композитные ГПУ системы доставки являются особенно пригодными для использования для форм дозировки, вводимых путем ингаляции. Например, 10% (вес/объем) α-ГПАЦ/ТОАЦ смешанные системы доставки являются устойчивыми по отношению к 95% относительной влажности (ОВ), но повторно кристаллизуются при контакте с жидкой водой и, таким образом, выпускают любые переносимые вещества, включенные в них. Это является особенно важным для порошков для ингаляций, поскольку эти порошки предпочтительно должны расстекловываться и выпускать переносимые вещества при достижении жидкости альвеол, а не во влажных трахеальных дыхательных путях.
Атомайзеры и вапорайзеры, наполненные порошками, также определяются настоящим изобретением. Существует разнообразие приборов, пригодных для использования при доставке порошков путем ингаляций. Смотри, например, Lindberg (1993) Summary of Lecture at Management Forum 6-7 December 1993 "Creating the Future for Portable Inhalers". Дополнительные устройства, пригодные для использования здесь, включают, но не являются ограниченными ими, устройства, описанные в WО 9413271, WО 9408552, WО 9309832 и в патенте США 5239993.
Настоящим изобретением определяются разнообразные другие твердые дозированные системы доставки. Они являются пригодными для доставки широкого разнообразия немедицинских переносимых веществ. Например, ГПУ стекло, включающее агрономическое переносимое вещество, является сухим на складе, даже в тропиках, но выпускает пестицид или агенты биологического контроля при контакте с жидкой водой на поверхности плантаций или в почве. ГПУ стекло, включающее фермент, является полезным для использования при добавлении к стиральным поверхностно-активным порошкам, поскольку оно стабилизирует фермент еще даже при высокой влажности, выпуская фермент непосредственно при контакте с водой. Многочисленные другие воплощения определяются заявляемым изобретением и являются доступными для понимания специалистам в данной области.
Последующие примеры приводятся для иллюстрации, но не ограничения настоящего изобретения.
Пример 1
Способы производства микроволоконных СП стеклообразных дозированных твердых систем доставки.
а) Получение СП микроволокна
Стекла получают путем сушки 20% растворов либо трегалозы, либо лактитола, либо палатинита, либо GPS, включающих МВН, и 1 мг/мл флуоресцентного белка морских водорослей фикоэритрина, в вакууме (80 мТорр) в течение 16 часов. Стекла перемалывают в домашней ручной мельнице для кофе с получением грубого порошка, который используют для наполнения вращающейся головки машины для получения сахарной ваты Kando K1 Kandy Floss(патент Великобритании 1533012). Затем включают мотор и порошкообразное сахарное стекло нагревают при настройке машины между 5 и 9. Время пребывания во вращающейся головке составляет 2-10 мин, и непрерывный процесс поддерживают путем непрерывного досыпания порошка в головку.
Полученные волокна перемалывают в домашней кофемолке, и полученные результаты представлены в Таблице 3, которая показывает среднее значение для полученных иголок. Эти данные показывают, что для всех трех сахарных стекол пониженные значения настроек дают в результате получение микроиголок меньшего диаметра. С трегалозой настройка 6 дает микроиголки со средним диаметром в 15 микрон, а настройка 9 микроиголки со средним диаметром в 40 микрон. С GPS настройка 9 дает микроиголки со средним диаметром в 15 микрон. Микроиголки, получаемые из стекол, содержащих буферные соли, остаются сухими при температурах и влажностях окружающей среды. Микроиголки, содержащие пикоэритрин, проявляют задержку биологической активности согласно оценкам по флуоресценции.
b) Получение микроволокон на основе бинарных СП/органических композитных стекол
Стекла создают путем сушки смеси 5: 1: 1 трегалозы, октаноата натрия и воды в вакууме (80 мТорр) в течение 16 часов. Стекла перемалывают в домашней ручной мельнице для кофе для получения грубого порошка, который используют для заполнения вращающейся головки машины для получения сахарной ваты Kando K1 Kandy Floss. Затем включают мотор и порошкообразное бинарное углеводород/органическое стекло нагревают при настройках между 5 и 9. Как и с чистыми трегалозными стеклами, уменьшенные значения настройки дают в результате получение микроиголок меньшего диаметра. Бинарные смеси для стекол могут быть подобраны для получения стекол со значительно отличающимися механическими свойствами по сравнению с соответствующими чистыми трегалозными стеклами. Время пребывания во вращающейся головке снова составляет 2-10 мин, и непрерывный процесс поддерживают путем непрерывного досыпания порошка в головку. Полученные результаты показывают, что разбросы температур плавления и времен растворения стекол и получающиеся в результате физические свойства микроволокон могут быть достигнуты путем варьирования как углеводород/органических молекул, так и используемых их отношений.
Пример 2
Способы получения порошкообразных СП стеклообразных дозированных твердых систем доставки
а) Включение активного агента в СП стеклообразный носитель доставки с получением порошков микронных размеров
Стекла создают путем сушки 20% растворов либо трегалозы, либо лактитола, либо палатинита, либо GPM, либо GPS, включающих эквимолярное отношение МВН и белка, путем сушки вымораживанием в вакууме (80 мТорр) в течение 16 часов. Стекла превращают в порошок, используя воздушно-струйную мельницу (Trost). Размеры частиц в порошках микронных размеров измеряют, используя лазерный измеритель размеров частиц Malvern Mastersizer. Результаты, полученные с порошками микронных размеров, полученными из исходного раствора 0,5 М трегалозы и 0,5 М лактата кальция, показывают монодисперсное распределение частиц со средними диаметрами частиц в 1,1 микрона (фигура 1). Порошки, включающие МВН, остаются в форме сыпучего порошка и не проявляют изменений размера частиц или слипания и поглощения воды при продолжительной экспозиции при температурах и влажностях окружающей среды (фигуры 2А и 2В).
b) Включение активного агента в СП стеклообразный носитель доставки с получением порошков, высушенных распылением
20% Растворы трегалозы, содержащие соли МВН и белок (фикоэритрин), сушат в сушке-распылителе Buchi или Lab-plant при производительности насоса в 500-550 мл/ч и выходной температуре в 180oС. Размер частиц измеряют, используя лазерный измеритель размера частиц SympaTec. Порошки, высушенные распылением, демонстрируют монодисперсное распределение частиц с достаточно узким пиком распределения по размерам для эффективного использования в качестве частиц в порошковом баллистическом устройстве. В результатах, представленных в фигуре 3, анализ размеров частиц порошков, полученных с помощью сушки распылением, которые получаются путем сушки распылением смеси 0,5 М трегалозы и 0,5 М лактата кальция в сушке-распылителе Lab-plant, демонстрирует средний диаметр частиц в 8,55 микрон и иллюстрирует полученный узкий пик распределения.
Варьирование среднего размера частиц может быть достигнуто путем варьирования либо композиции смеси, которая должна подвергаться сушке распылением, либо характеристик сопла используемого узла сушки-распылителя. Результаты, представленные в фигуре 4, дают возможность сравнения анализа размера частиц порошка, полученного сушкой распылением, как в фигуре 3, с порошком, полученным сушкой распылением, который получают путем сушки той же самой смеси в сушке-распылителе Buchi, который использует другой узел сопла. Пик распределения, представленный в фигуре 4, представляет в равной степени узкий диапазон, но средний размер частиц здесь составляет 7,55 микрона.
Эти данные показывают, что частицы, полученные с помощью различных процессов сушки распылением, являются в равной степени пригодными для создания композиций для баллистической доставки. Заметьте, что возможность варьировать размер частиц дает в результате композиции с различными характеристиками проникновения. Это является особенно важным для определения интрадермальной, внутримышечной, внутривенной или внутримышечной доставки, поскольку проникновение является функцией импульса частицы, а распределение является функцией разброса размеров частиц.
с) Включение активного агента в СП стеклообразный носитель доставки с помощью сушки из органических растворителей.
50 мг/мл раствор ЦСА в 1: 1 смеси этанол: вода, содержащий 20% трегалозы, сушат на воздухе при температуре окружающей среды с образованием прозрачного трегалозного стекла, содержащего ЦСА, в твердой суспензии или растворе. Стекло перемалывают, получая порошок согласно способу, описанному в примере 1, и поддерживая сыпучий порошок при температуре и влажности окружающей среды. Добавление порошка к воде дает в результате растворение трегалозы и образование однородной водной суспензии ЦСА.
d) Включение активного агента в СП стеклообразный носитель доставки путем соосаждения.
20% Растворы трегалозы, лактитола, палатинита, GPM или GPS, содержащие МВН и белок (фикоэритрин), сушат путем распыления в охлажденной бане, содержащей ацетон и твердую двуокись углерода. Осажденные порошки отделяют путем центрифугирования или фильтрования и сушат на воздухе для удаления остаточного растворителя. Порошки снова показывают монодисперсное распределение частиц, и порошки, содержащие соли буферных препаратов, остаются сухими при температурах и влажностях окружающей среды.
e) Получение композитного стеклообразного носителя доставки твердой дозы гидрофобного активного агента в СП путем сушки из органических растворителей.
Две различных системы растворителей используют для получения композитных стекол. В первом случае ЦСА растворяют в абсолютном этаноле, а затем медленно добавляют равный объем воды, так что ЦСА, который осаждается при каждом добавлении, имеет возможность повторно раствориться. Затем растворяют трегалозу в 50% этаноловом растворе (объем/объем) до конечной концентрации 50% вес/объем. Композитные стекла получают путем выпаривания смешанного растворителя на конфорке при 70oС. Во втором случае как ЦСА, так и трегалозу растворяют в ДМФ и снова композитное стекло получают путем выпаривания, как описано выше. В обоих случаях в результате получают слегка опалесцирующие стекло. Затем капли воды наносят на пленки стекла для изучения свойств растворения и высвобождения у стекол.
Полученные результаты показывают, что стекла ведут себя совершенно по-разному. Стекла, полученные из ДМФ, являются водоотталкивающими с очевидно гидрофобной поверхностью. Они постепенно образуют непрозрачные белые пятна и скопления осажденного ЦСА там, где они были в контакте с водой. Стекла, сделанные из 50% этанола, являются гидрофильными. Они быстро растворяются в воде и при этом выпускают облако очень мелких частиц ЦСА. Последнее стекло, вероятно, содержит ЦСА либо как мелкодисперсную суспензию твердых частиц, либо как твердый раствор в трегалозном стекле, которое выпускает ЦСА в виде осадка, когда трегалоза растворяется. Как таковое оно представляет очень полезную форму дозировки для ЦСА с высокой биологической доступностью из-за его однородного и мелкодисперсного состояния после высвобождения.
Различное поведение стекол идентичной композиции после сушки из различных растворителей подсказывает интересный и полезный способ обеспечения точного контроля над структурой осаждения различных стекол во время выпаривания растворителя. Поскольку ЦСА является более растворимым в ДМФ, чем трегалоза, композитные стекла 10-20% ЦСА в трегалозе, полученные из этого растворителя, имеют тенденцию создавать гидрофильные трегалозные ядра с гидрофобными ЦСА покрытиями. В противоположность этому, когда испаряется 50% этанол, ранняя потеря этанола при 97% азеотропии вызывает высвобождение ЦСА из раствора в окружении трегалозного сиропа, который затем отверждается в виде непрерывной фазы, приводя к твердой эмульсии ЦСА в трегалозном стекле.
Пример 3
Защита белков от органического растворителя и повышенных температур, осуществляемая путем сушки в трегалозе
a) Защита пероксидазы хрена и щелочной фосфатазы от ацетона, осуществляемая путем сушки в трегалозе
0,1 мг/мл раствор пероксидазы хрена или раствор 1 мг/мл щелочная фосфатаза /4 мг/мл бычий сывороточный альбумин сушат в сушке-морозильнике FTS Systems с 50% трегалозы или без нее. Используют вакуумную сушку и смеси сушат без замораживания. Четыре раза добавляют объем растворителя и позволяют раствору выпариться досуха. Содержимое повторно растворяют в 5 миллилитрах воды и активность фермента оценивают при последовательном разбавлении с помощью коммерческого "набора" реагентов. Набор для щелочной фосфатазы берут от Sigma Chemical Co. , а набор для пероксидазы хрена берут от Kirkegaard & Perry Laboratories, Inc. Как показано на фигурах 5А и 5В, ферменты, высушенные с трегалозой, являются более устойчивыми по отношению к ацетону, чем ферменты, высушенные без трегалозы.
b) Защита фикоэритрина от органических растворителей, осуществляемая путем сушки в трегалозе
400 мкг/мл фикоэритрина сушат вымораживанием в сушке-морозильнике Labconco с 20% трегалозы или без нее. Высушенный порошок белка подвергают действию ряда органических растворителей в течение 72 часов. Фикоэритрин остается флуоресцентным в ацетоне, ацетонитриле, хлороформе и метаноле. В пиридине фикоэритрин остается флуоресцентным в течение 24-48 ч, но начинает увлажнятся и теряет флуоресценцию через 72 ч. В диметилсульфоксиде порошок соллюбилизируется, но фикоэритрин остается флуоресцентным.
с) Защита фикоэритрина от температуры 100oС, осуществляемая путем сушки в трегалозе
400 мкг/мл фикоэритрина сушат вымораживанием в сушке FTS с 20% трегалозы или без нее. Высушенный белок хранят при температуре 100oС в течение одного месяца без потерь функциональной активности.
Пример 4
Приготовление стеклообразной системы доставки твердой дозы с переносимым веществом, включенным в композитное СП, и/или ГПУ, и/или карбоксилатное стекло
а) Совместное приготовление стеклообразной дозированной твердой системы доставки из композита СП и органических стекол путем испарения
Микрочастицы трегалозы, содержащие МВ9, получают путем сушки распылением, как описано в примере 2b. Высушенный раствор содержит 0,39 М трегалозы, 0,14 М лактата кальция и 0,5% МВ9. Эти частицы покрывают путем добавления их к насыщенному раствору пальмитата цинка (ZnC16) в толуоле и охлаждения от 60oС до 30oС. Это осаждает слой ZnC16 на частицах, которые затем отфильтровывают в вакууме для удаления избытка ZnC16, промывают ацетоном и сушат на воздухе. Полученный в результате порошок остается не смоченным в воде в течение по крайней мере трех дней (частицы флотируют в воде без погружения или высвобождения МВ9 и после этого медленно выпускают краситель в воду). Таким образом, растворимые без этого в воде порошки могут быть сделаны водонепроницаемыми путем покрытия карбоксилатами металлов, такими как ZnC16, для получения режимов медленного высвобождения. Заметьте, что покрывающий материал наиболее вероятно находится в кристаллической форме и не является стеклом; поэтому твердая фаза, в которой суспендированы переносимые вещества, не должна обязательно быть стеклообразной фазой, чтобы быть водонепроницаемой.
b) Совместное приготовление стеклообразной дозированной твердой системы доставки СП стекол, содержащих активный агент, и органические стекла путем выпаривания
Порошкообразное трегалозное стекло, содержащее фикоэритрин, добавляют к смешанному карбоксилатному стеклу, а именно к смеси 1: 1 октаноата натрия и этилгексаноата цинка, растворенной в избытке хлороформа и выпаренной в потоке N2 при комнатной температуре для получения карбоксилатного стекла, содержащего порошкообразный фикоэритрин в твердом растворе или суспензии. Совместно приготовленное стекло остается не растворимым в воде в течение по крайней мере 48 ч. Порошкообразный фикоэритрин остается флуоресцентным как в исходном органическом растворе, так и в конечном стекле.
c) Совместное приготовление стеклообразной дозированной твердой системы доставки из СП стекол, содержащих активный агент, и органические стекла путем совместного плавления.
Ранее полученное органическое стекло, получаемое путем гашения расплава смеси 1: 1 октаноата натрия и этилгексаноата цинка, размягчают при температуре 95oС и к расплаву добавляют порошкообразное трегалозное стекло, содержащее фикоэритрин. Полученную в результате смесь непосредственно гасят на алюминиевом бруске, предварительно охлажденном до 15oС. Образуется прозрачное карбоксилатное стекло, содержащее включенный порошкообразный фикоэритрин, который сохраняет свою биологическую функциональность, что оценивается по его способности к флуоресценции. Варьирование природы и отношений углевода, и органических остатков в совместно приготавливаемых стеклах дает в результате стекла с диапазоном характеристик медленного высвобождения, что оценивается по их различающимся временам растворения в воде.
d) Совместное приготовление стеклообразной дозированной твердой системы доставки из СП стекол, содержащих активный агент, и ГПУ стекла путем выпаривания.
Системы доставки приготавливают с помощью сушки распылением, используя сушку-распылитель Buchi B-191. Заранее приготовленные 6 мкм частицы (0,264 г) из смеси трегалозы, высушенной распылением/красителя МВ9 (1%) суспендируют в растворе ТОАЦ (4 г) и азобензола (0,029 г) в дихлорметане (100 мл) и сушат в сушке-распылителе при температуре входа 40oС. Мутно-желтый гидрофобный порошок получают с ТОАЦ стеклом, включающим желтый краситель азобензол, инкапсулирующий трегалозное стекло, включающее синий краситель МВ9. Композитный носитель доставки демонстрирует замедленное высвобождение интенсивного водорастворимого синего красителя МВ9 при погружении в водный раствор.
е) Совместное приготовление стеклообразной дозированной твердой системы доставки из СП стекол, содержащих активный агент, и пластики путем выпаривания.
Порошкообразное трегалозное стекло, содержащее фикоэритрин, полученное согласно примеру 1, добавляют к раствору перспекса, растворенного в избытке хлороформа, и выпаривают в потоке N2 при комнатной температуре с получением блока твердого перспекса, содержащего порошкообразный фикоэритрин в твердом растворе. Порошкообразный фикоэритрин остается флуоресцентным как в исходном органическом растворе, так и в повторно сформированном твердом перспексе, который является непроницаемым для воды даже через 4 недели. Подобные результаты получают с полиэфиром, растворенным в дихлорметане, и с полиуретаном, растворенным в диметилсульфоксиде.
Пример 5
Приготовление пустых иголок, заполненных системами доставки
Конец заготовки трубок из трегалозного стекла с центральной полостью, заполненной порошкообразным трегалозным стеклом, содержащим фикоэритрин, приготовленным в соответствии с примером 1, расплавляют в зонной печи и волокно натягивают по спирали на металлический барабан, вращающийся с постоянной скоростью. Образовавшиеся полые волокна содержат стабилизированное мелкодисперсным порошком трегалозы соединение и могут быть разрезаны до желаемого размера. Полое волокно также может быть сделано из биологически разлагаемого термопластика, или органики, или ГПУ, и путем изменения диаметра производимых волокон могут быть сформированы заполненные иголки, которые могут варьироваться от микро- до макроиголок, то есть от толщин в микроны до долей миллиметра. Полые иголки могут быть заполнены любым носителем твердой дозы, описанным здесь.
Пример 6
Баллистическая доставка дозированных твердых систем доставки
Порошкообразные стекла впрыскивают в кожу с помощью толчка при сверхзвуковых скоростях, используя ударную волну давления, образовавшуюся при высвобождении сжатого газа. Порошок содержится в камере, прикрепленной к более широкому концу полости воронкообразной формы, более узкий конец которой прикреплен к баллончику сжатого газа, герметизированному с помощью майларовой пленки, и сверхзвуковая ударная волна генерируется путем разрыва майларовой мембраны. Альтернативно, соленоид, управляемый реле времени, может быть использован для управления высвобождением гелия, который позволил бы функционировать при более низких давлениях гелия. Это представляет собой принцип, используемый в пистолете для доставки частиц (PIG), разработанном Файнером для преобразования тканей растений. Vain et al. (1993) Plant Cell Tissue and Organ Culture 33: 237-246.
Пример 7
Получение твердых дозированных систем доставки органических стекол путем выпаривания
a) Приготовление карбоксилатных твердых дозированных систем доставки с помощью выпаривания растворителя
Гексаноат алюминия растворяют в хлороформе (0,5 г/10 мл) вместе с 1 вес. % мелкодисперсной суспензией МВ9 в качестве красителя-трассера. Тонкую аморфную пленку (толщиной 100-200 мкм) формируют путем выливания на пластинки силикатного стекла и выпаривания растворителя в потоке теплого воздуха. Высвобождение красителя в дистиллированную воду наблюдается в течение 5 часов и представлен на фигуре 6. Расстекловывания этих стекол не наблюдается, и пленки остаются прозрачными, хотя они обесцвечиваются, поскольку краситель диффундирует из них в среду.
Аморфные пленки также формируют из неодеканоата кальция, растворенного в хлороформе (0,5 г/10 мл), как описано выше. Высвобождение красителя из этих более толстых пленок (толщиной 1-2 мм), в дистиллированную воду опять наблюдается в течение 24 часов и представлено на фигуре 6. В противоположность алюминиевым пленкам высвобождение красителя из пленок неодеканоата кальция сопровождается растворением пленок, что наблюдается с помощью атомно-адсорбционной спектроскопии Са2+.
b) Приготовление композитных стеклообразных твердых дозированных систем доставки СП стекла, содержащих активный агент, включенный в карбоксилатное стекло, путем выпаривания.
Пленки глюкозного стекла, включающего 1 вес. % МВ9, приготавливают путем гашения расплава. Эти пленки покрывают тонкими (толщиной 100 микрон) аморфными пленками карбоксилата металла путем выпаривания из раствора карбоксилата в хлороформе (0,5 г/10 мл). Используемые металлкарбоксилаты представляют собой гексаноат и октаноат алюминия, неодеканоат кальция и изостеарат и неодеканоат магния. Растворение пленок наблюдают по высвобождению красителя в дистиллированную воду. Эти системы доставки продлевают высвобождение красителя в течение времени в диапазоне от минут до часов, за исключением пленок, образованных из изостеарата магния, которые продлевают высвобождение красителя в течение 10 дней.
Пример 8
Приготовление ГПУ твердых дозированных систем
Несколько ГПУ стекол приготавливают путем плавления и гашения. В последующих примерах многокомпонентные ГПУ покупают у Aldrich Chemical за исключением ТОПР, которое синтезируют способом, описанным Akoh et al. (1987). Компоненты образуют стекла с небольшим разложением или вообще без него. Фруктоза, сахароза и в определенной степени глюкоза плавятся с заметным разложением или полимеризацией. Эфир, такой как α-D-глюкоза пентаацетат, является стабильным при его температуре плавления и образует прозрачное бесцветное стекло, когда его гасят. Более высокая стабильность производных простых и сложных эфиров представляет собой очевидное преимущество при инкапсулировании реакционноактивных органических материалов, таких как пестициды и биоциды.
ГПУ с особенно низкими температурами плавления образуют после гашения мягкие воскообразные стекла. Спектр ЯМР стеклообразного α-D-глюкоза пентаацетата, как обнаружено, является идентичным спектру кристаллизованного α-D-глюкоза пентаацетата.
Стекло, образованное из β-D-глюкоза пентаацетата, является плохо растворимым в воде, и диск (20 мм диаметром и 2,5 мм толщиной), приготовленный из этого эфира и помещенный в проточную воду, теряет приблизительно 33% от своего начального веса за 10 дней. Другой стеклянный диск с подобными размерами приготавливают из α-D-глюкоза пентаацетата и помещают в 1 л воды, которую сменяют ежедневно. Через 7 дней стекло теряет 20% своего исходного веса. Скорость высвобождения инкапсулированного красителя Кислотный Синий из этого стекла, как показано на фигуре 7, является практически постоянной. Скорость высвобождения красителя является более высокой в первый день, поскольку высвобождение происходит в основном с поверхности стеклянного диска.
Превосходное высвобождение получают при инкапсулировании нескольких органических веществ в стеклах. Стеклянные диски из α-D-глюкоза пентаацетата, содержащие 2% вес/вес материалов, перечисленных в Таблице 4, формируют путем расплава и гашения, а затем размола. Фотохром II представляет собой 5-хлор-1,3-дигидро-1,3,3-триметилспиро[2Н-индол-2,3'-[3Н] -нафт[2,1-b] [1/4] -оксазин.
Инкапсулированные материалы экстрагируют с помощью соответствующего растворителя, такого как метанол или вода. Полученные результаты представлены в Таблице 4.
Скорости высвобождения Кислотного Синего 129, как обнаружено, зависят от скоростей растворения и форм стекол. Подобный пестициду Оксадиазон легко, без проблем растворяется в расплаве этого стекла при приблизительно 15% вес/вес.
Пример 9
Получение и свойства высвобождения стеклообразных ГПУ твердых дозированных систем доставки путем гашения из расплава.
а) Получение и свойства высвобождения простых и композитных стеклообразных ГПУ стекол из расплава
В последующих экспериментах систему доставки предварительно приготавливают либо в виде гомогенного материала, либо в виде смешанной композиции. Это проделывается с помощью тщательного измельчения многокомпонентных ГПУ вместе с последующим осторожным контролируемым плавлением в печи при температуре приблизительно 120-140oС и при нормальной атмосфере с образованием расплавов. Расплавы гасят до стекла путем выливания на поверхность бронзового блока. Затем это стекло мелко перемалывают.
Краситель МВ9 (1 или 5 вес. %) смешивают с перемолотым стеклом перед повторным плавлением при 140oС, расплав гасят с образованием мелких стеклянных шариков 2,5 мм диаметром, которые используют в экспериментах по контролируемому высвобождению.
Контролируемое высвобождение инкапсулированного красителя наблюдают путем суспендирования трех таких шариков в 25 или 50 мл деионизированной воды или в растворе PBS при температурах окружающей среды (27-30oС) или при 37oС, как показано. Среды находятся в спокойном состоянии за исключением периодического перемешивания и заменяются через равные интервалы свежими средами (обычно через 72-часовые интервалы). Образуются как гомогенные ГПУ стекла, так и композитные ГПУ стекла. Полученные ГПУ композитные стекла представлены в Таблице 5. Высвобождение красителя измеряют с помощью спектрофотометрии (λmax равна 516 нм), и результаты представлены на фигурах 8-14. Стекло ТОАЦ демонстрирует характеристики кинетики высвобождения нулевого порядка. Использование других ГПУ в качестве модификаторов в композитных ГПУ препаратах делает возможным конструирование стекол, созданных для получения желаемых характеристик высвобождения.
Фигура 8 представляет характеристики кинетики высвобождения нулевого порядка ТОАЦ систем доставки. На фигуре 8 результаты получены на дисках из ТОАЦ стекла (6 мм • 2,5 мм) с красителем МВ9, однородно диспергированным в них при 2% весовых. Высвобождение контролируют при 25oС при осторожном перемешивании и заменах среды через регулярные интервалы. Обратите внимание на линейное высвобождение красителя МВ9 в течение периода в 55 дней. Результаты, представленные на фигуре 8, показывают, что чистые стеклообразные ГПУ системы носителей доставки дают скорости высвобождения нулевого порядка переносимых веществ. Результаты, представленные на фигурах 9-14, представляют изменение скоростей высвобождения путем изменения отношений различных ГПУ в системах доставки, изменяя длину углеводной основной цепи и изменяя природу производного на углеводной основной цепи. В каждом примере является ясным, что ГПУ системы доставки позволяют иметь широкий диапазон скоростей высвобождения, который может быть подобран для данного переносимого вещества и доставки.
Фигура 9 представляет результаты, полученные, когда отношение двух различных ГПУ в системе доставки варьируется. Скорость высвобождения МВ9 из ТОАЦ/РУДА матриц измеряют, как описано для фигуры 8. Скорость высвобождения, как обнаружено, изменяется с различными препаратами, но является прямо связанной с концентрацией РУДА. Например, наивысшая скорость высвобождения наблюдается при 75% ТОАЦ (25% РУДА), а наименьшая скорость высвобождения - при 95% ТОАЦ. Таким образом, скорость высвобождения из этих систем доставки может быть легко получена эмпирически.
Фигура 10 сравнивает изменение Тg трех различных со-препаратов ГПУ с различными количествами ТОАЦ. Исследуют три различных со-препарата, ТОАЦ/СГАЦ, ТОАЦ/РУДА и ТОАЦ/α-ГПАЦ с увеличивающимся молярным процентом ТОАЦ. Эти результаты указывают, что Тg носителей возрастает непосредственно с мольным процентом ТОАЦ в тех со-препаратах, которые исходно имеют более низкие значения Тg/ ТОАЦ/α--ГПАЦ и ТОАЦ/СГАЦ.
Фигура 11 сравнивает процент высвобождения красителя МВ9 из двух различных со-препаратов ТОАЦ/РУДА и только РУДА. РУДА имеет двухфазную скорость высвобождения с начальным быстрым высвобождением приблизительно 60% красителя через 5 дней и медленным выходом еще нескольких процентов носителя за следующие 25 дней. Скорость высвобождения чистого РУДА существенно модифицируется с помощью присутствия ТОАЦ. Препарат 50% РУДА проявляет линейную скорость высвобождения, большую, чем скорость высвобождения для 10% препарата РУДА.
Фигура 12 сравнивает высвобождение МВ9 из со-препаратов ТОАЦ (75%) либо с СОАЦ, либо с ЦОАЦ, чтобы продемонстрировать влияние изменения углеводной основной цепи. Результаты показывают, что таким путем скорости высвобождения могут быть изменены, ТОАЦ/СОАЦ со-препарат демонстрирует повышенную скорость высвобождения по сравнению с со-препаратом ТОАЦ/СОАЦ.
Фигура 13 сравнивает скорость высвобождения красителя МВ9 из со-препаратов двух компонентов ГПУ с различной длиной углеводной основной цепи, ТОАЦ и α-ГПАЦ. Скорости высвобождения не являются непосредственно связанными с весовым процентом ТОАЦ, при 50% ТОАЦ, имеющим самые низкие скорости высвобождения, и при 25%, имеющим самые высокие. Опять же скорости легко определяются эмпирически.
Фигура 14 сравнивает скорость высвобождения красителя МВ9 из двух различных со-препаратов ГПУ компонентов с одинаковыми углеводными основными цепями и различными производными, ТОАЦ и ТОПР. Результаты показывают, что добавление 25% ТОПР к ТОАЦ системе доставки драматически уменьшает скорость высвобождения переносимого вещества
b) Включение переносимых веществ в ГПУ путем гашения расплава
Производится растворение синтетического кортикостероида XPDO (описано ниже) в расплаве ТОАЦ и гашение для образования стеклообразной твердой дозированной системы доставки. С точки зрения высвобождения МВ9 в водный раствор, эти эксперименты исследуют совместимость стероида со стеклом, последующее извлечение стероида и изучает влияние, которое XPDO оказывает на свойства образованной системы доставки с точки зрения высвобождения MB 9 в водный раствор. ТОАЦ (3,21 г) предварительно расплавляют при 150oС перед тем как погасить до стекла. Стекло мелко перемалывают с XPDO (0,15 г) перед повторным расплавлением. Прозрачный расплав опять гасят с получением композитного стекла ГПУ/активный агент. Термический анализ проводят на Rheometric Scientific Differential Scanning Calorimeter (DSC) при скорости нагрева в 10o/мин в атмосфере азота. Получают следующие образцы:
1. ТОАЦ/ XPDO(5 вес. %) - Тg= 50, 6oС
2. TOAЦ/XPDO(5 вес. %)+МВ9 (1 вес. %) - Тg= 50, 9oС
3. ТОАЦ чистый - Тg= 50,1oС
4. ТОАЦ/МВ9 (2 вес. %) - Тg= 50,3oС
Характеристики высвобождения стеклообразных ГПУ дозированных твердых систем доставки изучают путем регистрации высвобождения МВ9 из ТОАЦ/XPDO стекол, как показано в фиг. 15. Для анализа стабильности активного агента в стеклообразных ГПУ твердых дозированных системах доставки XPDO извлекают из образцов путем растворения стекла в ацетонитриле и анализируют с помощью ВЭЖХ. Существует полное извлечение переносимого вещества даже после хранения при 45oС в течение 4 недель.
Пример 10
Получение стеклообразных ГПУ дозированных твердых систем доставки путем выпаривания растворителя
а) Получение ГПУ стекол путем выпаривания растворителя
Как описано выше, было обнаружено, что ТОАЦ дает хороший носитель доставки путем гашения расплава. Такая система доставки имеет низкую температуру плавления и очень небольшую тенденцию к повторной кристаллизации. Затем был проведен ряд экспериментов на ТОАЦ стеклах путем выпаривания растворителя на пластинках натриевого стекла 3•1 дюйм.
Дихлорметан (ДХМ) и хлороформ являются стандартными растворителями для ТОАЦ, который также является растворимым в других растворителях, таких как ацетонитрил. ДХМ используют во всех последующих экспериментах.
Стекла получают путем выпаривания ДХМ на наборе конфорок при 65oС из 25% растворов ТОАЦ (50% растворы часто осаждают кристаллы на конце пипетки). Сушку продолжают в течение 2 часов до уверенности в полной сухости. Однородные стекла получают путем использования пипетки типа Eppendorf для доставки 100 мкл на стеклянную пластинку, перед этим помещенную на конфорке, а затем удаляя около 50 мкл путем использования обратного хода поршня пипетки. Стекла являются очень прозрачными и прилипают к подложке сразу после получения, но постепенно повторно кристаллизуются в течение 1 месяца при комнатной температуре (Комн. темп. ) и 50-60% относительной влажности (OB).
Трегалозные стекла получают подобным образом путем выпаривания воды из 50% раствора трегалозы, они являются прозрачными сразу после получения, но постепенно повторно кристаллизуются в течение периода в несколько недель.
b) Включение активного агента в ГПУ стекла путем выпаривания растворителя; порошки, пригодные для ингаляции.
XPDO является стероидным противовоспалительным соединением. Химически он представляет собой 6α, 9α-дифтор-11β, 21-дигидрокси-16α,17α-пропилметилендиокси-4-прегнен-3, 20-дион. XPDO кристаллизуется в виде спиралей, которые упаковываются вместе в иголки, оставляя длинные междумолекулярные пустые пространства, которые присоединяют молекулы воды подобно цеолитам. Это делает стероид достаточно гигроскопичным, чтобы затруднить его использование в качестве сухого порошка для ингаляции, которая является предпочтительным способом его введения. В аморфной (некристаллической) форме XPDO не является гигроскопичным, но он является химически нестабильным. Исследования по стабилизации этого соединения трегалозой были безуспешными, поскольку было невозможно получить негигроскопичный порошок.
Поэтому XPDO включают в ТОАЦ стекло путем растворения как кристаллического ТОАЦ, так и XPDO в ДХМ и выпаривания растворителя при 70oС на конфорке. XPDO используют в пропорциях в 10% и 20% от общего твердого продукта в конечном ТОАЦ стекле. Эти стекла являются превосходно прозрачными подобно воде. Если их хранить при ОВ в 75%, 81%, 90% и 95% в течение 4 недель, они не проявляют никаких изменений в структуре стекла, таких как повторная кристаллизация.
Однако, когда они помещены в жидкую воду, поверхность стекол медленно повторно кристаллизуется, так что можно увидеть микроскопические пирамидальные кристаллы ТОАЦ под инверсионным микроскопом в течение 15-30 мин после добавления воды. Кристаллизация постепенно продолжается, и в течение следующих минут появляются маленькие кластеры типичных кристаллов XPDO иглообразной формы. Поскольку ни XPDO иглообразной формы, ни пирамидальные кристаллы ТОАЦ не прилипают к лежащему под ними стеклу, они легко отмываются, открывая свежую поверхность стекла для дальнейшего медленного растворения. Полное вытеснение XPDO из кристаллов ТОАЦ подтверждает то, что эта молекула, первоначально включенная в стеклообразную ТОАЦ матрицу, теперь высвобождается в жидкую фазу.
с) Высвобождение активного агента в HDC стекла путем выпаривания раствора; порошки, высушенные распылением, пригодные для введения путем ингаляции
Производят исследования, используя синтетический кортикостероид XPDO, растворенный в ДХМ. Раствор высушивают распылением в сушке-распылителе Buchi B191, используя температуру входа в 40oС. Это дает в результате тонкий белый порошок, который содержит XPDO в твердом растворе. XPDO включают при 20% весовых. Порошок является полностью аморфным, что подтверждается с помощью термического анализа (Тg= 46oС).
Для анализа XPDO экстрагируют из порошка, высушенного распылением путем растворения порошка в ацетонитриле, а затем разбавления ацетонитрила натрийфосфатным буфером перед анализом с помощью ВЖЭХ. Образцы собирают для исследований стабильности XPDO в препаратах, полученных сушкой распылением при 45oС, и хранят над насыщенным сульфатом цинка (ОВ равна 80-85%).
Для высвобождения в натрийфосфатный буфер 0,0868 г порошка, высушенного распылением, встряхивают в 10 мл буфера в течение 1 минуты. Затем суспензию фильтруют сквозь 0,2 мкм фильтр. При анализе с помощью ВЭЖХ делают вывод, что XPDO является эффективно высвобождающимся в водный раствор. Биодоступность стероида из системы доставки исследуют путем погружения в водный раствор в течение короткого времени. Стабильность стероида в препарате, высушенном распылением, исследуют при высокой влажности и 45oС (оба фактора являются важными, чтобы применение в виде порошка для ингаляций было успешным). Результаты показывают устойчивость по отношению к высокой влажности, стабильность в стекле и легкую биодоступность в исследованиях in vitro. При ВЭЖХ анализе не было замечено никаких доказательств разложения порошка стекла, высушенного распылением, даже через 4 недели хранения при 45oС и 85% ОВ.
d) Включение переносимых веществ в ГПУ стеклах путем выпаривания растворителя; ЦСА с медленным высвобождением.
Циклоспорин (ЦСА, Sandimmune©) представляет собой гидрофобный циклический пептид, используемый в качестве иммуносупрессивного агента, в частности для пациента с трансплантированными органами. ЦСА вводят орально или внутривенно. Для введения его растворяют в спирте. В клинической практике уровни этого лекарства в крови подвергаются сильным флуктуациям из-за ненадежной адсорбции в проксимальном тонком кишечнике (тонкая кишка). Эта проблема может быть преодолена, если ЦСА выходит с постоянной скоростью в течение нескольких часов в форме, подходящей для адсорбции.
ЦСА вводят в ТОАЦ стекло путем растворения как кристаллического ТОАЦ, так и ЦСА, в ДХМ и выпаривания растворителя при 70oС на конфорке. ЦСА используют в пропорциях в 5%, 10% и 20% от общего твердого продукта в конечном ТОАЦ стекле. Эти стекла являются совершенно прозрачными подобно воде. При хранении при ОВ в 75%, 81%, 90% и 95% в течение 4 недель они не проявляют изменений в структуре стекла, таких как повторная кристаллизация. При погружении в воду эти стекла ведут себя подобно XPDO-содержащим стеклам, то есть они медленно повторно кристаллизуются в виде отдельных кристаллов ТОАЦ и ЦСА.
e) Получение стеклообразных твердых дозированных носителей доставки из композитных ГПУ стекол путем выпаривания растворителя.
В дополнение к ТОАЦ два других гидрофобно модифицированных сахарида, α-ГПАЦ и ТОПР исследуют в смесях для создания смешанных стекол с улучшенными свойствами.
Смешанные стекла пар этих ГПУ получают путем смешивания кристаллических компонентов в различных пропорциях, а затем получения стекол либо путем выпаривания растворителя ДХМ на конфорке, либо путем плавления при 150oС и гашения на бронзовой пластине.
Полученные в результате стекла исследуют на их полезность в качестве матриц с контролируемым высвобождением двумя способами. Во-первых, их оценивают на их способность противостоять расстекловыванию при экспозиции в высоких ОВ и Комн. темп. Во-вторых, их помещают в воду или солевой раствор с фосфатным буфером (ФБСР) для исследования их растворимости и скорости разрушения путем поверхностной повторной кристаллизации.
Однокомпонентные стекла как из α-, так и из β-ГПАЦ могут быть получены только путем гашения из расплава. Когда растворитель испаряется, растворы этих ГПУ всегда кристаллизуются. Однокомпонентные стекла из ТОАЦ и ТОПР легко получают либо путем выпаривания растворителя, либо путем гашения, но они являются очень восприимчивыми к расстекловыванию при высоких ОВ, демонстрируя полную повторную кристаллизацию тонких стеклянных пленок на пластинках для микроскопа и поверхностную повторную кристаллизацию на погашенных дисках при ОВ от 75% до 95% после экспозиции в течение ночи. Смешанные стекла ведут себя так, как описано в Таблице 6.
Полученные результаты показывают, что влияние различных ОВ являются очень однородным. В то время как чистое ТОАЦ и некоторые из композитных стекол кристаллизуются при всех ОВ от 75% до 95%, другие композитные стекла остаются аморфными при всех исследованных значениях OB.
Стекла с 10% α-ГПАЦ и 10% ТОПР в ТОАЦ и стекло с молярным отношением ТОАЦ: α-ГПАЦ 50: 50 также погружают в воду для исследования их скорости расстекловывания скорее в жидкой воде, чем во влажном воздухе. Первое стекло повторно кристаллизуется в течение 20-30 мин, в то время как второе стекло образует небольшое количество мелких кристаллов через 4 часа, в то время как стекло 50: 50 не меняется в течение 4 дней, демонстрируя неожиданно низкую растворимость.
В качестве носителя для доставки лекарств в порошкообразной форме в глубину легких, стекла с 10% α-ГПАЦ в ТОАЦ демонстрируют очень желательные свойства устойчивости по отношению к 95% ОВ, такой, которая может встретиться в ингаляторе и при прохождениях воздуха, в то же самое время с быстрой повторной кристаллизацией в жидкой воде, такой как в слое жидкости, покрывающем альвеолы.
Стекла из ТОАЦ с добавлением 10% или более α--глюкозапентаацетата или трегалозаоктапропаноата или без них обеспечивают диапазон значений устойчивости к ОВ окружающей среды и скоростей растворения, делающих возможным соответствующий уровень конструирования контролируемого высвобождения лекарств, диспергированных в таких стеклах.
f) Включение активного агента в композитные ГПУ и/или СП стекла с медленным высвобождением путем выпаривания растворителя.
Для максимальной выгоды характеристики медленного высвобождения ГПУ должны быть пригодными для использования как для гидрофобных, так и для гидрофильных молекул. Первые легко приготавливать в твердом растворе в одном ГПУ либо путем выпаривания растворителя, либо путем прямого растворения в расплаве с последующим гашением. Гидрофильные молекулы не являются непосредственно растворимыми в ГПУ.
В настоящее время авторы обнаружили замечательно полезный способ для включения гидрофильных веществ с очень однородным и полезным распределением в матрице из ГПУ. Способ хорошо иллюстрируется с помощью использования трегалозы в качестве гидрофильного вещества и ТОАЦ в качестве гидрофобной матрицы. Хорошими растворителями как для модифицированной, так и для нативной трегалозы являются ДМФ и ДМСО. Когда раствор из 10% трегалозы и 90% ТОАЦ в ДМФ выпаривают досуха, в результате получают стекло, похожее на изморось, или опалесцентное. Под микроскопом видно, что распределение сферических стеклообразных микрошариков одинакового размера в сплошной матрице является очень однородным (фигуры 16 и 17). Путем грубого измерения с помощью линейки в окуляре микроскопа, размер микрошариков составляет приблизительно 4 микрометра в диаметре.
Идентичность двух фаз проверяют путем включения малого количества сильно гидрофобного липидного красителя Масляный Красный О вместе с малым количеством гидрофильного красителя Метилен Зеленый в растворе ДМФ, перед получением стекла. Как ожидается, гидрофобный Масляный Красный О распределяется исключительно в сплошной фазе, доказывая, что она представляет собой ТОАЦ, в то время как гидрофильный Метилен Зеленый распределяется исключительно среди дискретных однородных частиц, доказывая, что они представляют собой трегалозу (фигура 18). Композитное стекло, полученное таким образом, состоит из очень однородного и стабильного стекла в стеклянной "твердой эмульсии" или "твердой суспензии", скорее чем в твердых растворах, таких как те, которые наблюдаются для гидрофобных переносимых веществ XPDO, ЦСА или красителя Масляный Красный О.
Когда те же смеси трегалозы и ТОАЦ выпаривают из раствора в ДМСО, внешний вид композитного стекла является другим. В этом случае стекло является более прозрачным и сплошная трегалозная фаза представлена под микроскопом в двух формах. Одна форма является очень мелкой дисперсией исключительно малых трегалозных частиц, однородно распределенных в сплошной матрице. Другая форма состоит из больших сферических шариков трегалозы, концентрированных в кластере в центре композитного стекла.
Без желания быть связанными с какой-либо теорией выглядит правдоподобным, что различные обнаруженные структуры отражают различия в растворимости двух углеводов в используемых растворителях, так что их осаждение из раствора осуществляется на различных стадиях выпаривания растворителя. Убедительное доказательство в подтверждение этого объяснения обнаружено в экспериментах по получению композитных стекол при противоположной ориентации, то есть с гидрофобным переносимым веществом, мелко диспергированным в гидрофильной сплошной матрице.
g) Токсичность ГПУ стекол
Насыщенный раствор ТОАЦ в деионизированной дистиллированной воде (0,42 г в 20 мл) исследуют на токсичность in vitro, используя клетки, полученные из почки Африканской зеленой мартышки линии Vero, либо при 10-кратном последовательном разбавлении, либо путем добавления порошка ТОАЦ в среду культуры ткани. Через неделю не было обнаружено токсичного воздействия на культуру и деление клеток было нормальным.
Хотя описанное изобретение для иллюстрации и примера для ясности понимания было описано достаточно детально, для специалиста в данной области является понятным, что могут быть осуществлены определенные изменения и модификации. По этой причине описание и примеры не должны рассматриваться в качестве ограничивающих рамки изобретения, которые изложены с помощью прилагаемой формулы изобретения.
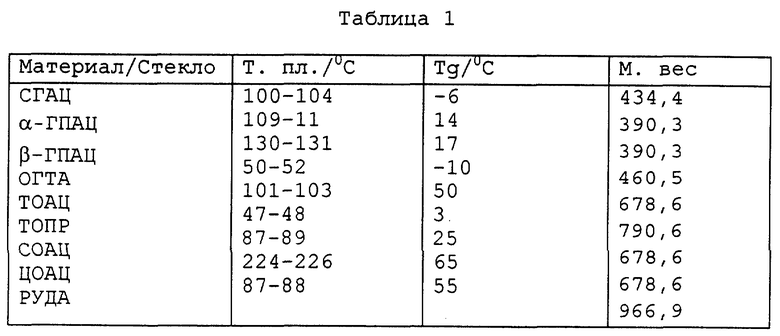
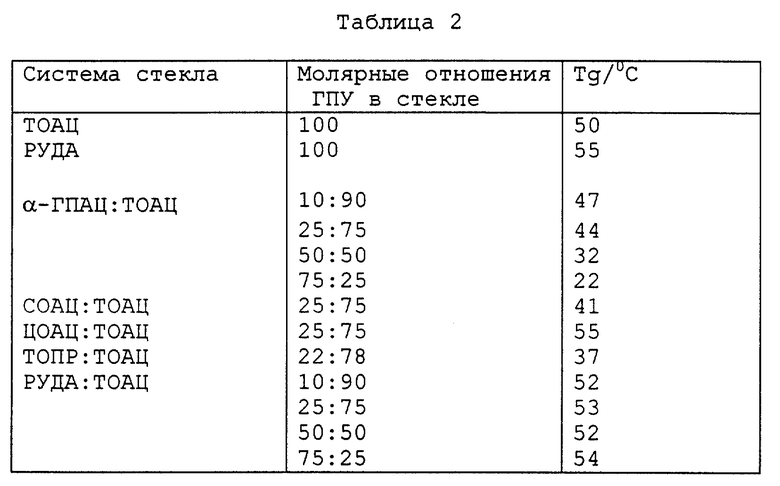
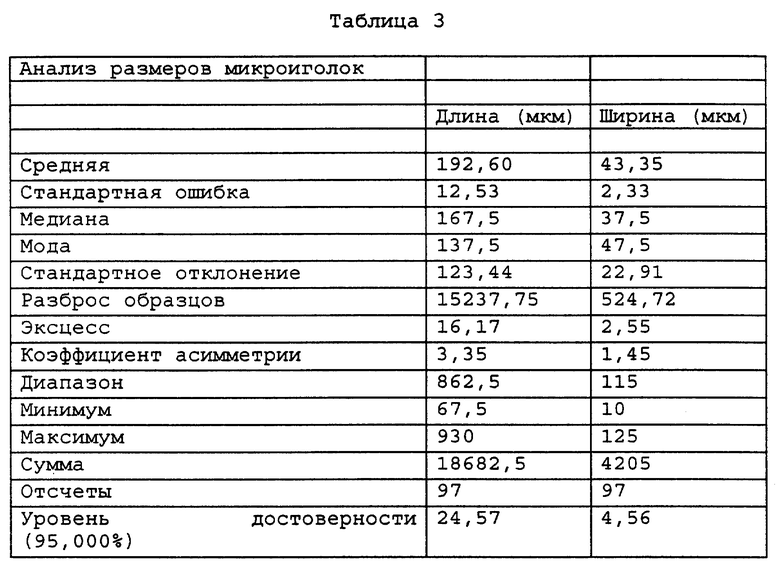
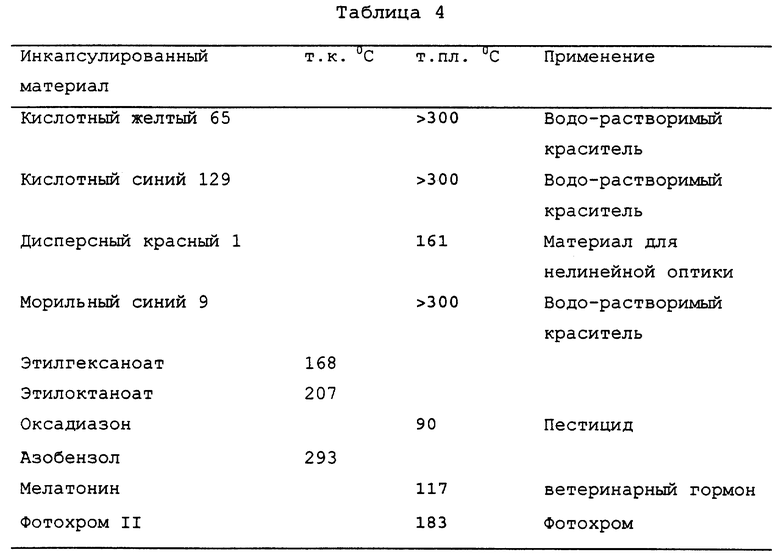

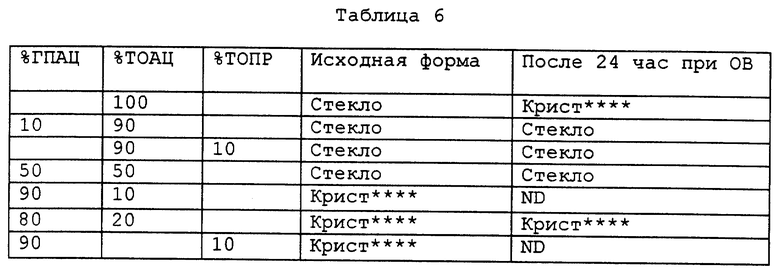
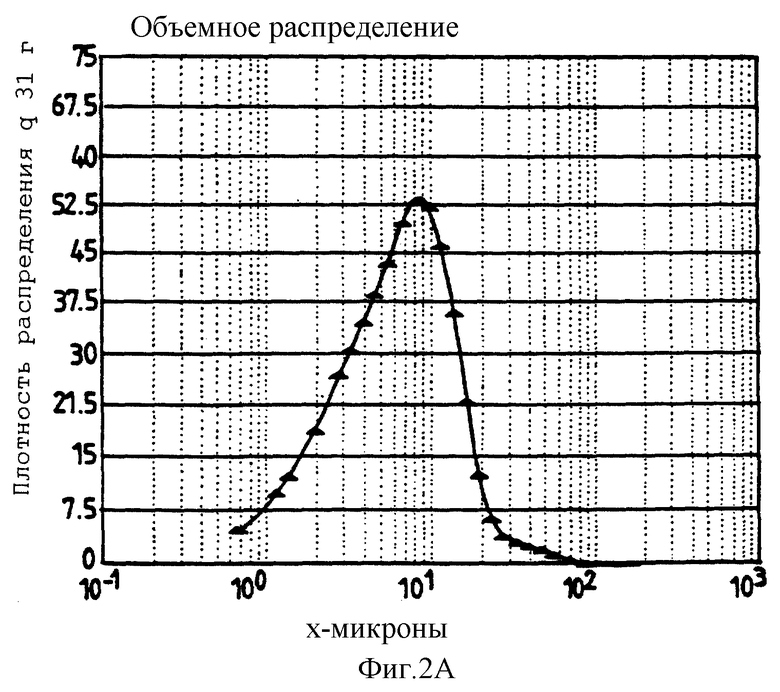
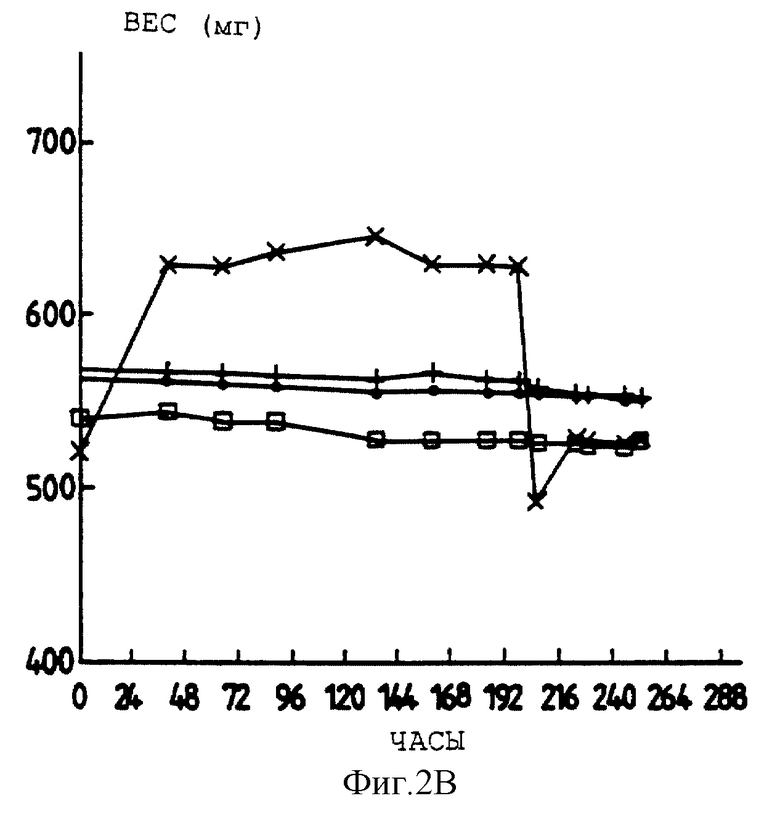
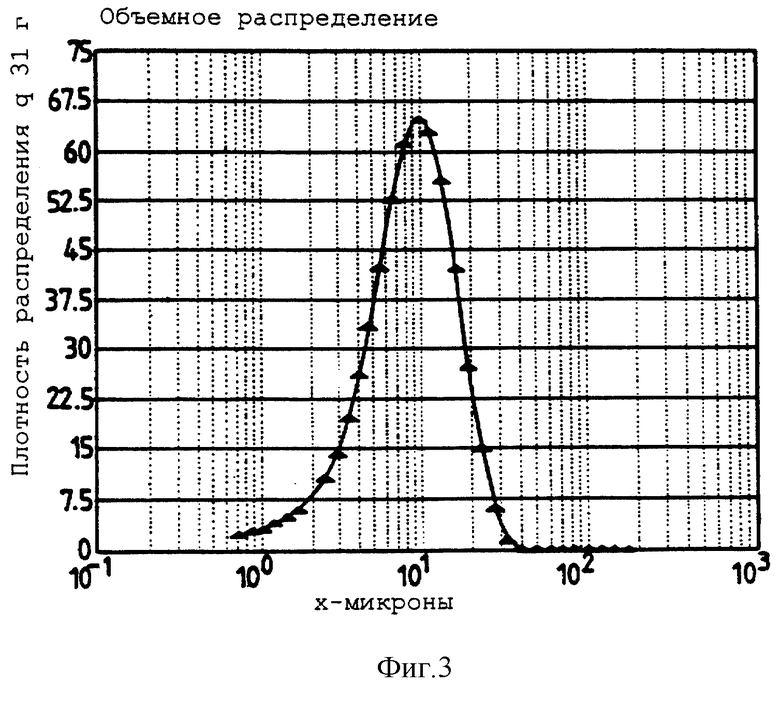
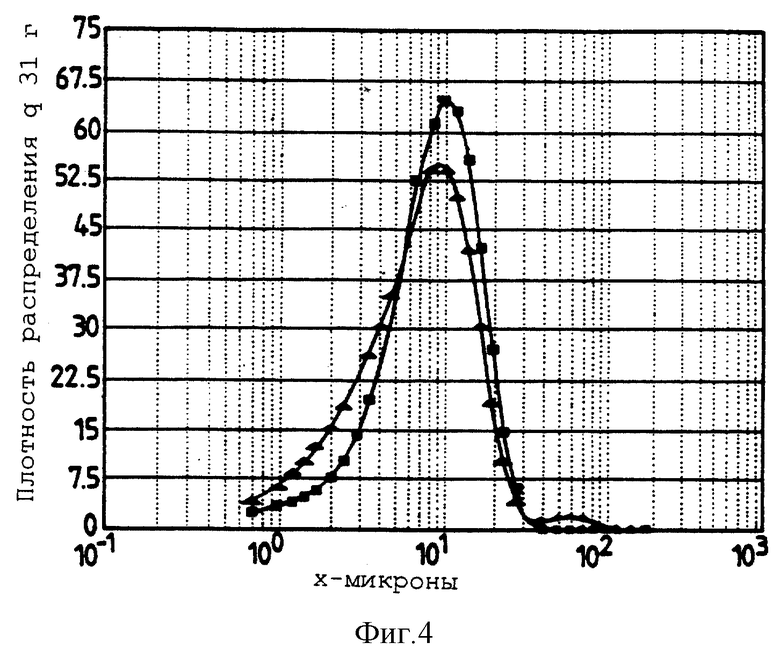
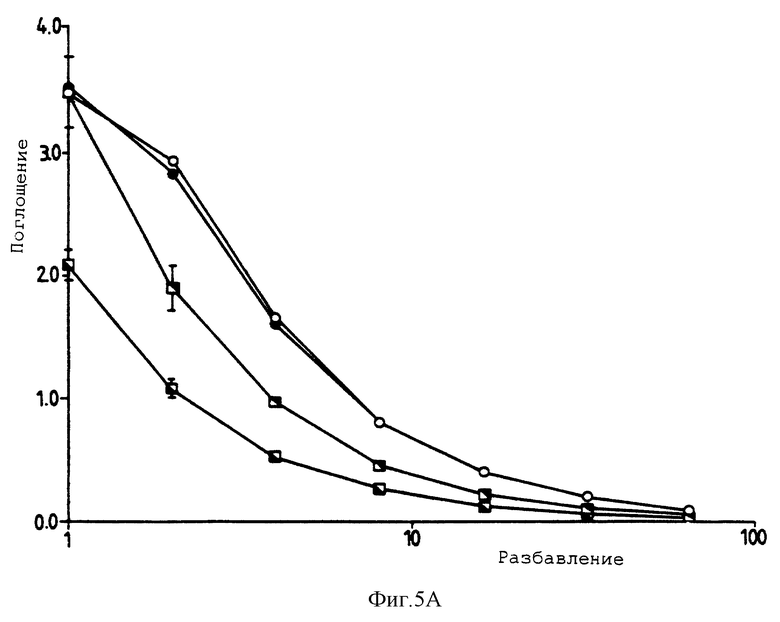
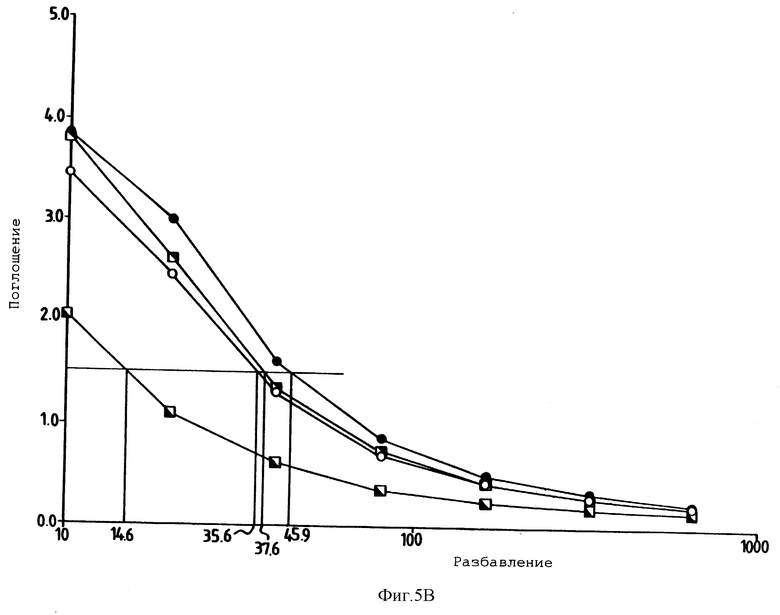
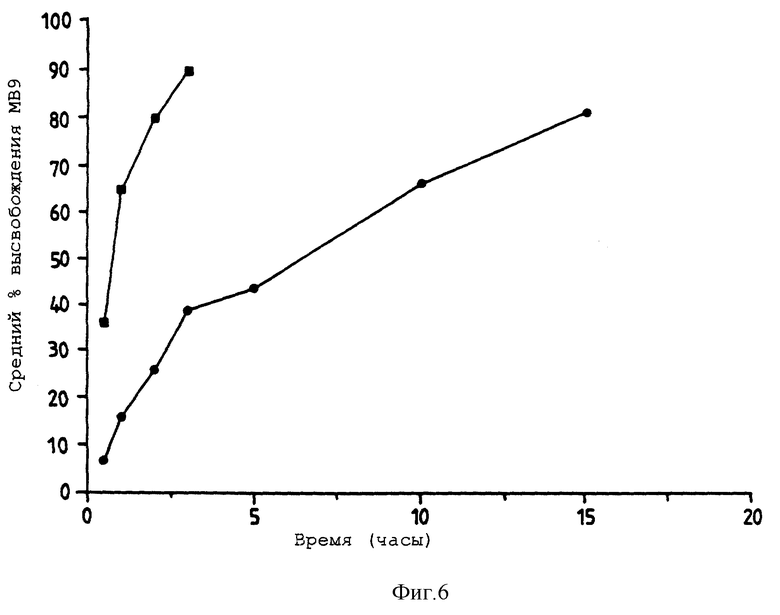
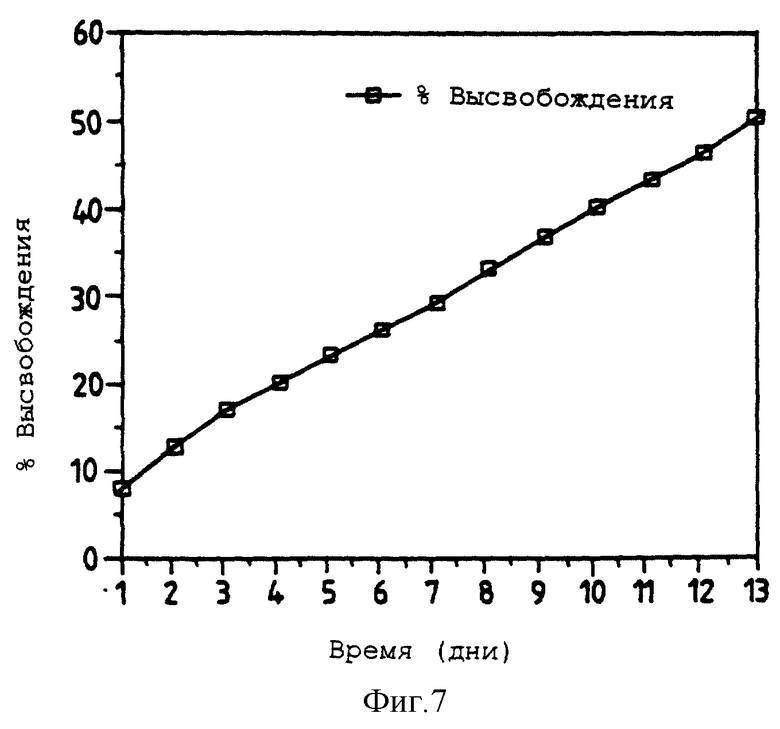
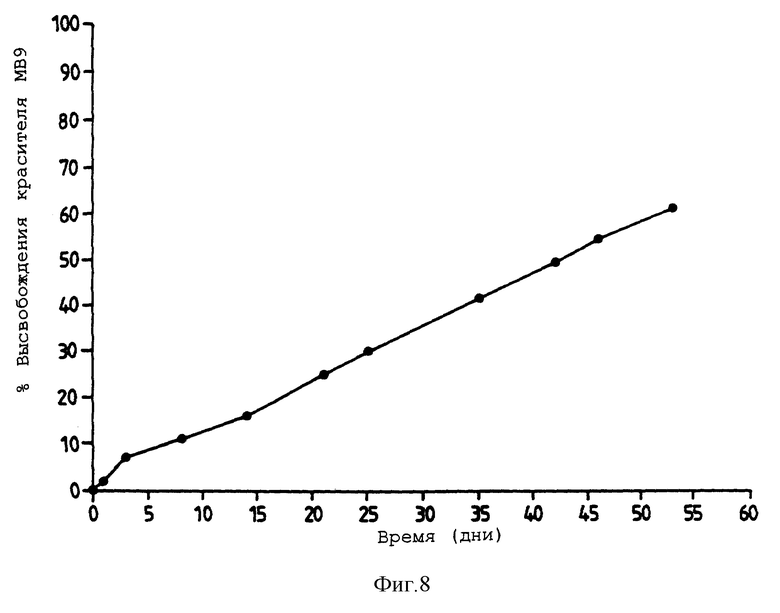
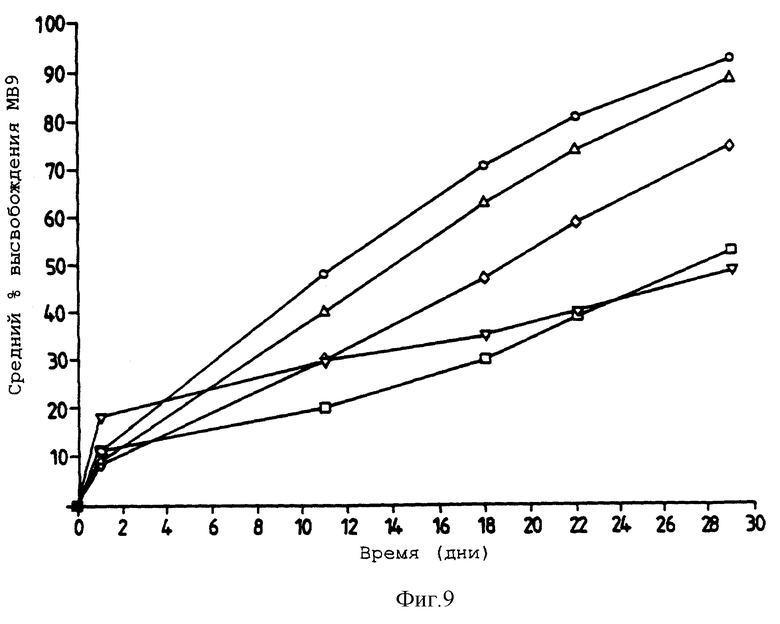
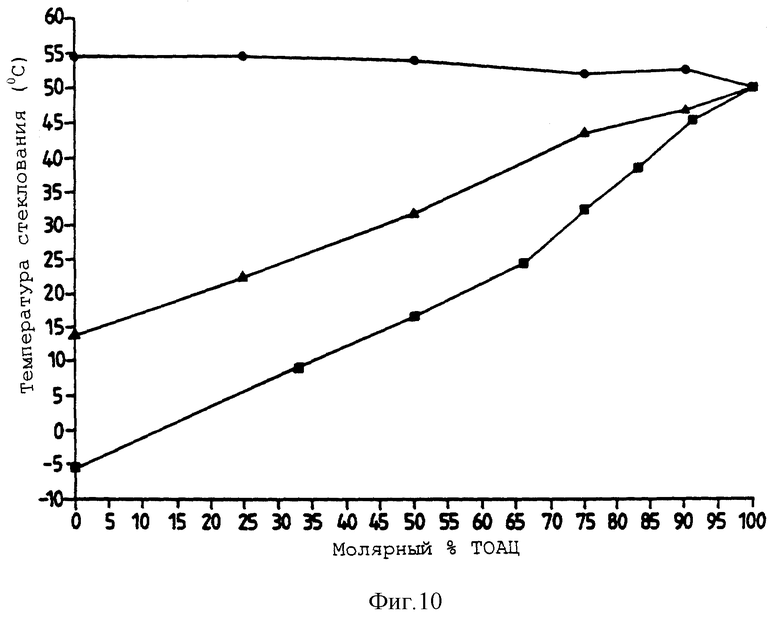
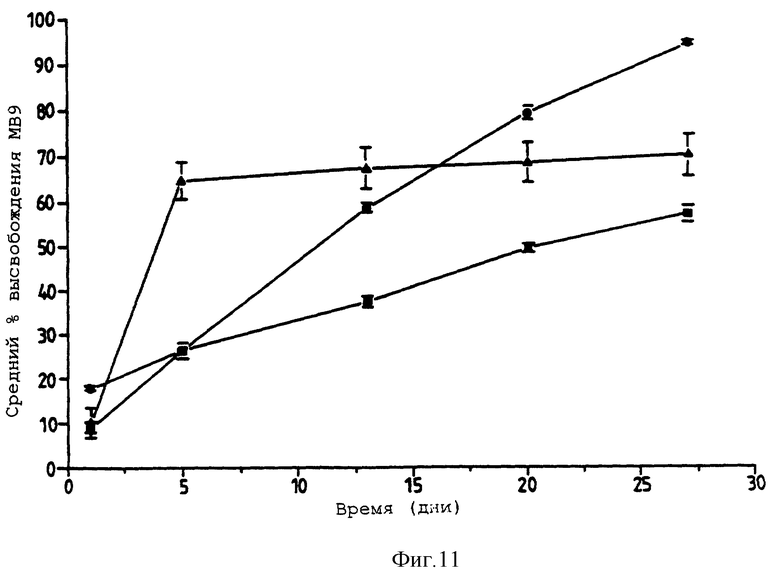
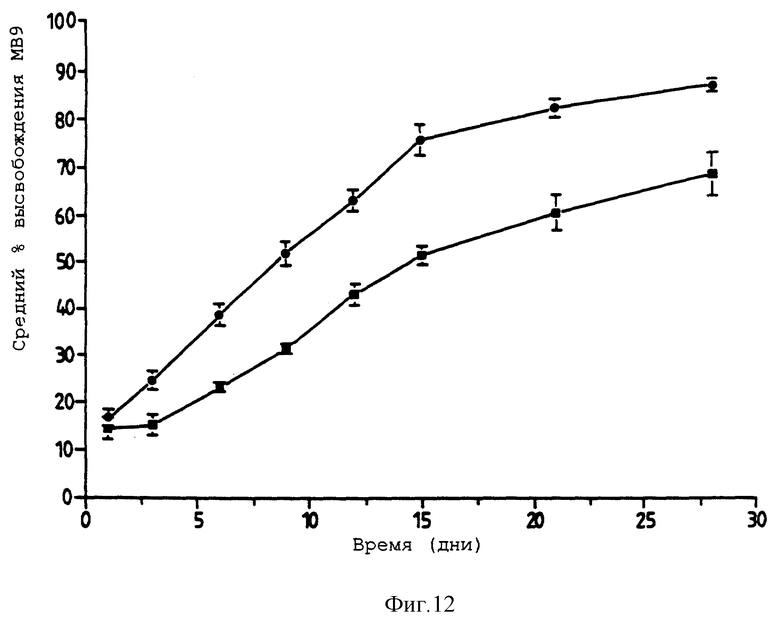
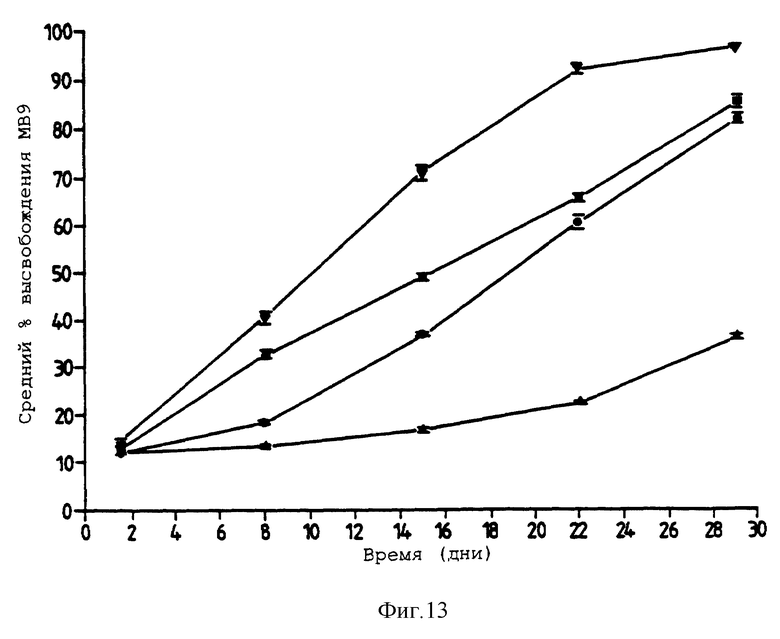
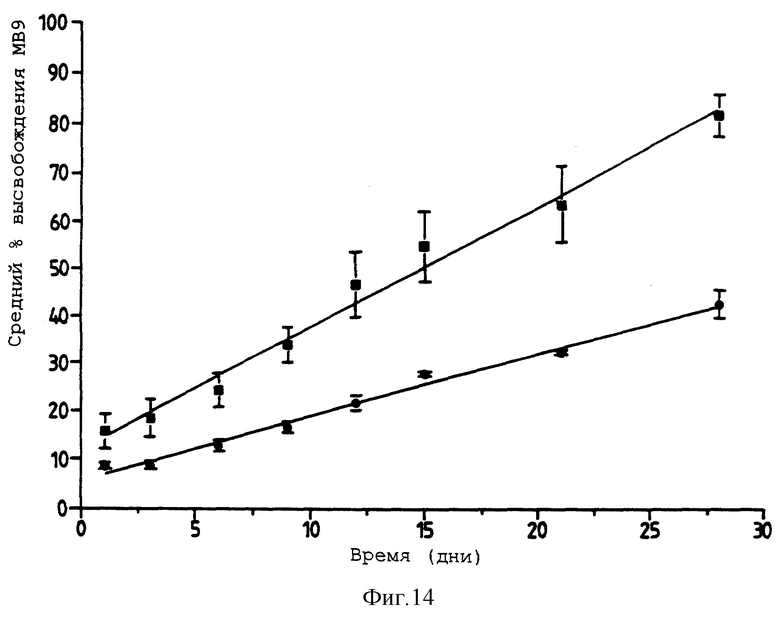
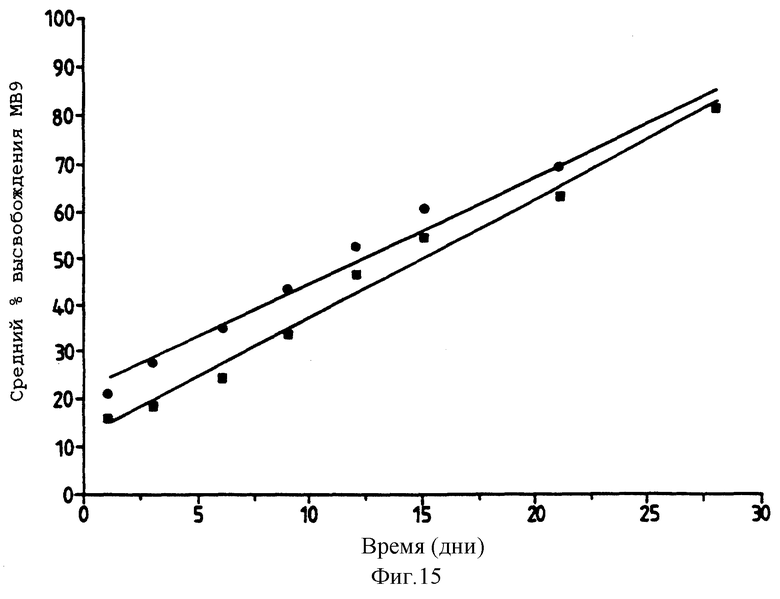



Система доставки содержит стеклообразный носитель и переносимое вещество. Носитель выбирают из стабилизирующего полиола и гидрофобного углеводного производного (ГПУ). Стабилизирующий полиол является дисахаридом, трисахаридом, олигосахаридом и их соответствующими сахарными спиртами. ГПУ имеет углеводную основную цепь и по меньшей мере одну гидроксильную группу, замещенную гидрофобным фрагментом. Переносимое вещество является фармацевтическим агентом или биологическим модификатором. Форма твердой дозированной системы доставки выбирается из лепешек, таблеток, дисков, пленок, суппозиториев, иголок, микроиголок, частиц, микрочастиц, сфер, микросфер, порошков и имплантируемых средств. Предпочтительно носитель является трегалозой, а переносимое вещество - циклоспорином А. Стеклообразная система доставки обеспечивает стабильность переносимого вещества и его сохранность без потерь активности. Обеспечивается широкое разнообразие типов и скоростей доставки переносимого вещества. 2 с. з. и 37 з. п. ф-лы, 18 ил. , 6 табл.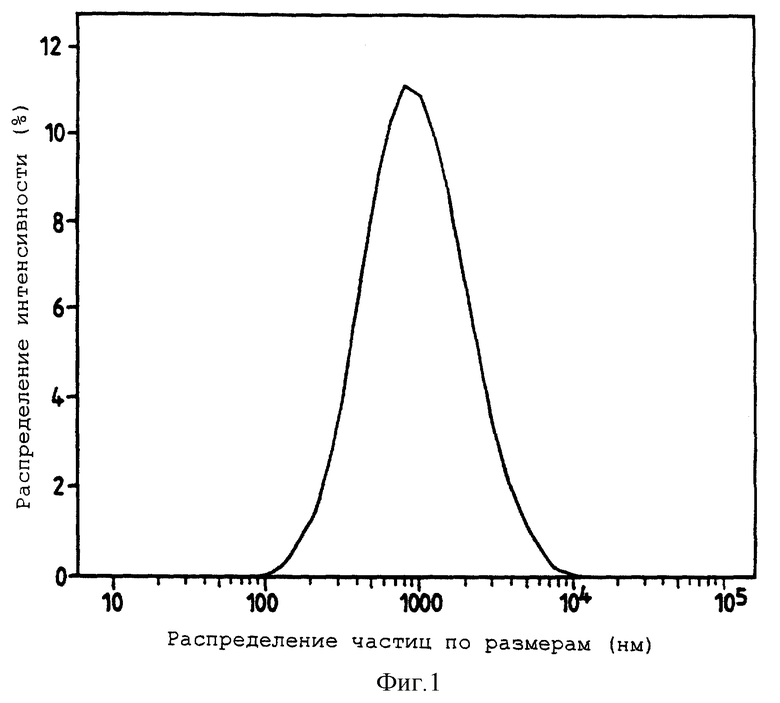
Приоритет по пунктам:
04.08.1994 - по пп. 1, 2, 8-22, 24-27, 30-39 в части признака "стабилизирующий полиол" и пп. 3-5, 28, 29;
04.08.1995 - по пп. 1, 2, 8-22, 24-27, 30-39 в части признака "ГПУ" и пп. 6, 7, 23.
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Шланговое соединение | 0 |
|
SU88A1 |
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
2002-01-10—Публикация
1995-08-04—Подача