Изобретение относится к медицине, а именно к нейроонкологии, и может быть использовано для прогнозирования выживаемости больных с низкодифференцированными глиальными опухолями головного мозга.
Глиомы - группа злокачественных опухолей головного мозга нейроэктодермального происхождения. Продолжительность жизни больных с глиальными опухолями головного мозга после хирургического лечения следующая: у больных с анапластическими астроцитомами - около 24 месяцев, а у пациентов с глиобластомами редко превышает 12 месяцев (Аннин Е.А., Щеглов В.И., Осинский С.П. «О целесообразности оперативного лечения злокачественных глиом и перспективности внутриартериальной химиотерапии». // Украинский журнал малоинвазивной и эндоскопической хирургии. - 1998. - №2; 4. - С.50).
Известен способ прогнозирования при опухолях надпочечников (Высоцкая О.В., Марченко И.А. Исследование экспрессии металлопротеиназ при новообразованиях надпочечников. Тезисы V Конференции молодых ученых России с международным участием «Фундаментальные науки и прогресс клинической медицины» 19-22 мая 2008 г., стр.97-98.) Автор исследовал экспрессию трех металлопротеиназ: ММР-1, ММР-7 и ММР-9 в доброкачественных опухолях: аденоме коркового вещества надпочечников, феохромоцитоме и в злокачественных новообразованиях мозгового вещества надпочечников - феохромобластоме. Обнаружена тенденция к увеличению уровня экспрессии исследуемых металлопротеиназ в случае злокачественного перерождения тканей надпочечников. Замечено, что экспрессия ММР была достаточно низкая в большинстве нормальных клеток, однако заметно повышается в злокачественных опухолях и коррелировала с плохим клиническим прогнозом.
Однако этот способ относится к прогнозированию эффективности лечения при опухолях надпочечников и не может быть использован при прогнозировании выживаемости больных со злокачественными глиомами головного мозга.
Известен способ прогнозирования эффективности лечения больных с глиальными опухолями (Абсалямова О.В., Коршунов А.Г., Лошаков В.А, Кобяков Г.Л., Голанов А.В., Ураков С.В., Аманов Р.Д. «Влияние молекулярно-генетических факторов на прогноз больных с олигодендроглиальными и смешанными опухолями». Тезисы V Конференции молодых ученых России с международным участием «Фундаментальные науки и прогресс клинической медицины» 19-22 мая 2008 г., стр.6-7), выбранный в качестве прототипа. Авторы проводили оценку влияния делеций 1p19q и 9р на прогноз и эффективность лечения в этой группе больных методом флюоресцентной in-situ гибридизации. У больных с делецией 1p19q среднее время до прогрессирования было больше в группе ХТ+ЛТ - 45 мес., в случае применения только ЛТ - 30 мес. Таким образом, присутствие в опухоли коделеции 1p19q ассоциируется с улучшением сроков выживаемости, при наличии делеций 9р выживаемость ухудшается. Делеция 9р выявлялась в случаях отсутствия коделеции 1p19q.
Однако этот метод достаточно объемен, дорогостоящ и длителен в исполнении, что не позволяет использовать его в качестве поточного способа определения прогноза выживаемости больных с глиомами.
Целью настоящего изобретения является упрощение и ускорение способа прогнозирования выживаемости больных с низкодифференцированными глиальными опухолями головного мозга.
Поставленная цель достигается тем, что в крови больных после операции до комплексного лечения определяют содержание гормона эпифиза - мелатонина, а в моче - 6-СОМ 6-сульфатоксимелатонин. при уровне 6-СОМ 6-сульфатоксимелатонин 292,7 нмоль/мл - прогнозируют выживаемость больных до 2,3±0,5 месяца, при уровне 6-СОМ 22,4 нмоль/мл - выживаемость более 12 месяцев, после химиотерапии при уровне 6-СОМ 268,2 нмоль/мл, прогнозируют выживаемость до 2,1±0,6 месяца, а при уровне 6-СОМ 32,8 нмоль/мл - более 12 месяцев, через месяц после лечения при уровне 6-СОМ 479,3 нмоль/мл прогнозируют выживаемость 1,2±0,5 месяца, а при уровне 6-СОМ 6-сульфатоксимелатонина 37,4 нмоль/мл - выживаемость более 12 месяцев.
Изобретение «Способ прогнозирования выживаемости больных злокачественными глиомами» является новым, так как оно неизвестно из уровня достижений медицины в области прогнозирования выживаемости больных с низкодифференцированными глиальными опухолями головного мозга на основе биохимических исследований.
Анализ известных способов прогнозирования дает основания говорить о новизне предлагаемого способа, который представлен исследованием объективного показателя в моче больных.
В отличие от прототипа предлагаемый «Способ прогнозирования выживаемости злокачественных глиом» осуществляется в течение 1 рабочего дня и дает возможность проводить коррекцию лечебных воздействий в соответствии с исследуемой объективной реакцией организма на это воздействие.
Разработанный способ обладает изобретательским уровнем, так как явным образом не следует для специалиста из известного уровня развития медицины и оценки эффективности противоопухолевой терапии. В известных источниках информации России, стран СНГ и за рубежом подобный способ не обнаружен.
Изобретение является промышленно применимым, так как оно может быть многократно воспроизведено в лечебных учреждениях онкологического профиля, располагающих биохимическими лабораториями.
Биохимическое исследование определении содержания 6-СОМ (6-сульфатоксимелатонина) в моче выполняется следующим образом:
Моча больных собирается утром натощак. Определение уровня мелатонина проводят по методу Левина И.М., Кветного И.М., Громовой Н.В. (Повышение чувствительности и специфичности флюорометрического определения мелатонина в моче // Лаб. дело, 1988. - №5. - С.54-57). К 40 мл мочи добавляют 2 мл 2% р-ра 1-цистеина в бидистиллированной воде, а затем с помощью 40% едкого натра доводят pH до 12,0. раствор фильтруют, к 10 мл фильтрата добавляют 50 мл хлороформа и интенсивно перемешивают на магнитной мешалке 20 мин. Водную фазу отбрасывают, а хлороформный экстракт дважды промывают 50 мл бидистиллированной воды, а затем 5 мл 0,1 М соляной кислоты. Хлороформ выпаривают при температуре 60°С под вакуумом до сухого остатка, к которому приливают 0,6 мл 5 н. соляной кислоты. По 0,2 мл кислотной фазы переносят в две пробирки, в одной из которых находится 0,02 мл перекиси водорода. В обе пробирки приливают по 0,6 мл 0,015% раствора ортофталиевого альдегида в 0,1 н. соляной кислоте и выдерживают на водяной бане при температуре 100°С в течение 10 мин. В каждую пробирку добавляют по 1 мл воды и флюориметрируют.
Для доказательства приводим выписки из историй болезни, подтверждающих клинический эффект от прогнозирования предлагаемым «Способом прогнозирования выживаемости больных злокачественными глиомами.
Пример клинического применения №1.
Наблюдение №1. Больной П., 1985 г.р., Ист. болезни №18046/р.
Диагноз: Анапластическая астроцитома левой лобной доли головного мозга.
Из анамнеза: 28.09.2004 г. выполнена костно-пластическая краниотомия с радикальным удалением опухоли.
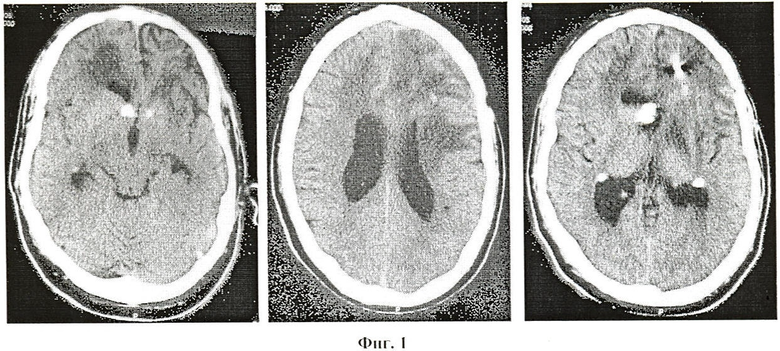
Гистоанализ №764640: анапластическая астроцитома. В неврологическом статусе: состояние средней тяжести, апатико-абулический синдром, правосторонний центральный гемипарез (4 балла) с правосторонней гемигипестезией, генерализованные эпилептические приступы, моторная афазия. РКТ головного мозга, выполненная после операции, выявило послеоперационный отек, занимающий 3 доли - левую лобную, левую теменную, правую лобную (фиг.1) РКТ головного мозга больного П. после операции до начала комплексного лечения. Уровень 6-СОМ (6-сульфатоксимелатонина) 292,7 нмоль/мл.
Больному проведен курс комплексного лечения, суммарно получено 60 Гр на ложе удаленной опухоли и введено 500 мг кармустина, 200 мг этопозида на фоне противоотечной терапии.
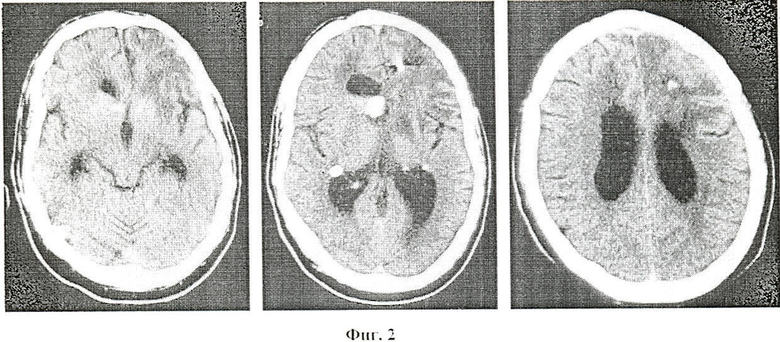
В процессе лечения отмечена постепенная положительная динамика в виде восстановления речи, чувствительности и силы в правых конечностях, уменьшение частоты и выраженности эпиприступов. При контрольной РКТ головного мозга, выполненной после окончания курса лечения, отмечено значительное уменьшение послеоперационного отека, занимающего только левую лобную долю и отсутствие дислокации срединных структур (фиг.2) РКТ головного мозга больного П. после курса комплексного лечения (полная ремиссия). Уровень 6-СОМ (6-сульфатоксимелатонина) 32,8 нмоль/мл. В настоящее время безрецидивный срок у этого пациента составляет 5 лет, качество жизни удовлетворительное. После комплексного лечения с положительным клиническим эффектом уровень 6-СОМ (6-сульфатоксимелатонина) 32,8±3,1 нмоль/мл, что подтверждает его значение как прогностического критерия для определения продолжительности жизни больных.
Наблюдение №2. Больной М., 1965 г.р., ист. болезни №2875/о.
Диагноз: Глиобластома левой лобной доли головного мозга.
Из анамнеза: 03.05.2005 г. в РНИОИ выполнена костно-пластическая краниотомия с радикальным удалением опухоли.
Гистоанализ №788232-238: глиобластома.
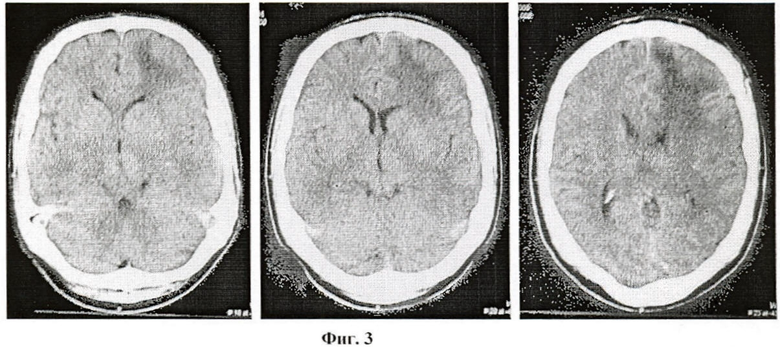
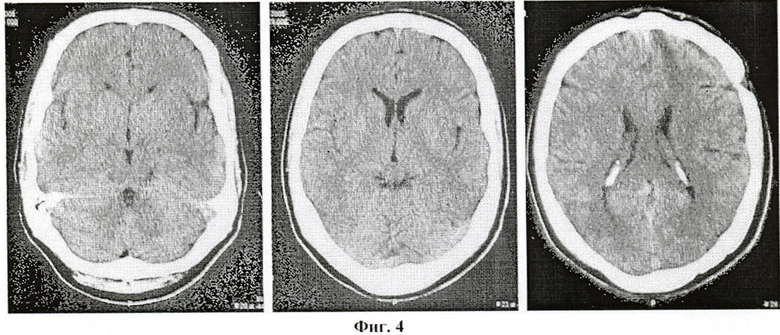
В неврологическом статусе: состояние средней тяжести, апатико-абулический синдром, генерализованные эпилептические приступы, моторная афазия. РКТ головного мозга, выполненная после операции, выявила послеоперационный отек, занимающий всю левую лобную долю со смещением срединных структур вправо на 4 мм (фиг.3) РКТ головного мозга больного М. до начала комплексного лечения. Уровень 6-СОМ (6-сульфатоксимелатонина) 268,2 нмоль/мл. Больному проведен курс комплексного лечения, суммарно получено 60 Гр на ложе удаленной опухоли и введено 500 мг кармустина, 200 мг этопозида на фоне противоотечной терапии. В процессе лечения отмечены постепенная положительная динамика в виде восстановления речи, уменьшение частоты и выраженности эпиприступов. При контрольной РКТ головного мозга, выполненной после окончания курса лечения, отмечены полный регресс послеоперационного отека и отсутствие дислокации срединных структур (фиг.4) РКТ головного мозга больного М. после курса комплексного лечения. Уровень 6-СОМ (6-сульфатоксимелатонина) 37,4 нмоль/мл.
В настоящее время безрецидивный срок у этого пациента составляет 4,5 года, качество жизни удовлетворительное.
Через месяц после лечения положительный клинический эффект подтверждается определением уровня 6СОМ (6-сульфатоксимелатонина) 37,4±3,3 нмоль/мл.
Наблюдение №3. Больной Л., 1951 г.р., Ист. болезни №21353/х.
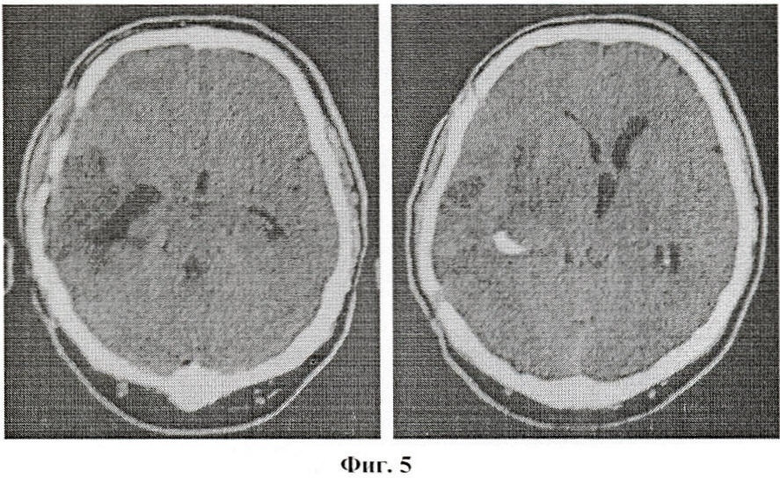
Диагноз: Глиобластома правой височно-теменной области головного мозга. Из анамнеза: 19.04.07 г. в РНИОИ выполнена костнопластическая краниотомия с радикальным удалением опухоли, гистоанализ №936310: глиобластома. В послеоперационном периоде предъявлял жалобы на головные боли, слабость, онемение в левых конечностях. В неврологическом статусе: состояние средней тяжести, общемозговой синдром, левосторонний центральный гемипарез (3 балла), левосторонняя гемигипестезия. Индекс по Карновскому составил 40%, общесоматический статус - 3 балла. На пятнадцатые сутки послеоперационного периода контрольная РКТ головного мозга, в зоне оперативного вмешательства; гиподенсивный очаг в правой височной доле размерами 92×72×90 мм, сдавление правого бокового желудочка со смещением срединных структур головного мозга на 5 мм влево (фиг.5) РКТ головного мозга больного Л. после операции.
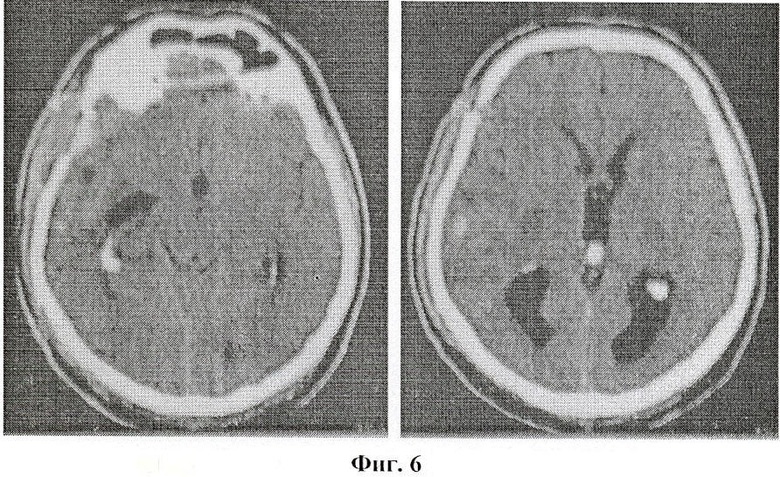
Больному проведен курс комплексного лечения по описанной методике, суммарно получено 60 Гр на ложе удаленной опухоли и введено 500 мг кармустина, 200 мг этопозида. После курса комплексного лечения отмечено как отсутствие положительной динамики, отсутствии регресса очаговой неврологической симптоматики. Индекс по шкале Карновского составил 80%, общесоматический статус по ECOG-ВОЗ - 2 балла. РКТ головного мозга, выполненной через месяц после лечения отрицательный клинический эффект после окончания лечения, выражающийся в отсутствие уменьшения послеоперационного отека и дислокации срединных структур (фиг.6) РКТ головного мозга больного Л. после курса комплексного лечения. Уровень 6-СОМ (6-сульфатоксимелатонина) составил 479,3±43,1 нмоль/мл.
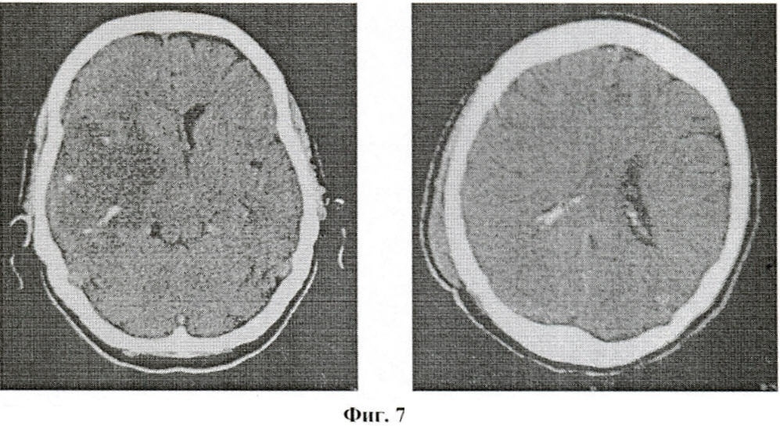
Динамическое наблюдение в течение последующих 1,5 месяцев (РКТ через месяц после XT+ДГТ) демонстрирует, несмотря на проводимую после XT+ДГТ базисную терапию, прогрессирующее ухудшение качества жизни пациента и отрицательный результат лечения (фиг.7) РКТ головного мозга больного Л. через 1 месяц после комплексного лечения.
Таким образом, данные клинического наблюдения коррелируют с показателями уровня мелатонина в моче, который может служить прогностическим критерием для определения продолжительности жизни больных.
Предлагаемым способом было проведено исследование 107 больных с глиальными опухолями головного мозга в процессе проводимой противоопухолевой терапии. Данные исследования представлены в таблице.
Как видно из представленных данных, показатель уровня мелатонина в моче больных при эффективном лечении превосходил показатели в моче здоровых доноров в 2-3,5 раза, тогда как при отсутствии клинического эффекта он был повышен более чем в 20 раз, что подтверждено выживаемостью больных.
Положительный клинический эффект (n=24 живы более 12 мес)
Технико-экономическая эффективность «Способа прогнозирования выживаемости злокачественных глиом» заключается в том, что
- удается объективизировать результаты специфической терапии;
- удается индивидуализировать для каждого больного специфическое лечение и вносить необходимые коррективы;
- сокращается время проведения химиотерапии, так как не приходится терять время на проведение неэффективного лечения;
- уменьшаются токсические побочные проявления неэффективной противоопухолевой терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ АДЪЮВАНТНОЙ ХИМИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ГЛИОМ ГОЛОВНОГО МОЗГА | 2010 |
|
RU2466739C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ЦЕРЕБРАЛЬНЫХ МЕТАСТАЗОВ ПРИ РАКЕ ЛЕГКОГО У ЖЕНЩИН | 2009 |
|
RU2439579C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ НАПРАВЛЕННОСТИ ПАТОЛОГИЧЕСКОГО ПРОЦЕССА У БОЛЬНЫХ С ОПУХОЛЯМИ ГОЛОВНОГО МОЗГА | 2009 |
|
RU2433410C2 |
| СПОСОБ ХИМИОЛУЧЕВОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ГЛИАЛЬНЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА | 2005 |
|
RU2296567C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАПРАВЛЕННОСТИ ПАТОЛОГИЧЕСКОГО ПРОЦЕССА ПРИ РАКЕ ЛЕГКОГО | 2009 |
|
RU2440037C2 |
| СПОСОБ МЕСТНОЙ ХИМИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ГЛИАЛЬНЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА | 2009 |
|
RU2392987C1 |
| СПОСОБ КОМПЛЕКСНОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2005 |
|
RU2307655C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ БОЛЬНЫХ ВНУТРИМОЗГОВЫМИ ЗЛОКАЧЕСТВЕННЫМИ ОПУХОЛЯМИ | 2003 |
|
RU2255745C2 |
| СПОСОБ ХИМИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ СПИННОГО МОЗГА | 2004 |
|
RU2280446C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ АКТИВАЦИИ ПРОЦЕССА У БОЛЬНЫХ ЛИМФОМОЙ ХОДЖКИНА | 2009 |
|
RU2405454C1 |
Изобретение относится к медицине, а именно к нейроонкологии, и может быть использовано для прогнозирования выживаемости больных с низкодифференцированными глиальными опухолями головного мозга. Сущность способа заключаются в том, что в моче пациента определяют содержание 6-сульфатоксимелатонина. При выявлении содержания 6-сульфатоксимелатонина после операции перед комплексным лечением, равным 292,7 нмоль/мл, прогнозируют выживаемость до 2,3±0,5 месяцев, при выявлении 22,4 нмоль/мл - выживаемость более 12 месяцев. При выявлении содержания 6-сульфатоксимелатонина после химиотерапии, равным 268,2 нмоль/мл, прогнозируют выживаемость до 2,1±0,6 месяца, при 32,8 нмоль/мл - более 12 месяцев. При выявлении содержания 6-сульфатоксимелатонина через месяц после лечения, равным 479,3 нмоль/мл, прогнозирую выживаемость 1,2±0,5 месяца, при 37,4 нмоль/мл - выживаемость более 12 месяцев. 7 ил., 1 табл.
Способ прогнозирования выживаемости больных злокачественными глиомами, отличающийся тем, что в моче пациента определяют содержание 6-сульфатоксимелатонина, при выявлении содержания 6-сульфатоксимелатонина после операции перед комплексным лечением равным 292,7 нмоль/мл прогнозируют выживаемость до 2,3±0,5 мес, при выявлении 22,4 нмоль/мл - выживаемость более 12 мес; при выявлении содержания 6-сульфатоксимелатонина после химиотерапии равным 268,2 нмоль/мл прогнозируют выживаемость до 2,1±0,6 мес, при 32,8 нмоль/мл - более 12 мес; при выявлении содержания 6-сульфатоксимелатонина через месяц после лечения равным 479,3 нмоль/мл прогнозируют выживаемость 1,2±0,5 мес, при 37,4 нмоль/мл - выживаемость более 12 мес.
| АБСАЛЯМОВА О.В | |||
| и др | |||
| Влияние молекулярно-генетических факторов на прогноз больных с олигоденроглиальными и смешанными опухолями | |||
| Тезисы V Конференции молодых ученых России с международным участием «Фундаментальные науки и прогресс клинической медицины», 19-22 мая, 2008, с.6-7 | |||
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ХИМИОТЕРАПИИ У БОЛЬНЫХ СО ЗЛОКАЧЕСТВЕННЫМИ ГЛИОМАМИ | 2007 |
|
RU2341794C1 |
| WO 2007111733 A3, 04.10.2007. | |||
Авторы
Даты
2012-01-10—Публикация
2010-02-25—Подача