Изобретение относится к области медицины, в частности к терапевтической стоматологии, и может быть использовано для оценки биосовместимости полимерных пломбировочных материалов.
Известен способ определения биосовместимости полимерных стоматологических материалов, который включает в себя имплантацию полимерного пломбировочного материала в мышцы, подслизистую и альвеолярную кость лабораторных животных (1).
Недостатками данного способа являются его трудоемкость и необходимость использования лабораторных животных.
Также существует способ определения биосовместимости полимерных стоматологических материалов, который включает в себя контактный тест полимерных пломбировочных материалов с базофилами цельной крови человека для выявления выброса гистамина (2).
Недостатками данного способа являются его инвазивность и трудоемкость.
В настоящее время для определения биосовместимости стоматологических пломбировочных материалов широко используются in vitro тесты с клеточными культурами.
Наиболее близким по технической сущности и достигаемому результату для определения биосовместимости полимерных пломбировочных стоматологических материалов является метод определения потенциальной цитотоксичности биоматериала на культуре клеток мышиных фибробластов (L929), основанный на определении качественных и количественных изменений в культуре клеток после инкубации с пломбировочным материалом (3).
При всех достоинствах известного способа следует отметить, что он достаточно трудоемкий, дорогостоящий и не специфичный, т.е. не воссоздает специфическую клиническую ситуацию, в которой материал будет использован.
Данный способ принят за прототип.
Техническим результатом, на достижение которого направлено создание данного изобретения, является разработка быстрого и минимально затратного способа определения биосовместимости стоматологических полимерных пломбировочных материалов, а также индивидуализации их выбора.
Поставленный технический результат достигается тем, что что до начала лечения у пациента осуществляют взятие ротовой жидкости в количестве не менее 6 мл, из которых 2 мл остаются в качестве контроля, оставшиеся 4 мл разделяем поровну на 2 порции по 2 мл и инкубируем в течение 30 минут с навесками по 30 мг предварительно полимеризованных в течение 40 с изучаемых полимерных пломбировочных материалов, исследуем все пробы ротовой жидкости, включая контрольную на спектрометре после извлечения навесок, определяя активность α-амилазы и лактатдегидрогеназы, и по степени изменения активности ферментов ротовой жидкости в сравнении с контролем судят о биосовместимости полимерного пломбировочного материала.
Способ осуществляют следующим образом.
На десятый день после профессиональной гигиены полости рта до начала лечения у пациента с клинико-рентгенологическими признаками кариеса собирают ротовую жидкость после предварительного полоскания полости рта кипяченой водой за 30 минут до исследования, далее ротовую жидкость разливают в пробирки по 2 мл, одна пробирка остается в качестве контроля, в другие пробирки (количество которых зависит от количества сопоставляемых полимерных материалов) добавляют предварительно полимеризованные в течение 40 секунд навески полимерных пломбировочных материалов по 30 мг и проводят инкубацию в течение 30 минут, после чего порции материала извлекают стерильным пинцетом; далее проводят спектрографическое исследование взятой ротовой жидкости на спектрометре типа «Lambda», определяя активность α-амилазы (в кювете к 1,0 мл реагента добавляют 25 мкл предварительно разведенной в отдельных пробирках в десять раз ротовую жидкость) и лактатдегидрогеназы (в кювете к 1,0 мл реагента добавляют 25 мкл ротовой жидкости) при длинах волн соответственно 405 нм, t-60 с, интервал 5 с и 340 нм, t-60 с, интервал 30 с; после чего рассчитывают активность α-амилазы и лактатдегидрогеназы и сопоставляют данные активности ферментов в исследуемых образцах ротовой жидкости после инкубации с полимерными пломбировочными материалами с данными активности α-амилазы и лактатдегидрогеназы контрольной ротовой жидкости, которые выбраны в связи с тем, что α-амилаза - это фермент, секретируемый слюнными железами и играющий ведущую роль в начальной стадии расщепления углеводов в полости рта, а лактатдегидрогеназа рекретируется из крови и является ключевым ферментом гликолиза, одного из основных путей метаболизма глюкозы в организме, начинающегося в ротовой полости, оба фермента содержатся в ротовой жидкости, непосредственно контактирующей с пломбировочным материалом при его клиническом применении. Отсутствие изменения активности ферментов в сравнении с контролем говорит о полной биоинертности материала. Предпочтение при индивидуальном подборе пломбировочного материала отдается тому материалу, который минимально влияет на активность ферментов ротовой жидкости в сравнении с контролем.
Клинический пример. Пациентка А., 24 года. Обратилась с жалобами на кратковременные боли при накусывании в области 34 зуба, кровоточивость межзубного сосочка в области 34, 33 зубов. Год назад пациентка проходила лечение по поводу кариеса 34, 44 зубов (II класс по Блэку) симметрично расположенного на медиальной - контактной поверхностях 34 и 44 зубов. При лечении 44 зуба был использован полимерный пломбировочный материал на основе оксирана (Filtek Silorane), а при пломбировании 34 зуба использовали полимерный пломбировочный материал на основе метакрилата (Filtek Supreme XT). На заводе-производителе перед выходом в продажу оба материала проходили биологическое тестирование на цитотоксичность с использованием мышиных фибробластов и были допущены к применению за отсутствием цитотоксического эффекта.
Объективно: на медиально-контактной поверхности 34 зуба пломба, вертикальная перкуссия 34 зуба безболезненна, горизонтальная перкуссия чувствительна, что говорит о воспалении межзубного сосочка. Вертикальная и горизонтальная перкуссии 44 зуба безболезненны. Индекс ИГР-У - 0,16, что соответствует хорошему уровню гигиены. При оценке реставрации 34 зуба по критериям USPHS (критерии для оценки качества реставраций, рекомендованные службой здравоохранения США) анатомическая форма - В, краевое прилегание - В, краевое окрашивание - В, гладкость поверхности - В, цветовое соответствие - В, чувствительность - С, контактный пункт - В, вторичный кариес - В, что показывает необходимость замены реставрации. При оценке реставрации 44 зуба по критериям USPHS: анатомическая форма - А, краевое прилегание - А, краевое окрашивание - А, гладкость поверхности - В, цветовое соответствие - В, чувствительность - А, контактный пункт - А, вторичный кариес - А, что показывает отсутствие необходимости замены реставрации. Сделали вывод о недостаточной совместимости пломбы из полимерного пломбировочного материала на основе метакрилата.
Диагноз: рецидивирующий кариес 34 зуба.
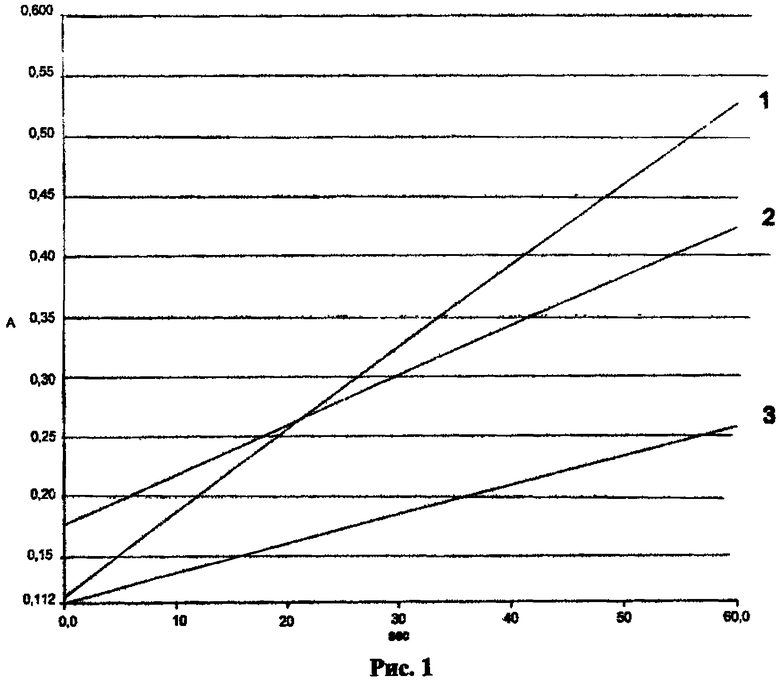
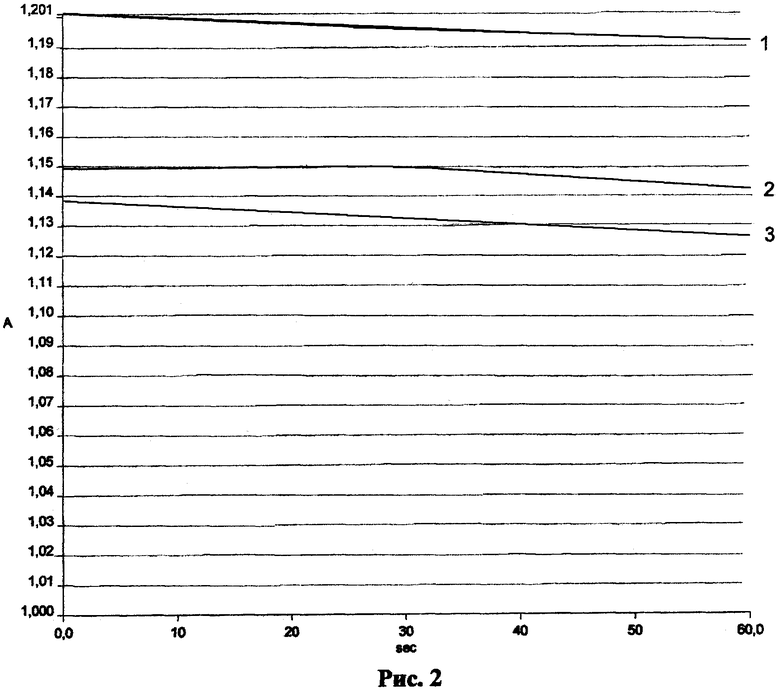
Была проведена профессиональная гигиена. На десятый день после профессиональной гигиены полости рта у пациента собирали 6 мл ротовой жидкости после предварительного полоскания полости рта кипяченой водой за 30 минут до исследования, далее ротовую жидкость разлили в пробирки по 2 мл, одна пробирка осталась в качестве контроля, в две другие пробирки добавили предварительно полимеризованные в течение 40 секунд навески полимерных пломбировочных материалов по 30 мг Filtek Supreme XT и Filtek Silorane и провели инкубацию в течение 30 минут, после чего порции материала извлекли стерильным пинцетом; далее провели спектрографическое исследование взятой ротовой жидкости на спектрометре «Lambda», определяя активность α-амилазы и лактатдегидрогеназы. В приложении показано изменение активности α-амилазы в образцах ротовой жидкости пациентки с рецидивирующим кариесом (рис.1: 1 - ротовая жидкость после инкубации с полимеризованной порцией Filtek Supreme XT, 2 - ротовая жидкость после инкубации с полимеризованной порцией Filtek Silorane, 3 - ротовая жидкость контроль) и изменение активности лактатдегидрогеназы в образцах ротовой жидкости пациентки с рецидивирующим кариесом (рис.2: 1 - ротовая жидкость контроль, 2 - ротовая жидкость после инкубации с полимеризованной порцией Filtek Supreme XT, 3 - ротовая жидкость после инкубации с полимеризованной порцией Filtek Silorane).
После чего рассчитали активность α-амилазы и лактатдегидрогеназы в Е/л и сопоставили данные активности ферментов в исследуемых образцах ротовой жидкости после инкубации с полимерными пломбировочными материалами с данными активности α-амилазы и ЛДГ контрольной ротовой жидкости. Установили значимо большее изменение активности α-амилазы и лактатдегидрогеназы по сравнению с контролем в ротовой жидкости после инкубации с полимерным материалом на основе метакрилата (Filtek Supreme XT), нежели на основе оксирана (Filtek Silorane), что говорит о его большем потенциале повреждающего и цитотоксического действия. Приняли решение о замене пломбы на основе метакрилата, используя пломбировочный материал на основе оксирана.
Далее произвели замену пломбы на пломбировочный материал Filtek Silorane и адгезивной системы Silorane system adhesive self-etch Primer и Bond, с формированием контактного пункта с помощью малой секционной матрицы и деревянных клиньев. Через шесть месяцев после пломбирования произвели оценку реставрации 34 и 44 зубов по критериям USPHS: анатомическая форма - А, краевое прилегание - А, краевое окрашивание - А, гладкость поверхности - В, цветовое соответствие - В, чувствительность - А, контактный пункт - А, вторичный кариес - А, что показывает отсутствие необходимости замены реставрации. Жалобы со стороны пациентки отсутствовали. Горизонтальная перкуссия 34 и 44 зубов безболезненна, что говорит об отсутствии воспаления межзубного десневого сосочка в области этих зубов.
Предлагаемый способ может быть использован в стоматологии при индивидуализированном подборе полимерного пломбировочного материала для восстановления зубов, фиксации ортодонтических и ортопедических конструкций для оценки биосовместимости сопоставляемых полимерных пломбировочных материалов и особенно в терапевтической стоматологии.
Литература
1. Gottfried Schmalz, Dorthe Arenholt-Bindslev. Biocompatibility of Dental Materials. Library of Congress Control Number: 2008925341© 2009 Springer-Verlag Berlin Heidelberg. 114.
2. Babakhin AA, Volozhin AI, Dubova LV, Lebedenko IIu, Babakhina IuA, Zhuravleva AA, Diubuske LM. Histamine releasing activity of dental materials as the indicator of their biocompatibility. Stomatologiia (Mosk). 2008; 87 (1): 8-17.
3. ГОСТ Р ИСО 10993-5-2009.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ КАРИЕСА ЗУБОВ | 2013 |
|
RU2539422C1 |
| СПОСОБ ВЫБОРА СТОМАТОЛОГИЧЕСКОГО БОРА ДЛЯ ФИНИШНОЙ ОБРАБОТКИ ПОВЕРХНОСТИ ДЕНТИНА ПРИ ЛЕЧЕНИИ КАРИЕСА | 2012 |
|
RU2506923C1 |
| СПОСОБ ОЦЕНКИ БИОСОВМЕСТИМОСТИ СКАФФОЛДОВ | 2014 |
|
RU2571232C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОНТАКТНОГО ПУНКТА МОЛЯРОВ И ПРЕМОЛЯРОВ, УТРАЧЕННЫХ ВСЛЕДСТВИЕ КАРИОЗНОГО ПРОЦЕССА | 2024 |
|
RU2839212C1 |
| СПОСОБ РЕСТАВРАЦИИ ЗУБОВ ПРИ ПОВЫШЕННОЙ СТИРАЕМОСТИ | 2016 |
|
RU2632532C1 |
| СПОСОБ ПЛОМБИРОВАНИЯ КАРИОЗНОЙ ПОЛОСТИ | 2015 |
|
RU2602496C1 |
| СПОСОБ ДИАГНОСТИКИ МЕМБРАНОТОКСИЧНОСТИ | 2013 |
|
RU2527698C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КУЛЬТЕВОЙ ШТИФТОВОЙ ВКЛАДКИ ДЛЯ ПЕРЕДНЕЙ ГРУППЫ ЗУБОВ | 2012 |
|
RU2504343C1 |
| Способ пломбирования зубов композитным материалом | 2019 |
|
RU2731821C1 |
| Устройство для пломбирования зубов композитным материалом | 2024 |
|
RU2837969C1 |
Настоящее изобретение относится к области медицины, в частности к терапевтической стоматологии, и описывает способ оценки биосовместимости стоматологических полимерных пломбировочных материалов, основанный на инкубации пломбировочного материала с культурой клеток, где до начала лечения у пациента осуществляют взятие ротовой жидкости в количестве не менее 6 мл, из которых 2 мл остаются в качестве контроля, оставшиеся 4 мл разделяют поровну на 2 порции по 2 мл и инкубируют в течение 30 минут с навесками по 30 мг предварительно полимеризованных в течение 40 с изучаемых полимерных пломбировочных материалов, исследуют все пробы ротовой жидкости, включая контрольную на спектрометре после извлечения навесок, определяя активность α-амилазы и лактатдегидрогеназы, и по степени изменения активности ферментов ротовой жидкости в сравнении с контролем судят о биосовместимости полимерного пломбировочного материала. Способ обеспечивает быстроту определения биосовместимости стоматологических полимерных пломбировочных материалов с минимальными затратами. 2 ил., 1 пр.
Способ оценки биосовместимости стоматологических полимерных пломбировочных материалов, основанный на инкубации пломбировочного материала с культурой клеток, отличающийся тем, что до начала лечения у пациента осуществляют взятие ротовой жидкости в количестве не менее 6 мл, из которых 2 мл остаются в качестве контроля, оставшиеся 4 мл разделяют поровну на 2 порции по 2 мл и инкубируют в течение 30 мин с навесками по 30 мг, предварительно полимеризованных в течение 40 с изучаемых полимерных пломбировочных материалов, исследуют все пробы ротовой жидкости, включая контрольную на спектрометре после извлечения навесок, определяя активность α-амилазы и лактатдегидрогеназы, и по степени изменения активности ферментов ротовой жидкости в сравнении с контролем судят о биосовместимости полимерного пломбировочного материала.
| Регулятор электрической дуги для прожектора | 1926 |
|
SU10993A1 |
| - М.: Стандартинформ, 2010 | |||
| Кузнецов И.А | |||
| Биосовместимость пломбировочных материалов с тканями зуба при восстановительном лечении среднего кариеса | |||
| - Иркутск, 2004 | |||
| Македонова Ю.А | |||
| Биосовместимость стоматологических материалов, используемых в современном эндодонтическом | |||
Авторы
Даты
2013-03-10—Публикация
2011-04-05—Подача