Настоящее изобретение относится к применению силибининового компонента для получения лекарственного средства для лечения вирусного гепатита, предпочтительно гепатита В или С, в частности для снижения вирусной нагрузки. Предпочтительно лекарственное средство адаптировано для парентерального введения. Предпочтительно силибининовый компонент является сложным эфиром силибинина.
Силибинин {3,5,7-тригидрокси-2-(3-(3-гидрокси-4-метоксифенил)-2-(гидроксиметил)-2,3-дигидробензо[b][1,4]-диоксин-6-ил)хроман-4-он, или по номенклатуре Европейской фармакопеи (2R,3R)-3,5,7-тригидрокси-2-[(2R,3R)-3-(4-гидрокси-3-метоксифенил)-2-(гидроксиметил)-2,3-дигидро-1,4-бензодиоксин-6-ил]-2,3-дигидро-4Н-1-бензопиран-4-он}, представляет основную составную часть силимарина и основной флавоноид, экстрагированный из расторопши (Silybum marianum Gaertneri).
Силибинин имеет структуру:
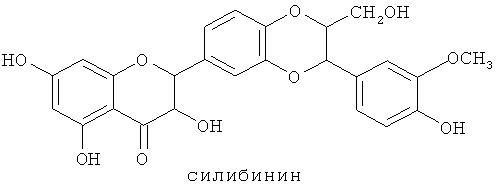
Диастереоизомеры силибинин А и силибинин В представляют в литературе раздельно:
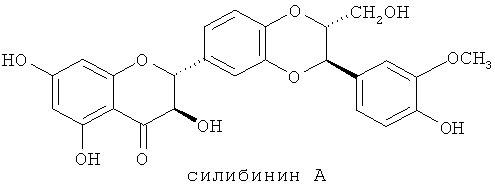
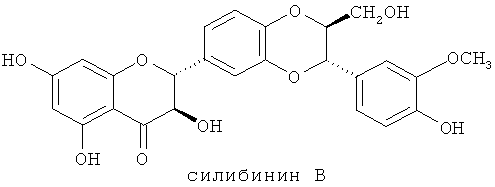
Силибинин представляет основную составляющую часть силимарина (в смеси 50:50 силибина А и силибина В). К другим составляющим частям относятся изосилибинин (изосилибин А и изосилибин В), силидианин, силикристин, изосиликристин, таксифолин и другие. Способы выделения силибинина известны в предшествующем уровне техники (например, US 4871763).
Силибинин и силимарин подробно изучены и описаны. В связи с этим можно сослаться на работы N.-C. Kim и др., Org. Biomol. Chem. 1, 2003, сс.1684-1689; D.Y.W. Lee и др., J. Nat. Prod. 66, 2003, сс.1171-1174; D.J. Kroll и др., Integrative Cancer Therapies, 6, 2007, сс.110-119; Z.Wen и др., DMD Fast Forward, doi:10.1124/dmd.107.017566; и US 4871763.
История лекарственного растения Silybum marianum насчитывает примерно 2000 лет. Силимарин - экстракт семян расторопши, представляет старинное лекарство для лечения различных расстройств печени и желчного пузыря, включая гепатит, цирроз, а также гепатопротектор, защищающий печень от отравления дикими грибами, алкоголем, химическими веществами и токсинами из окружающей среды. Механизм действия силимарин разнообразен. Самое большое рандомизированное контролируемое исследование, проведенное в 1970-е годы, показало, что длительное применение силимарина может снизить смертность пациентов с хроническим циррозом (P.Ferenci и др., J Hepatol 9, 1989, сс.105-113). Тем не менее, роль этого лекарственного средства для лечения болезней печени остается противоречивой (S.Verma и др., Clinical Gastroenterology and Hepatology 5, 2007, сс.408-416; F.Rainone, Am Fam Phys 72(7), 2005, cc.1285-1288). Частично эта неопределенность вызвана ограниченными сведениями по фармакокинетике и по оптимальным режимам дозирования. Силимарин плохо растворим в воде, и пероральное применение приводит к ограниченной биодоступности.
Фармацевтические применения силибинина также известны. Силибинин обладает сильными антиоксидативными свойствами (см. A.Pietrangelo и др., Gastroenterology 109, 1995, сс.1941-1949; М.I.Lucena и др., Int J Clin Pharmacol Ther 40, 2002, cc.2-8; L.Mira и др., Biochem Pharmacol 48, 1994, cc.753-759) и противофиброзными свойствами (см. G.Boigk и др., Hepatology 26, 1987, сс.643-649; С.Dehmlow и др., Hepatology 23, 1996, сс.749-754), поэтому он потенциально применим в качестве лекарственного средства для лечения хронических заболеваний печени. Чистое вещество силибинин вводят внутривенно, например, при отравлении печени бледной поганкой (токсины аменитин, фаллоидин) для предотвращения разрушения печени (см. К.Hruby и др., Hum Toxicol 2, 1983, сс.138-195). Действие при грибном отравлении частично объясняется стимулированием ядрышковой полимеразы А, которая повышает синтез рибосомального белка и ингибирует перекисное окисление липидов (J.Sonnenbichler и др., Prog Clin Biol Res. 213, 1986, cc.319-331). Клинические исследования также были успешны в предупреждении и лечении некоторых типов рака (L.Varghese и др., Clin Cancer Res 11(23), 2005, сс.8441-8447; К. Letschert и др., Toxicological Sciences 91, 2006, сс.140-149).
Сложный эфир силибинина получают в виде раствора для инфузии, например продукт Legalon® SIL в Федеративной Республике Германии.
Вирусный гепатит относится к инфекциям, которые поражают печень и вызываются вирусами. Вирусные гепатиты активно исследуют во всем мире. Вирусный гепатит не только вызывает высокую смертность, но также истощает медицинские ресурсы и может вызвать тяжелые экономические последствия. Большинство всех вирусных гепатитов можно предотвратить.
К понятию «вирусный гепатит» относится пять разных заболеваний, которые вызываются по меньшей мере пятью разными вирусами. Гепатит А и гепатит В (инфекционный гепатит и сывороточный гепатит соответственно) представляют разные заболевания и оба диагностируются по специфическому серологическому тесту. Гепатиты С и Е представляют третью категорию, отличающуюся по типу, причем гепатит С передается парентерально, а гепатит Е передается энтерально. Гепатит D, или дельта гепатит, представляет заболевание, вызываемое вирусом другого типа, зависящего от инфицирования гепатитом В. Эта форма гепатита может быть в форме суперинфекции у носителя гепатита В или в форме совместного инфицирования у индивидуума с острым гепатитом В.
Гепатит С - инфекционное заболевание людей, вызываемое вирусом гепатита С (ВГС). Инфицирование вирусом гепатита С может привести к тяжелому поражению печени, например воспалению паренхимы печени, фиброзу печени, циррозу печени и карциноме печени. Более чем у 80% инфицированных пациентов инфекция ВГС становится хронической. Передача ВГС обычно происходит парентеральным путем через кровь.
Установлено, что примерно 170 миллионов людей в мире инфицировано вирусом гепатита С (ВГС). На протяжении десятилетий у инфицированных пациентов симптомы заболевания отсутствуют до тех пор, пока не разовьется цирроз печени и/или гепатоцеллюлярная карцинома. Примерно в 40-50% случаев в США трансплантация печени вызвана инфекциями ВГС. Было идентифицировано шесть генотипов ВГС (ВГС1-ВГС6), которые отличаются по географическому распространению и по их ответу на лечение.
Установлено, что белки ВГС индуцируют активирование STAT-3 через оксидативный стресс и Са2+ передачу сигнала (К.Koike и др., Hepatol Res 34, 2006, сс.65-73; G.Waris и др., J Virol 79, 2005, сс.1569-1580), а также продукты перекисного окисления липидов и антиоксидантную генную экспрессию (М.Okuda и др., Gastroenterology 122, 2002, сс.366-375). Предполагают, что баланс оксидативного и восстановительного потенциалов в клетке (клеточный окислительно-восстановительный потенциал) имеет выраженные последствия в отношении метаболических путей сигнальной трансдукции (Y.M.Janssen и др., Am J Physiol 273, 1997, сс.789-796), включая ослабленную ИФН-альфа передачу сигнала (D.Di Bona и др., J Hepatol. 45, 2006, сс.271-279).
Инфекция ВГС поделена по требованиям ICD10 (ВОЗ, версия 2007) на острый (В17.1) и хронический гепатит С (В18.2).
ВГС является одной из наиболее важных причин развития острого или хронического гепатита. Однако течение болезни может сильно различаться и в высокой степени подвержено изменчивости. Поэтому нельзя говорить о типичном течении болезни, поскольку инфекция ВГС проявляется широким спектром клинического проявления, т.е. вариабельными симптомами, разными клиническими картинами и различными вторичными заболеваниями печени и поражениями за пределами печени.
Примерно у 20% пациентов с острым гепатитом воспаление печени является следствием инфекции ВГС. Однако в острой фазе гепатит С обычно протекает бессимптомно и поэтому примерно в 85% случаев не диагностируется. В некоторых случаях имеются только неспецифические симптомы, напоминающие грипп. Обычно инфекция не проявляется во время острой фазы.
Гепатит С становится хроническим примерно у 85% пациентов с острой инфекцией ВГС. Такая высокая степень перехода заболевания в хроническую фазу является результатом высокой изменчивости ВГС, т.е. ген, который кодирует оболочку ВГС, мутирует с высокой частотой. Из-за высокой вариабельности вируса и, в частности, высокой вариабельности антигенного эпитопа ВГС, мутантный ВГС избегает распознавания иммунной системой человека. Примерно у 25% пациентов результатом хронического воспаления печени является формирование цирроза печени и повышение риска развития карциномы печени (см., например, J.Н.Hoofnagle, Hepatology 1997, 26, приложение 1, сс.15S-20S; М.I. Memon и др., Journal of Viral Гепатит 9, 2002, сс.84-100; S.L.Tan и др., Nature Reviews, Drug Discovery 1, 2002, cc.867-881).
Пациенты, инфицированные ВГС, обычно получают стандартное комбинированное лечение пэгелированным интерфероном-α2а или интерфероном-α2b и рибавирином. При инфекциях ВГС с генотипами 2 или 3 (инфекции ВГС2 или ВГС3) такое комбинированное лечение проводят в течение 24 недель. При инфекциях ВГС с генотипом 1 (ВГС1) для ВГС1-положительных пациентов проводят комбинированное лечение в течение 48 недель. Многие из ВГС-инфицированных пациентов, однако, прерывают лечение из-за имеющихся побочных эффектов и/или из-за неприятия парентерального введения и длительности применения. Кроме того, только примерно 50% пациентов с инфекцией ВГС1 достигают положительного результата столь длительного лечения, т.е. оставшиеся не реагируют на такое лечение, т.е. являются нон-респондерами (см., например, R.E.T.Smith, Nature Reviews, Drug Discovery, 5, 2006, с.715). Лечение вызываемого вирусом гепатита С заболевания пэгелированным интерфероном плюс рибавирином оказывается неэффективным примерно у половины пациентов с генотипом 1. Неэффективность лечения происходит или из-за отсутствия реакции организма на лечение (минимальное снижение титра вируса), или из-за рецидива (сильный первоначальный ответ на лечение сменяется новым ростом титра вируса во время или после лечения). Такие разные последствия лечения могут зависеть от разных факторов, включая генетический статус хозяина, иммунный ответ и генетические отличия вирусов (см. M.W.Fried и др., New England Journal of Medicine 347, 2002, сс.975-982; H.S.Conjeevaram и др., Gastroenterology 131, 2006, сс.470-477; M.P.Manns и др., Lancet 358, 2001, сс.958-965; D.B.Strader и др., Hepatology 39, 2004, с.114771; S.J.Hadziyannis и др., Ann Intern Med, 140, 2004, сс.346-355). Генетические отличия вирусов могут включать или различия, имевшиеся до начала лечения, или различия, которые возникают во время лечения из-за эволюции вируса в ответ на давление применяемого лечения.
Разрабатывают новые варианты лечения, включающие оптимизацию имеющегося стандартного лечения пэгелированным интерфероном плюс рибавирином, особенно целевую противовирусную терапию в отношении ВГС, новые иммуномодулирующие агенты и лечение, направленное на снижение фиброза (см. R.E.Stauber и др., Drugs 68(10), 2008, с.1347).
До настоящего времени нет вакцины против ВГС. Стандартные методы лечения очень дорогие, дают незначительный эффект в плане уничтожения инфекции ВГС и иногда вызывают значительные побочные эффекты (S.L.Tan и др., Nature Reviews, Drug Discovery 1, 2002, с.867; R.Bartenschlager, там же, с.911).
Существует потребность в лекарственных средствах для лечения вирусного гепатита, особенно гепатита В и С.
Задача, решаемая в настоящем изобретении, заключается в получении эффективного лекарственного средства для лечения вирусного гепатита, в частности гепатита В или С, которое обладает преимуществами по сравнению с лекарственными средствами предшествующего уровня техники. Лекарственное средство по возможности не должно иметь побочных эффектов или иметь слабовыраженные побочные эффекты, и быть эффективным, например, для пациентов с гепатитом С, которые существенным образом не отвечают на традиционное комбинированное лечение пэгинтерфероном/рибавирином. Кроме того, лекарственное средство должно обладать выраженными противовирусными свойствами и, таким образом, надежно снижать нагрузку вируса.
Достижение указанной задачи изложено в формуле настоящего изобретения.
Неожиданно было установлено, что силибинин, его фармацевтически приемлемые соли и/или производные применимы для лечения воспаления, вирусных болезней печени, особенно гепатита С. Таким образом, у пациентов с гепатитом С, которые не отвечают на лечение иммуномодулирующей/ противовирусной комбинированной терапией (нон-респондеры), например пэгинтерфероном/рибавирином, которая представляет в настоящее время стандартное лечение гепатита С, существенное снижение нагрузки вируса может быть достигнуто путем введения, предпочтительно парентерального введения, силибининового компонента. Также было показано, что предварительное лечение силибининовым компонентом повышает ответ пациентов на более позднее введение интерферона и рибавирина.
Исследования, касающиеся лечения инфекций ВГС, особенно касающиеся подавления инфекций ВГС, путем введения силимарина, описаны в предшествующем уровне техники (см., например, R.Sailer и др., Drugs 61(14), 2001, сс.2035-2063; К.Е.Mayer и др., Journal of Viral Hepatitis, 12, 2005, cc.559-67; US 2005/0123628; S.J.Polyak и др., Gastroenterology 132, 2007, cc.1925-1936).
R.Sailer и др. сообщают, что хотя не установлено влияния силимарина на репликацию вируса, по фармакологическим оценкам можно ожидать, что он ингибирует воспаление и цитотоксический каскад событий, запускаемых вирусной инфекцией. Пероральное введение комплекса силибинина-фосфатидилхолина (IdB1016, 240 мг силибинина дважды в сутки) в краткосрочном с плацебо-контролем экспериментальном исследовании 20 пациентов с хроническим гепатитом показало, что эволюция уровней AST существенно понижена в группе силибинина при отсутствии существенных отличий других исследовавшихся показателей функции печени (см. A.Vailati и др., Fitoterapia, 64(3), 1993; G.Buzzelli и др., Int. J.Clin. Pharmacol. Ther. Toxicol. 31, 1993, cc.456-460).
K.E.Mayer и др. описывают, что пероральное лечение силимарином приводит к снижению трансаминаз в сыворотке по сравнению с исходными показателями в четырех исследованиях и с плацебо только в одном исследовании. Однако нет доказательства, что силимарин влияет на нагрузку вируса или улучшает гистологию печени при гепатите В или С (см. M.L.Chavez, J.Herb. Pharmacother. 1(3), 2001, сс.79-90; L.B.Seeff и др., Hepatology, 34(3), 2001, сс.595-603). Был сделан вывод, что силимариновые соединения вероятно снижают уровень сывороточных трансаминаз у пациентов с хроническим вирусным гепатитом, но предположительно не влияют на нагрузку вируса или гистологию печени.
US 2005/0123628 относится inter alia к получению и пероральному введению композиций, включающих глицирризин, препарат лимонника, аскорбиновую кислоту, L-глутатион, силимарин, липоевую кислоту и D-альфа-токоферол. Сообщают, что указанные композиции применимы для снижения оксидативного стресса и перекисного окисления липидов, для лечения хронического заболевания печени, хронической инфекции вирусного гепатита С и неалкогольного жирового гепатита. Многочисленные исследования сообщают о гепатопротекторных свойствах, которые силимарин проявляет против большого количества разных токсинов, включая ацетаминофен, этанол, четыреххлористый углерод и D-галактозамин, а также против ишемического повреждения, радиации и токсичности железа. В течение первых двадцати недель открытого нерандомизированного одноцентрового клинического исследования субъектам давали для орального введения два раза в сутки в совокупности 1000 мг глицирризина; три раза в сутки в суммарном количестве 1500 мг экстракта растения лимонника; три раза в сутки в суммарном количестве 6000 мг аскорбиновой кислоты; два раза в сутки в суммарном количестве 300 мг L-глутатиона; три раза в сутки в суммарном количестве 750 мг экстракта расторопши; два раза в сутки в суммарном количестве 300 мг липоевой кислоты; и один раз в сутки в количестве 800 ME D-альфа-токоферола. В течение первых десяти недель исследования субъектам вводили внутривенной инъекцией дважды в неделю четыре разные парентеральные композиции, из которых ни одна не содержит силимарина. Через 10 недель 12,0% субъектов, через 20 недель 24,0% субъектов проявили 1 log снижение нагрузки вируса. В US 2005/0123628 нет даже намека на то, что силимарин, или что только силибинин, может быть ответственным за относительно небольшое снижение вирусной нагрузки.
S.J.Polyak и др. сравнивают in vitro стандартизированный экстракт силимарина (МК-001) с коммерческими препаратами силимарина. Сообщают, что оба препарата проявляют противовирусное действие при использовании моделей, основанных на культуре клеток, хотя воздействие коммерческих препаратов не такое сильное по сравнению с МК-001. МК-001 ингибирует экспрессию фактора альфа некроза опухоли в анти-CD3 простимулированных мононуклеарных клетках периферической крови и зависимую от ядерного фактора каппа В транскрипцию в клетках гепатомы человека Huh7. Кроме того, доза МК-001 подавляет инфекцию клеток Huh7 и Huh7.5.1 вирусом JFH-1 дозозависимым способом. МК-001 проявляет действие против инфекции ВГС в выделенных клетках и при комбинировании с интерфероном-α ингибирует репликацию ВГС в большей степени по сравнению с ингибированием только одним интерфероном-α. Для сравнения анти-ВГС действия МК-001 с коммерческими препаратами силимарина, также тестируют продукт Ultrathistle® (фирма Natural Wellness, Монтгомери Нью-Йорк) и продукт Silybinin® (фирма Indena SpA, Милан). Однако сообщают, что МК-001 проявляет более сильное противовирусное действие по сравнению с продуктами Ultrathistle® и Silybinin®. На основании исследований in vitro был сделан вывод о том, что поскольку есть действие анти-ВГС, стандартизированный экстракт силимарина МК-001 превосходит два коммерческих продукта. S.J.Polyak ничего не сообщает о парентеральном введении очищенного силибинина, не говоря уже о лечении нон-респондеров. Кроме того, выводы, сделанные Polyak и др., противоречат клиническим исследованиям, которые показали отсутствие воздействия силимарина на ВГС у пациентов с хроническим гепатитом С (M.D.Tanamly и др., Dig Liver Dis. 36, 2004, сс.752-759; Е.Gabbay и др., World J Gastroenterol. 13, 2007, сс.5317-5323).
В настоящее время неожиданно было обнаружено, что введение, особенно парентеральное введение, предпочтительно чистого компонента силибинина снижает in vivo нагрузку вируса у пациентов с вирусным гепатитом. Таким образом, компонент силибинин способен понизить вирусную нагрузку. Это обстоятельство позволяет оптимизировать дозу силибинина при отсутствии других компонентов силимарина, которые могут вызвать нежелательные побочные эффекты.
Снижение вирусной нагрузки путем парентерального введения силибининового компонента особенно неожиданно, поскольку клинические исследования показывают, что силимарин не влияет на ВГС у пациентов с хроническим гепатитом С (М.Torres и др., P.R.Health Sci J 23(2), 2004, сс.69-74; M.D.Tanamly и др., Dig Liver Dis., 36, 2004, сс.752-759; A Gordon и др., J Gastroenterol Hepatol. 21, 2006, cc.275-280; E.Gabbay и др., World J Gastroenterol. 13, 2007, cc.5317-23; L.B.Seeff и др., Hepatology, 80(11), 2008, cc.1900-1906).
M.Torres и др. сообщают о клиническом исследовании, в котором приглашали принять участие пациентов в возрасте 21-65 лет с хроническим гепатитом С, не подвергавшихся воздействию противовирусной терапии. Рандомизируют 34 пациентов для лечения S.marianum 160 мг перорально трижды в неделю в течение четырех недель или лечение не проводилось (контроль). Исследование показало, что S.marianum не действует в качестве противовирусного агента.
M.D.Tanamly и др. сообщают о клиническом исследовании, в котором 177 пациентов с хроническим гепатитом, вызванным вирусом гепатита С, были рандомизированно поделены для получения или перорально силимарина или поливитаминных добавок. Исследование показало, что рекомендованная доза силимарина не воздействует на вирусемию вирусом гепатита С.
A.Gordon и др. сообщают о клиническом исследовании, в которое были вовлечены 24 субъекта с хроническим гепатитом С, а именно в рандомизированное двойное слепое с плацебо-контролем исследование. Субъекты получали 12 недель S.marianum (или 600 мг, или 1200 мг/сутки) и плацебо. Поводили биохимические, вирусологические, психологические исследования, а также анализ качества жизни. Семнадцать пациентов полностью прошли исследование. Исследование показало, что средние изменения титров РНК ВГС не отличались существенным образом у субъектов, получавших S.marianum, по сравнению с теми, кто получал плацебо.
Е.Gabbay и др. сообщают о клиническом исследовании, в которое было вовлечено 100 пациентов с хронической инфекцией ВГС, для которых лечение интерфероном было неудачным, и которые были рандомизированы для получения семи разных антиоксидантов наряду с капсулами силимарина, 250 мг, трижды в сутки. Основными конечными точками исследования были ферменты печени, уровни РНК ВГС и гистология. Исследование показало, что антиоксидативная терапия не влияет на вирусную нагрузку.
L.B.Seeff и др. сообщают об исследовании длительного противовирусного лечения цирроза при гепатите С с циррозом (HALT-C), включающем субъектов со сформированным хроническим гепатитом С, которые являются нон-респондерами в отношении первичной противовирусной терапии, но готовы участвовать в долгосрочном лечении пэгелированным интерфероном. Не обнаружено полезного воздействия силимарина на уровни РНК вируса гепатита С (ВГС). Таким образом, у получавших силимарин были сходные уровни ВГС при сравнении с уровнями у тех, кто не получал такого лечения.
Кроме того, неожиданно было обнаружено, что введение, особенно парентеральное введение, компонента силибинина способствует общепринятому лечению пэгинтерфероном/рибавирином. Установлено, что компонент силибинин активирует (реактивирует) чувствительность пациентов к традиционному лечению пэгинтерфероном/рибавирином и/или энхансерами антивирусного действия традиционной терапии пэгинтерфероном/рибавирином.
Краткое описание фигур
Фиг.1. Пример 1, исследование 1: параметры оксидативного стресса до и после инфузии 10 мг/кг силибининового компонента на протяжении 4 ч (п-РКМ = производные соединения реактивных кислородных метаболитов, БАП = биологический антиоксидантный потенциал).
Фиг.2. Пример 1, исследование 1: РНК ВГС (log МЕ/мл; средняя величина ± стандартное отклонение) до (1 сутки) и после (7 суток) внутривенного введения 10 мг/кг силибининового компонента/сутки.
Фиг.3. Пример 1, исследование 1: изменения ВГС-РНК после внутривенного введения 10 мг/кг/сутки силибининового компонента в течение 7 суток с последующей комбинированной терапией пэгинтерфероном альфа 2а/рибавирином и 140 мг силимарина три раза в сутки.
Фиг.4. Пример 1, исследование 2: изменения ВГС-РНК во время введения силибининового компонента в разных дозах в течение 14 суток с последующей комбинированной терапией пэгинтерфероном альфа 2а/рибавирином, начатой на 8 сутки.
Фиг.5. Пример 1, исследование 2: средняя величина ± среднеквадратичное отклонение снижения ВГС-РНК в течение 7 суток монотерапии в виде внутривенного введения компонента силибинина и 7 суток внутривенного введения компонента силибинина с пэгинтерфероном альфа 2а/рибавирином в разных дозах.
Фиг.6. Пример 1, исследование 2: изменения ВГС-РНК после завершения внутривенного введения силибинина (2 недели) у 14 пациентов, получавших силибинин в количестве 15 или 20 мг/кг/сутки. Комбинированную терапию пэгинтерфероном альфа 2а/рибавирином начинают на 8 сутки и 280 мг силимарином три раза в сутки на 15 сутки.
Фиг.7. Пример 2, конкретный пациент, изменения ВГС-РНК после внутривенного введения 20 мг/кг/сутки силибининового компонента во время двух интервалов введения, включающих 14 суток подряд, первый интервал во внутривенном введении начинается на 24 сутки, а второй интервал во введении, начиная с 35 недели, на протяжении непрерывной комбинированной терапии с применением 180 мкг пэгинтерферона альфа 2а/рибавирина в течение 60 недель.
Фиг.8. Пример 2, конкретный пациент, изменения в ВГС-РНК после внутривенного введения 20 мг/кг/сутки силибининового компонента во время интервала введения, включающего 14 последовательных суток, и начиная с 32-й недели на протяжении непрерывной комбинированной терапии с применением 180 мкг пэгинтерферона альфа 2а/рибавирина в течение 60 недель.
Фиг.9. Пример 2, конкретный пациент, изменения в ВГС-РНК после внутривенного введения 20 мг/кг/сутки силибининового компонента во время интервала введения, включающего 14 последовательных суток и начиная с 72-й недели на протяжении непрерывной комбинированной терапии с применением 180 мкг пэгинтерферона альфа 2а/рибавирина в течение 80 недель.
Фиг.10. Схематически показаны различные способы совместного применения рибавирина и/или пэгелированного интерферона альфа и лекарственного средства, содержащего силибининовый компонент.
Фиг.11. Данные, полученные в исследовании подавления in vitro NS5B для шести очищенных компонентов силимарина.
Фиг.12. Данные, полученные в исследовании подавления in vitro NS5B для силибинин-бис(гидрогенсукцината).
Настоящее изобретение относится к применению силибининового компонента для получения лекарственного средства, предпочтительно вирусостатического или противовирусного, более предпочтительно снижающего вирусную нагрузку, для лечения вирусного гепатита, в частности гепатита В или С, предпочтительно инфекций хронического или острого вирусного гепатита С, предпочтительно парентеральным введением.
В контексте настоящего изобретения понятие «лекарственное средство» предпочтительно является синонимом «лекарственного лечения».
В предпочтительном варианте осуществления настоящее изобретение относится к применению силибининового компонента для получения лекарственного средства, которое практически не содержит силидианина, и/или силикристина, и/или изосилибинина, для лечения вирусного гепатита, предпочтительно гепатита В или С.
В предпочтительном варианте осуществления настоящего изобретения лечение вирусного гепатита, в частности гепатита В или С, проводят путем снижения вирусной нагрузки. Установлено, что силибининовые компоненты способны снижать вирусную нагрузку у пациентов с гепатитом В или С. Это особенно неожиданно, поскольку в предшествующем уровне техники нет доказательства, что силимарин, смесь которого содержит определенное количество силибинина, влияет на вирусную нагрузку или улучшает гистологию печени при гепатите В или С (см. К.Е.Mayer и др., Journal of Viral Hepatitis, 2005, 12, 559-567).
В другом предпочтительном варианте осуществления настоящего изобретения лечение вирусного гепатита, в частности гепатита В или С, проводят у пациентов, которым предстоит или которые перенесли трансплантацию печени. Пациенты, перенесшие трансплантацию печени из-за вирусного гепатита, подвержены риску возобновления вирусного гепатита в трансплантированной печени. Обычно вирус удаляется не полностью из организма, когда инфицированную печень удаляют хирургически, и оставшиеся в организме вирусы заново инфицируют трансплантированную печень. При хроническом гепатите С инфицированные пациенты заново инфицируются после трансплантации печени в 100% случаев. Неожиданно было установлено, что силибинин может снизить вирусную нагрузку, риск повторной инфекции после трансплантации печени может быть существенно понижен путем введения, предпочтительно парентерального введения, компонента силибинина.
Формы вирусного гепатита известны специалистам в данной области.
В настоящее время установлено по меньшей мере шесть разных форм: гепатиты А, В, С, D, Е и G. Организмами-возбудителями этих инфекций являются гепатотропные вирусы. Они принадлежат к разным семействам вирусов в каждом случае и имеют геном из ДНК или РНК. Трансмиссия происходит или через пищу, или через тканевые жидкости, например сперму и кровь. Также имеются различия у разных форм, касающиеся течения заболевания и его тяжести. Хотя гепатиты А и Е обычно бывают в острой форме, гепатиты В, С и D могут привести к хроническому течению заболевания, и в некоторых случаях, к тяжелым осложнениям.
В настоящем описании понятие «вирусный гепатит» предпочтительно включает гепатиты В и С.
В предпочтительном варианте осуществления настоящего изобретения проводят лечение путем снижения вирусной нагрузки одного или нескольких вирусов, выбранных из группы, состоящей из генотипов ВГС1, ВГС2, ВГС3, ВГС4, ВГС5 и ВГС6, предпочтительно ВГС1, но не только из них.
Если генотипом является генотип вируса ВГС1, предпочтительны подтипы 1a, 1b, 1c, 1d, 1e, 1f, 1g, 1h, 1i, 1j, 1k и 1l. Если генотипом является генотип вируса ВГС2, предпочтительны подтипы 2а, 2b, 2с, 2d, 2е, 2f, 2g, 2h, 2i, 2j, 2k, 2l, 2m, 2n, 2o, 2p и 2q. Если генотипом является генотип вируса ВГС3, предпочтительны подтипы 3а, 3b, 3с, 3d, 3е, 3f, 3g, 3h, 3i, 3j и 3k. Если генотипом является генотип вируса ВГС4, предпочтительны подтипы 4а, 4b, 4с, 4d, 4е, 4f, 4g, 4h, 4i, 4j, 4k, 4l, 4m, 4n, 4o, 4p, 4q, 4r и 4t. Если генотипом является генотип вируса ВГС5, предпочтителен подтип 5а. Если генотипом является генотип вируса ВГС6, предпочтительны подтипы 6а, 6b, 6с, 6d, 6е, 6f, 6g, 6h, 6i, 6j, 6k, 6l, 6m, 6n, 6o, 6p и 6q. О номенклатуре генотипов и подтипов вируса гепатита С см., например, P.Simmonds и др., Hepatology, 42, 2005, 962-973.
В предпочтительном варианте осуществления настоящее изобретение относится к применению компонента силибинина для получения лекарственного средства, которое предпочтительно адаптировано для парентерального введения для лечения вирусного гепатита, предпочтительно гепатита С, пациентам, которые не отвечают на обычную иммуномодулирующую/противовирусную комбинированную терапию, например терапию рибавирином/интерфероном («нон-респондеры»), и/или пациентам, которые частично отвечают на традиционную иммуномодулирующую/противовирусную комбинированную терапию, например, терапию рибавирином/интерфероном («частичные респондеры»), и/или пациентам, которые проявляют четкий начальный ответ с последующим возобновлением вирусных титров во время или после терапии («рецидивы»).
Настоящее изобретение также относится к лечению вирусного гепатита С с помощью силибининового компонента, причем это лечение следует за традиционной комбинированной терапией с помощью рибавирина/интерферона. Предпочтительно лечение введением силибининового компонента начинается после неудачного лечения рибавирином/интерфероном (или сначала, или после определенного периода лечения).
В связи с традиционным лечением гепатита С путем введения рибавирина/интерферона понятия «нон-респондеры», «частичные респондеры» и «больные с рецидивом» известны специалистам в данной области. В настоящее время лечение вирусного гепатита С пэгилированным интерфероном вместе с рибавирином неудачно примерно для половины случаев у пациентов при генотипе 1. Неудача в лечении проявляется или в виде отсутствия ответа на лечение (минимальное снижение титров вируса), или в развитии рецидива (первоначальный четкий ответ на лечение сменяется восстановлением титров вируса во время или после лечения).
С целью спецификации нон-респондерами предпочтительно называют пациентов, у которых отсутствует снижение вирусной нагрузки на <2 log10 МЕ/мл (т.е. в 100 раз) при введении рибавирина/интерферона (обычно пэгинтерферона α), предпочтительно в течение 12 недель. В предпочтительном варианте осуществления настоящего изобретения у нон-респондеров титры вируса снижаются на величину ≤2,1 log10 МЕ/мл и абсолютные титры ≥4,62 log10 МЕ/мл при минимальной величине.
С целью спецификации частичными респондерами предпочтительно называют пациентов, у которых отсутствует снижение вирусной нагрузки на ≥2 log10 МЕ/мл к 12 неделе при выявляемой ВГС РНК на 24 неделю.
С целью спецификации больными с рецидивом предпочтительно называют пациентов, у которых снижение титров вирусов составляет ≥2,8 log10 и абсолютные титры временно падают ниже предела обнаружения (2,78 log10 МЕ/мл).
В настоящем описании понятие «лекарственная форма» предпочтительно является синонимом понятию «вводимая форма» или «дозированная форма». Например, если лекарственная форма предназначена для перорального введения, например, в форме таблетки, такая таблетка предпочтительно представляет дозированную форму для введения, которая содержит дозу компонента силибинина, предназначенную для введения в соответствующее время в рамках схемы введения. Если дозированная единица включает одну таблетку, дозированная единица соответствует вводимой форме. Однако дозированная форма также может быть поделена на ряд вводимых форм, например, на ряд таблеток, которые в каждом случае содержат только часть дозы, но вместе они содержат целую дозу компонента силибинина, предназначенную для введения в соответствующее время в рамках схемы введения (такие таблетки дозированной единицы предназначены для практически одновременного введения).
В настоящем изобретении понятие «силибининовый компонент» предпочтительно относится к силибинину, включая все его стереоизомеры, например силибинин А и силибинин В, его фармацевтически приемлемые соли и/или производные, в частности сложные эфиры. Предпочтительными сложными эфирами являются производные неорганических кислот, например фосфорной кислоты или серной кислоты; или органических кислот, например муравьиной кислоты, уксусной кислоты, пропионовой кислоты, лимонной кислоты, яблочной кислоты, миндальной кислоты и др.
Среди гемиэфиров дикарбоновых кислот особенно предпочтительны гемиэфиры, например, яблочной кислоты, глутаровой кислоты, янтарной кислоты, адипиновой кислоты, суберовой кислоты, азелаиновой кислоты, себациновой кислоты, фумаровой кислоты, малеиновой кислоты, итаконовой кислоты, фталевой кислоты, терефталевой кислоты, изофталевой кислоты и др. Предпочтительными гемиэфирами являются дигемисукцинаты, которые могут содержаться в виде свободных кислот или их солей, например солей натрия, калия или аммония. Одна или несколько гидроксильных групп силибинина может быть этерифицирована. Предпочтительно, 1, 2, 3, 4 или все гидроксильные группы силибинина этерифицированы.
В предпочтительном варианте осуществления настоящего изобретения силибининовым компонентом является силибинин-С-2',3-бис(гидрогенсукцинат) или его фармацевтически приемлемая соль, например натриевые соли, калиевые соли, соли аммония и др., а также их смеси. Особо предпочтительна динатриевая соль.
Соответствующими сложными эфирами являются также сложные эфиры глюконовой кислоты.
Предпочтительно силибининовый компонент представляет соединение с общей формулой (I)
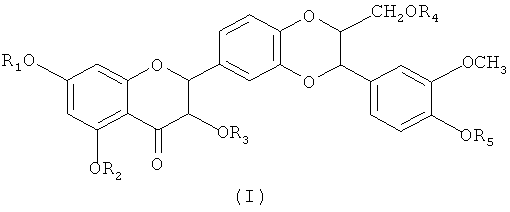
в которой
R1, R2, R3, R4 и R5 независимо друг от друга выбраны из группы, состоящей из -Н, -SO3H, -PO3H2, -СО-С1-С8-алкилен-ОН, -СО-С1-С8-алкилен-CO2H, -СО-С1-С8-алкилен-SO3H, -СО-С1-С8-алкилен-OPO3H2, -СО-С1-С8-алкилен-PO3H2, -(С2-С3-алкилен-O)n-Н, где n= от 1 до 20, -СО-С1-С8-алкилен-N(С1-С3-алкил)3 +Х-, где X- представляет фармацевтически допустимый анион,
или их фармацевтически допустимые соли. Предпочтительно, R1, R2 и R5 представляют -Н.
Более предпочтительно, силибининовый компонент общей формулы (I) имеет стереохимическую общую формулу (I-A) или (I-Б)
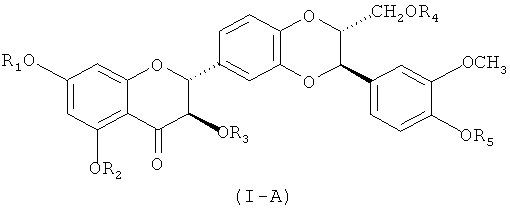
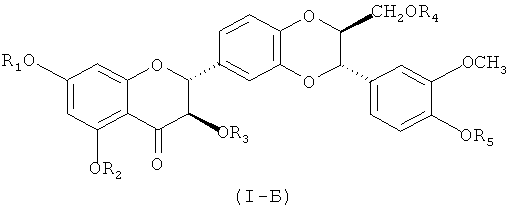
В предпочтительном варианте осуществления настоящего изобретения соединение общей формулы (I-A) перемешивают с соединением общей формулы (I-Б) в каком-либо относительном соотношении массы, например 50±5:50±5. В предпочтительном варианте осуществления настоящего изобретения, однако, диастериомерный избыток (ди) соединения общей формулы (I-A) составляет по меньшей мере 50% ди, более предпочтительно по меньшей мере 75% ди, еще более предпочтительно по меньшей мере 90% ди, еще более предпочтительно по меньшей мере 95% ди, наиболее предпочтительно по меньшей мере 98% ди и особенно предпочтительно по меньшей мере 99% ди. В другом предпочтительном варианте осуществления настоящего изобретения диастериомерный избыток (ди) соединения общей формулы (1-Б) составляет по меньшей мере 50% ди, более предпочтительно по меньшей мере 75% ди, еще более предпочтительно по меньшей мере 90% ди, еще более предпочтительно по меньшей мере 95% ди, наиболее предпочтительно по меньшей мере 98% ди и особенно предпочтительно по меньшей мере 99% ди.
Другие предпочтительные силибининовые компоненты описаны в патенте WO 03/090741, на сущность которого в настоящем описании приводится ссылка.
Предпочтительно силибининовый компонент в чистой воде при комнатной температуре имеет лучшую растворимость по сравнению с силибинином как таковым.
В предпочтительном варианте осуществления настоящее изобретение относится к применению сложного эфира силибинина для получения лекарственного средства, которое предпочтительно перерабатывают для парентерального или перорального введения, для лечения вирусного гепатита, в частности гепатита В или С. Предпочтительно лекарственное средство практически не содержит силидианина, и/или силикристина, и/или изосилибинина.
В предпочтительном варианте осуществления настоящего изобретения лекарственное средство перерабатывают для парентерального введения. Парентеральное введение может проводиться, например, подкожно, внутривенно, внутримышечно, внутриартериально, внутрибрюшинно, внутрикожно, внутрисуставно, подоболочечно, внутрисердечно, в стекловидное тело глаза, ретробульбарно, внутрилегочно и внутрикостно.
Особенно предпочтительно лекарственное средство перерабатывают для инъекции или инфузии, в частности для внутривенного или внутриартериального введения.
Соответствующими лекарственными средствами, применимыми для инъекции или инфузии, известны специалистам в данной области. Подробнее см., например, кн.: К.Н.Bauer и др. «Lehrbuch der Pharmazeutischen Technologie [Textbook of Pharmaceutical Technology]», 1999, 6-е изд., WVG Stuttgart.
Лекарственные средства, применимые для инъекций, представляют обычные стерильные растворы, эмульсии или суспензии, которые получают растворением, эмульгированием или суспендированием действующего вещества и необязательно также эксципиентов в воде, в соответствующей жидкости помимо воды, которая не должна стерилизоваться, если этому есть обоснование, или в смеси этих растворителей.
Лекарственные средства для инфузии представляют обычные стерильные водные растворы или эмульсии с водой в качестве постоянной фазы.
Лекарственные средства для инъекции или инфузии могут необязательно содержать дополнительные эксципиенты. Эксципиентами этого типа предпочтительно являются растворители, например лецитин и полоксамер 188, вещества для придания изотоничности, например натрий хлорид, глюкоза и маннит, буферы, например, ацетатный, фосфатный и цитратный, антиоксиданты, например аскорбиновая кислота, натрий метагидрогенсульфит, натрий сульфит и натрий гидрогенсульфит, хелатирующие агенты, например динатриевый эдитат, консерванты, например, эфиры гидроксибензойной кислоты, бензиловый спирт и холестерин, а также эмульгаторы, например лецитин, жирные спирты, стеролы, эфиры сорбита и жирных кислот, полиоксиэтиленовые эфиры сорбита и жирных кислот, полиоксиэтиленовые глицериды жирных кислот, полиоксиэтиленовые эфиры жирных кислот, полиоксиэтиленовые эфиры жирных спиртов, эфиры глицерина и жирных кислот и полоксамеры.
Особенно предпочтительным лекарственным средством является порошок для приготовления раствора для инфузии, включающего силибинин-С-2',3-бис(гидрогенсукцинат) предпочтительно в виде динатриевой соли, и необязательно инулин в качестве эксципиента. Контейнеры, содержащие 598,5 мг порошка силибинина-С-2',3-бис(гидрогенсукцината) динатриевой соли и инулина, адаптированы для приготовления раствора для инфузии и производятся в Германии под торговой маркой Legalon® SIL. В предпочтительном варианте осуществления настоящего изобретения лекарственное средство по настоящему изобретению биоэквивалентно этому составу.
В другом предпочтительном варианте осуществления настоящего изобретения лекарственное средство переработано для перорального введения. Предпочтительно лекарственное средство представляет форму для перорального введения, выбранную из группы, состоящей из таблеток, капсул, таблеток с оболочкой из сахара, пилюль и саше.
При введении силибининового компонента пероральным путем следует убедиться, что биодоступность компонента силибинина в пероральной дозированной форме достаточно высокая. Поэтому ограничивающим фактором является выраженная липофильность силибинина.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к применению силибининового компонента для получения лекарственного средства, которое переработано для перорального введения и практически не содержит силидианина и/или силикристина, и/или изосилибинина, для лечения вирусного гепатита, предпочтительно гепатита В или С.
Представляется, что эти дополнительные компоненты силимарина также обладают физиологическим действием (например, могут вызывать побочные эффекты), но для лечения вирусного гепатита силибинин (или его аналоги) наиболее эффективен, особенно для снижения вирусной нагрузки. Таким образом, при введении силимарина, т.е. смеси силибинина, силидианина, силикристина, изосилибинина и других компонентов, общая доза силимарина должна быть относительно высокой для обеспечения определенного количества силибинина. Например, если силимарин содержит, например, 42 мас.% силибинина, введение 125 мг силимарина обеспечивает только примерно 52 мг силибинина и примерно 73 мг других соединений, также обладающих физиологическим действием (но не требуемым эффектом). Риск нежелательных побочных эффектов возрастает вместе с дозой физиологически активного вещества. Таким образом, поскольку осложнением является профиль нежелательных побочных эффектов, введение 52 мг в высокой степени чистого силибинина превосходит введение 125 мг силимарина с содержанием силибинина 42 мас.% (см. Т.Ding и др., J.Pharm. Biomed. Anal. 26(1), 2001, сс.155-161).
Структуры силибинина (силибина), силидианина, силикристина и изосилибинина (изосилибина), описанные ниже, приводятся по работам D.Y.-W. Lee и др., J. Nat. Prod. 66, 2003, сс.1171-1174; N.-C. Kim и др., Org. Biomol. Chem., 1, 2003, сс.1684-1689):


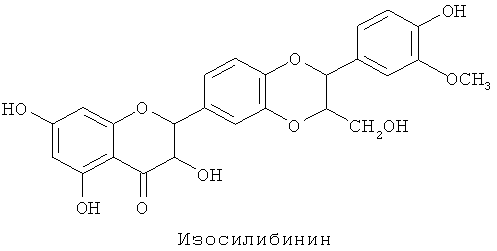
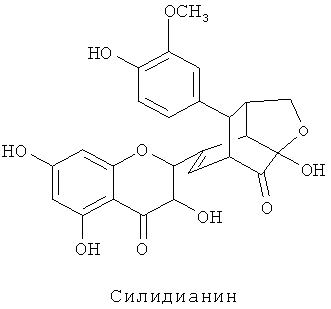
Соответствующие формы для введения, которые применимы для перорального введения (пероральных лекарственных средств), известны специалистам в данной области. Подробнее см., например, кн.: К.Н.Bauer и др. «Lehrbuch der Pharmazeutischen Technologie [Textbook of Pharmaceutical Technology]», 1999, 6-е изд., WVG Stuttgart.
Форма перорального введения предпочтительно выбрана из группы, состоящей из таблеток, порошков, пилюль, гранул, таблеток с покрытием из сахара, сиропов, соков, растворов, шипучих порошков, шипучих гранул, шипучих таблеток, лиофилизатов и капсул. Особенно предпочтительной формой перорального введения является таблетка, таблетка с покрытием из сахара, гранулы, пилюли или порошки, особенно предпочтительно таблетки.
Соответствующие эксципиенты для составов в формах перорального введения известны специалистам в данной области. См., например, Н.P.Fiedler, Lexikon der Hilfstoffe für Pharmazie, Kosmetik und angrenzende Gebiete [Encyclopedia of excipients for pharmacy, cosmetics и related areas], Editio Cantor Aulendorf, 2001.
Таблетки могут быть получены, например, путем смешивания силибининового компонента с известными эксципиентами, например инертными разбавителями, например, кальцием карбонатом, кальцием фосфатом и лактозой, разрыхлителями, например кукурузным крахмалом и альгиновой кислотой, связующими, например крахмалом и желатином, смазывающими агентами, например магнием стеаратом или тальком, и/или агентами для достижения эффекта депо, например, карбоксиметилцеллюлозой, ацетатфталатом целлюлозы или поливинилацетатом. Таблетки могут также состоять из ряда слоев. Помимо указанных растворителей таблетки также могут содержать добавки, например натрий цитрат, кальций карбонат и дикальций фосфат, вместе с различными дополнительными веществами, например крахмалом, предпочтительно картофельным крахмалом, желатином и др. Кроме того, для таблетирования могут дополнительно применяться агенты скольжения, например магний стеарат, натрий лаурилсульфат и тальк.
Таблетки с покрытием из сахара могут быть получены, например, нанесением покрытия на сердцевины, которые получают способом, близким к способу получения таблеток с агентами, обычно применяемыми для получения покрытий из сахара для таблеток, например, коллидона или шеллака, гуммиарабика, талька, диоксида титана или сахара. Чтобы избежать эффекта депо или несовместимости, сердцевина также может состоять из ряда слоев. Таблетки с покрытием из сахара также могут состоять из ряда слоев для получения эффекта депо, причем их можно получить, используя указанные выше эксципиенты для таблеток.
Соки, сиропы, эмульсии, суспензии и растворы для перорального введения могут дополнительно содержать подсластитель, например сахарин, цикламат, глицерин или сахар, а также вкусовой агент, например ароматизатор, например ванилин или экстракт апельсина. Кроме того, они могут содержать дополнительные агенты для получения суспензии или загустители, например натриевую соль карбоксиметилцеллюлозы, увлажняющие агенты, например, продукты конденсации жирных спиртов с оксидом этилена, или консерванты, например эфиры p-гидроксибензойной кислоты.
Капсулы могут быть получены, например, перемешиванием силибининового компонента с инертными носителями, например лактозой или сорбитом, и помещением в желатиновые капсулы. Эксципиентами, которые могут быть использованы, являются, например, вода, фармацевтически приемлемые органические растворители, например парафины (например, фракции нефти), масла растительного происхождения (например, арахисовое или кунжутное), моно- или полифункциональные спирты (например, этанол или глицерин), растворители, например природные минералы (например, каолины, глины, тальк, мел), измельченные синтетические материалы (например, высокодисперсные кремниевая кислота и силикаты), сахара (например, сахароза, лактоза и декстроза), эмульгаторы (например, лигнин, сульфитно-спиртовая барда, метилцеллюлоза, крахмал и поливинилпирролидон) и смазывающие агенты (например, магний стеарат, тальк, стеариновая кислота и натрий лаурит сульфат).
Лекарственное средство может выделять силибининовый компонент немедленно или из контролируемой формы. Если происходит высвобождение из контролируемой формы, предпочтительно такой формой является формаретарда. Замедленное выделение в настоящем изобретении предпочтительно подразумевает профиль высвобождения, по которому силибининовый компонент высвобождается на протяжении относительно длительного перида с пониженной скоростью для пролонгированного терапевтического действия. Это может быть, в частности, достигнуто при пероральном введении. Выражение «с по меньшей мере частично замедленным высвобождением» по настоящему изобретению включает какое-либо лекарственное средство, которое гарантирует модифицированное высвобождение содержащегося в лекарственной форме компонента силибинина. Лекарственные средства предпочтительно в формах введения с покрытием или без покрытия, которые получают, используя специальные эксципиенты, по определенным процессам или путем комбинирования обеих форм, для избирательно модифицированной скорости высвобождения или места высвобождения. В связи с длительностью курса высвобождения в случае лекарственных средств по настоящему изобретению включены следующие типы: отсроченное высвобождение (продленное высвобождение), высвобождение повторного действия, пролонгированное высвобождение и устойчивое высвобождение. Подробнее см., например, кн.: К.Н.Bauer и др. «Lehrbuch der Pharmazeutischen Technologie [Textbook of Pharmaceutical Technology]», 1999, 6-е изд., WVG Stuttgart.
Соответствующие измерения контролируемого высвобождения действующего соединения известны специалистам в данной области. Если лекарственное средство в форме для перорального введения, например в форме таблетки, отсроченное высвобождение может быть достигнуто, например, погружением силибининового компонента в полимерную матрицу и/или пленочное покрытие формы перорального введения с мембраной.
В настоящем изобретении могут применяться твердые, полутвердые или жидкие лекарственные средства с контролируемым типом высвобождения. Твердые лекарственные средства предпочтительны, например пероральные осмотические системы, таблетки с покрытием, матричные таблетки, многослойные таблетки, джеккет-таблетки, джеккет-таблетки с покрытием из сахара, пилюли с контролем диффузии, адсорбаты и мягкие желатиновые капсулы-депо. Пероральные лекарственные средства с контролируемым высвобождением действующего соединения особенно предпочтительны в виде таблеток с покрытием (филм-таблеток), джеккет-таблеток или матричных таблеток, особенно предпочтительны матричные таблетки.
Лекарственные средства с контролируемым высвобождением действующего вещества могут содержать силибининовый компонент в растворимой, суспендированной и/или твердой, аморфной или кристаллической форме.
Для получения лекарственных форм с контролируемым высвобождением действующего соединения по настоящему изобретению с контролируемым высвобождением действующего соединения, силибининовый компонент может применяться в виде частиц разного размера, например неизмельченных, измельченных частиц или микроформы.
В лекарственных средствах с контролируемым высвобождением действующее соединение, силибининовый компонент, предпочтительно содержится в форме частиц, содержащих действующее вещество, например, пилюль, гранул, микрокапсул, таблеток, экструдатов или кристаллов, которые покрыты мембраной, контролирующей диффузию.
Такие лекарственные средства с контролируемой диффузией предпочтительно состоят из многих частиц, т.е. они предпочтительно состоят из множества сердцевин с покрытием, например, нейтральных пилюль, на которые наносят смесь силибининового компонента с обычным связующим и загустителем, необязательно вместе с обычными смягчителями и растворителями, и затем их покрывают глазурью для диффузии, смягчителем и другими эксципиентами. Лекарственные средства с контролируемой диффузией по настоящему изобретению, кроме того, могут состоять из гомогенных сердцевин, включающих силибининовый компонент, которые получают, например, путем гранулирования, роторного гранулирования, агломерирования в псевдоожиженном слое, таблетирования, влажной экструзией или экструзией плавления, необязательно с приданием сферической формы, и покрывают глазурью для диффузии, который может содержать смягчители и другие эксципиенты.
Частицы, содержащие силибининовый компонент, могут содержать эксципиенты, например кислоты или буферные вещества, которые модифицируют pH и посредством этого влияют на снижение зависимости высвобождения силибининового компонента от pH среды высвобождения.
Контролирующая диффузию мембрана может также включать дополнительные эксципиенты, которые за счет pH-зависимой растворимости влияют на проницаемость мембраны при разных величинах pH и таким образом влияют на минимизирование зависимости высвобождения силибининового компонента от pH.
Связующими и загустителями, применяемыми для получения нейтральных пилюль с покрытием, предпочтительно являются гидроксипропилметилцеллюлоза (ГПМЦ) и поливинилпирролидон (ПВП). Сходным образом могут быть использованы другие природные, синтетические или частично синтетические полимеры, например метилцеллюлоза (МЦ), гидроксипропилцеллюлоза (ГПЦ), другие гидроксиалкилцеллюлозы и гидроксиалкилметилцеллюлозы, карбоксиметилцеллюлозы и их соли, полиакриловые кислоты, полиметакрилаты, желатин, крахмал и производные крахмала.
Для получения пилюль, частиц и (мини)таблеток, содержащих силибининовый компонент, предпочтительно применяют целлюлозу, микрокристаллическую целлюлозу, производные целлюлозы, например ГМПЦ, ГПЦ и гидроксипропилцеллюлозу с низкой степенью замещения (ГПЦ-нсз), дикальциевый фосфат, лактозу, ПВП и сахарозу, в качестве связующих и наполнителей, методами гранулирования, агломерации в псевдоожиженном, слое, влажной экструзии и таблетирования.
Для получения пилюль экструзией плавления силибининовый компонент погружают в термопластические эксципиенты. Предпочтительно соответствующими термопластическими эксципиентами предпочтительно являются ГПЦ, ГПМЦ, этилцеллюлоза, ацетосукцинат гидроксипропилметилцеллюлозы, ПВП, сополимер винилпирролидона/винилацетата, полиэтиленгликоль, полиэтиленоксид, полиметакрилаты, поливиниловые спирты, частично гидролизированный поливинилацетат, полисахариды, например альгиновая кислота, альгинаты, галактоманнаны, воски, жиры и производные жирных кислот.
В частицах, которые содержат силибининовый компонент, также могут быть включены pH-модифицирующие вещества, например кислоты, основания и буферные вещества. Добавлением таких веществ можно существенно снизить зависимость высвобождения силибининового компонента и его солей, гидратов, сольватов от pH.
Эксципиентами, которые используют для модификации pH в сердцевинах, содержащих силибининовый компонент, являются, например, адипиновая кислота, яблочная кислота, L-аргинин, аскорбиновая кислота, аспарагиновая кислота, бензолсульфоновая кислота, бензойная кислота, янтарная кислота, лимонная кислота, этансульфоновая кислота, 2-гидроксиэтансульфоновая кислота, фумаровая кислота, глюконовая кислота, глюкороновая кислота, глутаминовая кислота, гидрогентартран калия, малеиновая кислота, малоновая кислота, метансульфоновая кислота, толуолсульфоновая кислота, трометамол, винная кислота. Предпочтительно используют лимонную кислоту, янтарную кислоту, винную кислоту и гидрогентартрат калия.
Для получения глазури для диффузии особенно предпочтительными являются этилцеллюлозы (например, продукты Aquacoat® или Surelease®) и полиметакрилаты (например, продукты Eudragit® NE, Eudragit® RS и RL). Однако другие материалы, например ацетат целлюлозы и ацетобутират целлюлозы, также могут применяться в качестве формирующих пленочное покрытие контролирующих диффузию полимеров.
Помимо контролирующего диффузию полимера, распыленная глазурь также может содержать дополнительные эксципиенты с pH-зависимой растворимостью, например полимеры кишечного растворения, например фталат целлюлозы, в частности ацетофталат целлюлозы и фталат гидроксипропилметилцеллюлозы, сукцинаты целлюлозы, в частности ацетосукцинат целлюлозы и ацетосукцинат гидроксипропилметилцеллюлозы или полиметакрилаты (например, продукт Eudragit® L). Путем добавления таких веществ можно понизить зависимость высвобождения силибининового компонента от pH.
Применяемыми смягчителями являются, например, производные лимонной кислоты, производные фталевой кислоты, бензойная кислота и эфиры бензойной кислоты, другие эфиры ароматических карбоновых кислот, эфиры алифатических дикарбоновых кислот, моноацетат-, диацетат- и триацетат глицерина, полиолы, жирные кислоты и их производные, глицериды ацетилированных жирных кислот, касторовое масло и другие природные масла, миглиол и спирты жирных кислот.
Для предупреждения слипания частиц с покрытием во время процесса и в конечном продукте, к глазури могут добавляться агенты понижения вязкости, например тальк, магний стеарат, моностеарат глицерина и аэросил.
Скорость высвобождения контролируют составом глазури и толщиной слоя глазури. Добавками, повышающими проницаемость покрытия, являются агенты формирования пор, которые могут быть добавлены к глазури или к частицам, на которые наносят покрытие и которые содержат силибининовый компонент. Агенты формирования спор - растворимые полимеры, например полиэтиленгликоли, ПВП, ПВА, ГПМЦ, ГПЦ, гидроксиэтилцеллюлозы (ГЭЦ), МЦ, карбоксиметилцеллюлозы и их соли, декстрины, мальтдекстрины, циклодекстрины, декстраны или другие растворимые вещества, например мочевина, натрий хлорид, калий хлорид, аммоний хлорид, сахароза, лактоза, глюкоза, фруктоза, мальтоза, маннит, сорбит, ксилит и лактит.
Эксципиентами с pH-зависимой растворимостью, которые могут быть компонентами диффундирующего покрытия, являются, например, кишечно-растворимые полимеры, например фталаты целлюлозы, в частности ацетофталат целлюлозы и фталат гидроксипропилметилцеллюлозы, сукцинаты целлюлозы, в частности ацетосукцинат целлюлозы и ацетосукцинат гидроксипропилметилцеллюлозы и полиметакрилаты (например, продукт Eudragit® L).
Кроме того, лекарственное средство с контролируемым высвобождением силибининового компонента может быть формой для введения с покрытием, которая содержит один или несколько набухающих эксципиентов, которые сильно увеличиваются при проникновении жидкости через мембрану и вызывают разрыв оболочки в качестве результата набухания и увеличения объема. В результате разрыва оболочки высвобождение фармацевтического агента из лекарственного средства становится возможным (пульсирующее высвобождение). Такие лекарственные средства в качестве набухающих эксципиентов предпочтительно содержат поливинилпирролидоны, кроспивидоны, перекрестно связанную натриевую соль карбоксиметилцеллюлозы, перекрестно связанную натриевую соль карбоксиметилкрахмала, полиэтиленоксиды, полиметакрилаты, гидроксипропилцеллюлозу с низкой степенью замещения (ГПЦ-нсз). Соответствующими покровными материалами предпочтительно являются ацетат целлюлозы, этилцеллюлоза и полиметакрилаты.
Лекарственные средства с покрытием, контролируемой диффузией и пульсирующим высвобождением могут применяться непосредственно в качестве готовой фармацевтической формы. Они, однако, также могут быть дополнительно процессированы, необязательно с добавлением эксципиентов, для получения конечной формы введения (например, капсулы, таблетки, саше). Для достижения желаемого профиля высвобождения, различные частицы с покрытием также могут комбинироваться с другими частицами в фармацевтическую форму, и начальная доза может вводиться, например, комбинированием частиц быстрого высвобождения, например пилюль без покрытия, гранул или порошков.
Лекарственными средствами с контролируемым высвобождением, которые могут применяться, также являются составы, которые содержат силибининовый компонент в матрице. Такие матричные составы высвобождают силибининовый компонент диффузией и/или эрозией. Предпочтительно эти лекарственные средства содержатся в форме таблетки или ряда таблеток, которые, например, могут быть инкапсулированы. Таблетки могут иметь покрытие (филм-таблетки) или лакировку. Такие лекарственные средства получают, например, смешиванием компонентов и прямым таблетированием, или сухим или влажным гранулированием с последующим таблетированием.
Агенты, формирующие матрицу, могут быть водорастворимыми, разбухающими в воде или водонерастворимыми веществами. Предпочтительно лекарственные средства содержат одно или несколько разбухающих в воде полимеров.
Применяемыми водорастворимыми и разбухающими в воде полимерами, формирующими матрицу, предпочтительно являются гидроксипропилметилцеллюлоза (ГПМЦ), гидроксиэтилметилцеллюлозы, гидроксипропилцеллюлозы (ГПЦ), гидроксиэтилцеллюлозы, метилцеллюлозы (МЦ), этилцеллюлозы, другие алкилцеллюлозы, гидроксиалкилцеллюлозы и гидроксиалкилметилцеллюлозы, натриевая соль карбоксиметилцеллюлозы, альгинаты, галактоманнаны, например гауровая камедь и мука бобов рожкового дерева, ксантаны, полиэтиленоксиды, полиакриловые кислоты, полиметакрилатные кислоты, производные полиметакрилатной кислоты, поливиниловые спирты (ПВС), частично гидролизированный поливинилацетат, поливинилпирролидон, агар, пектин, гуммиарабик, трагакант, желатин, крахмал или производные крахмала и смеси указанных веществ. Применение ГПМЦ особенно предпочтительно.
Кроме того, водонерастворимые вещества могут применяться в качестве агентов, формирующих структуру, например, ненасыщенные или насыщенные (гидрогенированные) жирные кислоты и их соли, сложные эфиры или амиды, моно-, ди- и триглицериды жирных кислот, воска, керамиды, производные холестерина и смеси этих веществ.
Лекарственные средства, кроме того, могут содержать обычные эксципиенты для таблетирования, предпочтительно высокодисперсный кремний (продукт Aerosil®), магний стеарат, тальк, ПВП, лактозу или микрокристаллическую целлюлозу.
Кроме того, вещества могут быть внедрены в матрицу, которые контролируют pH в матрице. Добавлением таких модифицирующих pH эксципиентов и/или добавлением веществ, которые повышают pH или вымываются растворением из матрицы и таким образом повышают пористость или проницаемость матрицы и/или индуцируют эрозию матрицы, возможно для таких предпочтительных вариантов настоящего изобретения достичь в наибольшей степени pH-независимого высвобождения.
Матрица, содержащая силибининовый компонент, также может быть в специальных геометрических формах, причем высвобождение из матрицы зависит от специальной геометрии и поверхности матрицы. Поверхность матрицы и высвобождающая поверхность могут контролироваться, например, сжатием для получения специальных форматов (например, кольцеобразных таблеток), и/или нанесением подзоны, или нанесением барьерных слоев с помощью многослойного пресса.
Составы с разными свойствами высвобождения могут предпочтительно комбинироваться для получения фармацевтической формы в виде многослойных таблеток или таблеток с джаккет-сердцевиной. Например, с помощью многослойных таблеток, включающих слой быстрого высвобождения, или таблеток с джаккет-сердцевиной, имеющих оболочку быстрого высвобождения, достигается контролируемое высвобождение по настоящему изобретению с высоким первоначальным высвобождением силибининового компонента, хотя может быть достигнуто с помощью таблеток с джаккет-сердцевиной с быстро высвобождающейся сердцевиной и повышенным высвобождением в конце.
Другим лекарственным средством с контролируемым высвобождением силибининового компонента является лекарственное средство, в котором силибининовый компонент добавляют в матрицу, состоящую из одного или нескольких физиологически приемлемых эксципиентов процессом плавления. Высвобождение силибининового компонента из таких «сплавленных экструдатов» происходит за счет диффузии и/или эрозии. Предпочтительно такие составы с контролируемым высвобождением силибининового компонента имеют форму гранул, пилюль или таблеток. К формам, полученным экструзией плавления, относятся, в частности, пилюли и гранулы, которые могут быть процессированы для получения других фармацевтических форм, например, путем инкапсулирования или таблетирования, необязательно с добавлением других традиционных фармацевтических эксципиентов. Кроме того, сплавленные экструдаты по настоящему изобретению могут быть измельчены и впоследствии применены в такой измельченной форме для получения других лекарственных средств, например матричных таблеток. Дополнительный процессинг также включает комбинацию составов, имеющих разное фармацевтическое высвобождение, например, ретард-частицы и частицы быстрого высвобождения, для получения лекарственного средства.
На сплавленные экструдаты и/или фармацевтические формы, которые получают из сплавленных экструдатов, может быть нанесено покрытие или они могут быть лакированы. Сплавленные экструдаты предпочтительно получают смешиванием силибининового компонента по меньшей мере с одним плавким физиологически приемлемым (носителем) и необязательно обычными дополнительными фармацевтическими веществами, плавящимися при температуре от 50 до 250°С, предпочтительно 60 до 200°С, впрыскиванием расплава или экструдата и приданием формы. При таком способе смешивание компонентов может производиться до плавления или во время плавления, или некоторые из компонентов сплавляют и другие компоненты добавляют к этому расплаву. Смесь растворителей, силибининового компонента и необязательно дополнительных веществ поддается термопластической деформации и, следовательно, может быть экструдирована. Многочисленные методы, исходя из их названий, дают представление о способе придания формы смеси, например горячее гранулирование, холодное гранулирование, каландрирование, экструзия и деформация все еще пластичной массы или придание округлой формы.
Используемыми термопластическими носителями, которые предпочтительно набухают и растворяются в физиологических средах, предпочтительно являются: поливинилпирролидон (ПВП), сополимеры N-винилпирролидона (NВП) и виниловых эфиров, в частности винилацетат, сополимеры винилацетата и кротоновой кислоты, частично гидролизованный поливинилацетат, поливиниловый спирт, сложные эфиры целлюлозы, в частности метилцеллюлоза и этилцеллюлоза, гидроксиалкилцеллюлозы, в частности гидроксипропилцеллюлоза, гидроксиалкилметилцеллюлозы, в частности гидроксипропилметилцеллюлозы, и гидроксиэтилметилцеллюлоза, карбоксиметилцеллюлозы, фталаты целлюлозы, в частности ацетатфталат целлюлозы и фталат гидроксипропилметилцеллюлозы, сукцинат целлюлозы, в частности ацетосукцинат целлюлозы и ацетосукцинат гидроксипропилметилцеллюлозы, полигидроксиалкилакрилаты, полигидроксиалкилметакрилаты, полиакрилаты и полиметакрилаты (продукты типа Eudragit®), сополимеры метилметакрилата и акриловой кислоты, полилактиды, полиэтиленгликоли, полиэтиленоксиды и полисахариды, например галактоманнаны и альгиновая кислота и ее соли щелочных металлов и аммония.
Предпочтительными термопластическими эксципиентами для получения лекарственных средств с контролируемым высвобождением силибининового компонента являются гиброксипропилцеллюлоза, поливинилпирролидон, сополимеры винилпирролидона/винилацетата, полиметакрилаты, в частности продукт Eudragit® L, ацетосукцинат гидроксипропилметилцеллюлозы, полиэтиленгликоли, полиэтиленоксиды и их смеси. Смягчающими эксципиентами, которые могут применяться для снижения температуры стеклования смеси, являются, например, пропиленгликоль, глицерин, триэтиленгликоль, бутандиолы, пентанолы, например, пентаэритритол, гексанолы, длинноцепочечные спирты, полиэтиленгликоли, полипропиленгликоли, полиэтилен/полипропиленгликоли, силиконы, производные фталевой кислоты (например, диметилфталат, диэтилфталат, дибутилфталат), бензойная кислота и эфиры бензойной кислоты, другие эфиры ароматических карбоновых кислот (например, эфиры тримеллитовой кислоты), производные лимонной кислоты (например, триэтилцитрат, трибутилцитрат, ацетилтриэтилцитрат), эфиры алифатических дикарбоновых кислот (например, диалкиладипаты, эфиры себациновой кислоты, в частности диэтилсебацинаты, эфиры винной кислоты), моноацетат глицерина, диацетат глицерина, триацетат глицерина, жирные кислоты и производные (например, моностеараты глицерина, ацетилированные глицериды жирных кислот, касторовое масло и другие природные масла, миглиол), спирты жирных кислот (например, цетиловый спирт, цетеариловый спирт), сахара, многоатомные спирты и производные сахаров (например, эритритол, изомальтит, лактит, маннит, мальтит, мальтдекстрин, ксилитол).
Помимо силибининового компонента, носителя (носителей) и необязательно смягчителя (смягчителей), экструдируемая смесь может содержать также другие фармацевтические традиционные дополнительные вещества, например агенты скольжения и агенты высвобождения смазки, агенты скольжения и агенты текучести, наполнители и адсорбенты, стабилизаторы, ловушки свободных радикалов, комплексообразующие агенты, антиоксиданты, фотостабилизаторы, пропелланты, поверхностно-активные вещества, консерванты, красители, подсластители и ароматизаторы.
Агенты скольжения и смазки для форм могут включать, например, стеариновую кислоту и стеараты, в частности стеараты алюминия, кальция и магния, кальций бегенат, натрий стеарилфумарат, тальк, силиконы, воски, и моно-, ди- и триглицериды, например моностеарат глицерина, дистеарат глицерина, дибегенат глицерина, моноолеат глицерина, пальмитинстеарат глицерина.
Применяемыми агентами текучести предпочтительно являются животные и растительные масла, предпочтительно в гидрогенированной форме с точкой плавления по меньшей мере 50°С, воски (например, карнаубский воск), моно-, ди- и триглицериды (например, моностеарат глицерина, дистеараты глицерина, дибегенат глицерина, моноолеат глицерина, пальмитостеарат глицероила), фосфатиды, в частности лецитин.
Применяемыми веществами-наполнителями, например, являются диоксид титана, оксид алюминия, оксид магния, кремниевая кислота и силикаты, стеариновая кислота и стеараты, производные целлюлозы (например, метилцеллюлоза), крахмал и производные крахмала, сахара, многоатомные спирты и производные сахаров.
Лекарственные средства с контролируемым высвобождением силибининового компонента также могут быть сплавленными экструдатами, которые содержат эксципиента с pH-модифицирующими свойствами и/или pH-зависимой растворимостью. С помощью этих эксципиентов (например, кислот, оснований, буферных веществ кишечно-растворимых полимеров, уже описанных выше) можно минимизировать зависимость высвобождения силибининового компонента от pH.
При получении сплавленных экструдатов может быть формирование «твердых растворов», в которых силибининовый компонент содержится в матрице в молекулярно-дисперсной форме.
Лекарственные средства с контролируемым высвобождением силибининового компонента также могут быть осмотическими фармацевтическими системами высвобождения. В принципе осмотические системы этого типа известны в предшествующем уровне техники. В настоящем изобретении фармацевтическое высвобождение из фармацевтической формы обычно основано на осмотическом давлении в качестве движущей силы.
Осмотическая система предпочтительно состоит из сердцевины, которая содержит силибининовый компонент, необязательно гидрофильный агент набухания и необязательно водорастворимое вещество для индукции осмоса и необязательно также фармацевтически приемлемые эксципиенты, и оболочки, которая состоит из водопроницаемого материала, который непроницаем для компонентов сердцевины и имеет по меньшей мере один выход, через который могут высвобождаться компоненты сердцевины.
Материал, из которого сформировано покрытие лекарственных средств по настоящему изобретению с контролируемым высвобождением силибининового компонента, сформирован из полупроницаемого, т.е. проницаемого для воды, водных сред и биологических жидкостей, и непроницаемого или весьма ограничено проницаемого для компонентов сердцевины, и пригоден для формирования пленочного покрытия. Избирательно полупроницаемый материал оболочки нерастворим в тканевых жидкостях, не разъедается, не разрушается в желудочно-кишечном тракте и выводится неизменным, или он подвергается биоэрозии только к концу периода высвобождения.
Типичными материалами для получения покрытий для осмотической системы предпочтительно являются производные ацилированной целлюлозы (сложные эфиры целлюлозы), которые являются от моно- до тризамещенных ацетильными группами или от моно- до дизамещенных ацетильными группами и дополнительно ацильным радикалом вместо ацетила, например ацетат целлюлозы, триацетат целлюлозы, ацетат целлюлозы/этилкарбамат, ацетофталат целлюлозы, ацетометилкарбонат целлюлозы, ацетосукцинат целлюлозы, ацетодиметиламиноацетат целлюлозы, ацетодиэтиламиноацетат целлюлозы, ацетоэтилкарбонат целлюлозы, ацетохлорацетат целлюлозы, ацетоэтилоксалатацетат целлюлозы, ацетометилсульфонат целлюлозы, ацетобутилсульфонат целлюлозы, ацетопропионат целлюлозы, ацетооктат целлюлозы, ацетолаурат целлюлозы, ацето-р-толуолсульфонат целлюлозы, ацетобутират целлюлозы и другие производные ацетата целлюлозы, а также ацетат агара и ацетат амилозы.
Пригодным полупроницаемым материалом мембраны осмотической системы также являются этилцеллюлоза, сополимеры алкиленоксида и эфира алкилглицидила, полимерные эпоксиды, полигликоли и производные полимолочной кислоты. Кроме того, смеси водонерастворимых акрилатов per se, например, могут быть применены сополимер этилакрилата и метилметакрилата.
При необходимости оболочка осмотической системы также может содержать смягчители, например смягчающие вещества, указанные выше, и другие дополнительные вещества, например агенты формирования пор. При необходимости фотозащитная глазурь может применяться для полупроницаемой оболочки, которая может состоять, например, из ГПМЦ и ГПЦ, и соответствующего смягчителя (например, полиэтиленгликоля) и пигментов (например, оксида титана, оксидов железа).
С целью осуществления контроля начальной дозы силибининового компонента, осмотическая система также может быть предусмотрена с покрытием, которое содержит силибининовый компонент, из которого силибининовый компонент предпочтительно быстро высвобождается при контакте с высвобождающей средой перед началом осмотически контролируемого высвобождения силибининового компонента из сердцевины.
Соответствующие набухающие в воде полимеры, которые могут содержаться в сердцевине осмотической системы, предпочтительно являются полиэтиленоксидами (например, продуктом Polyox®), ксантановой камедью, сополимерами винилпирролидона и винилацетата, поливинилпирролидонами, кросповидонами, перекрестно связанной натриевой солью карбоксиметилцеллюлозы, перекрестно связанной натриевой солью карбоксиметилкрахмала, гидроксипропилцеллюлозой с низкой степенью замещения (ГПЦ-нсз), поли(гидроксиалкилметакрилатом), альгинатами и галактоманнанами а также другими гидрофильными полимерными набухающими агентами и их смесями.
Соответствующими осмотически активными веществами, которые могут быть добавлены к сердцевине для индукции осмоса, являются водорастворимые соли органических и неорганических кислот или неионные органические вещества с высокой растворимостью в воде, например углеводы, в частности сахара, или аминокислоты. В качестве примера можно привести несколько веществ, которые могут быть включены в сердцевину осмотической системы отдельно или в смеси для индукции осмоса: неорганические соли, например хлориды, сульфаты, сульфиты, карбонаты, бикарбонаты, фосфаты, двузамещенные фосфаты, однозамещенные фосфаты щелочных металлов и щелочноземельных металлов, например натрия, лития, калия, кальция или магния, органические кислоты, например адипиновая кислота, аскорбиновая кислота, янтарная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, бензойная кислота и их соли щелочных или щелочноземельных металлов, ацетаты, пентозы, например арабиноза, рибоза или ксилоза, гексозы, например глюкоза, фруктоза, галактоза или манноза, и сахариды, например сахароза, мальтоза или лактоза, трисахариды, например раффиноза, многоатомные спирты, например маннит, сорбит, мальтит, ксилит или инозит, и мочевина. Предпочтительно используют натрий хлорид и натрий карбонат.
Кроме того, осмотическая система может включать другие обычные фармацевтические дополнительные вещества, например, смазывающие и разделяющие агенты, агенты скольжения, связующие, красители, загустители, защитные коллоиды, стабилизаторы и поверхностно-активные вещества.
Осмотическую систему высвобождения предпочтительно получают стандартными методами, например влажным гранулированием или сухим прессованием, таблетированием и последующим нанесением органического покрытия.
Покрытие осмотической системы имеет по меньшей мере один открытый выход, через который высвобождается силибининовый компонент необязательно вместе с другими компонентами сердцевины. Выход может быть сделан в оболочках разными способами, например перфорированием, механической обработкой или лазерным сверлением. Понятие «открытый» также включает биоразрушаемые материалы, которые выступают из оболочки при введении лекарственного средства по настоящему изобретению и в результате приводят к формированию открытых выходов in situ.
В другом варианте осуществления настоящего изобретения для контролируемого высвобождения силибининового компонента, силибининовый компонент также может содержаться в качестве ионообменного комплекса (адсорбата).
Предпочтительно лекарственное средство перерабатывают для введения один раз в сутки, два раза в сутки, три раза в сутки или четыре раза в сутки.
В предпочтительном варианте осуществления настоящего изобретения от 0,5 до 75 мас.% изначально содержащегося силибининового компонента высвобождалось из лекарственного средства через 1 ч в условиях in vitro. Соответствующие условия для определения высвобождения действующих веществ in vitro известны специалистам в данной области. В связи с этим информация может быть получена, например, в Европейской фармакопее. Предпочтительно определение высвобождения проводят с помощью прибора с лопастной мешалкой в искусственном желудочном соке (буфер с величиной pH 1,2) или в искусственном кишечном соке (буфер с величиной pH 7,6). Количество высвободившегося силибининового компонента может быть исследовано, например, с помощью ВЭЖХ и УФ-скопии.
Предпочтительные профили высвобождения от A1 до A8 суммированы в приводимой ниже таблице
прошествии
времени
[ч]
В предпочтительном варианте осуществления настоящего изобретения лекарственное средство содержит циклодекстрин и/или фосфолипид.
Фармацевтические составы, содержащие силибинин и циклодекстрины, известны из предшествующего уровня техники (см., например, ЕР 422497). Предпочтительно, силибинин формирует включенный комплекс с циклодекстрином. Предпочтительными циклодекстринами являются α-, β- и γ-циклодекстрины, их О-С1-С4-алкильные и гидрокси-С1-С4-алкильные производные.
Фармацевтические композиции, которые содержат силибинин и фосфолипиды, также известны из предшествующего уровня техники (см. US 4764508). Предпочтительно силибинин формирует комплекс с фосфолипидом. Предпочтительными фосфолипидами являются фосфатидилхолин, фосфатидилэтаноламин и фосфатидилсерин. Предпочтительными силибининовыми фосфолипидными комплексами являются третичные комплексы, дополнительно содержащие витамин Е (токоферол). Комплексы такого типа известны из предшествующего уровня техники и обозначаются «комплексами SPV» (см. A.Federico, Gut. 55(6), 2006, сс.901-902).
Помимо силибининового компонента лекарственное средство может содержать один или несколько терпенов. За счет действия терпена и необходимые условия для адсорбции, и процессы адсорбции в целом могут быть улучшены. Терпены могут быть природными или синтетическими эфирными маслами и/или их терпеноидные компоненты в форме чистых веществ или смесей, или производных таких чистых веществ. Среди эфирных масел можно отметить, в частности, масло чебреца, масло эвкалипта, масло сосновой хвои, масло чайного дерева, масло каепутового дерева, масло кардамона, масло перечной мяты, масло шалфея и масло розмарина, предпочтительно масло чебреца. Из терпенов - веществ, также предназначенных к включению, в частности можно использовать гемитерпены, к которым относятся, например, изопрен, тиглиновая кислота, изовалериановая кислота; монотерпены, включая ациклические монотерпены, например, 2,6-диметилоктан, α-миркен, (Е)-р-оцимен, периллен, линалул, гераниол, (S)-(+)цитронеллол и моноциклические монотерпены, например циклопропановые монотерпены и циклобутановые монотерпены, например хризантемовая кислота или юнионон, циклопентановые монотерпены, например иридоиды или непеталактоны или (-)-секологанин и (-)-олеуропеин, монотерпены циклогексана, например, о-ментан, цис- или транс-р-ментан, (R)-(+)-лимонен, терпинолы, (-)-ментол, (+)-периллальдегид, (-)-ментон или (+)-карвон, бициклические монотерпены, например, терпены с кислородными мостиками 1,4-цинеол, 1,8-цинеол или аскаридол; циклопропановые бициклы карана и туйяна, циклобутановый бицикл пинана, и бициклогептаны камфан и фенхан; сесквитерпены, например, фамосан, бисаболан, гермакран, элемен и гумилан. Особенно предпочтительными терпенами являются тимол, ментол, цинеол, борнеол, карвон, лименон и пинен, обычно предпочтительно тимол.
Лекарственное средство содержит силибининовый компонент. Силибинин представляет составную часть силимарина. Предпочтительно, помимо силибинина или силибининовых компонентов, лекарственное средство не содержит ни одного из других составных частей силимарина. Если силибининовым компонентом является сам силибинин, лекарственное средство предпочтительно не содержит ни одного из других силибининовых компонентов силимарина. Если силибининовым компонентом не является сам силибинин, а, например, силибининовый эфир, лекарственное средство предпочтительно не содержит ни одного из других компонентов силимарина, т.е. также не содержит силибинина.
Предпочтительно одно или несколько веществ, выбранных из группы, состоящей из изосилибинина, силидианина, силикристина, таксифолина, изосиликристина, силимонина, силандрина, силигермина и неосилигермина, отсутствуют в лекарственном средстве, т.е. лекарственное средство предпочтительно практически не содержит по меньшей мере одного из указанных выше веществ. В связи с этим понятие «практически не содержится» означает, что остаточное содержание вещества предпочтительно менее 2,0 мас.%, более предпочтительно менее 1,0 мас.%, еще более предпочтительно менее 0,5 мас.%, наиболее предпочтительно менее 0,1 мас.% и особенно менее 0,05 мас.% от общей массы лекарственного средства. Аналитические методы определение остаточных количеств этих веществ известны специалистам в данной области, например, ВЭЖХ.
Установлено, что отдельные составные части силимарина отличаются по химическим и физическим свойствам и влияют на фармакологическое действие силимарина в разной степени, поэтому полезно назначать силибинин, или его производные, и/или соли в качестве единственной составляющей части силимарина, т.е. исключительно. Очевидно, что таким способом и эффективность, и податливость пациента могут быть улучшены.
Кроме того, неожиданно было установлено, что переносимость разных составляющих частей силимарин различна, и что силибин лучше переносим, особенно менее токсичен, по сравнению с силимарином (т.е. по сравнению со смесью, содержащей другие компоненты помимо силибинина).
В предпочтительном варианте осуществления настоящее изобретение относится к применению силибининового компонента для получения лекарственного средства, которое предпочтительно перерабатывают для парентерального или перорального введения и которое помимо силибининового компонента не содержит ни одной из составляющих частей силимарина, для лечения вирусного гепатита, в частности гепатита В и или С.
Ниже описаны особенно предпочтительные лекарственные средства, которые адаптированы для перорального введения силибининового компонента. Все эти пероральные дозированные формы в совокупности содержат предпочтительно силибининовый компонент в существенной степени чистой форме, т.е. предпочтительно в отсутствии других компонентов силимарина, особенно в отсутствии изосилибинина, и/или силикристина, и/или силидианина.
Предпочтительно пероральные дозированные формы представляют пероральные дозированные формы немедленного высвобождения, т.е. силибининовый компонент быстро высвобождается из лекарственной формы, что приводит к быстрому поступлению лекарственного средства в желудочно-кишечный тракт. В предпочтительном варианте осуществления настоящего изобретения через 30 мин после введения пероральной дозированной формы, по меньшей мере 75 мас.%, более предпочтительно по меньшей мере 80 мас.%, еще более предпочтительно по меньшей мере 85 мас.%, наиболее предпочтительно по меньшей мере 90 мас.% и особенно по меньшей мере 95 мас.% первоначально содержащегося силибининового компонента высвобождается из пероральной дозированной формы.
В предпочтительном варианте осуществления настоящего изобретения предусмотрено лекарственное средство в качестве твердого раствора. Твердый раствор предпочтительно получают путем погружения силибининового компонента в молекулярную дисперсную форму в высокой степени растворимую, предпочтительно аморфную полимерную матрицу с большой специфической площадью поверхности. Силибининовый компонент может содержаться в молекулярной дисперсионной форме, т.е. не в микрокристаллической, и не в тонкоизмельченной кристаллической. В высокой степени растворимое аморфное состояние может быть достигнуто путем применения высокорастворимых твердых полимерных растворителей при экстрагировании силибинина или силибининового компонента из экстракта силимарина. Такой технический лекарственный состав повышает растворимость силибининового компонента и скорость его растворения.
Пример такого твердого раствора включает силибининовый компонент, соответствующий полимер (например, поливинилпирролидон (ПВП) или сополимер поливинилпирролидона, например продукт Kollidon® 25) и необязательно декстрин (например, мальтодекстрин). Состав может содержать дополнительные эксципиенты, например аэрозоль и/или тальк.
Предпочтительные варианты твердого раствора от В1 до В6 представлены в таблице ниже.
Состав может быть предусмотрен, например, в твердой желатиновой капсуле.
В другом предпочтительном варианте осуществления настоящего изобретения предусмотрено лекарственное средство в виде самоэмульгирующейся микроэмульсии. Самоэмульгирующиеся липидные системы могут применяться в качестве носителей и могут привести к высокой биодоступности содержащегося в них лекарственного агента. Липидная система имеет коллоидную природу и позволяет всасываться микрочастицам, особенно коллоидного размера, также через лимфатическую систему в желудочно-кишечном тракте. Обычно растворенное лекарственное средство насыщают, но перекристаллизации не происходит. При пероральном введении липофильных лекарственных средств, например силибининового компонента, микроэмульсия в основном служит оптимизированным переносчиком, который повышает степень растворимости растворенных или в высокой степени дисперсных лекарственных средств в месте всасывания. Иначе говоря, липидная система действует в качестве усилителя адсорбции.
Примером такой липидной системы является силибининовый компонент, соответствующий первый эмульгатор (например, лауроилмакроголглицерид, например продукт Gelucire® 44/14), и необязательно соответствующий второй эмульгатор (например, каприлокаприлмкроголглицерид, например продукт Labrasol®). Состав может дополнительно включать эксципиенты, например полисорбат.
Предпочтительные варианты твердого раствора от C1 до С6 представлены в таблице ниже.
Состав, который может быть твердым или предпочтительно полужидким, может быть предусмотрен, например, в твердой желатиновой капсуле или в мягкой желатиновой капсуле.
В еще одном предпочтительном варианте осуществления настоящего изобретения предусмотрено лекарственное средство в виде нанотехнологического состава. Средний размер частиц предпочтительно менее 1 мкм. Наночастицы способны проникать через биологические клеточные структур. Силибининовый компонент предпочтительно адсорбируется на поверхности указанных наночастиц. Наночастицы предпочтительно отбирают из группы, состоящей из неорганических наночастиц и органических наночастиц.
Неорганические наночастицы включают кристаллические силикаты, например, минерального происхождения или искусственные силикаты, например металлосиликаты, например алюмосиликаты (например, цеолиты). Такие неорганические наночастицы предпочтительно химически модифицированы таким образом, что они несут электростатические заряды. Силикаты являются ультратонкой основой для наночастиц и силибининовый компонент связан (адсорбирован) с микропористой поверхностью наночастиц.
Органические наночастицы включают кластеры или агломераты низкомолекулярных белков, или олигопептидов, или липидов. Соответствующим носителем белка является, например, протамин.
Способы получения наночастиц известны специалистам в данной области. Например, коллоидные наночастицы в качестве носителей для перорального высвобождения лекарственного средства, могут быть получены распылением лекарственного средства, т.е. силибининового компонента, совместно с соответствующими материалами-носителями под давлением при температуре, например, 60°С, через форсунки, оснащенные перфорированными ситами (матрицами) в сильно охлажденных башнях. Самопроизвольное охлаждение формирует аморфную фазу, состоящую из наночастиц.
Твердые липидные наночастицы могут быть получены, например, гомогенизированием высокого давления и последующим охлаждением распылением. Предпочтительно лекарственное средство, т.е. силибининовый компонент, применяют в качестве раствора в соответствующем растворителе или номинально в виде субмикрочастиц. Силибининовый компонент может быть распылен и гомогенизирован давлением, соответственно, при смешивании с липидным растворителем и поверхностно-активным веществом при температуре, например, 60°С. После необязательного добавления мелкоизмельченных наполнителей в качестве внешней фазы, а также агентов скольжения и другие поверхностно-активные вещества, полученным в результате составом можно наполнять твердые желатиновые капсулы.
К примерам таких плотных липидных наночастиц относится ядро силибининового компонента, соответствующий первый эмульгатор (например, стеароилмакроголглицерид, например, продукт Gelucire® 50/13), и необязательно соответствующее макромолекулярное неионное поверхностно-активное вещество (например, полоксамер). Состав предпочтительно также содержит внешнюю фазу (покрытие), включающую первое поверхностно-активное вещество (например, Tween 20), аэросил и второе поверхностно-активное вещество (например, глицерилпальмитостеарат, например, продукт Percirol®).
Предпочтительные варианты осуществления от D1 до D6 твердого раствора представлены ниже в таблице.
Нагруженные наночастицы достигают значительно более быстрого начала поступления лекарственного средства.
Лекарственное средство содержит силибининовый компонент предпочтительно в дозе по меньшей мере 10 мг, по меньшей мере 15 мг, по меньшей мере 20 мг, по меньшей мере 25 мг, по меньшей мере 50 мг, по меньшей мере 75 мг, по меньшей мере 100 мг, по меньшей мере 125 мг, по меньшей мере 150 мг, по меньшей мере 175 мг или по меньшей мере 200 мг; более предпочтительно по меньшей мере 225 мг, по меньшей мере 250 мг, по меньшей мере 275 мг, по меньшей мере 300 мг, по меньшей мере 325 мг, по меньшей мере 350 мг, по меньшей мере 375 мг или по меньшей мере 400 мг; еще более предпочтительно по меньшей мере 425 мг, по меньшей мере 450 мг, по меньшей мере 475 мг, по меньшей мере 500 мг, по меньшей мере 525 мг, по меньшей мере 550 мг, по меньшей мере 575 мг или по меньшей мере 600 мг; наиболее предпочтительно по меньшей мере 625 мг, по меньшей мере 650 мг, по меньшей мере 675 мг, по меньшей мере 700 мг, по меньшей мере 725 мг, по меньшей мере 750 мг, по меньшей мере 775 мг или по меньшей мере 800 мг; и особенно по меньшей мере 825 мг, по меньшей мере 850 мг, по меньшей мере 875 мг, по меньшей мере 900 мг, по меньшей мере 925 мг, по меньшей мере 950 мг, по меньшей мере 975 мг, или по меньшей мере 1000 мг; в каждом случае в качестве эквивалентной дозы, основанной на силибинине.
Лекарственное средство содержит силибининовый компонент предпочтительно в дозе по меньшей мере 1,0 мг/кг, более предпочтительно по меньшей мере 2,5 мг/кг, еще более предпочтительно по меньшей мере 5,0 мг/кг, наиболее предпочтительно по меньшей мере 7,5 мг/кг и, особенно по меньшей мере 10 мг/кг, по меньшей мере 12,5 мг/кг, по меньшей мере 15 мг/кг, по меньшей мере 17,5 мг/кг, по меньшей мере 20 мг/кг, по меньшей мере 22,5 мг/кг, по меньшей мере 25 мг/кг, по меньшей мере 27,5 мг/кг или по меньшей мере 30 мг/кг, исходя из массы тела пациента и в каждом случае в виде эквивалентной дозы силибинина. Предпочтительно указанная доза является суточной дозой. Таким образом, если лекарственное средство адаптировано, например, для введения дважды в сутки, соответствующая суточная доза делится на две части равного количества. Сходным образом, например, если лекарственное средство адаптировано для введения трижды в сутки, соответствующую суточную дозу делят на три части равного количества.
В предпочтительном варианте осуществления настоящего изобретения суточная доза силибининового компонента составляет по меньшей мере 5, более предпочтительно по меньшей мере 10, еще более предпочтительно по меньшей мере 15, и наиболее предпочтительно по меньшей мере 20 мг на кг массы тела, основываясь на равной массе силибинина.
В предпочтительном варианте осуществления настоящего изобретения суточная доза силибининового компонента составляет 20 мг на кг массы тела, основываясь на равной массе силибинина. Таким образом, если лекарственное средство адаптировано для введения раз в сутки, оно предпочтительно содержит все количество силибининового компонента, например 1400 мг силибинина для пациента с массой тела 70 кг. Если лекарственное средство адаптировано для введения дважды в сутки, оно предпочтительно содержит половину количества силибининового компонента, например 700 мг силибинина для пациента с массой тела 70 кг. Если лекарственное средство адаптировано для введения трижды в сутки, оно предпочтительно содержит треть количества силибининового компонента, например 467 мг силибинина для пациента с массой тела 70 кг. Если лекарственное средство адаптировано для введения четыре раза в сутки, оно предпочтительно содержит четверть количества силибининового компонента, например 350 мг силибинина для пациента с массой тела 70 кг.
Если лекарственное средство адаптировано для парентерального введения, предпочтительно для инфузии, предпочтительным режимом лечения является 4 равные инфузии, длящиеся по 2 ч каждое. Предпочтительно через 4 ч такую же инфузию повторяют таким образом, что на протяжении 24 ч в общей сложности проводят 4 инфузии. Такой режим схематически может быть сокращенно обозначен «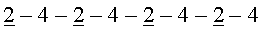 », где каждая цифра означает число часов и подчеркнутые цифры означают длительность инфузии, а неподчеркнутые цифры означают lag-фазу между двумя периодами инфузии. Предпочтительно режим лечения разнородный, т.е. за 24 ч все инфузии равно дозированы на протяжении равных периодов времени, и lag-фазы между следующими друг за другом инфузиями также идентичны.
», где каждая цифра означает число часов и подчеркнутые цифры означают длительность инфузии, а неподчеркнутые цифры означают lag-фазу между двумя периодами инфузии. Предпочтительно режим лечения разнородный, т.е. за 24 ч все инфузии равно дозированы на протяжении равных периодов времени, и lag-фазы между следующими друг за другом инфузиями также идентичны.
Исходя из вышесказанного, предпочтительные режимы парентерального введения суммированы в таблице ниже.
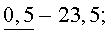
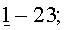
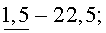
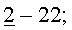
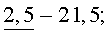
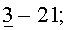
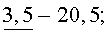
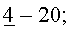
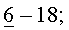
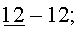
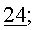
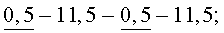
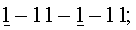
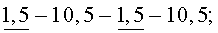
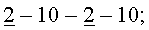
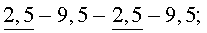
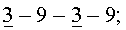
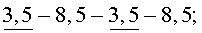
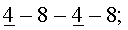
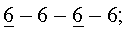
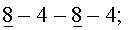
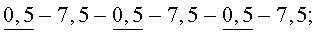
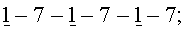
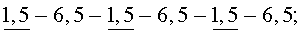
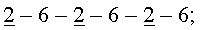
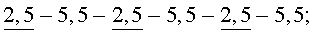
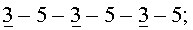
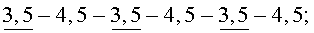
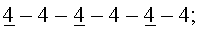
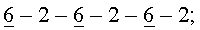
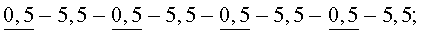
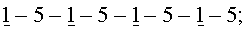
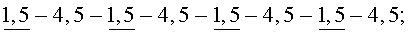
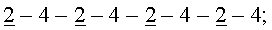
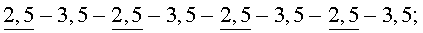
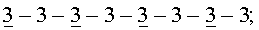
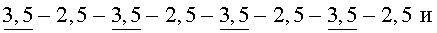
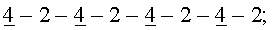
В предпочтительном варианте осуществления настоящего изобретения лекарственное средство адаптировано для введения один, два, три или четыре раза в сутки таким образом, что введенная суммарная суточная доза, вводимая установленным способом, содержит по меньшей мере 300 мг, по меньшей мере 325 мг, по меньшей мере 350 мг, по меньшей мере 375 мг или по меньшей мере 400 мг; более предпочтительно по меньшей мере 425 мг, по меньшей мере 450 мг, по меньшей мере 475 мг, по меньшей мере 500 мг, по меньшей мере 525 мг, по меньшей мере 550 мг, по меньшей мере 575 мг или по меньшей мере 600 мг; еще более предпочтительно по меньшей мере 625 мг, по меньшей мере 650 мг, по меньшей мере 675 мг, по меньшей мере 700 мг, по меньшей мере 725 мг, по меньшей мере 750 мг, по меньшей мере 775 мг или по меньшей мере 800 мг; более предпочтительно по меньшей мере 825 мг, по меньшей мере 850 мг, по меньшей мере 875 мг, по меньшей мере 900 мг, по меньшей мере 925 мг, по меньшей мере 950 мг, по меньшей мере 975 мг, или по меньшей мере 1000 мг; наиболее предпочтительно по меньшей мере 1050 мг, по меньшей мере 1100 мг, по меньшей мере 1150 мг, по меньшей мере 1200 мг или по меньшей мере 1250 мг; и особенно по меньшей мере 1300 мг, по меньшей мере 1350 мг, по меньшей мере 1400 мг, по меньшей мере 1450 мг или по меньшей мере 1500 мг; в каждом случае эквивалентная доза основана на силибинине.
Предпочтительные фармакокинетические параметры AUC0-t, AUCt-∞, AUC0-∞ и AUC0-∞ (исправлено) (предпочтительно после нескольких инфузий, например после 11 инфузии; одна доза: 12,5 мг/кг; суточная доза: 4 инфузии; суммарная доза: 11 инфузии) суммированы в качестве вариантов осуществления от E1 до E8 в приводимой ниже таблице.
(исправлено)
В предпочтительном варианте осуществления настоящего изобретения лекарственное средство, содержащее силибининовый компонент, адаптировано для вспомогательной терапии, предпочтительно к иммуномодулирующей/противовирусной комбинированной терапии, например интерфероном/рибоварином.
В предпочтительном варианте осуществления настоящего изобретения помимо силибининового компонента лекарственное средство содержит дополнительный фармацевтический агент, который предпочтительно применим для лечения воспалительных заболеваний печени, особенно предпочтительно вирусных заболеваний печени, особенно для лечения гепатита В или С.
Предпочтительно, дополнительный фармацевтический агент выбран из группы, включающей средства лечения печени, липотропные агенты [А05В]; нуклеозиды, нуклеотиды, избирательные ингибиторы обратной транскриптазы [J05AB]; интерфероны [L03AB] и моноклональные антитела против ВГВ (вируса гепатита В). Обозначения в квадратных скобках относятся к индексу АТС, предпочтительно в немецкой версии 2007 года.
Особенно предпочтительно, если другой фармацевтический агент выбран из группы, включающей аргинин глютамат, цитиолон, эподемиол, орнитин оксоглурат, тидиацикаргинин, миоинозитол, метионин и N-ацетилметионин, холин, орнитин аспартат, цианиданол, тиопронин, бетаин, цианокобаламин, лейцин, левулозу, ацикловир, удоксуридин, видарабин, рибавирин, ганцикловир, фамцикловир, валацикловир, цидофовир, пенцикловир, валганцикловир, бривудин, интерферон альфа, интерферон бета, интерферон гамма, интерферон альфа-2а, интерферон альфа-2b, интерферон альфа-n1, интерферон бета-1а, интерферон бета-1b, интерферона альфакон-1, ПЭГинтерферон альфа-2b, ПЭГинтерферон альфа-2а и интерферон гамма 1b.
В предпочтительном варианте осуществления настоящего изобретения лечение пациента силибининовым компонентом предназначено для поддержания и/или лечения вирусного гепатита, особенно гепатита В или С, с последующим лечением другим фармацевтическим средством, которое предпочтительно выбрано из группы, состоящей из аргинина глутамата, силимарина, цитиолона, эподемиола, орнитина оксоглурата, тидиацикаргинина, миоинозита, метионина и N-ацетилметионина, холина, орнитина аспартата, цианиданола, тиопронина, бетаина, цианокобаламина, лейцина, лавулезы, ацикловира, удоксуридина, видарабина, рибавирина, ганцикловира, фамцикловира, валацикловира, цидофовира, пенцикловира, валганцикловира, бривудина, интерферона альфа, интерферона бета, интерферона гамма, интерферона альфа-2а, интерферона альфа-2b, интерферона альфа-n1, интерферона бета-1а, интерферона бета-1b, интерферона альфакон-1, пэгинтерферона альфа-2b, пэгинтерферона альфа-2а и интерферона гамма 1b.
Таким образом, предпочтительно после лечения вирусного гепатита, особенно гепатита В или С, лекарственным агентом, который содержит силибининовый компонент, проводить лечение вирусного гепатита, особенно гепатита В или С, другим лекарственным агентом.
В предпочтительном варианте осуществления настоящего изобретения лекарственное средство переработано в качестве составляющей части последующего лечения, причем лекарственное средство сначала вводят на протяжении первого периода, предпочтительно парентерально, и затем другое лекарственное средство вводят на протяжении второго периода. Предпочтительно первый период включает по меньшей мере 2 суток, более предпочтительно по меньшей мере 3 суток, еще более предпочтительно по меньшей мере 4 суток, наиболее предпочтительно по меньшей мере 5 суток и особенно предпочтительно по меньшей мере 6 суток. Предпочтительно, второй период включает больше суток, чем первый период. Предпочтительно, второй период включает по меньшей мере двое суток, более предпочтительно по меньшей мере 3 суток, еще более предпочтительно по меньшей мере 4 суток, наиболее предпочтительно по меньшей мере 5 суток и особенно по меньшей мере 6 суток. В особенно предпочтительном варианте осуществления настоящего изобретения второе лекарственное средство содержит комбинацию рибавирина и пэгелированного интерферона альфа, причем второй период длится 24-48 недель.
Предпочтительно, другое лекарственное средство содержит одно или несколько фармацевтических агентов, выбранных из группы, включающей аргинин глютамат, силимарин, цитиолон, эподемиол, орнитин оксоглурат, тидиацикаргинин, миоинозитол, метионин и N-ацетилметионин, холин, орнитин аспартат, цианиданол, тиопронин, бетаин, цианокобаламин, лейцин, левулозу, ацикловир, удоксуридина, видарабин, рибавирин, ганцикловир, фамцикловир, валацикловир, цидофовир, пенцикловир, валганцикловир, бривудин, интерферон альфа, интерферон бета, интерферон гамма, интерферон альфа-2а, интерферон альфа-2b, интерферон альфа-n1, интерферон бета-1a, интерферон бета-1b, интерферона альфакон-1, ПЭГинтерферон альфа-2b, ПЭГинтерферон альфа-2а и интерферон гамма 1b и моноклональные антитела к ВГВ, особенно предпочтительно интерферон, и/или рибавирин, и/или силимарин. Если другое лекарственное средство содержит интерферон, то это предпочтительно пэгелированный интерферон альфа (ПЭГинтерферон альфа-2а или ПЭГинтерферон альфа-2b).
В особенно предпочтительном варианте осуществления настоящего изобретения другое лекарственное средство содержит одно или несколько фармацевтических агентов, выбранных из группы, включающей изосилибинин, силидианин, силикристин, таксифолин, изосиликристин, силимонин, силандрин, силигермин и неосилигермин, более предпочтительно только один фармацевтический агент, выбранный из указанного выше перечня. Предпочтительно, другое лекарственное средство включает силибининовый компонент, охарактеризованный в связи с описанным выше лекарственным агентом, который вводят на протяжении первого периода, и предпочтительно практически не содержит по меньшей мере одного, предпочтительно всех из указанных выше веществ. В связи с этим понятие «практически не содержит» означает, что остаточное содержание вещества предпочтительно составляет менее 2,0 мас.%, более предпочтительно менее 1,0 мас.%, еще более предпочтительно менее 0,5 мас.%, наиболее предпочтительно менее 0,1 мас.% и особенно менее 0,05 мас.% от общей массы лекарственного средства.
Другое лекарственное средство может в принципе быть переработано для парентерального или перорального введения. По настоящему изобретению оно предпочтительно переработано для другого способа введения в отличие от лекарственного средства, которое вводят на протяжении первого периода. Особенно предпочтительно другое лекарственное средство переработано для перорального введения. В особенно предпочтительном варианте осуществления настоящего изобретения лекарственное средство, которое вводят во время первого периода, адаптировано для парентерального, предпочтительно внутривенного введения, и другое лекарственное средство, которое вводят во время второго периода, следующего после первого периода, адаптировано для перорального введения.
В предпочтительном варианте осуществления настоящего изобретения режим лечения по настоящему изобретению включает две фазы, следующие одна за другой, которые называют первым периодом и вторым периодом. Предпочтительно, во время первого периода вводят лекарственное средство, содержащее силибининовый компонент, предпочтительно парентерально, но другие средства лечения печени одновременно не вводят. Во время второго периода вводят другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа. В предпочтительном варианте осуществления настоящего изобретения лекарственное средство, содержащее силибининовый компонент, также вводят во время второго периода, предпочтительно парентерально. В другом предпочтительном варианте осуществления настоящего изобретения лекарственное средство, содержащее силибининовый компонент, не вводят во время второго периода, т.е. вводят только указанное другое лекарственное средство.
Предпочтительные варианты осуществления с F1 по F15 режима двухфазного введения суммированы ниже в таблице.
В другом предпочтительном варианте осуществления настоящего изобретения режим лечения по настоящему изобретению включает три фазы, следующие одна за другой, которые называются первым периодом, вторым периодом и третьим периодом. Предпочтительно, во время первого периода вводят лекарственное средство, содержащее силибининовый компонент, предпочтительно парентерально, но другие средства лечения печени одновременно не вводят. Во время второго периода также вводят другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, и лекарственное средство, содержащее силибининовый компонент, предпочтительно парентерально. Предпочтительно, во время третьего периода вводят указанное другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, но лекарственное средство, содержащее силибининовый компонента, не вводят во время третьего периода, т.е. вводят только указанное другое лекарственное средство.
Предпочтительные варианты осуществления от G1 до G15 трехфазного режима лечения суммированы в приводимой ниже таблице.
период
период
период
В еще одном предпочтительном варианте осуществления настоящего изобретения режим лечения по настоящему изобретению включает три фазы, которые следуют последовательно друг за другом, а именно первый период, второй период и третий период. Предпочтительно, во время первого периода вводят другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, и не вводят лекарственное средство, содержащее силибининовый компонент, во время первого периода. Во время второго периода по прежнему вводят указанное второе лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, и также вводят (совместно) лекарственное средство, содержащее силибининовый компонент, во время второго периода, предпочтительно парентерально. Предпочтительно, во время третьего периода вводят указанное другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, но не вводят лекарственное средство, содержащее силибининовый компонент, во время третьего периода, т.е. вводят только указанное другое лекарственное средство. Иначе говоря, согласно предпочтительному варианту осуществления настоящего изобретения постоянно вводят указанное другое лекарственное средство, которое предпочтительно содержит рибавирин и/или пэгелированный интерферон альфа, и во время промежуточного периода (= второго периода) совместно вводят лекарственное средство, содержащее силибининовый компонент, предпочтительно парентерально.
Предпочтительные варианты осуществления от H1 до H15 трехфазного периода лечения суммированы в приведенной ниже таблице.
период
период
период
Фиг.10 визуализирует различные способы совместного введения рибавирина и/или пэгелированного интерферона альфа и лекарственного средства, содержащего силибининовый компонент (варианты от а1) до m2)). Каждая полоса относится к периоду времени введения. Например, по варианту f1, введение начинается с рибавирина/пэгелированного интерферона альфа и продолжается. Во время промежуточного периода одновременно вводят силибининовый компонент.
Другой объект настоящего изобретения относится к лекарственному средству, согласно описанному выше, предпочтительно адаптированному для парентерального введения, для лечения вирусного гепатита, согласно описанному выше.
Еще один объект настоящего изобретения относится к набору, включающему по меньшей мере одно лекарственное средство по настоящему изобретению, которое включает силибининовый компонент, и по меньшей мере одно другое лекарственное средство. Оба лекарственных средства по настоящему изобретению, которые содержат силибининовый компонент, и другое лекарственное средство описаны выше таким образом, что во всех сходных предпочтительных вариантах осуществления настоящего изобретения также применяется набор по настоящему изобретению.
В предпочтительном варианте осуществления настоящего изобретения набор содержит столько лекарственных средств (отдельных дозированных единиц), сколько необходимо для выполнения непрерывной терапии, причем лекарственное средство, которое содержит силибининовый компонент, сначала вводят в течение первого периода, и затем второе лекарственное средство вводят в течение второго периода. Предпочтительно, первый период включает по меньшей мере 2 суток, более предпочтительно по меньшей мере 3 суток, еще более предпочтительно по меньшей мере 4 суток, наиболее предпочтительно по меньшей мере 5 суток и особенно предпочтительно по меньшей мере 6 суток. Предпочтительно, второй период включает больше суток по сравнению с первым периодом. Предпочтительно, второй период включает по меньшей мере 2 суток, более предпочтительно по меньшей мере 3 суток, еще более предпочтительно по меньшей мере 4 суток, наиболее предпочтительно по меньшей мере 5 суток и особенно предпочтительно по меньшей мере 6 суток.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к применению силибининового компонента, предпочтительно сложного эфира силибинина, для получения лекарственного средства, которое переработано для парентерального введения, для лечения вирусного гепатита С у нон-респондеров при лечении рибавирином/интерфероном, т.е. у пациентов, которые не отвечают на иммуномодулирующую/противовирусную комбинированную терапию, например терапию рибавирином/интерфероном.
Другой объект настоящего изобретения относится к силибининовому компоненту, предпочтительно сложному эфиру силибинина, предпочтительно для парентерального введения, для лечения вирусного гепатита, предпочтительно гепатита С. Предпочтительные варианты осуществления настоящего изобретения становятся очевидны из приведенного выше описания предпочтительных вариантов других объектов настоящего изобретения и соответственно не повторяются.
Другой объект настоящего изобретения относится к лечению вирусного гепатита, предпочтительно гепатита С, включающему введение, предпочтительно парентеральное введение, фармацевтически эффективного количества силибининового компонента, предпочтительно сложного эфира силибинина, субъекту, нуждающемуся в этом. Предпочтительные варианты осуществления объектов настоящего изобретения становятся очевидными из указанного выше описания предпочтительных вариантов осуществления других объектов настоящего изобретения и, следовательно, не повторяющихся.
Приводимые ниже примеры дополнительно иллюстрируют настоящее изобретение, но они не ограничивают его области охвата.
Пример 1
Силибининовый компонент вводят парентерально в форме силибинин-С-2',3-бис(гидрогенсукцината) (продукта Legalon Sil®, Madaus, Кёльн) (называемого ниже силибинином).
Пациенты и методы
** все были положительными через 24 недели
Для этих исследований отбирают пациентов, проявивших себя к качестве нон-респондеров, для комбинированной терапии полными дозами пэгинтерферона/рибавирина. Отсутствие ответа на лечение проявляется в виде отсутствия снижения >2 log вирусной нагрузки через 12 недель лечения, и/или по отсутствию ответа к концу лечения. У пациентов была сделана биопсия печени за 2 года до включения в настоящее исследование. Применяют стандартные критерии включения/исключения для лечения пэгинтерфероном/ рибавирином.
Протокол исследования
На протяжении фазы скрининга в течение 35 суток до первого дозирования при исследовании лекарственного средства оценивают приемлемость пациентов по критериям включения/исключения. У всех пациенты должно быть по меньшей мере одно количественное исследование ВГС-РНК в течение 6 месяцев до фазы скрининга.
Протокол 1
Сначала пациенты получают ежедневно 10 мг/кг силибинина (продукта Legalon Sil®, Madaus, Кёльн), который вводят инфузией на протяжении 4 ч в течение 7 последовательных суток. В первые сутки берут кровь на анализ для определения исходных показателей окислительного стресса, а также каждые 30 мин во время инфузии и через 2 ч после завершения инфузии. На 8 сутки лечение заменяют на 140 мг силимарина (продукт Legalon, фирма Madaus, Кёльн) три раза в сутки перорально в комбинации с 180 мкг/неделю пэгинтерферона альфа-2а (продукт PEGASYS®, фирма Roche, Базель) и 1-1,2 г/сутки рибавирина (продукт COPEGUS®, фирма Roche, Базель).
Протокол 2
После получения результатов по первому протоколу проводят лечение силибинином в течение 2 недель и вводят разные дозы силибинина. Сначала пациенты получают ежедневно 5, 10, 15 или 20 мг/кг силибинина инфузией в течение 4 ч на протяжении 14 последовательных суток. На 8 сутки лечения начинают вводить 180 мкг/неделю пэгелированного интерферона альфа-2а и 1-1,2 г/сутки рибавирина. Через 14 суток пациенты получают 280 мг силимарина (продукта Legalon®, Madaus, Кёльн) перорально три раза в сутки. На протяжении 14 суток периода инфузии ежедневно берут кровь для определения вирусной нагрузки.
В обоих протоколах в случае непереносимости пэгелированного интерферона альфа-2а или рибавирина используют стандартные рекомендации по подбору дозировки. Противовирусную комбинированную терапию получают в течение в общей сложности 24 недель (при остановке лечения пациентов при >2 log снижении на 12 неделю); респондерам на противовирусную терапию на 24 неделю предлагают продолжить лечение в течение дополнительных 48 недель. После окончания периода проведения инфузии пациентов оценивают через 2, 4 недели и затем ежемесячно до окончания терапии через 24 недели.
Протокол был одобрен Комитетом по этике Медицинского университета Вены. Детали исследования объясняют пациентам, и они все дают подписку о согласии участвовать в исследовании.
Методы
Уровень ВГС РНК в сыворотке определяют методом TaqMan ПЦР (Cobas Ampliprep/ Cobas TaqMan VHC Test; предел обнаружения 15 МЕ/мл, фирма Roche Diagnostics).
Реакционноспособные окислительные метаболиты в крови измеряют методом производных соединений реактивных кислородных метаболитов (п-РКМ; фирма Diacron, Grosseto, Италия), и количества антиоксидантов методом биологического антиоксидантного потенциала (БАП; фирма Diacron, Grosseto, Италия), используя портативную систему определения свободных радикалов (FRAS 4, SEAC, Calenzano, Италия), до инфузии силибинина, каждые 30 мин на протяжении инфузии (в 1 сутки) и через 2 ч после инфузии. Методом п-РКМ измеряют реакционноспособные окислительные метаболиты (преимущественно гидропероксиды), высвободившиеся из белков плазмы под воздействием кислого буфера, которые в присутствии железа вырабатывает алкоксильные и пероксильные радикалы, в соответствии с реакцией Фентона. Такие радикалы в свою очередь способны окислить алкил-замещенный ароматический амин (N,N-диэтилпарафенилендиамин), таким образом, получая окрашенное в розовый цвет производное, которое подсчитывают количественно при 505 нм. Результаты по реакционноспособным окислительным метаболитам выражают в единицах Карателли (Екар; норма: 250-300, 1 Екар=0,08 мг гидрогенапероксида/дл). Методом БАП измеряют интенсивность обесцвечивания раствора хлорида железа, смешанного с производным тиоцианата, путем добавленного образца плазмы фотометрически при 505 нм, которая пропорциональна способности восстанавливать ионы железа имеющимися в плазме количествами антиоксидантов (норма >2200 пМ). В описании методов производителя не оговаривают, какие именно вещества определяют.
Статистика
Сначала основной результирующей переменной является вирусный ответ, выраженный в виде процента пациентов, являющихся ПЦР-отрицательными к концу лечения (24 недели). Вторичными эффективными переменными являются степени вирусного ответа через 12 недель, безопасность и переносимость лечения пэгинтерфероном/рибавирином/силимарином, качество жизни относительно исходного показателя, через 24 недели, 48 недель, 72 недели (SF-36, цифровая оценочная шкала боли), и окислительный статус после инфузии силибинина. Из-за неожиданно сильного вирусного ответа после 7 суток инфузии силибинина, инфузии приостанавливают и исследование перепланируют, основываясь на параметрах вирусного ответа и используя более длительные периоды инфузии и повышенные дозы силибинина. Для первоначального исследования размер образца устанавливают, основываясь на двухстадийном плане Гехана. Исходя из предшествующих исследований, степень ответа >10% представляется обоснованием для дальнейшего исследования режима лечения. 29 пациентов поправились на первой стадии соответственно (вероятность ошибки β=5%).
Результаты
Протокол 1
Включают шестнадцать охарактеризованных нон-респондеров (подробнее см. таблицу выше). Все пациенты получали полную дозу лечения пэгелированным интерфероном (12 пэгинтерферона альфа 2а, 2 пэгинтерферона альфа 2b) и рибавирином (1000-1200 мг/сутки) в течение по меньшей мере 12 недель. Параметры окислительного стресса не изменяются во время проведения инфузии силибинина (фиг.1).
Содержание сывороточной ВГС РНК падает у всех пациентов при внутривенной монотерапии силибинином (фиг.2) (базовый уровень: 6,59±0,53, сутки 8: 5,26±0,81 log МЕ/мл, [средняя величина ± среднеквадратичное отклонение], р<0,001) со средним log снижением 1,32±0,55 в течение одной недели. Параллельно ALT снижается с 162±133 до 118±107 Ед/л (р=0,004). У всех пациентов ВГС РНК остается выявляемым при инициации лечения пэгинтерфероном/рибавирином. Трое пациентов отказались от комбинированной терапии пэгинтерфероном/рибавирином. У 11 из оставшихся 13 пациентов ВГС-РНК опять повышается после завершения инфузии силибинина несмотря на начало лечения пэгинтерфероном/рибавирином. К 12 неделе все пациенты остаются ВГС-РНК-положительными, но у 5 падение >2 log и они продолжают лечение (фиг.3). Ни один из них не стал ВГС-РНК отрицательным к 24 неделе, у одного пациента было 5,5 log падение, и он продолжил лечение по собственному желанию.
Протокол 2
Включают двадцать нон-респондеров с определенными признаками (подробнее см. таблицу выше). Все пациенты получают полную дозу лечения пэгелированным интерфероном (18 ПЭГинтерферон альфа 2а, 4 ПЭГинтерферон альфа 2b; 2 пациента получили 2 курса лечения) и рибавирином (1000-1200 мг/сутки) в течение по меньшей мере 12 недель.
Фиг.4 показывает кинетику содержания вируса у указанных пациентов. Нагрузка вируса снижается постоянно. Через 7 суток монотерапии силибинином в дозе 5 мг/кг проявляется минимальная эффективность (n=3, log падения 0,55±0,5), причем дозы 10 мг/кг (n=19 [включая пациентов в протоколе 1], log падения 1,41±0,59), 15 мг/кг (n=5, log падения 2,11±1,15) и 20 мг/сутки (n=9, 3,02±1,01) приводят к высокой степени существенному снижению нагрузки вируса (р<0,001).
Через 1 неделю комбинированной терапии силибинином и пэгинтерфероном/ рибавирином нагрузка вирусом дополнительно снижается (log падения: 5 мг/кг: 1,63±0,78; 10 мг/кг: 4,16±1,28; 15 мг/кг 3,69±1,29; 20 мг/кг 4,8±0,89; все величины р<0,0001 относительно исходного уровня) (фиг.5). Два из пяти пациентов в группе применения дозы 15 мг/кг и четыре из девяти пациентов в группе применения дозы 20 мг/кг имеют величину ВГС-РНК<15 ME на 15 сутки. ВГС-РНК составляет <15 МЕ/мл у 8 и 7 пациентов на 4 недели (протокол 5-недельного исследования) и на 12 недель (протокол 13-недельного исследования) после начала применения пэгинтерферона/рибавирина соответственно. Противовирусная комбинированная терапия продолжают для всех пациентов (фиг.6).
Безопасность
Обычно силибинин переносят хорошо. Пять пациентов отмечают умеренные симптомы желудочно-кишечного расстройства (боль в животе: 5, диарея: 2, тошнота 1), двое жалуются на головную боль и один на боль в суставах. Пациентами все они оценены в качестве умеренных и падают после завершения инфузии; изменения в дозировании не требуются. Все пациенты в группах 15 и 20 мг/кг отмечают ощущение тепла в начале инфузии, которое убывает в течение 30 мин без лечения. Отсутствуют тяжелые побочные эффекты. При монотерапии не выявляют изменений гемоглобина, лейкоцитов, тромбоцитов и креатинина. Отмечают типичные побочные эффекты противовирусной комбинированной терапии (в том числе у одного пациента усилилась одышка из-за индуцированной Hemophilus influenzae пневмонии, потребовавшее прекращение лечения пэгинтерфероном/рибавирином в течение 8 недель).
Этот пример показывает, что парентеральное введение силибинина-(С-2',3-бис(гидрогенсукцината)) обладает выраженным противовирусным действием против вируса гепатита С. Это наблюдение показывает, что указанное лекарственное средство может применяться для лечения хронического гепатита С, особенно у нон-респондеров.
Неожиданно было обнаружено, что внутривенно силибинин-(С-2',3-бис(гидрогенсукцинат)) является мощным противовирусным агентом у пациентов с хроническим гепатитом С, не отвечающих на стандартную противовирусную комбинированную терапию. Внутривенно силибинин хорошо переносится, но проявляются побочные эффекты. Сообщают, что наиболее частым побочным эффектом является временное ощущение тепла. Противовирусное действие является дозозависимым, но не сохраняется после завершения периода инфузии пероральным введением силимарина.
При сопоставлении установлено, что близкие количества силимарина, введенные перорально, не влияют на нагрузку ВГС (A.Gordon и др., J Gastroenterol Hepatol. 21, 2006, сс.275-80), отражая различия в биодоступности и метаболизме силибинина и приводя к существенно более низким уровням содержания в плазме. После перорального дозирования флавонолигнаны силимарина быстро глюкоронидируются и быстро элиминируют с короткими периодами полураспада (Z.Wen и др., Drug Metab Dispos. 36(1), 2008, сс.65-72).
Пример 2
Пациентов постоянно лечат 180 мкг пэгинтерферона альфа 2а и зависящим от веса количеством рибавирина. Несмотря на такое лечение, пять пациентов ВГС-РНК-положительны через 24 недели лечения: трое мужчин и двое женщин; четыре пациента с ВГС генотипа 1 и один пациент с ВГС генотипа 3а; трое пациентов с циррозом.
Четырех пациентов можно оценить в качестве не подвергнутых какому-либо воздействию, но один пациент может быть оценен пребывающим в стадии рецидива относительно двух предыдущих терапий (24 и 48 недель).
При прохождении курса лечения 180 мкг пэгинтерферона альфа 2а и зависящим от веса количеством рибавирина, всем пациентам вводят по меньшей мере один раз на протяжении 14 последовательных суток 20 мг/кг/сутки силибинина внутривенно. На протяжении этого периода комбинированную терапию пэгинтерфероном/рибавирином продолжают.
Все 5 пациентов становятся отрицательными по РНК ВГС.
Фиг.7 показывает результаты по одному конкретному пациенту (мужчина, 55 лет). Можно видеть, что лечение пэгинтерфероном/рибавирином вызывает снижение вирусной нагрузки только примерно от log 7 МЕ/мл до примерно log 4,5 МЕ/мл через 24 недели. Совместное лечение 20 мг/кг/сутки внутривенно силибинин-бис(гидрогенсукцинатом) в течение 14 суток, однако, приводит к резкому снижению вирусной нагрузки примерно с log 4,5 МЕ/мл до величины, ниже предела чувствительности. После первого интервала введения парентерального силибинин-бис(гидрогенсукцината), вирусная нагрузка повышается опять примерно до 2 МЕ/мл, которая тем не менее постоянно подавляется ниже предела обнаружения вторым совместным внутривенным введением с 20 мг/кг/сутки силибинин-бмс(гидрогенсукцината) в течение 14 суток.
Фиг.8 показывает результаты по другому конкретному пациенту (женщина, 44 года). Из фигуры следует, что пэгинтерферон/рибавирин редко вызывает снижение вирусной нагрузки примерно с log 7 МЕ/мл до примерно log 5 МЕ/мл через 30 недель. Совместное внутривенное лечение 20 мг/кг/сутки силибинин-бис(гидрогенсукцинатом) в течение 14 суток через 30 недель, однако, приводит к резкому и постоянному снижению вирусной нагрузки примерно от log 4 МЕ/мл до величины ниже предела обнаружения.
Фиг.9 показывает результаты по одному конкретному пациенту (мужчина, 52 года). Из фигуры следует, что пэгинтерферон/рибавирин вызывает эффективное снижение вирусной нагрузки примерно с log 5 МЕ/мл до величины, близкой к пределу обнаружения <15 МЕ/мл. Совместное внутривенное введение 20 мг/кг/сутки силибинин-бис(гидрогенсукцината) в течение 14 суток через 72 недели вызывает дальнейшее снижение вирусной нагрузки ниже уровня обнаружения.
Указанные клинические исследования показывают, что парентеральное лечение силибининовым компонентом на протяжении относительно короткого отрезка времени поддерживает и существенно улучшает традиционное лечение пэгинтерфероном/рибавирином. Показано, что парентеральное введение силибининового компонента активирует (реактивирует) чувствительность пациентов к традиционному лечению пэгинтерфероном/рибавирином (фиг.7 и 8) и/или повышает противовирусное действие традиционного лечения пэгинтерфероном/рибавирином (фиг.9).
Пример 3
Исследование in vivo проводят для описания концентрации в плазме/временных профилей силибинин у 8 пациентов с хроническим гепатитом С, которым 7 суток внутривенно инфузией вводят 20 мг силибинин/кг массы тела (продукт Legalon® SIL). Для многократных доз 20 мг/кг массы тела анализируют профили концентрации в плазме/времени и РК параметры свободного и общего силибинин на 1 сутки (= условия одной дозы) и сравнивают с показателями на 7 сутки (= ожидаемые условия установившегося режима).
Аналитический метод
Исследуют образцы с помощью известного метода ВЭЖХ-УФ. На протяжении исследования аналитический метод подтверждают двумя калибровочными кривыми на каждый аналитический пробег. Анализ хроматограмм с данными, представленными на калибровочных кривых, и образцах контроля качества показывает, что результат определения концентраций общего и свободного силибинина А и силибинина В в таком исследовании является надежным.
Фармакокинетические параметры суммированы в приводимой ниже таблице.
Пример 4
Исследование in vitro проводят для оценки цитотоксического действия силимарина, силибинина, силибинина-бис(гидрогенсукцината) динатриевой соли и янтарной кислоты с помощью теста ХТТ, используя линию клеток мыши L929 (см. D.A.Scudiero и др., Cancer Res. 48, сс.4827-4833; O.S.Weislow и др., J.Natl. Cancer Inst., 81, 577-586; N.W.Roehirm др., J. Immunol. Methods, 142).
Исследуют следующие концентрации по исследуемым позициям: 9,77, 19,53, 39,06, 78,13, 156,25, 312,5, 625, 1250 мкг/мл. Полноценную среду (RPMI 1640, содержащую 10 об.% ФСТ) используют в качестве отрицательного контроля. Контролем растворителя для исследуемой позиции является среда RPMI 1640, содержащая 10 об.% ФСТ и 1% ДМСО. Контролем растворителя для положительного контроля также является среда RPMI 1640, содержащая 10 об.% ФСТ и 10,0 об.% деионизированной воды. Натрий додецилсульфат используют в качестве положительного контроля. Применяют следующие концентрации: 3,125, 6,25, 12,5, 25, 50, 100, 125, 250 мкг/мл. Время инкубирования составляет 24 ч при 37±1,5°С.
Отрицательный контроль и контроль растворителя не проявляют снижения жизнеспособности клеток. Положительный контроль (SDS) индуцирует особое дозозависимое снижение жизнеспособности клеток.
Токсические эффекты наблюдают после инкубирования с силимарином с 39,06 мкг/мл и до самой высокой исследуемой концентрации (1250 мкг/мл). Рассчитанная величина ХТТ50 составляет 35,2 мкг/мл.
Токсические эффекты наблюдают после инкубирования с силибинином с 78,13 мкг/мл и до самой высокой исследуемой концентрации (1250 мкг/мл). Рассчитанная величина ХТТ50 составляет 67,5 мкг/мл.
Не наблюдают существенных цитотоксических эффектов после инкубирования с натриевой солью силибинин-бис(гидрогенсукцината) вплоть до наибольшей анализируемой концентрации (1250 мкг/мл). Из-за утраты цитотоксичности величина ХХТ50 не может быть подсчитана.
Не наблюдают существенных цитотоксических эффектов после инкубирования с янтарной кислотой до наивысшей тестируемой концентрации (1250 мкг/мл). Из-за утраты цитотоксичности величина ХХТ50 не может быть подсчитана.
Проведенные исследования показывают, что в данных условиях цитотоксический потенциал силимарина примерно на 100% выше цитотоксического потенциала силибинина. Поэтому можно ожидать, что силибинин может вводиться в повышенных дозах относительно силимарина без индукции серьезных побочных эффектов.
Пример 5
NS5B РНК-зависимая РНК-полимераза (RNA-dependent RNA polymerase - RdRp) представляет важный фермент для вирусной репликации (см. S.B.Hwang и др., Virology 227, 1997, сс.439-446). Затем очищенные соединения тестируют в бесклеточном ферментном анализе для выявления ВГС RdRp действия: силибинин А, силибинин В, изосилибинин А, изосилибинин В, силикристин, силидианин и двухнатриевую соль сложного эфира силибинина силибинин-С-2',3-бис(гидрогенсукцината) (действующий ингредиент продукта Legalon® SIL).
Концентрацию ДМСО во всех реакциях сохраняют постоянной, составляющей 5%. Приготовляют исходные растворы (100 мМ) соединений в 100% ДМСО. Целевым ферментом в исследовании является ВГС NS5BΔ21 полимераза генотип J4 (1b).
Фиг.11 показывает данные, полученные для шести очищенных составляющих частей силимарина (т.е. силибинина А, силибинина В, изосилибинина А, изосилибинина В, силикристинаи силидианина). Фиг.12 соответственно показывает данные по сложному эфиру силибинина. Сложный эфир силибинина проявляет наибольшую эффективность.
Величину IC50 сложного эфира силибинина определяют по кривой дозы-ответа по двум измерениям. Определенная величина IC50 составляет 47±14 мкМ. Кривые согласовывают по точкам данных и величины IC50 интерполируют по получаемым кривым, используя программное обеспечение SigmaPlot 8.0.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОГНОЗ КИНЕТИКИ ВИРУСА ГЕПАТИТА С ПРИ ЛЕЧЕНИИ, ИСКЛЮЧАЮЩЕМ ИНТЕРФЕРОН | 2011 |
|
RU2590691C2 |
| СПОСОБ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА С | 2012 |
|
RU2496512C1 |
| СПОСОБЫ УЛУЧШЕНИЯ ФАРМАКОКИНЕТИКИ | 2010 |
|
RU2591830C2 |
| СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2371195C2 |
| ОДНОНУКЛЕОТИДНЫЕ ПОЛИМОРФИЗМЫ ДЛЯ ПРОГНОЗИРОВАНИЯ РЕЗУЛЬТАТОВ ЛЕЧЕНИЯ ЗАРАЖЕНИЯ ВИРУСОМ ГЕПАТИТА С | 2011 |
|
RU2567663C2 |
| ПРИМЕНЕНИЕ ПЭГИЛИРОВАННЫХ ИНТЕРФЕРОНОВ ТИПА III ДЛЯ ЛЕЧЕНИЯ ГЕПАТИТА С | 2009 |
|
RU2496514C2 |
| ФАРМАЦЕВТИЧЕСКАЯ ГЕПАТОПРОТЕКТОРНАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2391989C2 |
| Пангенотипичный ингибитор белка NS5A вируса гепатита С, фармацевтическая композиция и способы их получения и применения | 2019 |
|
RU2723482C1 |
| ОДНОНУКЛЕОТИДНЫЙ ПОЛИМОРФИЗМ НА ХРОМОСОМЕ 15, КОТОРЫЙ ПОЗВОЛЯЕТ ПРОГНОЗИРОВАТЬ ВОСПРИИМЧИВОСТЬ К ЛЕЧЕНИЮ ВИРУСА ГЕПАТИТА С | 2012 |
|
RU2606759C2 |
| СПОСОБЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ИНФЕКЦИИ ГЕПАТИТА С | 2006 |
|
RU2440822C2 |
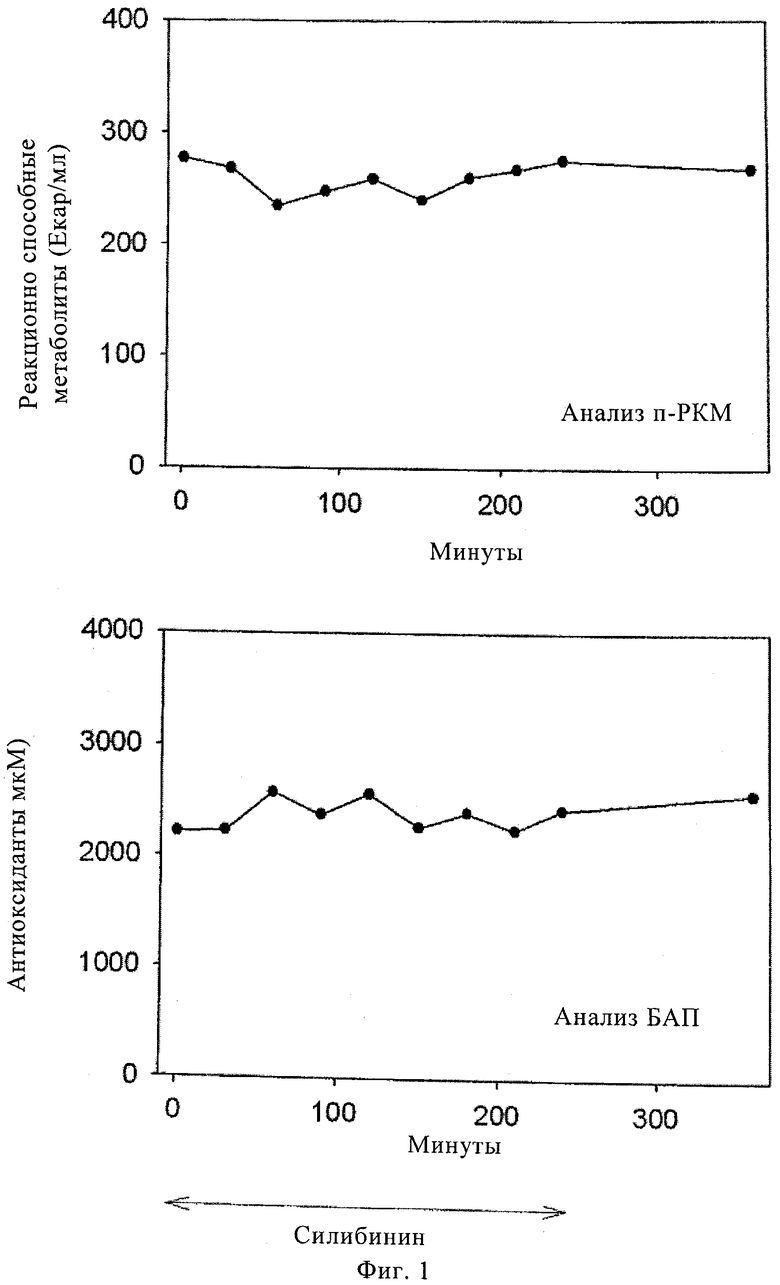
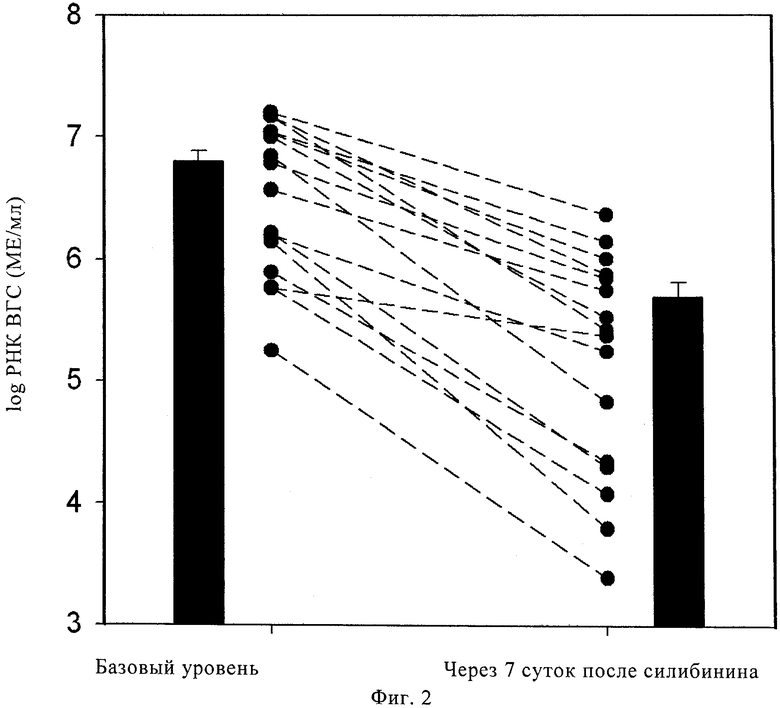
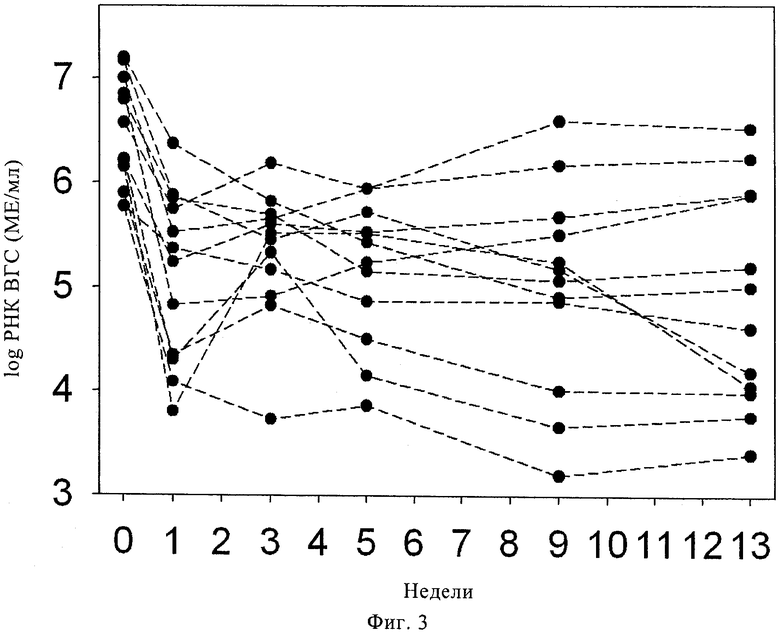
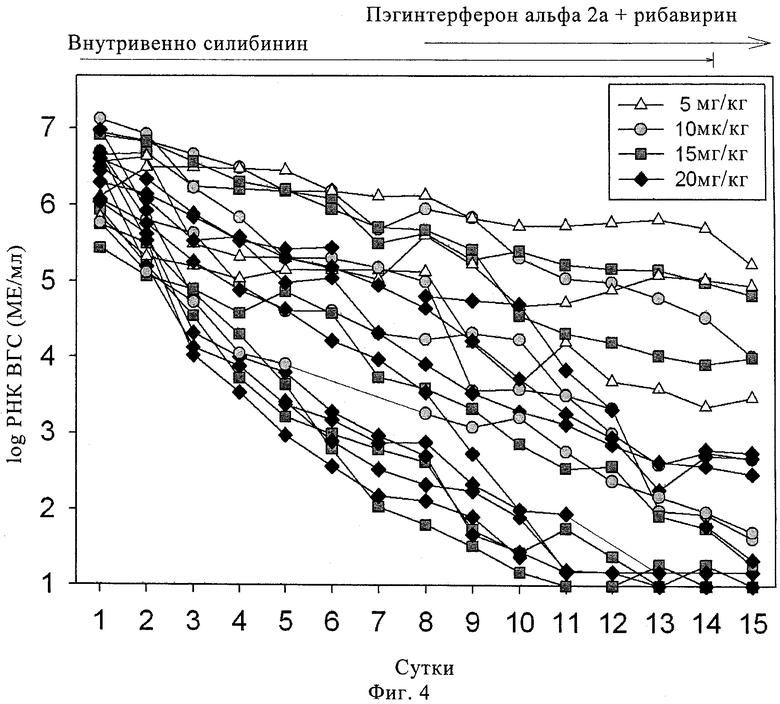
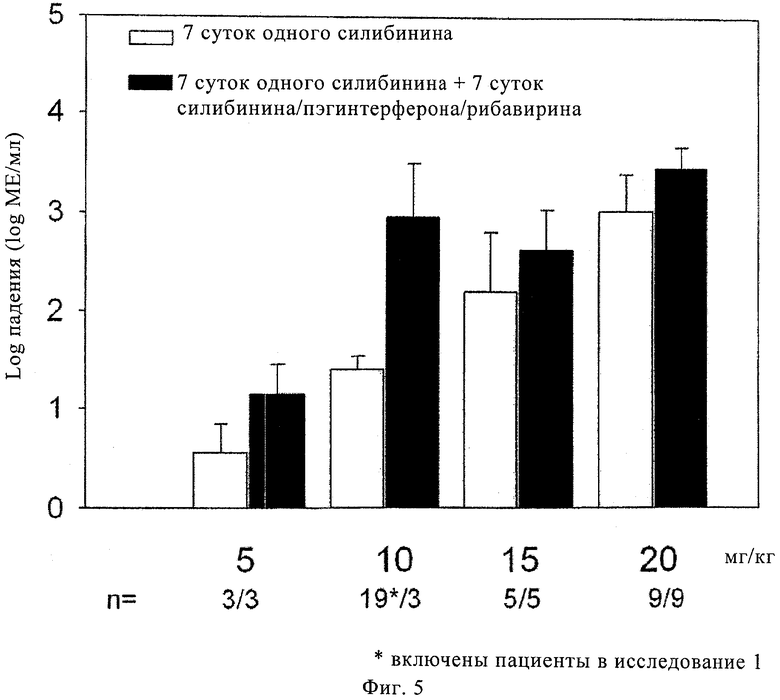
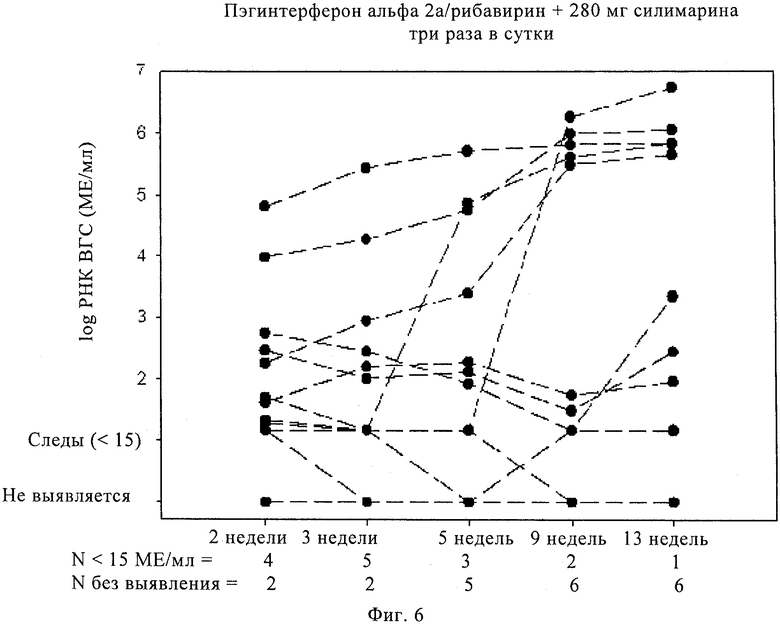
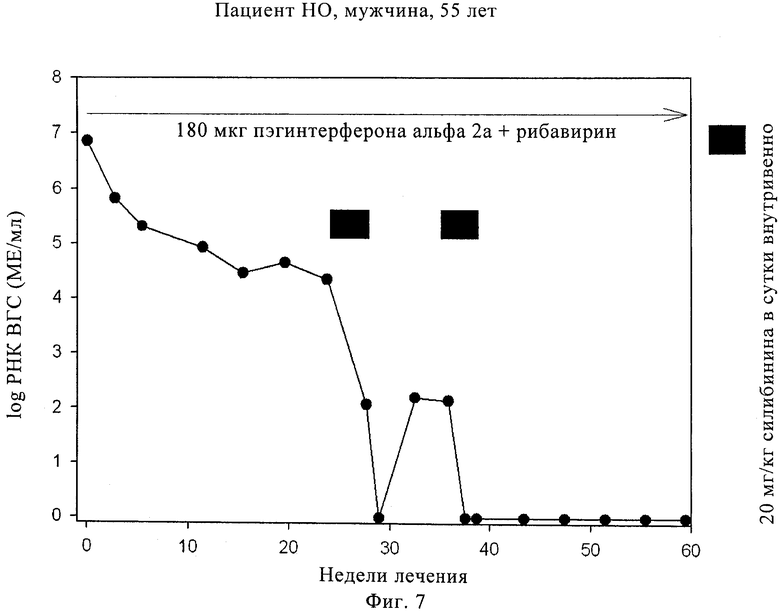
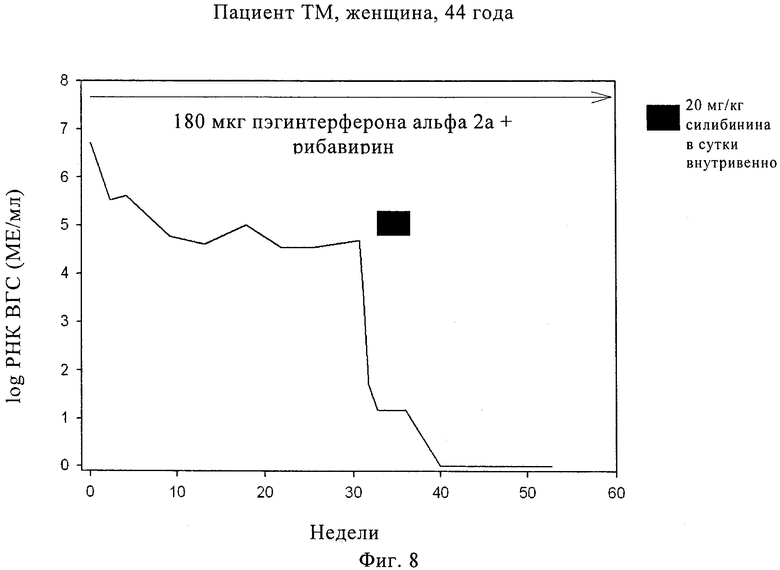
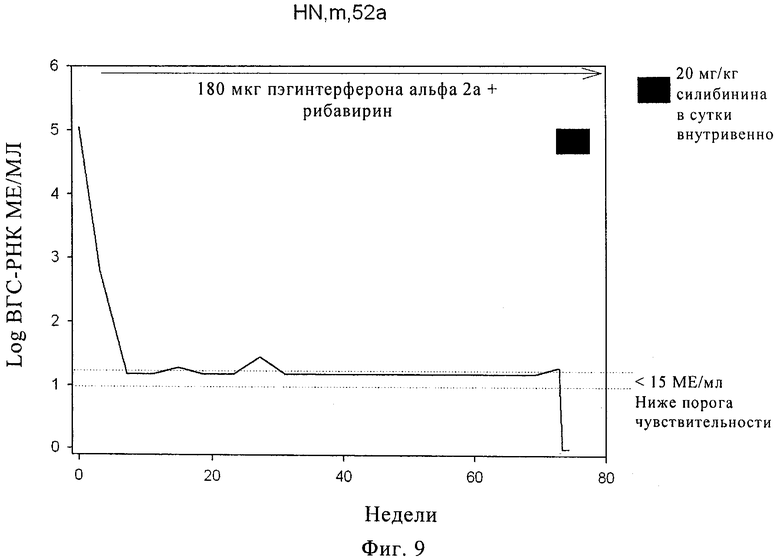
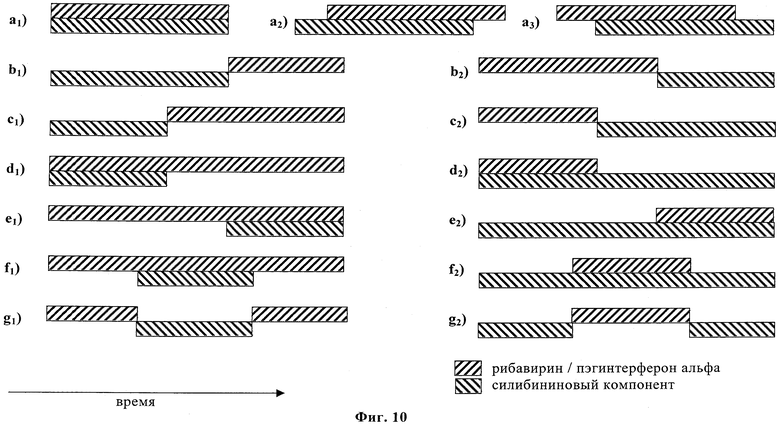
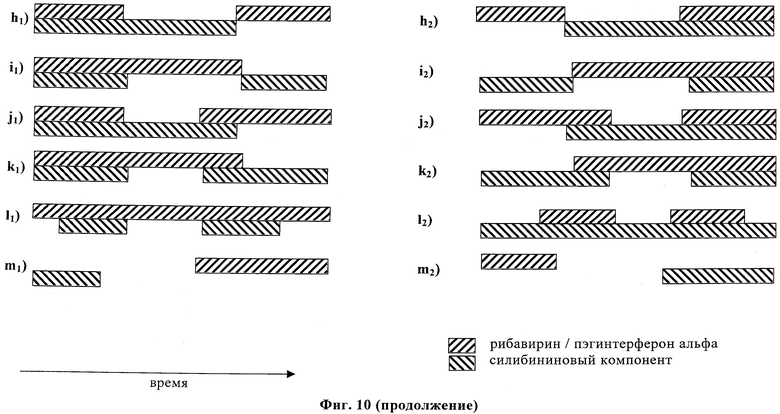
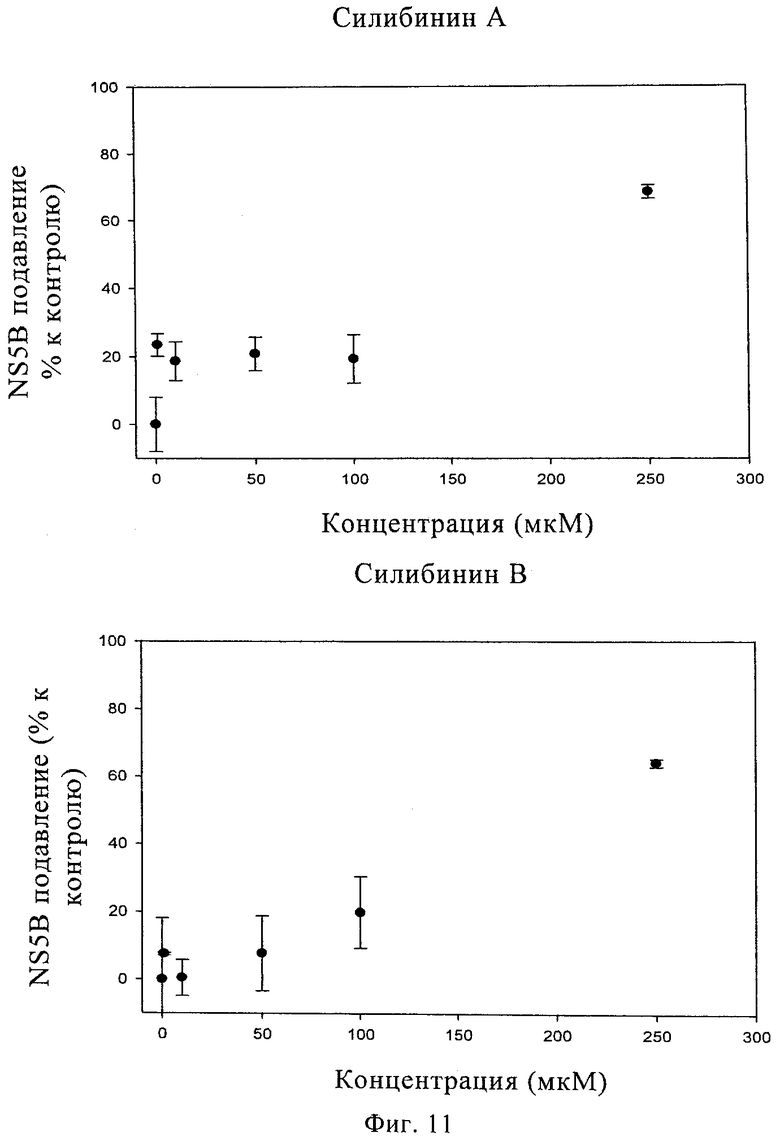
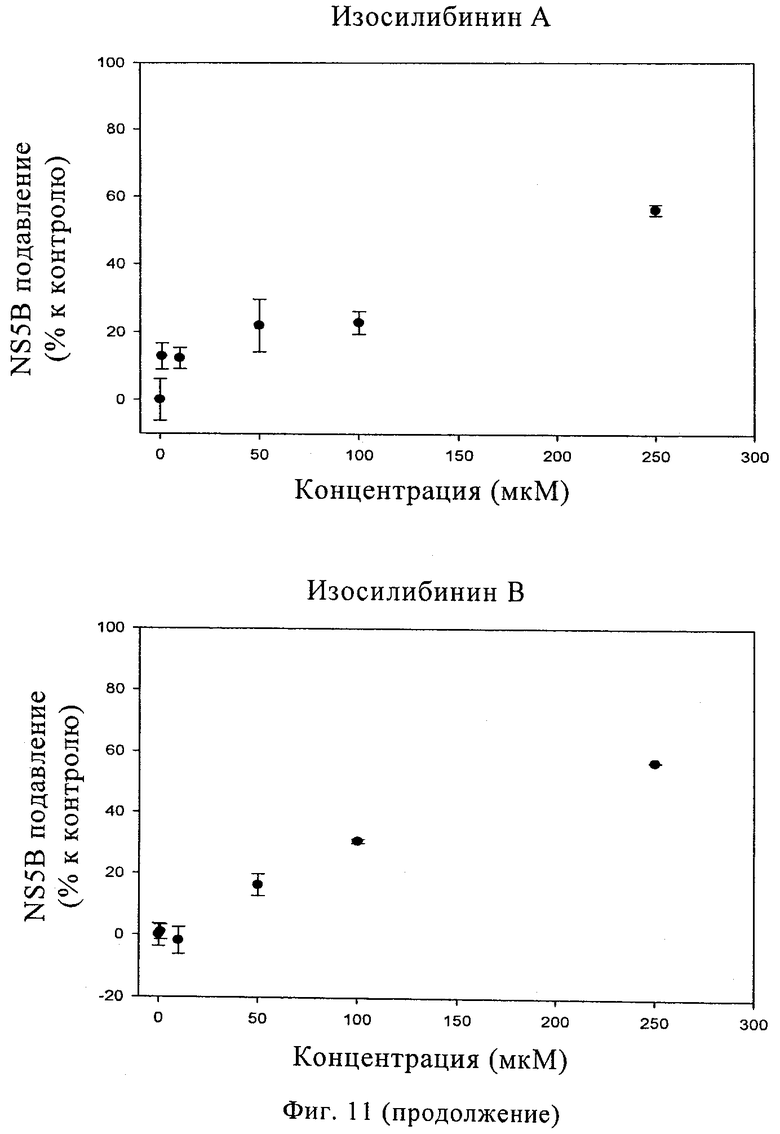
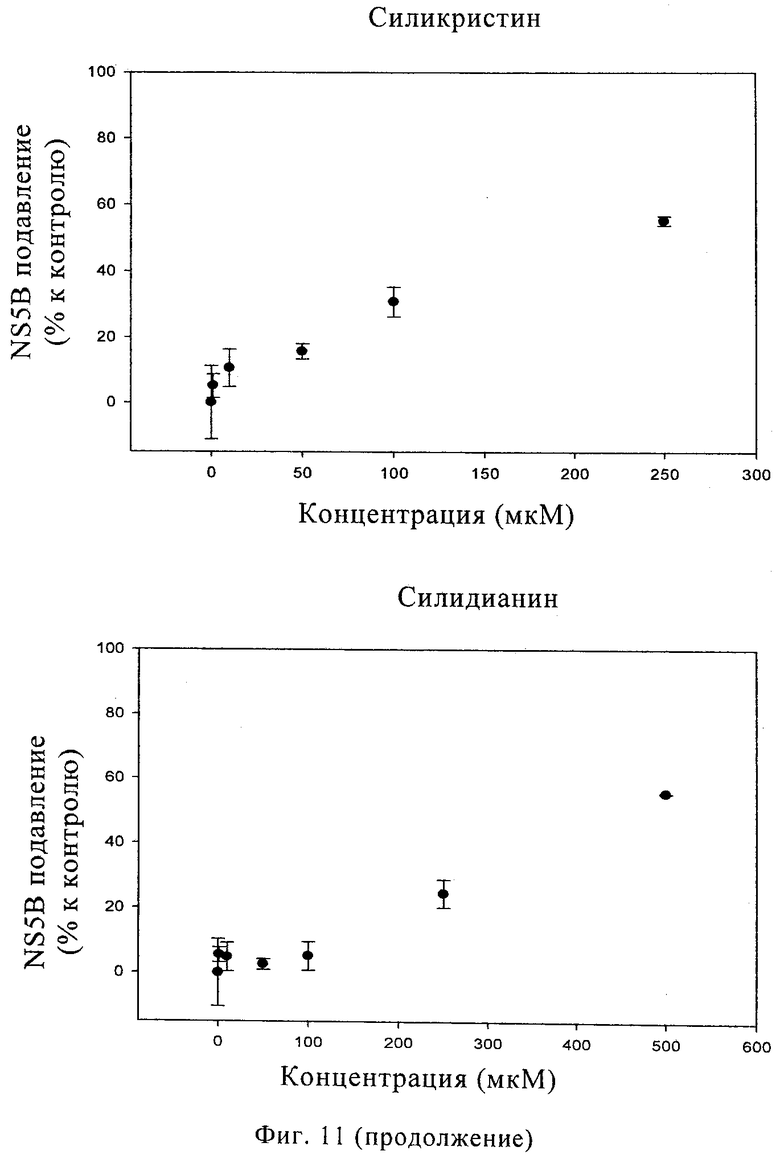
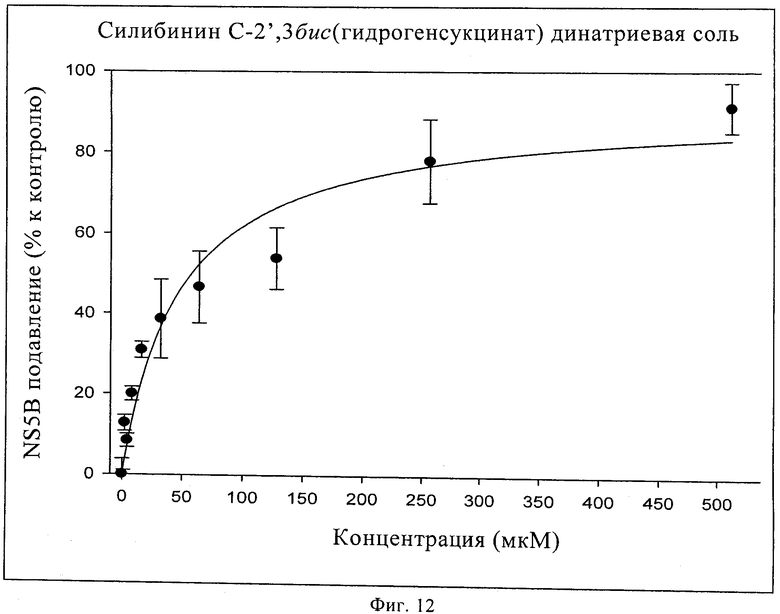
Предложены: применение силибининового компонента общей формулы (I) для получения лекарственного средства для парентерального введения для лечения вирусного гепатита, причем лекарственное средство необязательно содержит циклодекстрин и/или фосфолипид, и набор того же назначения, включающий указанный силибининовый компонент и другое лекарственное средство, представляющее собой один или несколько фармацевтических агентов: из аргинина глутамата, силимарина, цитиолона, эподемиола, орнитина оксоглурата, тидиацикаргинина, миоинозита, метионина и N-ацетилметионина, холина, орнитина аспартата, цианиданола, тиопронина, бетаина, цианокобаламина, лейцина, левулозы, ацикловира, идоксуридина, видарабина, рибавирина, ганцикловира, фамцикловира, валацикловира, цидофовира, пенцикловира, валганцикловира, бривудина, интерферона. Показано снижение вирусной нагрузки и реактивация пациентов после парентерального введения заявленного силибининового компонента. Лекарственное средство предпочтительно не содержит силидианина, и/или силикристина, и/или изосилибинина. 2 н. и 19 з.п. ф-лы, 12 ил., 5 пр., 12 табл.
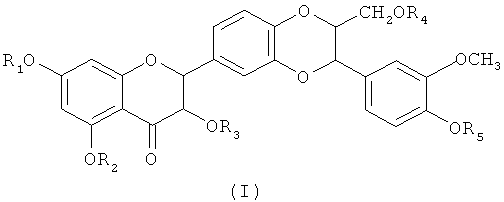
1. Применение силибининового компонента с общей формулой (I)

в которой R1, R2, R3, R4 и R5 независимо друг от друга выбраны из группы, состоящей из -Н, -SO3H, -РО3Н2, -СО-С1-С8-алкилен-ОН, -СО-С1-С8-алкилен-CO2H, -СО-С1-С8-алкилен-SO3H, -СО-С1-С8-алкилен-ОРО3Н2, -СО-С1-С8-алкилен-РО3Н2, -(С2-С3-алкилен-O)n-Н, где n = от 1 до 20, -CO-С1-С8-алкилен-N(C1-C3-алкил)3 +X-, где X- представляет фармацевтически допустимый анион,
или их фармацевтически допустимые соли,
для получения лекарственного средства, созданного для парентерального введения при лечении вирусного гепатита, причем лекарственное средство необязательно содержит циклодекстрин и/или фосфолипид.
2. Применение по п.1, причем силибининовый компонент представляет сложный эфир силибинина.
3. Применение по п.2, причем сложный эфир силибинина представляет силибинин-С-2',3-бис(гидрогенсукцинат) или его физиологически приемлемую соль.
4. Применение по п.1, причем лекарственное средство, по существу, не содержит силидианина, и/или силикристина, и/или изосилибинина.
5. Применение по п.1, причем вирусным гепатитом является гепатит В или гепатит С.
6. Применение по п.1, причем лекарственное средство переработано для инъекции или инфузии.
7. Применение по п.1, причем лекарственное средство переработано для внутривенного введения.
8. Применение по п.1, причем лекарственное средство не содержит ни одной из составляющих частей силимарина помимо силибининового компонента.
9. Применение по п.1, причем лекарственное средство содержит силибининовый компонент в дозе, составляющей по меньшей мере 50 мг по силибинину.
10. Применение по п.1, причем лекарственное средство содержит дополнительные фармацевтические агенты помимо силибининового компонента.
11. Применение по п.10, причем дополнительное лекарственное средство выбрано из группы, состоящей из аргинина глутамата, цитиолона, эпомедиола, орнитина оксоглурата, тидиацикаргинина, миоинозита, метионина и N-ацетил-метионина, холина, орнитина аспартата, цианиданола, тиопронина, бетаина, цианокобаламина, лейцина, левулозы, ацикловира, идоксуридина, видарабина, рибавирина, ганцикловира, фамцикловира, валацикловира, цидофовира, пенцикловира, валганцикловира, бривудина, интерферона альфа, интерферона бета, интерферона гамма, интерферона альфа-2а, интерферона альфа-2b, интерферона альфа-n1, интерферона бета-1а, интерферона бета-1b, интерферона альфакона-1, пэгинтерферона альфа-2b, пэгинтерферона альфа-2а и интерферона гамма-1b.
12. Применение по п.1 для снижения вирусной нагрузки у больных гепатитом.
13. Применение по п.1 для лечения вирусного гепатита у пациента, которому предстоит или который уже перенес пересадку печени.
14. Применение по п.1 для лечения вирусного гепатита у пациента, который не отвечает на лечение рибавирином/интерфероном.
15. Применение по п.1 для поддерживающего и/или превентивного лечения вирусного гепатита фармацевтическим агентом, выбранным из группы, состоящей из аргинина глутамата, силимарина, цитиолона, эпомедиола, орнитина оксоглурата, тидиацикаргинина, миоинозита, метионина и N-ацетилметионина, холина, орнитина аспартата, цианиданола, тиопронина, бетаина, цианокобаламина, лейцина, левулозы, ацикловира, идоксуридина, видарабина, рибавирина, ганцикловира, фамцикловира, валацикловира, цидофовира, пенцикловира, валганцикловира, бривудина, интерферона альфа, интерферона бета, интерферона гамма, интерферона альфа-2а, интерферона альфа-2b, интерферона альфа-n1, интерферона бета-1а, интерферона бета-1b, интерферона альфакон-1, пэгинтерферона альфа-2b, пэгинтерферона альфа-2а и интерферона гамма-1b.
16. Применение по п.1, причем после лечения вирусного гепатита указанным лекарственным средством лечат вирусный гепатит другим лекарственным средством.
17. Применение по п.1, причем лекарственное средство создано в виде составляющей части для последующего лечения, сначала лекарственное средство вводят на протяжении первого периода и впоследствии вводят другое лекарственное средство на протяжении второго периода.
18. Применение по п.17, причем первый период составляет по меньшей мере 2 суток.
19. Применение по п.16, причем другое лекарственное средство содержит один или несколько фармацевтических агентов, выбранных из группы, состоящей из аргинина глутамата, силимарина, цитиолона, эпомедиола, орнитина оксоглурата, тидиацикаргинина, миоинозита, метионина и N-ацетилметионина, холина, орнитина аспартата, цианиданола, тиопронина, бетаина, цианокобаламина, лейцина, левулозы, ацикловира, идоксуридина, видарабина, рибавирина, ганцикловира, фамцикловира, валацикловира, цидофовира, пенцикловира, валганцикловира, бривудина, интерферона альфа, интерферона бета, интерферона гамма, интерферона альфа-2а, интерферона альфа-2b, интерферона альфа-n1, интерферона бета-1а, интерферона бета-1b, интерферона альфакон-1, пэгинтерферона альфа-2b, пэгинтерферона альфа-2а и интерферона гамма-1b.
20. Применение по п.16, причем другое лекарственное средство создано для перорального введения.
21. Набор для лечения вирусного гепатита, включающий по меньшей мере одно лекарственное средство по одному из пп.1-11 и по меньшей мере одно лекарственное средство по п.19 или 20.
| Mayer KE et al | |||
| Silymarin treatment of viral hepatitis: a systematic re-view | |||
| J Viral Hepat | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Polyak SJ et al | |||
| Inhibition of T-cell inflammatory cytokines, hepa-tocyte NF-kappaB signaling, and HCV infection by standardized Silymarin. | |||
Авторы
Даты
2013-05-27—Публикация
2008-11-14—Подача