Изобретение относится к медицине, в частности к химико-фармацевтической промышленности, может быть использовано для получения нового средства на основе сухого экстракта из травы аврана лекарственного (Gratiola officinalis L.), обладающего биологической активностью.
В настоящее время достаточно эффективно разрабатываются способы получения композиций лекарственных растений с наименьшими побочными эффектами и, вместе с тем, с максимально возможным положительным фармакологическим действием. Значительной биологической активностью могут обладать алкалоидсодержащие, ядовитые растения, которые за счет содержания алкалоидов, могут применяться только в незначительных количествах и под строгим контролем врача. К таким растениям относится, например, авран лекарственный.
Авран лекарственный (Gratiola officinalis L.) - травянистое растение семейства Норичниковые, широко распространенное в Евразии и Северной Америке. Растение ядовито. Используются в народной медицине при сердечной недостаточности, болезнях печени, при хронических заболеваниях кожи, а также как противоглистное средство. Домашние животные распознают авран лекарственный и на пастбищах его не поедают, но это растение может попасть к ним вместе с сеном и вызвать отравление; особенно чувствительны к аврану лошади.
Известен способ получения водного извлечения из травы аврана лекарственного, обладающего положительным эффектом, но ядовитым даже в небольшом количестве. Водное извлечение получается при длительном (в течение 2 часов) кипячении и употребляется в крайне малых дозах в составе сбора Здренко (входит 31 растение), используемого как симптоматическое средство при лечении папилломатоза мочевого пузыря и анацидных гастритов (Библиотечка лекарственных растений, том 2, составитель Зимин В.Н., Санкт-Петербург, АО «Дорваль», 1992, с.181-182).
Недостатками водного извлечения являются его высокая токсичность за счет присутствия ядовитых соединений и недостаточное количество выхода целевых продуктов, в частности флавоноидов, а также трудность расчета точной дозировки для дальнейшего использования.
Известен способ получения 10% спиртовой настойки листьев аврана лекарственного, которая применяется в крайне малых дозах в связи со значительным количеством побочных эффектов и содержит ядовитые гликозиды грациозид (грациолин), грациотоксин, кукурбитациновый гликозид - элатерицид, жирное масло, эфирное масло, сапонины, яблочную и бетулиновую кислоты, углеводы (стахиоза), терпеноиды (элатеризид, дезацетилэлатеринид, кукурбитацин Е и I), карденолиды, сапонины, флавоноиды (лигнозид, изолигнозид, апигенин, космосиин, лигнозид, аврозид, изоаврозид, неоаврозид, изонеоаврозид) и алкалоиды (0.2%) (Куркин В.А. Фармакогнозия: Учебник для студентов фармацевтических вузов. Самара: ООО «Офорт» СамГМУ, 2004. 1180 с.; Алефиров А.Н. Фитотерапия против онкологии. Издательство: Крылов. Серия: Медицина XXI века. 2010 г. 240 с.: http://www.travolekar.ru/articles.php; http://fitocenter.ru/). В научной медицине спиртовая настойка листьев аврана назначается при асците сердечного происхождения (лечебный эффект обусловлен действием кукурбитацина элатеризида, кукурбитацинового гликозида). Настойка действует на сердце подобно дигиталису; малые дозы настойки повышают чувствительность зрения к зеленому цвету.
Недостатками 10% спиртовой настойки являются ее высокая токсичность за счет присутствия ядовитых соединений, которые выходят в водную часть настойки, и недостаточное количество выхода целевых продуктов, в частности флавоноидов, а также трудность расчета точной дозировки для дальнейшего использования.
Все полученные ранее извлечения из сырья аврана обладали достаточно сильной токсичностью, поэтому при внутреннем применении использовались вместе со слизистыми отварами с большой осторожностью и под обязательным врачебным контролем (http://www.ayzdorov.ru/tvtravnik_avran.php).
Задачей данного способа является получение сухого экстракта из ядовитого растительного сырья (аврана лекарственного), не содержащего токсичные соединения алкалоиды и гликозиды, обогащенного флавоноидами и обладающего биологической активностью.
Нами разработан способ получения сухого экстракта из травы аврана лекарственного, содержащего новую, ранее не известную для данного растения биологически активную композицию, обогащенную значительным количеством флавоноидов и лишенную алкалоидов, гликозидов. По сравнению со способом получения 10% спиртовой настойки разработанный нами способ позволяет получить нетоксичный раствор сухого экстракта и в то же время содержащий новые, ранее не известные для данного растения химические соединения (кверцетин), обладающие высокой биологической активностью, в частности антиоксидантной, что может найти широкое применение в онкологии для снижения побочных эффектов от химиотерапии. Положительный эффект полученного экстракта заключается в резком снижении токсичности (за счет отсутствия в экстракте ядовитых веществ) и повышении степени извлечения целевых продуктов.
Сущность способа заключается в экстракции надземной части аврана лекарственного 96% этиловым спиртом, фильтровании, упаривании спиртового экстракта, растворении сухого экстракта в теплой дистиллированной воде, охлаждении, ускоренной очистке хлороформом с помощью центрифуги. Выбор 96% этилового спирта в качестве основного экстрагента обусловлен значительным выходом флавоноида кверцетина и снижением выхода алкалоидов. Растворение сухого экстракта в дистиллированной воде необходимо для образования водной фазы с целью дальнейшей очистки хлороформом. Выпаривание и сгущение экстракта проводили при температуре не выше 55-60°C для предотвращения разрушения флавоноидов. Технический результат заключается в получении новой для данного растения композиции биологически активных веществ, Количественный выход сухого экстракта из 10 г сухого сырья травы аврана - в среднем 225±11,06 мг сухого экстракта.
Описание способа. Трава аврана измельчается до получения частиц не более 3 мм, что способствует увеличению выхода целевых продуктов. 10 г измельченного сырья помещается в колбу, добавляется 100 мл этилового спирта 90-96% (более низкая концентрация спирта способствует выходу водорастворимых токсичных соединений алкалоидов, гликозидов и снижает выход целевых продуктов), на водяной бане доводится до кипения и кипятится 14-15 мин (менее 14-15 минут не способствует выходу целевых продуктов, а более может приводить к их разрушению). Сливается спирт из колбы, экстракт процеживается. Затем профильтровывается, для удаления крупных балластных частиц. Спиртовой экстракт сливаются в стеклянную емкость и выпаривается досуха в термостате при температуре не выше 55-60°C (при более высоких температурах происходит разрушении целевых продуктов). К выпаренному экстракту добавляют 8 мл (4/5 части от общего объема) дистиллированной воды 40-50°C, тщательно перемешивается, затем прибавляют 2 мл хлороформа (1/5 части от общего объема); встряхивается до однородности, охлаждается до комнатной температуры и центрифугируется со скоростью 1500 оборотов в минуту, что позволяет получить наиболее полное разделение на водную фракцию - целевых продуктов и хлороформную фракцию токсичных продуктов, содержащих неполярные примеси, такие как хлорофилл и др., а также алкалоиды и гликозиды. Водная фракция собирается с помощью разделительной воронки или шприца, снова высушивается в чашке Петри, что позволяет получить сухой остаток целевых продуктов и в дальнейшем дает возможность определять точную концентрацию целевых продуктов и рассчитывать точную дозировку для экспериментов как in vitro, так и in vivo, а также позволяет длительное время хранить экстракт до начала применения.
Нами исследовался полученный сухой экстракт из аврана лекарственного методом хромато-масс-спектрометром, модели Trace GC - Trace DSQ (фирма "ThermoFinnigan", США). В рамках выполненной работы были выделены органические вещества, вероятность обнаружения которых соответствует параметрам «превосходное и хорошее соответствие» (Таблица 1).
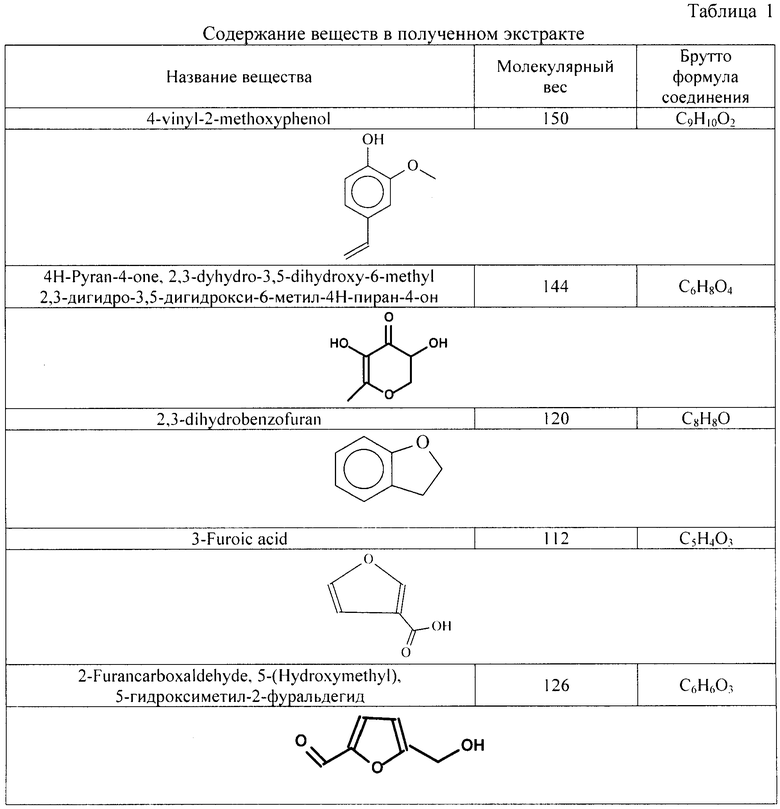
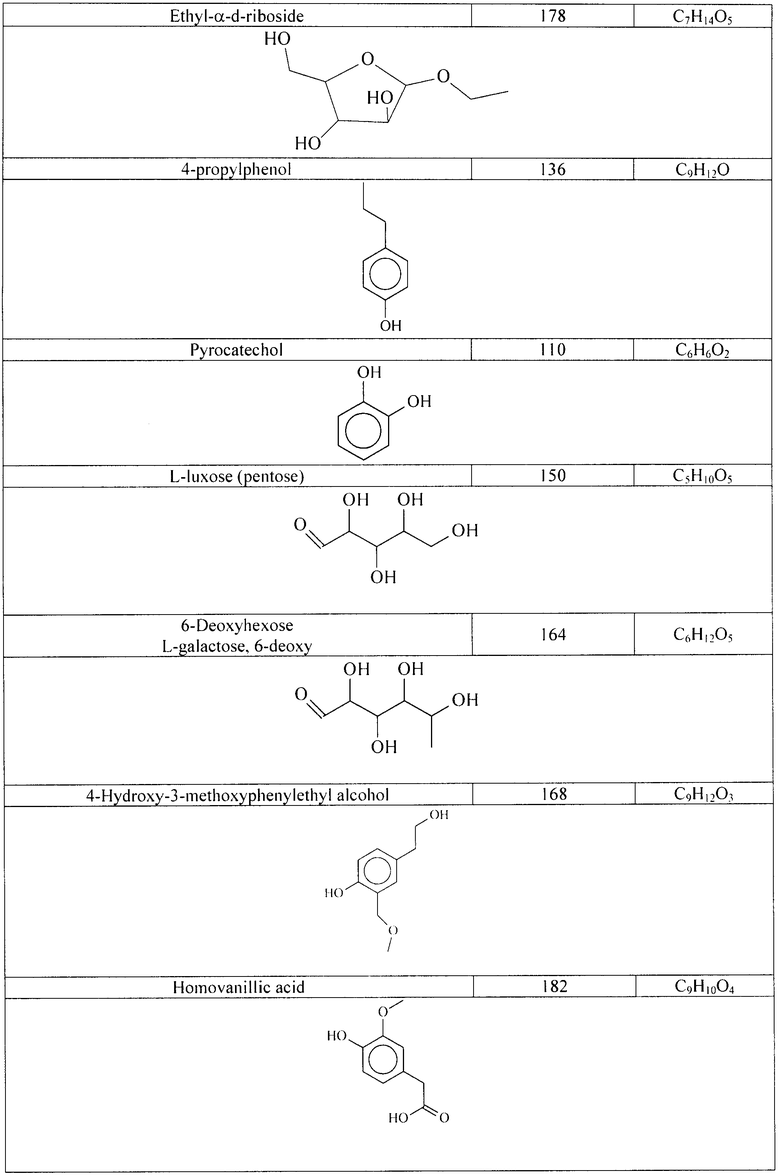
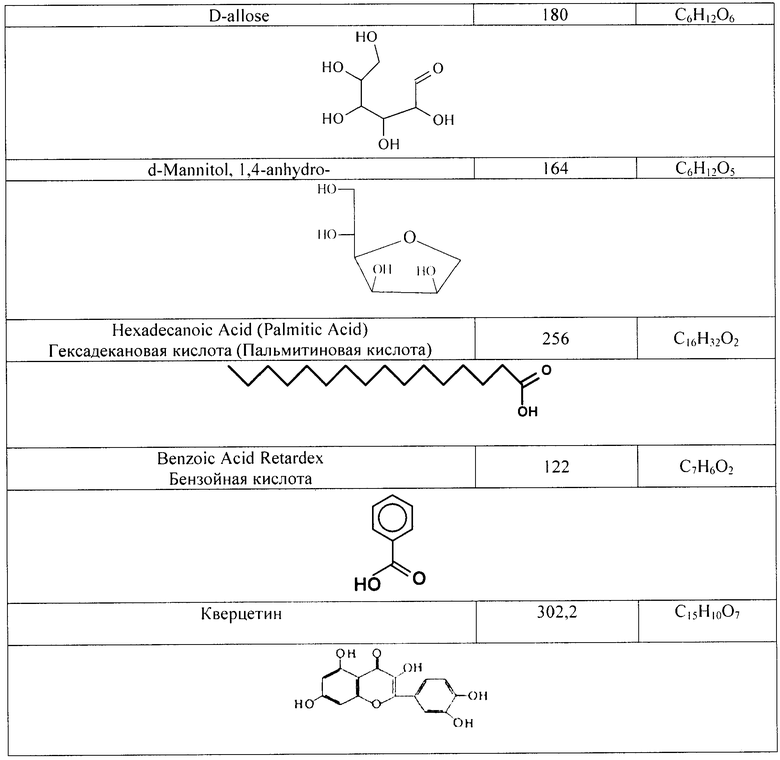
Таким образом, лабораторным методом было подтверждено отсутствие токсичных соединений (алкалоидов и гликозидов) и выявлено наличие новых, ранее не описанных для данного растения химических соединений, в частности флавоноида-кверцетина, а также других фенольных соединений.
Так как наиболее ценным на наш взгляд является кверцетин, то мы провели определение количественного содержания методом жидкостной хроматографии. Использована стандартная методика проведения «Высокоэффективная жидкостная хроматография» на приборе «Стайер UV/VIS» (фирма «Аквилон») в изократическом режиме, со спектрофотометрическим детектором (Золотов Ю.А. Аналитическая химия: фрагменты картины. - М.: изд-во ОНТИ ГЕОХИ РАН, 1999. 144 с.).
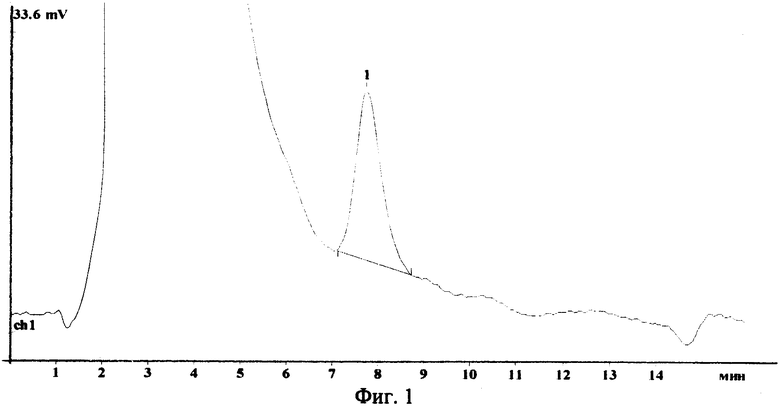
На фигуре 1 представлена хроматограмма модельного раствора кверцетина, концентрации 10 мкг/мл,
на фигуре 2 - хроматограмма исследуемого раствора кверцетина, концентрации - 10 мкг/мл.
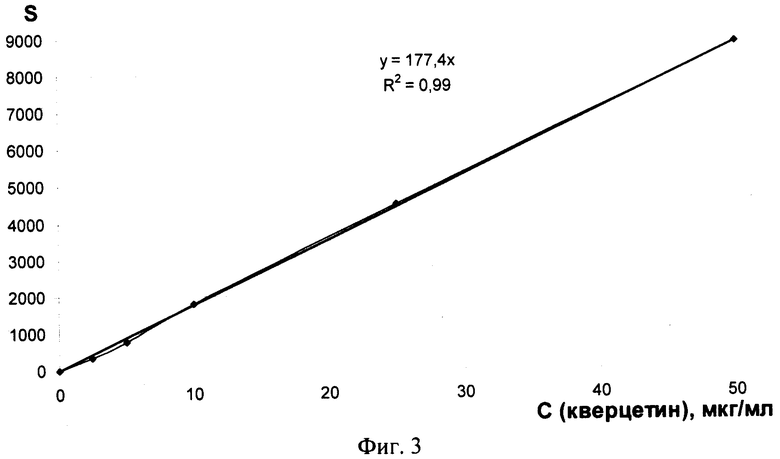
На фигуре 3 представлен градуировочный график зависимости сигнала хроматографа (мВ·сек) от концентрации кверцетина, построенный в диапазоне концентраций 0-50 мкг/мл. В результате среднее значение полученных определений кверцетина в смеси составило 70 мкг/мл. Количество кверцетина в сухом остатке составило 350 мкг.
Нами была проведена экспериментальная работа на лабораторных крысах по определению класса токсичности полученного сухого экстракта аврана по установлению LD50.
Перед началом эксперимента, который предусматривал введение экстракта лабораторным животным (белым лабораторным крысам), сухой экстракт разводили до концентрации экстракта 45 мг/мл для перорального введения, 90 мг/мл для внутримышечного введения и для внутрибрюшинного введения. Полученный водный раствор сухого экстракта аврана лекарственного вводили крысам с помощью шприца перорально, внутримышечно и внутрибрюшинно. Состояние животных оценивалась по четырехбалльной шкале по таким показателям, как: состояние шерсти, двигательная активность, болевая реакция, изменение мышечного тонуса, почесывания за 1 минуту, температура тела (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ, Хабриев Р.У., Москва, 2005).
Животным весом 220±12,3 г перорально вводился раствор сухого экстракта в дозировке 205 мг/кг экстракта. После чего в течение суток проводилось наблюдение за состоянием животных. Животным весом 220±12.3 г внутримышечно вводился раствор сухого экстракта в дозировке 1323 мг/кг, после чего в течение суток проводилось наблюдение за состоянием животных. Животным весом 220±12,3 г внутрибрюшинно вводился раствор сухого экстракта в дозировке 1663 мг/кг, после чего в течение суток проводилось наблюдение за состоянием животных.
Через сутки ни одно животное не умерло, а состояние животных изменилось по значению таких показателей, как состояние шерсти (увеличилось на два балла до четырех в экспериментальной группе по сравнению с контрольной), двигательная активность (увеличилось на один балл до четырех в экспериментальной группе по сравнению с контрольной), болевая реакция (снизилась на один балл до одного в экспериментальной группе по сравнению с контрольной), мышечный тонус (увеличился на один балл до четырех в экспериментальной группе по сравнению с контрольной), почесывания за 1 минуту (увеличилось на один балл до двух в экспериментальной группе по сравнению с контрольной), температура тела (снизилась в среднем с 36,9 до 35,8°C).
Таким образом, для сухого экстракта аврана лекарственного не были определены LD50 при пероральном, внутримышечном и внутрибрюшинном введении, так как было установлено, что при пероральном введении экстракта в дозировке 205 мг/кг; внутримышечном введении в дозировке 1323 мг/кг и внутрибрюшинном - в дозировке 1663 мг/кг сухой экстракт аврана лекарственного не вызывает гибели крыс.
Так как указанные нами дозировки экстракта, не вызывающие гибели животных, согласно ГОСТу 12.1.007-76 и СанПиН 2.1.4.1074-01 соответствуют значениям LD50 третьего класса опасности от 151 до 5000 мг/кг (мало опасные химические вещества), свидетельствуют о том, что LD50 полученного нами экстракта аврана будет значительно выше, по крайней мере, третьего класса токсичности (малоопасные химические вещества).
Полученная нами новая композиция в виде сухого экстракта из травы аврана лекарственного не содержит в себе токсичные соединения алкалоиды и гликозиды, что ограничивало применение данного растения, но содержит в больших количествах кверцетин, который, как известно, обладает множеством полезных биологических свойств, и другие флавоноиды, которые могут потенцировать свойства кверцетина или иметь собственные, уникальные биологические свойства.
Пример. Траву аврана измельчали и просеивали через сито с размером ячеек не более 3 мм. Взвесили 10 г измельченного сырья, поместили его в колбу объемом 500 мл, добавили 100 мл этилового спирта 96%, на водяной бане довели до кипения и кипятили в течение 14-15 мин. Экстракт из колбы процедили в стеклянную емкость через 4 слоя широкого бинта, остаток растительного материала тщательно отжали, залили еще 100 мл этилового спирта 96%. Довели до кипения и снова профильтровали в ту же стеклянную емкость. Полученный экстракт выпарили досуха в термостате при температуре не выше 55-60°C. В стеклянную емкость с выпаренным экстрактом добавили 8 мл дистиллированной воды, затем с помощью шприца перенесли полученный раствор в пластиковую центрифужную пробирку объемом 11 мл, добавили 2 мл хлороформа, встряхнули несколько раз до однородности, остудили до комнатной температуры и центрифугировали в течение 15 мин (для удаления неполярных примесей (хлорофилла) и др.) при скорости 1500 оборотов в минуту. Водную фракцию собирали с помощью шприца, поместили в заранее взвешенную чашку Петри, высушили и в таком виде хранили до начала эксперимента. Вес сухого экстракта подсчитали как разницу между весом взвешенной чашкой Петри с сухим экстрактом и весом пустой чашки Петри. Получили 225 мг сухого экстракта аврана.
Как видно из описания и примера, способ позволил получить нетоксичный сухой экстракт из травы аврана лекарственного, содержащий фенольные соединения, в частности неизвестный ранее для аврана лекарственного кверцетин. Способ уникален тем, что позволяет получать из сырья ядовитых растений, содержащих, в том числе, и флавоноиды, нетоксичную композицию, обладающую высокой биологической активностью. Кроме того, предложенный нами метод легко воспроизводим в стандартных лабораториях, позволят получать большой выход целевых продуктов и хранить полученный сухой экстракт в течение длительного времени.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2013 |
|
RU2519769C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2549477C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ, ЖАРОПОНИЖАЮЩИМ И АНТИМИКРОБНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2535155C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 2018 |
|
RU2714930C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕВОЙ КАХЕКСИИ | 2015 |
|
RU2578440C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2017 |
|
RU2657423C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИЗБИРАТЕЛЬНЫМ ДЕЙСТВИЕМ НА ОПУХОЛЕВЫЕ КЛЕТКИ, АКТИВИРУЮЩЕЕ ИХ АПОПТОЗ И ПРЕПЯТСТВУЮЩЕЕ ФОРМИРОВАНИЮ ИХ РЕЗИСТЕНТНОСТИ | 2018 |
|
RU2694547C1 |
| Средство, обладающее противогрибковым действием в отношении грибов рода Candida | 2017 |
|
RU2657779C1 |
| Способ комбинированной терапии рака печени РС-1 в эксперименте | 2020 |
|
RU2734143C1 |
| СРЕДСТВО, ВЫЗЫВАЮЩЕЕ В ЭКСПЕРИМЕНТАХ IN VIVO ЗАМЕЩЕНИЕ ОПУХОЛЕВОЙ ТКАНИ СОЕДИНИТЕЛЬНОЙ И ПЕРЕВОДЯЩЕЕ КЛЕТКИ ОПУХОЛИ ИЗ ФАЗЫ G1 КЛЕТОЧНОГО ЦИКЛА В СОСТОЯНИЕ ПОКОЯ G0 | 2018 |
|
RU2731105C2 |
Изобретение относится к фармацевтической промышленности и касается способа получения сухого экстракта из травы аврана лекарственного. Способ получения сухого экстракта из растительного сырья, обладающего биологической активностью, включающий измельчение травы аврана лекарственного, экстракцию спиртом 96% на водяной бане, выпаривание экстракта, добавление хлороформа, удаление хлороформа, отделение водной фазы и высушивания, при определенных условиях. Сухой экстракт, полученный вышеописанным способом, является не токсичным и обогащенным флавоноидом-кверцетином, а также рядом других фенольных соединений. 3 ил., 1 табл., 1 пр.
Способ получения сухого экстракта из растительного сырья, обладающего биологической активностью, включающий измельчение травы аврана лекарственного, экстракцию спиртом 96%, выпаривание экстракта, добавление хлороформа, удаление хлороформа, отличающийся тем, что экстракцию спиртом проводят на водяной бане до кипения и кипятят в течение 14-15 мин, выпаривают при температуре 55-60°С, выпаренный экстракт разводят сначала дистиллированной водой 40-50°С, затем добавляют хлороформ в пропорции 4/5 части воды и 1/5 части хлороформа, охлаждают до комнатной температуры и центрифугируют со скоростью 1500 оборотов в минуту в течение 15 мин, далее отделяют водную фракцию и высушивают ее.
| GB 1063118 А, 30.03.1967 | |||
| Пономарев В.Д | |||
| Экстрагирование лекарственного сырья.: Медицина, 1976, с.110-122 | |||
| US 20020132021 A1, 19.09.2002. |
Авторы
Даты
2013-05-27—Публикация
2012-02-15—Подача