Изобретение относится к медицине, а именно к акушерству, и предназначено для прогнозирования отслойки хориона и плаценты на ранних сроках при полиморфизме генов PAI-1.
Отслойка хориона и плаценты на ранних сроках беременности в общей популяции составляет 3%, у женщин с привычной потерей беременности может достигнуть 10-15%. Наиболее часто встречаются субхориальные отслойки в среднем в 7 недель беременности, что соответствует наиболее активной фазе инвазии цитотрофобласта в стенки спиральных артерий [3].
Наличие отслоек сопровождается наружным кровотечением в 71%, бессимптомным течением - в 29%. Если не происходит гибель эмбриона (плода), то в дальнейшем возможно развитие плацентарной недостаточности - в 24% случаев, преждевременных родов - в 16-19%, преэкламсии - в 8%, задержки развития плода - в 7%, дистресс-синдрома у новорожденного - в 19%. Частота кесарева сечения у данного контингента беременных составляет 27% [2].
Существенное значение в процессе инвазии цитотрофобласта играет соотношение фибринолитических и антифибринолитических компонентов системы гемостаза на локальном (эндометрий) уровне. Процесс регуляции фибринолиза зависит от активности активаторов плазминогена тканевого и урокиназного типа (t-PA и u-РА) и от уровня синтеза и секреции ингибиторов активации плазминогена (PAI-1 и PAI-2). [1, 5]
PAI-1 ответственен не только за повышение депозиции фибрина в маточных сосудах и снижении маточно-плацентарного кровотока, ему принадлежит также важная роль в снижении степени инвазии трофобласта в ранние сроки беременности. Имеется также связь между ранними преэмбриотическими потерями и уровнем PAI-1, что в основном связано с дефектами имплантации [4].
При подготовке к имплантации под влиянием прогестерона в эндометрии происходит повышение содержания PAI-1, тканевого фактора и снижение уровня активаторов плазминогена тканевого и урокиназного типов (t-PA и u-РА) и других протеаз, необходимых для разрушения экстрацеллюлярного матрикса в процессе имплантации. В условиях гипофибринолиза, в частности, связанных с полиморфизмом генов PAI-1 происходит десинхронизация локальных процессов фибринолиза и фибринообразования при имплантации. В такой ситуации протеаз, синтезируемых бластоцистой, становится недостаточно для разрушения экстрацеллюлярного матрикса и адекватного внедрения в эндометрий. В связи с этим происходит образование ретрохориальных отслоек наиболее часто в сроки 8,3±0,4 недели [2].
Ингибитор активатора плазминогена (PAI-1) образуется в клетках эндотелия, гепатоцитах, а также в неактивной форме может высвобождаться из тромбоцитов. Концентрация PAI-1 зависит как от внешних (уровень триглицеридов [8], курение [9]), так и внутренних (генетических) факторов. Известен полиморфизм в промоторной области гена PAI-1. Различия в фенотипических проявлениях генотипа PAI-1 обусловлены тем, что с промотором гена 5G может связываться как активатор, так и репрессор, а с промотором гена 4G - только активатор. Поэтому ген 5G, легко включается и легко выключается, а ген 4G легко включается, но слабо выключается [6, 7].
Полиморфный вариант 4G сопровождается повышенной экспрессией гена и повышением уровня PAI-1 в крови [9]. В результате снижается активность фибринолитической системы. В крови людей, имеющих вариант 4G/4G, концентрация PAI-1 значительно выше, чем при вариантах 5G/4G и 5G/5G.
Задача изобретения - повысить эффективность прогнозирования отслойки хориона и плаценты на ранних сроках беременности на основании определения полиморфизма гена PAI-1.
Поставленная задача решается тем, что на основании определения полиморфизма гена PAI-1 вне беременности с высокой степенью вероятности возможно прогнозирование отслойки хориона и плаценты на ранних сроках беременности и проведение лечебно-профилактических мероприятий.
Определение полиморфизма гена PAI-1 необходимого производить у женщин:
1) с метаболитическим синдромом;
2) при наличии репродуктивных потерь;
3) при наличии плацентарной недостаточности в анамнезе;
4) при наличии преэкламсии в анамнезе.
Практически способ осуществляется следующим образом:
Материалом для проведения исследования является периферическая кровь. Взятие крови для исследования осуществляется путем пункции кубитальной вены. В качестве антикоагулянта используется ЭДТА. Допустимо также использовать цитрат.
1-й Этап: Выделение ДНК
Для выделения ДНК используется комплект реагентов ПРОБА-РАПИД-ГЕНЕТИКА или ПРОБА-ГС-ГЕНЕТИКА (000 «НПО ДНК-Технология», Россия)
Полученный препарат ДНК можно хранить до 7 суток при температуре 2-8°C, при температуре минус 20°C до одного месяца.
2-й Этап. Проведение реакции амплификации
Для проведения амплификации используется комплект реагентов для определения генетических полиморфизмов, ассоциированных с нарушениями функций сердечно-сосудистой системы «КардиоГенетика» (ООО «НПО ДНК-Технология», Россия).
1. Внести в промаркированные пробирки по 20 мкл соответствующей смеси для амплификации.
2. Приготовить в отдельной пробирке смесь ПЦР-буфера и Taq-AT полимеразы. Добавить в каждую пробирку со смесью для амплификации по 10 мкл смеси ПЦР-буфера и Taq-AT полимеразы.
3. Добавить в каждую пробирку по одной капле (20 мкл) минерального масла.
4. Добавить в соответствующие пробирки по 5,0 мкл анализируемого препарата ДНК.
5. Добавить в пробирки, предназначенные для «К-», по 5,0 мкл отрицательного контрольного образца, прошедшего этап выделения ДНК.
6. Центрифугировать пробирки на микроцентрифуге/вортексе в течение 1-3 сек.
7. Установить пробирки в блок детектирующего амплификатора, заполнить протокол в программном обеспечении детектирующего амплификатора и запустить программу амплификации.
Регистрация и учет результатов ПЦР проводится автоматически программным обеспечением для амплификаторов детектирующих.
Результаты испытаний
Для оценки информативности данного метода обследовано 67 женщин с синдромом привычной потери беременности с учетом особенностей полиморфизма генов PAI-1. Средние сроки выявления субхориальных отслоек составляли 8,3±0,4 недели, средний объем - 1,32±0,25 см2. Средние сроки выявления субамниотических отслоек составляли 12,1±0,5 недель, средний объем - 17,7±6,0 см2. При субхориальных отслойках гипоплазия хориона встречалась в 4 раза чаще, чем при субамниотических (p>0,01).
Субхориальные/субамниотические отслойки в 2 раза чаще встречались среди носительниц полиморфизма PAI-1 (4G4G и 4G5G), чем в группе PAI-1 (5G5G).
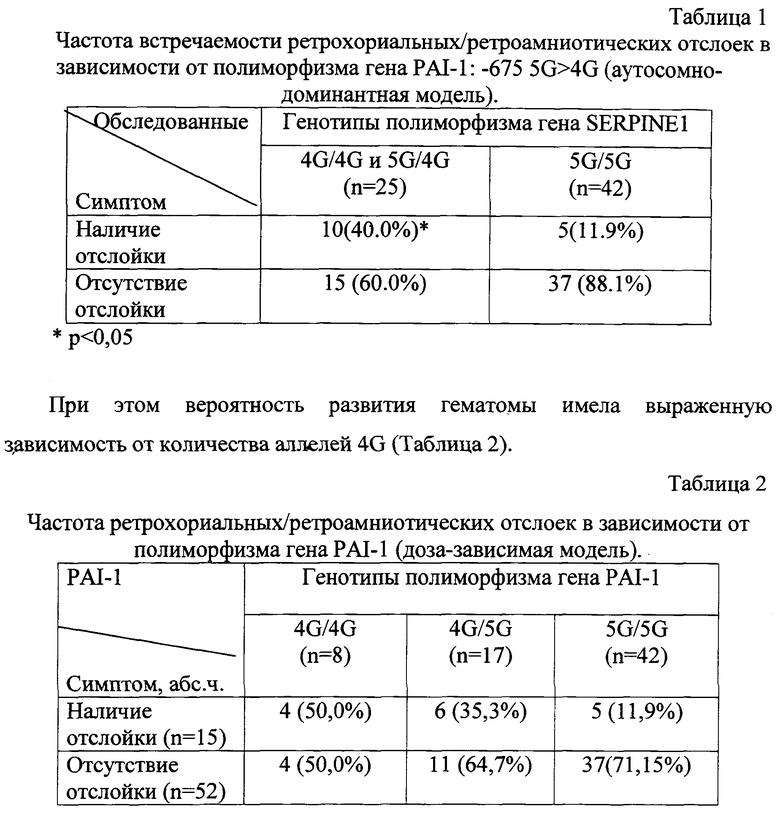
При генотипах 4G5G отслойки встречались в 1,5 раза чаще, чем при генотипе 4G4G (p<0,05).
Отношение шансов (OR) образования отслоек при носительстве аллели 4G при гетерозиготном генотипе полиморфизма гена PAI-1 (4G/5G) равнялось 4,04 (1,06-15,34, р=0.062) при 95% конфиденциальном интервале (95% CI 1,06-15,34, р=0.062). При гомозиготном генотипе полиморфизма гена PAI-1 (4G/4G) отношение шансов (OR) равнялось 7.4 (95% CI 1.51-36.33, p=0.026).
Для решения вопроса о влиянии 4G аллели на образование ретрохориальных/ретроамниотических отслоек были рассчитаны частоты образования отслоек в зависимости от генотипа. Полученные результаты отражены в таблице 3.
Как следует из представленных в таблице 3 данных, частота образования ретрохориальных/ретроамниотических отслоек «дозозависима» от аллели 4G (p<0,05, коэффициент достоверности аппроксимации R2=0,98).
В результате проведенного исследования была установлена высокая прогностическая значимость определения полиморфизма генов PAI-1 при развитии отслойки хориона/плаценты на ранних сроках беременности.
В соответствии с полученными ранее данными при наличии полиморфизма генов PAI-1 и образование ретрохориальных/ретроамниотических отслоек в ранние сроки беременности с лечебно-профилактической целью следует использовать селективные ингибиторы фибринолиза (транексам) в сочетании с антиагрегантами (курантил). При наличии тромбофилических состояний возможно одновременное назначение антифибринолитиков и низкомолекулярных гепаринов. Наряду с общепринятыми методами терапии подобная тактика позволяет снизить частоту развития плацентарной недостаточности, преэкламсии, преждевременных родов и ряда других осложнений [2].
Ниже следует пример, который иллюстрирует способ по изобретению.
Беременная И., 30 лет, обратилась на обследование и подготовку к беременности. Наследственность не отягощена. Из соматических заболеваний: хронический цистит, хронический панкреатит. Аллергологический анамнез не отягощен. Менструальная функция с 13 лет через 28 дней по 6 дней, без особенностей.
Гинекологические заболевания: бактериальный вагиноз.
Имела 3 самопроизвольные потери беременностей в сроках 8-9 недель, 7-8 недель и 5-6 недель. Обследование вне беременности:
1. Бак. посев из цервикального канала - роста микроорганизмов не обнаружено.
2. Гормональный профиль - в пределах N
3. Гемостазиограмма - в пределах N
4. Спектр антифисфолипидных антител и антител к ХГЧ - в пределах N.
5. Кариотип супругов - в пределах N
6. HLA типирование I и II классов - отклонений нет.
7. Гомоцистеин - в пределах N
8. Диагностика полиморфизма генов тромбофилии:
- С677Г - гетерозиготная форма (метилентетрагидрофолатредуктаза)
- Полиморфизм генов F5 и F2 (кодирующих V и II факторы) - отсутствует
- Выявлен полиморфизм гена PAI-1 - генотип 4G/4G (гомозиготная форма).
В сроке 7 недель беременности отмечала сукровичные выделения из половых путей. По данным УЗИ - хорион кольцевидный, толщиной 5 мм, определяются 2 ретрохориальные отслойки размерами 2,4×1,1×2,6 см и 2,7×1,1×2,4 см. Гемостазиограмма - гиперкоагуляция. К терапии добавлен транексам 1 табл. × 3 р.
В сроке 9 недель - сукровичные выделения прекратились. По данным УЗИ - хорион по передней стенке, толщиной 9 мм, ретрохориальная отслойка в стадии организации, размерами 3,3×1,6×0,7 см. Гемостазиограмма - нарастание гиперкоагуляции, повышение функции тромбоцитов. Дополнительно назначен курантил по 1 т (25 мг) × 3 р.
В сроке 13 недель - выделения светлые. По данным УЗИ - плацента по передней стенке, толщиной 12 мм, определяется организовавшаяся ретроамниотическая отслойка размерами 2,2×0,6×2,1 см.
Гемостазиограмма - признаки хронической формы синдрома ДВС. Транексам и курантил отменены, назначен фрагмин по 2500 ЕДх1р п/к - сроком на 3 недели.
При сроке беременности - 20 недель - хирургическая коррекция истмико-цервикальной недостаточности, дальнейшее течение беременности без осложнений.
Родоразрешена в 39 недель путем операции кесарева сечения. Ребенок женского пола массой 3152, ростом 50 см, оценка по шкале Апгар 8/9 баллов. Течение послеродового и раннего неонатального периодов без особенностей.
В заключение следует отметить, что предложенный нами метод позволяет с довольно высокой точностью прогнозировать вероятность отслойки хориона и плаценты на ранних сроках, что способствует более рациональному ведению беременности и улучшению ее исходов.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОТСЛОЙКИ ХОРИОНА В ПЕРВОМ ТРИМЕСТРЕ БЕРЕМЕННОСТИ | 2014 |
|
RU2566729C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА НЕВЫНАШИВАНИЯ БЕРЕМЕННОСТИ | 2014 |
|
RU2552302C1 |
| Способ прогнозирования высокого риска репродуктивных потерь в первом триместре беременности | 2016 |
|
RU2611358C1 |
| Способ прегестационного прогнозирования рецидива ранних репродуктивных потерь и первичной плацентарной недостаточности | 2019 |
|
RU2709246C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРЕЖДЕВРЕМЕННОЙ ОТСЛОЙКИ НОРМАЛЬНО РАСПОЛОЖЕННОЙ ПЛАЦЕНТЫ | 2024 |
|
RU2825067C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ФЛОТАЦИИ ТРОМБА В СИСТЕМЕ НИЖНЕЙ ПОЛОЙ ВЕНЫ С ДОПОЛНИТЕЛЬНЫМ ИСПОЛЬЗОВАНИЕМ МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКОГО МОНИТОРИНГА | 2012 |
|
RU2517215C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ | 2017 |
|
RU2703463C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ СУБ- И ДЕКОМПЕНСИРОВАННОЙ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ В СЕМЬЯХ С ТРОМБОФИЛИЕЙ ОБОИХ РОДИТЕЛЕЙ | 2017 |
|
RU2637873C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ КРИОГЛОБУЛИНЕМИЧЕСКОГО ВАСКУЛИТА У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2016 |
|
RU2642626C1 |
| Способ прогнозирования неразвивающейся беременности при нормальном кариотипе эмбриона | 2021 |
|
RU2766750C1 |
Изобретение относится к области медицины. Предложен способ прогнозирования отслойки хориона и плаценты на ранних сроках беременности. Осуществляют выделение ДНК с последующей амплификацией полиморфизма -675 5G>4G гена ингибитора активатора плазминогена I типа (PAI-1) при помощи метода ПЦР. Вероятность развития отслойки хориона и плаценты у женщин с высоким риском самопроизвольных репродуктивных потерь при генотипе 4G/4G прогнозируют как 50,0%, при генотипе 4G/5G - как 35,3%. Изобретение позволяет с довольно высокой точностью прогнозировать вероятность отслойки хориона и плаценты на ранних сроках, что способствует более рациональному ведению беременности и улучшению ее исходов. 3 табл., 1 пр.
Способ прогнозирования отслойки хориона и плаценты на ранних сроках беременности, включающий выделение ДНК с последующей амплификацией полиморфизма -675 5G>4G гена ингибитора активатора плазминогена I типа при помощи метода ПЦР, при этом вероятность развития отслойки хориона и плаценты у женщин с высоким риском самопроизвольных репродуктивных потерь при генотипе 4G/4G прогнозируют как 50,0%, при генотипе 4G/5G - как 35,3%.
| НОВИКОВА В.А | |||
| и др | |||
| Влияние нарушений в системе гемостаза на особенности течения беременности в различные ее триместры // Материалы V Регионального научного форума «Мать и дитя» | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| КОАГУЛОГРАММА, ГЕМОСТАЗИОГРАММА | |||
| Стиральная машина для войлоков | 1922 |
|
SU210A1 |
Авторы
Даты
2013-09-27—Публикация
2012-01-16—Подача