Изобретение относится к области медицины, в частности к терапии и пульмонологии, и касается лечения фиброза легких.
Идиопатический фиброз легких, достаточно распространенное тяжелое интерстициальное легочное заболевание, являющееся серьезной проблемой для клиницистов, так как обладает неблагоприятным прогнозом [1]. До настоящего времени не ясны механизмы возникновения заболевания, и как следствие этого нет лекарственных препаратов, препятствующих развитию фиброза легких. Терапия фиброза легких направлена главным образом на профилактику быстрого прогрессирования заболевания, а не на его предупреждение. Для этого в настоящее время используют глюкокортикостероиды, часто в комбинации с цитостатическими агентами, антиоксиданты (N-ацетилцистеин), антифиброзные средства (D-пеницилламин, колхицин) [2]. Как правило, изучение патогенеза фиброгенных изменений в легких и выявление средств, препятствующих интерстициальному отложению коллагена, проводят на блеомициновой модели пневофиброза [3, 4].
Известен способ коррекции блеомицин-индуцированного фиброза легких под влиянием единичной интраназальной инокуляции препарата гиалуронидазы [5].
Данный способ является близким к заявляемому по технической сущности и достигаемому результату и выбран в качестве прототипа.
Недостатками способа являются кратковременность действия фермента, высокая вероятность аллергических реакций, которые в сочетании с плохим периодом полувыведения препарата могут ограничивать клиническую эффективность гиалуронидазы [3, 6].
Задачей, решаемой данным изобретением, является повышение эффективности способа лечения фиброза легких и уменьшение побочного действия препарата гиалуронидазы.
Поставленная задача достигается техническим решением, представляющим собой способ лечения фиброза легких, заключающийся в интраназальном введении лабораторным животным иммобилизированной на полиэтиленгликоле гиалуронидазы в дозе 16 ЕД 1 раз в сут на 1, 3, 7, 10-е сут после введения блеомицина.
Новым в предлагаемом изобретении является использование препарата иммобилизированной на полиэтиленгликоле гиалуронидазы 1 раз в сут на 1, 3, 7, 10-е сут после введения блеомицина.
Регулирование восстановления тканей при их повреждении - это тщательно скоординированный ответ организма, направленный на ликвидацию повреждения и восстановление целостности тканей [7]. Механизмы, которые участвуют в регуляции ответа организма на повреждение ткани, не полностью понятны. Известно, что различные легочные заболевания характеризуются избыточным отложением отдельных компонентов экстрацеллюлярного матрикса, в результате чего может развиться органный фиброз. При бронхиальной астме, эмфиземе легких, легочном фиброзе и других хронических заболеваниях легких обнаруживается дисбаланс между синтезом и деградацией гиалуроновой кислоты [7, 8].
Гиалуроновая кислота основной компонент экстрацеллюлярного матрикса, который динамически изменяется во время повреждения тканей и воспалений. Взаимодействуя с протеогликанами (аггрекан, версикан) гиалуроновая кислота участвует в организации фибрина, фибронектина и коллагена [8]. В эксперименте показано, что продукция гиалуроновой кислоты возрастает в несколько раз после интратрахеальной инсталляции блеомицина, что связывают с повреждением паренхемы легких и воспалением [7].
Основным ферментом, регулирующим метаболизм гиалуроновой кислоты, является гиалуронидаза. Расщепляя гиалуроновую кислоту на фрагменты (глюкозамины и глюкуроновая кислота), фермент тем самым ремодулирует экстрацеллюлярный матрикс [3, 7, 8, 9]. Основным показанием для применения гиалуронидазы являются контрактуры суставов, рубцы после ожогов и операций, анкилозирующий спондилоартрит, склеродермия, травматические поражения сплетений и периферических нервов (плексит, неврит), гематомы, тяжелые заболевания поясничных дисков и другие [3]. В эксперименте показано, что на фоне введения блеомицина в легких гиалуронидаза препятствует развитию фиброза. Это связывают со снижением концентрации глюкуроновой кислоты в паренхиме [5]. Однако, несмотря на выявленную эффективность действия препарата, использование нативной гиалуронидазы во многом ограничено, благодаря высокой способности фермента вызывать аллергические реакции и короткому периоду полувыведения из плазмы при системном введении [3, 6].
На сегодняшний день модификация пептидных препаратов пегилированием активно развивающееся направление фармакологии. Пегилированные лекарственные препараты пептидной структуры имеют ряд весомых и несомненных преимуществ, которые ранее были просто невозможны при использовании нативных аналогов: усиление биологической активности, удлинение периода полураспада, замедление выведения, отсутствие пиков плазменной/тканевой концентрации, понижение токсичности и иммуногенности [10]. Результаты экспериментальных исследований последних лет дают основание говорить о перспективах лечения пегилированной гиалуронидазой миелосупрессии, вызванной цитостатиком [11].
Отличительные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и неочевидные для специалиста. Идентичной совокупности признаков не обнаружено в проанализированной патентной и научно-медицинской литературе.
Изобретение может быть использовано для повышения устойчивости легочной ткани к отложению фибротических масс при фибротических заболеваниях в легких.
Исходя из вышеизложенного, заявляемое изобретение соответствует критериям патентоспособности изобретения «Новизна», «Изобретательский уровень» и «Промышленная применимость».
Предлагаемый способ был изучен в экспериментах на 7-8 недельных мышах линии C57BL/6J в количестве 100 штук. Животные первой категории, инбредные мыши, получены из питомника отдела экспериментального биомедицинского моделирования ФГБУ «НИИ фармакологии» СО РАМН (сертификат имеется). Использование животных в экспериментах обосновано и согласовано с Комиссией по контролю за содержанием и использованием лабораторных животных ФГБУ «НИИ фармакологии» СО РАМН.
Способ будет понятен из следующего описания и приложенного к нему рисунка 1.
На рис.1 изображено легкое мыши, при окрашивании ткани легкого гематоксилином и эозином: а - интактной, б - получавшей блеомицин, в - получавшей нативную гиалуронидазу на фоне моделирования фиброза; г - получавшей иммобилизированную гиалуронидазу на фоне моделирования фиброза; легкое мыши, при окрашивании ткани легкого по Ван-Гизону на соединительную ткань: д - интактной; е - получавшей блеомицин; ж - получавшей нативную гиалуронидазу на фоне моделирования фиброза; з - получавшей иммобилизированную гиалуронидазу на фоне моделирования фиброза.
Способ осуществляют следующим образом:
Фиброз легкого моделировали однократным интратрахеальным введением 80 мкг блеомицина («Блеомицетин», ОАО «Лэнсфарм», Россия) в 30 мкл физиологического раствора. Контрольным животным в аналогичных условиях вводили эквивалентный объем физиологического раствора (контроль). Блеомицин относится к группе противоопухолевых антибиотиков. Его механизм действия до конца не выяснен, хотя известно, что он способен подавлять синтез нуклеиновых кислот (преимущественно ДНК) и белка. Препарат активен в отношении клеток, находящихся как в митотическом цикле, так и вне его, но проявляет большую активность в фазе G2. Основное токсическое действие цитостатик оказывает на легкие: вызывает пневмонию, фибротические изменения в паренхиме легких [3].
Иммобилизированную гиалуронидазу (ООО «Scientific Future Management», г.Новосибирск), модифицированную активированным полиэтиленоксидом молекулярной массой 1500 Да с помощью электроннолучевого синтеза вводили интраназально в дозе 16 ЕД/18 мкл/20 г на 1, 3, 7, 10-е сутки после интратрахеального введения блеомицина.
Нативную гиалуронидазу (ООО «Scientific Future Management», г.Новосибирск) вводили интраназально в дозе 16 ЕД/18 мкл/20 г на 1, 3, 7, 10-е сутки после интратрахеального введения блеомицина.
Заявляемая доза и режим введения нативной и иммобилизированной гиалуронидазы подобраны опытным путем и являются оптимальными для получения заявленного технического результата. Повышение дозы и кратности введения отменяют получение заявленного технического результата. Снижение дозы и/или однократное введение препарата значительно снижают эффективность способа.
В качестве фона использовали интактных животных (интактный контроль).
На 3, 7, 14 и 21-е сутки после введения блеомицина проводили эвтаназию мышей передозировкой CO2 и изучали морфологическую картину легких. Для гистологического исследования из средней части правого легкого по стандартной методике готовили парафиновые блоки. С каждого блока получали срезы, которые окрашивали гематоксилином и эозином для изучения содержания лимфоцитов, макрофагов, нейтрофилов и плазматических клеток и по Ван-Гизону на соединительную ткань [12].
Математическую обработку результатов производили с применением стандартных методов вариационной статистики. Достоверность различий оценивали с использованием параметрического t критерия Стьюдента или непараметрического U критерия Манна-Уитни.
Пример.
При интратрахеальном введении блеомицина в легких мышей отмечаются изменения, характерные для токсического фиброзирующего альвеолита. В ранние сроки после инсталляции блеомицина (3 сут) наблюдается выраженная сосудистая реакция, характеризующаяся венозным полнокровием в стенках альвеол и отеком эпителия межальвеолярных перегородок (рисунок). Вокруг крупных сосудов и перибронхиально обнаруживаются воспалительные инфильтраты, содержащие лимфоциты, гистиоциты, альвеолярные макрофаги, нейтрофильные и эозинофильные лейкоциты (рис.1). На 7 сут происходит усиление гиперемии и отечных явлений, в просветах альвеол появляются спущенные альвеоциты. Одновременно увеличивается интенсивность интерстициального воспаления, отмечается утолщение стенок альвеол за счет инфильтрации их воспалительными клетками. 14 сут опыта характеризуются значительным усилением процессов воспаления и отека по сравнению с 7 сут опыта. В альвеолах появляется серозно-фибринозный экссудат, повышается количество слущенных альвеоцитов и клеток инфильтрата. При изучении лейкоцитарной формулы выявляется, что число нейтрофильных лейкоцитов превышает количество макрофагов и лимфоцитов. У корня легкого встречаются участки, где легочный рисунок отсутствует за счет массивной воспалительной инфильтрации. В этот период наблюдения в патологический процесс вовлекаются бронхиолы с образованием мелких кист и разрушением структуры альвеол, что является начальным этапом формирования так называемого «сотового легкого». На 21 сут воспалительный процесс в легких достигает максимальной выраженности. С помощью гистохимической окраски выявляется повышение интенсивности отложения коллагеновых волокон в легочной ткани фиброзных животных на протяжении всего периода наблюдения. На ранних сроках эксперимента отмечается преимущественно перибронхиальный и околососудистый фиброз (7 сут), который в дальнейшем распространяется на альвеолярные перегородки и превращается в интерстициальный (14 сут) (рис.1, табл.1). На 21-е сут опыта наблюдается картина обширного распространенного пневмофиброза.
Нативная гиалуронидаза и иммобилизированная гиалуронидаза замедляют прогрессирование фиброза в блеомициновых легких на протяжении всего периода наблюдения (табл.1). Пегилированная форма гиалуронидазы более эффективно замедляет отложение фиброзных масс в легких мышей, по сравнению с животными, получавшими нативную гиалуронидазу на 7, 14-е сут опыта (рис.1).
У животных, леченных нативной гиалуронидазой или иммобилизированной гиалуронидазой, имеет место диффузная инфильтрация воспалительными клетками, в отличие от мышей, получавших только блеомицин, у которых инфильтрат локализуется преимущественно у корня легкого (рис.1). При изучении лейкоцитарной формулы у мышей, получавших препараты гиалуронидазы, отмечается незначительное увеличение количества альвеолярных макрофагов и снижение количества нейтрофилов в инфильтрате по сравнению с группой блеомицинового контроля.
Таким образом, интраназальное введение иммобилизированной гиалуронидазы препятствует отложению фибротических масс в паренхиме легких у мышей в условиях интратрахеального введения блеомицина, при этом антифибротический эффект пегилированного фермента более выражен, чем у нативной гиалуронидазы.
Предлагаемый способ позволяет рассматривать иммобилизированную гиалуронидазу в качестве средства антифиброзной терапии легких.
Литература
1. Илькович М.М., Новикова Л.Н., Сперанская А.А. Идиопатический фиброзирующий альвеолит // Участковый терапевт - 2009. - №6. - С.1-3.
2. Андреева И.И. Фиброзирующие альвеолиты. В кн.: Саперов В.Н., Андреева И.И., Мусалимова Г.Г. (ред.) Практическая пульмонология. Чебоксары: Изд-во Чуваш, гос. ун-та; 2007. С.511-514.
3. Машковский М.Д. Лекарственные средства. Пособие для врачей. - 15-е изд., перераб., испр. и доп. - М.: «Новая волна», Издатель Умеренков, 2008. - С.660-661, 1003-1004.
4. Moeller A., Ask K., Warburton D. et al. The bleomycin animal model: a useful tool to investigate treatment options for idiopathic pulmonary fibrosis? // Int. J. Biochem. Cell Biol. - 2008. - Vol.40, №3. - P.362-382.
5. Bitencourt C.S., Pereira P.А.Т., Ramos S.G. et al. Hyaluronidase recruits mesenchymal-like cells to the lung and ameliorates fibrosis // Fibrogenesis & Tissue Repair. - 2011. - Vol.4, №3. - P.1-14.
6. Thompson С.В., Shepard M.H., O'Connor P.M., et al. Enzymatic Depletion of Tumor Hyaluronan Induces Antitumor Responses in Preclinical Animal Models // Mol Cancer Ther. - 2010. - Vol.9. - P.3052-3064.
7. Noble P.W., Jiang D. Matrix Regulation of Lung Injury, Inflammation, and Repair. The Role of Innate Immunity // Proc Am Thorac Soc. - 2006. - Vol.3. - P.401-404.
8. Delpech В., Girard N., Bertrand P. et al. Hyaluronan: fundamental principles and applications in cancer // J. Intern. Med. - 1997. - №242. - P.41-48.
9. Kemparaju K., Girish K.S. Snake venom hyaluronidase: a therapeutic target // Cell Biochem. Funct. - 2006. - Vol.24. - P.7-12.
10. Piedmonte D.M., Treuheit M.J. Formulation of Neulasta (pegfilgrastim) // Advanced Drug Delivery Reviews. - 2008. - Vol.60. - P.50-58.
11. Дыгай A.M., Скурихин Е.Г., Першина О.В. и др. Гемопоэзстимулирующая активность препаратов иммобилизированных олигонуклеотидов и гиалуронидазы в условиях цитостатической миелосупрессии // Бюл. эксперим. биол. и медицины. - 2010. - Т.150, №11. - С.545-549.
12. Меркулов Г.А. Курс патогистологической техники. - СПб: Медицина, 1969. - С.14, 36-38, 58, 98-100, 163, 170.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ТЕРАПИИ НАРУШЕНИЙ В ЛЕГОЧНОЙ ТКАНИ ПРИ ЦИТОСТАТИЧЕСКИХ ВОЗДЕЙСТВИЯХ | 2012 |
|
RU2497523C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПНЕВМОФИБРОЗА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2646810C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РЕГЕНЕРАТИВНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2480236C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНТИФИБРОТИЧЕСКИМ ДЕЙСТВИЕМ В ЛЕГОЧНОЙ ТКАНИ ПРИ ЦИТОСТАТИЧЕСКОМ ВОЗДЕЙСТВИИ | 2012 |
|
RU2479312C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНТИФИБРОТИЧЕСКИМ ДЕЙСТВИЕМ В ЛЕГОЧНОЙ ТКАНИ ПРИ ЦИТОСТАТИЧЕСКОМ ВОЗДЕЙСТВИИ | 2013 |
|
RU2530651C1 |
| СРЕДСТВО, ПРЕПЯТСТВУЮЩЕЕ РАЗВИТИЮ НАРУШЕНИЙ В ЛЕГОЧНОЙ ТКАНИ И СИСТЕМЕ КРОВИ ПРИ ЦИТОСТАТИЧЕСКОМ ВОЗДЕЙСТВИИ | 2011 |
|
RU2464983C1 |
| СРЕДСТВО, ПРЕПЯТСТВУЮЩЕЕ РАЗВИТИЮ НАРУШЕНИЙ В ЛЕГОЧНОЙ ТКАНИ ПРИ ЦИТОСТАТИЧЕСКОМ ВОЗДЕЙСТВИИ | 2011 |
|
RU2455991C1 |
| СРЕДСТВО, УСИЛИВАЮЩЕЕ МОБИЛИЗАЦИЮ СТВОЛОВЫХ КЛЕТОК | 2009 |
|
RU2442601C2 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2010 |
|
RU2444569C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО И СПОСОБ СТИМУЛЯЦИИ ГЕМОПОЭЗА | 2009 |
|
RU2414926C1 |
Изобретение относится к области экспериментальной медицины, а именно к разработкам способа лечения фиброза легких. Для этого лабораторным животным интраназальным путем вводят иммобилизированную на полиэтиленгликоле гиалуронидазу в дозе 16 ЕД. Введение осуществляют 1 раз в сутки на 1, 3, 7, 10-е сутки после введения блеомицина - фактора моделирования фиброза легких. Способ обеспечивает повышение устойчивости легочной ткани к отложению фибротических масс, в том числе предупреждает обратный процесс формирования фиброза, за счет свойств пегилированной гиалуронидазы и разработанного режима ее введения, что приводит к длительному антифибротическому эффекту при низкой токсичности и иммуногенности воздействия на организм. 1 пр., 1 табл., 1 ил.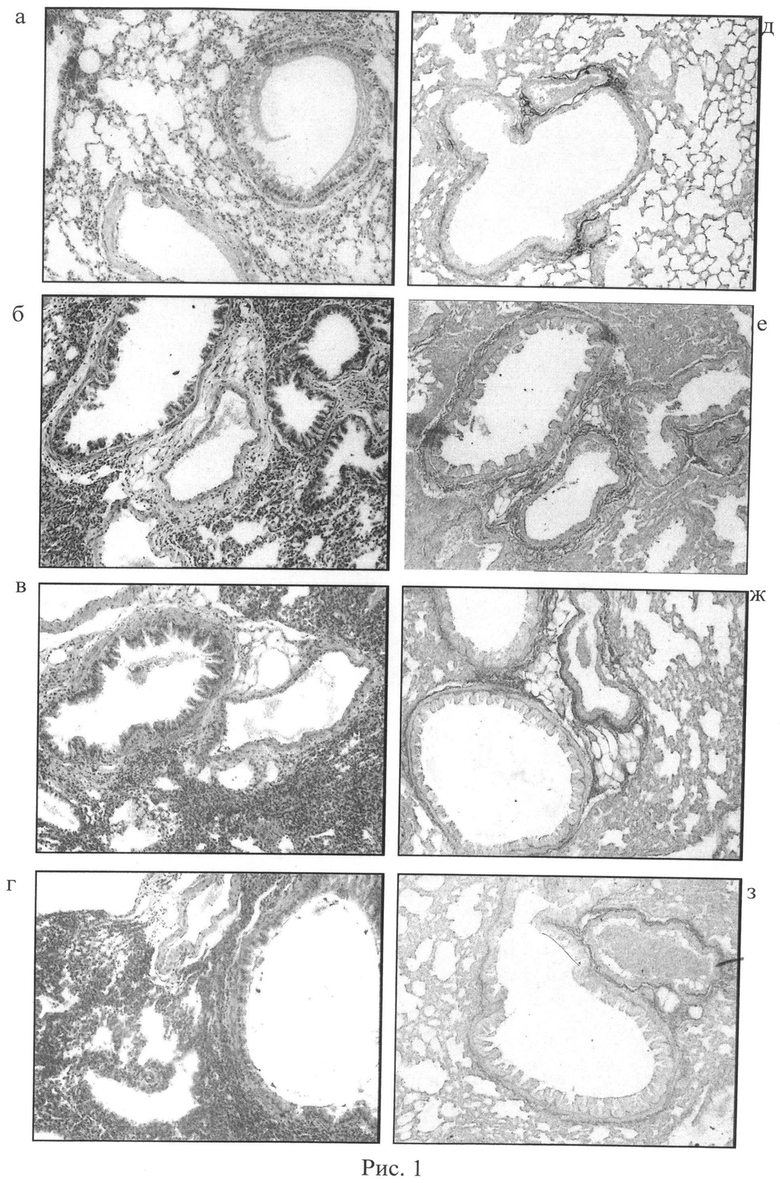
Способ лечения фиброза легких, заключающийся в интраназальном введении лабораторным животным (мыши) препарата гиалуронидазы в дозе 16 ЕД, отличающийся тем, что вводят иммобилизированную на полиэтиленгликоле гиалуронидазу 1 раз в сутки на 1, 3, 7, 10-е сутки после введения блеомицина.
| BITENCOURT C.S | |||
| et | |||
| al | |||
| Hyaluronidase recruits mesenchymal-like cells to the lung and ameliorates fibrosis, Bitencourt | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| RU 2004115390 A, 20.04.2005 | |||
| WO | |||
Авторы
Даты
2013-09-27—Публикация
2012-04-04—Подача