Изобретение относится к области медицины, в частности к радиационной биологии, и может быть использовано для ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения за счет введения интегрального показателя - величины относительного сдвига среднего радиуса эритроцитов периферической крови.
На данный момент весьма актуальной проблемой практической медицины является создание экспресс-метода ранней диагностики тяжести радиационного поражения, который наряду с прогнозированием исхода острого лучевого поражения способствовал бы также экстренному проведению лечебно-профилактических противорадиационных мероприятий после массовых поражений.
Известен способ диагностики радиационных поражений людей путем выявления аутоантител в сыворотке крови методом непрямой иммунофлуоресценции (НРИФ) на криостатных средах тимуса и 14-дневной культуре эпителиальных клеток тимуса новорожденных мышей (Сборник тезисов "Иммунный статус человека и радиация". - М., 1991, - c.31).
Однако криоконсервирование клеток и тканей, использование лабораторных животных, иммунофлуоресцентной и иммуногистохимической техники, являются очень дорогостоящими, сложными и длительными методами, оценка результатов которых к тому же субъективна.
Сравнительно близким по поставленной цели является способ диагностики тяжести острого лучевого поражения (патент RU №2099709, G01N 33/483, опубл. 20.12.1997 г.) путем исследования периферической крови, заключающийся в одномоментном определении прочности эритроцитарных агрегатов, содержания лейкоцитов и полупериода агрегации эритроцитов с последующим установлением корреляции между тяжестью острого лучевого поражения и максимальным отклонением величины индекса тяжести лучевого поражения, который рассчитывают по формуле J=Ud/τ(L+n), где J - индекс тяжести лучевого поражения, (отн.ед); Ud - максимальная прочность агрегатов эритроцитов (B); τ - полупериод агрегации эритроцитов (с); L - содержание лейкоцитов (тыс/мкл); n - поправочный коэффициент, n равен 0 при L, не равном нулю, n равен 0,1 при L, равном нулю, и при максимальном отклонении J, зарегистрированном в диапазоне от 0,31 до 3,0, диагностируют легкое лучевое поражение, от 3,1 до 9,0 - среднее, от 9,1 и выше - тяжелое лучевое поражение, а в диапазоне величин J от 0,05 до 0,30 диагностируют норму.
Основными недостатками данного способа являются, во-первых, трудоемкость и дороговизна метода; во-вторых, ограниченность применения метода из-за резкого снижения уровня лейкоцитов и лимфоцитов (вплоть до полного отсутствия) при высоких и даже средних дозах облучения, что не позволяет дифференцировать тяжесть острого лучевого поражения и прогнозировать его исход, а также обуславливает низкую чувствительность этих способов.
Наиболее близким техническим решением, взятым в качестве прототипа, является способ диагностики тяжести острого лучевого поражения [Мкоян Ф.А. Дифрактометрический анализ популяции эритроцитов белых крыс при лучевом поражении / Ф.А. Микоян. - Ереван, 1994. - 125 с.] на основе исследования характерных изменений размерного состава эритроцитов периферической крови в РПП по оценке модального размера эритроцитов периферической крови (МРЭПК) методом лазерного дифрактометрирования сухого мазка крови. О тяжести острого лучевого поражения судят по величине относительного сдвига МРЭПК по сравнению с нормой, которую получают с помощью дифрактометрической оценки этого параметра в первые часы-сутки РПП. Прогнозирование исхода острого лучевого поражения делают на основе сопоставления величин относительных сдвигов МРЭПК по сравнению с нормой для разных стадий РПП с последующим нахождением соответствующей точки на кривой доза - эффект через трое суток после лучевого поражения.
Предложенный дифрактометрический способ оценки МРЭПК имеет ряд существенных недостатков: во-первых, результаты анализа существенно зависят от выбора участка на сухом мазке крови (субъективные факторы); во-вторых, процесс сушки мазка приводит к изменению размеров эритроцитов, в-третьих, полуавтоматизированный вариант технической реализации способа создает дополнительные трудности, что приводит к потере точности на 1-2%.
Техническим результатом изобретения является повышение точности ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения в раннем пострадиационном периоде (РПП).
Технический результат достигается тем, что в способе ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения путем исследования эритроцитов периферической крови новым является то, что для оценки вводят интегральный показатель - величину относительного сдвига среднего радиуса эритроцитов периферической крови (ВОС СРЭПК) по сравнению с нормой и осуществляют автоматизированную оценку данного показателя путем компьютерной обработки цифровой информации микроизображения эритроцитов в тонком слое периферической крови с помощью оптического микроскопа и ПЗС-камеры на разных стадиях раннего пострадиационного периода, и если через 72 часа после тотального облучения ВОС СРЭПК увеличивается по сравнению с нормой более 10%, то диагностируют острое лучевое поражение средней тяжести и прогнозируют, что животное выживет, если через 72 часа после тотального облучения ВОС СРЭПК уменьшается по сравнению с нормой на 10% и более, то диагностируют смертельную дозу и прогнозируют, что в течение 30 суток животное погибнет.
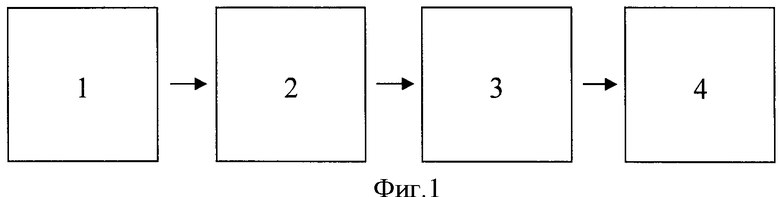
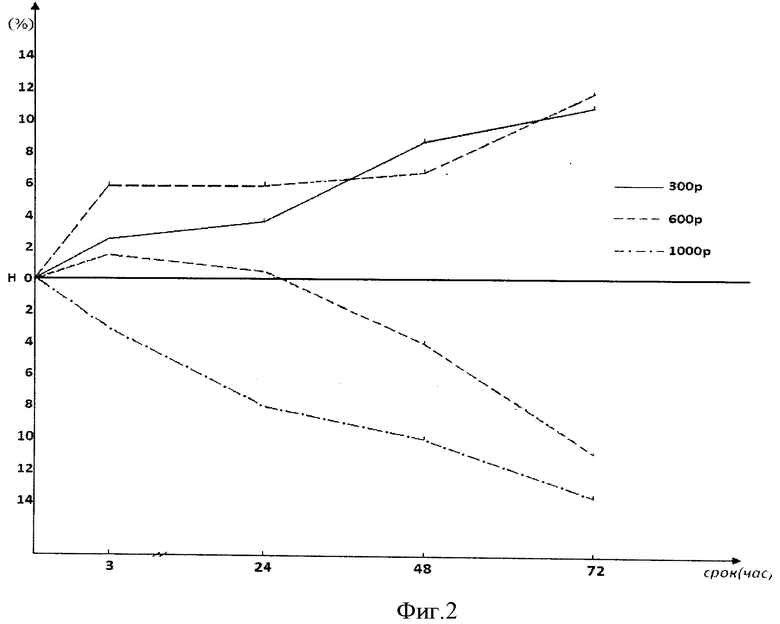
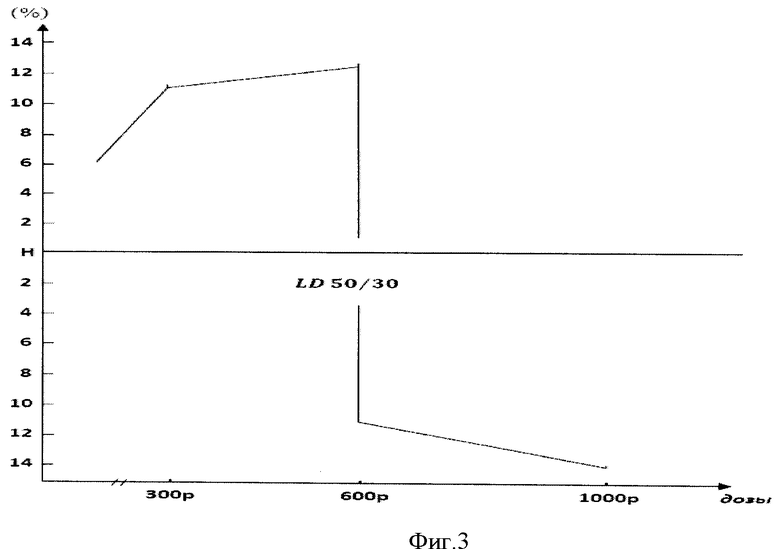
Изобретение поясняется чертежами. На фиг.1 представлена блок-схема устройства для цифровой обработки микроизображений, с помощью которого осуществляется оценка среднего радиуса совокупности эритроцитов некоторого участка тонкого слоя периферической крови. На фиг.2 представлен график временной зависимости относительных сдвигов (в процентах по сравнению с нормой; норма (Н)-0%) средних радиусов эритроцитов крыс, подвергнутых тотальному однократному облучению (приведены данные в норме и через 24; 48 и 72 часа после облучения дозами 300 Р, 600 Р и 1000 Р). На фиг.3 представлен график дозовой зависимости относительных сдвигов (в процентах по сравнению с нормой; норма (Н)-0%) средних радиусов эритроцитов крыс через трое суток после тотального однократного облучения (дозы 300Р, 600Р и 1000 Р).
Сущность способа заключается в том, что осуществляют оценку среднего радиуса эритроцитов периферической крови (СРЭПК) для достаточно большой выборки по методике оценки среднего радиуса совокупности объектов, близких по форме к кругу, путем компьютерной обработки цифровых данных микроизображения тонкого слоя исследуемого препарата. О тяжести острого лучевого поражения судят по величине относительного сдвига СРЭПК по сравнению с нормой - после первых, вторых и третьих суток раннего пострадиационного периода (РПП), на основании результатов оценки этого параметра. Прогнозирование исхода острого лучевого поражения делается на основе сопоставления величины относительного сдвига (ВОС) СРЭПК по сравнению с нормой для разных стадий РПП, с последующим нахождением точки на корреляционной кривой доза - эффект через трое суток после лучевого поражения.
Общепринята точка зрения, что в процессе лучевой болезни, вызванной различными дозами облучения, динамика сдвига исследуемого параметра отражает изменение тяжести лучевого поражения организма. Степень тяжести лучевого поражения организма зависит от двух основных факторов: величины дозы облучения и исходного функционального состояния организма. Следовательно, очевидна необходимость разработки нового способа ранней диагностики тяжести острого лучевого поражения, который позволит без больших затрат времени и средств обеспечить индивидуальный подход в достижении поставленной цели. Также очевидна необходимость выбора такого параметра исследования, который поддается измерению на протяжении всего РПП. Это особенно важно при чрезвычайных ситуациях, когда возникает необходимость обследования пострадавших в результате массового поражения.
Реализация способа ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения станет возможна при использовании известной методики оценки среднего радиуса совокупности объектов путем выполнения двумерного преобразования Фурье от изображения объектов и нахождения двумерной периодограммы этого изображения [Квеглис Л.И. Диссипативные структуры в тонких нанокристаллических пленках / Л.И. Квеглис, В.Б. Кашкин. - Красноярск: Сибирский федеральный университет, 2011, - с.88-101].
Эти отличия позволяют сделать вывод о соответствии заявляемого технического решения критерию «новизна». Признаки, отличающие заявляемое устройство от прототипа, не выявлены в других технических решениях при изучении данной и смежных областей техники и, следовательно, обеспечивают заявляемому решению соответствие критерию «изобретательный уровень».
Оценка среднего радиуса совокупности эритроцитов некоторого участка тонкого слоя периферической крови осуществляется с помощью устройства, блок-схема которого представлена на фиг.1. Устройство состоит из оптического микроскопа 1, специального держателя 2 образца крови, прибора с зарядовой связью (ПЗС-камера) 3 для цифровой регистрации микроизображения исследуемого участка тонкого слоя крови и ЭВМ 4 для обработки цифровой информации.
Тонкий слой периферической крови готовят по следующей схеме: производят забор крови у исследуемого объекта и разбавляют ее 0,8% раствором хлорида натрия в 200 раз. Затем смачивают предметное стекло дистиллированной водой и с помощью микропипетки 1 мкл разбавленной крови наносят на предметное стекло, ожидают 20 секунд и закрывают слой покровным стеклом. После этого сразу с помощью оптического микроскопа и ПЗС-камеры проводят цифровую регистрацию микроизображения совокупности микрообъектов-эритроцитов.
В результате такой последовательности цифровой регистрации и анализа соответствующего участка тонкого слоя периферической крови оказывается возможным преодоление ряда недостатков прототипа. Во-первых, путем унификации методики подготовки тонкого слоя крови и выбора фиксированного участка для цифровой регистрации микроизображения эритроцитов сводится к минимуму зависимость полученных данных от характеристик отдельного мазка (существенно уменьшается роль субъективных факторов). Во-вторых, цифровая регистрация участка несушенного тонкого слоя исключает влияние процесса сушки на полученные данные. В-третьих, точность метода существенно повышена за счет полной автоматизации обработки данных.
Заявляемый способ реализуется следующим образом. Для каждого организма, подвергнутого однократному тотальному облучению определенной дозой, готовят тонкий слой периферической крови в норме (за сутки до облучения) и на разных стадиях РПП - через 24; 48 и 72 часа после облучения, после чего крепят образец крови в специальном держателе 2 и вслед за этим с помощью оптического микроскопа 1 и ПЗС-камеры 3 выполняют цифровую регистрацию микроизображения исследуемого участка тонкого слоя крови. Вся получаемая информация передается на ЭВМ 4 для цифровой обработки. Всю дальнейшую работу ведут с цифровым банком данных микроизображений исследуемого участка тонкого слоя крови.
Такая технология приводит к значительному упрощению реализации способа, повышению экспрессности, производительности труда, достоверности результатов анализа, а также его унификации и расширению области применения.
Пример 1. Крыса, вес 195 г, самец. Доза тотального облучения 300 Р (сублетальная доза для этого вида животного, когда в течение первых 30 суток РПП смертельный исход не обнаруживается). По описанной схеме для данного животного готовят 4 образца - норма; 24 часа; 48 часов и 72 часа и осуществляют оценку среднего радиуса эритроцитов периферической крови (фиг.2). Из рисунка видно (непрерывная линия), что уже на вторые сутки РПП исследуемый параметр - ВОС СРЭПК увеличивается на 6% и через трое суток превосходит 10%. В литературе эту дозу называют дозой средней тяжести. По аналогии с этим можно утверждать, что при регистрации увеличения ВОС СРЭПК по сравнению с нормой более 10% имеет место острое лучевое поражение средней тяжести, и делать прогноз, что животное выживет.
Пример 2. Крыса, вес 215 г, самец. Доза тотального облучения 1000 Р (абсолютно смертельная доза для этого вида животного, когда в течение первых 7 суток РПП обнаруживается 100% смертельный исход). По описанной схеме для данного животного готовят 4 образца - норма; 24 часа; 48 часов и 72 часа и осуществляют оценку среднего радиуса эритроцитов периферической крови (фиг.2). Из рисунка видно (пунктирная линия с точками), что уже через 24 часа после облучения исследуемый параметр уменьшается на 7%, а через 72 часа это уменьшение достигает 14%. Таким образом, если ВОС СРЭПК через 72 часа становится меньше, по сравнению с нормой, на 14% и больше, тогда по тяжести это соответствует абсолютно смертельной дозе и можно прогнозировать, что в течение 7 суток животное погибнет.
Пример 3. Крыса, вес 205 г, самец. Доза тотального облучения 600 Р (полусмертельная доза для этого вида животного - LD50/30, когда в течение первых 30 суток РПП одна половина этих животных погибает, а вторая половина выживает). По описанной схеме для данного животного готовят 4 образца - норма; 24 часа; 48 часов и 72 часа и осуществляют оценку среднего радиуса эритроцитов периферической крови (фиг.2). Исследование показало, что для дозы 600Р имеет место достоверное качественное и количественное различие в значениях ВОС СРЭПК между погибающими и выживающими подгруппами (две пунктирные линии с противоположной динамикой поведения на фиг.2). У выживающей подгруппы имеет место рост ВОС СРЭПК в течение всего РПП и через 24 часа значение больше 7%. Через 48 часов больше 8%, а в течение третьих суток достигает 12%. Для погибающей подгруппы отмечено достоверное уменьшение ВОС СРЭПК спустя 72 часа после лучевого поражения, более 10% по сравнению с нормой. Важно заметить, что при дозе облучения 600Р характер поведения ВОС СРЭПК в РПП проявляет специфичные для сублетальной (300 Р) и абсолютно смертельной (1000 Р) доз динамику изменения.
Таким образом можно утверждать, что при дозе облучения LD50/30 погибающие животные ведут себя аналогично абсолютно смертельной дозе, а выживающие аналогично сублетальной дозе облучения (фиг.2). Данный факт достаточно наглядно продемонстрирован на фиг.2 и его можно назвать «эффектом расщепления». На фиг.3 видно, что «эффект расщепления» происходит при облучении дозой в 600 Р. Таким образом, на основании построенного графика (фиг.3) делают прогноз исхода острого лучевого синдрома, как для сублетальных и абсолютно смертельных доз, так и для полусмертельной дозы облучения.
Предлагаемый способ ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения позволяет провести быстрое и достоверное разделение облученных организмов на подгруппы по степени тяжести поражения при одинаковой дозе радиации окружающей среды, особенно при уровне радиации, близкой к полусмертельной дозе облучения для данного вида животного. Также заявляемый способ позволяет повысить точность ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения в раннем пострадиационном периоде, приводит к значительному упрощению реализации способа, повышению экспрессности, производительности труда, достоверности результатов анализа, а также его унификации и расширению области применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ РАДИАЦИОННЫХ ПОРАЖЕНИЙ ОРГАНИЗМА И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1997 |
|
RU2145712C1 |
| ТЕТРАКИС-(L-ГИСТИДИНАТО)-μ-ПЕРОКСИДИКОБАЛЬТА (III) ГЕПТАГИДРАТ, ПРОЯВЛЯЮЩИЙ АНТИАНЕМИЧЕСКУЮ, РАДИОПРОТЕКТОРНУЮ И АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 1999 |
|
RU2151773C1 |
| СПОСОБ ДИАГНОСТИКИ ТЯЖЕСТИ ОСТРОГО ЛУЧЕВОГО ПОРАЖЕНИЯ | 1995 |
|
RU2099709C1 |
| СПОСОБ ДИАГНОСТИКИ ОСТРОЙ ЛУЧЕВОЙ БОЛЕЗНИ | 1986 |
|
SU1519366A1 |
| СПОСОБ ЛАБОРАТОРНО-ГЕМАТОЛОГИЧЕСКОЙ ДИАГНОСТИКИ СТЕПЕНИ ТЯЖЕСТИ ОСТРОЙ ЛУЧЕВОЙ БОЛЕЗНИ НА ЭТАПАХ МЕДИЦИНСКОЙ ЭВАКУАЦИИ | 2007 |
|
RU2356051C1 |
| Способ диагностики радиационных поражений организма и способ получения противолучевого антительного бентонитового препарата для диагностики радиационных поражений организма | 2019 |
|
RU2731521C1 |
| СПОСОБ ДИАГНОСТИКИ ВОЗДЕЙСТВИЯ МАЛЫХ ДОЗ РАДИАЦИИ НА ОРГАНИЗМ ЧЕЛОВЕКА | 1995 |
|
RU2089904C1 |
| Способ моделирования комбинированного радиационно-механического поражения тяжелой степени с лапароскопическим повреждением печени | 2024 |
|
RU2828152C1 |
| Способ моделирования комбинированного радиационно-механического поражения, включающего в качестве нелучевого компонента обширное повреждение мягких тканей конечности, подвергшееся первичной хирургической обработке с установкой аппарата внешней фиксации | 2024 |
|
RU2833131C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТРОЙ ЛУЧЕВОЙ БОЛЕЗНИ В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2551619C1 |
Изобретение относится к области медицины, в частности к радиационной биологии, и может быть использовано для ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения. Способ ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения заключается в том, что исследуют эритроциты периферической крови. Для оценки исследования эритроцитов вводят интегральный показатель - величину относительного сдвига среднего радиуса эритроцитов периферической крови (ВОС СРЭПК) по сравнению с нормой, и если через 72 часа после тотального облучения ВОС СРЭПК увеличивается по сравнению с нормой более 10%, то диагностируют острое лучевое поражение средней тяжести и прогнозируют, что животное выживет, если через 72 часа после тотального облучения ВОС СРЭПК уменьшается по сравнению с нормой на 10% и более, то диагностируют смертельную дозу и прогнозируют, что в течение 30 суток животное погибнет. 3 пр., 3 ил.
Способ ранней диагностики тяжести и прогнозирования исхода острого лучевого поражения путем исследования эритроцитов периферической крови, отличающийся тем, что для оценки вводят интегральный показатель - величину относительного сдвига среднего радиуса эритроцитов периферической крови (ВОС СРЭПК) по сравнению с нормой и осуществляют автоматизированную оценку данного показателя путем компьютерной обработки цифровой информации микроизображения эритроцитов в тонком слое периферической крови с помощью оптического микроскопа и ПЗС-камеры на разных стадиях раннего пострадиационного периода, и если через 72 часа после тотального облучения ВОС СРЭПК увеличивается по сравнению с нормой более 10%, то диагностируют острое лучевое поражение средней тяжести и прогнозируют, что животное выживет, если через 72 часа после тотального облучения ВОС СРЭПК уменьшается по сравнению с нормой на 10% и более, то диагностируют смертельную дозу и прогнозируют, что в течение 30 суток животное погибнет.
| МКОЯН Ф.А | |||
| Дифрактометрический анализ популяции эритроцитов белых крыс при лучевом поражении // Автореферат, Ереван, 1994 | |||
| Способ раннего распознавания лучевого поражения организма | 1955 |
|
SU103249A1 |
| СПОСОБ ДИАГНОСТИКИ РАДИАЦИОННЫХ ПОРАЖЕНИЙ ОРГАНИЗМА И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1997 |
|
RU2145712C1 |
| СПОСОБ ДИАГНОСТИКИ ТЯЖЕСТИ ОСТРОГО ЛУЧЕВОГО ПОРАЖЕНИЯ | 1995 |
|
RU2099709C1 |
Авторы
Даты
2014-04-27—Публикация
2012-12-13—Подача