Изобретение относится к области медицины и может быть использовано для определения противосвертывающей активности крови.
Проблема оценки состояния противосвертыващей активности крови является актуальной, поскольку механизмы, лежащие в основе высокой сосудистой смертности при ряде тяжелых заболеваниях, связанных с повреждением эндотелия, остаются окончательно не выясненными. Нарушения показателей гемостаза наблюдаются на всех этапах свертывания крови. Повышение свертываемости крови вследствие депрессии антикоагулянтного звена системы гемостаза ввиду недостаточности лабораторной диагностики, как правило, остается нераспознанным, а следовательно, при отсутствии своевременной коррекции может иметь фатальный исход. Общеизвестно, что своевременная и адекватная коррекция системы гемостаза, в том числе и ее противосвертывающего компонента, предотвращает дисциркуляторные нарушения в жизненно важных органах. Поэтому темой разработки является предложение способа определения противосвертывающей активности крови на основании показателей низкочастотной пьезотромбоэластограммы (НПТГ) пациента.
При повреждении сосуда кровь должна свертываться лишь в месте повреждения. Это обеспечивается имеющейся в крови противосвертывающей системой. Она же, в условиях нормы, играет ведущую роль в сохранении жидкого состояния крови. Различают два типа антикоагулянтов: антикоагулянты прямого действия (предсуществующие) - самостоятельно синтезированные (гепарин, антитромбин III - АТ-III, протеин С, протеин S, α2-макроглобулин); антикоагулянты непрямого действия, образующиеся во время свертывания крови, фибринолиза и активации других протеолитических систем (фибрин-антитромбин I, антитромбин IV, ингибиторы факторов VIII, IX и др.) [4].
Из всех предсуществующих антикоагулянтов наиболее универсален по действию и активности антитромбин III (АТ-III). Это один из α2-глобулинов плазмы. Концентрация его в плазме крови около 240 мг/мл, и он составляет 75% антикоагулянтной ее активности. Он инактивирует тромбин и почти все другие активированные факторы - XIIa, X1a, Xa, IXa. Другой антикоагулянт - гепарин - активен только вместе с АТ- III. Гепарин способствует фиксации АТ-III на поверхности эндотелиальных клеток, что в сотни раз повышает его активность. В печени в присутствии витамина К синтезируются протеин С и протеин S. Они снижают активность факторов V и VIII. Эндотелиальные клетки неповрежденной сосудистой стенки не только препятствуют адгезии тромбоцитов, но и синтезируют простациклин и гепариноподобный фактор (последний синтезируется также и тучными клетками соединительной ткани). Простациклин является мощным ингибитором агрегации тромбоцитов. В процессе свертывания крови и фибринолиза многие прокоагулянты и их метаболиты приобретают антикоагулянтные свойства. Наиболее мощным из них является фибрин, который адсорбирует и инактивирует образующийся при свертывании тромбин, который также проявляет антикоагулянтные свойства. Действуя ферментативно на протромбин, он отщепляет от последнего ингибитор фактора Xa [1,2,5].
Наиболее близким к предлагаемому является способ измерения начальных этапов свертывания крови с помощью низкочастотного пьезоэлектрического преобразователя, используя такие показатели крови, как:
A0 - начальный показатель агрегатного состояния крови,
A1 - показатель, характеризующий максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации,
A3 - показатель, характеризующий агрегатное состояние крови на этапе начала процесса полимеризации,
t3 - время достижения A3, которые используют при расчете
интенсивности коагуляционного драйва - показатель, характеризующий интегративное влияние про- и антикоагуляционных систем, который имеет следующий вид ИКД=(A3-A0)/t3,
A4 - показатель, характеризующий агрегатное состояние крови через 10 минут после достижения величины A3,
t4 всегда равен 10 мин.
Интенсивность полимеризации сгустка определяли как tgβ=(A4-A3)/(t4 - показатель, характеризующий скорость соединения мономерных молекул) [3]. Недостатком известного способа является недостаточная точность и информативность
Новый технический результат - повышение точности и информативности способа. Для решения поставленной задачи в способе определения противосвертывающей активности крови, заключающемся в проведении низкочастотной пьезотромбоэластографии и измерении вязкостных характеристик крови: A0 - начального показателя агрегатного состояния крови, A1 - показателя, характеризующего максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации, A3 - показателя, характеризующего агрегатное состояние крови на этапе начала процесса полимеризации, t3 - времени достижения A3, A4 - показателя, характеризующего агрегатное состояние крови через 10 мин после достижения величины A3, показателя t4, всегда равного 10 минутам, а также интенсивности полимеризации сгустка определенного, как tgβ=(A4-A3)/t4, коэффициент противосвертывающей активности крови КПА рассчитывают по формуле:
КПА=ИКД/ИПС, где
уравнение ИКД (интенсивность коагуляционного драйва) имеет вид ИКД=(A3-A1)/t3, и при значении КПА в пределах 1,5-2 определяют нормальную противосвертывающую активность, а при значениях меньше 1,5 определяют снижение противосвертывающей активности крови.
Способ осуществляют следующим образом: В условиях стандартизации процесса забора (силиконированным шприцем объемом 5 мл без наложения жгута из кубитальной вены) берут для исследования 0,5 мл цельной нестабилизированной венозной крови и в течение 5-10 секунд помещают в кювету прибора АРП-01М «Меднорд» (Регистрационное удостоверение № ФСР 2010/09767 от 30 декабря 2010 года). Время исследования составляет 60±10 минут. Методом низкочастотной пьезотромбоэластографии с использованием аппаратно-программного комплекса для клинико-диагностических исследований реологических свойств крови АРП-01М «Меднорд» оценивают следующие показатели:
A0 - начальный показатель агрегатного состояния крови (о.е.).
A1 - показатель, характеризующий максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации (о.е.).
A3 - показатель, характеризующий агрегатное состояние крови на этапе начала процесса полимеризации (о.е.).
t3 - время достижения A3 (мин).
ИКД - (A3-A1)/t3 - интенсивность коагуляционного драйва - показатель, характеризующий интегративное влияние про- и антикоагулянтных систем на скорость образования сгустка (о.е.).
A4 - показатель, характеризующий агрегатное состояние крови через 10 мин после достижения величины A3 (мин).
t4=10 мин.
ИПС - интенсивность полимеризации сгустка, определяется как tgβ=(A4-A3)/(t4 - показатель, характеризующий скорость соединения мономерных молекул).
Рассчитывают коэффициент противосвертывающей активности КПА по формуле:
КПА=ИКД/ИПС
и при значении КПА от 1,5 до 2 определяют норму, при значениях КПА менее 1,5 определяют снижение противосвертывающей активности крови.
Предлагаемый способ основан на анализе данных клинических исследований у пациенток с гестозом на фоне коррекции изменений системы гемостаза прямыми антикоагулянтами. После подписания информированного согласия, у 15 пациенток с гестозом методом низкочастотной пьезотромбоэластографии с использованием аппаратно-программного комплекса для клинико-диагностических исследований реологических свойств крови АРП-01М «Меднорд» (Регистрационное удостоверение № ФСР 2010/09767 от 30 декабря 2010 года). Комплекс основан на принципе низкочастотной пьезометрии и позволяет проводить исследование реологических свойств цельной крови, осуществлять контроль и регистрацию самых незначительных изменений ее агрегатного состояния, производить вычисление амплитудных и хронометрических констант, определять интенсивность процессов, характеризующих основные этапы свертывания крови, получать результаты стандартных реологических характеристик в виде графиков и таблиц показателей, характеризующих основные этапы свертывания крови, определяли следующие показатели крови (единицами измерения амплитудных показателей являются относительные единицы (о.е.), временных - минуты):
«A0» - начальный показатель агрегатного состояния крови.
«t0» - время начала исследования.
«A1» - показатель, характеризующий максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации.
«t1» - показатель, отражающий время достижения A1 (мин).
«t2» - время, за которое амплитуда A увеличивается на 100 единиц.
«ИКК» - интенсивность контактной фазы коагуляции, вычисляется эмпирически, отношением A0-A1/t1.
«КТА»=(100/t2-t1) - константа тромбиновой активности, определяется как время, прошедшее от конца периода реакции до увеличения значений амплитуды на 100 относительных единиц от уровня минимального значения амплитуды за период реакции.
«A3» - показатель, характеризующий агрегатное состояние крови на этапе начала процесса полимеризации.
«t3» - время достижения «A3».
«ИКД» - (A3-A1)/t3 - интенсивность коагуляционного драйва - показатель, характеризующий интегративное влияние про- и антикоагулянтных систем на скорость образования сгустка.
«A4» - показатель, характеризующий агрегатное состояние крови через 10 мин после достижения величины «A3».
«t4» - всегда равно 10 мин.
«ИПС» - интенсивность полимеризации сгустка, определяется как tgβ=(A4-A3)/t4 - показатель, характеризующий скорость соединения мономерных молекул «бок-в-бок», «конец-в-конец», формирующую сеть фибрина.
«A5» - показатель, отражающий агрегатное состояние крови в заключительном, стабилизационном этапе тромбообразования.
«Т» - время формирования сгустка (константа тотального времени свертывания крови).
«ИТС» - интенсивность тотального свертывания крови, отражает плотность фибрин-тромбоцитарной структуры сгустка. Определяется эмпирически (A5-A1)/(Т5-Т1).
«ИРЛС» - интенсивность ретракции и лизиса сгустка. Показатель, характеризующий спонтанный лизис сгустка.
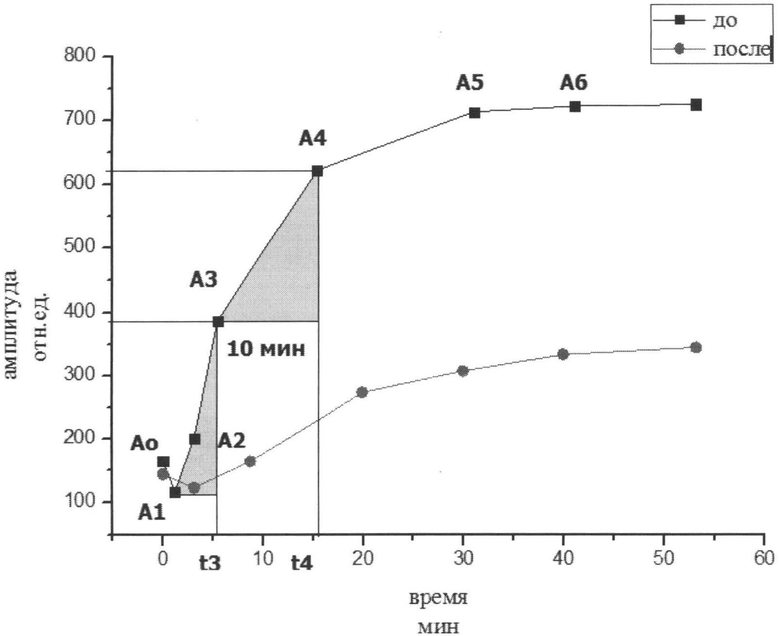
При анализе полученных данных (см. фиг.1) и зная, что включение противосвертывающей системы в коагуляционный каскад происходит с некоторым опозданием, были выбраны для определения противосвертывающей активности следующие показатели: «ИКД» - интенсивность коагуляционного драйва - показатель, характеризующий интегративное влияние про- и антикоагулянтных систем на скорость образования сгустка; «ИПС» - интенсивность полимеризации сгустка - показатель, характеризующий скорость соединения мономерных молекул «бок-в-бок», «конец-в-конец», формирующую сеть фибрина (как результирующая действия свертывающей и противосвертывающей систем).
Расчитывали коэффициент противосвертывающей активности КПА=ИКД/ИПС, который отражает суммарную антикоагулянтную активность до и через 6 часов после подкожного введения 0,6 мл фраксипарина. Статистическую обработку проводили на персональном компьютере с использованием программы SPSS 13.0 for Windows с подсчетом медианы, нижнего и верхнего квартилей (Me [LQ; UQ]). Критический уровень значимости p принимался равным 0,05.
Показатели низкочастотной пьезотромбоэластограммы (НПТГ) до и после введения препарата были следующими (табл.1, фиг.1). После введения препарата, направленного на увеличения противосвертывающей активности крови, КПА статистически достоверно (p<0,05) вырос с 1,13 [1,07; 2,90] до 6,66 [4,13; 7,41], что говорит о том, что предлагамым способом можно с достаточной точностью и достоверностью определять противосвертывающую активность крови
Пример 1 (выписка из истории болезни): Пациентка П., 29 лет, срок гестации 33 недели поступила в ОГАУЗ «Областной перинатальный центр» с жалобами на нарастание отеков в течение 3 недель, увеличение АД до 180/100 мм рт.ст. В анализах отмечалась анемия умеренная, гипопротеинемия, гиперкоагуляция (ПТИ=147%, о. фибриноген 5,82 г/л, АЧТВ 30,2 с, AT III 79%, плазминоген 87%, D-димер 6,92 мг/дл). В условиях стандартизации процесса забора (силиконированным шприцем объемом 5 мл без наложения жгута из кубитальной вены) взяли для исследования 0,5 мл цельной нестабилизированной венозной крови и в течение 5-10 секунд поместили в кювету прибора АРП-01М «Меднорд». Используя показатели полученной НПТГ ИКД=36,41 и ИПС=26,42, рассчитали КПА=36,41/26,42=1,37, что свидетельствовало об угнетении противосвертывающей активности, хотя лабораторное определение отдельных показателей этой системы не показало уменьшения их ниже значения нормы (AT III 79%, плазминоген 87%). Пациентке был назначен прямой антикоагулянт фраксипарин 0,6 мл подкожно 1 раз в день. Контрольные анализы на следующий день не показали значительных изменений лабораторных тестов, характеризующих отдельные компоненты противосвертывающей системы (AT III 81%, плазминоген 86%), зато коэффициент противосвертывающей активности, характеризующий суммарную активность противосвертывающей системы, увеличился более чем в 3 раза (КПА=5,26). Это позволяло говорить том, что применение предлагаемого способа позволило назначить адекватную и своевременную терапию выявленного состояния нефракционированным гепарином.
Пример 2 (выписка из истории болезни): Пациентка Б., 23 лет, срок гестации 25 недель поступила в ОГАУЗ «Областной перинатальный центр» с жалобами на тянущие боли внизу живота и скудные кровянистые выделения из половых путей. В анализах отмечалась гипопротеинемия, нормокоагуляция (ПТИ=97%, о. фибриноген 3,92 г/л, АЧТВ 35,7 с, AT III 92%, плазминоген 89%, D-димер 4,9 мг/дл). В условиях стандартизации процесса забора (силиконированным шприцем объемом 5 мл без наложения жгута из кубитальной вены) взяли для исследования 0,5 мл цельной нестабилизированной венозной крови и в течение 5-10 секунд поместили в кювету прибора АРП-01М «Меднорд». Используя показатели полученной НПТГ ИКД=49,21 и ИПС=26,42, рассчитали КПА=45,21/23,37=1,94, что свидетельствовало об нормальной противосвертывающей активности, как и по лабораторным тестам (AT III 92%, плазминоген 89%). Пациентка была госпитализирована с угрозой преждевременных родов и успешно пролечена от этого состояния генипралом. Проведение коррекции гемостаза ей не требовалось, за время госпитализации не наблюдалось тромботических или геморрагических осложнений.
Таким образом, проведенные клинические наблюдения позволяют сделать вывод о том, что предлагаемый способ дает возможность диагностировать изменения в противосвертывающей системе и осуществлять лабораторный контроль за эффективностью проводимой терапии, что, несомненно, позволит снизить частоту и выраженность осложнений, в том числе прямыми антикоагулянтами, которая, как известно, требует тщательного контроля.
Источники информации
1. Баркаган З.С. Диагностика и контролируемая терапия нарушений гемостаза [Текст]: монография / З.С. Баркаган, А.П. Момот. - М.: Ньюдиамед, 2008. - 292 с.
2. Баркаган З.С. О новых подходах к мониторингу антитромботических средств [Текст] / З.С. Баркаган, Е.Ф. Котовщикова, А.Н. Шилова // Клиническая фармакология и терапия. - 2005. - Т. 14, №3. - С.51-53.
3. Тютрин И.И. и др. Инструментальные методы оценки функционального состояния системы регуляции агрегатного состояния крови (PACK) с использованием низкочастотной вибрационной пьезоэлектрической гемокоагулографии (НПГК) // Материалы первой международной конференции «Диагностика, лечение и профилактика тромбозов и тромбоэмболий. Томск, 2011, С.11-17 (прототип).
4. Кишкун А.А. Клиническая лабораторная диагностика: учебное пособие [Текст] / А.А. Кишкун. - М.: ГЭОТАР-Медиа, 2010. - 976 с.
5. Момот А.П. Патология гемостаза. Принципы и алгоритмы клинико-лабораторной диагностики [Текст]: монография. - СПб.: Форма Т, 2006. - 208 с.
6. Диагностика, лечение и профилактика тромбозов и тромбоэмболий [Текст]: сборник статей / Под ред. Каирова Г.Т. - Томск, 2011. - 130 с.
Приложение: Таблица 1
Основные показатели НПТГ до и после введения фраксипарина, Me [LQ; UQ], n=15
На фиг.1 Интегральные НПТГ пациенток с гестозом (n=15) до и после введения фраксипарина.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выполнения низкочастотной пьезотромбоэластографии у мелких лабораторных животных | 2016 |
|
RU2634567C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИКОАГУЛЯНТНОГО ПОТЕНЦИАЛА СОСУДИСТОЙ СТЕНКИ | 2018 |
|
RU2690856C1 |
| Способ забора крови у мелких лабораторных животных для выполнения низкочастотной пьезотромбоэластографии | 2017 |
|
RU2648032C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНТРАОПЕРАЦИОННОЙ КРОВОПОТЕРИ У БОЛЬНЫХ С ИДИОПАТИЧЕСКИМ СКОЛИОЗОМ | 2016 |
|
RU2635503C1 |
| СПОСОБ НАЗНАЧЕНИЯ ИНДИВИДУАЛЬНОЙ АНТИТРОМБОТИЧЕСКОЙ ТЕРАПИИ В ОСТРЫЙ И РАННИЙ ПЕРИОДЫ ПОЗВОНОЧНО-СПИННОМОЗГОВОЙ ТРАВМЫ ШЕЙНОГО ОТДЕЛА | 2021 |
|
RU2770633C1 |
| Способ оценки функции тромбоцитов в цельной цитратной крови | 2016 |
|
RU2659421C2 |
| Способ оценки повышенного риска возникновения флеботромбозов у пациентов с ишемической болезнью сердца | 2016 |
|
RU2624859C1 |
| Способ коррекции гиперкоагуляционного состояния при введении противоопухолевого препарата цисплатина | 2020 |
|
RU2743848C1 |
| Способ эндоскопического лечения синдрома Меллори-Вейсса | 2021 |
|
RU2762121C1 |
| СПОСОБ ОЦЕНКИ УРОВНЯ АНТИКОАГУЛЯЦИИ НЕФРАКЦИОНИРОВАННЫМ ГЕПАРИНОМ ПРИ ПРОВЕДЕНИИ ГЕМОДИАЛИЗА У ПАЦИЕНТОВ С ОСТРЫМ ПОВРЕЖДЕНИЕМ ПОЧЕК | 2014 |
|
RU2571505C1 |
Изобретение относится к области медицины, а именно к определению противосвертывающей активности крови. Сущность способа состоит в том, что проводят низкочастотную пьезотромбоэластографию и измеряют вязкостные характеристики крови: A0 - начальный показатель агрегатного состояния крови, A1 - показатель, характеризующий максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации, A3 - показатель, характеризующий агрегатное состояние крови на этапе начала процесса полимеризации, t3 - время достижения A3, A4 - показатель, характеризующий агрегатное состояние крови через 10 мин после достижения величины A3, показатель t4, всегда равного 10 минутам, а также интенсивности полимеризации сгустка (ИПС), рассчитывают коэффициент противосвертывающей активности крови (КПА) по формуле. При значении КПА в пределах 1,5-2 определяют нормальную противосвертывыющую активность, а при значениях меньше 1,5 определяют снижение противосвертывающей активности крови. Использование заявленного способа позволяет осуществлять мониторинг противосвертывающей активности крови, как на этапе диагностики, так и на любом этапе терапии нарушений в системе гемостаза, с высокой точностью и достоверностью, за счет возможности комплексной оценки противосвертывающей активности. 1 табл., 1 ил., 2 пр.
Способ определения противосвертывающей активности крови, заключающийся в проведении низкочастотной пьезотромбоэластографии и измерении вязкостных характеристик крови: A0 - начального показателя агрегатного состояния крови, A1 - показателя, характеризующего максимальное изменение агрегатного состояния исследуемой крови на этапе контактной активации, A3 - показателя, характеризующего агрегатное состояние крови на этапе начала процесса полимеризации, t3 - времени достижения A3, A4 - показателя, характеризующего агрегатное состояние крови через 10 мин после достижения величины A3, показателя t4, всегда равного 10 минутам, а также интенсивности полимеризации сгустка (ИПС), определенного как tgβ=(A4-A3)/t4, отличающийся тем, что коэффициент противосвертывающей активности крови КПА рассчитывают по формуле:
КПА=ИКД/ИПС, где
уравнение ИКД (интенсивность коагуляционного драйва) имеет вид ИКД=(A3-A1)/t3, и при значении КПА в пределах 1,5-2 определяют нормальную противосвертывыющую активность, а при значениях меньше 1,5 определяют снижение противосвертывающей активности крови.
| ТЮТРИН И.И | |||
| и др | |||
| Инструментальный метод оценки функционального состояния системы регуляции агрегатного состояния крови (РАСК) с использованием низкочастотной вибрационной пьезоэлектрической гемокоагулографии (НПГК)// Материалы первой международной конференции "Диагностика, лечение и профилактика тромбозов и тромбоэмболий" | |||
| Томск | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| RU | |||
Авторы
Даты
2014-10-10—Публикация
2012-12-20—Подача