Уровень техники, к которой относится изобретение
Диацереин [4,5-бис(ацетилокси)-9,10-диоксо-2-антраценкарбоновая кислота] представляет собой очищенное в высокой степени производное антрахинона. В нескольких странах он утвержден как симптоматичное медленно действующее лекарственное средство для лечения остеоартрита (SYSADOA). Реин представляет собой основной активный метаболит диацереина. Показано, что реин контролирует уровень концентрации глюкозы в крови страдающих диабетом 2 типа (или II типа) подопытных грызунов. Однако никакие исследования не показали, что диацереин способен контролировать уровень глюкозы в крови человека с диабетом 2 типа. В литературе отсутствуют сведения о том, что диацереин можно использовать в качестве дополнительного средства для лечения страдающих диабетом II типа пациентов с недостаточной реакцией на существующие в настоящее время средства противодиабетического лечения.
Распространение диабета растет во всем мире. Приблизительно 7% населения в возрасте от 45 до 64 лет страдает диабетом, и это число значительно увеличивается для населения в возрасте старше 65 лет. Существуют две формы диабета. В форме заболевания, известного как тип II, инсулиннезависимый сахарный диабет (NIDDM), или возникающий во взрослом возрасте (в отличие от возникающего в молодом возрасте диабета типа I) он представляет собой расстройство, которое отличается высоким уровне глюкозы в крови в сочетании с инсулинорезистентностью и относительным недостатком инсулина. Поджелудочная железа у страдающих диабетом II типа пациентов зачастую продолжает выделять инсулин. Однако этот инсулин не является эффективным в предотвращении симптомов диабета, которые включают увеличение сердечно-сосудистых факторов риска, таких как гипергликемия, повышенное кровяное давление, гипертригликемия, высокие сывороточные концентрации содержащего липопротеины низкой плотности (LDL) холестерина, низкие сывороточные концентрации содержащего липопротеины высокой плотности (HDL) холестерина, нарушенный углеводный метаболизм, глюкозурия, пониженная чувствительность к инсулину и общее ожирение. Как известно, многие из этих сердечно-сосудистых факторов риска предшествуют возникновению диабета вплоть до десяти лет. Симптомы диабета II типа приводят к серьезным осложнениям, включая макрососудистые осложнения (заболевание коронарных артерий, заболевание периферических артерий и инсульт) и микрососудистые осложнения (ретинопатия, нефропатия и нейропатия). В настоящее время признана важность контроля уровня глюкозы в крови и поддержание уровня гликозилированного гемоглобина A1c (HbA1c) ниже 7,0% в предотвращении диабетических осложнений.
В течение нескольких последних лет появился ряд классов противогипергликемических средств, каждый из которых обладает своим уникальным механизмом действия: сульфонилмочевины, бисгуаниды, ингибиторы α-глюкозидазы, тиазолидиндионы (TZD), ингибиторы дипептидилпептидазы-4 (ингибиторы DPP-4), не содержащие сульфонилмочевины стимуляторы секреции инсулина, аналог глюкагоноподобного пептида-1 и инсулин. Согласно клиническим инструкциям, используемое, в первую очередь, снижающее уровень глюкозы в крови лечение диабета II типа представляет собой монотерапию метформином или сульфонилмочевиной. Однако монотерапия метформином или сульфонилмочевиной производит ограниченный эффект. Лишь приблизительно 44% пациентов сохраняют HbA1c ниже 7% после лечения в течение трех лет, и только 13% пациентов сохраняют этот уровень после девяти лет. Если первоочередное лечение оказывается неудовлетворительным, пациентов переводят на комбинированные терапии второй очереди, такие как сочетания метформина с сульфонилмочевиной. Среди пациентов, которым не помогла монотерапия каким-либо из этих средств, лишь приблизительно 30% пациентов при комбинированной терапии второй очереди сочетанием метформина и сульфонилмочевины достигают уровня HbA1c ниже 7% после двух лет лечения. Если такого рода лечение все же оказывается недостаточным для контроля уровня глюкозы в крови пациентов, то для лечения в режиме второй очереди можно вводить ингибиторы DPP-4, тиазолидиндион, аналоги глюкагоноподобного пептида-1, меглитиниды, ингибиторы α-глюкозидазы и/или инсулин.
Несмотря на существование противодиабетических средств, некоторым пациентам не удается достижение целей лечения. Соответственно, по-прежнему существует потребность в новом средстве, которое эффективно улучшает гликемический контроль диабета II типа
Сущность изобретения
Настоящее изобретение относится к способам лечения страдающих диабетом II типа пациентов. Описанные способы являются особенно подходящими для страдающих диабетом II типа пациентов, у которых существует недостаточный гликемический контроль при использовании текущего противодиабетического лечения.
Более конкретно, настоящее изобретение предлагает способы применения диацереина или его производных для лечения диабета II типа.
В одном варианте осуществления настоящее изобретение предлагает способ дополнительного лечения сахарного диабета II типа, включающий введение пациенту с диабетом II типа, у которого существует недостаточная реакция на противодиабетическое средство, терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита.
В еще одном варианте осуществления настоящее изобретение предлагает способ улучшения гликемического контроля у пациента, принимающего, по меньшей мере, одно противодиабетическое средство, включающий введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, пролекарства, аналога или активного метаболита и b) указанного противодиабетического средства.
В еще одном варианте осуществления настоящее изобретение предлагает способ комбинированного лечения сахарного диабета II типа, включающий введение нуждающемуся в этом пациенту: a) по меньшей мере, одного противодиабетического средства и b) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита.
В еще одном варианте осуществления настоящее изобретение предлагает способ уменьшения побочного эффекта противодиабетического средства, вводимого страдающему диабетом пациенту, включающий введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита и b) указанного противодиабетического средства.
В еще одном варианте осуществления настоящее изобретение предлагает способ уменьшения сердечно-сосудистого риска противодиабетического средства, вводимого страдающему диабетом пациенту, включающий введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита и b) указанного противодиабетического средства.
Краткое описание чертежей
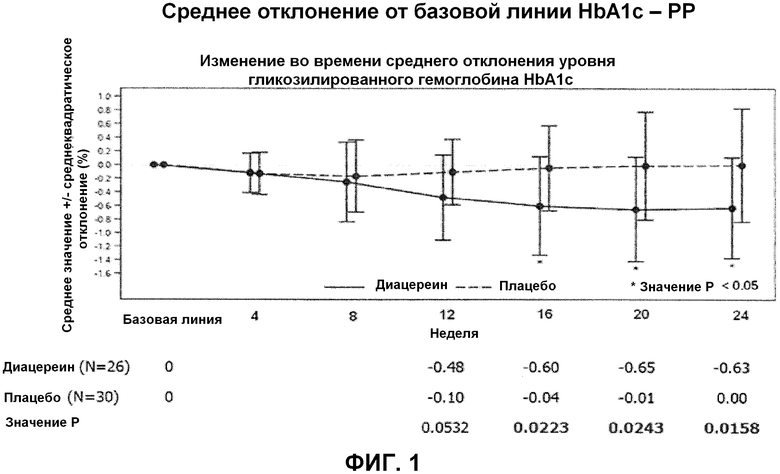
Фиг.1 представляет график, демонстрирующий среднее изменение уровней гликозилированного гемоглобина (HbA1c) пациентов в ходе приема диацереина или плацебо.
Фиг.2 представляет график, демонстрирующий среднее изменение уровней глюкозы в плазме натощак у пациентов в ходе приема диацереина или плацебо.
Фиг.3 представляет график, демонстрирующий среднее изменение оценки гомеостатической модели (HOMA) уровней функции β-клеток пациентов в ходе приема диацереина или плацебо.
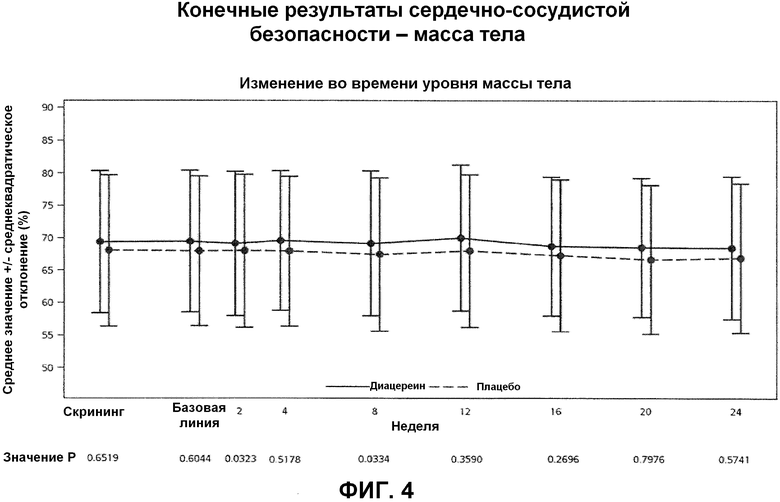
Фиг.4 представляет график, демонстрирующий среднее изменение уровней массы тела пациентов в ходе приема диацереина или плацебо.
Подробное описание изобретения
Согласно настоящему изобретению, диацереин можно использовать для лечения диабета II типа в виде монотерапии или в сочетании с традиционными противодиабетическими средствами. Предпочтительно диацереин можно вводить в текущие противодиабетические средства для повышения реакционной способности или синергии функций текущих средств, по отношению к которым пациенты уже проявили недостаточную реакцию.
При упоминании в настоящем документе диацереин (4,5-бис(ацетилокси)-9,10-диоксо-2-антраценкарбоновая кислота) означает соединение, имеющее следующую структурную формулу:
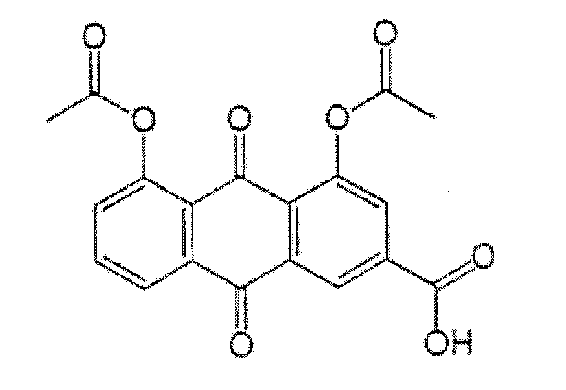
Фармацевтически приемлемые соли, пролекарства и активные метаболиты диацереина также предусмотрены для использования в настоящем изобретении. Фармацевтически приемлемые соли включают соли кислотных или основных групп. Реин (9,10-дигидро-4,5-дигидрокси-9,10-диоксо-2-антраценкарбоновая кислота) и моноацетилреин представляют собой известные активные метаболиты диацереина. Пролекарство представляет собой фармакологически неактивное производное активного лекарства, которое предназначено для превращения в активное лекарство в живом организме под действием физиологических процессов, таких как гидролиз, метаболизм и т.п.
В одном варианте осуществления настоящее изобретение предлагает способ дополнительного лечения сахарного диабета II типа, включающий введение пациенту с диабетом II типа, у которого существует недостаточная реакция на противодиабетическое средство, терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита.
При использовании в настоящем документе термин «лечить» или «лечение» означает преодоление, предотвращение, ингибирование или замедление развития заболевания, расстройства или состояния, к которому относится данный термин, или один, или более симптомов указанного заболевания, расстройства или состояния.
При использовании в настоящем документе термин «дополнительное лечение» или «сопутствующее лечение» означает вспомогательное лечение пациента, который уже получал, по меньшей мере, один из других видов противодиабетического лечения. Средство, используемое для дополнительного лечения, вводят пациенту, чтобы улучшить эффективность первичного лечения.
При использовании в настоящем документе термин «противодиабетические средства» означает средства, используемые для лечения сахарного диабета путем снижения уровней глюкозы в крови. Примеры имеющихся в настоящее время противодиабетических средств составляют, но не ограничиваются этим, сульфонилмочевина, бигуанидины, ингибиторы α-глюкозидазы, тиазолидиндионы (TZD), ингибиторы дипептидилпептидазы-4 (ингибиторы DPP-4), не содержащие сульфонилмочевины стимуляторы секреции инсулина, аналоги глюкагоноподобного пептида-1 (аналоги GLP-1) и инсулин. Более конкретно, противодиабетические средства включают, но не ограничиваются этим, метформин, глибурид, глимепирид, глипирид, глипизид, хлорпропамид, гликлазид, акарбоза, миглитол, пиоглитазон, троглитазон, розиглитазон, изаглитазон, мураглитизар, пелиглитазан, ситаглиптин, саксаглиптин, вилдаглиптин, алоглиптин, линаглиптин, дутоглиптин, дутоглиптин, репаглинид, натеглинид, митиглинид, эксенатид, лираглутид, албиглутид и инсулин. Эти средства можно вводить в ходе монотерапии или в сочетании.
При использовании в настоящем документе термин «субъект» включает людей и животных.
Традиционно пациенты с диагностированным диабетом II типа обычно получают одно или более пероральных противодиабетических средств, чтобы контролировать у себя уровень глюкозы в крови, кровяное давление и уровень липидов в целях сведения до минимума риска осложнений.
В одном варианте осуществления настоящее изобретение предлагает способ дополнительного лечения сахарного диабета II типа, включающий введение пациенту с диабетом II типа, у которого имеет место недостаточная реакция на противодиабетическое средство, терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита.
Согласно одному варианту осуществления дополнительного лечения по настоящему изобретению, диацереин добавляют в противодиабетические средства, которые уже принимают пациенты. Более конкретно, дополнительное лечение согласно настоящему изобретению можно использовать для снижения уровня глюкозы в крови, уменьшения инсулинорезистентности, уменьшения гликозилированного гемоглобина A1c (HbA1c), повышения уровней инсулина после приема пищи или снижения уровня глюкозы после приема пищи.
В одном варианте осуществления страдающие диабетом II типа для пациентов с инсулинорезистентностью, непереносимостью глюкозы, гипергликемией или гиперинсулинемией, для которых оказывался недостаточным контроль при противодиабетическом лечении противодиабетическим средством в чистом виде или в сочетании с другими противодиабетическими средствами, является подходящим дополнительное лечение согласно настоящему изобретению.
В предпочтительном варианте осуществления пациент с диабетом II типа, у которого имеет место недостаточная реакция на противодиабетическое средство (т.е. пациент, у которого инсулинорезистентность, непереносимость глюкозы, гипергликемия или гиперинсулинемия недостаточно контролируется посредством противодиабетического лечения), представляет собой пациента, у которого уровень гемоглобина A1c (HbA1c) составляет выше 7%, несмотря на прием одного или более противодиабетических средств. Уровень HbA1c представляет собой процентную долю гемоглобина, связанного с глюкозой, и является показателем долгосрочного гликемического контроля. Предпочтительно для пациентов, у которых уровень HbA1c составляет от 8 до 10% в процессе приема, по меньшей мере, одного противодиабетического средства, дополнительное лечение согласно настоящему изобретению является особенно подходящим.
Терапевтически эффективное количество диацереина может изменяться в зависимости от индивидуальных различий возраста, массы тела, степени диабета и состояния пациента, и его может определить опытный специалист в данной области медицины. В предпочтительном варианте осуществления настоящего изобретения терапевтически эффективное количество диацереина находится в интервале от 25 до 200 мг в сутки. В одном варианте осуществления диацереин или его производные (включая, но не ограничиваясь этим, фармацевтически приемлемые соли, пролекарства, аналоги и активные метаболиты диацереина) можно вводить один или два раза в сутки. Терапевтически эффективное количество фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита диацереина предпочтительно представляет собой эквивалент от 25 до 200 мг основания диацереина в сутки.
Субъекты, которым поставлен диагноз сахарного диабета II типа, могут принимать диацереин, его фармацевтически приемлемые соли, аналоги, пролекарства или активные метаболиты в сочетании с одним или несколькими противодиабетическими средствами для достижения целей лечения.
Цель лечения может представлять собой снижение уровня глюкозы в крови, уменьшение инсулинорезистентности, уменьшение гликозилированного гемоглобина A1c (HbA1c), повышение уровней инсулина после приема пищи или снижение уровней глюкозы после приема пищи. Более конкретно, цели лечения включают, но не ограничиваются этим: (a) HbA1c от 6% до 7,0%; (b) уровень глюкозы в крови натощак: от 4,0 до 6,0 ммоль/л (от 72 до 108 мг/дл) и (c) уровень глюкозы в крови через 2 часа после приема пищи: от 5,0 до 8,0 ммоль/л (от 90 до 144 мг/дл).
В одном варианте осуществления способ дополнительного лечения диабета II типа улучшает почечные функции пациента. Улучшение почечных функций можно продемонстрировать уменьшением клиренса креатинина у пациента.
В еще одном варианте осуществления способ дополнительного лечения диабета II типа уменьшает инсулинорезистентность пациента. Уменьшение инсулинорезистентности можно продемонстрировать снижением уровней гликозилированного гемоглобина у пациента.
В еще одном варианте осуществления способ дополнительного лечения диабета II типа приводит к уменьшению воспалительных цитокинов (включая, но не ограничиваясь этим, интерлейкины и факторы некроза опухолей) у пациента. Интерлейкины включают, но не ограничиваются этим, интерлейкин IL-6 и интерлейкин IL-12. Факторы некроза опухолей включают, но не ограничиваются этим, TNF-α.
В еще одном варианте осуществления настоящее изобретение предлагает способ улучшения гликемического контроля у пациента, принимающего, по меньшей мере, одно противодиабетическое средство, причем указанный способ включает введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита и b) указанного противодиабетического средства.
В одном варианте осуществления способ улучшения гликемического контроля улучшает почечные функции пациента. Улучшение почечных функций можно продемонстрировать уменьшением клиренса креатинина у пациента.
В еще одном варианте осуществления способ улучшения гликемического контроля уменьшает инсулинорезистентность пациента. Уменьшение инсулинорезистентности можно продемонстрировать снижением уровней гликозилированного гемоглобина у пациента.
В еще одном варианте осуществления способ улучшения гликемического контроля приводит к уменьшению воспалительных цитокинов (включая, но не ограничиваясь этим, интерлейкины и факторы некроза опухолей) у пациента. Интерлейкины включают, но не ограничиваются этим, интерлейкин IL-6 и интерлейкин IL-12. Факторы некроза опухолей включают, но не ограничиваются этим, TNF-α.
В одном варианте осуществления для страдающих диабетом II типа пациентов инсулинорезистентностью, непереносимостью глюкозы, гипергликемией или гиперинсулинемией, состояние которых недостаточно контролировало противодиабетическое лечение, по меньшей мере, одним противодиабетическим средством или их сочетанием, является подходящим способ улучшения гликемического контроля согласно настоящему изобретению. Предпочтительно для пациентов с диабетом II типа, у которых оказывается недостаточная реакция на противодиабетическое средство, является подходящим способ улучшения гликемического контроля согласно настоящему изобретению.
В еще одном варианте осуществления настоящее изобретение предлагает способ комбинированного лечения сахарного диабета II типа, включающий введение нуждающемуся в этом пациенту: a), по меньшей мере, одного противодиабетического средства и b) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита.
В еще одном варианте осуществления настоящее изобретение предлагает способ уменьшения побочного эффекта противодиабетического средства, вводимого страдающему диабетом пациенту, включающий введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита и b) указанного противодиабетического средства.
В еще одном варианте осуществления настоящее изобретение предлагает способ уменьшения сердечно-сосудистого риска противодиабетического средства, вводимого страдающему диабетом пациенту, включающий введение указанному пациенту: a) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, аналога, пролекарства или активного метаболита и b) указанного противодиабетического средства.
При введении нуждающемуся в этом пациенту диацереин или его фармацевтически приемлемые соли, аналоги, пролекарства или активные метаболиты можно приготовить в виде фармацевтической композиции. Фармацевтические композиции, предусмотренные для использования по настоящему изобретению, могут принимать форму твердого материала, раствора, эмульсии, дисперсии, мицеллы, липосомы и т.п. Композиции можно вводить, используя любые способы, известные в медицине, в том числе перорально, назально, парентерально, местно, трансдермально или ректально. Предпочтительно композиции приспособлены для перорального введения. Например, лекарственное средство можно смешивать с подходящими наполнителями, изготавливая таблетки, капсулы, шарики, пастилки, лепешки, растворы, порошки или гранулы, суспензии, твердые или мягкие капсулы и любые другие формы, подходящие для использования. Способы изготовления фармацевтических композиций и выбор подходящих наполнителей легко понятны специалисту в данной области медицины.
Следующий пример демонстрирует некоторые аспекты настоящего изобретения. Данный пример не предназначен для ограничения настоящего изобретения каким-либо образом.
Пример 1
Рандомизированное двойное слепое контролируемое плацебо для исследования диацереина для пациентов с неконтролируемым сахарным диабетом 2 типа
Задачи: оценка эффективности и безопасности диацереина для лечения сахарного диабета 2 типа.
Первичные конечные результаты: сравнение воздействия лечения с добавкой диацереина и без него (плацебо) на гликозилированный гемоглобин (HbA1c) после 24 недель двойного слепого лечения страдающих сахарным диабетом 2 типа пациентов, недостаточно контролируемых предшествующим противодиабетическим лечением.
Пациенты: страдающие сахарным диабетом 2 типа пациенты мужского или женского пола (BMI≤35 кг/м2) на стабильной пероральной гипогликемической монотерапии в течение, по меньшей мере, 3 месяцев, предшествующих посещению для скринингового обследования. Уровни гемоглобина A1c (HbA1c), измеренные при посещении для скринингового обследования, составляли от 7% до 12%. Участвующие в исследовании пациенты принимали одно или несколько пероральных противогипергликемических средств, включая сульфонилмочевину, бигуанидины, ингибиторы α-глюкозидазы, тиазолидиндионы (TZD) и не содержащие сульфонилмочевины стимуляторы секреции инсулина.
Процедура: это было рандомизированное двойное слепое параллельное сравнительное исследование с использованием 50 мг диацереина по сравнению с плацебо для страдающих сахарным диабетом 2 типа пациентов, недостаточно контролируемых предшествующим противодиабетическим лечением. Начальная доза диацереина составляла 50 мг один раз в сутки каждое утро в течение 4 недель и могла быть доведена до 50 мг два раза в сутки (утром и вечером), если пациенты привыкали к лечению. Скрининг пациентов на пригодность к исследованию проводили за четыре недели (неделя - 4) перед началом на базовой линии (неделя 0). Во время этого четырехнедельного периода скрининга участники продолжали свое предшествующее противодиабетическое лечение, соблюдали принятую диету и другие условия привычного образа жизни. Чтобы получить допуск на рандомизацию после четырехнедельного периода скрининга, пациенты не должны были испытывать гипогликемию и должны были показывать в двух измерениях уровня глюкозы в плазме натощак (FPG) результаты от 135 до 250 мг/дл. После окончания периода скрининга пациентам, которые соответствовали требованиям допуска, случайным образом назначали прием 50 мг диацереина или плацебо два раза в сутки в течение 24 недель наблюдения. Во время периода лечения/наблюдения предшествующее противодиабетическое лечение, в том числе класс и/или дозировку лекарственного средства, не изменяли. За это время пациентам назначали посещение медицинского центра восемь раз (скрининг, базовая линия, недели 4, 8, 12, 16, 20 и 24). Суммарная продолжительность исследования, включая период скрининга, для каждого пациента составляла 28 недель. После завершения лечения/наблюдения следовал двухнедельный проверочный период. Во время этого проверочного периода пациентов проверяли на нежелательные явления.
Статистический метод (статистические методы) для оценок эффективности/безопасности: разность (диацереин минус плацебо) уменьшения HbA1c между двумя исследуемыми группами изучали методом ковариационного анализа (ANCOVA), в котором использован уровень базовой линии как ковариата. Вычисляли соответствующий доверительный интервал 95%. Кроме того, анализировали изменения в пределах группы, используя парный критерий Стьюдента для оценки отклонений от базовой линии в каждой группе пациентов.
Для параметров эффективности представлена описательная статистика при посещении. Статистический анализ осуществляли для оценки среднего отклонения от базовой линии. Площадь под кривой зависимости концентрации от времени (AUC) использовали для оценки параметров, измеряемых в исследовании переносимости перорального введения глюкозы.
Нежелательные явления обобщали, как указывает Медицинский словарь терминологии регуляторной деятельности (MedDRA) в разделе терминологии нежелательных явлений. В таблице приведено число пациентов с индивидуальным патологическим состоянием как нежелательной реакцией на лекарственный препарат и суммарное число пациентов, имевших, по меньшей мере, одно нежелательное явление на класс системы органов. Если это было целесообразно, частоту нежелательных явлений сравнивали для каждой из двух групп пациентов, используя точный критерий Фишера (Fisher).
Результаты: в данном двойном слепом исследовании параллельных групп принимали участие 76 пациентов с диабетом 2 типа, недостаточно контролируемым текущим пероральным противодиабетическим лечением (таблица 1). Пациентов случайным образом распределяли по двум исследуемым группам. Одна группа получала диацереин (38 пациентов), и другая группа получала плацебо (38 пациентов). Из получавших диацереин 38 пациентов 26 пациентов выполнили исследование, как и 30 из 38 пациентов, получавших плацебо. Никто из пациентов не сменил свое противодиабетическое лечение в течение 24 недель периода исследования.
Противодиабетическое лечение всех рандомизированных пациентов
Сочетания лекарственных средств: лечение двумя, тремя или четырьмя пероральными противодиабетическими средствами (выбранными из метформина, сульфонилмочевины, акарбозы, репаглинида, пиоглитазона и ситаглиптина).
Первичные конечные результаты: средняя абсолютная разность уровней HbA1c между базовой линией и результатом через 24 недели представляла собой уменьшение на 0,63 процентных пункта в группе диацереина и отсутствие изменения в группе плацебо; таким образом, разность между группами составила 0,63 процентных пункта (P=0,0158). См. фиг.1, которая представляет среднее отклонение от базовой линии уровней HbA1c.
Число пациентов, у которых происходило какое-либо уменьшение уровней HbA1c в течение 24 недель, составляло 20 из 26 пациентов в группе диацереина по сравнению с 15 из 30 пациентов в группе плацебо. Уровни HbA1c были значительно ниже в группе диацереина после 20 недель, чем в группе плацебо (абсолютное уменьшение составило 0,60%; P=0,0223). См. фиг.1.
Вторичные конечные результаты:
Гликемия
Уровни глюкозы в плазме натощак были систематически ниже в группе диацереина, чем в группе плацебо после 24 недель. См. фиг.2.
Функция β-клеток
Постоянное улучшение оценки гомеостатической модели (HOMA) функции β-клеток (HOMA-BETA) наблюдали в группе диацереина, но не в группе плацебо. Как демонстрирует фиг.3, после 24 недель одна и та же доза глюкозы вызывала большее выделение инсулина у принимавших диацереин пациентов, чем у принимавших плацебо пациентов (диацереин 56,26 и плацебо 45,53). Внутригрупповое отклонение от базовой линии в HOMA-BETA было значительным в группе диацереина, но не в группе плацебо.
Конечные результаты сердечно-сосудистой безопасности
Отсутствовали статистически значимые различия между группами пациентов в отношении массы тела (фиг.4), кровяного давления (таблицы 2 и 3), частоты пульса (таблица 4) и липидных профилей (таблицы 5-8) при сравнении уровней базовой линии и уровней после 24 недель. Конечные результаты сердечно-сосудистой безопасности показали, что введение диацереина в текущее противодиабетическое лечение не увеличивало риски сердечных приступов и сердечно-сосудистых расстройств.
Конечные результаты сердечно-сосудистой (CV) безопасности - систолическое кровяное давление
Конечные результаты сердечно-сосудистой безопасности - диастолическое кровяное давление
Конечные результаты сердечно-сосудистой безопасности -
частота пульса
Конечные результаты сердечно-сосудистой безопасности -
Суммарное содержание холестерина
Конечные результаты сердечно-сосудистой безопасности - содержание триглицеридов
Конечные результаты сердечно-сосудистой безопасности - содержание липопротеинов высокой плотности (HDL)
Конечные результаты сердечно-сосудистой безопасности - содержание липопротеинов низкой плотности (LDL)
Нежелательные явления: в течение периода исследований, по меньшей мере, один нежелательный эффект (AE) отметили 20 (54,1%) пациентов в группе диацереина и 18 (47,4%) пациентов в группе плацебо. Никаких статистически значимых различий между двумя группами не обнаружено в доле пациентов, жаловавшихся на нежелательные явления. В обеих группах часто отмечаемые нежелательные явления представляли собой инфекции дыхательных путей и диарею. В частности, симптоматическая гипогликемия не наблюдалась даже у пациентов с отмеченным улучшением уровней HbA1c.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ ИНГИБИТОРА DPP-IV ДЛЯ СНИЖЕНИЯ ПРИСТУПОВ ГЛИКЕМИИ | 2006 |
|
RU2440143C2 |
| СПОСОБ СНИЖЕНИЯ ВЕСА | 2013 |
|
RU2664442C2 |
| ЛИКСИСЕНАТИД И МЕТФОРМИН ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА ТИПА 2 | 2012 |
|
RU2623023C2 |
| СПОСОБ УЛУЧШЕНИЯ ФУНКЦИИ ПЕЧЕНИ | 2013 |
|
RU2653478C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2007 |
|
RU2442585C2 |
| АНТИДИАБЕТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2000 |
|
RU2276604C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ГИПЕРУРИКЕМИИ И МЕТАБОЛИЧЕСКИХ НАРУШЕНИЙ, СВЯЗАННЫХ С ГИПЕРУРИКЕМИЕЙ | 2012 |
|
RU2603050C2 |
| ФАРМАЦЕВТИЧЕСКИЕ АГЕНТЫ, КОМПОЗИЦИИ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К НИМ | 2018 |
|
RU2765286C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ГЛИКЕМИЧЕСКОМ КОНТРОЛЕ У ПАЦИЕНТОВ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА | 2012 |
|
RU2650616C2 |
| ПРОФИЛАКТИКА ГИПОГЛИКЕМИИ У ПАЦИЕНТОВ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА | 2012 |
|
RU2583134C2 |


Группа изобретений относится к улучшению гликемического контроля субъектов, страдающих диабетом I и II типа. Предложены: способ дополнительного лечения к лечению противогликемическими средствами субъектов, страдающих диабетом I и II типа, способ улучшения гликемического контроля субъектов, страдающих диабетом I и II типа и способ комбинированного лечения субъектов, страдающих диабетом I и II типа. Все способы включают в дополнение к противодиабетическому средству введение эффективного количества диацереина или его фармацевтически приемлемой соли, моноацетилреина или реина. Технический результат: обеспечено снижение инсулинорезистентности по показателю уровней гликозилированного гемоглобина у больных, уменьшение уровней глюкозы в плазме крови натощак. 3 н. и 8 з.п. ф-лы, 4 ил., 8 табл., 1 пр.
1. Способ дополнительного к лечению противогликемическими средствами лечения сахарного диабета типа 1 и типа 2, включающий введение субъекту с диабетом типа 1 и типа 2, у которого существует недостаточная реакция на противодиабетическое средство, терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, моноацетилреина или реина.
2. Способ по п. 1, в котором указанный субъект представляет собой страдающего диабетом II типа пациента с состоянием, выбранным из группы, состоящей из инсулинорезистентности, непереносимости глюкозы, гипергликемии или гиперинсулинемии.
3. Способ по п. 1, в котором указанное терапевтически эффективное количество диацереина составляет от 25 до 200 мг в день.
4. Способ улучшения гликемического контроля у пациента, принимающего противодиабетическое средство, включающий введение указанному пациенту: а) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, моноацетилреина или реина, и b) указанного противодиабетического средства.
5. Способ по п. 4, в котором указанное противодиабетическое средство представляет собой, по меньшей мере, одно средство, выбранное из группы, состоящей из сульфонилмочевины, бигуанида, ингибитора α-глюкозидазы, тиазолидиндиона, агониста рецептора активируемого пролифератором пероксисом, ингибитора дипептидилпептидазы-4, не содержащего сульфонилмочевины стимулятора секреции инсулина, аналога глюкагоноподобного пептида-1, метформина, глибурида, глимепирида, глипирида, глипизида, хлорпропамида, гликлазида, акарбозы, миглитола, пиоглитазона, троглитазона, розиглитазона, изаглитазона, мураглитизара, пелиглитазара, ситаглиптина, саксаглиптина, вилдаглиптина, алоглиптина, линаглиптина, дутоглиптина, репаглинида, натеглинида, митиглинида, эксенатида, лираглутида, албиглутида и инсулина.
6. Способ по п. 4, в котором указанный субъект представляет собой страдающего диабетом II типа пациента с состоянием, выбранным из группы, состоящей из инсулинорезистентности, непереносимости глюкозы, гипергликемии или гиперинсулинемии.
7. Способ по п. 4, в котором указанное терапевтически эффективное количество диацереина составляет от 25 до 200 мг в день.
8. Способ комбинированного лечения сахарного диабета типа 1 и типа 2, включающий введение нуждающемуся в этом пациенту: а) по меньшей мере, одного противодиабетического средства и b) терапевтически эффективного количества диацереина или его фармацевтически приемлемой соли, моноацетилреина или реина.
9. Способ по п. 8, в котором указанное противодиабетическое средство представляет собой, по меньшей мере, одно средство, выбранное из группы, состоящей из сульфонилмочевины, бигуанида, ингибитора α-глюкозидазы, тиазолидиндиона, агониста рецептора активируемого пролифератором пероксисом, ингибитора дипептидилпептидазы-4, не содержащего сульфонилмочевины стимулятора секреции инсулина, аналога глюкагоноподобного пептида-1, метформина, глибурида, глимепирида, глипирида, глипизида, хлорпропамида, гликлазида, акарбозы, миглитола, пиоглитазона, троглитазона, розиглитазона, изаглитазона, мураглитизара, пелиглитазара, ситаглиптина, саксаглиптина, вилдаглиптина, алоглиптина, линаглиптина, дутоглиптина, репаглинида, натеглинида, митиглинида, эксенатида, лираглутида, албиглутида и инсулина.
10. Способ по п. 8, в котором указанный субъект представляет собой страдающего диабетом II типа пациента с состоянием, выбранным из группы, состоящей из инсулинорезистентности, непереносимости глюкозы, гипергликемии или гиперинсулинемии.
11. Способ по п. 8, в котором указанное терапевтически эффективное количество диацереина составляет от 25 до 200 мг в день.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| МОНО- И ДИСУЛЬФОЗАМЕЩЕННЫЕ АНТРАХИНОНЫ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ КОСТНОГО МАТРИКСА | 1996 |
|
RU2202534C2 |
| MALAGUTI C et al | |||
| Diacerhein downregulate proinflammatory cytokines expression and decrease the autoimmune diabetes frequency in nonobese diabetic (NOD) mice Int | |||
| Immunopharmacol | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| ВЕЩЕСТВА, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ПСОРИАЗА | 2001 |
|
RU2266740C2 |
Авторы
Даты
2015-09-27—Публикация
2011-04-07—Подача