Изобретение относится к области медицинской диагностики, может быть использовано в акушерстве для прогнозирования осложнений во второй половине беременности, а именно риска развития преэклампсии (ПЭ) у женщин с неотягощенной наследственностью по генетическим данным.
Преэклампсия или гестоз - это осложнение беременности, возникающее во второй ее половине и характеризующееся появлением отеков, протеинурии, артериальной гипертензии, а также глубокими расстройствами функции сосудистой системы, гемостаза, иммунитета, гемодинамики и микроциркуляции, развитием плацентарной недостаточности, нарушений функции почек, печени, легких [Сидорова И.С. Эндотелиальная дисфункция в развитии гестоза [Текст] / И.С. Сидорова, И.Л. Галинова // Вопросы гинекологии, акушерства и перинатологии. - 2006. - Т. 5, №1. - С. 75-81].
В настоящее время ПЭ является одной из самых актуальных проблем современного акушерства ввиду широкой распространенности, сложности этиопатогенеза, высокой частоты материнской и перинатальной заболеваемости и смертности [Киселева Н.И. Маркеры дисфункции эндотелия при гестозе [Текст] / Н.И. Киселева, С.Н. Занько, А.П. Солодков // Дисфункция эндотелия: эксперим. и клинич. исслед.: тр. III междунар. науч.-практ. конф., Витебск, 18-20 мая 2004 г./ Белорус. респ. Фонд фундамент. исслед.; Витеб. гос. мед. ун-т. - Витебск, 2004. - С. 201-204]. ПЭ может варьироваться от легкой до тяжелой формы. Как правило, в тяжелых случаях преэклампсии единственным способом улучшить состояние пациентки является ее родоразрешение.
Для ПЭ характерно прогрессирующее течение. Это выражается в неуклонном нарастании тяжести отдельных ее проявлений или присоединении новых клинических признаков. У большинства женщин определяется медленное прогрессирование патологии. Однако в некоторых случаях ПЭ прогрессирует очень быстро до тяжелой формы - за несколько дней или недель. В самых тяжелых случаях прогрессирование может быть молниеносным - в течение нескольких дней или часов [Патогенез гестоза как проявление иммуно-комплексной патологии эндотелия (острый иммунный эндотелиоз) [Текст] / И.С. Сидорова, О.И. Турина, А.П. Милованов [и др.] // Акушерство и гинекология. - 2008. - №6. - С. 13-17]. В итоге развиваются такие критические состояния, как отслойка плаценты, ДВС-синдром, церебральные кровоизлияния, печеночная недостаточность, острая почечная недостаточность, гипотрофия, ЗВРП и гибель плода, эклампсия [Эндотелиальная дисфункция при гестозе. Патогенез, генетическая предрасположенность, диагностика и профилактика [Текст]: метод. рекомендации / Е.В. Мозговая, О.В. Малышева, Т.Э. Иващенко [и др.]; ред. Э.К. Айламазян. - Санкт-Петербург: Изд-во Н-Л, 2003. - 32 с.].
В настоящее время многие исследователи рассматривают ПЭ как острую патологию эндотелия - генерализованное поражение эндотелия сосудов или эндотелиальную дисфункцию, приводящую к нарушению сосудистого тонуса, сосудистой проницаемости, баланса между тромбогенным потенциалом сосудистой стенки и ее тромборезистентностью [Киселева Н.И. Маркеры дисфункции эндотелия при гестозе [Текст] / Н.И. Киселева, С.Н. Занько, А.П. Солодков // Дисфункция эндотелия: эксперим. и клинич. исслед.: тр. III междунар. науч.-практ. конф., Витебск, 18-20 мая 2004 г./ Белорус. респ. Фонд фундамент. исслед.; Витеб. гос. мед. ун-т. - Витебск, 2004. - С. 201-204.; Марков X.М. Молекулярные механизмы дисфункции сосудистого эндотелия [Текст] / X.М. Марков // Кардиология. - 2005. - Т. 45, №12. - С. 62-72; Шифман Е.М. Преэклампсия, эклампсия, HELLP-синдром [Текст] / Е.М. Шифман; Респ. перинат. центр М-ва здравоохранения Респ. Карелия. - Петрозаводск: ИнтелТек, 2002. - 432 с.].
Как свидетельствуют результаты ряда исследований, значимую роль в развитии преэклампсии играют генетические факторы. Среди генов-кандидатов важное значение в развитии ПЭ отводится генам цитокинам, активация которых происходит после запуска цепи иммуновоспалительных реакций. К этой группе генов цитокинов относятся: -308 G/A TNFα (rs1800629), +250 A/G Ltα (rs909253), -403 G/A RANTES (rs2107538), I- TAC (rs 4512021), -801 G/A SDF1 (rs180U57), C/G MCP-1 (rs285765), +1931 A/T MIP1β (rs1719153).
TNFα - гликопротеин с молекулярной массой 17 кДа, является продуктом моноцитов/макрофагов, эндотелиальных, тучных и миелоидных клеток, клеток нейроглии, в особых случаях - активированных Т-лимфоцитов [Suzuki J. et al., 1998; Hollegaard M.V. et al., 2006; Brian E.G., 2009]. Ген TNFα расположен на шестой хромосоме человека (6р21.3) в локусе, кодирующем молекулы главного комплекса гистосовместимости первого (HLA-A, В, С) и второго классов (HLA-DP, DQ, DR) [Байнак О.В. и др., 2005; Seidemann К. et al., 2005]. TNFα синтезируется в основном моноцитарно-макрофагальными и тучными клетками.
CCL5/RANTES (Regulated on Activation Normal T-cell Expressed and Secreted/Регулятор активности нормальной экспрессии и секреции Т-клеток).
Низкомолекулярный протеин (молекулярная масса у человека колеблется между 7, 8 и 8, 7 кДа), находится на хромосоме 17q12. Принадлежит к b-семейству СС-хемокинов. Регулирует активность и секрецию Т-лимфоцитов.
Хемоаттрактант селективен по отношению к субпопуляциям CD4+/CD45RO+-T-лимфоцитов, а также моноцитам и эозинофильным гранулоцитам. Хемокин RANTES влияет на биологическую активность лейкоцитов [Kaburagi Y et al.,2001].
I-TAC (CXCL11) (Интерферон-индуцируемых Т-клеток альфа хемоатрактант) является членом семейства хемокинов малых секреторных белков, участвующих в иммунных и воспалительных реакциях. Ген I-TAC находится на хромосоме 4q11.12. Этот хемокин играет ключевую роль в воспалительных процессах путем активации различных субпопуляций лейкоцитов [Mackay 2001], индуцирует провоспалительные цитокины в нейтрофилах, моноцитах, макрофагах, Т-клетках, астроцитах, фибробластах и эндотелиальных клетках [Fernandez E.J. et al. 2002].
SDF-1 (Производный фактор стромальных клеток-1) содержит 4 экзона и находится на хромосоме 10q12. Встречается в двух формах: SDF-1α/CXCL12α и SDF-1β/CXCL12β [Bajetto A. et al., 2001]. SDF-1 во время эмбриогенеза определяет миграцию гемопоэтических клеток и формирование кровеносных сосудов. Играет важную роль в ангиогенезе путем привлечения эндотелиальных клеток-предшественников из костного мозга через CXCR4-зависимый механизм [Shih СС et al., 2000].
Ген МСР-1 находится на 17 хромосоме в области 17q11.2-q12. МСР-1 проявляет наиболее сильную хемотаксическую активность по отношению к моноцитам и Т-лимфоцитам. Является промотором миграции циркулирующих лимфоцитов из периферической крови в ткани и очаги воспаления, одновременно влияя на их активацию и прилипание к сосудистой стенке. МСР-1 стимулирует моноциты к продукции провоспалительных цитокинов и образованию аниона перекиси водорода [Chazov E.I. et al., 2007; Ukkonen М. et al., 2007]. Этот хемокин способствует окислению липопротеинов низкой плотности в моноцитах, эндотелиальных и васкулярных клетках гладких мышц человека [Carr M.W. et al., 1994; Rollins B.J., 1996; Takahara N. et al., 1997].
MIP-1 - хемоатрактант для естественных клеток-киллеров, моноцитов и других иммунных клеток. Принадлежащий к β-семейству СС-хемокинов низкомолекулярный протеин. Ген MIP-1 локализуется на 17q12 хромосоме. Существуют три биологически подобные изоформы MIP-1: α, β, δ. Макрофаги Th1 и Th2 CD4+-клетки стимулируют продукцию MIP1α, который участвует в острых воспалительных состояниях, активизирует полиморфноядерные лейкоциты и может препятствовать ВИЧ-инфицированию [Kaburagi Y et al, 2001]. Наряду со свойствами хемоаттрактанта MIP-1β (преимущественно для CD8+-клеток) усиливает прилипание циркулирующих лимфоцитов к эндотелию. Является ингибитором стволовых кроветворных клеток [Campbell J.J. et al., 1998; Bradley L.M. et al., 1999; Ghosh Т.К. et al., 2006; Stasikowska O. et al., 2007].
Ltα - представляет собой белок, который в организме человека является цитокином, продуцируемым Т-лимфоцитами и лейкоцитами, и секретируется фибробластами, астроцитами, миеломными клетками, эпителио- и эндотелиоцитами. Имеет массу около 33 кД [Кетлинский С.Л., Калинина Н.М, 1995; Титов В. Н., 2003]. Ген Ltα находится на шестой хромосоме (6р21.3), содержит 4 экзона. Ltα обладает рядом подобных TNFα биологических активностей, включая способность вызывать геморрагический некроз опухолей [Hollegaard M.V. et al., 2006; Brian E.С. 2009]. Тем не менее, оба этих гена регулируются независимо друг от друга. Ltα связывается с теми же рецепторами, что и TNFα, однако способность активировать рецепторы у Ltα менее выражена, зачастую он проявляет лишь частичную агонистическую активность. Ltα является хемоаттрактантом для нейтрофилов, стимулирует в них образование пероксид-ионов, усиливает фагоцитоз и адгезию к эндотелию, стимулирует активность фибробластов, играет роль в процессе заживления ран, а также провоцирует выработку стресс-гормонов, влияет на метаболизм глюкозы [Suzuki J., 1998; Mentula P., 2005; Кетлинский С.С. и др. 2008].
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития преэклампсии у женщин с неотягощенной наследственностью на основе данных о полиморфизме генов цитокинов -308 G/A TNFα (rs1800629), +250 A/G Ltα (rs909253), -403 G/A RANTES (rs2107538), I-TAC (rs4512021), -801 G/A SDF1 (rs1801157), C/G MCP-1 (rs285765), +1931 А/Т MIP1β (rs1719153).
Известен способ по заявке РФ №2012131290 (дата публикации заявки 27.01.2014), согласно которому, для раннего выявления риска развития преэклампсии у беременной женщины на ранней стадии беременности на сроке от 14 до 16 недель беременности до развития обычных клинических симптомов, проводят анализ исследуемого биологического образца для определения концентрации 5-гидрокситриптофана, причем пониженная концентрация 5-гидрокситриптофана относительно контрольной концентрации при нормальной беременности коррелирует с риском развития преэклампсии у беременной женщины. Где контрольная концентрация представляет собой концентрацию 5-гидрокситриптофана в биологическом образце, полученном у субъекта, у которого действительно развилась преэклампсия, и в котором повышенная концентрация 5-гидрокситриптофана относительно контрольной концентрации коррелирует с риском развития преэклампсии у беременной женщины. Одновременно проводят анализ для определения концентрации по существу всех биомаркеров: 5-гидрокситриптофана, моносахарида, деканоилкарнитина, метилглутаровой кислоты и/или адипиновой кислоты, олеиновой кислоты, докозагексаеновой кислоты и/или докозатрииновой кислоты, Y-бутиролактона и/или оксолан-3-она, 2-оксовалериановой кислоты и/или оксометилбутановой кислоты, ацетоуксусной кислоты, гексадеценоилэйкозатетраеноил-sn-глицерина, сфингозин-1-фосфата, сфинганин-1-фосфата и производных витамина D3, и установления кореляции концентрации и комбинации всех биомаркеров с риском развития преэклампсии у беременной женщины.
В заявке на получение патента РФ №2012123860 (дата публикации заявки 20.12.2013) предложен способ оценки риска возникновения патологии беременности, заключающийся в том, что для оценки риска возникновения преэклампсии, преждевременных родов, а также преэклампсии на фоне артериальной гипертензии проводят анализ биологических жидкостей человека, а именно сыворотки крови, с помощью обращенно-фазовой жидкостной хроматографии с регистрацией результата анализа в ультрафиолетовой области спектра, а в качестве биомаркеров патологии беременности используются гипоксантин, ксантин, мочевая кислота.
В заявке на получение патента РФ №2011125546 (дата публикации заявки 27.12.2012) прогноз повышенного риска развития преэклампсии осуществляют на основании того, что концентрация Н2-релаксина, полученного из организма беременной женщины до проявления симптома преэклампсии, меньше предельного значения нижнего квартиля концентрации, равной примерно 500 пг/мл, характерной для беременной женщины. При этом концентрацию Н2-релаксина измеряют с использованием антитела к Н2-релаксину с помощью твердофазного иммуноферментного анализа (ELISA). Кроме того, дополнительно измеряют концентрацию С-реактивного белка (CRP) в биологическом образце и определяют, что беременная женщина имеет повышенный риск развития преэклампсии, если концентрация CRP больше чем примерно 13,5 мкг/мл или меньше чем 1,5 мкг/мл, даже если концентрация Н2-релаксина больше чем примерно 500 пг/мл.
В патенте РФ №2481578, по заявке №2012107573/15, 28.02.2012, опубликованном 10.05.2013, раскрыт способ прогнозирования развития тяжелой преэклампсии с помощью анализа крови, отличающийся тем, что у беременной во втором триместре рассчитывают лейкоцитарный индекс интоксикации и при его значении выше 1,6 прогнозируют развитие тяжелой преэклампсии.
За прототип выбран «Способ прогнозирования гестоза» по патенту РФ №2191384 по заявке №2000115821, 16.06.2000. Заявляемый способ позволяет прогнозировать развитие гестоза за 2-4 недели до его клинических проявлений (артериальная гипертензия, протеинурия, отеки). Способ заключается в том, что у женщин с 16-й недели беременности определяют устойчивость эритроцитов к перекисному гемолизу, инициированному двухвалентным железом и гемолизатом аутокрови. При этом за 2-4 недели до появления клинических признаков гестоза (артериальная гипертензия, протеинурия, отеки) время устойчивости эритроцитов составляет менее 150 с; при показателе больше 150 с гестоз у беременных не развивается. Изобретение позволяет просто и надежно осуществить прогнозирование гестоза.
Общий недостаток указанных способов заключается в том, что не рассматриваются генетические полиморфизмы и их сочетания с риском развития преэклампсии у женщин с неотягощенной наследственностью.
Задачей настоящего исследования является расширение арсенала способов диагностики, а именно создание способа прогнозирования риска развития ПЭ у женщин с неотягощенной наследственностью по данным о генетических полиморфизмах - 308 G/A TNFα (rs1800629), +250 A/G Ltα (rs909253), - 403 G/A RANTES (rs2107538), I- TAC (rs4512021), - 801 G/A SDF1 (rs1801157), C/G MCP-1 (rs285765), +1931 A/T MIP1β (rs1719153).
Технический результат использования изобретения - получение критериев оценки риска развития преэклампсии у женщин с неотягощенной наследственностью.
В соответствии с поставленной задачей был разработан способ прогнозирования преэклампсии у женщин русской национальности, уроженок Центрального Черноземья с неотягощенной наследственностью, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфизмов генов цитокинов - 308 G/A TNFα (rs1800629), +250 A/G Ltα (rs909253), - 403 G/A RANTES (rs2107538), I- TAC (rs4512021), -801 G/A SDF1 (rs1801157), C/G MCP-1 (rs285765), +1931 A/T MIP1β (rs1719153);
- прогнозирование минимального риска развития преэклампсии у женщин с неотягощенной наследственностью по шести сочетаниям генетических вариантов семи генетических полиморфизмов: +1931 A MIP1β, +250 A Ltα, -403 G/A RANTES; -801 G SDF1, G MCP-1, +250 A Ltα; -801 G SDF1, +250 A Ltα, G I-TAC; +250 A Ltα, G I-TAC, -308 GG TNFα; +1931 A MIP1β, -403 A RANTES; -801 G SDF1, G MCP-1.
Новизна и изобретательский уровень заключается в том, что из уровня техники не известна возможность прогноза развития преэклампсии у женщин с неотягощенной наследственностью по наличию различных сочетаний генетических вариантов полиморфных локусов -308 G/A TNFα (rs1800629), +250 A/G Ltα (rs909253), - 403 G/A RANTES (rs2107538), I- TAC (rs4512021), -801 G/A SDF1 (rs1801157), C/G MCP-1 (rs285765), +1931A/T MIP1β (rs1719153).
Способ осуществляют следующим образом.
ДНК выделяют из образцов периферической венозной крови пациентки в 2 этапа. На первом этапе к 4 мл крови добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4°C, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (pH=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10 мг/мл) и инкубируют образец при 37°C в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. Сформированную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°C.
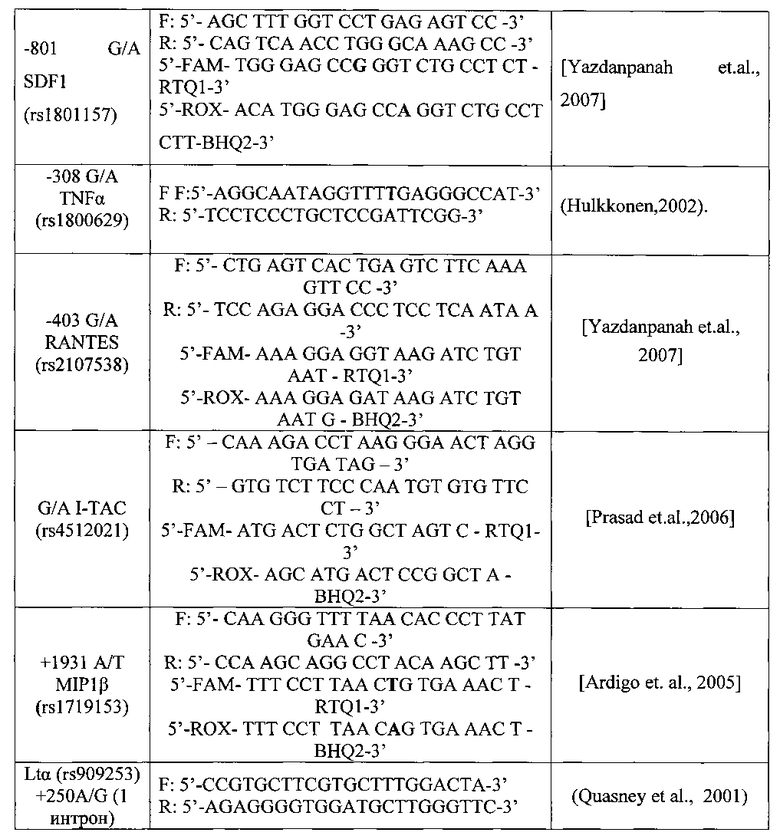
Выделенную ДНК затем подвергают полимеразной цепной реакции с использованием стандартных олигонуклеотидных праймеров (таблица 1).

Изобретение характеризуется следующими графическими материалами.
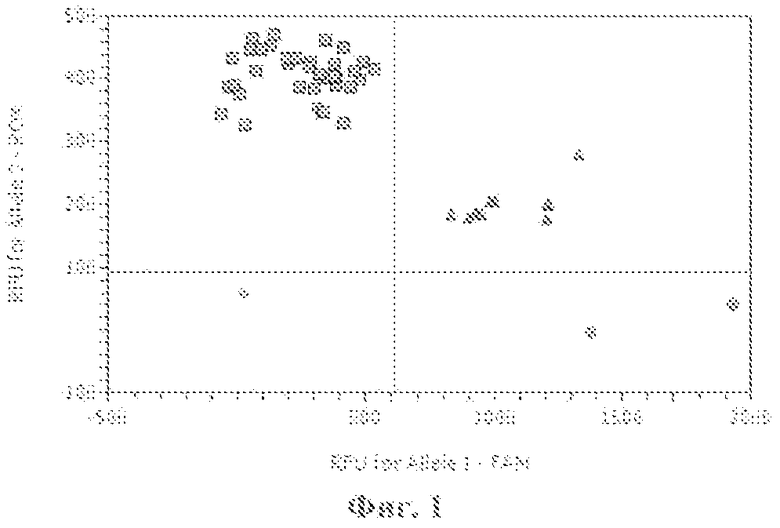
Фиг.1. Дискриминации аллелей методом детекции TaqMan зондов по данным величин УОФ (уровень относительной флуоресценции) каждого зонда на амплификаторе IQ5 с детектирующей системой в режиме реального времени полиморфизма C/G МСР1 (rs 2857657) (где ● - гомозиготы GG, ■ - гомозиготы СС, ▲ - гетерозиготы GC, ♦ - отрицательный контроль).
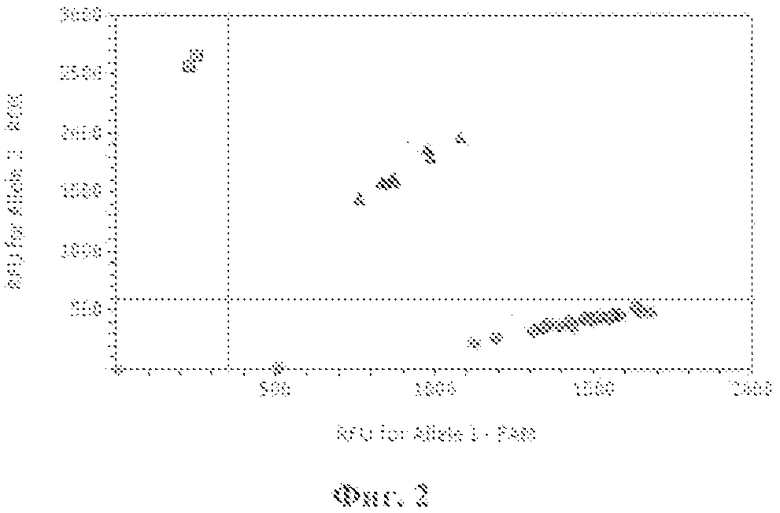
Фиг. 2. Дискриминации аллелей методом детекции TaqMan зондов по данным величин УОФ (уровень относительной флуоресценции) каждого зонда на амплификаторе IQ5 с детектирующей системой в режиме реального времени полиморфизма -801 G/A SDF1 (rs1801157) (где ● - гомозиготы -801GG, ■ - гомозиготы - 801АА, ▲ - гетерозиготы -801GA, ♦ - отрицательный контроль).
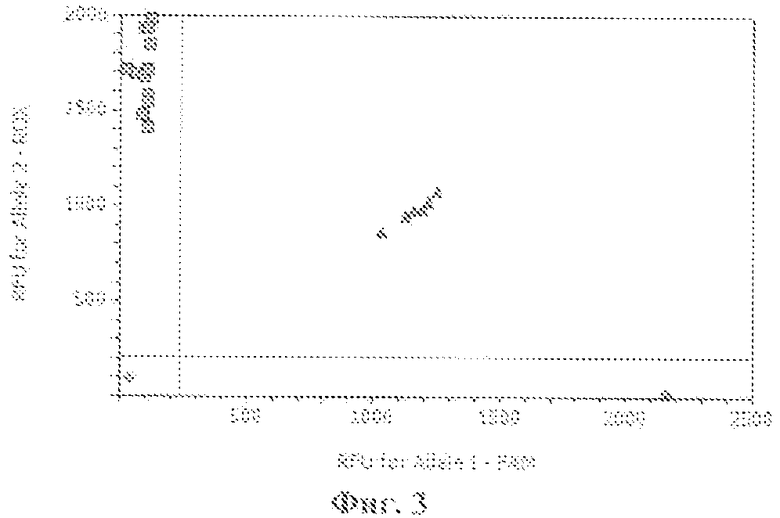
Фиг. 3. Электрофоретическое разделение продуктов амплификации - 308 G/A TNFα (где ● - гомозиготы - 308АА, ■ - гомозиготы - 308GG, ▲ - гетерозиготы - 308GA, ♦ -отрицательный контроль).
Фиг. 4. Дискриминация аллелей по локусу +250 A/G Ltα (где ● - гомозиготы +250GG, ■ - гомозиготы +250АА, ▲ - гетерозиготы+250AG, ♦ - отрицательный контроль).
Фиг. 5. Дискриминация аллелей по локусу +1931 А/Т MIP-1β (rs1719153) (где ● -гомозиготы +1931АА, ■ - гомозиготы +1931ТТ, ▲ - гетерозиготы +1931AT, ♦ - отрицательный контроль).
Фиг. 6. Дискриминация аллелей по локусу G/A I-TAC (rs4512021) (где ● - гомозиготы GG, ■ - гомозиготы АА, ▲ - гетерозиготы AG, ♦ - отрицательный контроль).
Фиг. 7. Дискриминация аллелей по локусу - 403 G/A RANTES (rs2107538) (где ● - гомозиготы - 403GG, ■ - гомозиготы - 403АА, ▲ - гетерозиготы - 403GA, ♦ - отрицательный контроль).
Анализ генетического полиморфизма C/G МСР 1 (rs285765) проводили методом полимеразной цепной реакции синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (3 мин при t+95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин при t+51,5°C; денатурация -15 сек при t+95°C.
При проведении ПЦР в амплификаторе с флюоресцентной детекцией (на амплификаторе IQ5) генотипирование осуществлялось методом Tag Man зондов по данным величин RFU (уровень относительной флуоресценции) каждого зонда, представленным. Зонд с флуоресцентным красителем ROX соответствует аллелю С, зонд с красителем FAM - аллелю G (фиг. 1).
Анализ полиморфизма гена -801 G/A SDF1 (rs1801157) проводили методом ПЦР синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов (табл. 5) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (4 мин при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин при t +66°C; денатурация - 15 сек при t +95°C (фиг. 2).
Анализ полиморфизма гена TNFα проводили методом полимеразной цепной реакции синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием соответствующих олигонуклеотидных праймеров и зондов [Hulkkonen J., 2002] (табл. 5) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (5 мин. при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин при 52°C; денатурация - 15 сек при 95°C (фиг. 3).
Анализ полиморфизма гена Ltα в 1 интроне проводили методом полимеразной цепной реакции синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием соответствующих олигонуклеотидных праймеров и зондов [Sugiura S., 2002] (табл. 2) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (5 мин при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин. при 50°C; денатурация - 15 сек при 95°C (фиг. 4).
Анализ полиморфизма гена -801 G/A SDF1 (rs1801157) проводили методом ПЦР синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов (табл. 2) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (4 мин при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин при t +66°C; денатурация - 15 сек при t +95°C (фиг. 5).
Анализ генетического полиморфизма G/A I-TAC (rs4512021) проводили методом полимеразной цепной реакции синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов (табл. 2) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (4 мин при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин. при t +49°C; денатурация - 15 сек при t +95°C (фиг. 6).
Анализ генетического полиморфизма -403 G/A RANTES (rs2107538) проводили методом полимеразной цепной реакции синтеза ДНК на амплификаторе IQ5 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов (табл. 2) с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5 мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (4 мин. при 95°C) выполняли 40 циклов амплификации по схеме: отжиг праймеров - 1 мин при t +55°C; денатурация - 15 сек при t +95°C (фиг. 7).
Возможность использования предложенного способа для оценки риска возникновения и развития ПЭ подтверждает анализ результатов наблюдений 247 пациенток с ПЭ и 245 женщин контрольной группы. Средний возраст женщин с ПЭ составил 31,2±7,5 лет (варьировал от 18 до 42 лет), а в контрольной группе 31,7±7,3 лет (варьировал от 18 до 43 лет) (p>0,05). В исследуемые выборки включались индивидуумы русской национальности, являющиеся уроженцами Центрального Черноземья России и не имеющие родства между собой. Таким образом, контрольная группа не отличалась от группы беременных с ПЭ по полу, возрасту (p>0,05), месту рождения и национальности.
Все клинические и клинико-лабораторные исследования проводились на базе Перинатального центра Белгородской областной клинической больницы, с информированного согласия пациенток на использовании материалов лечебно-диагностических мероприятий, проводимых за период госпитализации и после, связанной с ПЭ, для научно-исследовательских целей и протоколировались по стандартам этического комитета Российской Федерации. Анализ ассоциаций сочетаний генетических вариантов с ПЭ проведен с помощью программного обеспечения АР Sampler (http://sources.redhat.com/cygwin/), использующего метод Монте-Карло марковскими цепями и байесовскую непараметрическую статистику [A Gibbs sampler for identification of symmetrically structured, spaced DNA motifs with improved estimation of the signal length [Text] / A.V. Favorov, M.S. Gelfand, A.V. Gerasimova [et al.] // Bioinformatics. - 2005. -Vol. 21, №10. - P. 2240-2245].
Выявлено, что комбинации генетических вариантов цитокинов, являющиеся «своеобразными» для беременных с ПЭ без наследственной отягощенности и включающие по три молекулярно-генетических маркера, сформированы следующими полиморфными вариантами: +1931 A MIP1β, +250 A Ltα, -403 A RANTES; -801 G SDF1, G МСР-1, +250 А Ltα; -801 G SDF1, +250 A Ltα, G I-TAC; +250 A Ltα, G I-TAC, -308 GG TNFα. Эти сочетания генетических вариантов встречаются у 14,46%, 17,78%, 51,11% и 41,57% беременных с ПЭ без отягощенного семейного анамнеза соответственно, тогда как в контрольной группе их распространенность равна 27,35% (OR=0,45 95% CI 0,22-0,88, р=0,01); 30,61% (OR=0,49 95% CI 0,27-0,90, р=0,01); 64,08% (OR=0,59 95% CI 0,36-0,96, p=0,02); 54,69% (OR=0,59 95% CI 0,36-0,96, p=0,02) соответственно.
Следующие два сочетания полиморфных маркеров цитокинов представлены двумя генетическими вариантами каждое. Эти комбинации зарегистрированы у 15,66% (+1931 А MIP1β, -403А RANTES), 20,00% (-801 G SDF1, G MCP-1) беременных с ПЭ без наследственной отягощенности, что более чем в 1,57 раза меньше аналогичных показателей контрольной группы, где они составляют 28,57% (OR=0,46 95% CI 0,24-0,89, р=0,01), 31,43%(OR=0,54 95% CI 0,30-0,98, р=0,02) соответственно.
Итак, резюмируя полученные данные, можно сделать вывод, что семь генетических полиморфизмов цитокинов формирует шесть комбинаций генетических вариантов, определяющих подверженность к развитию ПЭ у женщин с неотягощенной наследственностью +1931 A MIP1β, +250 A Ltα, -403 A RANTES (OR=0,45); -801 G SDF1, G MCP-1, +250 A Ltα (OR=0,49); -801 G SDF1, +250 A Ltα, G I-TAC (OR=0,59); +250 A Ltα, G I-TAC, -308 GG TNFα (OR=0,59); +1931 A MIP1β, -403 A RANTES (OR=0,46); -801 G SDF1, G MCP-1 (OR=0,54). Данные комбинации снижают риск развития ПЭ у женщин с неотягощенной наследственностью.
Примеры конкретного выполнения.
1. У беременной А., русской национальности, уроженки Центрального Черноземья, была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено сочетание трех генетических вариантов +1931 А MIP1β, +250 A Ltα, -403 A RANTES, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. В течении беременности у нее не было выявлено признаков ПЭ.
2. У женщины Л., при прегравидарной подготовке, была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено сочетание -801 G SDF1, G МСР-1, +250 A Ltα, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. При возникновении беременности у нее не было выявлено признаков ПЭ.
3. У беременной М., русской национальности, уроженки Центрального Черноземья, была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено сочетание трех генетических вариантов -801 G SDF1, +250 A Ltα, G I-TAC, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. У нее не были выявлены признаки ПЭ.
4. У женщины Г., русской национальности, уроженки Центрального Черноземья, была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено сочетание трех генетических вариантов +250 A Ltα, G I-TAC, -308 GG TNFα, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. При возникновении беременности у нее не было выявлено признаков ПЭ.
5. У женщины В., при прегравидарной подготовке, была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено сочетание двух генетических вариантов +1931 A MIP1β, -403 A RANTES, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. При возникновении беременности у нее не было выявлено признаков ПЭ.
6. У беременной П., русской национальности, уроженки Центрального Черноземья, была взята венозная кровь, при генотипировании ДНК- маркеров было выявлено сочетание двух генетических вариантов -801 G SDF1, G МСР-1, что позволило отнести ее в группу беременных с пониженным риском развития ПЭ. Это подтвердило дальнейшее наблюдение. У нее не были выявлены признаки ПЭ.
Применение данного способа позволит формировать среди женщин при прегравидарной подготовке и на ранних сроках беременности группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития ПЭ у женщин с неотягощенной наследственностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития преэклампсии у женщин в зависимости от наследственной отягощенности | 2016 |
|
RU2646455C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ ТЯЖЕЛОГО ТЕЧЕНИЯ | 2014 |
|
RU2568892C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЭНДОМЕТРИОЗА | 2014 |
|
RU2558854C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ НА ОСНОВЕ КОМБИНАЦИЙ ГЕНОВ ЦИТОКИНОВ | 2014 |
|
RU2568891C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ СОЧЕТАННЫХ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ РЕПРОДУКТИВНОЙ СИСТЕМЫ У ЖЕНЩИН | 2014 |
|
RU2557954C1 |
| Способ прогнозирования риска развития преэклампсии тяжелого течения с учетом генетических данных | 2017 |
|
RU2653765C1 |
| Способ прогнозирования риска развития генитального эндометриоза | 2017 |
|
RU2650994C1 |
| Способ прогнозирования риска развития преэклампсии на основе комбинаций генов матриксных металлопротеиназ | 2017 |
|
RU2646448C1 |
| Способ прогнозирования риска развития преэклампсии тяжелого течения | 2016 |
|
RU2638785C1 |
| Способ прогнозирования риска развития сочетания миомы матки и аденомиоза с использованием генетических данных | 2018 |
|
RU2677866C1 |
Изобретение относится к области медицины, а именно к акушерству и гинекологии, и предназначено для выявления риска развития преэклампсии у женщин с неотягощенной наследственностью. Для прогнозирования риска развития преэклампсии у женщин русской национальности, уроженок Центрального Черноземья, с неотягощенной наследственностью, выделяют ДНК из периферической крови и проводят анализ полиморфизмов генов цитокинов. Прогнозируют минимальный риск развития преэклампсии у женщин с неотягощенной наследственностью по шести сочетаниям генетических вариантов семи генетических полиморфизмов: +1931 A MIP1β, +250 A Ltα, -403 G/A RANTES; -801 G SDF1, G MCP-1, +250 A Ltα; -801 G SDF1, +250 A Ltα, G I-TAC; +250 A Ltα, G I-TAC, -308 GG TNFα; +1931 A MIP1β, -403 A RANTES; -801 G SDF1, G MCP-1. 7 ил., 1 табл., 6 пр.
Способ прогнозирования риска развития преэклампсии у женщин русской национальности, уроженок Центрального Черноземья, с неотягощенной наследственностью, включающий выделение ДНК из периферической крови, анализ полиморфизмов генов цитокинов и прогнозирование минимального риска развития преэклампсии у женщин с неотягощенной наследственностью по шести сочетаниям генетических вариантов семи генетических полиморфизмов: +1931 A MIP1β, +250 A Ltα, -403 G/A RANTES; -801 G SDF1, G MCP-1, +250 A Ltα; -801 G SDF1, +250 A Ltα, G I-TAC; +250 A Ltα, G I-TAC, -308 GG TNFα; +1931 A MIP1β, -403 A RANTES; -801 G SDF1, G MCP-1.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ГЕСТОЗА | 2000 |
|
RU2191384C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ТЯЖЕЛОЙ ПРЕЭКЛАМПСИИ | 2012 |
|
RU2481578C1 |
| WO 2010060102 А2, 27.05.2010 | |||
| Горелка для кухни типа "Примус" | 1939 |
|
SU59264A1 |
| WO 2011116958 A1, 29.09.2011 | |||
| PATERNOSTER DM et al | |||
| Predictive markers of pre-eclampsia in hypertensive disorders of pregnancy | |||
| Int J Gynaecol Obstet., 1999, 66(3), p.237-243. | |||
Авторы
Даты
2015-11-20—Публикация
2014-09-04—Подача