Настоящее изобретение относится к ультразвуковым диагностическим системам визуализации и, в частности, к ультразвуковым системам с автоматической установкой параметров доплеровского потока.
Ультразвуковые системы визуализации работают в B-режиме для визуализации ткани и в доплеровских режимах для анализа и визуализации кровотока. Типичные доплеровские режимы включают в себя энергетический доплеровский режим, применяемый для визуализации как движения тканей, так и кровотока, цветовую доплерографию кровотока для качественной визуализации кровотока и спектральную доплерографию для количественного определения кровотока. Доплерография может осуществляться в одном измерении (M-режим и спектральная доплерография), как двухмерная визуализация и как трехмерная визуализация.
Современные диагностические ультразвуковые системы предлагают ряд настроек сбора данных для управления пользователем, чтобы достигать оптимального качества изображений для облегчения диагностики пациентов. Во время сосудистых исследований пользователи часто используют режим цветовой доплеровской визуализации кровотока, чтобы оценивать и диагностировать кровеносные сосуды. Пользователи часто управляют расположением цветовой рамки, центрируя ее на исследуемом сосуде, и управляют доплеровским контрольным объемом, размещая его на исследуемых участках сосудов, для получения спектрального доплеровского сигнала от конкретного местоположения в организме. Пользователи также изменяют настройку коррекции доплеровского угла, чтобы совместить курсор направления потока с ориентацией сосуда. Делались предложения по автоматизации размещения курсора угла потока над потоком крови в сосуде, как показано в патенте США 6464637 (Criton и др.), WO 96/17549 (Goujon), патенте США 6068598 (Pan и др.) и патенте США 6176830 (Freiburger). Freiburger также рассматривает автоматическое размещение доплеровского контрольного объема на основании определенного местоположения максимальной скорости на изображении, установление частоты повторения импульсов (PRF) на основании максимального определенного сдвига частоты и автоматическое установление усиления на основании амплитуды данных цветовой визуализации кровотока. Патент США 6126605 (Washburn и др.) автоматически регулирует пороги и сжатие данных для доплеровского изображения с применением гистограмм и выборок данных цветовой визуализации кровотока, и патент США 6322509 (Pan и др.) регулирует расположение и размер доплеровского контрольного объема на основании данных изображения кровеносного сосуда. WO 03/19227 (Christopher и др.) описывает автоматическую установку параметров спектрального доплеровского и цветового доплеровского отображений кровотока на основании как спектральной доплеровской, так и цветовой доплеровской информации о кровотоке.
Для получения согласованных измерений скорости для множества исследований одного пациента или сравнения измерений различных пациентов пользователи пытаются поддерживать фиксированный доплеровский угол, т.е. угол относительно направления потока, под которым передаются доплеровские лучи, и существует два подхода к достижению данной цели. Один подход заключается в фиксировании курсора коррекции угла над изображением и манипулировании преобразователем движениями «с пятки на носок» для выравнивания сосуда с линией угла. Другой подход заключается в том, чтобы положиться на ультразвуковые системы, предлагающие приспособление, которое регулирует угол наклона луча каждый раз, когда коррекция угла изменяется пользователем, для получения фиксированного доплеровского угла. Однако коррекция угла все же осуществляется вручную. Требуется ультразвуковая система, которая будет автоматически регулировать угол наклона луча и цветовую рамку, в которой осуществляется сбор доплеровских данных, на основании характеристик кровеносных сосудов на изображении.
В соответствии с принципами настоящего изобретения, описана диагностическая ультразвуковая система, которая автоматизирует размещение цветовой рамки, размещение доплеровского контрольного объема, коррекцию угла и угол наклона луча с применением сегментации сосуда и анализа изображения потока. В предпочтительном варианте осуществления автоматизация осуществляется каждый раз, когда пользователь указывает точку в кровеносном сосуде для анализа потока, без необходимости регулирования каких-либо пользовательских настроек. Оптимальные параметры передачи ультразвука и просмотра определяются и устанавливаются автоматически каждый раз, когда пользователь указывает новое местоположение для диагностики, что избавляет от требующих времени и утомительных регулировок, в ином случае необходимых при каждом выборе нового исследуемого участка. Уменьшаются связанные с эргономикой повреждения из-за повторяющегося изменения настроек, особенно при сканировании длинных сосудов, таких как сонная артерия и сосуды нижних конечностей.
На чертежах
Фиг.1 иллюстрирует в форме блок-схемы диагностическую ультразвуковую систему, устроенную в соответствии с принципами настоящего изобретения.
Фиг.2 представляет собой блок-схему, иллюстрирующую работу процессора расположения и угла наклона цветовой рамки с Фиг.1.
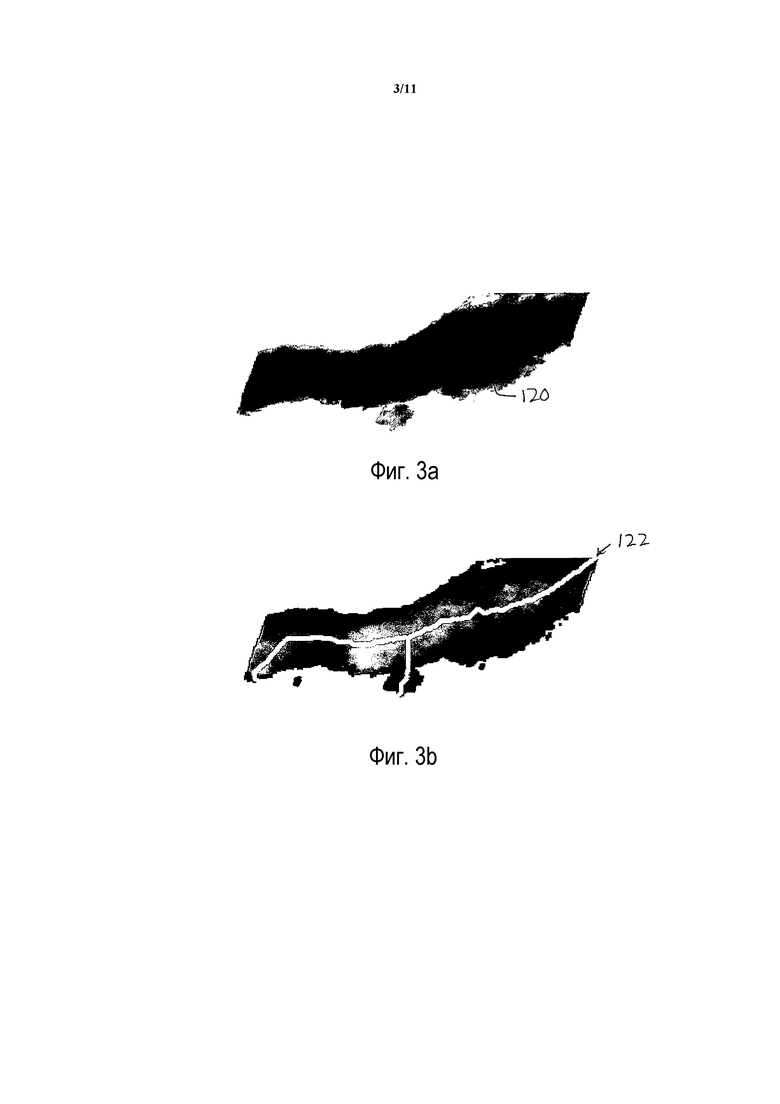
Фиг.3a и 3b иллюстрируют сегментацию и анализ изображения потока крови кровеносного сосуда.
Фиг.3c и 3d иллюстрируют автоматическое изменение позиционирования цветовой рамки в соответствии с принципами настоящего изобретения.
Фиг.4-7 представляют собой последовательность изображений на устройстве отображения ультразвуковой системы, иллюстрирующих воплощение настоящего изобретения.
Фиг.8 представляет собой изображение на устройстве отображения ультразвуковой системы, иллюстрирующее настройки автоматического слежения за потоком в соответствии с принципами настоящего изобретения.
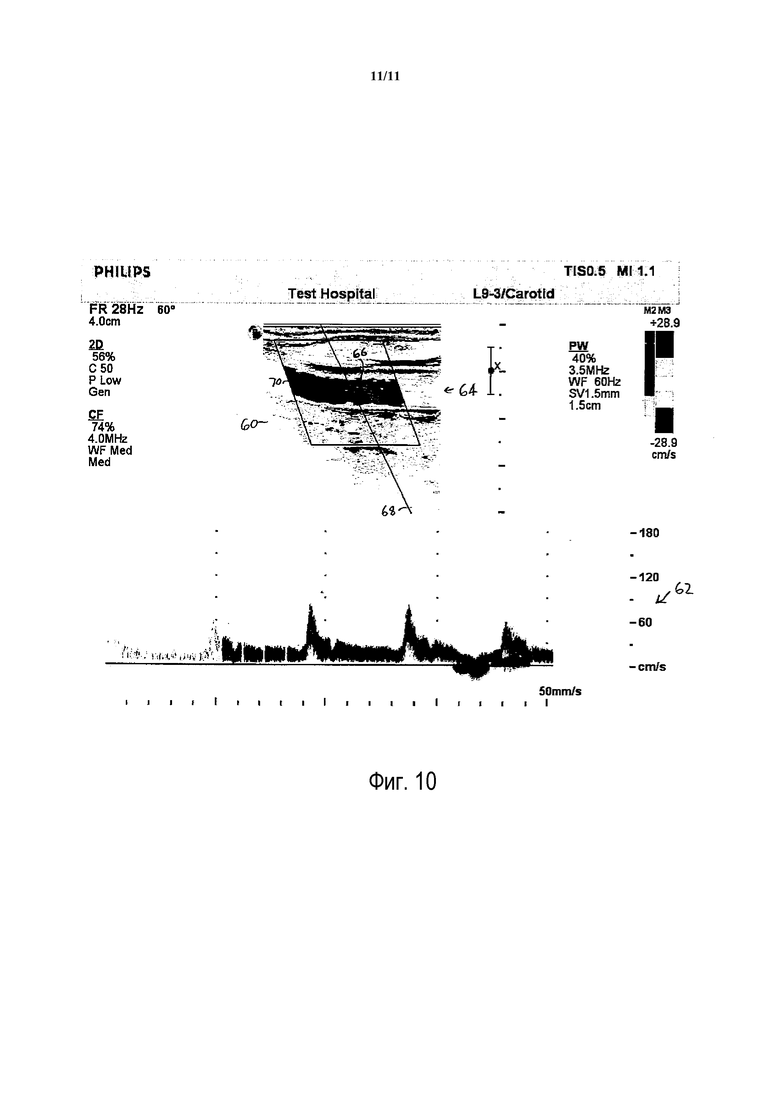
Фиг.9 и 10 представляют собой изображения на устройстве отображения ультразвуковой системы, демонстрирующие автоматическое слежение за контрольным объемом, размещением цветовой рамки и коррекцией угла во время ультразвукового исследования без участия пользователя.
Если начать рассмотрение с Фиг.1, ультразвуковая система, устроенная в соответствии с принципами настоящего изобретения, показана в форме блок-схемы. Ультразвуковой зонд 10 содержит массив 12 преобразователей из преобразовательных элементов, которые передают ультразвуковые волны в тело и принимают возвращающиеся эхо-сигналы. Передаваемые волны направляют в виде лучей или линий сканирования для сбора данных об исследуемой области в теле. Можно применять одномерный массив для передачи лучей по одной плоскости для двухмерной визуализации, или можно применять двухмерный массив преобразовательных элементов для передачи лучей по объемной области организма для трехмерной визуализации. С помощью зонда можно поворачивать и фокусировать лучи в различных направлениях для сбора данных о ткани в конкретных местоположениях или потоке крови в конкретных направлениях, как подробнее изложено ниже. Управление и обработка лучей при передаче и приеме обеспечивается контроллером 16 формирователя луча, который управляет формирователем 14 луча, соединенным с элементами массива 12 преобразователей, для надлежащей передачи сформированных лучей и формирования лучей из принимаемых сигналов посредством задержки и суммирования в когерентные эхо-сигналы. Формирователь луча может управлять массивом преобразователей так, чтобы сканировать лучами требуемую плоскость изображения, например, и так, чтобы периодически сканировать лучами участок плоскости изображения, в котором следует определить поток крови, с PRF, соответствующей скоростям потока крови, присутствующего в этой области тела.
Квадратурный полосовой фильтр 18 переводит эхо-сигнал в квадратурные компоненты I и Q. Отдельные компоненты используются устройством оценки доплеровского угла для оценки сдвига фазы или частоты доплеровского сигнала в точках, в которых осуществляется сбор доплеровских данных. Детектор B-режима использует компоненты I и Q для осуществления детектирования в B-режиме для изображений тканей посредством извлечения квадратного корня из суммы квадратов компонентов I и Q. Детектируемые интенсивности эхо-сигналов обрабатываются в пространственном базисе для формирования двух- или трехмерного изображения ткани в организме, которое обрабатывается для отображения процессором 36 отображения и отображается на экране 52 устройства отображения.
Доплеровские частоты в местоположениях на плоскости изображения, которые получают с помощью устройства 20 оценки доплеровского угла, могут быть преобразованы прямо в значения скорости потока в этих местоположениях. Эти доплеровские данные передаются на процессор 30 цветовой визуализации кровотока, который пространственно переводит данные в формат двух- или трехмерного изображения, на котором значения скорости закодированы цветом. Данная доплеровская цветовая карта накладывается на пространственно соответствующее изображение в B-режиме процессором 36 отображения, чтобы проиллюстрировать местоположения в анатомической области, где имеется поток, и скорость и направление данного потока посредством цветового кодирования. Доплеровские данные от конкретной точки на изображении, выбранной посредством размещения контрольного объема над данным местоположением на изображении, передаются на спектральный доплеровский процессор 32, который создает спектральное отображение изменения и распределения скоростей потока в данной точке с течением времени. Спектральное доплеровское отображение передается на процессор 36 отображения для обработки и отображения спектрального доплеровского отображения на экране 52 устройства отображения.
В соответствии с принципами настоящего изобретения данные цветовой визуализации кровотока от процессора 30 цветовой визуализации кровотока и, предпочтительно, данные B-режима от процессора 24 B-режима передаются на процессор 40 расположения и угла наклона цветовой рамки. Процессор расположения и угла наклона цветовой рамки управляет автоматизацией параметров и особенностей цветового изображения кровотока, включая надлежащее позиционирование цветовой рамки, установку доплеровского угла доплеровских лучей, локализацию контрольного объема на изображении и надлежащее позиционирование курсора угла потока. Для управления доплеровским углом процессор расположения и угла наклона цветовой рамки связан с контроллером 16 формирователя луча для управления направлениями доплеровских лучей. Установка и управление автоматизацией, обеспечиваемой процессором расположения и угла наклона цветовой рамки, обеспечивается посредством установки параметров на пользовательской панели 50 управления. Графическое отображение функций, управляемых процессором расположения и угла наклона цветовой рамки, таких как очертание цветовой рамки и курсора угла потока, обеспечивается посредством графического процессора 34, который связан с процессором 36 отображения для наложения графики на ультразвуковые изображения.
Работа процессора 40 расположения и угла наклона цветовой рамки проиллюстрирована с помощью блок-схемы на Фиг.2. Первый этап 102 данного способа представляет собой пространственную сегментацию потока на ультразвуковом изображении. Это может осуществляться посредством маскирования участков изображения, в которых нет потока. В данном воплощении доплеровское изображение от процессора цветовой визуализации кровотока может предоставлять пространственное изображение только местоположений потока на изображении. Данный этап может также включать в себя усреднение данных потока по нескольким или всем сердечным циклам для получения средних или медианных значений потока. На этапе 104 происходит сегментация кровеносных сосудов с отделением их от других динамических эффектов, таких как перфузия или движение ткани. На этапе 106 выбирается исследуемый сосуд. Исследуемый сосуд обычно будет расположен в центре изображения, получаемого пользователем. Исследуемый сосуд можно также выбирать посредством рассмотрения размера, потока и типа сегментированных кровеносных сосудов. При каротидном исследовании, например, сонная артерия будет идентифицирована как артерия и как наибольший сосуд на изображении. Фиг.3a показывает реальное ультразвуковое изображение 120 потока, полученное из потока в кровеносных сосудах, которые были сегментированы и выбраны для дальнейшей обработки.
На этапе 108 идентифицируется центр пути потока сосуда. Известно несколько методов нанесения на изображение центра пути потока, например, локализация центра поля ламинарного потока по скорости. Другой метод представляет собой аналитическое проведение линий через просвет кровеносного сосуда, как показано в вышеупомянутой патентной заявке Goujon. Центры линий или их точки пересечения определяют центр сосуда. Фиг.3b иллюстрирует поток в сосуде с Фиг.3a, в котором центр пути потока обозначен белой кривой 122. Данный пример показывает ответвление соединяющегося сосуда в нижней части изображения. На этапе 110 вычисляется взвешенный по потоку центр масс. Это осуществляется посредством анализа пространственных размеров потока в целевом сосуде и нахождения его центра. Простой подход заключается в измерении длины и ширины потока в сосуде и взятии их центров. Также можно применять более сложные подходы взвешивания и интегрирования.
В системе, в которой контрольный объем должен устанавливаться автоматически, в данном способе затем устанавливают местоположение контрольного объема на этапе 112 как точки на пути 122 потока, которая является ближайшей к вычисленному центру масс. Это обычно помещает контрольный объем в центр изображения кровеносного сосуда и в центр сосуда, где обычно осуществляются измерения потока. На этапе 114 устанавливается угол потока в соответствии с вектором потока, расположенном в местоположении контрольного объема. Для установки ориентации курсора угла потока может применяться один из методов, описанных в начале настоящего документа. Другой подход заключается в установке курсора угла потока параллельно центральной линии 122, поскольку центральная линия ориентирована поблизости от контрольного объема.
Используя центр масс потока, предварительно вычисленный на этапе 110, цветовую рамку располагают так, чтобы она была центрирована около центра масс. Если центр масс расположен слишком близко к краю изображения, часть площади цветовой рамки может быть обрезана при необходимости. Размеры цветовой рамки по длине или ширине также можно изменять, если потребуется, для стандартного внешнего вида. Фиг.3c и 3d иллюстрируют такое изменение позиционирования цветовой рамки 70 на ультразвуковом изображении 60. На Фиг.3c область 76 потока представляет собой однородную серую область в кровеносном сосуде в верхней части цветовой рамки 70. Вычисление центра масс потока 76 и его перемещение в центр цветовой рамки 70 показано на Фиг.3d, на которой положение цветовой рамки было изменено так, чтобы поток 76 был расположен ближе к центру цветовой рамки. На этапе 118 устанавливается угол наклона цветовой рамки и угол доплеровских лучей для достижения желаемого доплеровского угла. Например, если угол потока, установленный на этапе 114, показывает, что поток в целевом сосуде проходит из верхней левой в нижнюю правую часть изображения, то угол наклона будет установлен равным углу из верхней левой в нижнюю правую часть. Данное направление наклона ближе к расположению на одной прямой с направлением потока, чем угол наклона в направлении из верхней правой в нижнюю левую часть изображения, который был бы ближе к ортогональному к направлению потока и, следовательно, менее чувствительным к доплеровскому потоку. Типичный угол наклона для поверхностных сосудов составляет ±60°. Затем установка, производимая на этапе 118, установит угол наклона равным +60° или -60°, смотря какой из них даст лучшую доплеровскую чувствительность. Такое изменение установки угла наклона цветовой рамки также видно из сравнения угла цветовой рамки на Фиг.3c с заново установленным углом на Фиг.3d. Данная установка угла наклона цветовой рамки может быть установлена в соответствии с локальным направлением потока в местоположении контрольного объема или в соответствии со средним или медианным углами потока вдоль части или всей отображаемой длины кровеносного сосуда. При такой повторной установке угла цветовой рамки новая установка угла передается на контроллер 16 формирователя луча, так что ультразвуковые лучи, передаваемые в цветовую рамку, будут передаваться под заново определенным углом.
Последовательность изображений с Фиг.4-7 иллюстрирует пример того, как может работать ультразвуковая система, описанная выше. Фиг.4 показывает изображение на устройстве отображения ультразвуковой системы типичного цветового/спектрального доплеровского дуплексного изображения с неоптимизированными доплеровскими параметрами. Анатомическое ультразвуковое изображение 60 расположено в верхней части экрана, а спектральное доплеровское отображение 62 расположено в нижней части экрана. Сбор доплеровских данных осуществляют внутри цветовой рамки 70, и цветовое изображение кровотока отображается внутри данной рамки. Снаружи цветовой рамки 70 остальная часть изображения показана в оттенках серого в B-режиме. Применение цветовой рамки очерчивает область, в которой должна осуществляться доплерография, и снаружи цветовой рамки повторяющаяся доплеровская передача для получения множества доплеровских сигналов не осуществляется. Ограничение доплеровской передачи только цветовой рамкой устраняет необходимость в повторяющемся прямом сборе данных снаружи рамки и, следовательно, ограничивает общее количество циклов передачи-приема, необходимых для создания изображения, тем самым уменьшая время, необходимое для получения изображения, что улучшает частоту кадров отображения в реальном времени. Доплеровские лучи для спектральных доплеровских данных передаются и принимаются вдоль линии 68 направления луча, и данные, используемые для спектрального доплеровского отображения, получаются из эхо-сигналов, возвращающихся от контрольного объема SV на линии направления луча. Курсор 66 направления доплеровского потока, применяемый для коррекции угла, не совпадает по ориентации с сосудом 64 (он должен быть параллелен направлению потока), и доплеровский угол наклона не оптимизирован для наилучшей цветовой и спектральной доплеровской чувствительности. В данном примере доплеровский угол наклона равен 0°, является вертикальным на изображении и нормальным к торцу преобразовательного зонда.
Фиг.5 показывает изображение на устройстве отображения ультразвуковой системы после того, как процессором 40 расположения и угла наклона цветовой рамки были осуществлены несколько автоматических регулировок согласно настоящему изобретению. После того, как пользователь поместил доплеровский контрольный объем SV на исследуемый участок в кровеносном сосуде 64, процессор 40 сегментирует поток крови в сосуде 64 и легко идентифицирует сосуд 64 (этап 106) в качестве целевого сосуда, т.е. наибольшего сосуда в цветовой рамке 70. Идентифицируется центр пути потока (этап 108), и ориентация курсора 66 направления потока устанавливается параллельно направлению потока (этап 114), что проиллюстрировано на Фиг.5. Видно также, что угол цветовой рамки 70 и линия 68 направления луча были установлены так, чтобы получить угол 60° с ориентацией сосуда 64 (этап 118). Новые настройки будут давать лучшую доплеровскую чувствительность и точность благодаря более оптимальным параметрам.
Фиг.6 иллюстрирует сценарий, при котором пользователь сдвинул контрольный объем SV в другое местоположение над кровеносным сосудом 64. Автоматическая система ответила вычислением центра масс потока в сосуде 64 внутри цветовой рамки 70 (этап 110). Положение цветовой рамки 70 было изменено так, что рамка центрирована на вычисленном центре масс (этап 116); контрольный объем SV расположен в центре цветовой рамки 70. Углы курсора 66 направления потока и линии 68 направления луча и цветовой рамки 70 также были изменены для получения желаемого доплеровского угла 60° между направлением лучей и направлением потока.
На Фиг.7 пользователь изменил вид изображения, сдвинув ультразвуковой зонд, и переместил контрольный объем SV на другой сосуд выше сосуда 64. Вычисления, основанные на ранее выбранном сосуде 64, и его изображение больше не применимы к новому исследуемому участку. Теперь должны быть начаты вычисления по блок-схеме с Фиг.2 с применением новых данных от другого сосуда, чтобы применить автоматические регулировки к другому сосуду на новом изображении.
Фиг.8 иллюстрирует воплощение настоящего изобретения, в котором пользовательские настройки для автоматической регулировки потока реализованы в виде сенсорных клавиш на экране устройства отображения и выбираются и активируются посредством манипулятора типа мыши или трекбола на панели 50 управления. Кнопку 82, т.е. кнопку AutoFlow On/Off, активируют для включения или выключения автоматизации потока. Нажатие данной кнопки выключит автоматическую систему (если она включена) или включит (если выключена). Кнопка 84 AutoFlow Reset сбросит автоматические результаты, если пользователь ими не удовлетворен. Активация данной кнопки отменит все предшествовавшие вычисления процессора 40 и начнет их заново. Кнопка 86 AutoFlow Config открывает меню (не показано), в котором пользователь может выбрать, какие из возможностей автоматической настройки пользователь хочет использовать. Пользователь может хотеть, например, чтобы система автоматически изменяла местоположение цветовой рамки и углы цветовой рамки и направления луча, если не желает располагать курсор контрольного объема SV и устанавливать ориентацию курсора направления потока вручную. В данном случае процессор 40 может использовать ориентацию установленного вручную курсора направления потока для вычисления и установки углов наклона цветовой рамки и направления луча, или использовать вычисленные средний или усредненный углы потока. Активация кнопки 88 AutoFlow SV Track вынуждает систему динамически отслеживать контрольный объем, когда его положение меняется, и непрерывно производит автоматические регулировки потока, как описано ниже.
Фиг.9 иллюстрирует сценарий, при котором пользователь только что произвел доплеровские измерения в местоположении 80 в кровеносном сосуде 64 и хочет произвести серию измерений в различных точках вдоль фрагмента кровеносного сосуда. В системах предшествующего уровня техники должны были осуществляться регулировки параметров сбора доплеровских данных для каждого нового измерения, что требовало от пользователя постоянно осуществлять ручные регулировки настроек ультразвуковой системы. В данной иллюстрации пользователь закончил измерения в местоположении 80 и сдвинул контрольный объем SV влево в другое местоположение в кровеносном сосуде. Когда пользователь прекращает движение контрольного объема, чтобы остановиться в новом местоположении измерений слева, или нажимает на новое местоположение, ультразвуковая система немедленно осуществляет все автоматические регулировки установок, которые пользователь выбрал с помощью настроек, вызываемых кнопкой AutoFlow Config. Результат проиллюстрирован на Фиг.10, где система автоматически изменила положение цветовой рамки так, чтобы она была центрирована вокруг нового местоположения контрольного объема, автоматически отрегулировала доплеровский угол цветовой рамки 70 и линию 68 направления спектрального луча и автоматически установила угол курсора 66 направления потока. Система сразу готова к сбору спектральных доплеровских данных в оптимальном режиме в новом местоположении контрольного объема. Исследование можно продолжать таким образом. Каждый раз, когда пользователь сдвигает курсор контрольного объема в новое местоположение в сосуде и останавливается там или нажимает на новое местоположение, система будет автоматически сбрасывать настройки сбора доплеровских данных для оптимального сбора данных. Пользователь может осуществлять измерения непрерывно вдоль длины кровеносного сосуда без необходимости вручную повторно регулировать какие-либо настройки доплеровских параметров, что ускоряет проведение исследования и улучшает комфорт и удобство сонографиста.









Изобретение относится к ультразвуковым диагностическим системам визуализации. Техническим результатом является автоматическая регулировка угла наклона луча и цветовой рамки, в которой осуществляется сбор доплеровских данных на основании характеристик кровеносных сосудов на изображении. Предлагаемая ультразвуковая система осуществляет дуплексную цветовую и спектральную доплеровскую визуализацию, причем сбор спектральных доплеровских данных осуществляют в местоположении контрольного объема, указанном на цветовом изображении кровотока. Цветовое изображение кровотока отображается в цветовой рамке, наложенной на одновременно регистрируемое изображение в B-режиме. Процессор расположения и угла наклона цветовой рамки анализирует пространственные доплеровские данные и автоматически устанавливает угол и местоположение цветовой рамки над кровеносным сосудом для оптимальной доплеровской чувствительности и точности. Данный процессор может также автоматически устанавливать курсор коррекции угла потока по направлению потока. В предпочтительном варианте осуществления оптимизационные данные регулировки осуществляются автоматически и постоянно, когда пользователь останавливается в точках для доплеровских измерений вдоль длины кровеносного сосуда. 14 з.п. ф-лы, 13 ил.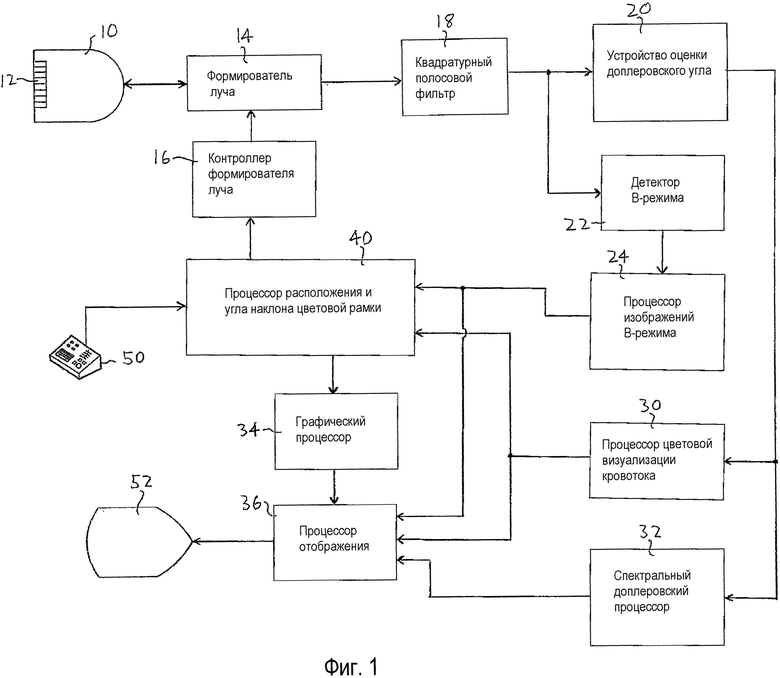
1. Ультразвуковая диагностическая система визуализации для создания спектральных доплеровских отображений потока для анатомических местоположений, выбранных на цветовом изображении кровотока, причем система содержит:
ультразвуковой зонд с массивом преобразователей, выполненный с возможностью передачи ультразвуковых лучей и приема эхо-сигналов из области субъекта, в которой присутствует поток;
формирователь луча, выполненный с возможностью управления направлениями, в которые зонд передает ультразвуковые лучи;
доплеровский процессор, реагирующий на эхо-сигналы и выполненный с возможностью создания доплеровских сигналов;
процессор доплеровских изображений, реагирующий на доплеровские сигналы и выполненный с возможностью создания доплеровских изображений;
устройство отображения, выполненное с возможностью отображения доплеровских изображений; и
процессор расположения и угла наклона цветовой рамки, реагирующий на доплеровские сигналы и выполненный с возможностью автоматического определения расположения отображения цветовой рамки на доплеровских изображениях, причем угол наклона цветовой рамки можно изменять, и процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью автоматического определения угла наклона цветовой рамки, который соответствует углу наклона ультразвуковых лучей, передаваемых зондом.
2. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки выполнен с возможностью автоматического определения расположения цветовой рамки посредством определения угла наклона цветовой рамки.
3. Ультразвуковая диагностическая система визуализации по п. 2, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью автоматического определения соответствия угла линии доплеровского угла наклона определенному углу наклона цветовой рамки.
4. Ультразвуковая диагностическая система визуализации по п. 3, в которой процессор расположения и угла наклона цветовой рамки связан с формирователем луча для управления соответствием угла передачи доплеровского луча с определенной линией доплеровского угла наклона.
5. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки выполнен с возможностью автоматического определения расположения цветовой рамки посредством определения расположения цветовой рамки относительно местоположения кровеносного сосуда на ультразвуковом изображении.
6. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки выполнен с возможностью автоматического определения расположения цветовой рамки посредством определения расположения цветовой рамки относительно местоположения доплеровского контрольного объема на ультразвуковом изображении.
7. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью автоматической установки ориентации курсора направления потока,
причем угол наклона цветовой рамки устанавливается с учетом ориентации курсора направления потока.
8. Ультразвуковая диагностическая система визуализации по п. 1, дополнительно содержащая графический процессор, реагирующий на процессор расположения и угла наклона цветовой рамки, для графического очерчивания местоположения цветовой рамки на ультразвуковом изображении.
9. Ультразвуковая диагностическая система визуализации по п. 8, в которой графический процессор дополнительно выполнен с возможностью графического вычерчивания графика местоположений доплеровского контрольного объема и линии доплеровского угла наклона на ультразвуковом изображении.
10. Ультразвуковая диагностическая система визуализации по п. 1, дополнительно содержащая процессор В-режима, реагирующий на эхо-сигналы, для создания изображений в В-режиме,
причем процессор доплеровских изображений выполнен с возможностью создания цветового доплеровского изображения кровотока и
причем цветовое доплеровское изображение кровотока отображается при пространственном согласовании с изображением в В-режиме в цветовой рамке.
11. Ультразвуковая диагностическая система визуализации по п. 10, в которой процессор доплеровских изображений дополнительно выполнен с возможностью создания спектрального доплеровского изображения, которое отображается одновременно с цветовым доплеровским изображением кровотока, отображаемым при пространственном совмещении с изображением в В-режиме в цветовой рамке.
12. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью реагирования на доплеровские сигналы от кровеносного сосуда для определения центра масс потока в кровеносном сосуде.
13. Ультразвуковая диагностическая система визуализации по п. 12, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью установления расположения цветовой рамки так, чтобы она была центрирована около определенного центра масс потока в кровеносном сосуде.
14. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью определения угла наклона цветовой рамки с учетом локального, или среднего, или медианного направления потока в кровеносном сосуде.
15. Ультразвуковая диагностическая система визуализации по п. 1, в которой процессор расположения и угла наклона цветовой рамки дополнительно выполнен с возможностью определения центральной линии потока в кровеносном сосуде на доплеровских изображениях.
| US 6086539 A, 11.07.2000 | |||
| WO 03019227 A1, 06.03.2003 | |||
| US 2011196237 A1, 11.08.2011 | |||
| US 2010189329 A1, 29.07.2010 | |||
| УЛЬТРАЗВУКОВОЙ ДОПЛЕРОВСКИЙ ИНДИКАТОР КРОВОТОКА | 1998 |
|
RU2152173C1 |
| Ручка для пера с резервуаром для чернил | 1928 |
|
SU10262A1 |
Авторы
Даты
2017-01-10—Публикация
2012-09-14—Подача