ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет согласно 35 U.S.C. §119 к предварительной патентной заявке № 61/222625, зарегистрированной 2 июля 2009, полное содержание которой включено в данное описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение, в основном, относится к способам лечения офтальмологического, ушного или назального нарушения. Настоящее изобретение, главным образом, относится к лечению офтальмологической, ушной или назальной инфекции с использованием композиции, включающей финафлоксацин или финафлоксациновое производное.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Микробная резистентность к традиционному антимикробному способу лечения вызывает постоянную обеспокоенность медицинских работников. Прежде чем проблема резистентности будет преодолена имеется надобность в непрерывной разработке новых методов лечения и методов терапии для того, чтобы ослабить эффект микробных мутаций, которые делают традиционные методы терапии менее эффективными или в некоторых случаях не эффективными. В частности, резистентность к хинолоновым антибиотикам вызывает постоянную озабоченность.
Известно, что хинолоновые антибиотики проявляют желательные противомикробные свойства. Например, хинолоновые соединения для использования в методах лечения офтальмологических, ушных или назальных патологических состояний раскрыты в Патенте США № 6716830, полное содержание которой включено посредством ссылки в данное описание.
Финафлоксацин был раскрыт как полезный для лечения инфекций, [вызываемых] H. pylori. Buissonniere et al., “Antimicrobial activity of a new flyoroquinolone, finafloxacin, against H. Pylori in comparison to levofloxacin” Helicobacter, Vol. 13(5):465, Oct. 2008; Patent U.S. № 6133260 на имя Matzke с сотр. Офтальмологическое, ушное и назальное применение финафлоксацина не описано.
Ссылаясь на одно из многих применений, использование композиций, имеющих антимикробные свойства, является важным для лечения офтальмологических инфекций, таких как конъюнктивит. Конъюнктивит может быть вызван различными видами микробов, в большинстве случаев обусловленных бактериями и/или вирусами. К сожалению, симптомы конъюнктивита не являются специфичными для этиологии инфекционного агента и статистически значимое тестирование может быть необходимо для определения причинного агента или микроба. Объем медицинской помощи должен проводиться путем селекции соответствующих агентов для лечения конъюнктивита, при условии, если имеются чувствительные ткани, пораженные инфекцией. Принимая во внимание вышеприведенные трудности, для лечения конъюнктивита требуются композиции, которые обладают широким спектром антимикробных свойств, благоприятным токсикологическим профилем и/или характеристиками, которые предотвращают передачу контагиозных инфекционных агентов.
Ушные инфекции, такие как острый отит наружного уха (AOE) и острый средний отит с тимпаностомическими трубками (AOMT), предпочтительно пролеченные посредством местных антимикробных композиций, в которых используются оральные антимикробные лекарственные средства, влекут за собой риск [развития] системных побочных эффектов и могут оказаться не в состоянии ликвидировать такие инфекции с возможным развитием лекарственно-резистентных штаммов. Последние годы показывают устойчивое увеличение хинолон-резистентных штаммов бактерий Staphylococcus и Pseudomonas, наиболее часто вызывающих ушные инфекции. В некоторых областях более чем половина штаммов Pseudomonas, изолированных из ушных инфекций, являются хинолон-резистентными (см. Ballenger's Otorhinolaryngology: Head and Neck Surgery, Snow, J. et al. page 194, (2009)). В дополнение к этому наружное ухо находится в общем в кислой окружающей среде вследствие присутствия ушной серы. Следовательно, существует необходимость в дополнительных местных композициях для лечения ушной инфекции, которые являются эффективными при низком pH.
КРАТКАЯ СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям для лечения офтальмологических, ушных или назальных нарушений, включающим финафлоксацин или фармацевтически приемлемую соль, производное, энантиомер, или его гидрат. В предпочтительных вариантах осуществления изобретения такие композиции служат для лечения офтальмологических, ушных или назальных инфекций, особенно инфекций, вызываемых различными бактериальными видами. Предпочтительные финафлоксациновые композиции имеют кислый pH, который обеспечивает увеличение антимикробной эффективности. Дополнительно настоящее изобретение относится к способам лечения инфекционной офтальмологической, ушной или назальной ткани, включающим обработку инфицированной ткани композицией, включающей финафлоксацин.
Композиции и способы настоящего изобретения используются для лечения острых ушных инфекций, особенно инфекций наружного ушного канала, таких как острый отит наружного уха (AOE) и острый средний отит с тимпаностомическими трубками (AOMT). Вследствие присутствия ушной серы окружающая среда наружного уха имеет обычно кислый pH. Неожиданно обнаружено, что, когда испытывали при кислом pH, композиции, включающие финафлоксацин, обычно более эффективны, чем другие хинолоновые композиции против микробов, обычно находимых в ушных инфекциях. Финафлоксациновые композиции настоящего изобретения также имеют низкий потенциал внутренней ушной токсичности, когда используются для местного лечения наружных ушных инфекций. Композиции и способы настоящего изобретения являются, следовательно, хорошо приемлемыми для местного лечения ушных инфекций.
Некоторые финафлоксациновые композиции обеспечивают увеличенную антимикробную активность и могут быть использованы для лечения инфекций, обусловленных хинолон-резистентными микробами. Подразумевается, что такая увеличенная активность возникает в результате комбинации увеличенной потенции и лучших характеристик проницаемости финафлоксацина относительно других антибиотиков. Офтальмологические финафлоксациновые композиции особенно хорошо приемлемы для местного лечения офтальмологической инфекции. Такие композиции могут быть формулированы при нейтральном pH и сохраняют свою эффективность против распространенных офтальмологических патогенов, таких Staphylococcus aureus.
Вышеизложенное краткое резюме широко описывает признаки и технические преимущества некоторых вариантов осуществления настоящего изобретения. Дополнительные признаки и технические преимущества должны быть описаны в подробном описании изобретения далее. Новые признаки, которые, как считается, характеризуют изобретение, должны быть лучше поняты из детального описания изобретения, когда обсуждаются в связи с любым прилагаемым чертежом. Однако чертежи, представленные в данном описании, предназначены для улучшения иллюстративности изобретения или содействия развитию понимания изобретения и не предназначены для будущих определений объема изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Более полное понимание настоящего изобретения и его преимуществ можно получить путем отсылки к нижеследующему описанию, предоставленному в связи с фигурами прилагаемого чертежа, в котором одинаковые номера ссылок указывают на одинаковые фигуры и где:
Фиг. 1a-1d представляют гистограммы, представляющие результаты модели ушной инфекции морской свинки;
Фиг. 2 предоставляет график, показывающий сравнительные данные перфузии роговицы для нескольких хинолоновых антимикробных лекарственных средств;
Фиг. 3 представляет результаты глазного фармакокинетического испытания финафлоксацина и ципрофлоксацина в ткани роговицы после местного применения;
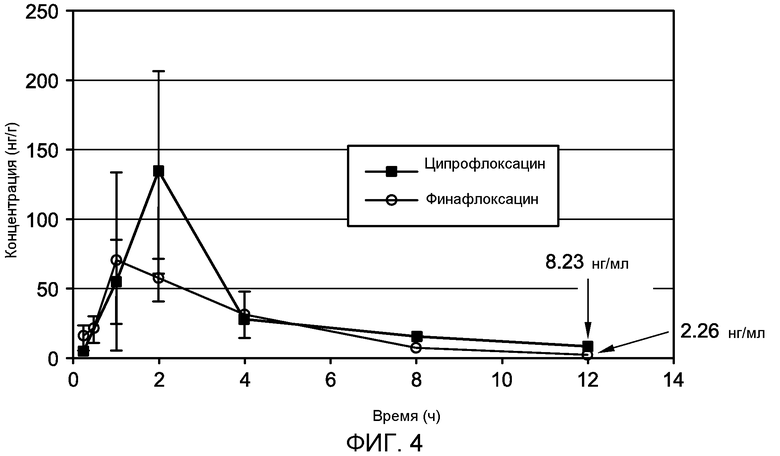
Фиг. 4 представляет результаты глазного фармакокинетического испытания финафлоксацина и ципрофлоксацина во внутриглазной жидкости после местного применения; и
Фиг. 5 представляет диаграмму, представляющую результаты испытания финафлоксациновых и ципрофлоксациновых композиций на модели кератита кролика с использованием Staphylococcus aureus.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Композиции настоящего изобретения включают финафлоксацин или фармацевтически приемлемую соль, производное, энантиомер или его гидрат. Финафлоксацин (8-циано-1-циклопропил-6-фтор-7-[(4aS, 7aS)-гексагидропирроло [3,4-b]-1,4-оксазин-6(2H)-ил]-1,4-дигидро-4-оксо-3-хинолинкарбоновая кислота) имеет следующую структуру:

Предпочтительная соль для использования в вариантах осуществления настоящего изобретения представляет собой финафлоксацина моногидрохлорид. Диастереомерно и энантиомерно чистый финафлоксацин также предпочтителен для использования в вариантах осуществления настоящего изобретения. Как использовано в данном описании, термин «финафлоксацин» предназначается для включения финафлоксацина и его фармацевтически приемлемых солей, производных, энантиомеров или гидратов. Фраза «фармацевтически приемлемый» принята в данной области и относится к композициям, полимерам и другим материалам и/или лекарственным формам, которые приемлемы для использования в контакте с тканями субъектов человека и животных без излишней токсичности, раздражения, аллергического ответа или другой проблемы, или осложнения, сопоставимого с благоприятным отношением польза/риск, как определено специалистом в данной области.
Финафлоксацин и его производные можно синтезировать в соответствии со способами, описанными в Патенте США № 6133260 на имя Matzke с сотр., содержание которого включено в данное описание посредством ссылки во всей своей полноте.
Композиции изобретения конкретно направлены на лечение субъектов млекопитающего и человека, страдающих микробной тканевой инфекцией или имеющих риск развития микробной тканевой инфекции. Микробные тканевые инфекции, которые можно лечить или предотвращать в соответствии со способом настоящего изобретения, относятся к J.P. Sanford et al., “The Sanford Guide to Antimicrobial Therapy 2007” 37th Edition (Antimicrobial Therapy, Inc.). Специфические микробные тканевые инфекции, которые могут быть пролечены посредством при посредстве вариантов осуществления настоящего изобретения, включают те инфекции, которые вызываются бактериями, простейшими, грибами, дрожжами, спорами и паразитами. Настоящее изобретение также специфически направлено на антимикробные композиции и способы лечения офтальмологических, ушных и назальных/синусных инфекций и способов лечения офтальмологических, ушных и назальных/синусовых инфекций.
Определенные варианты осуществления настоящего изобретения особенно полезны для лечения офтальмологических тканевых инфекций. Примеры офтальмологических патологических состояний, которые можно лечить с использованием композиций и способов настоящего изобретения, включают конъюнктивит, кератит, блефарит, дакриоцистит, ячмень и язвы роговицы. Способы и композиции изобретения можно также использовать профилактически в различных офтальмологических хирургических процедурах, которые создают риск развития инфекции.
Ушные и назальные/синусовые инфекции можно также лечить посредством вариантов осуществления настоящего изобретения. Примеры ушных патологических состояний, которые можно лечить композициями и способами настоящего изобретения, включают острый отит наружного уха и средний отит (когда барабанная перепонка разрушена или были имплантированы тимпаностомические трубки). Примеры назальных/синусовых патологических состояний, которые можно лечить композициями и способами настоящего изобретения, включают ринит, синусит, назальные инфекции и ситуации, когда назальные или синусовые ткани подвергаются хирургической операции.
Варианты осуществления настоящего изобретения можно также использовать профилактически для предотвращения инфекции ткани инфекционным агентом. В таких вариантах осуществления изобретения ткань при риске развития инфекции контактирует с композицией настоящего изобретения.
В конкретных вариантах осуществления изобретения композиция настоящего изобретения вводится один раз в день. Однако композиции настоящего изобретения можно также формулировать для введения с любой частотой введения, включая один раз в неделю, один раз в 5 дней, один раз в 3 дня, один раз в 2 дня, два раза в день, три раза в день, четыре раза в день, шесть раз в день, восемь раз в день, каждый час или с любой большей частотой. Такая частота введения дозы также сохраняется для варьирующего периода времени, зависящего от курса лечения. Продолжительность конкретного курса лечения может варьировать от однократного приема до курса лечения, которая продлиться до нескольких месяцев или лет. Специалисту в данной области следует быть знакомым с определением курса лечения для специфической индикации, которая включает фармацевтически эффективное количество финафлоксацина или его композиции. Фраза «фармацевтически эффективное количество» является принятым в данной области термином и отражает количество агента, который при включении в фармацевтическую композицию настоящего изобретения продуцирует некоторый желаемый эффект при благоприятном отношении польза/риск, применимое для любого терапевтического лечения. Эффективное количество может варьировать в зависимости от таких факторов, как болезнь или инфекционный агент, которые нужно лечить, конкретная композиция, которую нужно вводить, или тяжесть болезни, или агрессивность инфекционного агента.
В дополнение к финафлоксацину композиции настоящего изобретения необязательно включают один или несколько эксципиентов. Эксципиенты, обычно используемые в фармацевтических композициях, включают, но не ограничиваясь ими, агенты тоничности, консерванты, хелирующие агенты, буферные агенты, сурфактанты и антиоксиданты. Другие эксципиенты включают солюбилизирующие агенты, стабилизирующие агенты, увеличивающие комфорт агенты, полимеры, смягчающие агенты, регулирующие pH агенты и/или смачивающие агенты. Любой из ряда эксципиентов можно использовать в композициях настоящего изобретения, включая воду, смеси воды и смешиваемые с водой растворители, такие как C1-C7-алканолы, растительные масла или минеральные масла, включающие 0,5-5% нетоксичных водорастворимых полимеров, природных продуктов, таких как альгинаты, пектины, трагакант, камедь карайи, ксантановая камедь, каррагенин, агар и камедь, производные крахмала, такие как крахмал ацетат и гидроксипролил крахмал, а также другие синтетические продукты, такие как поливиниловый спирт, поливинилпирролидон, поливинилметиловый простой эфир, полиэтилен оксид, преимущественно поперечно сшитая полиакриловая кислота и смеси этих продуктов. В предпочтительных вариантах осуществления изобретения концентрация эксципиента(ов) составляет, типично, от 1 до 100 значений концентрации финафлоксацина, и эксципиент(ы) отбирают на основе их инертности по отношению к финафлоксацину.
Приемлемые регулирующие тоничность агенты включают, но не ограничиваясь ими, маннит, натрия хлорид, глицерин, сорбит и подобное. Приемлемые буферные агенты включают, но не ограничиваясь ими, фосфаты, бораты, ацетаты и подобное. Приемлемые сурфактанты включают, но не ограничиваясь ими, ионные и неионные сурфактанты, хотя неионные сурфактанты являются предпочтительней, RLM 100, POE 20 цетилстеариловые простые эфиры, такой как Procol® CS20, и полаксомеры, такой как Pluronic® F68. Приемлемые антиоксиданты включают, но не ограничиваясь ими, сульфиты, аскорбаты, бутилированный оксианизол (BHA) и бутилированный окситолуол (BHT).
Композиции, изложенные в данном описании, включают один или несколько стабилизирующих агентов. Примеры таких стабилизирующих агентов включают сложный эфир п-оксибензойной кислоты, алкил-ртуть соли тиосалицилой кислоты, такие как тиомерсал, фенилртуть нитрат, фенилртуть ацетат, фенилртуть борат, натрия перборат, натрия хлорит, парабены, такие как метилпарабен или пропилпарабен, спирты, такие как хлорбутанол, бензиловый спирт или фенил этанол, производные гуанидина, такие как полгексаметилен бигуанид, натрия перборат или сорбиновая кислота. В некоторых вариантах осуществления изобретения композиция может являться самостабилизирующейся, для которой не требуется стабилизирующий агент.
При использовании для синусовых аппликаций в можно использовать композиции, которые включают эксципиенты, приемлемые для образования аэрозоля с использованием распылителей или других таких устройств, хорошо известных специалистам в данной области.
Некоторые композиции настоящего изобретения являются офтальмологически приемлемыми для аппликации на глаза субъекта. Для офтальмологического введения композиция может представлять раствор, суспензию, гель или и мазь. В предпочтительных аспектах композиции, которые включают финафлоксацин, можно формулировать для местной аппликации на глаз в водном растворе в форме капель. Термин «водный» типично означает водную композицию, где эксципиент составляет >50%, более предпочтительно >75% и особенно >90% по массе воды. Эти капли можно выпускать из ампулы с однократной дозой, которая предпочтительно может быть стерильной и, таким образом, обеспечивать бактериостатические компоненты, которые не являются необходимыми для композиции. Альтернативно, капли можно выпускать из флакона с многоразовой дозой, который предпочтительно может включать устройство, которое экстрагирует любой консервирующий агент из композиции, так как считается, что такие устройства известны в данной области.
В других аспектах компоненты по изобретению можно выпускать в глаз в виде концентрированного геля или сходного носителя, или в виде растворимых прокладок, которые при наложении благоприятно действуют на веки. В еще других аспектах компоненты по изобретению можно выпускать в глаз в виде мази, эмульсий типа вода в масле и масло в воде.
Для местных композиций для глаза композиции являются предпочтительно изотоничными или слабо гипотоничными для того, чтобы противодействовать любой гипотоничности разрывов, вызванных испарением и/или болезнью. Данный агент тоничности в случае необходимости приводит к осмолярности композиции на уровне или около 210-230 миллиосмолей на килограм (мОсм/кг). pH раствора может находиться в офтальмологически приемлемом диапазоне 3,0-8,0. Композиции настоящего изобретения обычно имеют осмолярность в диапазоне 220-320 мОсм/кг, и предпочтительно имеют осмолярность в диапазоне 235-300 мОсм/кг. Офтальмологические композиции обычно формулируют в виде стерильных водных растворов.
В некоторых вариантах осуществления изобретения финафлоксацин формулируется в композиции, которая включает один или несколько заменителей слез. Множество заменителей слез известны в данной области и включают, но не ограничиваясь ими: мономерные полиолы, такие как глицерин, пропилен гликоль и этилен гликоль; полимерные полиолы, такие как полиэтиленгликоль; сложные эфиры целлюлозы, такие как оксипропилметил целлюлоза, натрий карбокси метилцеллюлоза и окси пропилцеллюлоза; декстраны, такие как декстран 70; виниловые полимеры, такие как поливиниловый спирт; и карбомеры, такие как карбомер 934P, карбомер 941, карбомер 940 и карбомер 974P. Определенные композиции по настоящему изобретению можно использовать с контрастными линзами или другими офтальмологическими продуктами.
В некоторых вариантах осуществления композиции, изложенные в данном описании, имеют вязкость 0,5-100 сПс, предпочтительно 0,5-50 сПс и более предпочтительно 1-20 сПс. Эта относительно низкая вязкость обеспечивает удобство применения продукта, не вызывает затуманивания и продукт легок в изготовлении, процессах транспортировки и заполнения.
Для эффективного лечения различных микробных инфекций и для минимизации побочных эффектов антимикробную активность композиции нужно максимизировать так, что используется минимальное количество активного ингредиента. Активность антимикробных композиций по настоящему изобретению является обычно результатом самого антимикробного агента; компоненты композиции, отличающиеся от финафлоксацина, в норме вызывают незначительное действие.
Также рассматривается, что концентрации ингредиентов, включающие композиции по настоящему изобретению, могут варьировать. В предпочтительных вариантах осуществления финафлоксацин представляется в офтальмологических композициях в концентрации от примерно 0,1% до 1,0% мас./об. Особенно предпочтительные варианты осуществления содержат концентрацию финафлоксацина 0,1-0,5% мас./об. и наиболее предпочтительными являются варианты осуществления, содержащие концентрацию финафлоксацина от примерно 0,3% до 0,4% мас./об. Специалист в данной области должен понимать, что концентрации могут варьироваться в зависимости от добавления, замены и/или удаления ингредиентов в данной композиции.
Предпочтительные композиции получают с использованием буферной системы, которая сохраняет композицию при pH от примерно 3 до pH примерно 8,0 и предпочтительно от 5,0 до 7,5. Особенно предпочтительные ушные композиции имеют pH 5,0-6,0 и наиболее предпочтительные ушные композиции имеют pH примерно 5,9. Особенно предпочтительные офтальмологические композиции имеют pH 6,0-8,0 и наиболее предпочтительные офтальмологические композиции имеют pH 7,5-8,0. В некоторых вариантах осуществления местные композиции (особенно местные офтальмологические композиции, как отмечалось выше) являются предпочтительными, которые имеют физиологический pH, соответствующей ткани, на которую композиция будет наноситься или распыляться.
В способах, излагаемых в данном описании, введение в субъекта фармацевтически эффективного количества композиции, которая включает финафлоксацин, может осуществляться любым способом, известным специалистам в данной области.
Например, композиция может быть введена местно, топически, интрадермально, внутрь повреждения, интраназально, подкожно, орально, путем ингаляции, путем инъекции, путем локальной перфузии запущенных в серийное производство мишенных клеток непосредственно через катетер или через лаваж.
В конкретных вариантах осуществления композиция наносится топически на глазную поверхность. Что касается офтальмологического введения, предполагается, что могут быть использованы все местные способы введения в глаз, включая топическое, субконъюктивальное, периокулярное, ретробульбарное, субтеноновое, интраокулярное, субретинальное, постериально околосклеральное и супрахороидальное.
Композиции настоящего изобретения могут также включать противовоспалительный агент. Композиции настоящего изобретению могут также содержать один или несколько противовоспалительных агентов. Противовоспалительные агенты, используемые в настоящем изобретении, приблизительно классифицируются, как стероидные или нестероидные. Предпочтительные стероидные противовоспалительные агенты представляют глюкокортикоиды. Глюкокортикоиды для офтальмологического, ушного или назального использования включают дексаметазон, лотепреднол, римексолон, преднизолон, фторметолон, гидрокортизон, мометазон, флутиказон, беклометазон, флунизолид, триамцинолон и будесонид.
Нестероидные противовоспалительные агенты представляют собой: ингибиторы постагландин H синтетазы (Cox I или Cox II), также упоминаемые как ингибиторы циклооксигеназы типа I и типа II, такие как диклофенак, флурбипрофен, кеторолак, супрофен, непафенак, амфенак, индометацин, напроксен, ибупрофен, бромфенак, кетопрофен, меклофенамат, пироксикам, сулиндак, мефанаминовая кислота, дифлузинал, оксапрозин, толметин, фенопрофен, беноксапрофен, набуметон, этодолак, фенилбутазон, аспирин, оксифенбутазон, NCX-4016, HCT-1026, NCX-284, NCX-456, теноксикам и карпрофен; селективные ингибиторы циклооксигеназы типа II, такие как NS-398, виокс, целекоксиб, P54, этодолак, L-804600 и S-33516; PAF антагонисты, такие как SR-27417, A-137491, ABT-299, апафант, бепафант, минопафант, E-6123, BN-50727, нупафант и модипафант; PDE IV ингибиторы, такие как арифло, торбафиллин, ролипрам, филаминаст, пикламиласт, ципамфиллин, CG-1088, V-11294A, CT-2820, PD-168787, CP-293121, DWP-205297, CP-220629, SH-636, BAY-19-8004, и рофлумиласт; ингибиторы продукции цитокина, такие как ингибиторы фактора транскрипции NF-каппа.B; или другие противовоспалительные агенты, известные специалистам в данной области.
Концентрации противовоспалительных агентов, содержащихся в композициях настоящего изобретения, будут варьироваться, основываясь на отобранном агенте или агентах и типе воспаления, которые требуют лечения. Концентрации должны быть достаточны для снижения воспаления в мишенных офтальмологических, ушных или назальных тканях, после местного нанесения композиции на те ткани. Такое количество упоминается в данном описании как «противовоспалительное эффективное количество». Композиции настоящего изобретению типично содержат один или несколько противовоспалительных агентов в количестве от примерно 0,01 до примерно 1,0 мас.%.
Также рассматриваются различные методики ушного введения. В конкретных вариантах осуществления композиция может доставляться непосредственно в ушной канал (например, местные ушные капли или мази; устройства для медленного высвобождения в ухе или имплантированные вблизи уха). Локальные способы лечения включают ушные внутримышечные, в интратимпанальную полость и интракохлеарные инъекционные способы лечения для композиций. Далее раскрывается, что определенные композиции изобретения можно формулировать во внутриушных вкладышах или имплантированных устройствах. Например, доставка композиций может осуществляться путем инъекции с эндоскопическим ассистированием (включая лазер-ассистированную эндоскопию для образования разреза в тимпаническую мембрану) в тимпанической полости, как изложено, например, у Tsue et al., Amer. J. Otolaringology, Vol. 16(3)158-164, 1995; Silvestein et al., Ear Nose Throat, Vol. 76:674-678, 1997; Silvestein et al., Otolaringol Head Neck Surg, Vol. 120:649-655, 1999. Местное введение также может быть выполнено путем инъекции через тимпаническую мембрану с использованием тонкой (EMG запись) иглы посредством использования постоянного катетера, помещенного через мирингитомический разрез, и инъекции или инфузии через евстахиеву трубу посредством маленького трубчатого катетера. Кроме того, композиции можно вводить во внутреннее ухо путем помещения гелевой пены или сходного абсорбента и адгезивного продукта, пропитанного композициями против болезни барабанной перепонки среднего/внутреннего уха или соседней структуры при праве принимать решения и предупреждении неблагоприятных последствий квалифицированных клиницистов. Различные другие устройства могут быть использованы для доставки композиций в пораженный ушной компартмент; например, через катетер или как подтверждается примером в Патенте США № 5476446, который предоставляет многофункциональное устройство, специфически сконструированное для использования в лечении и/или диагностики внутреннего уха субъекта. Также см. Патент США № 6653279 для других устройств для этой цели.
Введение композиций, описанных в данном описании, для лечения назальной инфекции может быть осуществлено посредством ряда способов, известных специалистам в данной области. Например, такие композиции могут быть введены в капельной форме или путем формирования аэрозоля.
ПРИМЕРЫ
Примеры 1-7, расположенные ниже, были получены в соответствии с вариантами осуществления настоящего изобретения.
ПРИМЕР 1
ПРИМЕР 2
ПРИМЕР 3
ПРИМЕР 4
ПРИМЕР 5
ПРИМЕР 6
Соляная кислота
ПРИМЕР 7
ПРИМЕР 8 - Испытания in vitro антимикробной эффективности
Финафлоксациновую композицию при pH 5,8 сравнивали с ципрофлоксациновыми (pH 5,8) и офлоксациновыми (pH 5,8 и pH 7) композициями с использованием стандартных in vitro тестов на антимикробную чувствительность (M07-08 Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically; Approved Standart-Eighth Edition (Jan 2009, Clinical and Laboratory Standarts Institute), в данное описание включенные посредством ссылки. Минимальные ингибирующие концентрации (MIC50) определяли с использованием грамположительных и грамотрицательных тест-организмов, обычно обнаруживаемых в ушных и офтальмологических инфекциях. MIC50 являлась наиболее низкой концентрацией антибиотика, который предотвращал рост тестируемого организма, как определяли визуально путем отсутствия мутности.
Результаты эксперимента представлены ниже в Таблице 1 (грамположительные организмы) и Таблице 2 (грамотрицательные организмы). Финафлоксациновые композиции показывали более низкие концентрации MIC50 для всех тестированных грамположительных организмов по сравнению с ципрофлоксациновыми и офлоксациновыми композициями.
Грамположительные бактерии
Грамотрицательные бактерии
ПРИМЕР 9 - Модель in vitro острого отита наружного уха (AOE)
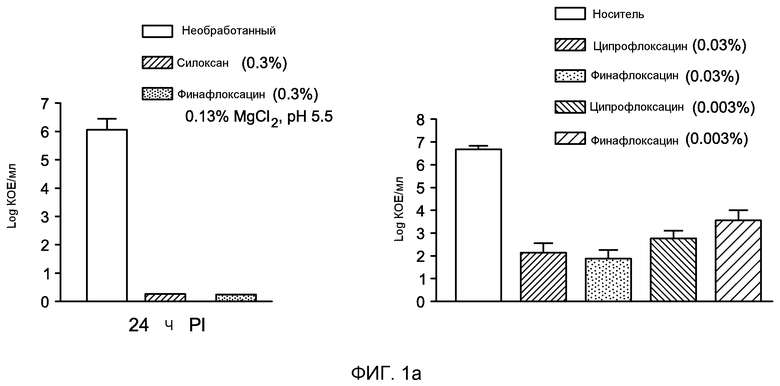
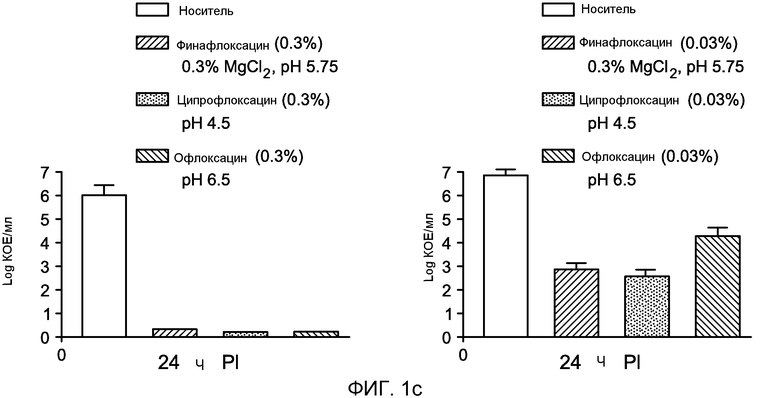
Финафлоксациновые тестируемые композиции (0,3%, 0,03% и 0,003%) сравнивали с офлоксациновыми (0,3% и 0,03%) и ципрофлоксациновыми композициями (CILOXAN®, Alcon Laboratories, Inc (0,3% ципрофлоксацин гидрохлорид), 003% и 0,003%) на модели острого отита наружного уха морской свинки (AOE) с использованием Pseudomonas aeruginosa. Уши морской свинки слегка выскабливали и 200 мкл бактериальной культуры (108 КОЕ) P. aeruginosa вкапывали в каждое ухо. Уши орошали физиологическим раствором и помещали на изолирующую среду для Pseudomonas. Фиг. 1a-1d суммируют результаты этих испытаний.
Как показано на Фиг. 1a, 0,3% концентрация финафлоксацина вызывает почти полную эрадикацию Pseudomonas с использованием двух раздельных доз тестируемой композиции. Наиболее низкая концентрация финафлоксациновых композиций (0,03% и 0,003%) все еще достигает очень существенного 5-6 log снижения Pseudomonas на модели. В тестах, суммированных на Фиг. 1a, финафлоксацин демонстрирует эффективность, такую же как ципрофлоксацин. Финафлоксацин также сравнивали с отофлоксацином и ципрофлоксацином в однодозовых испытаниях. Фиг. 1b показывает, что 0,3% финафлоксациновая композиция приводит к почти полной эрадикации Pseudomonas в однодозовом испытании. При использовании более низкой концентрации композиции (0,003%, показано на Фиг. 1c) финафлоксацин обеспечивал 4 log снижение КОЕ в однодозовом испытании. В этом испытании финафлоксациновая композиция демонстрировала эффективность, также как и ципрофлоксациновая композиция, и лучше чем отофлоксациновая композиция. Фиг. 1d демонстрирует, что использование консерванта (BAC) в 0,003% и 0,3% финафлоксациновых композициях не влияет на эффективность финафлоксацина против Pseudomonas по сравнению с самостерилизующими композициями.
ПРИМЕР 10 - Ушные фармакокинетические испытания
Фиг. 2 представляет сравнительные данные по перфузии роговицы для хинолоновых антимикробных средств (включая финафлоксацин) с использованием модели ex vivo. 0,1 мМ тестируемых растворов при pH 7,3 четырех хинолоновых антимикробных средств сравнивали в модели. Как показано на Фиг. 2, финафлоксациновая тест-композиция проявляет более лучшие свойства перфузии роговицы, чем ципрофлоксациновая тест-композиция и демонстрирует меньшую перфузию относительно офлоксациновой тест-композиции.
Фиг. 3 и 4 предоставляют результаты ушных фармакокинетических испытаний после местного введения финафлоксациновой и ципрофлоксациновой композиций. В испытаниях использовали новозеландских белых кроликов, и 45 мкл 0,3% тест-композиции вкапывали билатерально. Как показано на Фиг. 3 и 4, соответственно концентрации в ткани стромы роговицы и внутриглазной жидкости финафлоксацина и ципрофлоксацина можно было сравнивать в последние временные точки с ципрофлоксациновой композицией, что приводило к более высоким концентрациям непосредственно после вкапывания.
ПРИМЕР 11 - Испытание in vivo кератита
Две 0,33% финафлоксациновых офтальмологических композиций с различными буферными и pH характеристиками сравнивали с CILOXAN® на модели кератита кролика. Новозеландские белые кролики получали инъекцию в роговицу 100 КОЕ Staphylococcus aureus. Кроликов обрабатывали местно 45 мкл тест-композиции один раз в час начиная с 4 часов после инфицирования (всего 6 обработок). Роговицы собирали и культивировали на жизнеспособность клеток 1 час после окончания тест-обработки. Как показано на Фиг. 5, обе финафлоксациновые композиции демонстрировали log снижение Staphylococcus aureus на модели кератита, сходное с log снижением CILOXAN® композиции. В сходном тесте с использованием Pseudomonas aeruginosa финафлоксациновые композиции демонстрировали плохое снижение КОЕ Pseudomonas по сравнению с CILOXAN®.
ПРИМЕР 12 - Испытания in vivo ототоксичности
Таблица 3 ниже представляет результаты тестированной токсичности, выполненной на двух животных моделях (шиншилла и кролик). Тестированные финафлоксациновые композиции не демонстрируют болезненной чувствительности внутреннего или наружного уха на использованных животных моделях.
•Носитель c 0,13% ZnCl2
•0,3% финафлоксацин и 0,13% ZnCl2
•Носитель c 0,13% MgCl2
•Носитель pH 5,7 (0,3% Mg и BAC всего)
•Носитель pH 7,5
•0,3% финафлоксацин pH 5,7
•03% финафлоксацин pH 7,5
•0,6% финафлоксацин pH 7,5
•1,0% финафлоксацин pH 7,5
Настоящее изобретение и его варианты осуществления были описаны подробно. Однако объем настоящего изобретения не предназначен для ограничения практических вариантов осуществления любого процесса, производства, композиции вещества, соединений, средств, способов и/или стадий, описанных в изобретении. Различные модификации, замены и варианты могут быть сделаны для раскрытия материала без выхода за пределы существа и/или важных характеристик настоящего изобретения. Соответственно любой из специалистов в данной области может легко понять из раскрытия, что последние модификации, замены и/или варианты, выполняющие существенно сходную функцию или достигающие существенно сходного результата как варианты осуществления, описанные в данном описании, могут быть использованы в соответствии с такими родственными вариантами осуществления настоящего изобретения. Таким образом, следующая формула изобретения предназначена для включения в свой объем модификаций, замен и вариантов в процессах, производствах, композициях вещества, соединениях, средствах, способах и/или стадиях, раскрытых в данном описании.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ ФИНАФЛОКСАЦИНА В ВИДЕ СУСПЕНЗИИ | 2013 |
|
RU2693476C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИБИОТИК И ДИСПЕРГИРУЮЩЕЕ СРЕДСТВО ИЛИ АНТИАДГЕЗИВНЫЙ АГЕНТ | 2011 |
|
RU2607660C2 |
| СОСТАВ И СПОСОБ ПОЛУЧЕНИЯ ГЛАЗНОЙ МАЗИ | 2012 |
|
RU2531937C2 |
| СОСТАВ И СПОСОБ ПОЛУЧЕНИЯ ГЛАЗНЫХ КАПЕЛЬ | 2014 |
|
RU2595837C2 |
| Композиция, содержащая антибиотик и диспергирующее средство или антиадгезивный агент | 2011 |
|
RU2739249C2 |
| ВОДНЫЕ ПРОЗРАЧНЫЕ РАСТВОРЫ ФЛУОЦИНОЛОНА АЦЕТОНИДА ДЛЯ ЛЕЧЕНИЯ УШНОГО ВОСПАЛЕНИЯ | 2011 |
|
RU2549465C2 |
| ВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ БОРАТ-ПОЛИОЛЬНЫЕ КОМПЛЕКСЫ | 2009 |
|
RU2477631C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИЙ СРЕДНЕГО УХА | 2002 |
|
RU2295346C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ФТОРХИНОЛОНОВОЕ АНТИБИОТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2009 |
|
RU2494727C2 |
| Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) | 2016 |
|
RU2682171C2 |





Группа изобретений относится к медицине, а именно к оториноларингологии, и предназначена для лечения ушных инфекций, обусловленных хинолон-резистентными микробами, в частности Ципрофлоксацин резистентными микробами. Фармацевтическая композиции включает финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,1-1,0 мас./об.%. Также обеспечивается способ лечения острого отита наружного уха или острого среднего отита с тимпаностомическими трубками, обусловленных хинолон-резистентными микробами, в частности Ципрофлоксацин резистентными микробами. Указанный способ включает инстилляцию ушной композиции для местного нанесения, включающей финафлоксацин в концентрации 0,1-1,0 мас./об.%, в наружный ушной канал субъекта. Использование группы изобретений позволяет повысить эффективность местного лечения ушных инфекций. 3 н. и 13 з.п. ф-лы, 8 ил., 3 табл., 12 пр.
1. Фармацевтически приемлемая композиция для местного применения финафлоксацина, причем указанная композиция подходит для лечения ушных инфекций, обусловленных хинолон-резистентными микробами, в частности Ципрофлоксацин резистентными микробами, включающая финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,1-1,0 мас./об.%.
2. Композиция по п. 1, включающая финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,1-0,5 мас./об.%.
3. Композиция по п. 1, включающая финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,3-0,4 мас./об.%.
4. Композиция по п. 1, причем указанная композиция имеет pH 5,0-7,5.
5. Композиция по п. 1, причем указанная композиция имеет pH 5,0-6,0.
6. Композиция по п. 1, дополнительно включающая противовоспалительный агент.
7. Способ лечения ушной инфекции, обусловленной хинолон-резистентными микробами, в частности Ципрофлоксацин резистентными микробами, включающий: лечение инфекции фармацевтически эффективным количеством композиции, включающей финафлоксацин в концентрации 0,1-1,0 мас./об.%.
8. Способ по п. 7, где указанная инфекция представляет острый отит наружного уха или острый средний отит с тимпаностомическими трубками.
9. Способ по п. 7, где указанная композиция включает финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,1-0,5 мас./об.%.
10. Способ по п. 7, где указанная композиция включает финафлоксацин или его фармацевтически приемлемую соль в концентрации 0,3-0,4 мас./об.%.
11. Способ по п. 7, где указанная композиция имеет pH 5,0-7,5.
12. Способ по п. 7, где указанная композиция имеет pH 5,0-6,0.
13. Способ по п. 7, где указанная композиция дополнительно включает противовоспалительный агент.
14. Способ лечения острого отита наружного уха или острого среднего отита с тимпаностомическими трубками, обусловленных хинолон-резистентными микробами, в частности Ципрофлоксацин резистентными микробами, причем указанный способ включает:
инстилляцию ушной композиции для местного нанесения, включающей финафлоксацин в концентрации 0,1-1,0 мас./об.%, в наружный ушной канал субъекта.
15. Способ по п. 14, где указанная композиция содержит финафлоксацин в концентрации 0,3-0,4 мас./об.% и pH 5,0-6,0.
16. Способ по п. 15, где композиция дополнительно содержит хлорид магния в концентрации 0,3-1,0 мас./об.%.
Авторы
Даты
2015-12-10—Публикация
2010-07-02—Подача