Область техники
Настоящее изобретение относится к фармацевтической композиции и способу лечения гипертензии.
Предшествующий уровень техники
Гипертензия является проблемой общественного здравоохранения и поражает более 25% взрослого населения во всем мире [1, 2]. Гипертензия идентифицирована как ведущий фактор риска смертности, и ее оценивают как третьеочередную ведущую причину лет жизни, утраченных по инвалидности [1, 3]. Несмотря на доступность многочисленных гипотензивных средств, диагностика, лечение и контроль гипертензии далеки от идеала, при проценте контроля от 6% до 30% в различных обществах во всем мире [1]. Не соблюдение гипотензивного лечения ассоциировано с более низкими долями контроля кровяного давления (КД) и более высокими долями сердечно-сосудистых патологий [4-6]. Осуществление один раз в сутки комбинированной терапии с установленной дозой (FDC) с помощью более чем двух классов гипотензивных средств является стратегией, адаптированной к улучшенному соблюдению лечения и контролю КД. Данная стратегия описана в недавних руководствах, даже в качестве возможного начального метода лечения [7, 8].
Недавно показано, что НАДФ-Н оксидазы вносят вклад в патогенез гипертензии. См. Williams et al., 2007, J. Cardiovasc Pharmacol., 50:9-16 и ссылки, приведенные в данной статье. Предположили, что специфичные ингибиторы этих ферментов могут обладать потенциальной терапевтической пользой при гипертонической болезни. Показано, что два из наиболее специфичных ингибиторов, gp91ds-tat и апоцинин, снижают кровяное давление в животных моделях гипертензии. Другие ингибиторы, включающие дифенилениодоний, аминоэтилбензолсульфонофторид, S17834, PR39, ингибиторы протеинкиназы С и VAS2870, показаны как перспективные in vitro, но их специфичность in vivo, фармакокинетику и эффективность при гипертензии еще предстоит определить. Современные доступные гипотензивные средства, ингибиторы ангиотензинпревращающего фермента и блокаторы рецепторов ангиотензина, также эффективно ингибируют активацию НАДФ-Н оксидазы. Подобным образом, показано, что средства, снижающие холестерин, статины, ослабляют активацию НАДФ-Н оксидазы.
Декстрометорфан (DM) представляет собой правовращающий морфинан и широко применяется в качестве не опиоидного средства, подавляющего кашель, в ряде безрецептурных лекарственных средств [17]. Он является антагонистом рецептора NMDA. Точный механизм действия его противокашлевой активности, однако, остается неясным. Исследования с использованием животных моделей ишемии головного мозга и гипогликемических нервных повреждений продемонстрировали, что DM обладает нейропротективной активностью [18-23]. DM эффективно ингибировал индуцированное 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МРТР)-индуцированное образование активных форм кислорода (АФК). Нейропротективный эффект DM зависел от нормальной функции НАДФ-Н оксидазы [24]. Недавние in vitro и in vivo исследования показали, что DM снижает окислительный стресс и ингибирует атеросклероз и образование новообразований у мышей посредством прямого ингибирования НАДФ-Н оксидазы, и что он также уменьшает образование супероксида в аорте и каротидной артерии мышей с дефицитом аполипопротеина Е (ароЕ). Liu et al., 2009, Cardiovascular Research, 82: 161-169. Alvarez Y et al предполагают, что повышенное образование супероксидного аниона (O2 -) из НАДФ(Н) оксидазы в кровеносных сосудах гипертензивных крыс вносит вклад в вазоконстрикторные ответы и противодействует повышению образования NO из iNOS и соответствующему модулированию их ответов [25].
Блокаторы кальциевых каналов (БКК) показаны в качестве начальной терапии гипертензии. Их полезные эффекты и возможные риски исследованы в нескольких клинических испытаниях [9-14]. Применение высоких доз БКК ассоциировано с высокой частотой побочных действий (ПД), таких как периферический отек и констипация [8, 11, 12].
Амлодипин является БКК с гипотензивными свойствами, назначаемым в виде монотерапии. Он является одним из серии дигидропиридиновых антагонистов кальция. Обнаружено, что он хорошо переносится даже пациентами с высоким риском, такими как пациенты с коронарной болезнью, сердечной недостаточностью или множественными факторами риска сердечно-сосудистых патологий [12-16]. Амлодипин в целом обладает замедленным началом действия и большей продолжительностью действия, чем, например, нифедипин. (Jensen, H. et al., J. Hum. Hypertens., 42(5): 541-45, 1990). Метаболиты амлодипина, по-видимому, не обладают значительной активностью блокирования кальциевых каналов, тогда как исходное лекарственное средство дает возможность биологического периода полувыведения примерно 35-40 часов, что соответствует режиму дозировки один раз в сутки. (Lorimer, A.R., et al., J. Hum. Hypertens., 3(3): 191-96, 1989; Glasser, S.F. et al., AJH, 2(3): 154-57, 1989). Его способность к блокированию кальциевых каналов гладких мышц приводит к периферической вазодилатации, приводящей в результате к снижению как систолического, так и диастол ического кровяного давления. Рацемическую смесь амлодипина в настоящее время применяют, в основном, в качестве гипотензивного средства, которое приводит к периферической вазодилатации, приводящей в результате к снижению как систолического, так и диастол ического кровяного давления при применении в качестве гипотензивного средства. Этот гипотензивный эффект осуществляется при относительном отсутствии значительных или пролонгированных эффектов на частоту сердечных сокращений. Однако обнаружено, что введение рацемической смеси амлодипина человеку вызывает побочные эффекты, такие как отек конечностей, периферический отек, головная боль, покраснение/приливы крови, утомляемость, головокружение, мышечные судороги и умопомрачение.
Остается необходимость в новых и безопасных способах и фармацевтических композициях для лечения или предупреждения гипертензии и родственных симптомов. Такие способы и фармацевтические композиции описаны в настоящей заявке.
Краткое описание изобретения
В настоящее время обнаружено, что декстрометорфан не только эффективен для снижения кровяного давления у субъекта, страдающего гипертензией, но также обладает синергетическим действием с блокатором кальциевых каналов, приводящим в результате к значительному улучшению при лечении гипертензии с небольшими побочными эффектами или их отсутствием.
В одном общем аспекте воплощения настоящего изобретения относятся к способу лечения гипертензии или обусловленного ею симптома у субъекта. Этот способ включает введение субъекту фармацевтической композиции, содержащей эффективное количество декстрометорфана и фармацевтически приемлемый носитель.
В одном общем аспекте воплощения настоящего изобретения относятся к способу лечения гипертензии или обусловленного ею симптома у субъекта. Этот способ включает введение субъекту эффективного количества декстрометорфана и эффективного количества блокатора кальциевых каналов.
В другом общем аспекте воплощения настоящего изобретения относятся к фармацевтической композиции для лечения гипертензии или обусловленного ею симптома у субъекта, содержащей эффективное количество декстрометорфана и эффективное количество блокатора кальциевых каналов и фармацевтически приемлемый носитель.
В предпочтительном воплощении настоящее изобретение относится к фармацевтической композиции для лечения гипертензии или обусловленного ею симптома у субъекта, которая содержит эффективное количество декстрометорфана, эффективное количество амлодипина и фармацевтически приемлемый носитель.
В другом общем аспекте воплощения настоящего изобретения относятся к фармацевтической композиции для лечения гипертензии или обусловленного ею симптома у субъекта, содержащей эффективное количество блокатора кальциевых каналов, эффективное количество ингибитора НАДФ-Н оксидазы и фармацевтически приемлемый носитель.
Другие аспекты настоящего изобретения относятся к способам лечения гипертензии или обусловленного ею симптома у субъекта, включающим введение субъекту эффективного количества блокатора кальциевых каналов, такого как амлодипин, и эффективного количества ингибитора НАДФ-Н оксидазы, такого как декстрометорфан.
Другие аспекты, признаки и преимущества изобретения очевидны на основании нижеследующего описания, включающего подробное описание изобретения и его предпочтительных воплощений и прилагаемой формулы изобретения.
Краткое описание Фигур
Как приведенное выше краткое изложение, так и приведенное ниже подробное описание изобретения лучше понятно по прочтении в сочетании с сопроводительными графическими материалами. В целях иллюстрации изобретения в графических материалах показаны предпочтительные воплощения изобретения. Однако понятно, что изобретение не ограничено представленными точными устройствами и инструментами.
В графических материалах:
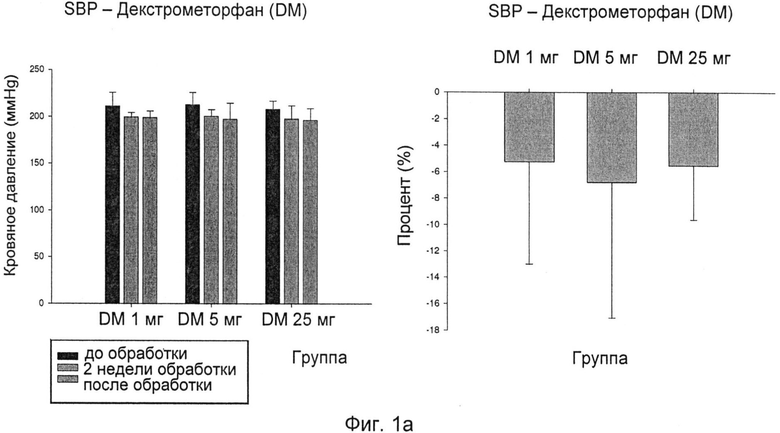
Фиг.1а-Фиг.1d иллюстрируют эффект декстрометорфана (DM), снижающий кровяное давление в животной модели гипертензии, то есть у спонтанно гипертензивных крыс (SHR), при трех уровнях дозировки, 1 мг/кг/сутки, 5 мг/кг/сутки, и 25 мг/кг/сутки:
Фиг.1а: изменения систолического артериального давления (SBP) после лечения DM;
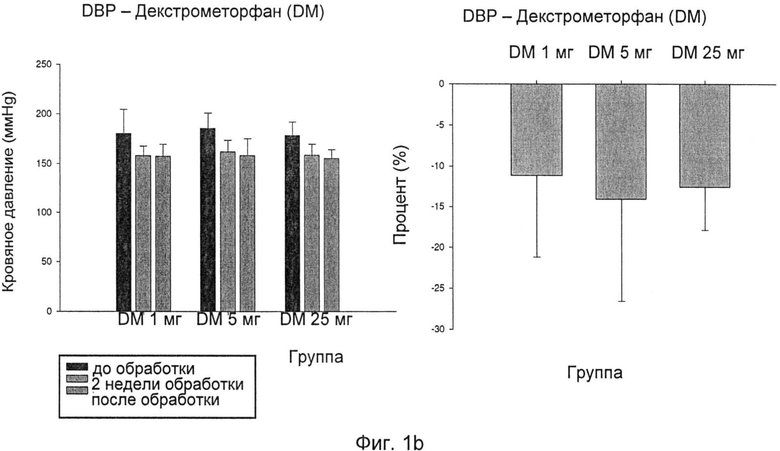
Фиг.1b: изменения диастолического артериального давления (DBP) после лечения DM;
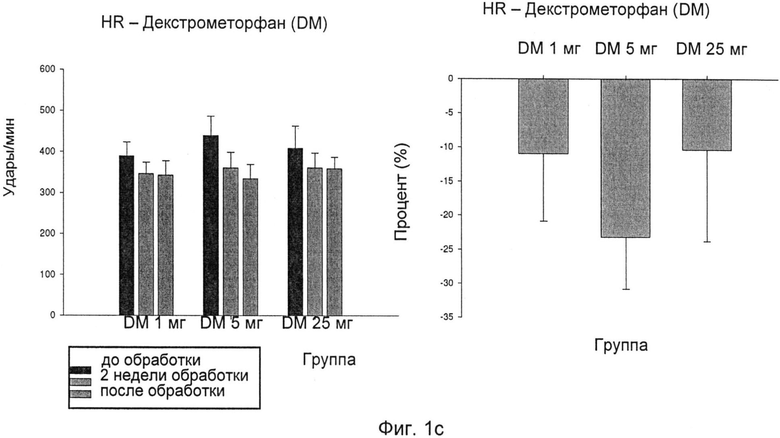
Фиг.1с: изменения частоты сердечных сокращений (HR) после лечения DM; и
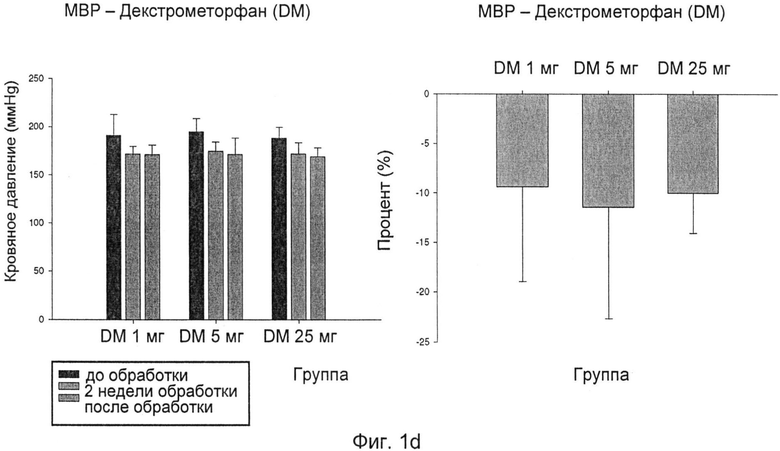
Фиг.1d: изменения среднего артериального давления (МВР) после лечения DM;
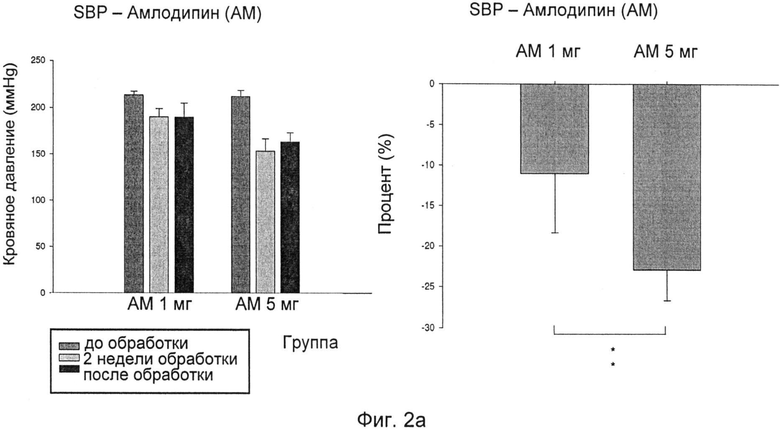
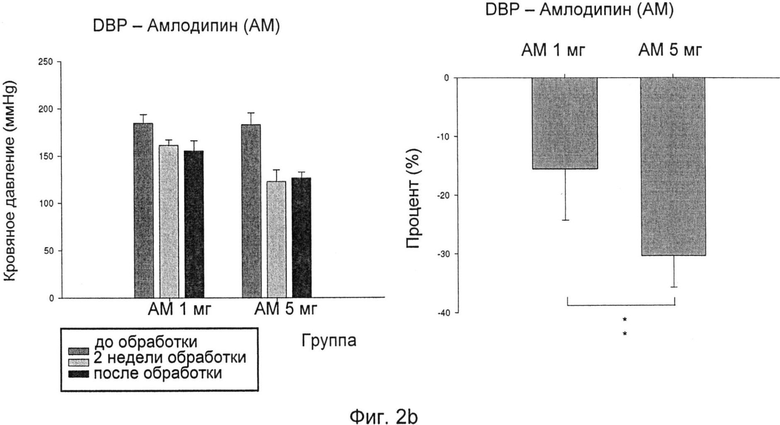
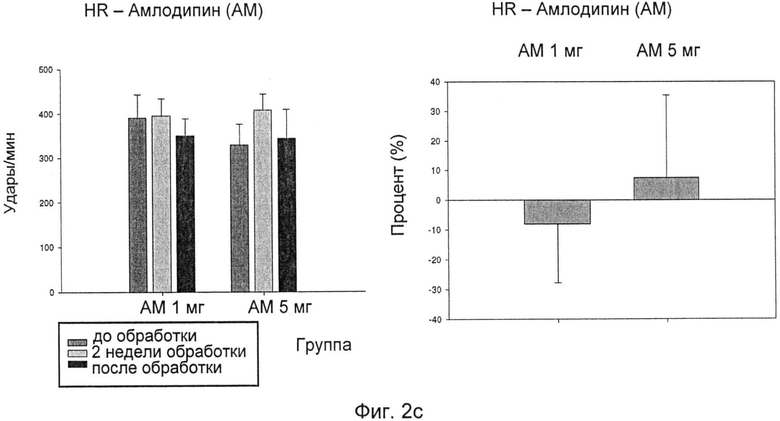
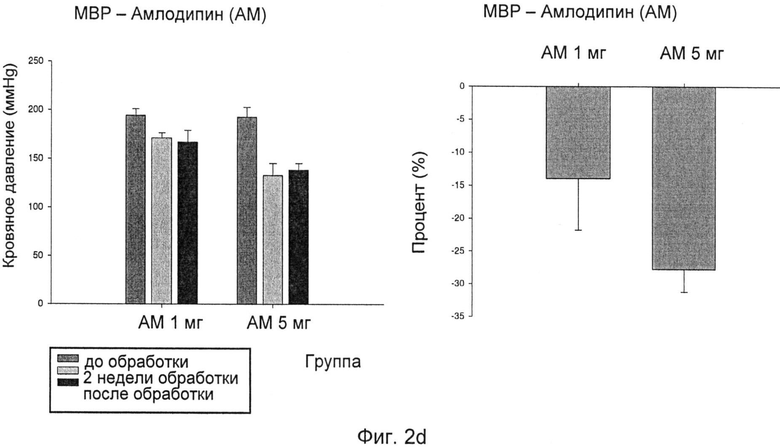
Фиг.2а-Фиг.2d иллюстрируют эффект, снижающий кровяное давление, амлодипина (AM) у SHR при двух уровнях дозировки, 1 мг/кг/сутки и 5 мг/кг/сутки:
Фиг.2а: изменения SBP после лечения AM;
Фиг.2b: изменения DBP после лечения AM;
Фиг.2с: изменения HR после лечения AM; и
Фиг.2d: изменения МВР после лечения AM;
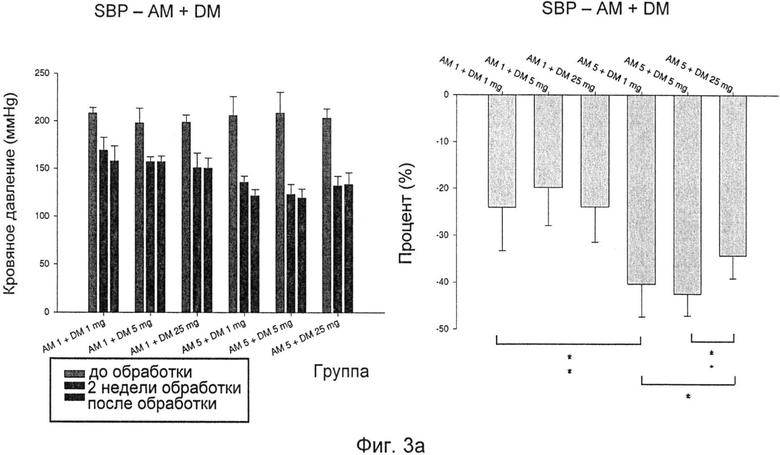
Фиг.3а-Фиг.3d иллюстрируют эффект, снижающий кровяное давление, комбинации DM и AM у SHR при различных уровнях дозировки:
Фиг.3а: изменения SBP после лечения DM+AM;
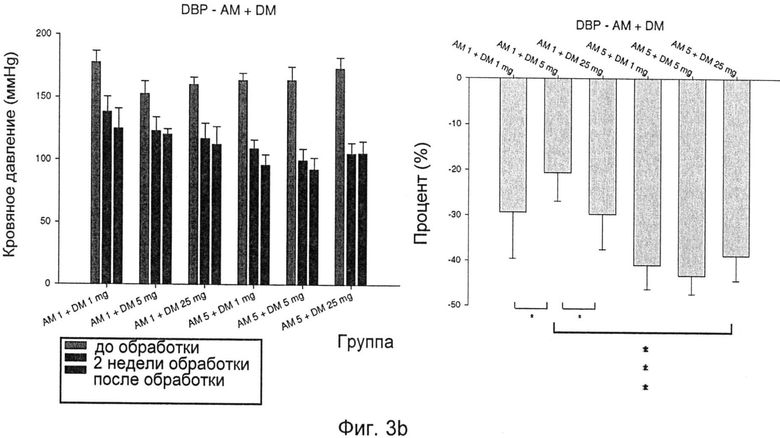
Фиг.3b: изменения DBP после лечения DM+AM;
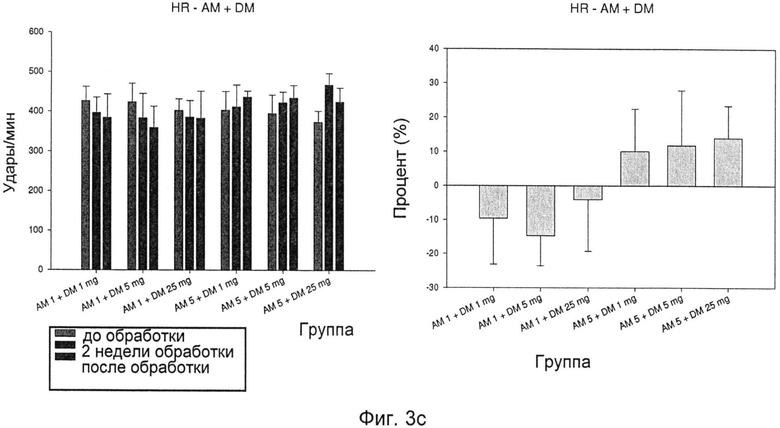
Фиг.3с: изменения HR после лечения DM+AM; и
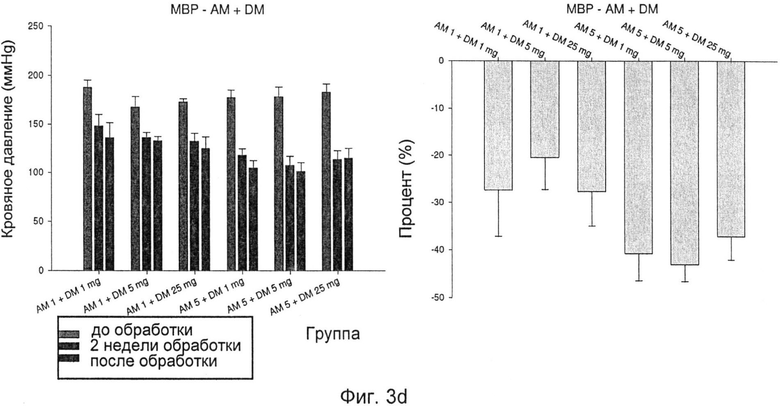
Фиг.3d: изменения МВР после лечения DM+AM;
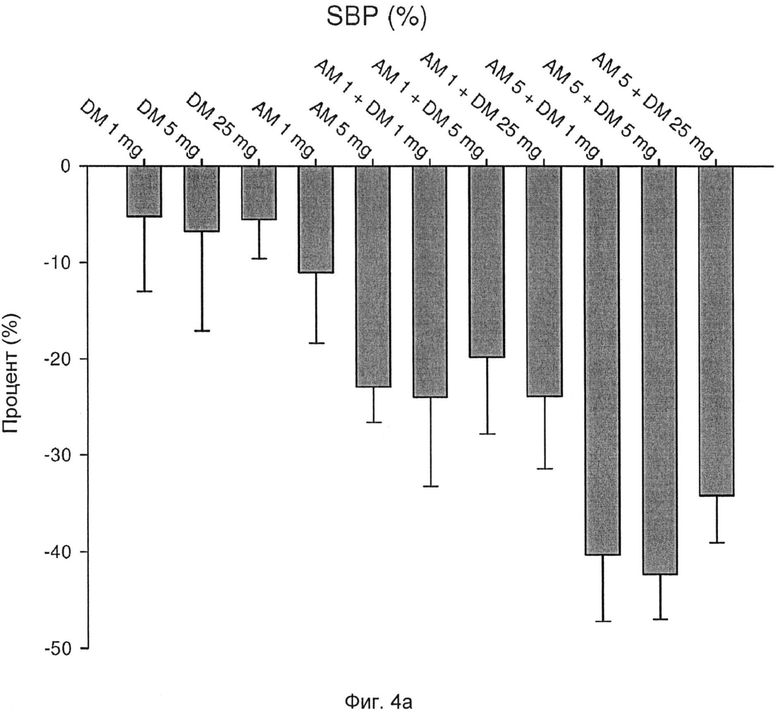
Фиг.4а-Фиг.4d иллюстрируют эффект, снижающий кровяное давление, при различных схемах лечения у SHR, выраженный в процентах изменения кровяного давления или частоты сердечных сокращений:
Фиг.4а: проценты изменения SBP после различных схем лечения;
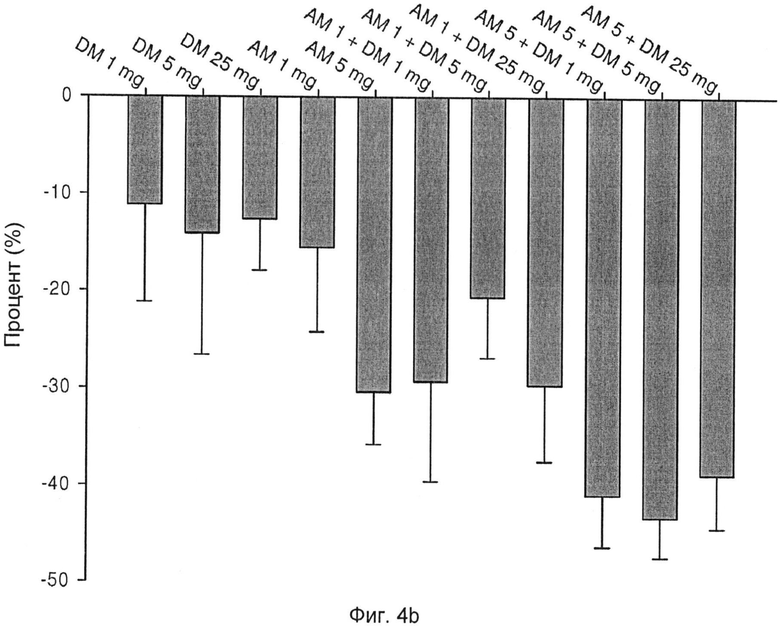
Фиг.4b: изменения DBP после различных схем лечения;
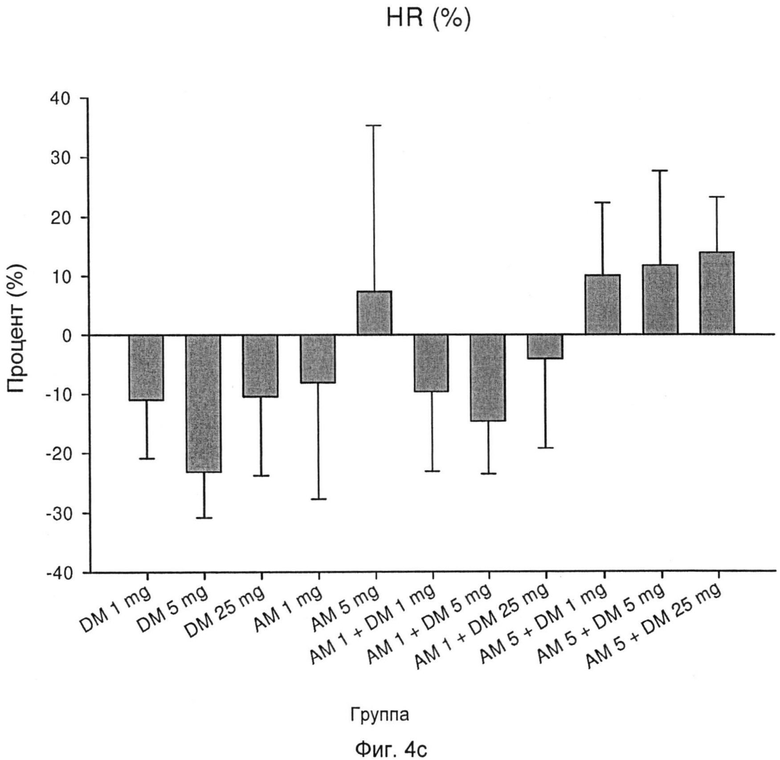
Фиг.4с: изменения HR после различных схем лечения; и
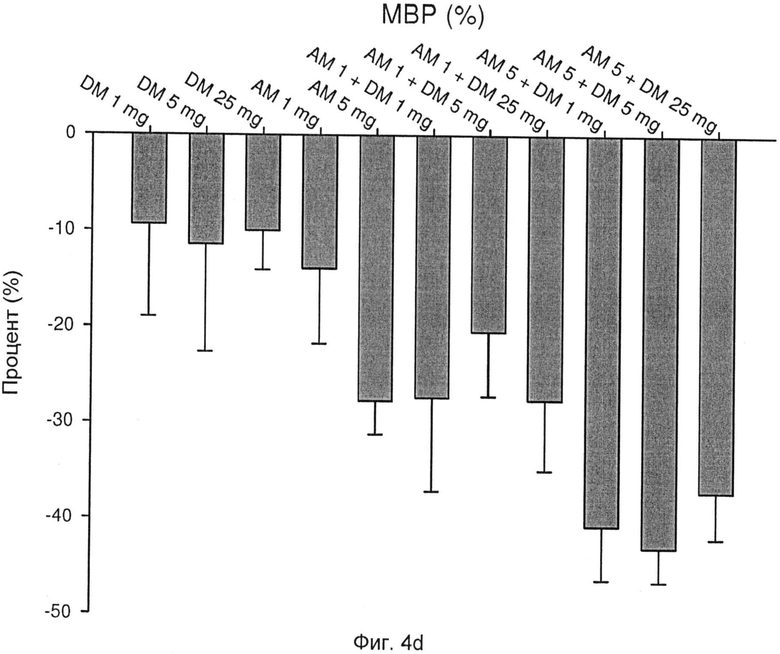
Фиг.4d: изменения МВР после различных схем лечения;
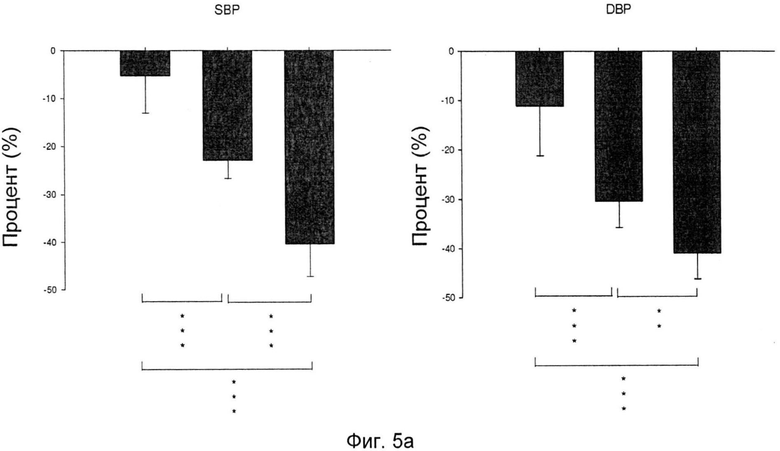
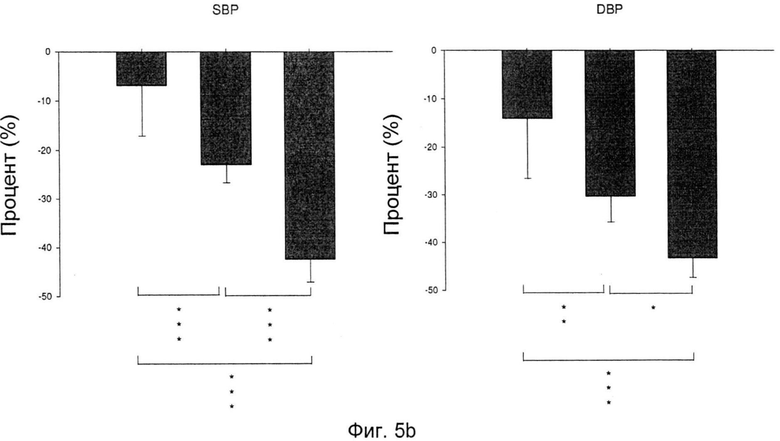
На Фиг.5а и Фиг.5b показано сравнение эффекта, снижающего кровяное давление, единственной и комбинированной терапий у SHR в виде процентов изменения SBP и DBP:
Фиг.5а: проценты изменения SBP и DBP после единственного лечения DM в дозе 1 мг/кг/сутки, единственного лечения AM в дозе 5 мг/кг/сутки и комбинированного лечения DM в дозе 1 мг/кг/сутки и AM в дозе 5 мг/кг/сутки; и
Фиг.5b: проценты изменения SBP и DBP после единственного лечения DM в дозе 5 мг/кг/сутки, единственного лечения AM в дозе 5 мг/кг/сутки и комбинированного лечения DM в дозе 5 мг/кг/сутки и AM в дозе 5 мг/кг/сутки;
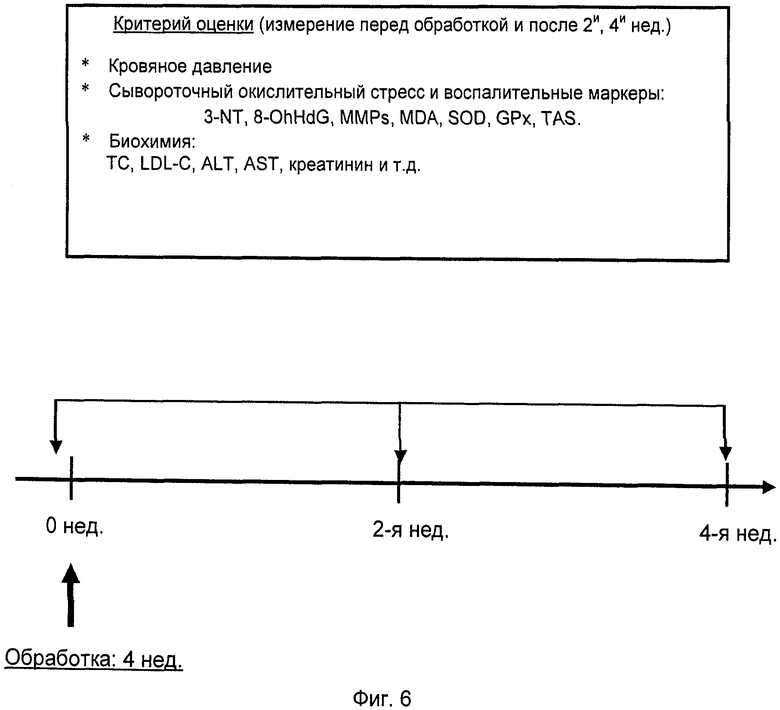
Фиг.6 представляет собой графическое представление, показывающее различные моменты времени, когда измеряли кровяное давление и брали образцы крови в исследовании на животных.
Подробное описание изобретения
Различные публикации, статьи и патенты процитированы или описаны в предшествующем уровне техники и на протяжении всего описания; каждая из этих ссылок полностью включена в данную заявку посредством ссылки. Обсуждение документов, актов, материалов, устройств, статей или тому подобного, которое включено в настоящее описание, предназначено в целях предоставления контекста для настоящего изобретения. Такое обсуждение не является признанием того, что любой или все из этих объектов составляют часть предшествующего уровня техники в отношении каких-либо раскрытых или заявленных изобретений.
Если не указано иное, все технические и научные термины, используемые в данной заявке, имеют такое же значение, которое обычно понятно обычному специалисту в области техники, к которой принадлежит данное изобретение. В других случаях термины, используемые в данной заявке, имеют значения, которые приведены в описании. Все патенты, опубликованные заявки на патенты и публикации, цитируемые в данной заявке, включены посредством ссылки, как если бы полностью были включены в данную заявку. Необходимо отметить, что, как используют в данной заявке и в прилагаемой формуле изобретения, формы единственного числа включают ссылку на множественное число, если контекстом четко не подразумевается другое.
Как используют в данной заявке, название соединения, такого как декстрометорфан или амлодипин, может включать все возможно существующие изомерные формы (например, оптический изомер, энантиомер, диастереомер, рацемат или рацемическую смесь), сложные эфиры, пролекарства, метаболитные формы, фармацевтически приемлемые соли, фармацевтически приемлемые сложные эфиры, фармацевтически приемлемые амиды и защищенные производные этого соединения.
Выражение "фармацевтически приемлемая соль (соли)", как используют в данной заявке, означает те соли интересующего соединения, которые являются безопасными и эффективными для фармацевтического применения у млекопитающих, и которые обладают желаемой биологической активностью. Фармацевтически приемлемые соли включают соли кислотных или основных групп, присутствующих в указанных соединениях. Кислотные или основные группы могут быть органическими или неорганическими. Фармацевтически приемлемые соли присоединения кислоты включают, но не ограничены ими, соли гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, пара-толуолсульфонат и памоат (то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Подходящие соли оснований включают, но не ограничены ими, соли алюминия, кальция, лития, магния, калия, натрия, цинка и диэтаноламина. Некоторые соединения, используемые в настоящем изобретении, могут образовывать фармацевтически приемлемые соли с различными аминокислотами, например, лизином, N,N'-дибензилэтилендиамином, хлорпрокаином, холином, диэтаноламином, этилендиамином, меглумином (N-метилглюкамином), прокаином и трисом, а также другие соли, которые в настоящее время находятся в широко распространенной фармацевтической практике и перечислены в источниках, хорошо известных специалистам в данной области техники, таких как The Merck Index. Любой подходящий компонент может быть выбран для получения соли активного лекарственного средства, обсуждаемого в данной заявке, при условии, что он является нетоксичным и по существу не препятствует желаемой активности. В качестве обзора фармацевтически приемлемых солей см. статью BERGE ЕТ AL, 66 J. PHARM. SCl. 1-19 (1977), включенную в жанную заявку посредством ссылки.
Как используют в данной заявке, "НАДФ-Н оксидазы" представляет собой лекарственное средство или природное вещество, которое ингибирует, уменьшает или сокращает ферментативную активность НАДФ-Н оксидазы, то есть никотинамидадениндинуклеотидфосфат-оксидазы. НАДФ-Н оксидаза генерирует супероксид путем переноса электронов с НАДФ-Н и спаривания электронов с молекулярным кислородом с образованием супероксида, активного свободного радикала, который может генерировать активные формы кислорода (АФК). "Ингибитор НАДФ-Н оксидазы" эффективен при предупреждении, уменьшении или сокращении образования супероксида, а, следовательно, АФК, в кровеносных сосудах субъекта. Примеры ингибиторов НАДФ-Н оксидазы, которые можно использовать в настоящем изобретении, включают, но не ограничены ими,, декстрометорфан, gp91ds-tat, апоцинин, дифенилениодоний, аминоэтилбензолсульфонофторид, S17834, PR39, ингибиторы протеинкиназы С, VAS2870, ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина и статины.
Как используют в данной заявке, "декстрометорфан" или "DM" относится к соединению (+)-3-метокси-17-метил-9α,13α,14α-морфинану, которое также называют (+)-3-метокси-N-метилморфинаном, и к его любой фармацевтически приемлемой соли. Например, декстрометорфан может находиться в форме фармацевтически приемлемой соли, выбранной из группы, состоящей из солей свободных кислот, неорганических кислот, солей сульфата, солей гидрохлорида и солей гидробромида. Декстрометорфан общедоступен в виде моногидрата соли гидробромида.
Декстрометорфан представляет собой правовращающий (d) энантиомер. Предпочтительно фармацевтическая композиция в соответствии с воплощениями настоящего изобретения содержит по существу оптически чистый декстрометорфан или по существу свободна от левовращающего (I) энантиомера DM.
Как используют в данной заявке, "по существу оптически чистый декстрометорфан" или "по существу свободна от левовращающего (I) энантиомера DM" означает, что фармацевтическая композиция содержит более высокую долю или процент DM по отношению к его I энантиомеру. Например, фармацевтическая композиция предпочтительно содержит примерно 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100 масс.% DM, где процентное содержание основано на общей массе DM и его I энантиомера в фармацевтической композиции.
Декстрометорфан может быть синтезирован и оптически очищен с использованием способов, известных в данной области техники, например, как описано в патенте США №2676177, содержание которого включено в данную заявку посредством ссылки. Он также доступен из различных коммерческих источников.
Как используют в данной заявке, "блокаторы кальциевых каналов" или "БКК" относятся к классу лекарственных средств и природных веществ, которые прерывают передачу (Са2+) кальциевыми каналами. Они блокируют потенциалозависимые кальциевые каналы (VGCC) в сердечной мышце и кровеносных сосудах и снижают кровяное давление. Термин "блока-горы кальциевых каналов" включает любой класс БКК, который можно применять для лечения гипертензии у субъекта, такой как класс дигидропиридина, фенилалкиламина, бензотиазепина и неселективных БКК. Примеры ББК, которые можно использовать в настоящем изобретении, включают, но не ограничены ими, амлодипин, бепридил, клентиазем, дилтиазем, фендилин, галлопамил, мибефрадил, прениламин, семотиадил, теродилин, верапамил, аранидипин, барнидипин, бенидипин, цилнидипин, эфонидипин, элгодипин, фелодипин, исрадипин, лацидипин, лерканидипин, манидипин, никардипин, нифедипин, нилвадипин, нимодипин, нисолдипин, нитрендипин, циннаризин, флунаризин, лидофлазин, ломеризин, бенциклан, этафенон, пергексилин и флуспирилен.
Как используют в данной заявке, "амлодипин" или "AM" относится к соединению 3-этил-5-метил-2-[(2-аминоэтокси)метил]-4-(2-хлорфенил)-1,4-дигидро-6-метилпиридин-3,5-дикарбоксилату и к любому его оптическому изомеру, энантиомеру, диастереомеру, рацемату или рацемической смеси, фармацевтически приемлемым солям или фармацевтически приемлемым сложным эфирам этого соединения. Например, амлодипин может находиться в форме фармацевтически приемлемой соли неорганических и органических кислот. Такие кислоты выбраны из группы, состоящей из уксусной, бензолсульфоновой (безилата), бензойной, камфорсульфоновой, лимонной, этенсульфоновой, фумаровой, глюконовой, глутаминовой, бромисто-водородной, соляной, изетионовой, молочной, малеиновой, яблочной, миндальной, метансульфоновой, муциновой, азотной, памовой, пантотеновой, фосфорной, янтарной, серной, винной кислоты, пара-толуолсульфоновой кислоты и тому подобного. Особенно предпочтительны безилат, бромисто-водородная, соляная, фосфорная и серная кислоты. (См. Campbell, S.F. et al., патент США №4806557). Амлодипин может также представлять собой фармацевтически приемлемый сложный эфир амлодипина, в частности, низшие алкиловые эфиры.
Амлодипин является хиральным соединением. Фармацевтическая композиция в соответствии с воплощениями настоящего изобретения может содержать рацемат, то есть смесь 1:1 (R)-(+)- и (S)-(-)-амлодипина, или рацемическую смесь (R)-(+)- и (S)-(-)-амлодипина в различных соотношениях. Фармацевтическая композиция может также содержать изолированный (R)-(+}~ амлодипин или (5)-(-)-амлодипин, который по существу свободен от другого стереоизомера.
(S)-(-)-амлодипин является более эффективным блокатором кальциевых каналов, чем (R)-(+)- амлодипин. Таким образом, предпочтительно фармацевтическая композиция в соответствии с воплощениями настоящего изобретения содержит по существу оптически чистый (S)-(-)-амлодипин или по существу свободна от (R)-(+)-амлодипина.
Как используют в данной заявке, "по существу оптически чистый (S)-(-)-амлодипин" или "по существу свободна от (R)-(+)-амлодипина" означает, что фармацевтическая композиция содержит более высокую долю или процент (S)-(-)" амлодипина по отношению к (R)-(+)-амлодипину. Например, фармацевтическая композиция предпочтительно содержит примерно 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100 масс.% (8)-(-)-амлодипина, где процентное содержание основано на общей массе (R)-(+)-амлодипина и (S)-(-)-амлодипина в фармацевтической композиции.
Химический синтез рацемической смеси амлодипина можно осуществить, используя способы, известные в данной области техники, например, как описано в Arrow/smith, J.E. et al., J. Med. Chem., 29: 1696-1702 (1986). Он также доступен из различных коммерческих источников. Выделение изомеров амлодипина из рацемической смеси можно осуществить способами, известными в данной области техники, такими как проиллюстрированы в патенте США №6448275 или в патенте США №7482464. Содержания этих ссылок включены в данную заявку посредством ссылки.
Как используют в данной заявке, термин "фармацевтическая композиция" подразумевает включение препарата или композиции, содержащей указанный ингредиент в указанном количестве, а также любого препарата, который является результатом, прямо или косвенно, комбинаций указанного ингредиента в указанном количестве.
Как используют в данной заявке, термин "субъект" означает любое животное, предпочтительно млекопитающее, наиболее предпочтительно человека, которому вводят или ввели соединения или фармацевтические композиции в соответствии с воплощениями изобретения. Термин "млекопитающее", как используют в данной заявке, включает любое млекопитающее. Примеры млекопитающих включают, но не ограничены ими, коров, лошадей, овец, свиней, кошек, собак, мышей, крыс, кроликов, морских свинок, обезьян, людей и т.д., более предпочтительно человека. Предпочтительно субъект нуждается в лечении или предупреждении гипертензии и обусловленных ею симптомов, либо является объектом наблюдения или эксперимента по лечению или предупреждению гипертензии и обусловленных ею симптомов.
Как используют в данной заявке, "лечение гипертензии или обусловленного ею симптома" означает вызывать гипотензивный эффект, например, посредством обеспечения нормализации повышенного систолического и/или диастолического артериального давления, и таким путем облегчать один или более чем один возможный симптом или другие гемодинамические эффекты, вызванные повышенным кровяным давлением.
В одном воплощении "лечение" относится к ослаблению, профилактике или купированию заболевания или расстройства или по меньшей мере одного его различимого симптома, например, к лечению гипертензии или обусловленного ею симптома путем снижения повышенного систолического и/или диастолического кровяного давления.
В другом воплощении "лечение" относится к ослаблению, профилактике или купированию по меньшей мере одного измеримого физического параметра, относящегося к заболеванию или расстройству, подлежащему лечению, не обязательно различимого симптома у млекопитающего или млекопитающим, например, к лечению гипертензии или обусловленного ею симптома путем снижения АФК в кровеносных сосудах.
Еще в одном другом воплощении "лечение" относится к ингибированию или замедлению прогрессирования заболевания или расстройства, либо физически, например, стабилизации различимого симптома, либо физиологически, например, стабилизации физического параметра, либо и того, и другого.
Еще в одном другом воплощении "лечение" относится к задержке возникновения заболевания или расстройства или к снижению риска приобретения заболевания или расстройства, такого как гипертензия или обусловленный ею симптом. Например, указанные фармацевтические композиции вводят в качестве превентивной меры субъекту, имеющему предрасположенность к гипертензии, даже если симптомы гипертензии отсутствуют или минимальны.
Как используют в данной заявке, термин "эффективное количество" соединения относится к количеству соединения, которое вызывает биологический или медицинский ответ в тканевой системе, животном или человеке, которого добивается исследователь, ветеринар, врач или другой клиницист, который включает ослабление симптомов заболевания или расстройства, подлежащего лечению. В предпочтительном воплощении эффективное количество соединения является достаточным для лечения, улучшения лечения, профилактического предупреждения гипертензии или обусловленного ею симптома, но недостаточным, чтобы вызвать значительные побочные эффекты, обусловленные введением соединения.
В данной области техники известны способы определения эффективного количества терапевтически активного ингредиента в соответствии с воплощениями настоящего изобретения. Кроме того, обычным специалистам в данной области техники также понятно, что конкретные уровни дозы для каждого конкретного субъекта зависят от ряда факторов, включающих возраст, массу тела, общее состояние здоровья, пол, режим питания, время введения, путь введения, скорость выведения, какие-либо дополнительные терапевтические агенты, вводимые в комбинации с ним, и тяжесть заболевания или состояния, подлежащего лечению. Вообще говоря, ожидают, что профилактическое или терапевтическое лечение идентифицированных выше состояний будет достигнуто посредством введения уровней доз активных ингредиентов в количествах от примерно 0,01 мг/кг до примерно 100 мг/кг, от 0,03 мг/кг до примерно 75 мг/кг, от 0,05 мг/кг до примерно 50 мг/кг массы тела в сутки, или от примерно 0,1 мг/кг до примерно 10 мг/кг массы тела в сутки. Какой бы ни был желательный или подходящий уровень дозировки, ее можно вводить в виде однократной суточной дозы, либо суммарную суточную дозу можно вводить в разделенных дозах два, три или четыре раза в сутки. Альтернативно дозу можно включать в препарат для доставки в виде по существу непрерывной доставки, что можно обеспечить с помощью лекарственных форм пролонгированного и/или контролируемого высвобождения или с помощью чрескожного пластыря.
Термин "побочные эффекты" включает, но не ограничен ими, сердечнососудистые эффекты (включающие тахикардию и сниженную сократимость сердца), отек конечностей, головную боль, умопомрачение, покраснение, утомляемость, головокружение, мышечные судороги, галлюцинации, диарею, лихорадку, задержку мочеиспускания, рвоту, сыпь/зуд тела и т.д.
Теперь обнаружено, что декстрометорфан эффективен для снижения кровяного давления у субъекта, страдающего гипертензией, либо отдельно, либо в комбинации с другим гипотензивным агентом. Кроме того, обнаружено, что декстрометорфан, ингибитор НАДФ-Н оксидазы, и амлодипин, БКК, обладают синергетическим действием при снижении кровяного давления у субъекта, страдающего гипертензией. Данный синергетический эффект является неожиданным. Новые и более эффективные фармацевтические композиции и способы лечения гипертензии или обусловленного ею симптома, таким образом, разработаны на основании настоящих открытий.
В одном общем аспекте настоящее изобретение относится к способу лечения гипертензии или обусловленного ею симптома у субъекта. Этот способ включает введение субъекту фармацевтической композиции, содержащей эффективное количество декстрометорфана и фармацевтически приемлемый носитель.
Любую из фармацевтически приемлемых солей декстрометорфана можно применять в фармацевтических композициях и способах в соответствии с воплощениями настоящего изобретения. В предпочтительном воплощении в настоящем изобретении используют по существу оптически чистый декстрометорфан, такой как по существу оптически чистый декстрометорфана гидробромид.
У большинства пациентов декстрометорфан быстро всасывается из желудочно-кишечного тракта и преобразуется в менее активный метаболит, декстрорфан, в печени ферментом цитохрома Р450 CYP2D6. Ингибирование ферментативной активности CYP2D6 повысило бы стабильность декстрометорфана и продлило его период полувыведения у субъекта, приводя в результате к более эффективному лечению с более постоянным и предсказуемым результатом.
Таким образом, способ в соответствии с воплощением настоящего изобретения может дополнительно включать введение субъекту ингибитора CYP2D6. Примеры ингибиторов CYP2D6, которые можно применять в настоящем изобретении, включают, но не ограничены ими, хинидин. Ингибиторы CYP2D6 можно вводить вместе с DM в одной и той же фармацевтической композиции или отдельно от DM в другой фармацевтической композиции пока режимы дозирования DM и ингибитора CYP2D6 перекрываются по времени таким образом, чтобы вводимый ингибитор CYP2D6 был эффективен для продления периода полувыведения декстрометорфана у субъекта.
В другом общем аспекте воплощения настоящего изобретения относятся к способу лечения гипертензии или обусловленного ею симптома у субъекта, включающему введение субъекту эффективного количества декстрометорфана и эффективного количества блокатора кальциевых каналов (БКК).
Любой из БКК, эффективный для лечения гипертензии у субъекта, можно применять в настоящем изобретении, включая, но не ограничиваясь ими, амлодипин, бепридил, кпентиазем, дилтиазем, фендилин, галлопамил, мибефрадил, прениламин, семотиадил, теродилин, верапамил, аранидипин, барнидипин, бенидипин, цилнидипин, эфонидипин, элгодипин, фелодипин, исрадипин, лацидипин, лерканидипин, манидипин, никардипин, нифедипин, нилвадипин, нимодипин, нисолдипин, нитрендипин, циннаризин, флунаризин, лидофлазин, ломеризин, бенциклан, этафенон, пергексилин и флуспирилен.
В одном воплощении настоящего изобретения БКК представляет собой амлодипин. Любое из оптического изомера, энантиомера, диастереомера, рацемата или рацемической смеси, фармацевтически приемлемых солей или фармацевтически приемлемых сложных эфиров амлодипина можно применять в настоящем изобретении.
В одном воплощении в настоящем изобретении применяют рацемическую смесь амлодипина или (R,S)-амлодипин.
В предпочтительном воплощении в настоящем изобретении применяют по существу оптически чистый (S)-(-)-амлодипин, такой как по существу оптически чистый (S)-(-)-амлодипина безилат, (S)-(-)-амлодипина мезилат или S)-(-)-амлодипина малеат.
В соответствии с воплощениями настоящего изобретения декстрометорфан и БКК можно вводить в одной и той же фармацевтической композиции или отдельно в различных фармацевтических композициях, насколько режимы дозирования DM и БКК перекрываются по времени.
В воплощении настоящего изобретения БКК и DM вводят в соотношении доз BKK:DM, таком как от 1:0,5 до 1:100, например, 1:1, 1:5, 1:10, 1:20, 1:30, 1:40, 1:50, 1:60, 1:70, 1:80, 1:90 или 1:100, в одной и той же фармацевтической композиции, например, в лекарственной форме, содержащей и БКК, и DM, или в отдельных фармацевтических композициях, например, в отдельной лекарственной форме для каждого из БКК и DM.
Другой общий аспект настоящего изобретения относится к фармацевтической композиции для лечения гипертензии или обусловленного ею симптома у субъекта, которая содержит эффективное количество декстрометорфана, эффективное количество блокатора кальциевых каналов и фармацевтически приемлемый носитель.
Воплощения настоящего изобретения также относятся к фармацевтической композиции для лечения гипертензии или обусловленного ею симптома у субъекта, которая содержит эффективное количество блокатора кальциевых каналов, эффективное количество ингибитора НАДФ-Н оксидазы и фармацевтически приемлемый носитель.
Любой из БКК, эффективный для лечения гипертензии у субъекта, такой как описано выше, можно применять в настоящем изобретении.
Примеры ингибитора НАДФ-Н оксидазы, который можно применять в настоящей заявке, включают, но не ограничены ими, gp91ds-tat, апоцинин, дифенилениодоний, аминоэтилбензолсульфонофторид, S17834, PR39, ингибиторы протеинкиназы С, VAS2870, ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина, статины и декстрометорфан.
Фармацевтические композиции в соответствии с воплощениями настоящего изобретения могут, возможно, содержать другие терапевтически активные ингредиенты, такие как другой класс гипотензивных агентов.
Воплощения настоящего изобретения также относятся к способам лечения гипертензии или обусловленного ею симптома у субъекта. Эти способы включают введение субъекту эффективного количества ингибитора НАДФ-Н оксидазы, такого как декстрометорфан, и эффективного количества БКК, такого как амлодипин.
Ингибитор НАДФ-Н оксидазы и БКК можно вводить вместе в одной фармацевтической композиции, отдельно примерно в одно и то же время или отдельно в отдельных режимах дозирования. Все, что необходимо, это, чтобы режимы дозирования ингибитора НАДФ-Н оксидазы и БКК перекрывались по времени и, следовательно, соблюдались одновременно.
Способы в соответствии с воплощениями настоящего изобретения могут, возможно, включать введение субъекту других терапевтически активных ингредиентов, таких как другой класс гипотензивных агентов.
Вводимый отдельно или в комбинации с другим терапевтически активным ингредиентом, терапевтически активный ингредиент можно вводить посредством любого известного пути введения, включая пероральный, местный, парентеральный (включая подкожную, внутривенную, внутримышечную и интрастернальную инъекцию или инфузию), введение посредством ингаляционного спрея или ректальный, в лекарственных формах или фармацевтических композициях, содержащих общепринятые фармацевтически приемлемые носители, и любые такие лекарственные формы или фармацевтические композиции, все вышеуказанное находится в пределах объема настоящего изобретения.
Фармацевтические композиции, адаптированные для перорального введения, включают твердые формы, такие как пилюли, таблетки, капсуловидные таблетки и твердые или мягкие капсулы (где каждая включает препараты быстрого высвобождения, высвобождения по времени и пролонгированного высвобождения), а также пастилки для рассасывания и диспергируемые порошки или гранулы. Жидкие формы фармацевтических композиций, адаптированные для перорального введения, включают растворы, сиропы, эликсиры, эмульсии и водные или масляные суспензии. Любые из этих лекарственных форм можно готовить в соответствии с любым способом или методом компаундирования, известным в данной области техники для получения фармацевтических композиций. Фармацевтически приемлемые носители, которые можно желательно использовать при получении твердых пероральных лекарственных форм, включают инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующие или разрыхляющие агенты, такие как кукурузный крахмал или альгиновая кислота; связующие агенты, такие как крахмал, желатин или аравийская камедь; и смазывающие агенты, такие как стеарат магния, стеариновая кислота или тальк. Если желательно, твердые фармацевтические композиции, адаптированные для перорального введения, могут дополнительно включать один или более чем один подсластитель, корригент, краситель или консервант с целью обеспечения привлекательных или приемлемых на вкус препаратов.
В тех воплощениях, где лекарственная форма представляет собой таблетку или пилюлю, она может быть либо без покрытия, либо с покрытием, и, если содержит покрытие, может быть покрыта любым известным методом. Кроме того, покрытие, если оно желательно представлено, можно готовить или наносить известными методами, так чтобы это покрытие могло замедлить разрыхление таблетки или пилюли и, следовательно, всасывание активного ингредиента, обеспечивая за счет этого лекарственную форму контролируемого и/ог пролонгированного высвобождения, способную обеспечивать пролонгированный терапевтический или профилактический эффект в течение более длительного периода. Например, таблетка или пилюля может содержать внутренний компонент лекарственной формы и внешний компонент лекарственной формы, где последний находится в форме оболочки над первым. Энтеросолюбильный слой, который служит для сопротивления разрыхлению в желудке и дает возможность внутреннему компоненту пройти по существу в интактном виде в двенадцатиперстную кишку или иметь замедленное высвобождение, может разделять два компонента. Разнообразные материалы можно использовать для таких энтеросолюбильных слоев или покрытий, включая ряд полимерных кислот, шеллак, цетиловый спирт и ацетат целлюлозы. Альтернативно в тех воплощениях, где желательно такое контролируемое или пролонгированное высвобождение, таблетки, пилюли или капсулы можно готовить в виде лекарственных форм, представляющих собой осмотический насос, любым известным способом.
Фармацевтические композиции, адаптированные для перорального введения, могут быть также представлены в виде твердых или мягких желатиновых капсул, где активный ингредиент может быть смешан с инертным твердым разбавителем, таким как карбонат кальция, фосфат кальция или каолин, в случае первых, либо с водой или смешиваемыми растворителями, такими как пропиленгликоль, ПЭГи и этанол, либо с масляной средой, такой как арахисовое масло, жидкий парафин или оливковое масло, в случае последних.
Можно готовить водные суспензии, которые содержат активный ингредиент(ы) в смеси с эксципиентами, пригодными для получения водных суспензий. Такие эксципиенты включают суспендирующие агенты, такие как натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь, декстран, поливинилпирролидон или желатин; и диспергирующие или увлажняющие агенты, такие как лецитин, полиоксиэтиленстеарат, гептадекаэтиленоксицетанол, полиоксиэтиленсорбита моноолеат и полиэтиленсорбитана моноолеат. Водные суспензии могут также содержать один или более чем один консервант, такой как этил- или н-пропил-пара-гидроксибензоат; один или более чем один краситель, один или более чем один корригент и один или более чем один подсластитель, такой как сахароза, сахарин или аспартам.
Масляные суспензии можно готовить путем суспендирования активного ингредиента(ов) в растительном масле, таком как хлопковое, оливковое, кунжутное или кокосовое масло, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, такой как пчелиный воск, твердый парафин или цетиловый спирт. Подсластители такие, как описано выше, и корригенты можно добавлять, чтобы обеспечить приемлемый на вкус пероральный препарат. Такие масляные суспензии можно консервировать путем включения антиоксиданта, такого как аскорбиновая кислота.
Диспергируемые порошки и гранулы, пригодные для приготовления водной суспензии, подходящей для перорального введения, могут обеспечивать активный ингредиент(ы) в смеси с диспергирующим или увлажняющим агентом, суспендирующим агентом и одним или более чем одним консервантом, все из которых обсуждены выше. Подсластители, корригенты или красители могут также присутствовать при желании.
Фармацевтические композиции, пригодные для перорального введения, могут быть также представлены в форме эмульсии масло-в-воде. Масляная фаза может представлять собой растительное или минеральное масло, такое как описано выше, или их смеси. Подходящие эмульгирующие агенты могут представлять собой природные фосфатиды, такие как соя, лецитин, сорбитана моноолеат или полиоксиэтиленсорбитана моноолеат. Эмульсии могут также содержать Подсластители или корригенты.
Сиропы и эликсиры можно готовить с подсластителями, например, глицерином, пропиленгликолем, сорбитом или сахарозой. Такие препараты могут также содержать средство, уменьшающее раздражение, консерванты и корригенты или красители.
Фармацевтические композиции могут быть, кроме того, представлены в форме, адаптированной для парентерального введения, то есть путем инъекции или инфузии. Инъекционные водные или масляные суспензии желательно стерильны, и их можно готовить в соответствии с известными способами, используя подходящие диспергирующие, увлажняющие и суспендирующие агенты, которые упомянуты выше. Можно также использовать парентерально приемлемый разбавитель или растворитель, такой как 1,3-бутандиол, вода, раствор Рингера и изотонический хлорид натрия. Можно также использовать сорастворители, такие как этанол, пропиленгликоль или полиэтиленгликоли. Кроме того, стерильные нелетучие масла общепринято используют в качестве растворителей или суспендирующих сред в инъекционных или инфузионных растворах, и они могут включать любое легкое нелетучее масло, такое как любой из синтетических моно- или диглицеридов. Жирные кислоты, такие как олеиновая кислота, также можно использовать при получении инъекционных или инфузионных растворов.
Фармацевтические композиции могут быть также представлены в форме суппозитория. Суппозитории можно готовить путем смешивания активного ингредиента(ов) и любого дополнительного желаемого терапевтического агента(ов) с подходящим не раздражающим эксципиентом, который является твердым при комнатной температуре, но плавится при температуре тела, высвобождая посредством этого активный ингредиент(ы). Подходящие материалы включают масло какао и полиэтиленгликоли.
Для местного применения можно готовить кремы, мази, гели, растворы или суспензии, содержащие активный ингредиент(ы). Как используют в данной заявке, местное применение включает средства для полоскания полости рта и горла. Местные препараты могут включать сорастворители, эмульгаторы, усилители проницаемости, консерванты, смягчающие средства и тому подобное.
Активные ингредиенты в соответствии с воплощениями настоящего изобретения могут быть также представлены в фармацевтической композиции в форме систем липосомной доставки, такой как мелкие однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы можно образовать из разнообразных липидов, включая, но не ограничиваясь ими, амфипатические липиды, такие как фосфатидилхолины, сфингомиелины, фосфатидилэтаноламины, фосфатидилхолины, кардиолипины, фосфатидилсерины, фосфатидилглицерины, фосфатидные кислоты, фосфатидилинозиты, диацилтриметиламмонийпропаны, диацилдиметиламмонийпропаны и стеариламин, нейтральные липиды, такие как триглицериды, и их комбинации. Они могут либо содержать холестерин, либо быть свободными от холестерина.
Предпочтительно фармацевтические композиции в соответствии с воплощениями настоящего изобретения готовят для перорального введения. Фармацевтические композиции могут быть удобно представлены в лекарственной форме, и их готовят любым из способов, известных в области фармации, в свете настоящего описания. Как правило, фармацевтические композиции готовят путем однородного и тщательного смешивания активного ингредиента с жидкими носителями, либо тонкоизмельченными твердыми носителями, либо с обоими носителями, а затем при необходимости формования препарата в желаемом представлении.
Количество терапевтически активных ингредиентов, которое нужно включать в лекарственную форму, зависит от пациента, подлежащего лечению, режима введения и желаемой дозы для доставки. Репрезентативные фармацевтические композиции, как правило, включают от примерно 0,01 мг до примерно 1000 мг, от примерно 0,1 мг до 500 мг, от примерно 1 мг до примерно 100 мг или от примерно 10 мг до примерно 100 мг активных ингредиентов.
В воплощении настоящего изобретения каждая лекарственная форма для перорального введения, такая как пилюля, таблетка, капсуловидная таблетка, твердая или мягкая капсула, содержит от примерно 10 мг до примерно 100 мг ингибитора НАДФ-Н оксидазы, такого как DM. Каждая из лекарственных форм может дополнительно содержать от 10 мг до примерно 100 мг ингибитора CYP2D6, такого как хинидин. Каждая из лекарственных форм может дополнительно содержать от примерно 0,5 мг до примерно 10 мг БКК, такого как AM.
В другом воплощении настоящего изобретения каждая лекарственная форма для перорального введения, такая как пилюля, таблетка, капсуловидная таблетка, твердая или мягкая капсула, содержит соотношение БКК (такого как AM): ингибитор НАДФ-Н оксидазы (такой как DM) от 1:0,5 до 1:100, например, 1:1, 1:5, 1:10, 1:20, 1:30, 1:40, 1:50, 1:60, 1:70, 1:80, 1:90 или 1:100.
В случае, когда применяют пероральную фармацевтическую композицию, подходящий диапазон дозы ингибитора НАДФ-Н оксидазы, такого как декстрометорфан, для применения в настоящем изобретении составляет от примерно 0,1 мг до примерно 500 мг общей суточной дозы, осуществляемой в виде однократного суточного введения утром или в разделенных дозах по потребности. Предпочтительно диапазон дозы от примерно 1 мг до примерно 300 мг дают в виде однократного суточного введения или в разделенных дозах по потребности, и наиболее предпочтительно диапазон дозы от примерно 10 мг до примерно 100 мг или диапазон дозы от примерно 20 мг до примерно 50 мг дают в виде однократного суточного введения или в разделенных дозах по потребности. Дозу пациентов можно титровать с повышением от более низкой дозы до дозы в пределах данного диапазона для удовлетворительного контроля симптомов или кровяного давления, как целесообразно.
В случае, когда применяют пероральную фармацевтическую композицию, подходящий диапазон дозы БКК, такого как амлодипин, для применения в настоящем изобретении составляет от примерно 0,01 мг до примерно 100,0 мг суммарной суточной дозы, даваемой в виде однократного суточного введения утром или в разделенных дозах по потребности. Предпочтительно диапазон дозы от примерно 0,5 мг до примерно 20,0 мг дают в виде однократного суточного введения или в разделенных дозах по потребности, и наиболее предпочтительно диапазон дозы от примерно 0,5 мг до примерно 10,0 мг дают в виде однократного суточного введения или в разделенных дозах по потребности. Дозу пациентов можно титровать с повышением от более низкой дозы до дозы в пределах данного диапазона для удовлетворительного контроля симптомов или кровяного давления, как целесообразно.
Данное изобретение станет лучше понятно путем ссылки на нижеследующий не ограничивающий пример, но специалистам в данной области техники понятно, что этот пример является только иллюстративным для изобретения, которое описано более полно в формуле изобретения, которая следует после него.
Пример 1
Исследование на животных монотерапии и комбинированной терапии декстрометорфаном и амлодипином
Было проведено исследование in vivo для измерения и сравнения гипотензивной эффективности и переносимости декстрометорфана и амлодипина в виде монотерапии и комбинированной терапии у спонтанно гипертензивных крыс, животной модели гипертензии. Такое же исследование может быть проведено с другим ингибитором НАДФ-Н оксидазы и БКК.
Материалы и методы
Животные
Исследование согласовано с Руководством по содержанию и использованию лабораторных животных, опубликованным Национальными институтами здравоохранения США (NIH Publications no. 85-23, revised 1996) и соблюдены современные законы Военного госпиталя тайпейских ветеранов. В данном исследовании использовали 18-недельных самцов крыс линии Вистар-Киото (WKY) с нормальным кровяным давлением и спонтанно гипертензивных крыс (SHR).
Необработанных WKY и SHR сравнивали с SHR, обработанными амлодипином (1, 5 мг/кг/сутки) или декстрометорфаном (1, 5, 25 мг/кг/сутки) и комбинацией установленных доз (AM+DM), используя матричную комбинацию вышеуказанных доз в течение 4 недель. Все группы обработки перечислены в таблице 1, включая G1-G12 для SHR и GO для WKY в качестве контроля.
Обработка: DO: без лекарственного средства; D1:1 мг/кг/сутки; D2: 5 мг/кг/сутки и D3: 25 мг/кг/сутки декстрометорфана.
Схема эксперимента
Как указано выше в таблице 1, крыс делили на несколько подопытных групп, как описано ниже:
GO: WKY в качестве контроля (крысы с нормальным кровяным давлением без лекарственных средств, n=10)
G1: SHR (гипертензивные крысы без лекарственных средств, n=10)
G2: SHR+D1 (DM 1 мг/кг/сутки, n=10)
G3: SHR+D2 (DM 5 мг/кг/сутки, n=10)
G4: SHR+D3 (DM 25 мг/кг/сутки, n=10)
G5: SHR+А1 (AM 1 мг/кг/сутки, n=10)
G6: SHR+А1+D1 (AM 1 мг/кг/сутки +DM 1 мг/кг/сутки, n=10)
G7: SHR+А1+D2 (AM 1 мг/кг/сутки +DM 5 мг/кг/сутки, n=10)
G8: SHR+А1+D3 (AM 1 мг/кг/сутки +DM 25 мг/кг/сутки, n=10)
G9: SHR+A2 (AM 5 мг/кг/сутки, n=10)
G10: SHR+A2+D1 (AM 5 мг/кг/сутки +DM 1 мг/кг/сутки, n=10)
G11: SHR+A2+D2 (AM 5 мг/кг/сутки +DM 5 мг/кг/сутки, n=10)
G12: SHR+A2+D3 (AM 1 мг/кг/сутки +DM 25 мг/кг/сутки, n=10)
Контрольные крысы (G0 и G1) получали 1% раствор метилцеллюлозы (1 мл/кг) через зонд в качестве носителя. AM и DM суспендировали в 1% растворе метилцеллюлозы и вводили через зонд в объеме 1 мл/кг. Все соединения вводили в течение 4 недель. Измерение артериального кровяного давления и взятие образцов крови осуществляли перед обработкой и после второй и четвертой недели введения лекарственного средства.
Определение кровяного давления
Артериальное кровяное давление измеряли у крыс в сознании автоматическим сфигмоманометром, используя способ непрямого измерения с помощью хвостовой манжеты. Перед измерениями животных помещали в камеру с подогревом (примерно 34°С) на 30 мин. Цель этой процедуры состояла в том, чтобы успокоить животных и расширить кровеносные сосуды хвоста. Артериальное кровяное давление измеряли по меньшей мере три раза для каждого животного. Изменения давления выражены в виде процента от базовых значений.
Биохимия
Общий холестерин, ЛПВП-холестерин, ALT (аланин-аминотрансфераза), AST (аспартат-аминотрансфераза) и креатинин измеряют путем использования автоматических биохимических анализаторов (Spotchem TM SP 4410 Kyoto Daiichi Kagaku Co. Ltd.).
Сывороточный окислительный стресс и воспалительные маркеры
Оксидантные системы включают ферменты, такие как супероксиддисмутаза, каталаза и глутатионинпероксидаза, макромолекулы, такие как альбумин, церулоплазмин и ферритин, малые молекулы, такие как аскорбиновая кислота, α-токоферол, β-каротин, восстановленный глутионин, мочевая кислота и билирубин. Сумма эндогенных антиоксидантов и антиоксидантов пищевого происхождения представляет собой общую антиоксидантную активность системы. Общая антиоксидантная способность или общий антиоксидантный статус (ОАС, ммоль/л) плазмы, сыворотки, мочи, слюны или клеточных лизатов можно измерить, используя имеющиеся в продаже наборы, такие как Antioxidant Assay Kit (№ по каталогу 709001, Cayman) или Total Antioxidant Status, Randox Lab Ltd), где результаты выражены в виде ммоль/л, следуя протоколу набора.
Кроме того, также оценивают сывороточный пероксинитрат (3-нитротирозин, 3-NT), 8-гидроксидезоксигуанозин (8-OHdG), эндотелин-1 (ЕТ-1), активности супероксиддисмутазы (SOD) и глутатионпероксидазы (GPx) (МЕ/г Hb).
Нитротирозин образуется в присутствии активного метаболита NO. Различные биохимические пути, включающие образование пероксинитрита, ведут к образованию нитротирозина. Поскольку нитротирозин является стабильным конечным продуктом окисления пероксинитрита, оценка его концентрации в плазме может быть полезна в качестве маркера NO-зависимого повреждения in vivo. Присутствие нитротирозина обнаружено при различных воспалительных процессах, включая атерокслеротические бляшки, глютеновую болезнь, ревматоидный артрит, хроническую почечную недостаточность и септический шок. Нитротирозин также идентифицирован в качестве маркера воспаления. В норме в плазме присутствуют низкие, не обнаружимые уровни нитротирозина. Количественное определение нитротирозина в плазме и в других биологических образцах можно осуществлять, используя имеющиеся в продаже наборы, такие как набор Нитротирозин ИФА (Hycult Biotech, HK501)
8-OHdG образуется в результате окислительного повреждения ДНК активными молекулами кислорода и азота и служит в качестве установленного маркера окислительного стресса. Повышенный 8-OH-dG ассоциирован как с гипертензией, так и с процессом старения и рядом других состояний, таких как рак и диабет. Количественное определение 8-OHdG в плазме и в других биологических образцах можно осуществлять, используя имеющиеся в продаже наборы, такие как набор 8-hydroxy-2-deoxy Guanosine EIA (Cayman, № по каталогу 589320 или 589321).
Эндотелин-1 (ЕТ-1), пептид из 21 аминокислотного остатка, является наиболее эффективным известным веществом-вазоконстриктором. Показано, что ЕТ-1 обладает сильными эффектами на гладкомышечные клетки, фибробласты, и вовлечен во многие болезненные процессы, в частности, сердечно-сосудистые заболевания. Показано, что он важен при застойной сердечной недостаточности, почечной недостаточности и легочной гипертензии. Количественное определение ЕТ-1 в плазме и в других биологических образцах можно осуществлять, используя имеющиеся в продаже наборы, такие как аналитический набор Endothelin-1 Assay Kit(L) (IBL, код №27165).
3-NT, 8-OhdG, ЕТ-1 можно также измерять в двух повторах с имеющимися в продаже наборами для твердофазного иммуноферментного анализа (Quantikine, R&D Systems, USA) в соответствии с инструкциями изготовителя.
Эти анализы основаны на формате двухточечного сэндвич-анализа ИФА с использованием двух антител, направленных против различных эпитопов ММР. 96-луночный микропланшет предварительно покрывают антителом к ММР. Образцы плазмы добавляют в микропланшет, и обнаружение осуществляют путем добавления антитела, конъюгированного с пероксидазой хрена. Затем используют субстрат тетраметилбензидин (ТМВ). Реакцию пероксид-ТМВ останавливают добавлением серной кислоты, и полученное в результате окрашивание измеряют при 450 нм в спектрофотометре для микропланшетов. Таким образом, 100 мкл образцы анализируют в двух повторах с рабочими стандартами и измеряют на считывающем устройстве для микропланшетов (Asys-Hitech, Austria). После построения стандартной кривой определяют значения образцов, используя считывающее устройство для микропланшетов с программным обеспечением (версия 3-1, Asys-Hitech, Austria).
Активности SOD и GPx, выраженные в виде МЕ/г Hb, оценивают, используя имеющиеся в продаже наборы (Ransod и Ransel, соответственно, от фирмы Randox Lab Ltd, Crumlin, UK).
Продукты перекисного окисления липидов, а именно малондиальдегид (MDA), оценивают с помощью анализа с использованием тиобарбитуровой кислоты (ТВА). Аналитическая смесь состоит из 0,1 мл сыворотки, 0,4 мл 0,9% NaCl, 0,5 мл 3% додецилсульфата натрия (ДСН) и 3 мл реагента ТВА (содержащего равные части 0,8% водной ТВА и уксусной кислоты); смесь нагревают в течение 75 минут при 95°С, а затем добавляют 1 мл холодного 0,9% NaCl и экстрагируют 5 мл м-бутанола. После центрифугирования при 730 г в течение 15 минут при 4°С органическую фазу анализируют спектрофотометрическим путем при 532 нм, используя 1,1,3,3-тетраметоксипропан в качестве внешнего стандарта. Результаты выражают в мкмоль/л MDA. Временные моменты измерения
Артериальное кровяное давление и взятые образцы крови измеряют перед обработкой и после второй и четвертой недели введения лекарственного средства (фиг.6).
Статистический анализ
Результаты выражают в виде среднего ±СО (стандартное отклонение). Нормальность распределения проверяли с помощью критерия Колмогорова-Смирнова и критерия Лиллиефорса. Статистическое оценивание осуществляли, используя анализ вариансы (ANOVA), и апостериорные сравнения проводили с помощью критерия минимальных значимых различий (LSD). Если данные не соответствовали нормальному распределению, статистическое оценивание проводили путем использования ANOVA (критерия Краскала-Уоллиса) и Li-критерия Вилкоксона - Манна - Уитни. Различия считали значимыми, когда р составляло менее 0,05.
В таблице 2 приведены измерения кровяного давления контрольных групп, то есть WKY и SHR, измеренные до и после того, как крысам давали контрольную обработку (1% раствор метилцеллюлозы). Как показано в таблице 2, измерения кровяного давления в целом оставались одинаковыми в двух точках измерения.
Таблица 2. Измерения кровяного давления контрольных групп
Как показано на фиг.1a-d, обработка одним DM при всех трех различных уровнях дозировки, 1 мг/кг/сутки, 5 мг/кг/сутки и 25 мг/кг/сутки, приводила в результате к снижению кровяного давления у SHR. Однако четкой зависимости ответа от дозы не наблюдали.
Как показано на фиг.2a-d, обработка одним AM при двух различных уровнях дозировки, 1 мг/кг/сутки и 5 мг/кг/сутки, также приводила в результате к снижению кровяного давления у SHR. Эффект снижения кровяного давления более выражен при более высокой дозе обработки AM.
Как показано на фиг.3а-d, комбинированная обработка DM и AM при различных уровнях дозировки резко улучшала эффекты снижения кровяного давления каждого из DM и AM.
Как более четко проиллюстрировано на фиг.4a-4d и фиг.5а и 5b, эффект снижения кровяного давления DM и AM, в частности, измеренный по систолическому кровяному давлению (SBP), выше, чем аддитивный эффект одного из DM и AM по отдельности. Это указывает на то, что DM и AM действуют синергетическим путем при снижении кровяного давления.
Пример 2
Исследование эндотелий-зависимой вазорелаксации
Механизм эффекта снижения кровяного давления декстрометорфана или его синергетического действия с блокатором кальциевых каналов при лечении гипертензии изучают путем исследования эндотелий-зависимой вазорелаксации, в котором измеряют изометрическое натяжение аортального кольца крысы в ответ на лекарственные средства. В частности, эффект тестирования лекарственного средства, например, декстрометорфана, амлодипина или комбинации декстрометорфана и амлодипина на сокращения, индуцированные высокой концентрацией KCl, исследуют, например, путем измерения кумулятивных кривых концентрация-ответ на эндотелий-зависимые и эндотелий-независимые агонисты релаксантов ацетилхолин (ACh) и нитропруссид натрия (SNP), соответственно, или на агонист 1-рецептора фенилэфрин (РЕ).
Получение препарата аортального кольца
Крыс анестезируют пентобарбиталом (60 мг·кг-1 массы тела интраперитонеально), нисходящую грудную аорту вырезают, режут на небольшие кольца (3-5 мм в ширину) и суспендируют в 5 мл инкубаторе органов, содержащем нормальный физиологический солевой раствор Кребса (KPSS) приведенной ниже композиции (мМ): NaCl 118,2, KCl 4,7, CaCl2.2H2O 2,5, KH2PO4 1,2, MgCl2 1,2, глюкоза 11,7, NaHCO3 25,0 и ЭДТА 0,026. Инкубационный раствор непрерывно газируют 95% кислородом и 5% диоксидом углерода при 37°С (рН 7,4).
Изометрическое натяжение (г) измеряют, используя позиционный датчик силы, соединенный с регистрирующей системой Mac Lab (ADI Instruments, Australia). Затем аортальные кольца постепенно вытягивают до оптимального базового натяжения 1 г и дают возможность уравновешивания в течение 45 мин. В течение этого периода инкубационный раствор заменяют каждые 15 и при необходимости базовый тон повторно регулируют до 1 г.
Затем аортальные кольца повторно стимулируют раствором KCl (высокий К+, 80 мМ) в течение 5 мин через 10-мин интервалы до получения двух последовательных одинаковых сокращений, свидетельства тканевой стабильности.
Фармакологические исследования
После вымывания ответов на высокий К+ аортальные кольца инкубируют в течение 20 мин с тестируемым лекарственным средством, например, с декстрометорфаном, амлодипином или комбинацией декстрометорфана и амлодипина, либо с его носителем (контроль), а затем измеряют кумулятивные кривые концентрация-ответ на эндотелий-зависимые и эндотелий-независимые агонисты релаксантов ацетилхолин (ACh, 10-10-10-5 М) и нитропруссид натрия (SNP, 10-11-10-6 М), соответственно, или на агонист 1-рецептора фенилэфрин (РЕ, 10-10-10-5 М). Для тестирования релаксационных ответов на ACh и SNP кольца предварительно приводят в контакт с РЕ (1 мкМ).
Концентрации тестируемого лекарственного средства выбраны на основании физиологически достижимых концентраций в плазме лекарственного средства. В экспериментах по характеристике механизмов, вовлеченных в эффекты тестируемых лекарственных средств, аортальные кольца подвергают воздействию различных фармакологических агентов в течение 5 мин перед инкубацией с лекарственным средством или с его носителем.
Где указано, эндотелий удаляют осторожным стиранием поверхности интимы кровеносного сосуда тупыми ножницами. Эндотелий считают эффективно удаленным, если ACh (1 мкМ) вызывал менее 10% релаксации аортальных колец, предварительно приведенных в контакт с РЕ.
Для исследования возможной роли релаксантных биохимических путей оксида азота, простациклина и циклического ГМФ в эффектах тестируемого лекарственного средства измеряют кривые концентрация-ответ на ACh в аортальных кольцах, инкубируемых в постоянном присутствии метилового эфира N-нитро-1-аргинина (L-NAME, 10 мкМ), ингибитором eNO, индометацина (10 мкМ), ингибитора циклооксигеназы, и метиленового синего (10 мкМ), ингибитора циклического ГМФ, соответственно.
Для исследования вклада эндотелиального фактора гиперполяризации (EDHF) или калиевых (К+) каналов в эффекты тестируемого лекарственного средства аортальные кольца частично деполяризуют возрастающей концентрацией KCl в KPSS (4,8-20 мМ), а затем строят кривые концентрация-ответ на ACh.
Статистический анализ
Сократительные ответы аортальных колец на плавно меняющиеся концентрации РЕ выражают в виде процентов максимального сократительного эффекта высокого К"*" в соответствующих тканях.
Вазодилататорный эффект возрастающих концентраций ACh или SNP выражают в виде процента снижения пика сокращения РЕ (10-6 М).
Строят кривую концентрация-ответ для каждого экспериментального условия, и на ее основании выводят значения максимального сокращения (Стах) или максимальной релаксации (Rmax) и концентрации тестируемого лекарственного средства (выражено в отрицательных логарифмах моль), дающей 50% зарегистрированного максимального сокращения или релаксации (рЕС50) (Prism версия 2.0, программное обеспечение GraphPad, USA).
Специалистам в данной области техники понятно, что в вышеописанных воплощениях могут быть проведены изменения без отклонения от их широкой изобретательской концепции. Поэтому понятно, что данное изобретение не ограничено конкретными раскрытыми воплощениями, но подразумевает включение модификаций в пределах сущности и объема настоящего изобретения, которые определены прилагаемой формулой изобретения.
Ссылки
1. Kearney PM, Whelton M, Reynolds К, et al. Global burden of hypertension: Analysis of worldwide data. Lancet. 2005; 365: 217-223.
2. Ong KL, Cheung BM, Man YB, et al. Prevalence, awareness, treatment, and control of hypertension among United States adults 1999-2004. Hypertension. 2007: 49: 69-75.
3. Ezzati M, Lopez AD, Rodgers A, et al, for the Comparative Risk Assessment Collaborating Group. Selected major risk factors and global and regional burden of disease. Lancet. 2002: 360: 1347-1360.
4. O'Connor PJ. Improving medication adherence: Challenges for physicians, payers, and policy makers. Arch Intern Med. 2006; 166: 1802-1804.
5. Nelson MR, Reid CM, Ryan P, et al. Self-reported adherence with medication and cardiovascular disease outcomes in the Second Australian National Blood Pressure Study (ANBP2). Med J Aust. 2006; 185: 487-489.
6. Mounier-Vehier С, Bernaud С, Cart6 A, et al. Compliance and antihypertensive efficacy of amlodipine compared with nifedipine slow-release. Am J Hypertens. 1998; 11: 478-486.
7. Chobanian AV, Bakris GL, Black HR, et al, for the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure; the National Heart, Lung, and Blood Institute; and the National High Blood Pressure Education Program Coordinating Committee. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension 2003; 42: 1206-1252.
8. Mancia G, De BackerG, Dominiczak A, et al, for the Task Force for the Management of Arterial Hypertension of the European Society of Hypertension and the European Society of Cardiology. 2007 Guidelines for the management of arterial hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). Eur Heart J. 2007; 28: 1462-1536.
9. Staessen JA, Fagard R, Thijs L, et al, for the Systolic Hypertension in Europe (Syst-Eur) Trial Investigators. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. Lancet. 1997; 350: 757-764.
10. Liu L, WangJG, Gong L, et al, for the Systolic Hypertension in China (Syst-China) Collaborative Group. Comparison of active treatment and placebo in older Chinese patients with isolated systolic hypertension. J Hypergens. 1998; 16: 1823-1829.
11. Brown M J, Palmer CR, Castaigne A, et al. Morbidity and mortality in patients randomised to doubleblind treatment with a long-acting calcium-channel blocker or diuretic in the International Nifedipine GITS study: Intervention as a Goal in Hypertension Treatment (INSIGHT) [published correction appears in Lancet. 2000: 356: 514]. Lancet. 2000; 356: 366-372.
12. Hansson L, Zanchetti A, Carruthers SG, et al, for the HOTStudy Group. Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: Principal results of the Hypertension Optimal Treatment (HOT) randomized trial. Lancet. 1998: 351: 1755-1762.
13. The ALLAHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high-risk hypertensive patients randomized to angiotensinconverting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-LoweringTreatment to Prevent Heart AttackTrial (ALLHAT). JAMA. 2002; 288: 2981-2997.
14. Dahlof В, Sever PS, Poulter NR, et al, for the ASCOT Investigators. Prevention of cardiovascular events with an antihypertensive regimen of amiodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): A multicentre randomised controlled trial. Lancet. 2005; 366: 895-906.
15. Packer M, O'Connor CM, Ghali JK, et al, for the Prospective Randomized Amiodipine Survival Evaluation Study Group. Effect of amiodipine on morbidity and mortality in severe chronic heart failure. N EnglJ Med 1996; 335: 1107-1114.
16. Julius S, Kjeldsen SE, Weber M, et al, for the VALUE Trial Group. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amiodipine: The VALUE randomized trial. Lancet. 2004; 363: 2022-2031.
17. Tortella FC, Pellicano M, and Bowery NG (1989) Dextromethorphan and neuromodulation: old drug coughs up new activities. Trends Pharmacol Sci 10: 501-507.
18. George CP, Goldberg MP, Choi DW, and Steinberg GK (1988) Dextromethorphan reduces neocortical ischemic neuronal damage in vivo. Brain Res 440: 375-379.
19. Monyer H and Choi DW (1988) Morphinans attenuate cortical neuronal injury induced by glucose deprivation in vitro. Brain Res 446: 144-148.
20. Prince DA and Feeser HR (1988) Dextromethorphan protects against cerebral infarction in a rat model of hypoxia-ischemia. Neurosci Lett 85: 291-296.
21. Steinberg GK, George CP, DeLaPaz R, Shibata DK, and Gross Т (1988) Dextromethorphan protects against cerebral injury following transient focal ischemia in rabbits. Stroke 19: 1112-1118.
22. Britton P, Lu XC, Laskosky MS, and Tortella FC (1997) Dextromethorphan protects against cerebral injury following transient, but not permanent, focal ischemia in rats. Life Sci 60: 1729-1740.
23. Tortella FC, Britton P, Williams A, Lu XC, and Newman AH (1999) Neuroprotection (focal ischemia) and neurotoxicity (electroencephalographic) studies in rats with AHN649, a 3-amino analog of dextromethorphan and low-affinity N-methyl-Daspartate antagonist. J Pharmacol Exp Ther 291: 399-408.
24. Wei Zhang, Tongguang Wang, Liya Qin, Hui-Ming Gao, Belinda Wilson, Syed F, Ali, Wanqin Zhang, Jau-Shyong Hong, And Bin Liu(2004). Neuroprotective effect of dextromethorphan in the MPTP Parkinson's disease model: role of НАДФН oxidasel. FASEB 18: 589-591.
25. Y Alvarez, AM Briones, R Hernanz, JV Pe'rez-Giro'n, MJ Alonso and M Salaices (2008). Role of NADPH oxidase and iNOS in vasoconstrictor responses of vessels from hypertensive and normotensive rats. British Journal of Pharmacology 153, 926-935.
Настоящая группа изобретений относится к медицине, а именно к терапии и кардиологии, и касается лечения гипертензии. Для этого вводят декстрометорфан в комбинации с другим гипотензивным агентом - амлодипином. Такое сочетанное введение обеспечивает эффективное лечение гипертензии при снижении побочных эффектов за счет синергетического действия этих лекарственных препаратов. 2 н. и 7 з.п. ф-лы, 2 пр., 2 табл., 6 ил.
1. Применение декстрометорфана для получения лекарственной формы для лечения гипертензии у субъекта, где лекарственная форма дополнительно включает блокатор кальциевых каналов, представляющий собой амлодипин.
2. Применение по п.1, где лекарственная форма дополнительно включает ингибитор CYP2D6.
3. Фармацевтическая композиция для лечения гипертензии у субъекта, включающая эффективное количество декстрометорфана, эффективное количество блокатора кальциевых каналов и фармацевтически приемлемый носитель, где блокатор кальциевых каналов представляет собой амлодипин.
4. Фармацевтическая композиция по п.3, содержащая от 0,1 мг до 500 мг декстрометорфана и от 0,01 мг до 100 мг амлодипина на лекарственную форму.
5. Фармацевтическая композиция по п.3, содержащая от 10 мг до 100 мг декстрометорфана и от 0,5 мг до 20 мг амлодипина на лекарственную форму.
6. Фармацевтическая композиция по п.3, где амлодипин представляет собой оптически чистый S-(-)-амлодипин.
7. Фармацевтическая композиция по п.3, где амлодипин представляет собой (R, S)-амлодипин.
8. Фармацевтическая композиция по п.3, характеризующаяся соотношением амлодипин : декстрометорфан от 1:0,5 до 1:100.
9. Фармацевтическая композиция по любому из пп.3-8, дополнительно включающая ингибитор CYP2D6.
| RU2005104418 А 27.10.2006 | |||
| КОМПОЗИЦИИ НЕСТЕРОИДНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРОТИВОЗАСТОЙНЫХ СРЕДСТВ И АНТИГИСТАМИНОВ | 2003 |
|
RU2322262C2 |
| US 2005107415 A1 19.05.2005 | |||
| US 2008039484 A1 19.05.2005 | |||
| WO 2007097765 A1 30.08.2007 | |||
| ШТРЫГОЛЬ С.Ю | |||
| "Блокаторы кальциевых каналов в кардиологии" | |||
| Провизор, 2004, вып.6, найдено из Интернет:http://www.provisor.com.ua/archive/2004/#6/art_12.php | |||
| GOJANOVIC B et al | |||
| "Concomitant calcium entry | |||
Авторы
Даты
2015-12-20—Публикация
2011-04-29—Подача