УРОВЕНЬ ТЕХНИКИ
Документально доказано наличие симбиоза между грамотрицательными почвенными бактериями, Rhizobiaceae и Bradyrhizobiaceae, и бобовыми растениями, такими как соя. Биохимическая основа этих взаимосвязей включает обмен молекулярными сигналами, причем соединения, передающие сигналы от растений к бактериям, включают флавоны, изофлавоны и флаваноны, и соединения, передающие сигналы от бактерий к растениям, включают конечные продукты экспрессии брадиризобиальных и ризобиальных генов nod, известных как липохитоолигосахариды (ЛХО). Симбиоз между этими бактериями и бобовыми растениями позволяет бобовым растениям связывать атмосферный азот, необходимый для роста растений, и тем самым устранять необходимость в азотных удобрениях. Поскольку азотные удобрения могут значительно повысить стоимость сельскохозяйственных культур и сопровождаются целым рядом загрязняющих воздействий, в сельском хозяйстве продолжаются исследования по использованию этой биологической взаимосвязи и разработке новых средств и способов улучшения урожайности растений без увеличения использования удобрений на основе азота.
В патенте U.S. 6979664 описан способ улучшения прорастания семян или появления ростков сельскохозяйственных культур, включающий стадии приготовления композиции, которая включает эффективное количество по меньшей мере одного липохитоолигосахарида и сельскохозяйственно подходящего носителя, и внесения композиции в непосредственной близости от семян или ростков в количестве, эффективном для улучшения прорастания семян или появления ростков по сравнению с необработанными семенами или ростками.
Дальнейшее развитие этого подхода представлено в WO 2005/062899, относящейся к комбинациям по меньшей мере одного индуктора растения, а именно ЛХО, в комбинации с фунгицидом, инсектицидом или их комбинацией для улучшения таких характеристик растения, как густота стояния, рост, мощность и/или урожайность растения. Указано, что композиции и способы применимы для бобовых и небобовых растений и могут использоваться для обработки семян (непосредственно перед посевом), ростков, корней или растений.
Аналогичным образом в WO 2008/085958 описаны композиции для усиления роста растений и повышения урожайности культур бобовых и небобовых растений, которые содержат ЛХО в комбинации с другим активным средством, таким как хитин или хитозан, флавоноид или гербицид, и которые можно наносить на семена и/или растения одновременно или последовательно. Как и в случае публикации WO 2005/062899, в публикации WO 2008/085958 описана обработка семян непосредственно перед посевом.
Недавно Halford, "Smoke Signals" в Chem. Eng. News (April 12, 2010) на стр. 37-38 сообщили, что каррикины или бутенолиды, которые содержатся в дыме, после лесного пожара действуют, как стимуляторы роста и активаторы прорастания семян и могут активировать семена, такие как семена кукурузы, томатов, латука и лука, которые находились на хранении. Эти молекулы являются объектом патента U.S. 7576213.
Однако все еще сохраняется необходимость в системах для улучшения или усиления роста растений.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Первым объектом настоящего изобретения является способ усиления роста растений кукурузы, включающий a) обработку (например, нанесение) семян кукурузы или растения кукурузы, которое прорастает из семян, эффективным количеством по меньшей мере одного хитоолигосахарида (ХО), где после уборки растение кукурузы характеризуется по меньшей мере одним из следующих: увеличенной урожайностью растений, измеренной в единицах бушель/акр, увеличенным количеством корней, увеличенной длиной корней, увеличенной массой корней, увеличенным объемом корней и увеличенной площадью листвы по сравнению с необработанными растениями кукурузы или растениями, выросшими из необработанных семян кукурузы.
В некоторых вариантах осуществления используют по меньшей мере два ХО. В некоторых вариантах осуществления обработка семян кукурузы включает непосредственное нанесение по меньшей мере одного ХО на семена кукурузы, которые затем можно высеять или хранить в течение некоторого времени до высевания. Обработка семян кукурузы может включать непрямую обработку, например, путем внесения по меньшей мере одного ХО в почву (которое известно в данной области техники как внесение в борозды). В других вариантах осуществления по меньшей мере один ХО можно нанести на растения кукурузы, которые прорастают из семян, например, путем некорневого опрыскивания. Методики дополнительно могут включать применение других агрономически полезных агентов, таких как питательные микроэлементы, жирные кислоты и их производные, сигнальные молекулы растений (кроме ХО), такие как липохитоолигосахариды, хитиновые соединения (кроме ХО), флавоноиды, жасмоновая кислота и ее производные, линолевая кислота и ее производные, линоленовая кислота и ее производные и каррикины и их производные, гербициды, фунгициды и инсектициды и солюбилизирующие фосфат микроорганизмы.
Как показывают рабочие примеры, в которых обобщаются данные экспериментов, проведенных в теплицах и в поле, результаты, полученные способами, предлагаемыми в настоящем изобретении, показывают, что нанесение по меньшей мере одного ХО на семена кукурузы или растения кукурузы, которые прорастают из семян, приводит к усиленному росту растений. Эти результаты представляются неожиданными, в особенности с учетом точки зрения, согласно которой ХО участвуют в системной приобретенной устойчивости (СПО), но необязательно участвуют в непосредственном усилении роста растений. Результаты, описанные в настоящем изобретении, показывают, что в некоторых случаях способы, предлагаемые в настоящем изобретении, приводят по существу к такому же эффекту или, в некоторых других случаях, приводят к более значительному усилению роста растений, чем обеспечиваемый с помощью ЛХО. В этом отношении особенно важны результаты, полученные с помощью экспериментов в теплицах, поскольку они проведены при условиях, когда практически отсутствуют болезни.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1a и 2a приведены химические структуры хитоолигосахаридов (ХО), применимых при практическом осуществлении настоящего изобретения.
На фиг. 1b и 2b приведены химические структуры липохитоолигосахаридов (ЛХО), которые соответствуют ХО, приведенным на фиг. 1a и 2a, и которые также применимы при практическом осуществлении настоящего изобретения.
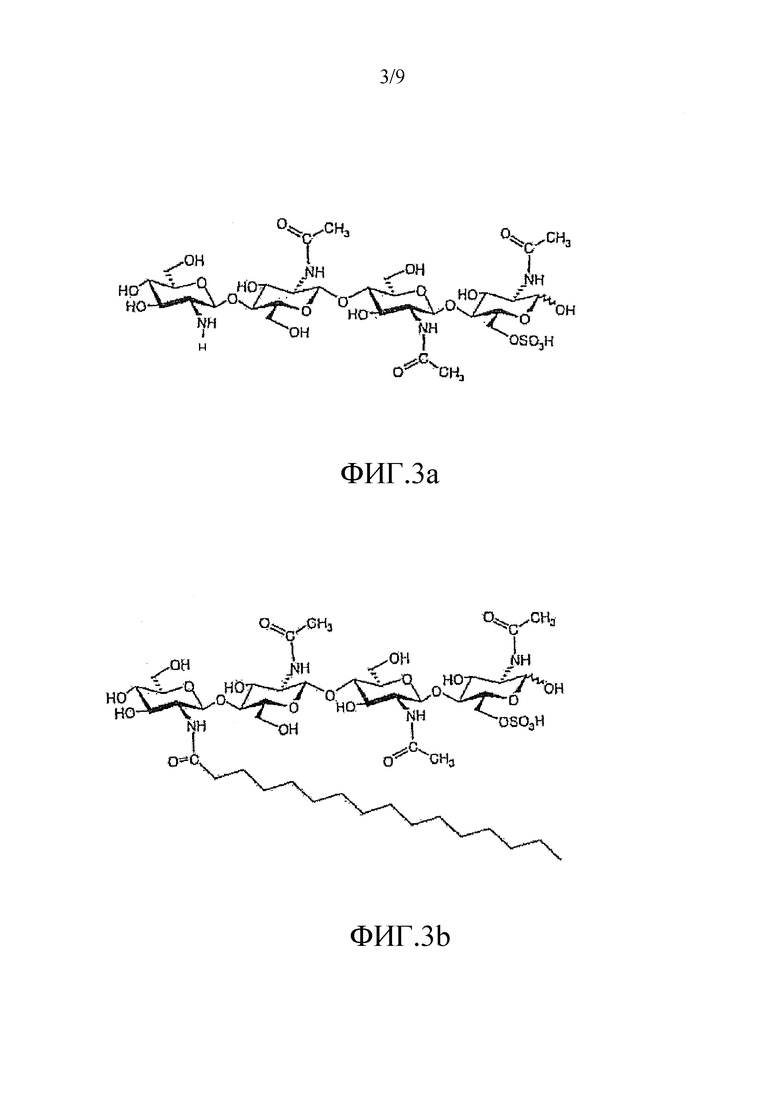
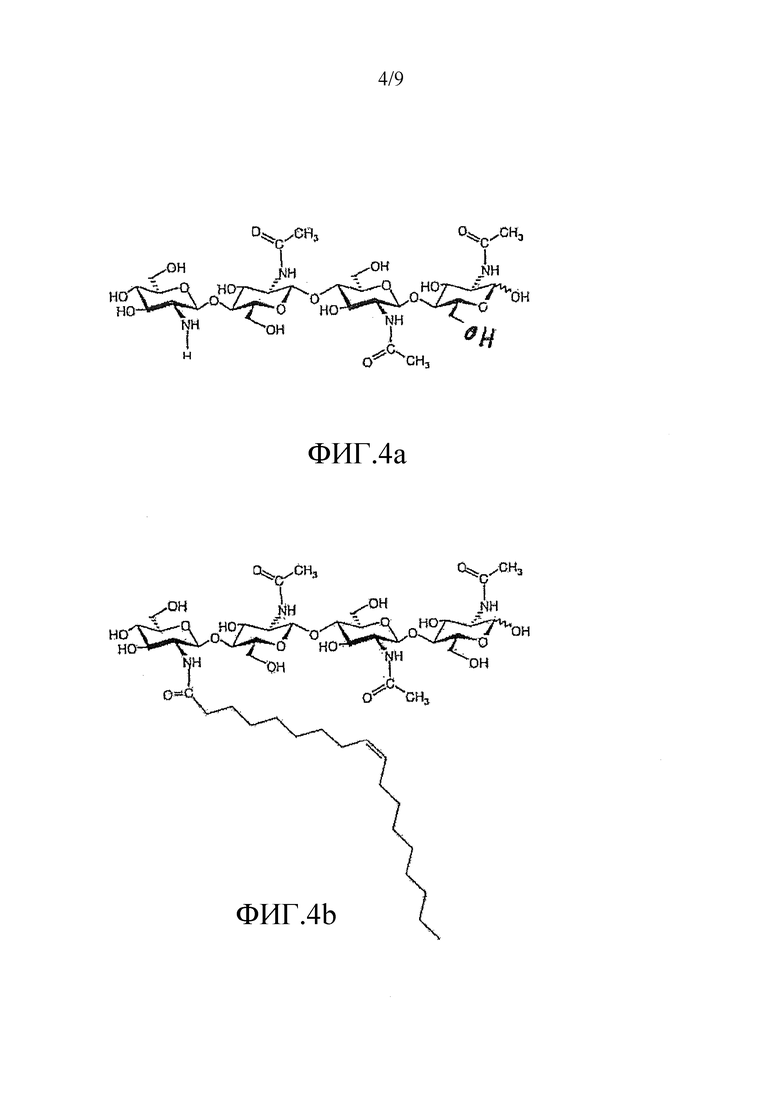
На фиг. 3a и 4a приведены химические структуры других ХО, применимых при практическом осуществлении настоящего изобретения.
На фиг. 3b и 4b приведены химические структуры Myc-факторов, которые соответствуют ХО, приведенным на фиг. 3a и 3b, и которые также применимы при практическом осуществлении настоящего изобретения.
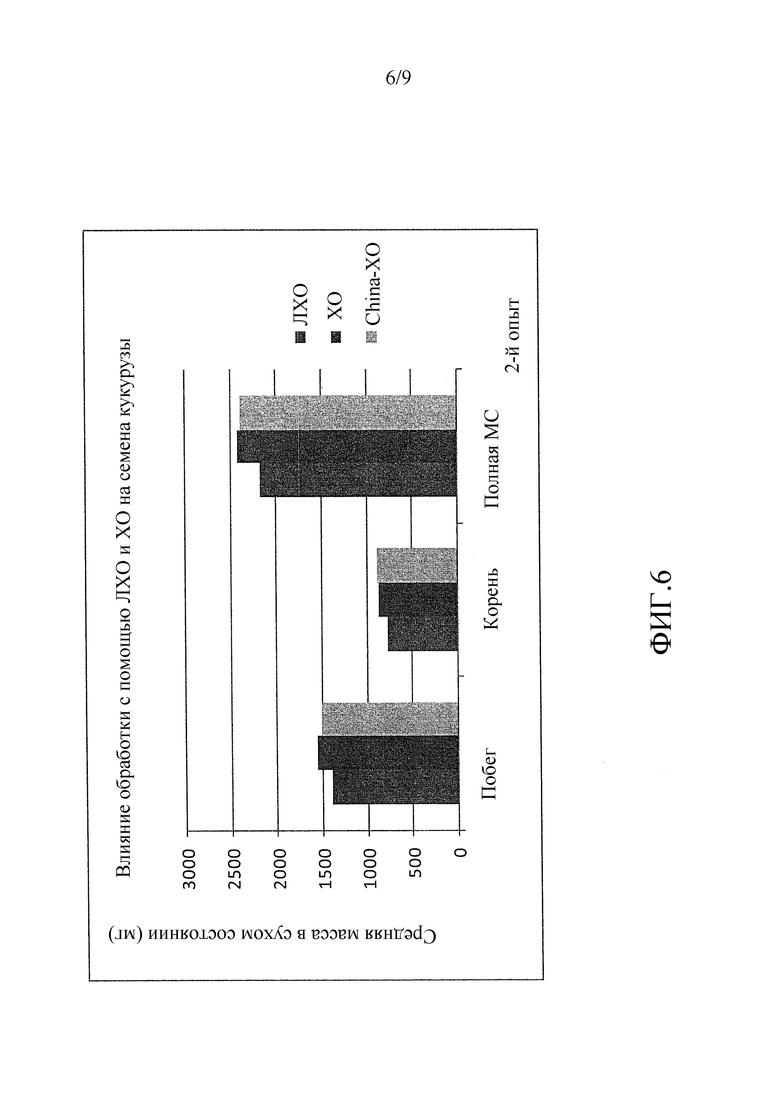
На фиг. 5 (эксперимент 1) и 6 (эксперимент 2) приведены столбцовые диаграммы, которые иллюстрируют влияние ХО, представленного на фиг. 2a, по сравнению с ЛХО, представленным на фиг. 2b, и смеси (не предлагаемых в настоящем изобретении) хитиновых соединений, выработанных с помощью хитиназы, при обработке семян кукурузы, выраженное с помощью средней массы в сухом состоянии побегов, корней и полной массы в сухом состоянии (суммарной массы в сухом состоянии побегов и корней).
На фиг. 7 приведена секторная диаграмма, которая иллюстрирует влияние ХО, представленного на фиг. 2a, по отдельности или в комбинации с одной из двух разных жирных кислот, по сравнению с ЛХО, представленным на фиг. 2b, и водой при обработке семян кукурузы, выраженное с помощью степени прорастания семян в процентах.
На фиг. 8 приведена диаграмма, которая иллюстрирует влияние ХО, представленного на фиг. 2a, по отдельности или в комбинации с одной из двух разных жирных кислот, по сравнению с ЛХО, представленным на фиг. 2b, каждой из жирных кислот по отдельности и контролем при обработке семян кукурузы, выраженное с помощью степени прорастания семян в процентах.
На фиг. 9 приведена столбцовая диаграмма, которая иллюстрирует влияние ХО, представленного на фиг. 2a, по отдельности или в комбинации с ЛХО, представленным на фиг. 2b, по сравнению с ЛХО, представленным на фиг. 2b, и водой при обработке семян кукурузы, выраженное с помощью средней массы растения в сухом состоянии.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Хитоолигосахариды
ХО известны в данной области техники как β-1-4-связанные N-ацетилглюкозаминовые структуры, идентифицированные как олигомеры хитина, также как N-ацетилхитоолигосахариды. ХО обладают особыми и различными структурами боковых цепей, которые делают их отличными от молекул хитина [(C8H13NO5)n, CAS No. 1398-61-4] и молекул хитозана [(C5H11NO4)n, CAS No. 9012-76-4]. См., например, Hamel, et al., Planta 232:787-806 (2010)(например, фиг. 1, на которой представлены структуры хитина, хитозана, Nod-факторов (ЛХО) и соответствующих ХО (в котором отсутствуют 18C, 16C или 20C ацильные группы)). ХО, предлагаемые в настоящем изобретении, также относительно хорошо растворимы в воде по сравнению с хитином и хитозаном и в некоторых вариантах осуществления, описанных ниже в настоящем изобретении, являются пентамерными. Типичной литературой, в которой описаны структура и получение ХО, которые могут быть подходящими для применения в настоящем изобретении, является следующая: Muller, et al., Plant Physiol. 124:733-9 (2000)(например, фиг. 1 в этой публикации); Van der Holst, et al., Current Opinion in Structural Biology, 11:608-616 (2001)(например, фиг. 1 в этой публикации); Robina, et al., Tetrahedron 58:521-530 (2002); D'Haeze, et al., Glycobiol. 12(6):79R-105R (2002); Rouge, et al. Chapter 27, "The Molecular Immunology of Complex Carbohydrates" в Advances in Experimental Medicine and Biology, Springer Science; Wan, et al., Plant Cell 21:1053-69 (2009); PCT/F100/00803 (9/21/2000); и Demont-Caulet, et al., Plant Physiol. 120(1):83-92 (1999).
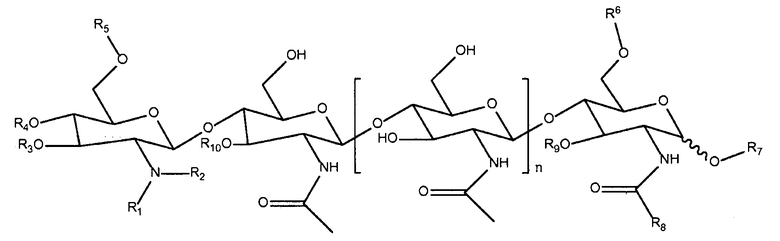
ХО по структуре отличаются от ЛХО в основном тем, что в них отсутствует боковая группа жирной кислоты. Образующиеся из микориза ХО и отсутствующие в природе их синтетические производные, которые можно использовать при практическом осуществлении настоящего изобретения, можно представить следующей формулой:
 ,
,
в которой R1 и R2 каждый независимо означает водород или метил; R3 означает водород, ацетил или карбамоил; R4 означает водород, ацетил или карбамоил; R5 означает водород, ацетил или карбамоил; R6 означает водород, арабинозил, фукозил, ацетил, сульфат, 3-О-S-2-О-MeFuc, 2-О-MeFuc и 4-О-AcFuc; R7 означает водород, маннозил или глицерин; R8 означает водород, метил или -CH2OH; R9 означает водород, арабинозил или фукозил; R10 означает водород, ацетил или фукозил; и n равно 0, 1, 2 или 3. Структуры соответствующих ризобиальных ЛХО описаны в публикации D'Haeze, et al., см. выше.
Два ХО, подходящие для применения в настоящем изобретении, представлены на фиг. 1a и 2a. Они соответствуют ЛХО, вырабатывающимся Bradyrhizobium japonicum и Rhizobium leguminosarum biovar viciae соответственно, которые симбиотически взаимодействуют с соей и горохом соответственно, но в них отсутствуют боковые цепи жирных кислот. Соответствующие ЛХО, вырабатывающиеся этими микоризами (и которые также применимы при практическом осуществлении настоящего изобретения), представлены на фиг. 1b и 2b.
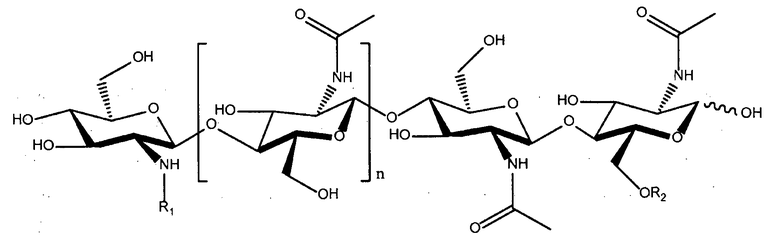
Структуры других ХО, которые могут быть подходящими для применения при практическом осуществлении настоящего изобретения, легко образовать из ЛХО, полученных (т.е. выделенных и/или очищенных) из микоризных грибов, таких как грибы группы Glomerocycota, например, Glomus intraradices. См., например, WO 2010/049751 и Maillet, et al., Nature 469:58-63 (2011) (описанные в ней ЛХО также называют "Myc-факторами"). Типичные ХО, образованные из микоризных грибов, описываются следующей структурой:
 ,
,
в которой n=1 или 2; R1 означает водород или метил; и R2 означает водород или SO3H. Два других ХО, подходящие для применения в настоящем изобретении, один из которых сульфатирован и другой не сульфатирован, представлены на фиг. 3a и 4a соответственно. Они соответствуют двум разным ЛХО, вырабатывающимся микоризными грибами Glomas intraradices, которые представлены на фиг. 3b и 4b (и которые также применимы при практическом осуществлении настоящего изобретения).
ХО могут быть синтетическими или рекомбинантными. Способы получения синтетических ХО описаны, например, в публикации Robina, см. выше. Способы получения рекомбинантных ХО, например, с использованием E. coli в качестве хозяина, известны в данной области техники. См., например, Dumon, et al., ChemBioChem 7:359-65 (2006), Samain, et al., Carbohydrate Res. 302:35-42 (1997); Cottaz, et al., Met. Eng. 7(4):311-7 (2005) и Samain, et al., J. Biotechnol. 72:33-47 (1999)(например, фиг. 1 в этой публикации, на котором представлены структуры ХО, которые можно образовать рекомбинантно в E. coli, содержащих различные комбинации генов nodBCHL). Для задач настоящего изобретения по меньшей мере один ХО структурно отличается от хитинов, хитозанов и других хитоолигосахаридов, получаемых ферментативным путем с использованием хитина в качестве исходного вещества.
Для задач настоящего изобретения в вариантах осуществления, в которых по меньшей мере один ХО является рекомбинантным, по меньшей мере один рекомбинантный ХО обладает чистотой, составляющей не менее 60%, например чистотой, составляющей не менее 60%, чистотой, составляющей не менее 65%, чистотой, составляющей не менее 70%, чистотой, составляющей не менее 75%, чистотой, составляющей не менее 80%, чистотой, составляющей не менее 85%, чистотой, составляющей не менее 90%, чистотой, составляющей не менее 91%, чистотой, составляющей не менее 92%, чистотой, составляющей не менее 93%, чистотой, составляющей не менее 94%, чистотой, составляющей не менее 95%, чистотой, составляющей не менее 96%, чистотой, составляющей не менее 97%, чистотой, составляющей не менее 98%, чистотой, составляющей не менее 99%, вплоть до чистоты, составляющей 100%.
Семена кукурузы можно обработать по меньшей мере одним ХО по различным методикам, таким как распыление или разбрызгивания. Обработку распылением и разбрызгиванием можно проводить путем приготовления эффективного количества по меньшей мере одного ХО в сельскохозяйственно приемлемом носителе, обычно водном по природе, и распыления или разбрызгивания композиции на семена с помощью непрерывной системы для обработки (которую калибруют для нанесения обрабатывающего средства с заранее заданной скоростью в соответствии с непрерывным потоком семян), такой как протравливатель барабанного типа. В этих методиках предпочтительно используются относительно небольшие объемы носителя, чтобы обеспечить относительно быструю сушку обработанных семян, таким образом можно эффективно обработать большие объемы семян. Также можно использовать системы периодического действия, в которых в смеситель подаются заранее заданные количества семян и композиций сигнальных молекул. Системы и аппаратуру для проведения такой обработки продают многочисленные поставщики, например Bayer CropScience (Gustafson).
В другом варианте осуществления обработка включает нанесение на семена кукурузы покрытия по меньшей мере из одного ХО. Одна такая методика включает нанесение композиции на внутреннюю стенку круглого контейнера, добавление семян и последующее вращение контейнера, так чтобы семена соприкасались со стенкой и композицией, эта методика известна в данной области техники, как "контейнерное нанесение покрытия". Наносить покрытия на семена с помощью комбинации методик нанесения покрытий. Замачивание обычно включает использование водного раствора, содержащего средство для усиления роста растений. Например, семена можно замачивать в течение от примерно 1 мин до примерно 24 ч (например, в течение не менее 1 мин, 5 мин, 10 мин, 20 мин, 40 мин, 80 мин, 3 ч, 6 ч, 12 ч, 24 ч). Некоторые типы семян (например, семена сои) чувствительны к влаге. Тогда замачивание таких семян в течение длительного периода времени может быть нежелательным и в этом случае замачивание обычно проводят в течение от примерно 1 мин до примерно 20 мин.
В тех вариантах осуществления, которые включают хранение семян кукурузы после нанесения по меньшей мере одного ХО, адгезия ХО к семенам в течение любой части времени хранения не является критически важной. Если не ограничиваться какой-либо конкретной теорией, то заявители полагают, что, несмотря на то, что обработка может не обеспечить соприкосновение сигнальной молекулы растения с поверхностью семени после обработки и в течение любой части времени хранения, ХО может оказать предназначенное воздействие вследствие явления, известного как память семян, или восприятие семян. См. Macchiavelli, et al., J. Exp. Bot. 55(408):1635-40 (2004). Заявители также полагают, что после обработки ХО диффундирует по направлению к молодому развивающемуся корешку и активирует гены, связанные с симбиозом и развитием, что приводит к изменению структуры корней растения. Тем не менее, композиции, содержащие ХО, могут дополнительно содержать желательное количество агента, придающего липкость или образующего покрытие. По эстетическим соображениям композиции могут дополнительно содержать образующий покрытие полимер и/или краситель.
Количество по меньшей мере одного ХО эффективно для усиления роста, так что после уборки растение кукурузы характеризуется по меньшей мере одним из следующих: увеличенной урожайностью растений, измеренной в единицах бушель/акр, увеличенным количеством корней, увеличенной длиной корней, увеличенной массой корней, увеличенным объемом корней и увеличенной площадью листвы по сравнению с необработанными растениями кукурузы или растениями кукурузы, выросшими из необработанных семян кукурузы (любым активным веществом). Эффективное количество по меньшей мере одного ХО, использующегося для обработки семян кукурузы, выраженное в единицах концентрации, обычно находится в диапазоне от примерно 10-5 до примерно 10-14 M (молярная концентрация) и в некоторых вариантах осуществления от примерно 10-5 до примерно 10-11 M, и в некоторых других вариантах осуществления от примерно 10-7 до примерно 10-8 M. Выраженное в единицах массы эффективное количество обычно находится в диапазоне от примерно 1 до примерно 400 мкг/центнер (ц) семян и в некоторых вариантах осуществления от примерно 2 до примерно 70 мкг/ц, и в некоторых других вариантах осуществления от примерно 2,5 до примерно 3,0 мкг/ц семян.
Для непрямой обработки семян кукурузы, т.е. обработки внесением в борозды, эффективное количество по меньшей мере одного ХО обычно находится в диапазоне от примерно 1 мкг/акр до примерно 70 мкг/акр, и в некоторых вариантах осуществления от примерно 50 мкг/акр до примерно 60 мкг/акр. Для нанесения на растения эффективное количество ХО обычно находится в диапазоне от примерно 1 мкг/акр до примерно 30 мкг/акр, и в некоторых вариантах осуществления от примерно 11 мкг/акр до примерно 20 мкг/акр.
Семена кукурузы можно обработать по меньшей мере одним ХО непосредственно перед высеванием или во время высевания. Обработка по время высевания может включать прямое нанесение на семена, как это описано выше, или в некоторых других вариантах осуществления путем внесения активных веществ в почву, известного в данной области техники как обработка внесением в борозды. В тех вариантах осуществления, которые включают обработку семян после хранения, после этого семена можно упаковать, например, в 50-фунтовые или 100-фунтовые мешки, или большие мешки, или контейнеры в соответствии со стандартными методиками. Семена можно хранить в течение не менее 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев и даже дольше, например в течение 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 месяцев или даже дольше при подходящих условиях хранения, которые известны в данной области техники.
Другие агрономически полезные агенты
Настоящее изобретение может дополнительно включать обработку семян кукурузы или растений кукурузы, которые прорастают из семян, по меньшей мере одним сельскохозяйственно/агрономически полезным агентом. При использовании в настоящем изобретении и в данной области техники термин "сельскохозяйственно или агрономически полезный" означает агенты, которые при нанесении на семена кукурузы или растения кукурузы приводят к улучшению (которое может быть статистически значимым) характеристик растения кукурузы, таких как густота стояния растений, рост (например, как это определено в связи с ХО) или мощность, по сравнению с необработанными семенами кукурузы или растениями кукурузы. Эти агенты можно приготовить вместе по меньшей мере с одним ХО или нанести на семена или растения с помощью отдельного состава. Типичные примеры таких агентов, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают питательные микроэлементы (например, витамины и микроэлементы), жирные кислоты и их производные, сигнальные молекулы растений (кроме ХО), гербициды, фунгициды и инсектициды, солюбилизирующие фосфат микроорганизмы.
Питательные микроэлементы
Типичные витамины, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают пантотенат кальция, фолиевую кислоту, биотин и витамин C. Типичные примеры микроэлементов, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают бор, хлор, марганец, железо, цинк, медь, молибден, никель, селен и натрий.
Количество по меньшей мере одного питательного микроэлемента, использующееся для обработки семян кукурузы, выраженное в единицах концентрации, обычно находится в диапазоне от 10 част./млн до 100 част./млн, и в некоторых вариантах осуществления от примерно 2 част./млн до примерно 100 част./млн. Выраженное в единицах массы эффективное количество в одном варианте осуществления обычно находится в диапазоне от примерно 180 мкг до примерно 9 мг/центнер (ц) семян, и в некоторых вариантах осуществления при некорневом внесении от примерно 4 мкг до примерно 200 мкг/растение. Другими словами, при обработке семян эффективное количество по меньшей мере одного питательного микроэлемента обычно находится в диапазоне от 30 мкг/акр до примерно 1,5 мг/акр и в некоторых вариантах осуществления при некорневом внесении от примерно 120 мг/акр до примерно 6 г/акр.
Жирные кислоты
Типичные жирные кислоты, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают жирные кислоты, которые являются заместителями в природных ЛХО, такие как стеариновая и пальмитиновая кислоты. Другие жирные кислоты, которые можно использовать, включают насыщенные C12-C18 жирные кислоты, которые (кроме стеариновой и пальмитиновой кислот) включают лауриновую кислоту и миристиновую кислоту, и ненасыщенные C12-C18 жирные кислоты, такие как миристоленовую кислоту, пальмитоленовую кислоту, сапиеновую кислоту, олеиновую кислоту, элаидиновую кислоту, вакценовую кислоту, линолевую кислоту, линоленовую кислоту и линоэлаидиновую кислоту. Линолевая кислота и линоленовая кислота образуются при биосинтезе жасмоновой кислоты (которая, как это описано ниже, также является агрономически полезным агентом для задач настоящего изобретения). Сообщают, что линолевая кислота и линолевая кислота (и их производные) являются индукторами экспрессии гена nod или продуцирования ЛХО ризобактериями. См., например, Mabood, Fazli, "Linoleic and linolenic acid induce the expression of nod genes in Bradyrhizobium japonicum," USDA 3, May 17, 2001.
Полезные производные жирных кислот, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают эфиры, амиды, гликозиды и соли. Типичными эфирами являются соединения, в которых карбоксигруппа жирной кислоты, например линолевой кислоты и линоленовой кислоты, заменена группой --COR, в которой R означает группу --OR1, в которой R1 означает: алкильную группу, такую как неразветвленная или разветвленная C1-C8 алкильная группа, например метильная, этильная или пропильная группа; алкенильную группу, такую как неразветвленная или разветвленная C2-C8 алкенильная группа; алкинильную группу, такую как неразветвленная или разветвленная C2-C8 алкинильная группа; арильную группу, содержащую, например, от 6 до 10 атомов углерода; или гетероарильную группу, содержащую, например, от 4 до 9 атомов углерода, где геетроатомами в гетероарильной группе могут быть, например, N, O, P или S. Типичными амидами являются соединения, в которых карбоксигруппа жирной кислоты, например линолевой кислоты и линоленовой кислоты, заменена группой --COR, в которой R означает группу NR2R3, в которой R2 и R3 независимо означают: водород; алкильную группу, такую как неразветвленная или разветвленная C1-C8 алкильная группа, например метильная, этильная или пропильная группа; алкенильную группу, такую как неразветвленная или разветвленная C2-C8 алкенильная группа; алкинильную группу, такую как неразветвленная или разветвленная C2-C8 алкинильная группа; арильную группу, содержащую, например, от 6 до 10 атомов углерода; или гетероарильную группу, содержащую, например, от 4 до 9 атомов углерода, где геетроатомами в гетероарильной группе могут быть, например, N, O, P или S. Сложные эфиры можно получить по известным методикам, таким как катализируемое кислотой нуклеофильное присоединение, при котором карбоновая кислота взаимодействует со спиртом в присутствии каталитического количества неорганической кислоты. Амиды также можно получить по известным методикам, например по реакции карбоновой кислоты с соответствующим амином в присутствии реагента сочетания, такого как дициклогексилкарбодиимид (ДЦК), в нейтральной среде. Подходящие соли жирных кислот, например линолевой кислоты и линоленовой кислоты, включают, например, соли присоединения с основаниями. Основания, которые можно использовать в качестве реагентов для получения метаболически приемлемых солей этих соединений с основаниями, включают образованные из катионов, таких как катионы щелочных металлов (например, калия и натрия) и катионы щелочноземельных металлов (например, кальция и магния). Эти соли можно легко получить смешиванием раствора жирной кислоты с раствором основания. Соль можно осадить из раствора и собрать фильтрованием или можно извлечь другими средствами, такими как выпаривание растворителя.
Количества жирной кислоты или ее производного, использующегося для обработки семян кукурузы или растений кукурузы, обычно составляют от примерно 10% до примерно 30% и в некоторых вариантах осуществления примерно 25% в пересчете на количество по меньшей мере одного ХО.
Сигнальные молекулы растений
Настоящее изобретение также может включать обработку семян кукурузы или растения кукурузы сигнальной молекулой растения, не представляющей собой ХО. Для задач настоящего изобретения термин "сигнальная молекула растения", который можно использовать взаимозаменяемым образом с термином "средство для усиления роста растений", в широком смысле означает любой агент, в природе содержащийся в растениях или микробах, и синтетический (и который может быть не находящимся в природе), который прямо или косвенно активирует биохимический путь растения, что приводит к усиленному росту растений кукурузы, который можно измерить с помощью по меньшей мере одного из следующих: увеличенной урожайности растений, измеренной в единицах бушель/акр, увеличенного количества корней, увеличенной длины корней, увеличенной массы корней, увеличенного объема корней и увеличенной площади листвы по сравнению с необработанными растениями кукурузы или растениями кукурузы, выросшими из необработанных семян кукурузы. Типичные примеры сигнальных молекул растений, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают липохитоолигосахариды, хитиновые соединения (кроме ХО), флавоноиды, жасмоновую кислоту, линолевую кислоту и линоленовую кислоту и их производные (см. выше) и каррикины и их производные.
Липохитоолигосахариды (ЛХО), также известные в данной области техники, как симбиотические Nod-сигналы или Nod-факторы, состоят из олигосахаридной главной цепи β-1,4-связанных N-ацетил-D-глюкозаминовых ("GIcNAc") остатков с присоединенной к атому N жирной ацильной цепью, сконденсированной на невосстанавливающем конце. ЛХО различаются по количеству остатков GIcNAc в главной цепи, по длине и степени насыщенности жирной ацильной цепи и степени замещения восстанавливающими и невосстанавливающими сахарными остатками. См., например, Denarie, et al., Ann. Rev. Biochem. 65:503-35 (1996), Hamel, et al., см. выше, Prome, et al., Pure & Appl. Chem. 70(1):55-60 (1998). Пример ЛХО приведен ниже в виде формулы I
 ,
,
в которой:
G означает гексозамин, который может быть замещен, например, ацетильной группой по атому азота, сульфатной группой, ацетильной группой и/или простой эфирной группой по атому кислорода,
R1, R2, R3, R5, R6 и R7, которые могут быть одинаковыми или разными, означают H, CH3 CO--, Cx Hy CO--, где x является целым числом, равным от 0 до 17, и y является целым числом, равным от 1 и 35, или любую другую ацильную группу, например карбамоил,
R4 означает моно-, ди- или триненасыщенную алифатическую цепь, содержащую по меньшей мере 12 атомов углерода, и n является целым числом, равным от 1 и 4.
ЛХО можно получить (выделить и/или очистить) из бактерий, таких как Rhizobia, например Rhizobium sp., Bradyrhizobium sp., Sinorhizobium sp. и Azorhizobium sp. Структура ЛХО характеристична для каждого такого вида бактерий и каждый штамм может продуцировать множество ЛХО, обладающих разными структурами. Например, конкретные ЛХО из S. meliloti также были описаны в патенте U.S. 5549718 как обладающие формулой II:
 ,
,
в которой R означает H или CH3 CO-- и n равно 2 или 3.
Еще более специфические ЛХО включают NodRM, NodRM-1, NodRM-3. В случае ацетилирования (R=CH3 CO--) они превращаются в AcNodRM-1 и AcNodRM-3 соответственно (патент U.S. 5545718).
ЛХО из Bradyrhizobium japonicum описаны в патентах U.S. 5175149 и 5321011. В широком смысле они являются пентасахаридными фитогормонами, содержащими метилфукозу. Описан целый ряд этих образованных из B. japonicum ЛХО: BjNod-V (C18:1); BjNod-V (Aс, C18:1), BjNod-V (C16:1); и BjNod-V (Aс, C16:0), где "V" указывает на наличие пяти N-ацетилглюкозаминов; "Ac" на ацетилирование; число после "C" указывает количество атомов углерода в боковой цепи жирной кислоты; и число после ":" количество двойных связей.
ЛХО, использующиеся в вариантах осуществления настоящего изобретения, можно получить (т.е. выделить и/или очистить) из штаммов бактерий, которые продуцируют ЛХО, таких как штаммы Azorhizobium, Bradyrhizobium (включая B. japonicum), Mesorhizobium, Rhizobium (включая R. leguminosarum), Sinorhizobium (включая S. meliloti), и штаммов бактерий, которым с помощью генной инженерии придана способность продуцировать ЛХО.
ЛХО являются первичными детерминантами специфичности по отношению к хозяину в симбиозе бобовых (Diaz, et al., Mol. Plant-Microbe Interactions 13:268-276 (2000)). Таким образом, в семействе бобовых специфические роды и виды микоризы образуют симбиотическую связывающую азот взаимосвязь со специфическим бобовым-хозяином. Эти комбинации растение-хозяин/бактерии описаны в публикации Hungria, et al., Soil Biol. Biochem. 29:819-830 (1997). Примеры этого симбиотического партнерства бактерии/бобовые включают S. meliloti/люцерна и донник белый; R. leguminosarum biovar viciae/горох и чечевица; R. leguminosarum biovar phaseoli/фасоль; Bradyrhizobium japonicum/соя; и R. leguminosarum biovar trifolii/красный клевер. В публикации Hungria также перечислены эффективные индукторы флавоноидного гена Nod ризобиальных видов и специфические структуры ЛХО, которые продуцируются различными ризобиальными видами. Однако специфичность ЛХО необходима только для образования образование клубеньков в бобовых растений. При практическом осуществлении настоящего изобретения применение данного ЛХО не ограничивается обработкой семян его симбиотического бобового партнера для обеспечения повышенной урожайности растения, измеренной в единицах бушель/акр, увеличенного количества корней, увеличенной длины корней, увеличенной массы корней, увеличенного объема корней и увеличенной площади листвы по сравнению с растениями, выросшими из необработанных семян, или по сравнению с растениями, выросшими из семян, обработанных сигнальными молекулами непосредственно перед высеванием или в течение недели или меньшего количества времени после высевания.
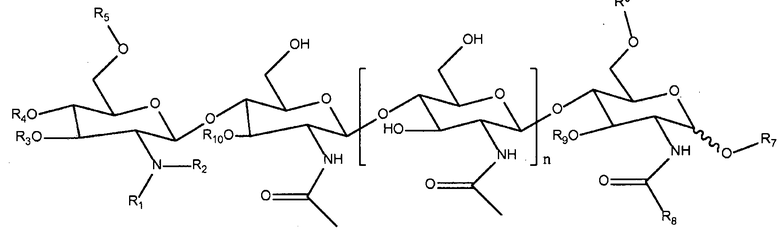
Таким образом, в качестве дополнительных примеров, ЛХО и не встречающиеся в природе их синтетические производные, которые можно использовать при практическом осуществлении настоящего изобретения, описываются следующей формулой:
 ,
,
в которой R1 означает C14:0, 3OH-C14:0, изо-C15:0, C16:0, 3-OH-C16:0, изо-C15:0, C16:1, C16:2, C16:3, изо-C17:0, изо-C17:1, C18:0, 3OH-C18:0, C18:0/3-OH, C18:1, OH-C18:1, C18:2, C18:3, C18:4, C19:1 карбамоил, C20:0, C20:1, 3-OH-C20:1, C20:1/3-OH, C20:2, C20:3, C22:1 и C18-26(ω-1)-OH (которые в соответствии с публикацией D′Haeze, et al., см. выше, включают C18, C20, C22, C24 и C26 гидроксилированные соединения и C16:1Δ9, C16:2 (Δ2,9) и C16:3 (Δ2,4,9)); R2 означает водород или метил; R3 означает водород, ацетил или карбамоил; R4 означает водород, ацетил или карбамоил; R5 означает водород, ацетил или карбамоил; R6 означает водород, арабинозил, фукозил, ацетил, сульфат, 3-О-S-2-О-MeFuc, 2-О-MeFuc и 4-О-AcFuc; R7 означает водород, маннозил или глицерин; R8 означает водород, метил или -CH2OH; R9 означает водород, арабинозил или фукозил; R10 означает водород, ацетил или фукозил; и n равно 0, 1, 2 или 3. Структуры природных ризобиальных ЛХО, описывающиеся этой структурой, описаны в публикации D′Haeze, et al., см. выше.
В качестве других дополнительных примеров ЛХО, полученный из B. japonicum, представленный на фиг. 1b, можно использовать для обработки семян бобовых растений, не являющихся соей, и семян небобовых растений, таких как кукуруза. В качестве другого примера, ЛХО, который можно получить из R. leguminosarum, представленный на фиг. 2b (обозначенный как ЛХО-V (C18:1), SP104) можно использовать для обработки семян бобовых растений, не являющихся горохом, и также небобовых растений.
В объем настоящего изобретения также входит применение ЛХО, полученных (т.е. выделенных и/или очищенных) из микоризных грибов, таких как грибы группы Glomerocycota, например Glomus intraradices. Структуры типичных ЛХО, полученных из этих грибов, описаны в WO 2010/049751 и WO 2010/049751 (описанные в ней ЛХО также называют "Myc-факторами"). Типичные ХО, образованные из микоризных грибов и не встречающиеся в природе их производные, описываются следующей структурой:
 ,
,
в которой n=1 или 2; R1 означает C16, C16:0, C16:1, C16:2, C18:0, C18:1Δ9Z или C18:1Δ11Z; и R2 означает водород или SO3H. В некоторых вариантах осуществления используются ЛХО, продуцируемые микоризными грибами, представленные на фиг. 3b и 4b.
В объем настоящего изобретения также входит применение синтетических соединений ЛХО, таких как описанные в WO 2005/063784, и рекомбинантных ЛХО, полученных с помощью генной инженерии. Основная структура природных ЛХО может содержать модификации или заместители, обнаруживаемые в природных ЛХО, такие как описанные в публикациях Spaink, Crit. Rev. Plant Sci. 54:257-288 (2000) и D′Haeze, et al., Glycobiology 12:79R-105R (2002). Молекулы олигосахаридов-предшественников (ХО, которые, как это описано ниже, также применимы в качестве сигнальных молекул растений в настоящем изобретении), использующиеся для получения ЛХО, также могут синтезировать полученные с помощью генной инженерии микроорганизмы, например, как это описано в публикациях Samain, et al., Carbohydrate Res. 302:35-42 (1997); Cottaz, et al., Met. Eng. 7(4):311-7 (2005) и Samain, et al., J. Biotechnol. 72:33-47 (1999)(например, фиг. 1 в этой публикации, на которой представлены структуры ЛХО, которые можно образовать рекомбинантно в E. coli, содержащих различные комбинации генов nodBCHL).
Можно использовать ЛХО разной чистоты и их можно использовать в чистом виде или в форме культуры продуцирующих ЛХО бактерий или грибов. Например, OPTIMIZE® (продающийся фирмой Novozymes BioAg Limited) содержит культуру B. japonicum, который продуцирует ЛХО (ЛХО-V(C18:1, MeFuc), MOR116), который представлен на фиг. 1b. Методики получения в основном чистых ЛХО включают простое удаление микробных клеток из смеси ЛХО и микробов или продолжение выделения и очистки молекул ЛХО путем отделения содержащей ЛХО фазы растворителя с последующей очисткой с помощью ВЭЖХ (высокоэффективная жидкостная хроматография), как это описано, например, в патенте U.S. 5549718. Очистку можно улучшить путем повторения ВЭЖХ и для длительного хранения очищенные молекулы ЛХО можно высушить вымораживанием. Хитоолигосахариды (ХО), описанные выше, можно использовать в качестве исходных веществ для получения синтетических ЛХО. Для задач настоящего изобретения рекомбинантные ЛХО обладают чистотой, составляющей не менее 60%, например чистотой, составляющей не менее 60%, чистотой, составляющей не менее 65%, чистотой, составляющей не менее 70%, чистотой, составляющей не менее 75%, чистотой, составляющей не менее 80%, чистотой, составляющей не менее 85%, чистотой, составляющей не менее 90%, чистотой, составляющей не менее 91%, чистотой, составляющей не менее 92%, чистотой, составляющей не менее 93%, чистотой, составляющей не менее 94%, чистотой, составляющей не менее 95%, чистотой, составляющей не менее 96%, чистотой, составляющей не менее 97%, чистотой, составляющей не менее 98%, чистотой, составляющей не менее 99%, вплоть до чистоты, составляющей 100%.
Хитины и хитозаны, которые являются основными компонентами стенок клеток грибов и экзоскелетов насекомых и ракообразных, также состоят из остатков GIcNAc. Хитиновые соединения включают хитин (IUPAC: N-[5-[[3-ацетиламино-4,5-дигидрокси-6-(гидроксиметил)оксан-2-ил]метоксиметил]-2-[[5-ацетиламино-4,6-дигидрокси-2-(гидроксиметил)оксан-3-ил]метоксиметил]-4-гидрокси-6-(гидроксиметил)оксан-3-ил]этанамид) и хитозан (IUPAC: 5-амино-6-[5-амино-6-[5-амино-4,6-дигидрокси-2(гидроксиметил)оксан-3-ил]окси-4-гидрокси-2-(гидроксиметил)оксан-3-ил]окси-2(гидроксиметил)оксан-3,4-диол). Эти соединения можно приобрести, например, у фирмы Sigma-Aldrich, или получить из насекомых, панцирей ракообразных или стенок клеток грибов. Методики получения хитина и хитозана известны в данной области техники и описаны, например, в патенте U.S. 4536207 (получение из панцирей ракообразных), Pochanavanich, et al., Lett. Appl. Microbiol. 35:17-21 (2002) (получение из стенок клеток грибов), и в патенте U.S. 5965545 (получение из панцирей крабов и гидролизом имеющегося в продаже хитозана). См. также Jung, et al., Carbohydrate Polymers 67:256-59 (2007); Khan, et al., Photosynthetica 40(4):621-4 (2002). Можно получить деацетилированные хитины и хитозаны, степень деацетилирования которых составляет от менее 35% до более 90% и которые характеризуются широким спектром молекулярных масс, например низкомолекулярные олигомеры хитозана, обладающие молекулярными массами, равными менее 15 кДа, и олигомеры хитина, обладающие молекулярными массами, равными от 0,5 до 2 кДа; "практическую марку" хитозана, обладающего молекулярной массой, равной примерно 150 кДа; и высокомолекулярный хитозан, обладающий молекулярной массой, равной до 700 кДа. Композиции хитина и хитозана, приготовленные для обработки семян, также имеются в продаже. Имеющиеся в продаже продукты включают, например, ELEXA® (Plant Defense Boosters, Inc.) и BEYOND™ (Agrihouse, Inc.).
Флавоноиды являются фенольными соединениями, в общей структуре которых содержатся два ароматических кольца, соединенные мостиком из трех атомов углерода. Флавоноиды продуцируются растениями и выполняют множество функций, например являются превосходными сигнальными молекулами и средствами защиты от насекомых, животных, грибов и бактерий. Классы флавоноиды включают халконы, антоцианидины, кумарины, флавоны, флаванолы, флавонолы, флаваноны и изофлавоны. См. публикации Jain, et al., J. Plant Biochem. & Biotechnol. 11:1-10 (2002); Shaw, et al., Environmental Microbiol. 11:1867-80 (2006).
Типичные флавоноиды, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают генистеин, дайдзеин, формононетин, нарингенин, гесперитин, лутеолин и апигенин. Флавоноидные соединения имеются в продаже, например, у фирмы Natland International Corp., Research Triangle Park, NC; MP Biomedicals, Irvine, CA; LC Laboratories, Woburn MA. Флавоноидные соединения можно выделить из растений или семян, например, как это описано в патентах U.S. 5702752; 5990291; и 6146668. Флавоноидные соединения также могут продуцировать полученные с помощью генной инженерии микроорганизмы, такие как дрожжи, как это описано в публикации Ralston, et al., Plant Physiology 137:1375-88 (2005).
Жасмоновую кислоту (JA, [1R-[1α,2β(Z)]]-3-оксо-2-(пентенил)циклопентануксусную кислоту) и ее производные (которые включают линолевую кислоту и линоленовую кислоту (которые описаны выше в связи с жирными кислотами и их производными) можно использовать при практическом осуществлении настоящего изобретения. Жасмоновая кислота и ее метиловый эфир, метилжасмонат (MeJA), совместно известные как жасмонаты, являются соединениями на основе октадеканоида, которые в природе встречаются в растениях. Жасмоновую кислоту вырабатывают корни ростков пшеницы и грибы-микроорганизмы, такие как Botryodiplodia theobromae и Gibbrella fujikuroi, дрожжи (Saccharomyces cerevisiae) и патогенные и непатогенные штаммы Escherichia coli. Линолевую кислоту и линоленовую кислоту получают во время биосинтеза жасмоновой кислоты. Сообщают, что, как и линолевая кислота и линоленовая кислота, жасмонаты (и их производные) являются индукторами экспрессии гена nod или продуцирования ЛХО ризобактериями. См., например, публикацию Mabood, Fazli, Jasmonates induce the expression of nod genes in Bradyrhizobium japonicum, May 17, 2001.
Полезные производные жасмоновой кислоты, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают эфиры, амиды, гликозиды и соли. Типичными эфирами являются соединения, в которых карбоксигруппа жасмоновой кислоты заменена группой --COR, в которой R означает группу --OR1, в которой R1 означает: алкильную группу, такую как неразветвленная или разветвленная C1-C8 алкильная группа, например метильная, этильная или пропильная группа; алкенильную группу, такую как неразветвленная или разветвленная C2-C8 алкенильная группа; алкинильную группу, такую как неразветвленная или разветвленная C2-C8 алкинильная группа; арильную группу, содержащую, например, от 6 до 10 атомов углерода; или гетероарильную группу, содержащую, например, от 4 до 9 атомов углерода, где геетроатомами в гетероарильной группе могут быть, например, N, O, P или S. Типичными амидами являются соединения, в которых карбоксигруппа жасмоновой кислоты заменена группой --COR, в которой R означает группу NR2R3, в которой R2 и R3 независимо означают: водород; алкильную группу, такую как неразветвленная или разветвленная C1-C8 алкильная группа, например метильная, этильная или пропильная группа; алкенильную группу, такую как неразветвленная или разветвленная C2-C8 алкенильная группа; алкинильную группу, такую как неразветвленная или разветвленная C2-C8 алкинильная группа; арильную группу, содержащую, например, от 6 до 10 атомов углерода; или гетероарильную группу, содержащую, например, от 4 до 9 атомов углерода, где геетроатомами в гетероарильной группе могут быть, например, N, O, P или S. Сложные эфиры можно получить по известным методикам, таким как катализируемое кислотой нуклеофильное присоединение, при котором карбоновая кислота взаимодействует со спиртом в присутствии каталитического количества неорганической кислоты. Амиды также можно получить по известным методикам, например по реакции карбоновой кислоты с соответствующим амином в присутствии реагента сочетания, такого как дициклогексилкарбодиимид (ДЦК), в нейтральной среде. Подходящие соли жасмоновой кислоты включают, например, соли присоединения с основаниями. Основания, которые можно использовать в качестве реагентов для получения метаболически приемлемых солей этих соединений с основаниями, включают образованные из катионов, таких как катионы щелочных металлов (например, калия и натрия) и катионы щелочноземельных металлов (например, кальция и магния). Эти соли можно легко получить смешиванием раствора линолевой кислоты, линоленовой кислоты или жасмоновой кислоты с раствором основания. Соль можно осадить из раствора и собрать фильтрованием или можно извлечь другими средствами, такими как выпаривание растворителя.
Каррикины являются винилогическими 4H-пиронами, например 2H-фуро[2,3-c]пиран-2-онами, включая их производные и аналоги. Примеры этих соединений описываются следующей структурой:
 ,
,
в которой: Z означает O, S или NR5; R1, R2, R3 и R4 все независимо означают H, алкил, алкенил, алкинил, фенил, бензил, гидроксигруппу, гидроксиалкил, алкоксигруппу, фенилоксигруппу, бензилоксигруппу, CN, COR6, COOR=, галоген, NR6R7 или NO2; и R5, R6 и R7 все независимо означают H, алкил или алкенил, или его биологически приемлемую соль. Примеры биологически приемлемых солей этих соединений могут включать соли присоединения с кислотами, образованные с биологически приемлемыми кислотами, примеры которых включают гидрохлорид, гидробромид, сульфат или бисульфат, фосфат или гидрофосфат, ацетат, бензоат, сукцинат, фумарат, малеат, лактат, цитрат, тартрат, глюконат; метансульфонат, бензолсульфонат и п-толуолсульфонат. Дополнительные биологически приемлемые соли металлов могут включать соли щелочных металлов с основаниями, примеры которых включают соли натрия и калия. Примеры соединений, описывающихся этой структурой и которые могут быть подходящими для применения в настоящем изобретении, включают следующие: 3-метил-2H-фуро[2,3-c]пиран-2-он (где R1=CH3, R2, R3, R4=H), 2H-фуро[2,3-c]пиран-2-он (где R1, R2, R3, R4=H), 7-метил-2H-фуро[2,3-c]пиран-2-он (где R1, R2, R4=H, R3=CH3), 5-метил-2H-фуро[2,3-c]пиран-2-он (где R1, R2, R3=H, R4=CH3), 3,7-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3=CH3, R2, R4=H), 3,5-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R4=CH3, R2, R3=H), 3,5,7-триметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3, R4=CH3, R2=H), 5-метоксиметил-3-метил-2H-фуро[2,3-c]пиран-2-он (где R1=CH3, R2, R3=H, R4=CH2OCH3), 4-бром-3,7-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3=CH3, R2=Br, R4=H), 3-метилфуро[2,3-c]пиридин-2(3H)-он (где Z=NH, R1=CH3, R2, R3, R4=H), 3,6-диметилфуро[2,3-c]пиридин-2(6H)-он (где Z=N--CH3, R1=CH3, R2, R3, R4=H). См. патент U.S. 7576213. Эти молекулы также известны как каррикины. См. указанную выше публикацию Halford.
Количество по меньшей мере одной сигнальной молекулы растения, использующееся для обработки семян кукурузы, выраженное в единицах концентрации, обычно находится в диапазоне от примерно 10-5 до примерно 10-14 M (молярная концентрация), и в некоторых вариантах осуществления от примерно 10-5 до примерно 10-11 M, и в некоторых других вариантах осуществления от примерно 10-7 до примерно 10-8 M. Выраженное в единицах массы эффективное количество обычно находится в диапазоне от примерно 1 до примерно 400 мкг/центнер (ц) семян и в некоторых вариантах осуществления от примерно 2 до примерно 70 мкг/ц, и в некоторых других вариантах осуществления от примерно 2,5 до примерно 3,0 мкг/ц семян.
Для непрямой обработки семян кукурузы, т.е. обработки внесением в борозды, эффективное количество по меньшей мере одной сигнальной молекулы растения обычно находится в диапазоне от 1 мкг/акр до примерно 70 мкг/акр, и в некоторых вариантах осуществления от примерно 50 мкг/акр до примерно 60 мкг/акр. Для нанесения на растения кукурузы эффективное количество по меньшей мере одной сигнальной молекулы растения обычно находится в диапазоне от 1 мкг/акр до примерно 30 мкг/акр и в некоторых вариантах осуществления от примерно 11 мкг/акр до примерно 20 мкг/акр.
Гербициды, фунгициды и инсектициды
Подходящие гербициды включают бентазон, ацифлюорфен, хлоримурон, лактофен, кломазон, флуазифоп, глуфосинат, глифосат, сетоксидим, имазетапир, имазамокс, фомесаф, флумиклорак, имазахин и клетодим. Имеющиеся в продаже продукты, содержащие каждое из этих соединений, легко доступны. Концентрация гербицида в композиции обычно соответствует указанной на этикетке норме расхода конкретного гербицида.
"Фунгицид" при использовании в настоящем изобретении и в данной области техники означает агент, который уничтожает грибы или подавляет рост грибов. При использовании в настоящем изобретении фунгицид "обладает активностью по отношению к" конкретному виду грибов, если обработка фунгицидом приводит к уничтожению или подавлению роста популяции грибов (например, в почве) по сравнению с необработанной популяцией. Эффективные фунгициды в соответствии с настоящим изобретением будут обладать надлежащей активностью по отношению к широкому спектру патогенов, включая, но не ограничиваясь только ими, Phytophthora, Rhizoctonia, Fusarium, Pythium, Phomopsis или Selerotinia и Phakopsora и их комбинации.
Имеющиеся в продаже фунгициды могут быть подходящими для применения в настоящем изобретении. Подходящие имеющиеся в продаже фунгициды включают PROTÉGÉ, RIVAL или ALLEGIANCE FL или LS (Gustafson, Plano, TX), WARDEN RTA (Agrilance, St. Paul, MN), APRON XL, APRON MAXX RTA или RFC, MAXIM 4FS или XL (Syngenta, Wilmington, DE), КАПТАН (Arvesta, Guelph, Ontario) и PROTREAT (Nitragin Argentina, Buenos Ares, Argentina). Активные ингредиенты в этих и других имеющихся в продаже фунгицидах включают, но не ограничиваются только ими, флудиоксонил, мефеноксам, азоксистробин и металаксил. Имеющиеся в продаже фунгициды наиболее предпочтительно использовать в соответствии с инструкциями изготовителей при рекомендованных концентрациях.
При использовании в настоящем изобретении инсектицид "обладает активностью по отношению к" конкретному виду насекомых, если обработка инсектицидом приводит к уничтожению или подавлению роста популяции насекомых по сравнению с необработанной популяцией. Эффективные инсектициды в соответствии с настоящим изобретением будут обладать надлежащей активностью по отношению к широкому спектру насекомых, включая, но не ограничиваясь только ими, проволочников, совок, личинок, кукурузного жука, личинки мухи ростковой, земляных блошек, земляных клопов, тлей, листоедов и щитников.
Имеющиеся в продаже инсектициды могут быть подходящими для применения в настоящем изобретении. Подходящие имеющиеся в продаже инсектициды включают CRUISER (Syngenta, Wilmington, DE), GAUCHO и PONCHO (Gustafson, Plano, TX). Активные ингредиенты в этих и других имеющихся в продаже инсектицидах включают тиаметоксам, клотианидин и имидаклоприд. Имеющиеся в продаже инсектициды наиболее предпочтительно использовать в соответствии с инструкциями изготовителей при рекомендованных концентрациях.
Солюбилизирующие фосфат микроорганизмы, диазотрофы (ризобиальные инокуляты) и/или микоризные грибы
Настоящее изобретение может дополнительно включать обработку семян кукурузы солюбилизирующими фосфат микроорганизмами. При использовании в настоящем изобретении "солюбилизирующий фосфат микроорганизм" означает микроорганизм, который способен увеличить количество фосфора, доступного для растения. Солюбилизирующие фосфат микроорганизмы включают штаммы грибов и бактерий. В варианте осуществления солюбилизирующим фосфат микроорганизмом является спорообразующий микроорганизм.
Неограничивающие примеры солюбилизирующих фосфат микроорганизмов включают виды рода, выбранные из группы, включающей Acinetobacter, Arthrobacter, Arthrobotrys, Aspergillus, Azospirillum, Bacillus, Burkholderia, Candida Chryseomonas, Enterobacter, Eupenicillium, Exiguobacterium, Klebsiella, Kluyvera, Microbacterium, Mucor, Paecilomyces, Paenibacillus, Penicillium, Pseudomonas, Serratia, Stenotrophomonas, Streptomyces, Streptosporangium, Swaminathania, Thiobacillus, Torulospora, Vibrio, Xanthobacter и Xanthomonas.
Неограничивающие примеры солюбилизирующих фосфат микроорганизмов выбраны из группы, включающей Acinetobacter calcoaceticus, Acinetobacter sp, Arthrobacter sp., Arthrobotrys oligospora, Aspergillus niger, Aspergillus sp., Azospirillum halopraeferans, Bacillus amyloliquefaciens, Bacillus atrophaeus, Bacillus circulans,Bacillus licheniformis, Bacillus subtilis, Burkholderia cepacia, Burkholderia vietnamiensis, Candida krissii, Chryseomonas luteola, Enterobacter aerogenes, Enterobacter asburiae, Enterobacter sp., Enterobacter taylorae, Eupenicillium parvum, Exiguobacterium sp., Klebsiella sp., Kluyvera cryocrescens, Microbacterium sp., Mucor ramosissimus, Paecilomyces hepialid, Paecilomyces marquandii, Paenibacillus macerans, Paenibacillus mucilaginosus, Pantoea aglomerans, Penicillium expansum, Pseudomonas corrugate, Pseudomonas fluorescens, Pseudomonas lutea, Pseudomonas poae, Pseudomonas putida, Pseudomonas stutzeri, Pseudomonas trivialis, Serratia marcescens, Stenotrophomonas maltophilia, Streptomyces sp., Streptosporangium sp., Swaminathania salitolerans, Thiobacillus ferrooxidans, Torulospora globosa, Vibrio proteolyticus, Xanthobacter agilis и Xanthomonas campestris.
В предпочтительном варианте осуществления солюбилизирующим фосфат микроорганизмом является штамм грибов Penicillium. Штаммы грибов Penicillium, которые могут быть применимы при практическом осуществлении настоящего изобретения, включают P. bilaiae (ранее известный как P. bilaii), P. albidum, P. aurantiogriseum, P. chrysogenum, P. citreonigrum, P. citrinum, P. digitatum, P. frequentas, P. fuscum, P. gaestrivorus, P. glabrum, P. griseofulvum, P. implicatum, P. janthinellum, P. lilacinum, P. minioluteum, P. montanense, P. nigricans, P. oxalicum, P. pinetorum, P. pinophilum, P. purpurogenum, P. radicans, P. radicum, P. raistrickii, P. rugulosum, P. simplicissimum, P. solitum, P. variabile, P. velutinum, P. viridicatum, P. glaucum, P. fussiporus и P. expansum.
В одном предпочтительном варианте осуществления видом Penicillium является P. bilaiae. В другом предпочтительном варианте осуществления штаммы P. bilaiae выбраны из группы, включающей ATCC 20851, NRRL 50169, ATCC 22348, ATCC 18309, NRRL 50162 (Wakelin, et al., 2004. Biol Fertil Soils 40:36-43). В другом предпочтительном варианте осуществления видом Penicillium является P. gaestrivorus, например NRRL 50170 (см. выше публикацию Wakelin).
В некоторых вариантах осуществления используют более одного солюбилизирующего фосфат микроорганизма, например по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, включая любую комбинацию Acinetobacter, Arthrobacter, Arthrobotrys, Aspergillus, Azospirillum, Bacillus, Burkholderia, Candida Chryseomonas, Enterobacter, Eupenicillium, Exiguobacterium, Klebsiella, Kluyvera, Microbacterium, Mucor, Paecilomyces, Paenibacillus, Penicillium, Pseudomonas, Serratia, Stenotrophomonas, Streptomyces, Streptosporangium, Swaminathania, Thiobacillus, Torulospora, Vibrio, Xanthobacte и Xanthomonas, включая один вид, выбранный из следующей группы: Acinetobacter calcoaceticus, Acinetobacter sp, Arthrobacter sp., Arthrobotrys oligospora, Aspergillus niger, Aspergillus sp., Azospirillum halopraeferans, Bacillus amyloliquefaciens, Bacillus atrophaeus, Bacillus circulans,Bacillus licheniformis, Bacillus subtilis, Burkholderia cepacia, Burkholderia vietnamiensis, Candida krissii, Chryseomonas luteola, Enterobacter aerogenes, Enterobacter asburiae, Enterobacter sp., Enterobacter taylorae, Eupenicillium parvum, Exiguobacterium sp., Klebsiella sp., Kluyvera cryocrescens, Microbacterium sp., Mucor ramosissimus, Paecilomyces hepialid, Paecilomyces marquandii, Paenibacillus macerans, Paenibacillus mucilaginosus, Pantoea aglomerans, Penicillium expansum, Pseudomonas corrugate, Pseudomonas fluorescens, Pseudomonas lutea, Pseudomonas poae, Pseudomonas putida, Pseudomonas stutzeri, Pseudomonas trivialis, Serratia marcescens, Stenotrophomonas maltophilia, Streptomyces sp., Streptosporangium sp., Swaminathania salitolerans, Thiobacillus ferrooxidans, Torulospora globosa, Vibrio proteolyticus, Xanthobacter agilis и Xanthomonas campestris.
В некоторых вариантах осуществления два разных штамма одного вида также можно объединить, например используют по меньшей мере два разных штамма Penicillium. Применение комбинации по меньшей мере двух разных штаммов Penicillium обладает следующими преимуществами. При нанесении на почву, уже содержащую нерастворимые (или умеренно растворимые) фосфаты, применение объединенных штаммов грибов приведет к увеличению количества фосфора, доступного для усвоения растениями, по сравнению со случаем применения только одного штамма Penicillium. В свою очередь, это может привести к увеличению усвоения фосфата и/или повышению урожайности растений, растущих на этой почве, по сравнению со случаями применения только отдельных штаммов. Комбинация штаммов также позволяет использовать нерастворимые фосфориты в качестве эффективного удобрения для почв, которые содержат недостаточные количества доступного фосфора. Таким образом, в некоторых вариантах осуществления используют один штамм P. bilaiae и один штамм P. gaestrivorus. В других вариантах осуществления этими двумя штаммами являются NRRL 50169 и NRRL 50162. В других вариантах осуществления этими по меньшей мере двумя штаммами являются NRRL 50169 и NRRL 50170. В других вариантах осуществления этими по меньшей мере двумя штаммами являются NRRL 50162 и NRRL 50170.
Солюбилизирующие фосфат микроорганизмы можно получить по любой подходящей методике, известной специалисту в данной области техники, такой как твердофазная или жидкостная ферментация с использованием подходящего источника углерода. Солюбилизирующий фосфат микроорганизм предпочтительно получают в виде стабильной споры.
В одном варианте осуществления солюбилизирующим фосфат микроорганизмом являются грибы Penicillium. Грибы Penicillium, соответствующие настоящему изобретению, можно выращивать с помощью твердофазной или жидкостной ферментации и подходящего источника углерода. Изоляты Penicillium можно выращивать по любой подходящей методике, известной специалисту в данной области техники. Например, грибы можно выращивать в твердой среде для выращивания, такой как картофельный агар с декстрозой или агар с солодовым экстрактом, или в матрацах, содержащих подходящие жидкие среды, такие как среда Чапека-Докса или картофельно-декстрозный бульон. Эти методики выращивания можно использовать для получения инокулята Penicillium spp. для обработки (например, нанесения покрытия) семян и/или нанесения на агрономически приемлемый носитель для внесения в почву. Термин "инокулят" при использовании в настоящем описании означает любую форму солюбилизирующего фосфат микроорганизма, клетки грибов, мицелий или споры, бактериальные клетки или бактериальные споры, которые способны размножаться на или в почве, когда значения температуры, влажности и т.п. благоприятны для роста грибов.
Твердофазное получение спор Penicillium можно провести путем посева в твердую среду, такую как субстрат на основе торфа или вермикулита, или зерна, включая, но не ограничиваясь только ими, овес, пшеницу, ячмень или рис. В стерилизованную среду (стерилизацию проводят с помощью обработки в автоклаве или путем облучения) высевают суспензию спор (1×102-1×107 КОЕ/мл) подходящего Penicillium spp. и в зависимости от субстрата устанавливают влажность, равную от 20 до 50%. Материал инкубируют в течение от 2 до 8 недель при комнатной температуре. Споры также можно получить жидкостной ферментацией (Cunningham et al., 1990. Can J Bot. 68:2270-2274). Жидкостное получение можно провести путем выращивания грибов в любых подходящих средах, таких как картофельно-декстрозный бульон или среды с сахарозой и дрожжевым экстрактом, при подходящих значениях pH и температуры, которые можно определить по стандартным процедурам, использующимся в данной области техники.
Полученный материал можно использовать без обработки или споры можно собрать, сконцентрировать центрифугированием, приготовить композицию и затем высушить по методикам сушки на воздухе, сушки вымораживанием или сушки в псевдоожиженном слое (Friesen, et al., 2005, Appl. Microbiol. Biotechnol. 68:397-404) и получить смачивающийся порошок. Затем смачивающийся порошок суспендируют в воде, наносят на поверхность семян и перед высеванием ему дают высохнуть. Смачивающийся порошок можно использовать вместе с другими средствами для обработки семян, такими как, но не ограничиваясь только ими, химические средства для обработки семян, носители (например, тальк, глина, каолин, силикагель, каолинит) или полимеры (например, метилцеллюлоза, поливинилпирролидон). Альтернативно, суспензию спор подходящего Penicillium spp. можно нанести на подходящий совместимы с почвой носитель (например, порошок или гранулы на основе торфа) с обеспечением подходящей конечной влажности. До использования материал можно инкубировать при комнатной температуре, обычно в течение от примерно 1 дня до примерно 8 недель.
Кроме ингредиентов, использующихся для выращивания солюбилизирующего фосфат микроорганизма, включая, например, ингредиенты, указанные выше для выращивания Penicillium, при приготовлении солюбилизирующего фосфат микроорганизма можно использовать другие агрономически приемлемые носители. При использовании в настоящем изобретении в связи с "носителем" термин "агрономически приемлемый" означает любой материал, который можно использовать для доставки активных веществ в семена кукурузы, почву или растение кукурузы, и предпочтительно, чтобы носитель можно было добавлять (к семенам, почве или растению) без неблагоприятного влияния на рост растений, структуру почвы, дренаж почвы и т.п. Подходящие носители включают, но не ограничиваются только ими, пшеничную мякину, отруби, измельченную пшеничную солому, порошки или гранулы на основе торфа, гранулы на основе гипса и глины (например, каолин, бентонит, монтмориллонит). При добавлении спор в почву гранулированный состав является предпочтительным. Составы в виде жидкости, с использованием торфа или смачивающегося порошка являются подходящими для нанесения на семена кукурузы. При использовании для нанесения на семена кукурузы материал можно смешать с водой, нанести на семена и дать высохнуть. Пример еще одного носителя включает увлажненный торф, высушенный, просеянный и нанесенный на семена до нанесения клея, например, гуммиарабика. В тех вариантах осуществления, которые включают приготовление активных веществ виде единой композиции, агрономически приемлемый носитель может быть водным.
Количество по меньшей мере одного солюбилизирующего фосфат микроорганизма меняется в зависимости от типа семян или почвы, типа культурного растения, количеств источников фосфора и/или питательных микроэлементов, содержащихся в почве или добавленных к ней и т.п. В каждом конкретном случае подходящее количество можно определить с помощью простых методик последовательных приближений. Обычно, например, для Penicillium наносимое количество находится в диапазоне 0,001-1,0 кг спор грибов и мицелия (масса в сыром виде) на гектар, или 102-106 колониеобразующих единиц (КОЕ) в пересчете на одно семя (когда используют семена с покрытием), или на гранулированном носителе наносят от 1×106 до 1×1011 колониеобразующих единиц на гектар. Грибковые клетки, например, в форме спор и носителя можно вносить в грядку с семенами в почву на уровне корней или можно использовать для нанесения на семена до высадки.
В вариантах осуществления, в которых, например, используют по меньшей мере два штамма солюбилизирующего фосфат микроорганизма, например два штамма Penicillium, имеющиеся в продаже удобрения можно внести в почву вместо (или даже вместе) с природным фосфоритом. Источник фосфора может содержать источник фосфора, находящийся в почве. В других вариантах осуществления источник фосфора можно добавить в почву. В одном варианте осуществления источником является фосфорит. В другом варианте осуществления источником является готовое удобрение. В продаже имеется много типов готовых фосфатных удобрении. Некоторыми обычными являются содержащие моноаммонийфосфат (МАФ), тройной суперфосфат (ТСП), диаммонийфосфат, обычный суперфосфат и полифосфат аммония. Все эти удобрения получают химической обработкой нерастворимых природных фосфоритов на крупномасштабных предприятиях по производству удобрений и продукт является дорогостоящим. С помощью настоящего изобретения можно уменьшить количество этих удобрений, вносимых в почву, при сохранении такого же количества фосфора, усваиваемого из почвы.
В другом варианте осуществления источник или фосфор является органическим. Органическое удобрение означает добавку к почве, полученную из природных источников, которое гарантирует по меньшей мере минимальное содержание азота, фосфата и калия. Примеры включают растительные и животные субпродукты, порошковые породы, водоросли, бактериальные удобрения и кондиционеры. Конкретные типичные примеры включают костяную муку, мясную муку, навоз, компост, осадки сточных вод или гуано.
Разумеется другие удобрения, такие как источники азота или другие улучшители почвы, также можно добавить к почве примерно в то же время, что и солюбилизирующий фосфат микроорганизм, или в другое время, если эти другие материалы нетоксичны для грибов.
Настоящее изобретение будет описано с помощью приведенных ниже неограничивающих примеров. Если не указано иное, в качестве контроля использовали воду (указано как "контроль" или "CHK").
Примеры
Эксперименты в теплице
Пример 1: Обработка семян кукурузы
В теплице проводили два эксперимента по обработке семян с использованием только ЛХО гороха, ХО гороха и смесей ХО, полученных из хитозана с помощью ферментативной методики (структурно отличающихся от ХО гороха и также называющихся в примерах как "China ХО"). Семена гибридной кукурузы (92L90, Peterson Farm, USA) обрабатывали раствором для обработки (10-8 M) при расходе, составляющем 3 жидкостных унции/100 фунтов семян. Семена высевали в пластмассовые горшки, содержащие смесь 1:1 песок:перлит. Семенам давали расти в течение примерно 3-4 недель и затем их собирали и измеряли их массу в сухом состоянии.
Результаты, полученные в обоих экспериментах, показывали, что предлагаемый в настоящем изобретении (ХО гороха) приводил к большему увеличению биомассы ростков, корней и суммарной биомассы, чем не предлагаемый в настоящем изобретении и использующийся для сопоставления ЛХО. В первом эксперименте ХО приводил к увеличению массы в сухом состоянии, на 11,84% большему, чем ЛХО (фиг. 5). Во втором эксперименте ХО приводил к увеличению массы в сухом состоянии, на 12,63% большему, чем ЛХО (фиг. 6). China ХО, который также можно рассматривать как заменяющий источник ХО гороха, также приводил к большему увеличению массы в сухом состоянии по сравнению с не предлагаемым в настоящем изобретении ЛХО.
Пример 2: Прорастание семян кукурузы в чашках Петри
Семена кукурузы помещали в чашки Петри, содержащие 5 мл раствора для обработки на фильтровальной бумаге. Семена кукурузы помещали на увлажненную фильтровальную бумагу для проращивания. Аналогичным образом семена пшеницы (яровой пшеницы) помещали в чашки Петри. Через 5 дней после помещения в чашки исследовали проращивание кукурузы. Корни собирали и с помощью системы WinRhizo измеряли их длину.
В случае кукурузы ЛХО гороха, ХО гороха и ХО с добавлением пальмитиновой кислоты приводили к усиленному проращиванию (фиг. 7) и они также приводили к значительно увеличенной длине корней ростков по сравнению с контролем. Различия их воздействий не были статистически значимыми, ХО с добавлением пальмитиновой кислоты приводил к наибольшим степени проращивания и длине корней. Добавление пальмитиновой кислоты к ХО, видимо, было немного более благоприятным (статистически незначимо) по сравнению с ЛХО или ХО (фиг. 8).
Пример 3: Нанесение на семена кукурузы
Семена кукурузы обрабатывали различными комбинациями ХО гороха (10-8 M) и ЛХО гороха (10-8, 10-9 M). Семена высевали в теплице в пластмассовые горшки, содержащие смесь 1:1 песок:перлит. Ростки собирали через 10 дней после высадки, тщательно промывали и затем сушили в сушильном шкафу при 60°C в течение 48 ч.
Как показано на фиг. 9, и ХО (10-8 M) (обозначен как CO8), и ЛХО (10-8 M) (обозначен как SP8) при использовании по отдельности увеличивали массу ростков кукурузы в сухом состоянии. Только комбинация ЛХО 10-9/ХО при 10-8 увеличивали массу ростков кукурузы в сухом состоянии в большей степени, чем ЛХО гороха (SP) или ХО гороха.
Исследования в полевых условиях
Пример 4: Кукуруза
Для оценки вариантов осуществления настоящего изобретения применительно к урожайности зерен при некорневом нанесении на кукурузу проведены шестнадцать (16) исследований в полевых условиях. Исследования в полевых условиях проводили в 8 штатах на разных почвах и при разных условиях окружающей среды.
При исследованиях обработку проводили водой (контроль), чистым ХО (хитоолигосахарид) - ХО-V (представлен на фиг. 2a) и чистым ЛХО (липохитоолигосахарид) - SP104 (представлен на фиг. 2b). Использовали различные имеющиеся в продаже гибриды кукурузы. Средства добавляли к гербициду глифосату и разбрызгивали на листья растений в обычный период нанесения гербицида. По 4 унции/акр средства для обработки, объединенного с гербицидом и водой, вносили при расходе, равном от 5 до 10 галлонов на акр. Кукурузу выращивали до созревания и собирали и определяли массу зерен.
Как показывает сопоставление контроля с ХО, при некорневой обработке с помощью ХО урожайность повышалась на 9,2 бушель/акр, что соответствовало составляющему 4,8% повышению по сравнению с контролем, и повышение урожайности происходило в 93,8% исследований.
По сравнению с повышением при некорневой обработке с помощью ЛХО в случае ХО средняя урожайность была на 5,0 бушель/акр больше, что приводило к на 2,6% большему повышению урожайности, и доля исследований, при которых повышалась урожайность, была на 18,8% больше.
Поэтому при некорневой обработке и ХО, и ЛХО приводили к повышению урожайности, но ХО был не менее чем вдвое более эффективным, чем ЛХО.
Пример 5: Кукуруза
Для оценки вариантов осуществления настоящего изобретения применительно к урожайности зерен при нанесении на зерна кукурузы до высевания проведены 10 исследований в полевых условиях. 5 Исследований в полевых условиях проводили в 5 штатах и 5 исследований проводили в Аргентине.
При исследованиях обработку проводили водой (контроль), чистым ХО (хитоолигосахарид) - ХО-V (представлен на фиг. 2a) и чистым ЛХО (липохитоолигосахарид) - SP104 (представлен на фиг. 2b). Обработку с помощью ХО и ЛХО проводили при молярной концентрации равной 1×10-8, что соответствовало внесению 1 мкг/акр. Использовали различные имеющиеся в продаже гибриды кукурузы. Перед высеванием на пятьдесят (50) фунтов семян наносили 3 жидкостные унции средства для обработки. Кукурузу выращивали до созревания и собирали и определяли массу зерен.
Результаты приведены в таблице 2.
(N=10)
Как показывает сопоставление контроля с ХО, при нанесении ХО на семена урожайность повышалась на 6,5 бушель/акр, что соответствовало составляющему 3,6% повышению по сравнению с контролем, и повышение урожайности происходило в 80,0% исследований.
При сопоставлении ХО с ЛХО видно, что в случае ХО средняя урожайность была на 4,6 бушель/акр меньше, что приводило к на 2,5% меньшему увеличению урожайности по сравнению с контролем, и в этих 10 исследованиях доля исследований, при которых повышалась урожайность, была на 10,0% меньше.
Обработка с помощью и ХО, и ЛХО при нанесении на семена кукурузы приводила к повышению урожайности по сравнению с контролем и ЛХО приводил к наибольшему повышению.
Все патентные и непатентные публикации, цитированные в настоящем описании, характерны для уровня подготовки специалистов в области техники, к которой относится настоящее изобретение. Все эти публикации включены в качестве ссылки в такой степени, как если бы для каждой отдельной публикации или заявки на патент было специально и по отдельности указано о включении в качестве ссылки.
Хотя настоящее изобретение описано с помощью конкретных вариантов осуществления, следует понимать, что эти варианты осуществления только иллюстрируют принципы и области применения настоящего изобретения. Поэтому необходимо понимать, что в эти иллюстративные варианты осуществления можно внести многочисленные изменения и что можно образовать другие сочетания без отклонения от сущности и объема настоящего изобретения, определяемых прилагаемой формулой изобретения.
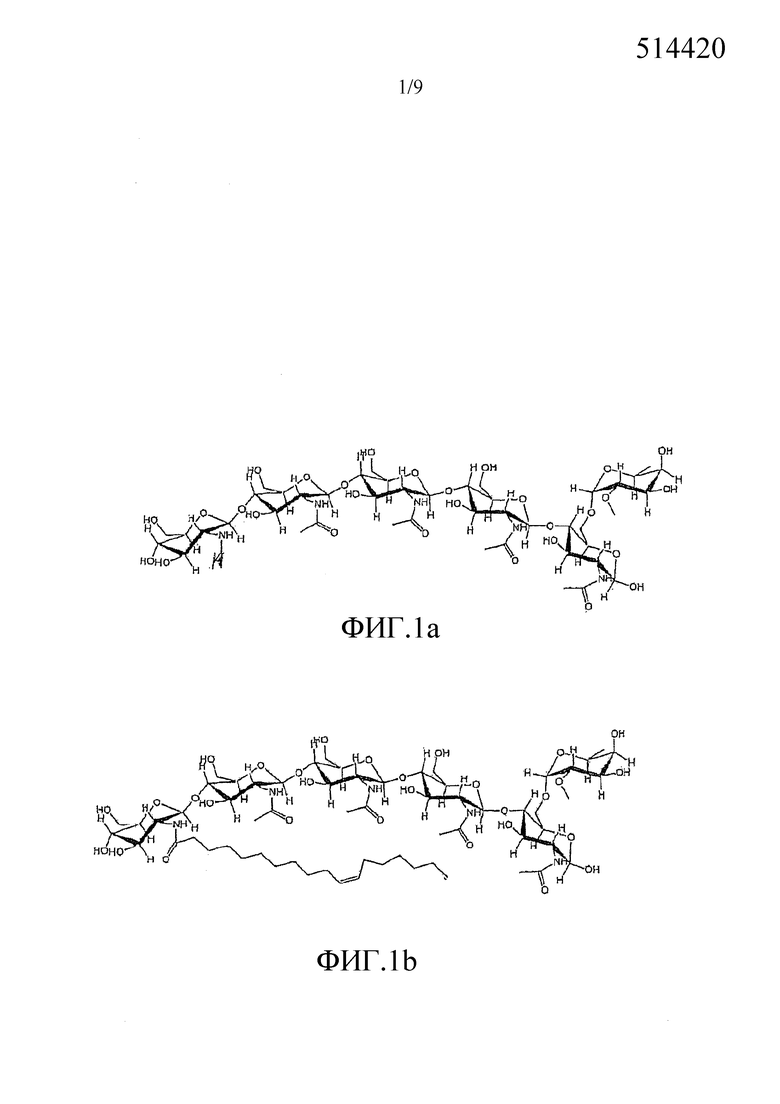





Изобретение относится к сельскому хозяйству. Проводят обработку семени кукурузы и/или растения кукурузы, которое прорастает из семени кукурузы, эффективным количеством по меньшей мере одного хитоолигосахарида (ХО), представленного формулой:

в которой R1 означает водород или метил; R2 означает водород или метил; R3 означает водород, ацетил или карбамоил; R4 означает водород, ацетил или карбамоил; R5 означает водород, ацетил или карбамоил; R6 означает водород, арабинозил, фукозил, ацетил, сульфат, 3-O-S-2-O-MeFuc, 2-O-MeFuc и 4-O-AcFuc; R7 означает водород, маннозил или глицерин; R8 означает водород, метил или -СН2ОН; R9 означает водород, арабинозил или фукозил; R10 означает водород, ацетил или фукозил; и n равно 0, 1, 2 или 3. Изобретение позволяет увеличить урожайность, количество, длину, массу, объем корней и площадь листвы. Изобретение позволяет усилить рост растения. 3 н. и 33 з.п. ф-лы, 9 ил., 2 табл., 5 пр.
1. Способ усиления роста растения кукурузы, включающий обработку семени кукурузы и/или растения кукурузы, которое прорастает из семени кукурузы, эффективным количеством по меньшей мере одного хитоолигосахарида (ХО), представленного формулой:
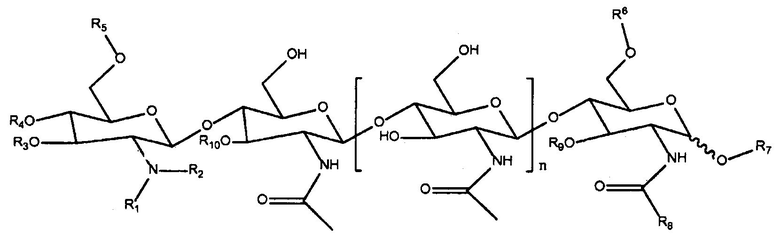 ,
,
в которой
R1 означает водород или метил;
R2 означает водород или метил;
R3 означает водород, ацетил или карбамоил;
R4 означает водород, ацетил или карбамоил;
R5 означает водород, ацетил или карбамоил;
R6 означает водород, арабинозил, фукозил, ацетил, сульфат, 3-О-S-2-О-MeFuc, 2-О-MeFuc и 4-О-AcFuc;
R7 означает водород, маннозил или глицерин;
R8 означает водород, метил или -СН2ОН;
R9 означает водород, арабинозил или фукозил;
R10 означает водород, ацетил или фукозил; и
n равно 0, 1, 2 или 3.
2. Способ по п. 1, в котором по меньшей мере один ХО включает ХО, представленный формулой:
 .
.
3. Способ по п. 1, в котором по меньшей мере один ХО включает ХО, представленный структурой:
 .
.
4. Способ по п. 1, в котором по меньшей мере один ХО включает ХО, представленный формулой:
 ,
,
в которой n=1 или 2; R1 означает водород или метил; и R2 означает водород или SO3H.
5. Способ по п. 1, в котором по меньшей мере один ХО включает ХО, представленный структурой:
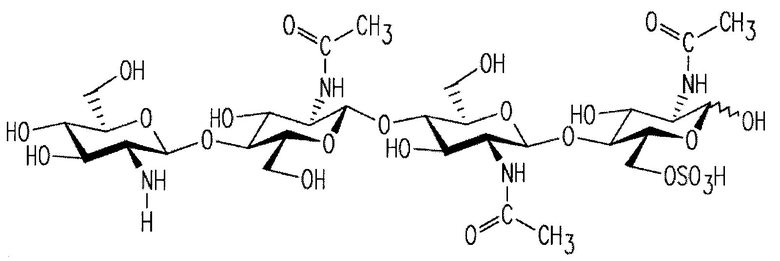 .
.
6. Способ по п. 1, в котором по меньшей мере один ХО включает ХО, представленный структурой:
 .
.
7. Способ по п. 1, в котором по меньшей мере один ХО включает синтетический ХО.
8. Способ по п. 1, в котором по меньшей мере один ХО включает рекомбинантный ХО.
9. Способ по п. 8, в котором рекомбинантный ХО обладает чистотой, составляющей по меньшей мере 60%.
10. Способ по п. 8, в котором рекомбинантный ХО обладает чистотой, составляющей по меньшей мере 70%.
11. Способ по п. 8, в котором рекомбинантный ХО обладает чистотой, составляющей по меньшей мере 80%.
12. Способ по п. 8, в котором рекомбинантный ХО обладает чистотой, составляющей по меньшей мере 90%.
13. Способ по п. 1, в котором по меньшей мере один ХО наносят на семя кукурузы перед высеванием и/или примерно во время высевания.
14. Способ по п. 1, в котором по меньшей мере один ХО наносят на семя кукурузы в бороздах.
15. Способ по п. 1, в котором по меньшей мере один ХО наносят на растения кукурузы с помощью некорневой обработки.
16. Способ по п. 1, в котором эффективное количество по меньшей мере одного ХО составляет от 10-5 до 10-14 М.
17. Способ по п. 16, в котором эффективное количество по меньшей мере одного ХО составляет от 1 мкг/акр до 70 мкг/акр.
18. Способ по п. 1, в котором эффективное количество по меньшей мере одного ХО составляет от 1 мкг/акр до 30 мкг/акр.
19. Способ по п. 1, дополнительно включающий нанесение по меньшей мере одного питательного микроэлемента на семя кукурузы и/или растение кукурузы, которое прорастает из семени кукурузы.
20. Способ по п. 19, в котором по меньшей мере один питательный микроэлемент включает один или несколько витаминов и/или микроэлементов.
21. Способ по п. 1, дополнительно включающий нанесение по меньшей мере одной жирной кислоты или ее производной на семя кукурузы и/или растение кукурузы, которое прорастает из семени кукурузы.
22. Способ по п. 1, дополнительно включающий нанесение по меньшей мере одной сигнальной молекулы растения на семя кукурузы и/или растение кукурузы, которое прорастает из семени кукурузы.
23. Способ по п. 22, в котором по меньшей мере одна сигнальная молекула растения включает по меньшей мере один липохитоолигосахарид (ЛХО).
24. Способ по п. 23, в котором по меньшей мере один ЛХО включает ЛХО, представленный структурой:
 .
.
25. Способ по п. 23, в котором по меньшей мере один ЛХО включает ЛХО, представленный структурой:
 .
.
26. Способ по п. 23, в котором по меньшей мере один ЛХО включает ЛХО, представленный структурой:
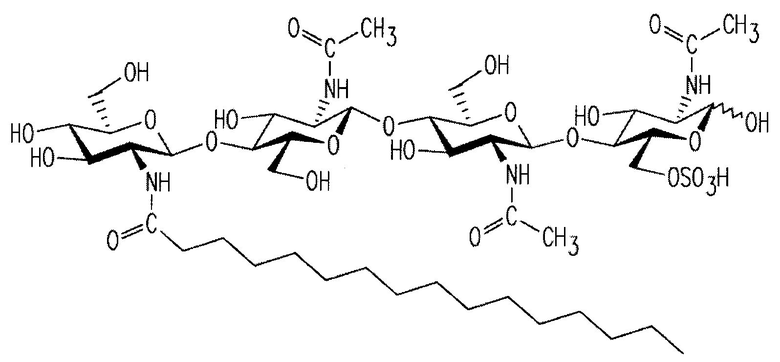 .
.
27. Способ по п. 23, в котором по меньшей мере один ЛХО включает ЛХО, представленный структурой:
 .
.
28. Способ по п. 22, в котором по меньшей мере одна сигнальная молекула растения включает сигнальную молекулу растения, выбранную из группы, состоящей из хитиновых соединений, флавоноидов, жасмоновой кислоты и ее производных, линолевой кислоты и ее производной, линоленовой кислоты и ее производных и каррикинов и их производных.
29. Способ по п. 1, дополнительно включающий нанесение по меньшей мере одного гербицида, инсектицида и/или фунгицида на семя кукурузы и/или растение кукурузы, которое прорастает из семени кукурузы.
30. Способ по п. 1, дополнительно включающий нанесение по меньшей мере одного солюбилизирующего фосфат микроорганизма на семя кукурузы и/или растение кукурузы, которое прорастает из семени кукурузы.
31. Способ по п. 30, в котором по меньшей мере один солюбилизирующий фосфат микроорганизм представляет собой штамм грибов Penicillium.
32. Способ по п. 30, в котором по меньшей мере один солюбилизирующий фосфат микроорганизм представляет собой штамм P. bilaiae.
33. Способ по п. 32, в котором по меньшей мере один штамм Р. bilaiae включает NRRL 50162, NRRL 50169, АТСС 20851, АТСС 22348 и/или АТСС 18309.
34. Способ по п. 30, в котором по меньшей мере один солюбилизирующий фосфат микроорганизм включает по меньшей мере один штамм P. gaestrivorus.
35. Семя, обработанное способом по любому из пп. 1-34.
36. Растение, произрастающее из семени по п. 35.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Фотоэлектрический автоматический синхронизатор | 1945 |
|
SU98630A1 |
Авторы
Даты
2016-08-20—Публикация
2012-09-24—Подача