Изобретение относится к медицине, а именно к акушерству, гинекологии и сосудистой хирургии, и может быть использовано для прогнозирования степени регресса опухоли при проведении эмболизации маточных артерий (ЭМА) у женщин с миомой матки с помощью ангиографических критериев. Миома матки является наиболее частым заболеванием женщин репродуктивного возраста. Относительно тяжелая симптоматика и невозможность реализации репродуктивной функции приводят к значительному снижению качества жизни и снижению физического здоровья. У большинства женщин миома матки обуславливает кровотечения чаще по типу меноррагий, сопровождается болью внизу живота и в поясничной области, приводит к сдавлению соседних органов, вследствие чего развиваются дизурические явления (частое мочеиспускание, никтурия, возможен гидронефроз почек), нарушается работа кишечника и в результате значительно снижается качество жизни пациенток, нарушается репродуктивная функция. До настоящего времени при симптомной миоме матки преимущественно проводят оперативные вмешательства в объеме гистерэктомии или миомэктомии при единичных узлах, поэтому актуальным является создание способов, которые направлены на прогнозирование степени регресса миомы матки, что позволит проводить эффективное лечение.
Известен способ лечения миомы матки путем фокусированной ультразвуковой (ФУЗ) терапии, при котором под контролем магниторезонансной томографии (МРТ) луч ФУЗ направляют на узел и за счет фокусировки волн происходит локальный нагрев ткани миомы до 60-70°C (55-90), что приводит к термическому некрозу, вызывая в течение 1 секунды гибель всех клеток за счет их дегидратации, повреждения сосудистых структур, денатурации белков и разрушения коллагеновых волокон.
Недостатком известного способа является его продолжительность (для воздействия на один узел необходимо время 2-4 часа), при этом пациентка должна находиться в неподвижном состоянии, что может привести к усилению тромбоза глубоких вен или эмболии легких, кроме того известным способом невозможно прогнозировать степени регресса миомы матки.
Наиболее близким по достигаемому техническому результату является способ лечения миомы матки путем эмболизации маточных артерий (ЭМЛ), заключающийся в введении эмболизата в маточные артерии для их окклюзии.
Эффект ЭМА заключается в прекращении кровотока по ветвям маточных артерий, кровоснабжающих миому, при этом ветви, снабжающие здоровую часть миометрия, не страдают благодаря особенностям кровотока в миоме, а именно кровоснабжение узлов осуществляется из перифиброидного сплетения - сосудистой сети, окружающей миому по периферии, однако им невозможно прогнозировать степени регресса миомы матки.
Авторами не обнаружено способов, позволяющих прогнозировать степени регресса миомы матки.
Авторы предлагают способ прогнозирования эффективности лечения миомы матки после проведения ЭМА, позволяющий высокоточно определять степень выраженности регресса миоматозных узлов на основании критериев ангиографии, которая проводится у всех пациенток в течение процедуры ЭМА.
Техническим результатом заявляемого способа является повышение точности прогноза регресса миомы матки после проведения ЭМА по предлагаемым ангиографическим критериям.
Технический результат заявляемого способа достигается тем, что после выполнения ангиографии с помощью рентгеноконтраста урографина или ультрависта во время ЭМА со скоростью введения контраста 1 мл/с, объемом 4-6 мл и одновременной покадровой съемкой со скоростью 2-4 кадра в секунду, для прогнозирования эффективности регресса миомы проводят оценку и характер кровоснабжения миоматозных узлов по двум параметрам ангиограмм: количеству ветвей в узле и площади узла, кровоснабжаемой одним сосудом, при этом площадь узла, кровоснабжаемую одним сосудом, рассчитывают по формуле
S1=Sy/n,
где S1 - площадь узла, кровоснабжаемая одним сосудом;
Sy - общая площадь узла;
n - количество ветвей, кровоснабжающих узел,
и при количестве ветвей, кровоснабжающих узлы, - 18,91±1,70, площади, кровоснабжаемой одним сосудом, - 141,67±13,09 мм2 прогнозируют выраженную степень регресса миомы матки; при количестве ветвей, кровоснабжающих узлы, - 10,36±1,04, площади, кровоснабжаемой одной сосудистой ветвью, - 329,47±38,10 мм2 прогнозируют невыраженную степень регресса миомы матки.
Способ осуществляют поэтапно следующим образом.
Для иллюстрации заявленного способа даны фигуры в виде ангиограмм.
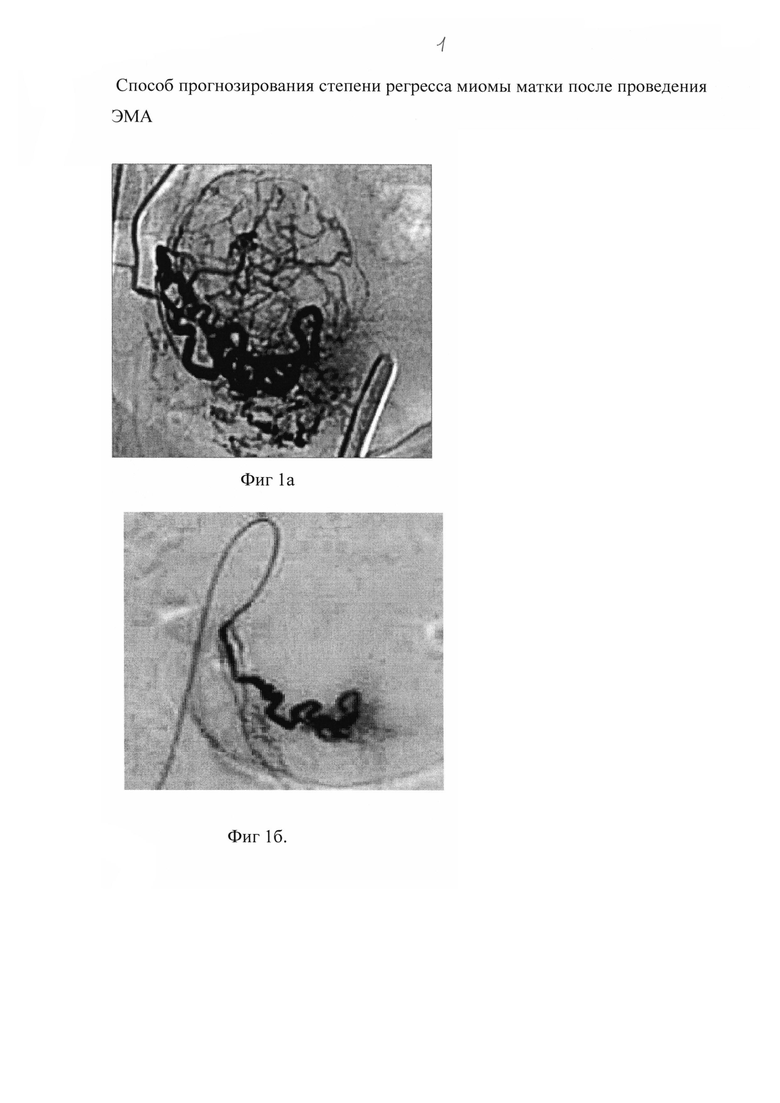
На фиг. 1а дана ангиограмма 1 типа, проведенная до ЭМА, и иллюстрирует хороший кровоток и выраженный регресс опухоли в прогнозе.
На фиг. 1б дана ангиограмма 1 типа после ЭМА.
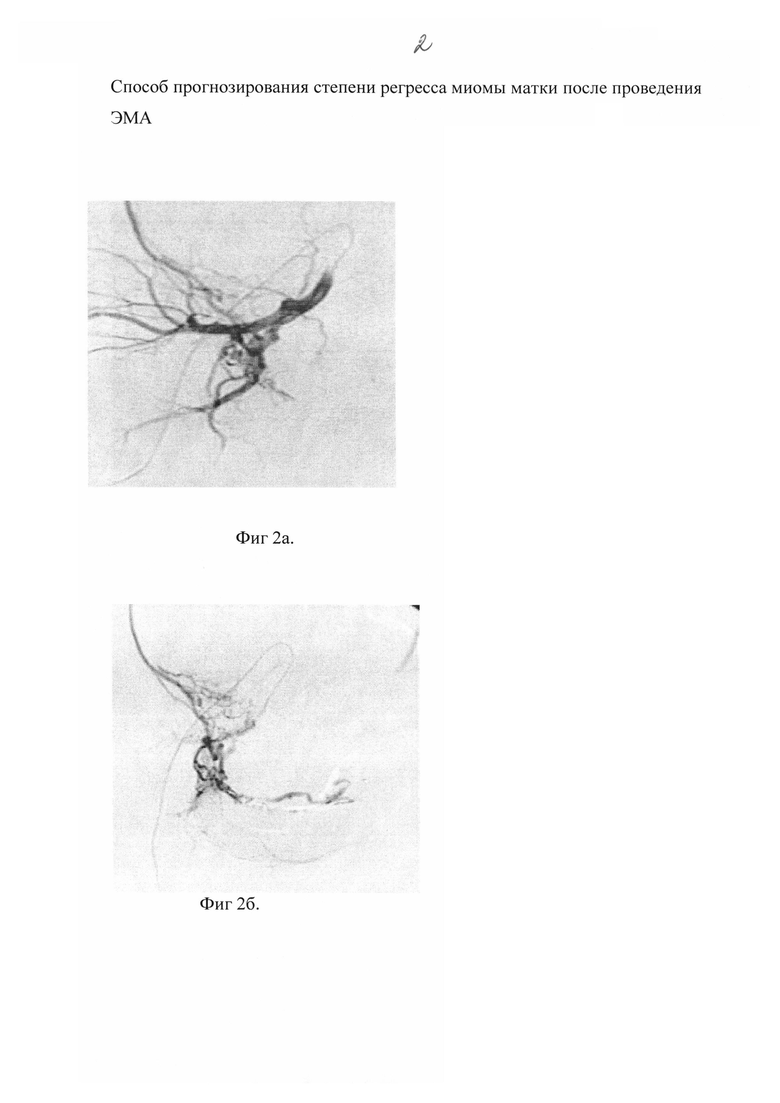
На фиг. 2а дана ангиограмма 2 типа, проведенная до ЭМА, и иллюстрирует плохое кровоснабжение миоматозного узла и предполагает невыраженный регресс опухоли в прогнозе.
На фиг. 2б дана ангиограмма 2 типа после ЭМА.
Процедуру ЭМА выполняют в условиях рентгеноперационной на ангиографе, например - «MULTISTAR Т.О.Р / Plus» фирмы SIEMENS (Германия).
1. В асептических условиях под местной анестезией выполняют пункцию правой или левой бедренной артерии. Затем по проводниковой системе в артерию устанавливают интрадюссер диаметром 6 или 7 френч (Fr). Далее по системе Сельдингера в аорту вводят специально моделированный катетер, которым осуществляют поочередную катетеризацию общей подвздошной (ОПА) и затем внутренней подвздошной артерии (ВПА) справа или слева.
2. После проведения катетеризации МА ангиографию проводят урографином или ультравистом, со скоростью введения контраста 1 мл/сек, объемом 4-6 мл.
Одновременно проводят покадровую съемку со скоростью 2-4 кадра в секунду, начиная с артериальной и заканчивая паренхиматозной фазой контрастирования.
3. На следующем этапе вводят эмболизат (ЭМА выполняют с помощью частиц поливинилалкоголя - PVA (СООС) и TruFfill™ («Johnson & Johnson») размером микрочастиц 500-700 н/м) с повторными контрольными ангиографиями в прежнем режиме.
4. Результат операции оценивают по полному прекращению артериального кровотока в миоматозных узлах, после чего систему катетера и интрадюссера удаляют, осуществляют гемостаз места прокола и накладывают асептическую повязку.
5. После процедуры соответственно характеру ангиограмм проводят прогноз регресса миоматозных узлов. При анализе ангиограмм для объективной оценки кровоснабжения миоматозных узлов рассчитывают 2 критерия:
а) количество ветвей в узле,
б) площадь узла, кровоснабжаемая одним сосудом.
Площадь узла, кровоснабжаемая одним сосудом, рассчитывают по формуле
S1=Sy/n,
где S1 - площадь узла, кровоснабжаемая одним сосудом;
Sy - общая площадь узла;
n - количество ветвей, кровоснабжающих узел.
Общую площадь узла определяют при помощи миллиметровой сетки в соответствии с масштабом ангиографического снимка.
Корректность прогнозирования степени регресса миомы матки заявляемым способом была апробирована в результате клинического исследования.
Первую группу составили 12 пациенток, у которых опухоль имела большие размеры (от 14 до 20 недель беременности). Средний возраст пациенток этой группы составил 40,41±2,30 лет. Локализация узлов почти у половины женщин данной группы (41,70%) была интерстицио-субсерозной, несколько реже (33,30%) встречалось интралигаментарное их расположение, которое наблюдалось только у женщин этой группы. В 16,70% узлы были интерстицио-субмукозными и только в 8,30% - субмукозными. В клинической картине у данных больных доминировали болевой (100,00%) и синдром сдавления соседних органов (91,70%). При этом более чем у половины пациенток (66,60%) имело место прогрессирование болевого синдрома.
Вторая группа состояла из 28 женщин. Средний возраст больных был 42,25±1,20 года. Величина опухоли у этих пациенток не достигала 12 недель беременности, расположение ее было преимущественно субмукозным (35,70%) и/или интерстицио-субмукозным (46,40%). Значительно реже и почти с равной частотой встречались интерстициальные и интерстицио-субсерозные узлы (7,20% и 10,70%). В клинической картине у них превалировали геморрагический (85,70%) и анемический (85,70%) синдромы.
Установлены различия кровоснабжения в зависимости от структуры и величины миоматозного узла. Выявлены различные ангиографические картины кровоснабжения миоматозных узлов. В зависимости от характера кровотока было выявлено 2 типа ангиограмм.
Для ангиограмм (первый тип) характерна выраженная васкуляризация миомы - на них контрастировались объемные образования различного размера, с четкими контурами, округлой формы.
Артерии, кровоснабжающие миоматозную матку, имели неправильную выпрямленную форму, без характерного штопорообразного хода и были расположены по периферии доминирующего узла, а также от основного сосуда внутрь узла шли множественные сосуды, имеющие в ряде случаев хаотичный ход. Во всех случаях отмечалось увеличение диаметра маточной артерии. По ребру матки и в параметрии наблюдалось обильное развитие артерий, которые были несколько дилатированы. Дилатация сосудов наблюдалась также и внутри узла.
1. Количество ветвей в опухоли составило 18,91±1,70.
2. Площадь, кровоснабжаемая одним сосудом, была 141,67±13,09 мм2.
Второй тип ангиограмм наблюдался у женщин второй группы. Ангиограммы отличались более слабой васкуляризацией миоматозных узлов, при этом расположение сосудов преимущественно было по периферии, также в параметрии контрастировались единичные сосуды.
1. Количество ветвей, кровоснабжающих узлы, составило 10,36±1,04.
2. Площадь узла, кровоснабжаемого 1 сосудистой ветвью, - 329,47±38,10 мм2.
Окончательная оценка регресса опухоли проводилась через 12 месяцев.
У больных первой группы наблюдался быстрый и значительный регресс опухоли - 97,00±3,55%.
Ангиографическими прогностическими критериями выраженного регресса опухоли в этой группе являются:
1) количество ветвей в опухоли - 18,91±1,70;
2) площадь, кровоснабжаемая одним сосудом, - 141,67±13,09 мм2.
У пациенток второй группы (28 женщин васкуляризация узлов была значительно менее выраженной) регресс опухоли был менее выражен и составил 67,20±12,10% (p<0,05).
Ангиографическими прогностическими критериями невыраженного регресса опухоли в этой группе являются:
1) количество ветвей в опухоли - 10,36±1,04;
2) площадь, кровоснабжаемая одним сосудом, составляет 329,47±38,10 мм2.
Клинические примеры:
1. Больная И., 27 лет, поступила в клинику с жалобами на ноющие боли внизу живота, усиливающиеся при физической нагрузке, а также до и в периоде менструации, обильные менструации со сгустками, слабость. Данные клинические симптомы отмечала в течение года. Ранее имела место одна беременность, закончившаяся срочными родами без осложнений. Из экстрагенитальной патологии выявлена вегето-сосудистая дистония по кардиальному типу. При лабораторном исследовании имелось снижение гемоглобина (106,00 г/л) и эритроцитов (3,50·1012/л). Изменений в биохимических анализах крови и коагулограмме обнаружено не было.
По данным УЗИ, сканируется матка, увеличенная до 9-10 недель беременности (91,00×75,00×83,00 мм), правильной формы. Контуры матки ровные, четкие. Стенки матки неоднородной эхоструктуры, мышечный слой с незначительным фиброзным компонентом. По задней стенке визуализируется эхонегативный, интерстициальный узел размерами 61,00×57,00×58,00 мм, с центрипетальным ростом, повышенно васкуляризирован во всех отделах, по периферии до гиперваскуляризированных участков, индекс резистентности - 0,46, пиковая скорость 57,00 см/с. Полость матки ровная, оттеснена узлом кпереди, толщина эндометрия 7,00 мм, однородной эхопозитивной структуры, контуры полости неравномерно утолщены, повышенной эхогенности. Яичники не увеличены, обычной эхоструктуры.
Учитывая молодой возраст женщины, с целью сохранения менструальной функции и репродуктивного органа методом терапии была выбрана ЭМА. В условиях рентгеноперационной под местной анестезией проведена пункция правой бедренной артерии с установлением в ней интрадюссера диаметром 6 Fr. Далее осуществлена последовательная катетеризация левой и правой маточных артерий с ангиографией и эмболизацией. При ангиографии выявлено контрастирование объемного образования размерами 5,50 на 5,70 см, с множественными истонченными сосудами, имеющими выпрямленный ход. В паренхиматозную фазу наблюдалось депонирование контраста. Анализ ангиограмм выявил характерную закономерность 1 типа - выраженный кровоток (фиг 1а):1) количество ветвей, кровоснабжающих узлы, составило около 19,91±1,70 при анализе ангиограмм;
2) площадь, кровоснабжаемая одним сосудом, - около 140,77±13,09 мм, что по прогнозу предполагало выраженный регресс опухоли. После эмболизации на ангиограммах зафиксирована блокада кровотока в миоматозных узлах (фиг 1б).
В течение первого месяца после ЭМА больная отметила значительное уменьшение болевого синдрома, нормализацию менструальной функции. По данным УЗИ, через 1 месяц произошло уменьшение матки до 7 недель беременности (75,00×71,00×82,00 мм) и интерстициального узла до 55,00 мм в диаметре, который был аваскулярен.
Через 2 месяца при УЗИ сканируется матка до 4-5 недель беременности, правильной формы. По задней стенке интерстициальный узел 37,00 мм, без отека и некроза, аваскулярный. Через 5 месяцев после ЭМА на УЗИ сканируется матка средних размеров (64,00×44,00×57,00 мм) правильной формы. По задней стенке узел 19,00×24,00 мм, без кровотока. ЦДК - перфузия матки несколько усилена преимущественно по задней стенке. На УЗИ через 8 месяцев сканируется матка нормальных размеров (50,00×39,00×43,00 мм). Миоматозные узлы не визуализируются.
2. Больная Ч., 42 лет, поступила в клинику с жалобами на боли внизу живота и поясничной области, усиливающиеся при физической нагрузке, а также до и во время менструации, иррадиирующие во влагалище, задний проход, обильные и длительные (до 8 дней) менструации со сгустками, слабость, затруднение при мочеиспускании, запоры, диспареунию. Данные клинические симптомы отмечает в течение полутора лет. Ранее имели место две беременности, закончившиеся срочными родами без осложнений. В течение последующих четырнадцати лет половая жизнь без контрацепции. Из экстрагенитальной патологии выявлено ожирение 1 степени тяжести.
При лабораторном исследовании наблюдалось снижение гемоглобина (110,00 г/л) и эритроцитов (3,40·1012/л). Изменений в биохимических анализах крови и коагулограмме не было обнаружено.
По данным УЗИ, сканируется матка, увеличенная до 20 недель беременности за счет множества интерстицио-субсерозных узлов, максимальным диаметром 93,00 мм, узлы гиперэхогенные. Визуализация затруднена из-за больших размеров матки. Контуры матки неровные. Стенки матки неоднородной эхоструктуры, мышечный слой с выраженным фиброзным компонентом. Трансвагинально сканируется только шейка матки и низко расположенные узлы. Полость матки не видна. Стенки шейки матки однородной эхоструктуры. Сканируются единичные кисты эндоцервикса. Деформаций цервикального канала нет. ЦДК - патологической васкуляризации в шейке матки нет. Кровоток в маточной артерии - пульсовая скорость - 17 см/сек, ИР - 0,60. Яичники не увеличены, обычной эхоструктуры. Свободной жидкости в малом тазу нет.
Учитывая гигантские размеры опухоли, возраст женщины, высокий риск интраоперационного травматизма, была проведена эмболизация маточных артерий. При ангиографии отмечается нормальное заполнение контрастом маточных и внутриматочных артерий с визуализацией объемного образования размерами 104,80 на 85,50 мм, с множественными истонченными сосудами, имеющими выпрямленный ход. Диаметр левой маточной артерии - 3,90 мм, правой - 2,00 мм. В паренхиматозную фазу наблюдается депонирование контраста. Анализ ангиограмм выявил характерную закономерность 2 типа - не выраженный кровоток (фиг 2а.):
1) количество ветвей, кровоснабжающих узлы, составило 11,46±1,04;
2) площадь узла, кровоснабжаемая 1 сосудистой ветвью, - 328,36±37,10 мм2, что предполагало низкий эффект ЭМА. После эмболизации на ангиограммах зафиксирована блокада кровотока в миоматозных узлах (фиг 2б.)
Постэмболизационный синдром протекал с выраженными болями в течение 2 суток, субфебрильной температурой, тошнотой и однократной рвотой. В то же время отклонений в анализах крови не выявлено. Выписана из клиники на 7-е сутки после операции. В течение первого месяца после ЭМА больная отметила уменьшение болевого синдрома и менструальной кровопотери. По данным УЗИ, через 2 месяца произошло уменьшение матки до 19 недель беременности и максимального интерстициального узла до 91,00 мм в диаметре, который аваскуляризирован.
Через 6 месяцев после ЭМА на УЗИ сканируется матка, увеличенная до 19 недель беременности за счет множества интерстицио-субсерозных узлов, максимальным диаметром 91,00 мм, узлы с преобладанием фиброзного компонента. Контуры матки неровные. Стенки матки неоднородной эхоструктуры, мышечный слой с фиброзным компонентом. Трансвагинально сканируется только шейка матки и низкорасположенные узлы. Полость матки не видна. ЦДК - узлы аваскуляризированы. Яичники не увеличены, обычной эхоструктуры. Свободной жидкости в малом тазу нет.
В связи с незначительным регрессом опухоли больной проведено оперативное лечение в плановом порядке в объеме надвлагалищной ампутации матки без придатков. Таким образом, в обоих случаях прогноз регресса оправдался по ангиографическим критериям.
Заявляемый способ обладает высокой точностью, прост в применении, не требует дополнительных затрат, учитывая, что в стандарт помощи входит обязательная ангиография, при этом требует лишь дополнительного расчета при анализе ангиограмм и найдет широкое применение, так как позволит объективно оценить эффективность предлагаемого органосохраняющего метода лечения, прогнозировать изменение качества жизни пациентки на основании предполагаемой степени регресса опухоли и информировать пациентку.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРАНСРАДИАЛЬНОЙ ЭНДОВАСКУЛЯРНОЙ ЭМБОЛИЗАЦИИ МАТОЧНЫХ АРТЕРИЙ | 2014 |
|
RU2551947C1 |
| Способ сочетанного лечения миом матки | 2019 |
|
RU2730926C1 |
| СПОСОБ ЛЕЧЕНИЯ МИОМЫ МАТКИ | 2006 |
|
RU2289415C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ЭМБОЛИЗАЦИИ МАТОЧНЫХ АРТЕРИЙ ПРИ МИОМАХ МАТКИ | 2008 |
|
RU2364335C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ШЕЕЧНОЙ БЕРЕМЕННОСТИ | 2013 |
|
RU2514548C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ ЭМБОЛИЗАЦИИ ВНУТРЕННИХ ПОДВЗДОШНЫХ АРТЕРИЙ У ПАЦИЕНТОК С НОВООБРАЗОВАНИЯМИ МАЛОГО ТАЗА | 2014 |
|
RU2576092C1 |
| Способ определения нецелевой эмболизации маточных артерий | 2021 |
|
RU2768142C1 |
| СПОСОБ СЕЛЕКТИВНОЙ КАТЕТЕРИЗАЦИИ И ЭМБОЛИЗАЦИИ МАТОЧНЫХ АРТЕРИЙ ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ С МИОМОЙ МАТКИ ИЛИ МАТОЧНЫМ КРОВОТЕЧЕНИЕМ | 2014 |
|
RU2550006C1 |
| Способ прогнозирования риска рецидива симптомной миомы матки после проведения селективной эмболизации маточных артерий | 2021 |
|
RU2766809C1 |
| СПОСОБ КОНСЕРВАТИВНОЙ МИОМЭКТОМИИ У БЕРЕМЕННЫХ | 2015 |
|
RU2606494C1 |
Изобретение относится к медицине, а именно к акушерству и гинекологии, сосудистой хирургии. Выполняют ангиографию с помощью рентгеноконтраста урографина или ультрависта во время эмболизации маточных артерий, со скоростью введения контраста 1 мл/с, объемом 4-6 мл и одновременной покадровой съемкой со скоростью 2-4 кадра в секунду. При этом, начиная с артериальной и заканчивая паренхиматозной фазой контрастирования, осуществляют оценку двух параметров: количество ветвей в узле и площадь узла, кровоснабжаемая одним сосудом. Площадь узла, кровоснабжаемую одним сосудом, рассчитывают по формуле. При количестве ветвей, кровоснабжающих узлы, - 18,91±1,70, площади, кровоснабжаемой одним сосудом, - 141,67±13,09 мм2 прогнозируют выраженную степень регресса миомы матки. При количестве ветвей, кровоснабжающих узлы, - 10,36±1,04, площади, кровоснабжаемой одной сосудистой ветвью, - 329,47±38,10 мм2 прогнозируют невыраженную степень регресса миомы матки. Способ позволяет объективно оценить эффективность предлагаемого органосохраняющего метода лечения, прогнозировать изменение качества жизни пациентки и возможность планирования беременности на основании предполагаемой степени регресса миомы матки. 4 ил., 2 пр.
Способ прогнозирования степени регресса миомы матки заключается в проведении ангиографии, которую выполняют с помощью рентгеноконтраста урографина или ультрависта во время эмболизации маточных артерий, со скоростью введения контраста 1 мл/с, объемом 4-6 мл и одновременной покадровой съемкой со скоростью 2-4 кадра в секунду, начиная с артериальной и заканчивая паренхиматозной фазой контрастирования с последующей оценкой кровоснабжения миоматозных узлов по двум параметрам ангиограммы - количеству ветвей в узле и площади узла, кровоснабжаемой одним сосудом, при этом площадь узла, кровоснабжаемую одним сосудом, рассчитывают по формуле
S1=Sy/n,
где S1 - площадь узла, кровоснабжаемая одним сосудом;
Sy - общая площадь узла;
n - количество ветвей, кровоснабжающих узел,
и при количестве ветвей, кровоснабжающих узлы, - 18,91±1,70, площади, кровоснабжаемой одним сосудом, - 141,67±13,09 мм2 прогнозируют выраженную степень регресса миомы матки; при количестве ветвей, кровоснабжающих узлы, - 10,36±1,04, площади, кровоснабжаемой одной сосудистой ветвью, - 329,47±38,10 мм2 прогнозируют невыраженную степень регресса миомы матки.
| САВЕЛЬЕВА Г | |||
| М | |||
| и др., Эффективность и профилактика возмозных осложнений эмболизации маточных артерий при лечении миомы матки, Акушерство и гинекология, 2014, 11, С.74-79 | |||
| СПОСОБ ПРОФИЛАКТИКИ ПОСТОККЛЮЗИОННОГО СИНДРОМА ПРИ РЕНТГЕНЭНДОВАСКУЛЯРНОМ ЛЕЧЕНИИ МИОМ ТЕЛА МАТКИ | 2007 |
|
RU2380098C2 |
| Тихомиров А | |||
| Л., Олейник Ч | |||
| Г., Дифференцированный подход к лечению больных миомой матки, Вопросы гинекологии, акушерства и перинатологии, 2008, | |||
Авторы
Даты
2016-08-27—Публикация
2015-04-16—Подача