Изобретение относится к области нанотехнологии, медицины, ветеринарии.
Ранее были известны способы получения микрокапсул. Так, в пат. 2092155 МПК А61К 047/02, А61К 009/16, опубл. 10.10.1997 Российская Федерация предложен метод микрокапсулирования лекарственных средств, основанный на применении специального оборудования с использованием облучения ультрафиолетовыми лучами.
Недостатками данного способа являются длительность процесса и применение ультрафиолетового излучения, что может оказывать влияние на процесс образования микрокапсул.
В пат. 2095055 МПК А61К 9/52, А61К 9/16, А61К 9/10 Российская Федерация, опубл. 10.11.1997 предложен способ получения твердых непористых микросфер включает расплавление фармацевтически неактивного вещества-носителя, диспергирование фармацевтически активного вещества в расплаве в инертной атмосфере, распыление полученной дисперсии в виде тумана в замораживающей камере под давлением, в инертной атмосфере, при температуре от -15 до -50°С, и разделение полученных микросфер на фракции по размерам. Суспензия, предназначенная для введения путем парентеральной инъекции, содержит эффективное количество указанных микросфер, распределенных в фармацевтически приемлемом жидком векторе, причем фармацевтически активное вещество микросферы нерастворимо в указанной жидкой среде.
Недостатки предложенного способа: сложность и длительность процесса, применение специального оборудования.
В пат. 2076765 МПК B01D 9/02 Российская Федерация, опубл. 10.04.1997 предложен способ получения дисперсных частиц растворимых соединений в микрокапсулах посредством кристаллизации из раствора, отличающийся тем, что раствор диспергируют в инертной матрице, охлаждают и, изменяя температуру, получают дисперсные частицы.
Недостатком данного способа является сложность исполнения: получение микрокапсул путем диспергирования с последующим изменением температур, что замедляет процесс.
В пат. 2101010 МПК А61К 9/52, А61К 9/50, А61К 9/22, А61К 9/20, А61К 31/19 Российская Федерация, опубл. 10.01.1998 предложена жевательная форма лекарственного препарата с вкусовой маскировкой, обладающая свойствами контролируемого высвобождения лекарственного препарата, содержит микрокапсулы размером 100-800 мкм в диаметре и состоит из фармацевтического ядра с кристаллическим ибупрофеном и полимерного покрытия, включающего пластификатор, достаточно эластичного, чтобы противостоять жеванию. Полимерное покрытие представляет собой сополимер на основе метакриловой кислоты.
Недостатки изобретения: использование сополимера на основе метакриловой кислоты, так как данные полимерные покрытия способны вызывать раковые опухоли; сложность исполнения; длительность процесса.
В пат. 2159037 МПК A01N 25/28, A01N 25/30 Российская Федерация, опубл. 20.11.2000 предложен способ получения микрокапсул реакцией полимеризации на границе раздела фаз, содержащих твердый агрохимический материал 0,1-55 мас. %, суспендированный в перемешивающейся с водой органической жидкости, 0,01-10 мас. % неионного диспергатора, активного на границе раздела фаз и не действующего как эмульгатор.
Недостатки предложенного метода: сложность, длительность, использование высокосдвигового смесителя.
В статье «Разраработка микрокапсулированных и гелеобразных продуктов и материалов для различных отраслей промышленности», Российский химический журнал, 2001, т. XLV, №5-6, с. 125-135 описан способ получения микрокапсул лекарственных препаратов методом газофазной полимеризации, так как авторы статьи считают непригодным метод химической коацервации из водных сред для микрокапсулирования лекарственных препаратов вследствие того, что большинство из них являются водорастворимыми. Процесс микрокапсулирования по методу газофазной полимеризации с использованием n-ксилилена включает следующие основные стадии: испарение димера n-ксилилена (170°С), термическое разложение его в пиролизной печи (650°С при остаточном давлении 0,5 мм рт.ст.), перенос продуктов реакции в «холодную» камеру полимеризации (20°С, остаточное давление 0,1 мм рт.ст.), осаждение и полимеризация на поверхности защищаемого объекта. Камера полимеризации выполнена в виде вращающегося барабана, оптимальная скорость для покрытия порошка 30 об/мин. Толщина оболочки регулируется временем нанесения покрытия. Этот метод пригоден для капсулирования любых твердых веществ (за исключением склонных к интенсивной сублимации). Получаемый поли-n-ксилилен высококристаллический полимер, отличающийся высокой ориентацией и плотной упаковкой, обеспечивает конформное покрытие.
Недостатками предложенного способа являются сложность и длительность процесса, использование метода газофазной полимеризации, что делает способ неприменимым для получения микрокапсул лекарственных препаратов в полимерах белковой природы вследствие денатурации белков при высоких температурах.
В статье «Разработка микро- и наносистем доставки лекарственных средств», Российский химический журнал, 2008, т. LII, №1, с. 48-57 представлен метод получения микрокапсул с включенными белками, который существенно не снижает их биологической активности, осуществляемый процессом межфазного сшивания растворимого крахмала или гидроксиэтилкрахмала и бычьего сывороточного альбумина (БСА) с помощью терефталоил хлорида. Ингибитор протеиназ - апротинин, либо нативный, либо с защищенным активным центром был микрокапсулирован при его введении в состав водной фазы. Сплющенная форма лиофилизованных частиц свидетельствует о получении микрокапсул или частиц резервуарного типа. Приготовленные таким образом микрокапсулы не повреждались после лиофилизации и легко восстанавливали свою сферическую форму после регидратации в буферной среде. Величина рН водной фазы являлась определяющим при получении прочных микрокапсул с высоким выходом.
Недостатком предложенного способа получения микрокапсул является сложность процесса, что, в свою очередь, приводит к уменьшению выхода конечных капсул.
В пат. 2359662 МПК А61К 009/56, A61J 003/07, B01J 013/02, A23L 001/00, опубл. 27.06.2009 Российская Федерация предложен способ получения микрокапсул с использованием распылительного охлаждения в распылительной градирне Niro при следующих условиях: температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 об/мин. Микрокапсулы по изобретению обладают улучшенной стабильностью и обеспечивают регулируемое и/или пролонгированное высвобождение активного ингредиента.
Недостатками предложенного способа являются длительность процесса и применение специального оборудования, комплекс определенных условий (температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 об/мин).
В пат. WO/2009/148058 JP МПК B01J 13/04, A23L 1/00, А61К 35/20, А61К 45/00, А61К 47/08), А61К 47/26, А61К 47/32, А61К 47/34, А61К 47/36, А61К 9/50, B01J 2/04, B01J 2/06, опубл. 10.12.2009 описан процесс получения микрокапсул, применимый для промышленного производства, в которых высокое содержание гидрофильного биологически активного вещества, заключенного в оболочку. Предлагаемые микрокапсулы могут быть использованы в пищевой, фармацевтической и в других областях промышленности. В процесс производства применяются диспергирующие композиции, состоящие из гидрофильных биологически активных веществ и ПАВ в твердом жире. Температура не ниже, чем температура плавления твердого жира.
Недостатками данного способа являются сложность и длительность процесса получения микрокапсул.
В пат. WO/2010/119041 ЕР МПК A23L 1/00, опубл. 21.10.2010 предложен способ получения микрошариков, содержащих активный компонент, инкапсулированный в гель-матрице сывороточного протеина, включающего денатурированный белок, сыворотку и активные компоненты. Изобретение относится к способу получения микрошариков, которые содержат такие компоненты, как пробиотические бактерии. Способ получения микрошариков включает стадию производства микрошариков в соответствии с методом изобретения, и последующее отверждение микрошариков в растворе анионный полисахарид с рН 4,6 и ниже в течение не менее 10, 30, 60, 90, 120, 180 минут. Примеры подходящих анионных полисахаридов: пектины, альгинаты, каррагинаны. В идеале, сывороточный протеин является тепло-денатурирующим, хотя и другие методы денатурации, также применимы, например, денатурация индуцированным давлением. В предпочтительном варианте сывороточный белок денатурирует при температуре от 75°С до 80°С, надлежащим образом в течение от 30 минут до 50 минут. Как правило, сывороточный протеин перемешивают при тепловой денатурации. Соответственно, концентрация сывороточного белка составляет от 5 до 15%, предпочтительно от 7 до 12%, а в идеале от 9 до 11% (вес/объем). Как правило, приостановление подлежит процесса, фильтрация осуществляется через множество фильтров с постепенным снижением размера пор. В идеале, фильтр тонкой очистки имеет субмикронных размеров пор, например от 0,1 до 0,9 микрон. Предпочтительным способом получения микрошариков является способ с применением вибрационных инкапсуляторов (Inotech, Швейцария) и машин производства Nisco Engineering AG. Как правило, форсунки имеют отверстия 100 и 600 мкм, а в идеале около 150 микрон.
Недостатком данного способа является применение специального оборудования (вибрационных инкапсуляторов (Inotech, Швейцария)), пролучение микрокапсул посредством денатурации белка, сложность выделения полученных денным способом микрокапсул - фильтрация с применением множества фильтров, что делает процесс длительным.
В пат. WO/2011/160733 ЕР МПК B01J 13/16, опубл. 29.12.2011 описан способ получения микрокапсул, которые содержат оболочки и ядра нерастворимых в воде материалов. Водный раствор защитного коллоида и раствор смеси по меньшей мере двух структурно различных бифункциональных диизоцианатов (А) и (В), нерастворимых в воде, собираются вместе до образования эмульсии, затем добавляется к смеси бифункциональных аминов и нагревается до температуры не менее 60°С до формирования микрокапсул.
Недостатками предложенного способа являются сложность, длительность процесса, использование в качестве оболочек микрокапсул полимеров синтетического происхождения и их смесей.
В пат. WO/2011/161229 ЕР МПК А61К 8/11; B01J 13/14; B01J 13/16; C11D 3/50, опубл. 29.12.2011 описан способ получения микрокапсул, содержащих оболочку из полимочевины и духов в масле, где оболочка получается в результате реакции двух структурно различных диизоцианатов в виде эмульсии. В процессе получения микрокапсул используются защитные коллоиды. Во время реакции изоцианатов и аминов должен присутствовать защитный коллоид. Это предпочтительно поливинилпирролидон (ПВП). Защитный коллоид - полимерная система, которая в суспензии или дисперсии, предотвращает слипание (агломерация, коагуляции, флокуляции). При данном способе может быть использован для духов и всевозможных потребительских товаров. Исчерпывающий перечень потребительских товаров не может быть перечислен. Наглядные примеры потребительских товаров включают в себя все приложения, включая жидкие моющие средства, и порошковых моющих средств; все личной гигиены и ухода за волосами приложений, включая шампуни, кондиционеры, кремы расчесывание, оставьте на кондиционеры, стайлинг крем, мыло, кремы для тела и т.п.; дезодоранты и антиперспиранты.
Недостатками данного способа получения микрокапсул являются сложность и длительность процесса, использование в качестве оболочки микрокапсул диизоцианатов, которые получают в результате реакции двух изоцианатов.
Наиболее близким методом является способ, предложенный в пат. 2134967 МПК A01N 53/00, A01N 25/28, опубл. 27.08.1999 Российская Федерация (1999). В воде диспергируют раствор смеси природных липидов и пиретроидного инсектицида в весовом отношении 2-4:1 в органическом растворителе, что приводит к упрощению способа микрокапсулирования.
Недостатком метода является диспергирование в водной среде, что делает предложенный способ неприменимым для получения микрокапсул водорастворимых препаратов в водорастворимых полимерах.
Техническая задача - упрощение и ускорение процесса получения нанокапсул водораствормых лекарственных препаратов группы пенициллинов в альгинате натрия, уменьшение потерь при получении нанокапсул (увеличение выхода по массе).
Решение технической задачи достигается способом получения нанокапсул лекарственных препаратов группы пенициллинов, характеризующимся тем, что в качестве оболочки нанокапсул используется альгинат натрия, а также получение нанокапсул физико-химическим способом осаждения нерастворителем с использованием осадителя - хлороформа.
Результатом предлагаемого метода является получение нанокапсул лекарственных препаратов группы пенициллинов в альгинате натрия в течение 15 минут. Выход нанокапсул составляет 100%.
ПРИМЕР 1 Получение нанокапсул канамицина в соотношении ядро : облолочка 1:3
К 1,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472 с (сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота - другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием) в качестве поверхностно-активного вещества. Полученную смесь ставят на магнитную мешалку и включают перемешивание. 0,5 г порошка канамицина добавляют небольшими порциями в суспензию альгината натрия в петролейном эфире. Затем добавляют 10 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 2 г белого порошка. Выход составил 100%.
ПРИМЕР 2 Получение нанокапсул канамицина в соотношение ядро : облолочка 1:1
К 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества. 0,5 г порошка канамицина добавляют небольшими порциями в суспензию альгината натрия в петролейном эфире. Затем добавляют 5 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 1 г белого порошка. Выход составил 100%.
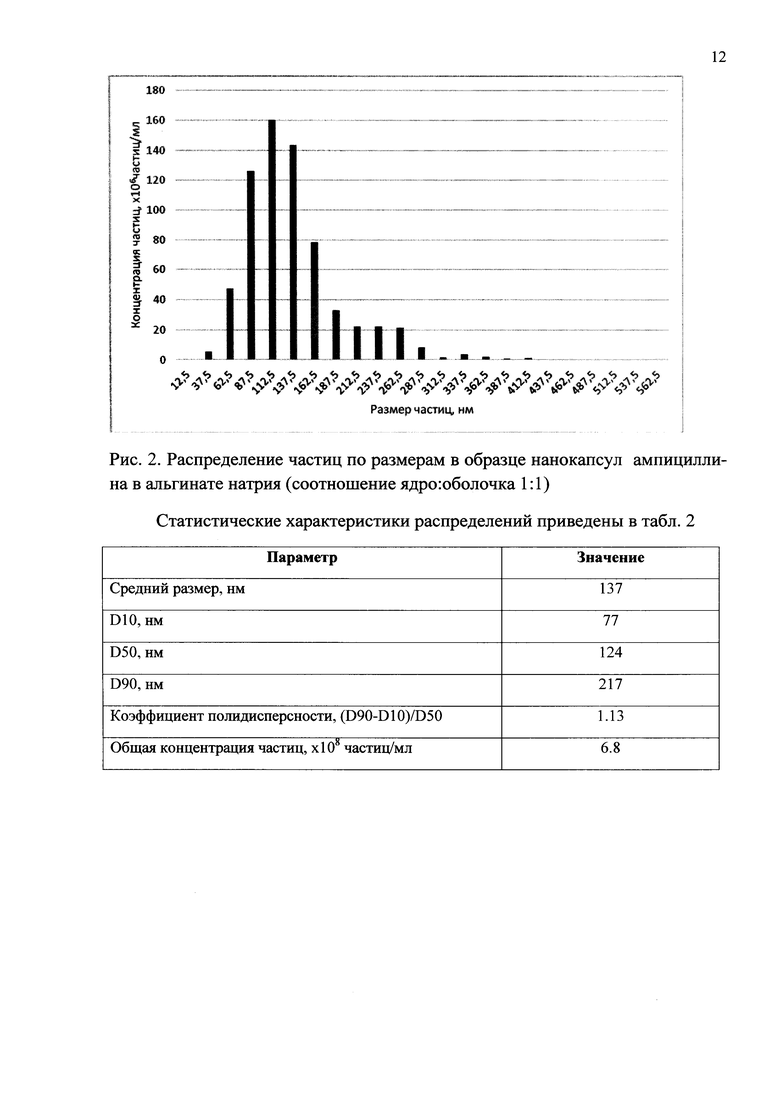
ПРИМЕР 3 Получение нанокапсул ампициллина в соотношении ядро : оболочка 1:1
К 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества. 0,5 г порошка ампициллина добавляют небольшими порциями к суспензии альгината натрия в петролейном эфире. Затем добавляют 5 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 1 г белого порошка. Выход составил 100%.
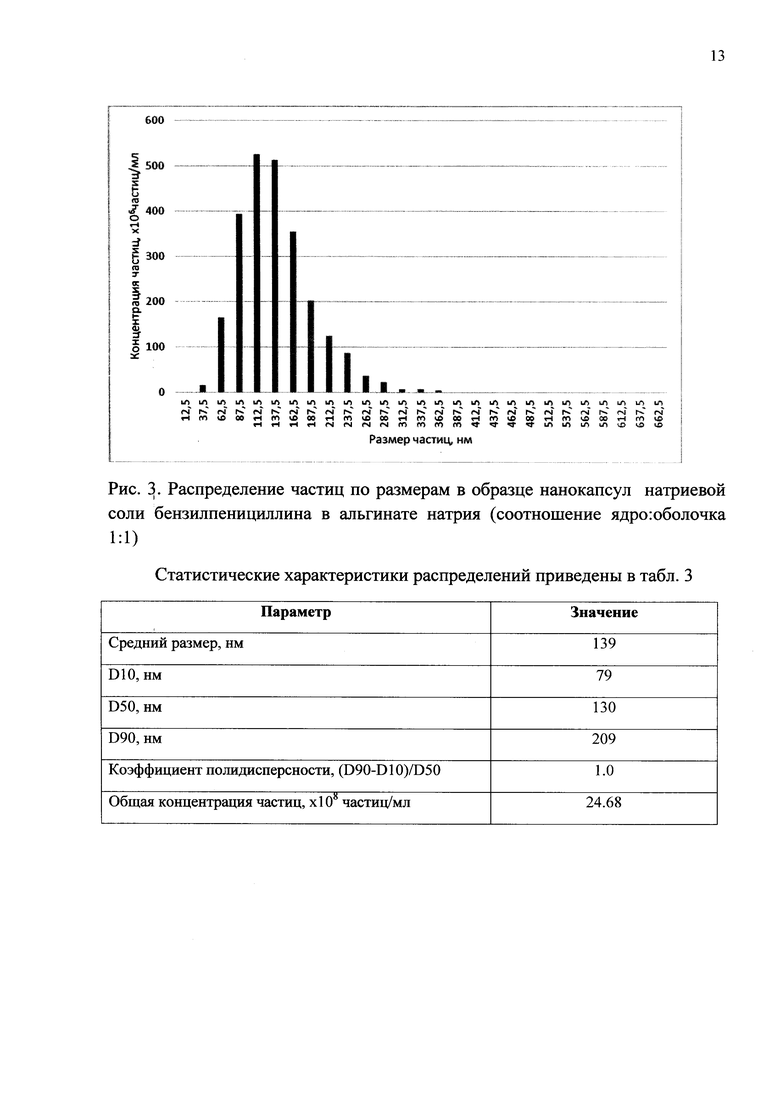
ПРИМЕР 4 Получение нанокапсул натриевой соли бензилпенициллина в соотношении ядро : оболочка 1:1
К 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества. 0,5 г порошка натриевой соли бензилпенициллина добавляют небольшими порциями к суспензии альгината натрия в петролейном эфире. Затем добавляют 5 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 1 г белого порошка. Выход составил 100%.
ПРИМЕР 5 Получение нанокапсул стрептомицина в соотношении ядро : оболочка 1:1
К 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества. 0,5 г порошка стрептомицина добавляют небольшими порциями к суспензии альгината натрия в петролейном эфире. Затем добавляют 5 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 1 г белого порошка. Выход составил 100%.
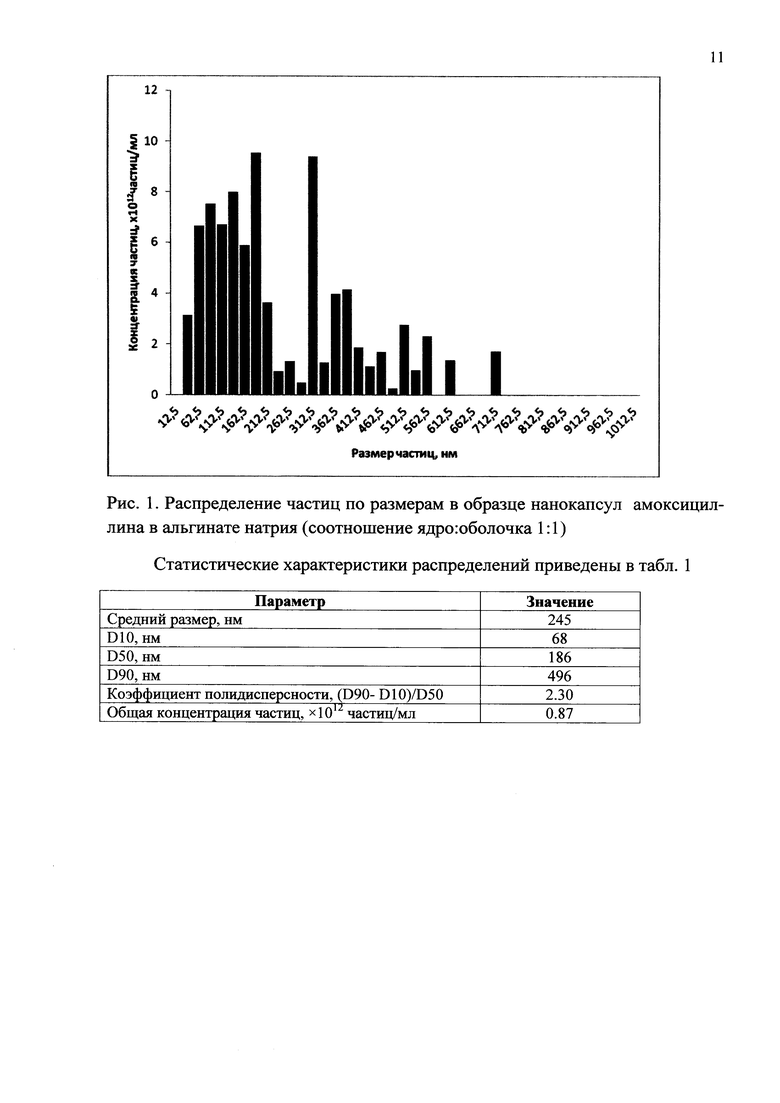
ПРИМЕР 6 Получение нанокапсул амоксициллина в соотношении ядро : оболочка 1:1
К 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества. 0,5 г порошка амоксициллина добавляют небольшими порциями к суспензии альгината натрия в петролейном эфире. Затем добавляют 5 мл хлороформа. Полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
Получено 1 г белого порошка. Выход составил 100%.
ПРИМЕР 7 Определение размеров нанокапсул антибиотиков пенициллинового ряда
Измерения проводили на мультипараметрическом анализаторе наночастиц Nanosight LM0 производства Nanosight Ltd (Великобритания) в конфигурации HS-BF (высокочувствительная видеокамера Andor Luca, полупроводниковый лазер с длиной волны 405 нм и мощностью 45 мВт). Прибор основан на методе Анализа траекторий наночастиц (Nanoparticle Tracking Analysis, NTA), описанном в ASTM E2834.
Оптимальным разведением для разведения было выбрано 1:100. Для измерения были выбраны параметры прибора: Camera Level=16, Detection Threshold=10 (multi), Min Track Length:Auto, Min Expected Size: Auto.длительность единичного измерения 215s, использование шприцевого насоса.
Изобретение относится к способу получения нанокапсул лекарственных препаратов группы пенициллинов, выбранных из ампициллина, натриевой соли бензилпенициллина или амоксициллина. Указанный способ характеризуется тем, что к 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества, к полученной суспензии добавляют небольшими порциями 0,5 г порошка антибиотика, затем добавляют 5 мл хлороформа, полученную суспензию нанокапсул отфильтровывают и сушат. Изобретение обеспечивает упрощение и ускорение процесса получения нанокапсул лекарственных препаратов группы пенициллинов, а также увеличение их выхода по массе. 3 ил., 7 пр.
Способ получения нанокапсул лекарственных препаратов группы пенициллинов, выбранных из ампициллина, натриевой соли бензилпенициллина или амоксициллина, в альгинате натрия, характеризующийся тем, что к 0,5 г альгината натрия в петролейном эфире добавляют 0,01 г препарата Е472с в качестве поверхностно-активного вещества, к полученной суспензии добавляют небольшими порциями 0,5 г порошка антибиотика, затем добавляют 5 мл хлороформа, полученную суспензию нанокапсул отфильтровывают и сушат при 25°С.
| NAGAVARMA B | |||
| V | |||
| N | |||
| "Different techniques for preparation of polymeric nanoparticles", Asian Journal Pharm Clin Res, vol.5, suppl 3, 2012, стр.16-23 | |||
| СОЛОДОВНИК В | |||
| Д., "Микрокапсулирование", 1980, стр.136-137 | |||
| ZHANG DONG "Preparation and property of nano-encapsulated phase change material", Effstock 2009: thermal energy storage for efficiency and sustainability, 2009, реферат, фиг.1,2 | |||
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННЫХ ПРЕПАРАТОВ, СОДЕРЖАЩИХ ПИРЕТРОИДНЫЕ ИНСЕКТИЦИДЫ | 1997 |
|
RU2134967C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ГРУППЫ ЦЕФАЛОСПОРИНОВ В КОНЖАКОВОЙ КАМЕДИ В ХЛОРОФОРМЕ | 2012 |
|
RU2491939C1 |
Авторы
Даты
2017-02-06—Публикация
2015-08-18—Подача