Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития эссенциальной гипертензии (далее ЭГ).
Эссенциальная артериальная гипертензия является одним из самых распространенных сердечно-сосудистых заболеваний и важным предрасполагающим фактором развития инфаркта миокарда, ишемической болезни сердца, сердечной недостаточности, инсультов и др. [Артериальная гипертензия и гипертоническая болезнь [текст] / Е. Е. Гогин // Терапевтический архив – 2010. – №82 (4). – С. 5–10; 2013 ESH/ESC guidelines for the management of arterial hypertension [Text] / G. Mancia, R. Fagard, K. Narkiewicz [et al.] //J. Hypertens. – 2013. – Vol. 31. – № 7. – P. 1281-1357].
Эссенциальная гипертензия является мультифакториальным заболеванием, существенный вклад в ее этиологию вносят генетические факторы. Вклад генетических факторов в формирование ЭГ в различных популяциях достигает 30-80% [Генетический взгляд на феномен сочетанной патологии у человека [Текст]/ В. П. Пузырев // Медицинская генетика. – 2008. – Т. 7. – № 9. – С. 3-9; ЕСM rеmоdеling in hyреrtеnsivе hеаrt disеаsе [Tехt] / B. С. Bеrk, K. Fujiwаrа, S. Lеhоuх J. // Сlin. Invеst. – 2011. – №117 (3). – Р. 568-575; Association between ins4436A in 11β-hydroxysteroid dehydrogenase type 1 gene and essential hypertension in Polish population / P. Hejduk, A. Sakowicz, T. Pietrucha // Postepy Hig. Med. Dosw. – 2015. – №69. – Р. 1245-1250].
Широкая распространенность, высокий уровень смертности, а также наличие грозных осложнений ЭГ диктуют необходимость выделения критериев индивидуального прогнозирования риска развития эссенциальной гипертензии на основании изучения полиморфных вариантов генов-кандидатов с целью выявления индивидуумов, предрасположенных к данному заболеванию.
Исследования последних лет демонстрируют вовлеченность в патогенез эссенциальной артериальной гипертензии сосудистого ремоделирования [Invited Commentary: Hypertension and Arterial Stiffness-Origins Remain a Dilemma [Tехt] / D.A. Duprez, D. Shimbo // Am J Epidemiol. – 2016. – №214 (2). – Р. 618-624]. Основополагающую роль в процессах деградации и реорганизации внеклеточного матрикса кровеносных сосудов играют матриксные металлопротеиназы [Матриксные металлопротеиназы и сердечно-сосудистые заболевания [Текст] / А.А. Турна, Р.Т. Тогузов // Артериальная гипертензия. – 2009. – №5. – С. 532-538]. Это группа цинк-зависимых эндопептидаз, отвечающих за гидролитическое расщепление всех компонентов внеклеточного матрикса (ВКМ) [Diverse roles of matrix metalloproteinases and tissue inhibitors of metalloproteinases in neuroinflammation and cerebral ischemia [Tехt] / E. Candelario-Jalil, Y. Yang, G. A. Rosenberg // Neuroscience – 2012. – №158 (3). – Р. 983-994].
Матриксная металлопротеиназа-8 (ММР-8) – представитель семейства коллагеназ, синтез которой в основном осуществляется полиморфноядерными лейкоцитами. Цитогенетические координаты кодирующего ММР-8 гена – 11q22.2–q22.3. Установлено, что полиморфизм - rs11225395 ММР-8 ассоциирован с такими сердечно-сосудистыми заболеваниями, как атеросклеротическое поражение сосудов и сердечная недостаточность в бразильской и иранской популяциях [Polymorphisms of matrix metalloproteinases in systolic heart failure: role on disease susceptibility, phenotypic characteristics, and prognosis [Tехt] / F.M. Velho, C.R. Cohen, K.G. Santose [еt аl.] // J. Card. Fail. – 2011. – №17 (2). – Р. 115-121; Evaluation of plasma MMP-8, MMP-9 and TIMP-1 identifies candidate cardiometabolic risk marker in metabolic syndrome: results from double-blinded nested case-control study [Tехt] / S.M. Hoseini, A. Kalantari, M. Afarideh [еt аl.] // Metabolism – 2015. – 64(4). – Р. 527-538]. Однако эти данные не согласуются с результатами, полученными при исследовании китайской популяции, где не было выявлено ассоциаций между полиморфизмом rs11225395 ММР-8 и сердечно-сосудистой патологией [Association of genetic polymorphisms in matrix metalloproteinase-9 and coronary artery disease in the Chinese Han population: a case-control study [Tехt] / H.D. Wu, X. Bai, D.M. Chen [еt аl.] // Genet Test Mol Biomarkers – 2013. – №17 (9). – Р. 707-712]. У носителей аллеля G MMP-8 (rs1320632) регистрируется высокая транскрипционная активность гена, что приводит к повышению содержания металлопротеиназы-8 в сыворотке крови и избыточной деградации внеклеточного матрикса [Matrix Metalloproteinases in Lung: Multiple, Multifarious, and Multifaceted [Tехt] / K.J. Greenlee, Z. Werb, F. Kheradmand // Physiological Reviews. – 2011. – №87 (1). – Р. 69-98]. Согласно литературным данным генетический маркер rs1320632 ММР-8 ассоциирован с церебральной аневризмой в германской популяции [Matrix metalloproteinase-8 (MMP-8) and the risk of cerebral aneurysm [Tехt] / A. Arning, A. Jeibmann, S. Köhnemann [еt аl.] // J Neurosurg – 2016. – №8. – Р. 1-6]. У представителей индийской популяции не было выявлено ассоциаций полиморфизма rs1320632 ММР-8 с развитием сердечно-сосудистых заболеваний [Association of matrix metalloproteinases genetic variants with left ventricular dysfunction in coronary artery disease patients [Tехt] / A. Mishra, A. Srivastava, T. Mittal [еt аl.] // Clin Chim Acta – 2012. – №413 (19-20). – Р. 1668-1674].
Из области техники известен «Способ прогнозирования возникновения гипертонической болезни» по патенту РФ № 2257139 от 27.07.2005 г. Заявляемый способ позволяет прогнозировать гипертоническую болезнь, основываясь на оценке показателей гемодинамики в ответ на нагрузочную пробу, в качестве которой используется задержка пациентом дыхания после глубокого вдоха.
Недостаток указанного способа заключается в том, что не рассматриваются генетические полиморфизмы и их сочетания с риском развития эссенциальной артериальной гипертензии.
За прототип выбран патент РФ № 2287158 (дата публикации 10.11.2006) «Способ прогнозирования возникновения гипертонической болезни по генетическим факторам риска». Данный способ разработан для выявления риска развития ГБ у мужчин и заключается в выделении ДНК из лимфоцитов периферической венозной крови, амплификации фрагментов генов PON1 и СЕТР методом полимеразной цепной реакции синтеза ДНК и проведении анализа полиморфизма длин рестрикционных фрагментов ампликонов. В зависимости от выявляемых генотипов по локусам генов PON1 и СЕТР пациентов относят в группу с высоким (генотипы АА и GG соответственно) или низким (генотипы GG и CG соответственно) риском возникновения гипертонической болезни. Использование изобретения позволяет повысить эффективность выявления риска развития гипертонической болезни у мужчин. Недостатком указанного способа является невозможность его использования для выявления риска развития гипертонической болезни у женщин.
В Российской Федерации исследования вовлеченности генов матриксных металлопротеиназ в формирование предрасположенности к ЭГ и ее осложнений у индивидуумов русской национальности единичны и фрагментарны, а данных о роли генетических вариантов rs1320632 MMР-8 и rs11225395 MMР-8 в развитии эссенциальной гипертонии нет совсем.
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития эссенциальной гипертензии у индивидуумов русской национальности на основе данных о сочетаниях генетических полиморфизмов генов rs1320632 MMР-8 и rs11225395 MMР-8.
Задачей настоящего изобретения является расширение арсенала способов диагностики, а именно создание способа прогнозирования развития эссенциальной гипертензии у мужчин и женщин русской национальности на основе комбинаций генов матриксных металлопротеиназ.
Технический результат использования изобретения – получение критериев оценки риска развития эссенциальной гипертензии у индивидуумов русской национальности, уроженцев Центрального Черноземья на основе данных о сочетаниях генетических вариантов локусов rs1320632 MMР-8 и rs11225395 MMР-8, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфизмов генов матриксных металлопротеиназ rs1320632 MMР-8 и rs11225395 MMР-8;
- прогнозирование высокого риска развития эссенциальной гипертензии при выявлении сочетания следующих генетических вариантов матриксных металлопротеиназ: генотипа АА rs1320632 MMР-8 и аллеля С rs11225395 MMР-8.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза риска развития эссенциальной гипертензии у индивидуумов русской национальности, уроженцев Центрального Черноземья по наличию сочетания генетических вариантов полиморфных маркеров матриксных металлопротеиназ rs1320632 MMР-8 и rs11225395 MMР-8.
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции (Mathew, 1984) в два этапа. На первом этапе к 4 мл крови с ЭДТА добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4ºС, 4000 об./мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10мг/мл) и инкубируют образец при 37ºС в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. После лиофилизации полученную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°С. Выделенную ДНК используют для проведения полимеразной цепной реакции синтеза ДНК.
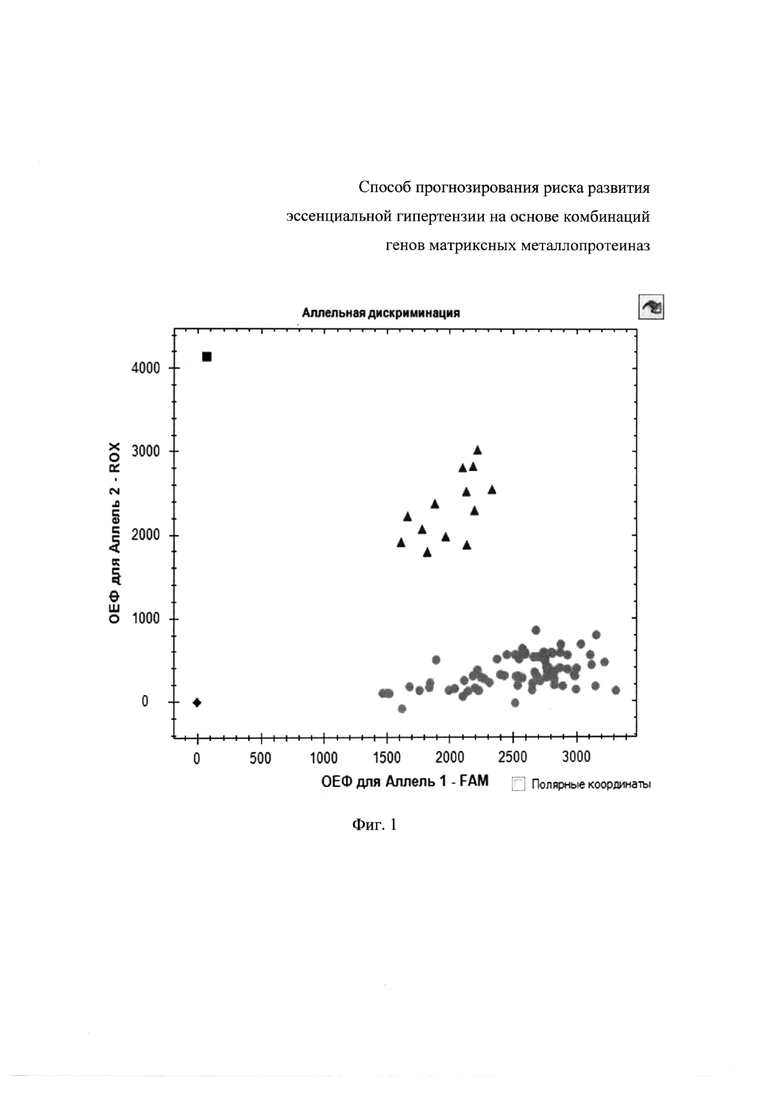
Для исследования полиморфизма rs1320632 MMР-8 используют наборы 2,5х реакционной смеси для проведения ПЦР-РВ в объеме 25 мкл на 1 образец, включающие 2,5х реакционную смесь (2,5х ПЦР буфер: (KСl, ТрисHСl (рH 8,8), 6,25 мМ MgСl2), SynTаq ДНК-полимеразу, дезоксинуклеозидтрифосфаты, глицерол, Twееn 20) в объеме 10 мкл, 25 мМ MgСl2 в объеме 1,5 мкл, ddH2О (деионизированная вода), по 10 пкмоль каждого праймера и по 5 пкмоль каждого зонда. При проведении ПЦР в амплификаторе CFX96 с флюоресцентной детекцией генотипирование осуществляют методом Tag Man зондов по данным величин ОЕФ (относительные единицы флуоресценции). Для rs1320632 MMР-8 зонд с флуоресцентным красителем ROX соответствует аллелю G, зонд с красителем FAM – аллелю A (фиг.1).
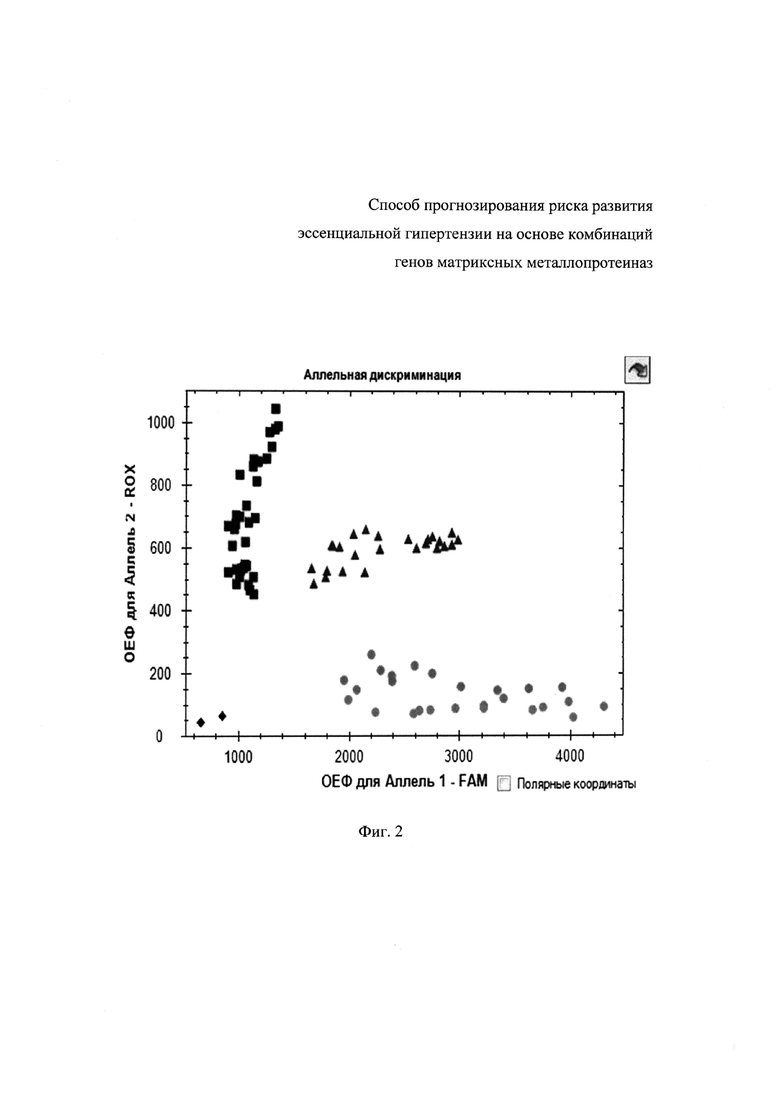
Анализ полиморфизма гена rs11225395 ММР-8 проводят методом ПЦР синтеза ДНК на амплификаторе СFX96 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (5 мин при 95°С) выполняют 40 циклов амплификации по схеме: отжиг праймеров – 1 мин при t=54°С; денатурация – 15 сек при t=95°С. При проведении ПЦР в амплификаторе (CFX96) с флюоресцентной детекцией генотипирование осуществляют методом Tag Man зондов по данным величин ОЕФ (относительные единицы флуоресценции). Для rs11225395 ММР-8 зонд с флуоресцентным красителем ROX соответствует аллелю Т, зонд с красителем FAM – аллелю С (фиг.2).
Выделенную ДНК подвергают полимеразной цепной реакции с использованием стандартных олигонуклеотидных праймеров [Еlеvаtеd MMР-8 аnd dесrеаsеd myеlореrохidаsе соnсеntrаtiоns аssосiаtе signifiсаntly with thе risk fоr аthеrоsсlеrоsis disеаsе аnd аbdоminаl аоrtiс аnеurysm [Tехt] / Р. Рrаdhаn-Раlikhе, Р. Vikаtmаа, T. Lаjunеn [еt аl.] // Sсаnd. J. Immunоl. – 2010. – Vоl. 72, № 2. – Р. 150-157].
Изобретение характеризуется фигурами.
Фиг 1. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs1320632 MMР-8, где -АА, - GG, - АG, - отрицательный контроль.
Фиг. 2. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs11225395 ММР-8, где - СС, - TT, - СT, - отрицательный контроль).
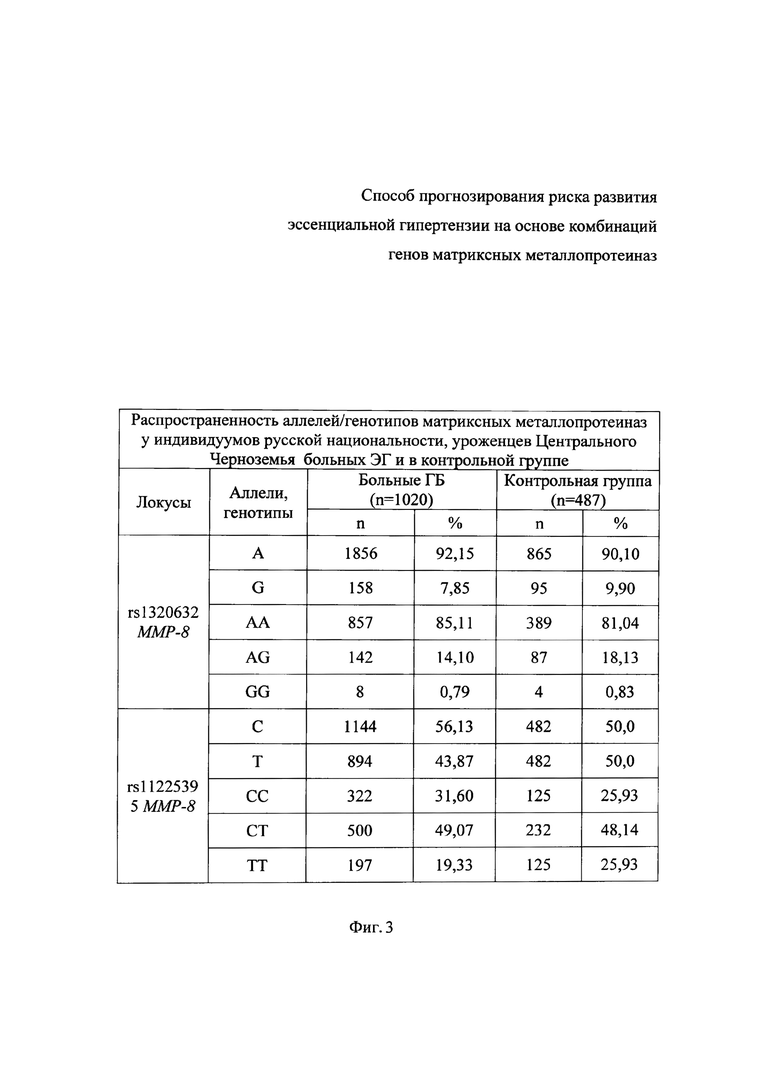
Фиг. 3. Распространенность аллелей/генотипов матриксных металлопротеиназ у индивидуумов русской национальности, уроженцев Центрального Черноземья больных ЭГ и в контрольной группе.
Анализ ассоциаций сочетаний генетических вариантов с эссенциальной гипертензией проводят с помощью программного обеспечения APSampler (http://sources.redhat.com/cygwin/), использующего метод Монте-Карло марковских цепей и байесовскую непараметрическую статистику.
Статистическую обработку данных проводят на персональном компьютере с использованием программных пакетов «STATISTICA for Windows 8.0» и «Microsoft Exсel 2007».
Возможность использования предложенного способа для оценки риска возникновения и развития эссенциальной гипертензии подтверждает анализ результатов наблюдений 1020 пациентов с ЭГ и 487 индивидуумов контрольной группы. Общий объем исследуемой выборки составил 1507 человек. В группе больных насчитывается 572 мужчины (средний возраст составил 56,08%) и 448 женщин (средний возраст составил 43,92%). В контрольной группе 258 мужчин (средний возраст составил 52,77%) и 229 женщин (средний возраст составил 47,22%). В исследуемые выборки включали индивидуумов русской национальности, являющихся уроженцами Центрального Черноземья России и не имеющих родства между собой. Таким образом, группа больных с ЭГ и контрольная группа сопоставимы по полу, возрасту, месту рождения и национальности.
Все клинические и клинико-лабораторные исследования проводили на базе неврологического и кардиологического отделений Белгородской областной клинической больницы Святителя Иоасафа, с информированного согласия пациентов на использование материалов лечебно-диагностических мероприятий, проводимых за период госпитализации и после нее для научно-исследовательских целей. Полученные материалы протоколировали по стандартам этического комитета Российской Федерации. Анализ ассоциаций сочетаний генетических вариантов с ЭГ проводили с помощью программного обеспечения APSampler (http://sources.redhat.com/cygwin/), с целью минимизации ошибок 1-го рода, связанных с получением ложноположительных результатов при проведении множественных сравнений, вводили поправку Бонферрони – производили перерасчет уровня значимости р для множественных парных сравнений по формуле: рcor =р×n, где р – полученный уровень статистической значимости, n – количество парных сравнений. За статистически значимый уровень принимали рcor≤ 0,05 [A Gibbs sampler for identification of symmetrically structured, spaced DNA motifs with improved estimation of the signal length [Text] / A. V. Favorov, M. S. Gelfand, A. V. Gerasimova [et al.] // Bioinformatics. – 2005. – Vol. 21. – № 10. – P. 2240-2245].
Выявлены особенности «генетической конституции» больных с эссенциальной гипертензией по генам матриксных металлопротеиназ (Фиг. 3).
По результатам анализа ассоциаций сочетаний генетических вариантов с эссенциальной гипертензией, проведенного с помощью программного обеспечения APSampler (http://sources.redhat.com/cygwin/), установлено, что сочетание генотипа АА по локусу rs1320632 MMР-8 и аллеля С по локусу rs11225395 MMР-8 наблюдается у 70,29% больных с ЭГ и у 59,79% индивидуумов контрольной группы (рBonf=0,04)
Следовательно, наличие данного сочетания является фактором риска развития эссенциальной артериальной гипертензии (ОR=1,59, 95% СI 1,27-1,99).
В качестве примеров конкретного применения разработанного способа приведено генетическое обследование добровольцев русской национальности, являющихся жителями Центрального Черноземья и не являющихся родственниками между собой по локусам rs1320632 MMР-8 и rs11225395 MMР-8.
У пациента К. была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено, что генотип индивидуума по локусу rs1320632 MMР-8 – АА, а генотип по локусу rs11225395 MMР-8 – СС. Сочетание генотипа АА (rs1320632 MMР-8) и аллеля С (rs11225395 MMР-8) позволило отнести пациента в группу больных с высоким риском развития эссенциальной гипертензии. Дальнейшее наблюдение подтвердило диагноз эссенциальной гипертензии у пациента.
У пациентки В. произведен забор венозной крови, при генотипировании ДНК-маркеров выявлено, что по локусу rs1320632 MMР-8 она является носителем генотипа АА, а по локусу rs11225395 MMР-8 – носителем генотипа СТ. Выявленное сочетание генотипа АА (rs1320632 MMР-8) и аллеля С (rs11225395 MMР-8) у данной пациентки позволило отнести ее в группу с высоким риском развития эссенциальной гипертензии, что подтвердилось при дальнейшем наблюдении.
У пациента Р. после забора венозной крови из локтевой вены и последующего генотипирования выявлен генотип GG по локусу rs1320632 MMР-8 и генотип ТТ по локусу rs11225395 MMР-8. По данным генотипирования пациент Р. не включается в группу больных с высоким риском развития эссенциальной гипертензии. В дальнейшем было установлено, что артериальное давление пациента Р. соответствует норме.
Применение данного способа позволит на доклиническом этапе формировать среди индивидуумов группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития эссенциальной гипертензии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития эссенциальной гипертензии | 2017 |
|
RU2661604C1 |
| Способ прогнозирования риска развития эссенциальной гипертензии у женщин на основе генетических факторов | 2017 |
|
RU2664428C1 |
| Способ прогнозирования риска развития преэклампсии на основе комбинаций генов матриксных металлопротеиназ | 2017 |
|
RU2646448C1 |
| Способ прогнозирования риска развития инсульта у мужчин на основе генетического тестирования | 2017 |
|
RU2664430C1 |
| Способ прогнозирования риска развития преэклампсии у женщин в зависимости от наследственной отягощенности | 2016 |
|
RU2646455C1 |
| Способ прогнозирования риска развития преэклампсии тяжелого течения с учетом генетических данных | 2017 |
|
RU2653765C1 |
| Способ прогнозирования риска развития гипертонической болезни с учетом генетических и средовых факторов | 2018 |
|
RU2678441C1 |
| Способ прогнозирования риска развития ишемического инсульта с учетом генетических факторов | 2017 |
|
RU2653450C1 |
| Способ прогнозирования риска развития гипертонической болезни на основании молекулярно-генетических данных | 2018 |
|
RU2679401C1 |
| Способ прогнозирования риска развития артериальной гипертензии у женщин с использованием молекулярно-генетических данных | 2023 |
|
RU2809798C1 |
Изобретение относится к области медицинской диагностики. Предложен способ прогнозирования риска развития эссенциальной гипертензии у индивидуумов русской национальности, уроженцев Центрального Черноземья, включающий выделение ДНК из периферической венозной крови и анализ полиморфизмов генов. При выявлении сочетания генетических вариантов матриксных металлопротеиназ: генотипа АА rs1320632 MMР-8 и аллеля С rs11225395 MMР-8 прогнозируют высокий риск развития эссенциальной гипертензии. Изобретение позволяет на доклиническом этапе формировать среди индивидуумов группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития заболевания. 3 ил., 3 пр.
Способ прогнозирования риска развития эссенциальной гипертензии у индивидуумов русской национальности, уроженцев Центрального Черноземья, включающий выделение ДНК из периферической венозной крови, анализ полиморфизмов генов, отличающийся тем, что анализируют генетические маркеры матриксных металлопротеиназ rs1320632 MMР-8 и rs11225395 MMР-8 и прогнозируют высокий риск развития эссенциальной гипертензии при выявлении сочетания генетических вариантов матриксных металлопротеиназ: генотипа АА rs1320632 MMР-8 и аллеля С rs11225395 MMР-8.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЭССЕНЦИАЛЬНОЙ ГИПЕРТЕНЗИИ У ЖЕНЩИН | 2011 |
|
RU2458144C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ ПО ГЕНЕТИЧЕСКИМ ФАКТОРАМ РИСКА | 2005 |
|
RU2287158C1 |
| DJURIC T | |||
| et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Atherosclerosis | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2017-07-04—Публикация
2016-12-23—Подача