Изобретение относится к биологии и медицине и может быть использовано в травматологии, ортопедии при изготовлении биологических имплантатов и их глубокой стерилизации при заготовке, консервации и последующем хранении. Также изобретение может быть использовано в работе "тканевых банков" для обеспечения костно-пластическим материалом учреждений здравоохранения.
Важным условием применения костных имплантатов является их абсолютная чистота и стерильность.
Высокая степень стерильности необходима в биоимплантологии, в частности, на завершающих стадиях изготовления костного имплантата в тканевых банках. При их использовании должна быть исключена возможность инфицирования реципиентов бактериальными, грибковыми и вирусными инфекциями. Поэтому технологический процесс изготовления любых имплантатов биологической природы должен завершаться надежной и адекватной стерилизацией с максимально возможным сохранением пластических свойств ткани. Отбор донорского материала, выбор технологии изготовления биологических имплантатов в мировой практике регулируется соответствующими стандартами и контролируется серологическими анализами. Параллельно с решением отмеченных вопросов существуют и другие, которые касаются способов стерилизации биологических тканей. К ним относятся воздействие различных факторов (температура, химическое, радиационное воздействие и т.д.) на эндо- и экзопатогенную флору, присутствующую в донорских тканях, что может привести к денатурации их белковых структур и свести комплекс пластических свойств имплантатов к минимуму или полному исчезновению. Не менее важно обеспечение безопасности производственного персонала тканевого банка, находящегося в непосредственном контакте с биологическим материалом в процессе изготовления имплантатов.
Наиболее применяемыми в настоящее время являются следующие технологии стерилизации имплантатов:
1) паровая стерилизация (автоклавирование),
2) стерилизация с использованием специальных растворов,
3) газовая стерилизация (окись этилена),
4) радиационная (потоком гамма-квантов или быстрых электронов).
Стерилизация, осуществляемая с помощью паровых, воздушных и газовых стерилизаторов, характеризующихся процессом нагрева, не позволяет провести обработку чувствительных к температуре материалов, включая биологические ткани.
Используемые для стерилизации химические вещества чрезвычайно токсичны, а степень ее эффективности зависит от продолжительности воздействия (экспозиции) и интенсивности (концентрации) используемых средств.
Стерилизующими агентами газовых стерилизаторов являются: смесь окиси этилена и бромида метила, формальдегид, этиленоксид в смеси с инертными газами. Такой метод приводит к инактивации морфогенетических белков, потере остеоиндуктивных свойств и усилению иммунологического ответа на имплантируемый материал. Кроме того, окись этилена - токсичное и канцерогенное химическое вещество, которое вызывает мутогенный эффект у растений, бактерий и лабораторных животных.
Известен способ стерилизации аллотрансплантата парами формалина, размещении в герметизируемые стеклянные ампулы, замораживании в холодильной камере при температуре минус 70°С и хранении заготовленного трансплантата до его клинического использования при температуре минус 30°С (см. кн: Имамалиев А.С. Биологическая оценка трансплантируемых тканей. М.: Наука, 1975 г., с. 48-57). Полученный замороженный кортикальный аллотрансплантат отличается высокой механической прочностью, но не обладает, однако, заметными остеоиндуктивными свойствами, не обеспечивает при клиническом использовании быстрой перестройки и высокой регенерации костной ткани в области пересадки.
Известен способ стерилизации и консервации заготовки аллотрансплантата путем размещения и выдерживания ее в соответствующей герметичной таре (упаковке), залитой раствором формалина с добавкой антибиотика, (см.: Савельев В.И. Деминерализованная кость как особая разновидность костно-пластического материала. Сборник научных трудов ЛНИИТО им P.P. Вредена. Заготовка и пересадка деминерализованной костной ткани в эксперименте и клинике. Л.: НИИТО, 1983, с. 3-12 [2]). Использование формалина в качестве консерванта и стерилизатора влечет за собой ряд проблем, обусловленных ограничением времени хранения трансплантата (не более 6-и месяцев), необходимостью отмывки приготовленного трансплантата перед клиническим использованием, токсичностью формалина, а также неудобством хранения и транспортировки трансплантата, погруженного в раствор формалина.
Эффективным обеззараживающим действием характеризуется радиационная обработка. Однако существенным недостатком способа является значительное влияние радиации на остеоиндуктивные свойства имплантатов. В радиационной технологии используется большое многообразие источников ионизирующих излучений, различающихся по активности (в диапазоне 106-1015 Бк). Наибольшее применение нашли опытно-промышленные установки с источником гамма-излучения радионуклида Со60 и ускорители электронов.
Радиационная стерилизация обладает рядом преимуществ: высокая проникающая способность, относительно низкий подъем температуры, что особенно важно, когда стерилизуются биологические материалы, чувствительные к теплу, возможность стерилизации упакованных имплантатов, что исключает их вторичное инфицирование. Стерилизация гамма-излучением Со60, а также потоком быстрых электронов является наиболее распространенным методом радиационного воздействия в работе тканевых банков Европы и Америки. (Trends in radiation sterilization of health care products. - Vienna: International Atomic Energy Agency, 2008). В России этот метод стерилизации, дозой поглощения 25 кГр, используется, например, в тканевом банке Самарского ГМУ. Перед стерилизацией спонгиозных имплантатов их предварительно обезжиривают, замораживают и проводят лиофилизацию. Следует отметить, что такая доза до недавнего времени считалась стандартной и обязательной. Однако сегодня ряд исследователей справедливо отмечают, что для некоторых тканей она может быть деструктивной.
Так известен способ стерилизации кости гамма-лучами (Cornu О. Effect of freeze-drying and gamma irradiation on the mechanical properties of human cancellous bone. / O. Cornu, X. Banse, P.L. Docquier et al. // J. Orthop. Res. - 2000. - Vol. 18, N 3. - Р. 426-431), при котором стерилизацию трансплантатов осуществляют в специальной установке с источником гамма-излучения Со60. До стерилизации образцы тканей подвергают либо замораживанию, либо высушиванию путем вымораживания, что предупреждает, по мнению специалистов, развитие нежелательных изменений, нарушающих в тканях их полезные качества. Оптимальной дозой при этом считают дозу в 2,5 Мрад (25 кГр). После такого воздействия гибнут бактерии, грибки, плесень и вирусы. Однако биологические ткани также не остаются интактными. В них возникают морфологические и биохимические нарушения, которые в зависимости от вида тканей могут привести к их полной клинической непригодности.
Известен способ стерилизации деминерализованного костного матрикса в виде крошки (пат. РФ 2456003) путем радиационного облучения гамма-лучами на установке ГУ-200 (ФГУП «НИИП», Лыткарино). Значение поглощенной дозы 15 кГр. В патенте не содержится сведений о результатах облучения. Данный метод стерилизации пригоден не во всех случаях, не исключает ряда нежелательных побочных эффектов, главным из которых следует считать снижение эффективности остеогенеза с увеличением радиационной дозы. При этом уменьшение дозы облучения может сопровождаться снижением эффективности процесса стерилизации.
Известен способ стерилизации костных трансплантатов химическими антисептиками и гамма-лучами (пат. РФ №2356224). При этом перед облучением трансплантаты замораживают в стерильной упаковке при -70°С и облучают гамма-лучами дозой в 1,2 Мрад. Недостатками известного способа являются: присутствие воды в костной ткани, что может приводить к нежелательным побочным процессам гидролиза при радиационном воздействии, длительность обработки целые сутки.
Известны различные технологии стерилизации и консервации при изготовлении костных имплантатов в зависимости от поставленных задач с использованием стерилизации потоком быстрых электронов дозой 15-18 кГр в течение 16-20 с, например, на ускорителе ЛУЭ-8-5М (пат. РФ №№2172104, 2147800). Основные недостатки данного способа - возможность морфологических изменений, а также разрушения костных морфогенетических белков в получаемом имплантате при величине поглощенной дозы выше 15 кГр.
Известен способ консервации аллотрансплантата с помощью лиофильной (сублимационной) сушки и его стерилизации после окончания сушки путем облучения заготовки, помещенной в герметичную упаковку, пучком ускоренных электронов дозой 15-18 кГр в течение 16-20 с. (пат. РФ №2147800).
Хотя в данном патенте и отмечено, что стерилизация заготовки путем ее облучения пучком ускоренных электронов позволяет надежно уничтожать бактерии, споры и вирусы, сохраняя костный морфогенетический белок в активном состоянии и необходимая для наиболее эффективной стерилизации доза облучения составляет 15-18 кГр (с точки зрения сохранения активности костного морфогенетического белка) и времени облучения помещенной в упаковку заготовки - 16-20 сек, однако многие отечественные и зарубежные исследователи утверждают, что при радиационной стерилизации минимально необходимая для полного уничтожения бактерий доза равна 20 кГр, а для спор и вирусов - 20-40 кГр, но эти дозы уже являются критическими с точки зрения сохранения морфогенетических белков. Более того, известно, что при радиационном облучении биоимплантатов имеют место нарушения морфологии образцов при величине поглощенной дозы выше 15 кГр (Шангина О.Р. Влияние радиационной стерилизации на структуру биоматериалов. Аллоплант: Экспериментально-морфологическое исследование. - Дисс. … канд. биол. наук. Уфа, 1999, 130 с.).
Известен способ стерилизации и консервации, (пат. РФ 2526429), выбранный в качестве прототипа, включающий обработку имплантата в два этапа озоно-воздушной смесью с концентрацией озона 5-50 мг/м3 в течение 7-10 мин перед механической обработкой имплантата и аналогичную окончательную стерилизацию после завершения технологического процесса изготовления имплантата. Озоновую обработку на этапе подготовки исходного костного фрагмента проводят для обеспечения безопасности персонала, непосредственно контактирующего с исходным материалом на всех стадиях изготовления имплантата. Однако в данном случае стерилизующий эффект достигается не только многократной обработкой костного имплантата озоно-воздушной смесью, но и дополнительным стерилизующим воздействием, оказываемым в процессе гидродинамической резки образца высокоэнергетической абразивно-жидкостной струей, связанным со стерилизацией рабочей жидкости режущей гидроструи при высоком давлении и возможном появлении рентгеновского излучения при ударе струи высокого давления о поверхность разрезаемого материала.
Общим недостатком известных методов стерилизации и консервации является невозможность получения 100% степени стерилизации от бактериальных, грибковых и вирусных инфекций, не нарушая остеоиндуктивных свойств образца. Кроме того, существенным недостатком известных способов является продолжительность и сложность процесса химической очистки и подготовки образцов для консервации. Важной составляющей является процесс обеспечения и стерильности герметичной упаковки имплантата, т.к. только при этом условии может осуществляться его длительное хранение. Однако этому вопросу не уделяется должное внимание, возможно потому, что при радиационной стерилизации воздействие оказывается одновременно и в равной степени и на имплантат, и на упаковку. При этом, соответственно, и имплантат, и упаковка получают одинаковую дозу.
Технический результат предлагаемого изобретения состоит в 100-% стерилизации костных имплантатов и герметичной упаковки для их хранения при значительном снижении уровня радиационного облучения трансплантатов, что приводит к морфологической и биопластической сохранности стерилизуемых объектов и сохранению остеоиндуктивных свойств образца, за счет комбинированного использования радиационного облучения и озоно-воздушной смеси.
Достижение технического результата возможно при использовании комбинированного способа стерилизации костного имплантата, включающего начальную обработку образцов озоно-воздушную смесью не менее 10 мин и повторную аналогичную обработку озоно-воздушной смесью перед хранением образцов. Для обработки образцов используют озоно-воздушную смесь с концентрацией озона 6-8 мг/л с последующим окончательным радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов.
Предложенные согласно заявленному изобретению усовершенствования способа стерилизации костных имплантатов являются результатом обобщения экспериментальных исследований по созданию и практическому использованию имплантатов (образцов), изготовленных с использованием вышеуказанных усовершенствований, новых по отношению к способу-прототипу действий, условий и параметров режимов их выполнения. Полученные результаты лабораторных испытаний подтверждают возможность решения поставленной в заявленном изобретении задачи.
Озон О3 - эффективный стерилизатор, способный эффективно уничтожать все виды бактерий, вирусов, грибов и простейших. Преимущества стерилизации озоном - низкотемпературный режим, короткая экспозиция, глубокое проникновение в материал, возможность стерилизации термо-неустойчивых изделий, создание больших объемов стерилизационной камеры, отсутствие токсичности, а также безопасность для окружающей среды. Согласно исследованиям озон обладает сильно выраженными фунгицидными, бактерицидными, вироцидными свойствами («Клинические аспекты озонотерапии» под ред. А.В. Змызговой и В.А. Максимова, М.: НПЦ Озонотерапии, 2003, 288 с.).
В заявляемом изобретении использование при стерилизации комбинированного подхода, на первом этапе которого осуществляется обработка костного имплантата озоно-воздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин, позволяет значительно снизить исходный уровень обсеменения имплантата, что в свою очередь приводит к снижению резистентности патогенов к воздействию радиации. В результате для обеспечения полной стерилизации оказывается достаточным существенно меньший уровень поглощенной дозы - 11-15 кГр, что в свою очередь гарантирует сохранение исходной морфологии костного имплантата, так и функционального потенциала морфогенетических белков костного материала и в целом остеиндуктивных свойств имплантата.
Пример 1 Осуществление заявляемого способа
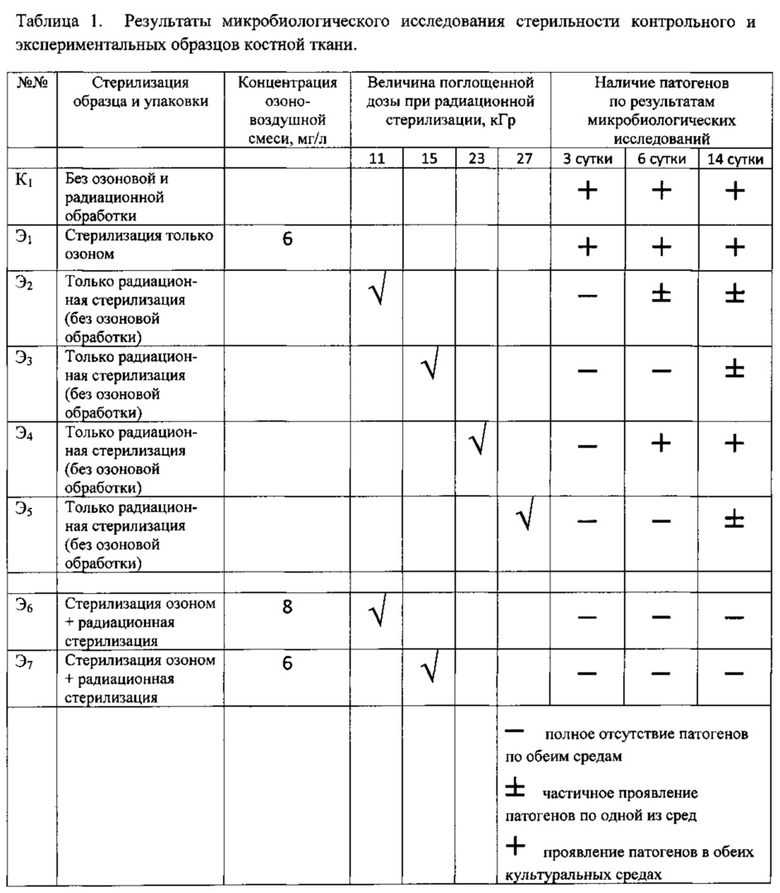
В качестве экспериментального материала были использованы образцы костной ткани быка. Из нативной компактной костной ткани механическим способом вырезаются образцы прямоугольной формы размером 18×8×6 мм. До стерилизации образцы были контаминированы смешанной микрофлорой, результаты эксперимента сведены в таблицу 1.
Контрольный образец K1 не подвергался никакой обработке и был упакован в нестерилизованную термопленку.
Экспериментальный образец Э1 подвергался обработке озоно-воздушной смесью к концентрацией 6-8 мг/л в течение 10-20 минут с последующей герметичной упаковкой в стерилизованную той же озоно-воздушной смесью термопленку.
Экспериментальные образцы Э2-Э5 не подвергались озоновой обработке, они были упакованы в нестерилизованную термопленку и после хранения в течение 3 суток в герметичной упаковке подвергались радиационной стерилизации посредством облучения потоком быстрых электронов с дозой облучения 11, 15, 23 и 27 кГр, соответственно.
Экспериментальные образцы Э6-Э7 подвергались обработке озоно-воздушной смесью к концентрацией 6-8 мг/л в течение 10-20 минут с последующей герметичной упаковкой в стерилизованную той же озоно-воздушной смесью термопленку. После хранения в течение 3 суток в герметичной упаковке образцы подвергались радиационной стерилизации посредством облучения потоком быстрых электронов с дозой облучения 11, 15, 23 и 27 кГр, соответственно.
Для герметичной упаковки использовали термоаппарат типа F70-400 (Нидерланды), позволяющий осуществлять герметизацию двухслойной термопленки DGM Steriguard.
Для получения озоно-воздушной смеси использовали промышленный генератор медицинского озона типа А-с-ГОКСф-5-02-ОЗОН (производство ОАО «Электромашиностроительный завод «Лепсе» (г. Киров, Россия), а также концентратор кислорода Vision Aire (США). Для контроля реального текущего значения концентрации озоно-воздушной смеси во время обработки костных образцов использовали Измеритель концентрации озона ИКО - 50 (производство ОАО «Электромашиностроительный завод «Лепсе» (г. Киров, Россия).
Облучение образцов проводилось на линейном ускорителе электронов непрерывного действия на энергию 1 МэВ с мощностью пучка до 25 кВт. При облучении поглощенные дозы составляли 11, 15, 23 и 27 кГр.
Дозиметрический контроль поглощенной дозы ионизирующего излучения осуществляли с помощью пленочного детектора-дозиметра СО ПД(Ф)Р-5/50 (ГСО 7865-2000) по методике, приведенной в инструкции по использованию детектора.
Далее осуществлялось микробиологическое исследование стерильности контрольного и экспериментальных образцов. Исследование осуществлялось на наличие на образцах костной ткани аэробных и анаэробных бактерий с использованием тиогликолевой среды и микроскопических грибов с использованием среды Сабуро. Инкубация образцов проводилась в пробирках в течение 14 суток при температуре 26°С на среде Сабуро и 37°С на тиогликолевой среде. Результаты регистрировались в динамике и сведены в таблицу 1.
В ходе микробиологических исследований установлено, что контрольный образец K1 и экспериментальный Э1 показали наличие обсеменения уже на 3 сутки культивирования на выбранных культуральных средах.
Экспериментальные образцы, не подвергавшиеся озоновой обработке показали наличие обсемененности на 6-14 сутки хотя бы на одной из культуральных сред.
Полную стерильность на обеих культуральных средах через 14 суток эксперимента продемонстрировали только образцы, подвергавшиеся комбинированному воздействию - последовательной обработке озоно-воздушной смесью с концентрацией 6-8 мг/л в течение 10-20 мин и радиационному облучению с величинами поглощенных доз - 11, 15 и 27 кГр.
Таким образом, показано, что раздельная обработка костных образцов либо только озоно-воздушной смесью, либо только радиационным воздействием с указанными параметрами не обеспечивают полной 100% стерильности костного материала, а их совместное использование обеспечивает надежную стерилизацию при последовательной обработке озоно-воздушной смесью с концентрацией 6-8 мг/л в течение 10-20 мин и последующим радиационным облучением с величиной поглощенной дозы, начиная уже с 11 кГр, при этом не оказывается негативное воздействие на морфологию образцов, функциональный потенциал морфогенетических белков и остеиндуктивные свойства костного материала. Структурно-функциональный анализ с использованием морфологических и биомеханических методов подтвердил отсутствие морфологических изменений и физико-механических свойств исследуемых костных образцов.
При таком подходе достигается значительное уменьшение уровня исходной обсемененности стерилизуемых образцов, а следовательно и их резистентности к радиационному воздействию, что и позволяет обеспечить достижение требуемой стерильности при снижении величины поглощенной дозы радиационного облучения вплоть до 11 кГр.
Необходимо особо отметить, что предлагаемый способ позволяет одновременно решить другой важный вопрос - обеспечение стерильности упаковки имплантата, которая при предлагаемом техническом решении проходит те же две последовательные стадии стерилизации, что и костный имплантат. На первой стадии обработка озоно-воздушной смесью с концентрацией 6-8 мг/л значительно снижает численность патогенов на внутренней поверхности упаковки, что приводит в свою очередь к уменьшению резистентности их оставшейся популяции к радиационному воздействию. В результате на второй стадии - радиационной обработки - пониженной дозой облучения быстрыми электронами в 10-15 кГр оказывается достаточно для обеспечения стерильности упаковки, что гарантирует обеспечение надежности длительного хранения, в то время как в условиях только радиационной обработки это потребовало бы значительно более высокой дозы - не менее 20-40 кГр.
Испытания подтвердили состоятельность предложенного способа по практическому использованию в медицине для стерилизации костных имплантатов. В таком виде имплантат готов к использованию в пластической операции и может храниться при температуре 18-20°С до 5 лет.
Клиническая практика подтверждает также отмеченные выше качества имплантатов, изготовленных по заявленному способу: высокая остеоиндуктивная активность при пересадке и низкая антигенность. Комбинированная стерилизация гарантирует стерильность с одновременным сохранением биопластических свойств материала при длительном хранении.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТОВ | 2013 |
|
RU2526429C1 |
| Способ получения костного имплантата на основе стерильного деминерализованного костного матрикса | 2018 |
|
RU2679121C1 |
| Способ получения биоимплантата на основе стерильного деорганифицированного костного матрикса | 2019 |
|
RU2708235C1 |
| Способ получения костного имплантата с деминерализованным поверхностным слоем | 2019 |
|
RU2732427C1 |
| Способ получения костного имплантата на основе стерильного костного матрикса | 2021 |
|
RU2756246C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТАТОВ | 2004 |
|
RU2268060C1 |
| Способ механической обработки костных образцов in vitro | 2016 |
|
RU2629664C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНОГО АЛЛОТРАНСПЛАНТАТА | 1999 |
|
RU2147800C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ АЛЛОИМПЛАНТАТА НА ОСНОВЕ ХРЯЩЕВОЙ ТКАНИ | 2009 |
|
RU2411923C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ СТЕРИЛИЗАЦИИ КОСТНЫХ ТРАНСПЛАНТАТОВ | 2007 |
|
RU2356224C1 |
Изобретение относится к области медицины, а именно к травматологии и ортопедии, и предназначено для стерилизации костного имплантата. Для стерилизации костного имплантата осуществляют начальную обработку образцов озоно-воздушной смесью и повторную аналогичную обработку озоно-воздушной смесью перед хранением образцов. Обработку образцов и упаковки для них осуществляют озоно-воздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин с последующим окончательным радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов. Использование изобретения обеспечивает эффективную стерилизацию костных имплантатов и герметичной упаковки для их хранения при значительном снижении уровня радиоационного облучения трансплантатов, что приводит к морфологической и биопластической сохранности стерилизуемых объектов и сохранению остеоиндуктивных свойств образца, за счет комбинированного использования радиационного облучения и озоно-воздушной смеси. 1 табл., 1 пр.
Комбинированный способ стерилизации костного имплантата, включающий начальную обработку образцов озоно-воздушной смесью и повторную аналогичную обработку озоно-воздушной смесью перед хранением образцов, отличающийся тем, что обработку образцов и упаковки для них осуществляют озоно-воздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин с последующим окончательным радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов.
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТОВ | 2013 |
|
RU2526429C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНОГО АЛЛОТРАНСПЛАНТАТА | 1999 |
|
RU2147800C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТАТОВ | 2004 |
|
RU2268060C1 |
| CN 104383600 А, 04.03.2015 | |||
| WO 2010070416 A1, 24.06.2010 | |||
| WO 03099346 A2, 04.12.2003. | |||
Авторы
Даты
2017-09-08—Публикация
2016-07-29—Подача