Изобретение относится к медицине, а именно: к травматологии, ортопедии, гнойной хирургии и остеологии, к другим отраслям восстановительной хирургии для репарации соединительной ткани в инфицированных ранах, может быть применено в работе «костных банков» для обеспечения костными имплантатами, а также в целях репродукции тканей и биопротезирования.
Известны различные технологии получения трансплантатов и имплантатов в зависимости от поставленных задач.
Так, известен способ насыщения трансплантатов костной губчатой ткани медикаментами путем помещения их в раствор лекарственных средств (пат. РФ №2170016). На отмытую губчатую ткань в виде крошки, залитую раствором лекарственного средства, воздействуют низкочастотным ультразвуком частотой 24,5-28,5 кГц средней интенсивности. Способ позволяет повысить качество насыщения костных трансплантатов и ускорить процесс насыщения. Однако, недостатком предложенного способа является то, что трансплантат изготавливается в виде крошки и отсутствует возможность придания ему необходимых форм и размеров с учетом ориентации остеонных структур костной ткани.
Известней способ получения биоактивного костно-пластического материала «Депротекс» (пат. РФ №2232585). Для получения материала депротеинизированную кость измельчают до размера частиц 0,1-0,5 мм, полученную костную муку соединяют с 9% желатином с добавлением антибактериального препарата, консервируют и стерилизуют. Данный метод кроме плюсов имеет и определенные недостатки: в результате удаления органической фазы, материал освобождают от морфогенетических белков, которые стимулируют остеогенез в костной ткани.
Известней способ получения биоактивного костно-пластического материала «Костма» (пат. РФ №2211708). Для получения биоактивного костно-пластического материала костную муку соединяют в пропорции 2:1 с 9% раствором желатина при 38-40°C с добавлением антибактериальных препаратов. Недостатком метода является то, что в качестве основного компонента используется нативная аллокостная мука, в которой костные морфогенетические белки находятся в связанном с минеральным компонентом состоянии, затрудняющем формирование очагов регенерации и проявление остеоиндуктивных свойств получаемого материала.
Известней способ получения биоактивного костно-пластического материала «Оргамакс» (пат. РФ №2344826). Деминерализованную кость измельчают до костной муки с размером частиц 0,1-0,5 мм и смешивают в соотношении 1:1 с приготовленным 20% коллагенсодержащим раствором. Для создания тканеинженерных композиций стерилизованный материал обогащают факторами роста или культурой клеток непосредственно перед операцией. Данный метод кроме очевидных плюсов имеет и определенные недостатки - костно-пластический материал не имеет антимикробных, противовирусных и противомикотических свойств.
Известен способ лечения оскольчатых переломов длинных трубчатых костей (пат РФ №2253393) с помощью аллопластического препарата «КоллапАн», который содержит синтетический гидроксиапатит, коллаген и антибиотик для профилактики гнойно-воспалительных дефектов. Известным недостатком этого метода являются возможные аллергические реакции на антибиотики, входящие в состав препарата (гентамицин, линкомицин, метронидазол, клафоран, рифампицин, диоксидин, изониазид). Кроме того, искусственная гидроксиапатитная керамика, входящая в состав препарата не содержит клеточных элементов и морфогенетического белка, который в норме содержится в костной ткани.
Кроме того, все вышеперечисленные известные методы получения костно-пластического материала, имеют один общий недостаток - в материале нарушена микроструктура каналов костной ткани, что затрудняет миграцию клеток в процессе остеосинтеза.
Известен способ изготовления костного имплантата (пат. РФ 2526429), включающий механическую обработку гидродинамической струей фрагмента костной ткани, деминерализацию заготовки в растворе неорганической кислоты, нейтрализацию остатков кислоты, промывку заготовки из костного материала, ее стерилизацию и консервацию. Стерилизацию имплантата осуществляют озоно-воздушной смесью с концентрацией озона 5-50 мг/м3 в течение 7-10 мин перед механической обработкой и аналогичную окончательную стерилизацию после завершения технологического процесса изготовления имплантата.
Известен способ получения костного трансплантата (пат РФ №2223104) путем депротеинизации фрагментов в 0,01% растворе химопсина, затем в 10% растворе перекиси водорода в течение 48 часов, обработку жидким эфиром, высушивание и обработку 10% раствором хлористого лития в течение 16 часов и стерилизацию целевого продукта. При этом фрагменты длинных трубчатых костей депротеинизируют в растворе химопсина в течение 96 часов, а при обработке 10% раствором перекиси водорода их помещают в переменное магнитное поле при 45°С. Очевидным недостатком этого метода является то, что в процессе удаления органической фазы, материал освобождают от морфогенетических белков, которые стимулируют остеогенез в костной ткани. Кроме того, трансплантату не придают антимикробных свойств, что затрудняет его применение в гнойной остеологии при репарации инфицированных ран.
Известен комбинированный способ стерилизации костного имплантата (пат РФ №2630464), выбранный в качестве прототипа, включающий начальную обработку образцов озоно-воздушной смесью и повторную аналогичную обработку озоно-воздушной смесью перед хранением образцов. Обработку образцов осуществляют озоно-воздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин с последующим окончательным радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов.
Технический результат изобретения состоит в технологии получения имплантатов с использованием инновационных методов изготовления со 100% стерилизацией костных имплантатов при сохранении их остеоиндуктивных свойств, морфологической и биопластической сохранности, с приданием имплантатам антимикробных, антивирусных и противомикотических свойств за счет иммобилизации лекарственного средства.
Достижение технического результата возможно при использовании способа получения костного имплантата на основе стерильного деминерализованного костного матрикса, включающего механическую обработку костной ткани, деминерализацию заготовки с последующей комбинированной стерилизацией озоно-воздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин и радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов. При этом механическую обработку костного матрикса проводят с учетом направления остеонных структур кости в стерильном охлажденном до 4°С растворе Рингера с содержанием сангвиритрина 0,01% в пересчете на активное вещество, и дополнительно осуществляют инкубацию деминерализованного костного матрикса в 0,2% растворе сангвиритрина при температуре 37°С в течении 72-144 часов, после чего готовое средство сушат при 20°С и упаковывают.
Препарат Сангвиритрин является природным фитоантисептиком, Производитель: ПЭЗ ВИЛАР ГУП (Россия). Сангвиритрин (ВФС 42-948-80 от 26.02.1980) представляет собой сумму бисульфатов природных алкалоидов сангвинарина и хелеритрина (близкие по структуре и свойствам четвертичные бензофенантридиновые алкалоиды), получаемых из травы маклейи сердцевидной (Macleya cordata Willd. R. Br.) и маклейи мелкоплодной (Macleya microcarpa Maxim. Fedde) семейства Papaveraceae. Это кристаллический порошок от светло-желтого до темно-оранжевого цвета, без запаха, горького вкуса, хорошо растворим в воде при нагревании до 50°С. Сангвиритрин обладает широким спектром антимикробной активности, ингибирует рост патогенных и условно патогенных микроорганизмов рода Staphylococcus, Streptococcus, Enterococcus, Shigella, Escherichia, Salmonella, Proteus, Acinetobacter, Citrobacter, Pseudomonas, Serratia, Klebsiella, Antracoides, Cryptococcus, патогенных грибов рода Microsporum, Trichophyton, Nocardia, Aspergillus, дрожжеподобных грибов рода Candida и др., а также Actinomyces и паразитических простейших рода Trichomonas и Entamoeba. Сангвиритрин активен в отношении моно- и полирезистентных штаммов микроорганизмов, в том числе рода Staphylococcus и Candida. Важной особенностью сангвиритрина является отсутствие возникновения устойчивости к нему микроорганизмов.
Изобретение иллюстрируется следующим примером.
Пример 1 Получение костного имплантата
С эндостальной и периостальной поверхностей кортикальной костной ткани из фрагмента диафиза бедренной кости быка удаляют мягкие ткани и костный мозг. Затем заготовки помещают в 3% раствор перекиси водорода на 1 час для удаления компонентов крови из компактного слоя и проводят первичную стерилизацию костных образцов методом озоновой стерилизации - обработкой в проточном режиме струей озоно-кислородной смеси с концентрацией 6-8 мг/л в течение 7-10 минут. Затем фрагмент кости механически обрабатывают в стерильном охлажденном до 4°С растворе Рингера с содержанием сангвиритрина 0,01% в пересчете на активное вещество с помощью полых цилиндрических фрез для получения необходимого количества цилиндрических образцов 5×7,5 мм и 5×12,5 мм, а также с использованием прецизионного отрезного станка и фрез с алмазным напылением для придания им требуемой формы с учетом направления остеонных структур кости. На заранее подготовленных контрольных образцах костной ткани осуществляют контроль качества костной ткани (механические испытания: на сжатие, микротвердость; микроскопические исследования: фрактографический 3D-анализ, исследование морфологии ткани с помощью световой и сканирующей микроскопии). Для улучшения сорбционной способности, прошедшие контроль заготовки подвергают деминерализации с помощью соляной кислоты 0,8 моль/дм3 (0,8 н) в течение 72 часов. Для контроля степени деминерализации производят контроль с помощью световой микроскопии и элементный анализ контрольных деминерализованных образцов с помощью энергодисперсионной рентгеновской спектроскопии. На основе полученных деминерализованных костных заготовок проводят иммобилизацию сангвиритрина, путем инкубации заготовок в 0,2% раствор сангвиритрина при 37°С на срок от 72 до 144 часов. При указанной температуре не наблюдается выпадения сангвиритрина в осадок.
Производят спектрофотометрический контроль времени высвобождения сангвиритрина в физиологический раствор (натрия хлорид) и проверку высвобожденного сангвиритрина на подлинность с помощью реактива Майера. Полученные образцы высушивают при 20°С и герметично упаковывают в инертной стерилизующей среде - озоно-воздушной смеси с последующим радиационным облучением с величиной поглощенной дозы 10-15 кГр, что обеспечивает 100% стерилизацию. После проведения окончательной стерилизации комбинированным способом - озоно-воздушной смесью и радиационным воздействием, проводят повторные механические испытания контрольных образцов.
Подлинность высвобожденного после отмывки образцов сангвиритрина в физиологический раствор проверяли в соответствии с фармакопейной статьей ФС42-3572-98 (Раствор сангвиритрина 0,2%). К 5 мл физиологического раствора с высвобожденным из образцов сангвиритрином прибавляли 3 капли реактива Майера. 5 мл раствора дали характерную реакцию на сульфаты, в растворе образовался осадок желто-оранжевого цвета (алкалоиды), что свидетельствует о подлинности высвобожденного из образцов сангвиритрина и отсутствии химического взаимодействия между коллагеном деминерализованного костного матрикса и сангвиритрином. Следовательно, высвобожденный в физраствор сангвиритрин обладает антимикробной и терапевтической активностью.
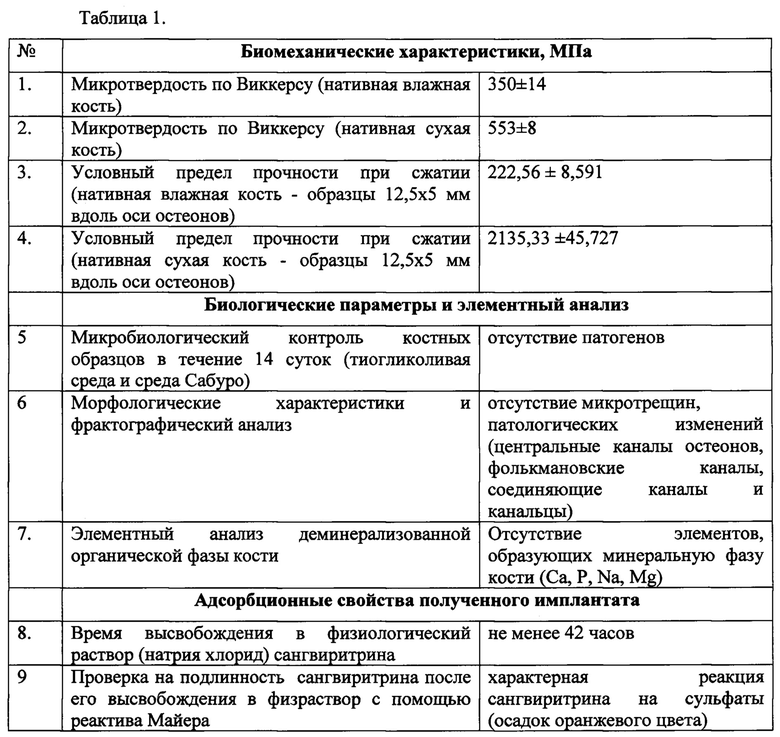
Результаты контрольных испытаний костного имплантаи до и после стерилизующего физико-химического воздействия соответствуют разработанным критериям качества (см. таблица 1) для производства костного импланта на основе деминерализованной кортикальной кости диафиза бедренной кости быка и сангвиритрина.
Испытания подтвердили состоятельность предложенного способа по практическому использованию для выполнения хирургической операции, репарации соединительной ткани в инфицированных ранах и гнойной остеологии и может храниться при температуре 18-20°С до 5 лет.
Комбинированная стерилизация и антимикробные, антивирусные и противомикотические свойства за счет иммобилизации лекарственного средства растительного происхождения - сангвиритрин гарантируют стерильность с одновременным сохранением биопластических и остеоиндуктивных свойств материала при длительном хранении.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения биоимплантата на основе стерильного деорганифицированного костного матрикса | 2019 |
|
RU2708235C1 |
| Способ получения костного имплантата с деминерализованным поверхностным слоем | 2019 |
|
RU2732427C1 |
| Способ получения костного имплантата на основе стерильного костного матрикса | 2021 |
|
RU2756246C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТОВ | 2013 |
|
RU2526429C1 |
| Способ механической обработки костных образцов in vitro | 2016 |
|
RU2629664C1 |
| Комбинированный способ стерилизации костных имплантатов | 2016 |
|
RU2630464C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТАТОВ | 2004 |
|
RU2268060C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕМИНЕРАЛИЗОВАННОГО КОСТНОГО МАТРИКСА В ВИДЕ КРОШКИ | 2011 |
|
RU2456003C1 |
| БИОРЕЗОРБИРУЕМЫЙ БИОЛОГИЧЕСКИЙ МАТРИКС ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2665962C1 |
| ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА ДЛЯ ЗАМЕЩЕНИЯ КОСТНОЙ ТКАНИ | 2019 |
|
RU2708639C1 |
Настоящее изобретение относится к способу получения костного имплантата на основе стерильного деминерализованного костного матрикса, включающий механическую обработку костной ткани, деминерализацию заготовки с последующей комбинированной стерилизацией озоновоздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин и радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов, причем механическую обработку костного матрикса проводят с учетом направления остеонных структур кости в стерильном охлажденном до 4°С растворе Рингера с содержанием сангвиритрина 0,01% в пересчете на активное вещество, и последующую инкубацию деминерализованного костного матрикса в 0,2% растворе сангвиритрина при температуре 37°С в течение 72-144 часов, после чего готовое средство сушат при 20°С и герметично упаковывают. Технический результат – создание инновационного метода получения костных имплантатов со 100% стерилизацией костных имплантатов при сохранении их остеоиндуктивных свойств, морфологической и биопластической сохранности при длительном хранении, с приданием имплантатам антимикробных, антивирусных и противомикотических свойств. 1 табл., 1 пр.
Способ получения костного имплантата на основе стерильного деминерализованного костного матрикса, включающий механическую обработку костной ткани, деминерализацию заготовки с последующей комбинированной стерилизацией озоновоздушной смесью с концентрацией озона 6-8 мг/л и продолжительностью 10-20 мин и радиационным облучением потоком быстрых электронов с величиной поглощенной дозы 11-15 кГр герметично упакованных образцов, отличающийся тем, что механическую обработку костного матрикса проводят с учетом направления остеонных структур кости в стерильном охлажденном до 4°С растворе Рингера с содержанием сангвиритрина 0,01% в пересчете на активное вещество, и последующую инкубацию деминерализованного костного матрикса в 0,2% растворе сангвиритрина при температуре 37°С в течение 72-144 часов, после чего готовое средство сушат при 20°С и герметично упаковывают.
| Способ механической обработки костных образцов in vitro | 2016 |
|
RU2629664C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТОВ | 2013 |
|
RU2526429C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОСТНОГО ТРАНСПЛАНТАТА | 2001 |
|
RU2223104C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТАТОВ | 2004 |
|
RU2268060C1 |
| Комбинированный способ стерилизации костных имплантатов | 2016 |
|
RU2630464C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНОГО АЛЛОТРАНСПЛАНТАТА | 1999 |
|
RU2147800C1 |
| КОМБИНИРОВАННЫЙ КОСТНЫЙ АЛЛОТРАНСПЛАНТАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2524618C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИОАКТИВНОГО КОСТНО-ПЛАСТИЧЕСКОГО МАТЕРИАЛА "ДЕПРОТЕКС" | 2001 |
|
RU2232585C2 |
| US 5513662 A, 07.05.1996. | |||
Авторы
Даты
2019-02-06—Публикация
2018-11-23—Подача