Изобретение относится к нефтедобывающей промышленности, в частности к составам и способам термогазохимической обработки призабойной и удаленной зон нефтеносных пластов.
Изобретение может быть использовано в условиях нормальных и низких пластовых давлений (с различным типом коллектора), для повышения проницаемости призабойной зоны продуктового пласта и увеличения производительности скважины при добыче нефти, газа и газового конденсата. Прежде всего изобретение направлено на расширение и увеличение естественных и образование вновь создаваемых искусственных трещин с последующим воздействием термогазохимическим составом на всю толщу нефтегазоносного пласт.
Известны разнообразные термогазохимические составы для обработки призабойной зоны нефтегазоносного пласта. Например, смеси гранулированного магния с аммиачной селитрой в углеводородной жидкости с последующей закачкой в пласт 15-18% раствора соляной кислоты (А.С. 640023, МПК2 Е21В 43/34). Известны способы термохимической обработки призабойной зоны пласта путем закачки в эту зону горюче-окислительных составов (ГОС) на основе смесей нитрата аммония (15-20%), нитрита натрия (15-40%), стабилизатора (0-2%), эмульгатора (0,1-25) и нефти (10-25%) (Патент RU 2525386C2 от 10.08.2014) и инициатора реакции, представляющего собой 15-37% раствор неорганической кислоты. Подобный процесс термо- и газохимической обработки, включающий последовательную закачку в продуктовый пласт бинарной смеси аммониевой соли минеральной кислоты (NH4Cl, (NH4)2SO4, NH4NO3 и др.) и раствора нитрита щелочного металла с последующей закачкой активатора реакции, в качестве которого используются слабые кислоты или растворы сильных минеральных кислот (US 2014/0090839 А1, Apr. 3.2014).
Наиболее близким к предлагаемому изобретению является способ химического инициирования реакций тепло- и газовыделения под действием 15-37% соляной кислоты или 15-100% раствора органической кислоты в углеводородной среде. При этом предполагаются следующие 5 реакций, приводящих к образованию азота и воды с выделением большого количества тепла:





Вышеприведенная схема не полностью отражает реальные процессы, происходящие при смешивании водных растворов нитрита натрия с минеральными или органическими кислотами. В частности, большой удельный вес в суммарном процессе имеет реакция образования азотистого ангидрида по реакции (6)

Общеизвестно, что большое количество азотистой кислоты в реакции нитрозирования аминов теряется по уравнению (6), даже в условиях проведения реакции с интенсивным перемешиванием в гомогенных растворах. В случае последовательной подачи кислоты, как инициатора реакции (1)-(6) в условиях отсутствия перемешивания, что реализуется в призабойной зоне, всегда будут существовать локальные зоны повышенных концентраций кислоты, что будет подавлять реакцию (4) и усиливать реакцию (6).
В реальных условиях при закачивании эмульсии горюче-окислительной смеси (ГОС) в пористый нефтеносный пласт образуется не перемешиваемый слой эмульсии нитрата аммония и нитрита натрия, отделенный слоем воды или слоем нефти и кислоты, добавленной в последнюю очередь. Контакт между кислотой и эмульсией бинарной смеси затруднен и взаимодействие компонентов по реакциям (1)-(6) происходит в результате диффузии в порах и трещинах продуктового слоя. Реальная скорость такого процесса очень низкая и соответственно коэффициент полезного использования энергетического потенциала системы NH4NO3-NaNO2 очень низкий.
Экспериментальная проверка подобных систем проведена на стендовой установке, в трубчатом реакторе длиной 1,5 м и диаметром 76 мм, заполненном гранулированным порошком (песком, пропантом и т.п.), моделирующим состав нефтегазонасыщенного пласта, показала, что даже после трехсуточной выдержки реакция разложения нитрита аммония образующегося по равновесной реакции (7)

не заканчивается полностью.
Этот принципиальный недостаток относится в полной мере и к патенту US 2014/0090839 A1.
Химическая схема, приведенная в патенте US 2014/0090839 А1
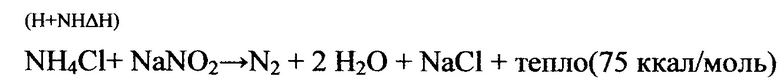
так же как в термохимическом составе для обработки призабойной и удаленной зон продуктивного пласта (Патент RU 2525386) чрезвычайно упрощена. Возможность образования азотистого ангидрида, так же как и других окислов азота, ни в одном патенте не упоминается. В то же время отмечается, что температура при завершении окислительно-восстановительной реакции может достигать 560°F (287°С). В этих условиях неизбежно будут протекать реакции нитрования и нитрозирования углеводородов от C1 до C8. При температурах 250-300°С конверсия углеводородов в соответствующие нитросоединения составляет 30÷40% за время 0,2÷0,5 сек. Образовавшиеся нитро- и нитрозосоединения будут попадать в добываемую нефть, что может существенно повлиять на безопасность дальнейшей переработки нефти (Ф. Азингер. Парафиновые углеводороды, Москва, 1959 год. Стр. 287-300).
Принципиальным недостатком термохимического состава для обработки призабойной и удаленной зон продуктивного пласта является повышенная опасность (Патент RU 2525386 С2 от 10.08.2014). Эмульсия смесей NaNO2/NH4NO3 с 10-25% нефти представляют собой ни что иное, как эмульсионные взрывчатые вещества (ВВ). Поступление таких ВВ в зону разложения бинарной смеси с температурой выше 250°С легко может перейти во взрыв, который в свою очередь может распространяться по коммуникациям закачки на поверхность и представлять реальную опасность для технологического персонала, выполняющего работу на скважине.
Целью предложенного изобретения является разработка термогазохимического бинарного состава и способа его применения для обработки призабойной и удаленной зон нефтегазоносного пласта, исключающего применение кислотных реагентов для инициирования реакций образования азота и воды, что полностью исключает образование азотистого ангидрида и других окислов азота, а также исключает попадания эмульсий ВВ в высокотемпературную, призабойную зону нефтегазоносного пласта.
Указанная цель достигается тем, что в термогазохимическом бинарном составе для обработки призабойной и удаленной зон нефтегазоносного пласта, содержащем эквимолярные растворы аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором, согласно изобретению в качестве инициирующего раствора используют растворы альдегидов, содержащие спирты или ацетон, превращающие альдегидные группировки в полуацетали, которые обладают пониженной реакционной способностью, что обеспечивает индукционный период, достаточный для безопасности закачки исходных реагентов в нефтегазоносный пласт, при этом инициирующий раствор, обеспечивающий индукционный период развития реакций тепло- и газовыделения от 20 до 180 минут, состоит из смеси водных растворов алифатических альдегидов с алифатическими спиртами или ацетоном в молярном соотношении от 0,5:1 до 2:1, а молярное соотношение между альдегидом, содержащимся в инициирующем растворе, и аммониевой солью в термогазохимическом бинарном составе используют в соотношении от 1: 40 до 1:250 и смесь аммониевых солей минеральных кислот и нитриты щелочных металлов в водном растворе используют в пределах от 40 до 85 мас.%.
В способе для обработки призабойной и удаленной зон нефтегазоносного пласта, включающем закачку в пласт термогазохимического бинарного состава - растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующем раствором, согласно изобретению смешение растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующем раствором производят в режиме интенсивного перемешивания до начала закачки термогазохимического бинарного состава в нефтегазоносный пласт, в качестве инициирующего раствора используют растворы альдегидов, содержащие спирты или ацетон, превращающие альдегидные группировки в полуацетали, которые обладают пониженной реакционной способностью, что обеспечивает индукционный период, достаточный для безопасной закачки исходных реагентов в нефтегазоносный пласт, при этом температуру водного раствора аммониевых солей минеральных кислот и нитритов щелочных металлов перед смешением с инициирующим раствором применяют в пределах от -10 до +30°С.
Предложенный термогазохимический бинарный состав, рекомендуемый для обработки призабойной и удаленной зон нефтегазоносного пласта, содержит эквимолярные растворы аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором, состоящим из растворов альдегидов, содержащих спирты или ацетон, превращающие альдегидные группировки в полуацетали, и которые обладают пониженной реакционной способностью. Эти свойства раствора позволят обеспечить индукционный период, достаточный для безопасной закачки исходных реагентов в нефтегазоносный пласт.
Реализация такого замысла возможна с использованием принципиально новых химических реакций, в которых из первоначально нейтральных веществ образуются свободные кислоты в количествах строго пропорциональных количеству прореагировавшей соли аммония с одновременным образованием основания более слабого, чем аммиак. Принципиальное существование таких реакций известно давно и наиболее подробно изучено для образования уротропина взаимодействием формальдегида с солями аммония

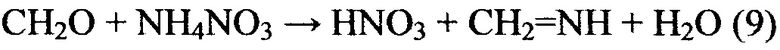
Метиленимин, образующийся одновременно с соляной или азотной кислотами по реакциям (8) и (9), является основанием более слабым, чем аммиак в солях аммония. В результате лабораторных экспериментов установлено, что иминогруппы продуктов конденсации альдегидов с солями аммония очень легко подвергаются нитрозированию с образованием соответствующих нитрозаминов

Азотистая кислота, необходимая для осуществления реакции (10), образуется взаимодействием нитрита щелочного металла с кислотами, образующимися по реакции (8) и (9).
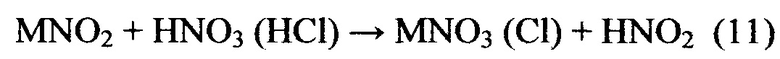
Значительно более высокая способность аминопроизводных альдегидов к реакции нитрозирования по сравнению с аминами обеспечивает быстрое связывание азотистой кислоты и соответственно исключает образование азотистого ангидрида по реакции (6).
В свою очередь нитрозамины, образующиеся по реакции (10), очень нестабильны и быстро разлагаются на молекулярный азот, воду и исходный альдегид, который получает возможность многократно участвовать в суммарном процессе взаимодействия солей аммония с нитритами металлов

Суммарное уравнение (12) фактически отражает способность алифатических альдегидов катализировать образование азота и воды из нитритов металлов и солей аммония без участия минеральных или органических кислот.
Как показывают прямые эксперименты один моль альдегида (формальдегид или глиоксаль) успевает принять участие в образовании 50-100 молей молекулярного азота в водных растворах солей аммония до момента полного израсходования соли аммония.
В качестве солей аммония использовали хлорид, нитрат и сульфат аммония. Наиболее высокую активность в образовании азота обнаруживает хлорид аммония. В то же время нитрат аммония, благодаря более высокой растворимости в воде, позволяет обеспечивать достижение более высоких температур в ходе реакции. Испытания на стендовой установке показали, что при содержании эквимолярной смеси нитрата аммония и нитрита натрия 70% температура в реакционной системе достигается 240-290°С при давлении до 130 кг/см2 при использовании 0,15 моль формальдегида на моль нитрата аммония.
Использование каталитических количеств альдегидов для реакций образования азота, воды и тепла вместо добавки минеральных или органических кислот, обеспечивает значительное экономическое преимущество благодаря низкой стоимости формальдегида.
Существенным преимуществом данной инициирующей системы является ее нейтральность, что обеспечивает низкую коррозионную способность и соответственно увеличивает срок службы оборудования скважин на нефтепромыслах.
Высокая каталитическая способность альдегида, наряду с вышеперечисленными преимуществами, обладает существенными недостатком, а именно очень быстрое развитие реакций: тепло- и газовыделение осложняет закачку растворов в призабойную зону скважины. Например, при добавлении 2 мл 38%-ного формалина к 60%-ному раствору 24,0 г нитрата аммония и 20,7 г нитрита натрия время до начала бурного тепло- и газовыделения составляет 4÷10 мин. При использовании 0,5 мл 40%-ного раствора глиоксаля уже через 1 минуту температура достигает 105-110°С при атмосферном давлении. Такая высокая реакционная способность водных растворов альдегидов не позволяет использовать их для одновременной закачки в призабойную зону наряду с бинарными составами солей аммония и нитритов металлов.
Попытка замедлить реакцию (12) дальнейшим уменьшением количества альдегида встретила значительные затруднения в связи с влиянием рН среды на дальнейшее поведение промежуточного образующегося метиленимина. Исследования химизма реакции образования уротропина взаимодействием формальдегида с солями аммония показало, что максимум скорость реакции находится при рН 9,0-9,2 (Y. Ogata, A. Kawasaki, Bull. Soc. ChimJap.1964, 37(4), 514-519). При этих величинах рН скорость превращения метиленимина в уротропин по реакции (13)

довольно высокая, а скорость реакции нитрозирования метиленимина существенно уменьшается из-за уменьшения содержания свободной азотистой кислоты в реакции (11). Соответственно, реакция бинарного раствора смеси солей с очень малыми количествами альдегидов может затухать вследствие образования уротропина по реакции (13) с использованием формальдегида или тетрагидроксидиазинов при использовании глиоксаля.
Возможен вариант осуществления реакции с последовательной закачкой в призабойную зону инициирующего раствора и водного раствора смеси солей. В лабораторных условиях в гомогенных средах реакция протекает быстро и процесс тепло- и газовыделения легко регулируется скоростью подачи растворов реагентов.
Проверка этих режимов проводилась на стендовой установке с использованием в качестве реактора трубы диаметром 76 мм и длиной 1500 мм, заполненной гранулированным порошком (песком, пропантом и т.п.), моделирующим состав горной породы, показала, что последовательная закачка растворов чрезвычайно сильно замедляет реакцию. Даже после 3 суток реакция не завершается полностью. Остается не прореагировавшим большое количество нитрита. Диффузия инициирующего раствора в слой раствора NH4NO3/NaNO2 очень медленная.
Для обеспечения максимального использования энергетического потенциала водного раствора смеси солей аммония и нитритов щелочных металлов необходимо обеспечить равномерное распределение в водном растворе смеси солей инициирующего раствора.
В результате лабораторных экспериментов установлено, что добавление алифатических спиртов (метанол, этанол, пропанол) или ацетона к водным растворам альдегида позволяет уменьшить скорость тепло- и газовыделения из растворов солей аммония с нитритами щелочных металлов до величин, приемлемых для практического применения в нефтепромысловых условиях. Известно, что альдегиды со спиртами или ацетоном способны образовывать полуацетали в равновесных реакциях (14)
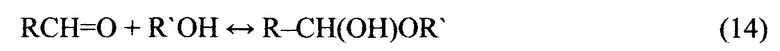
Для глиоксаля возможно образование циклического полуацеталя по реакции (15)

Реакционная способность полуацеталей в реакции с солями аммония существенно замедляется.
В результате лабораторных экспериментов нами установлено, что добавление алифатических спиртов (метанол, этанол и др.) или ацетона к водным растворам формальдегида или глиоксаля позволяет регулировать скорость тепло- и газовыделения в широких пределах, обеспечивая индукционный период от 20 до 180 минут, что позволяет осуществлять одновременную подачу водного раствора смеси солей и инициирующего раствора - это термогазохимический бинарный состав, в котором реакционная способность карбонильной группы уменьшена добавлением веществ, способных превращать альдегидную группу в полуацетали. Добавление такого инициирующего раствора к водному раствору смеси солей аммония и нитрита щелочного металла вызывает сдвиг равновесных реакций (14) и (15) в сторону исходных альдегидов, обладающих высокой реакционной способностью.
Увеличения индукционного периода до начала интенсивного процесса тепло- и газовыделения можно достичь разбавлением исходных растворов альдегидов от 3 до 10% вес. В таких растворах уменьшение скорости тепловыделения обеспечивается уменьшением молекулярной формы альдегида за счет превращения ее в нереакционноспособную гидратную форму

Приведенные ниже примеры поясняют сущность данного изобретения.
Примеры 1-4
В экспериментах 1-4 использовали инициирующий раствор, приготовленный добавлением 0,4 вес.ч. метанола к 1 вес.ч. формалина. Состав инициатора: CH2O - 21,7%, СН3ОН - 27,42%, вода - 50,8%.
24,0 г (0,3 моль) нитрата аммония в 19,2 мл воды растворяются с понижением температуры до -6°С. К холодному раствору добавляли 20,7 г (0,3 моль) нитрита натрия и перемешивали до полного растворения при -1°С÷+1°С, к холодному раствору приливали 0,5÷1,0 мл инициирующего раствора. Полученный термогазохимический бинарный состав помещали в коническую колбу с термометром и контролировали изменения температуры до достижения точки кипения и начала бурного выделения азота и паров воды. Время от момента добавления инициирующего раствора и до выброса реакционной массы из колбы составляет индукционный период. Зависимость индукционных периодов (τинд) от количества инициирующего раствора и концентрации солей в бинарной смеси приведена в таблице 1.

Примеры 5, 6
В экспериментах 5 и 6 инициирующий раствор готовили добавлением 5 вес.ч. ацетона к 1 вес.ч. водного раствора формалина. Состав инициирующего раствора: CH2O - 4,4%, ацетон - 85,12%, вода - 10,55%.
24,0 г (0,3 моль) нитрата аммония растворяли в 30,4 мл воды с понижением температуры до -4°С, к холодному раствору добавляли 20,7 г (0,3 моль) нитрита натрия и перемешивали до полного растворения. При -1°С добавляли инициирующий раствор, полученный при добавлении формалина к ацетону. Полученный термогазохимический бинарный состав помещали в коническую колбу и определяли индукционный период до полного бурного газовыделения и быстрого подъема температуры до точки кипения 104-105°С. Результаты приведены в таблице 2.

Примеры 7-12
В экспериментах 7-12 инициирующий раствор готовили добавлением 1 вес.ч. метанола к 1 вес.ч. водного раствора глиоксаля. Состав полученного инициирующего раствора: глиоксаль - 21,81%, метанол - 31,7%, вода - 48,48%.
24,0 г (0,3 моль) нитрата аммония растворяли в 19-46 мл воды с понижением температуры до (-6°С)-(-4°С). К холодному раствору нитрита аммония добавляли 20,7 г (0,3 моль) нитрита натрия и перемешивали до полного растворения. К холодному раствору добавляли 0,4-1,0 мл инициирующего раствора вышеуказанного состава. Индукционный период полученного термогазохимического бинарного состава до начала бурного газовыделения и повышения температуры до точки кипения определяли, как описано в предыдущих примерах.
Результаты приведены в таблице 3.

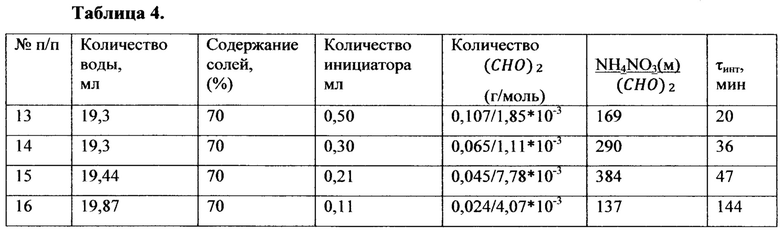
Примеры 13-16
В экспериментах 13-16 инициирующий раствор готовили добавлением 1 вес.ч. ацетона к 2 вес.ч. 32%-ного раствора глиоксаля. Состав использованного инициирующего раствора: глиоксаль - 21,5%, ацетон - 33, 24%, вода - 45,64%.
Определение индукционных периодов полученного термогазохимического бинарного состава производили аналогично предыдущим опытам. Результаты приведены в таблице 4.
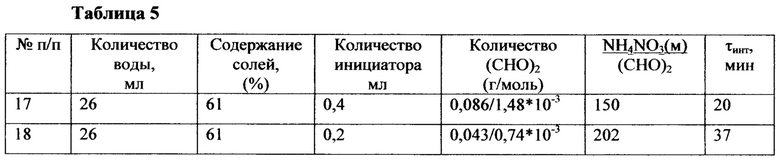
Пример 17 и 18
В экспериментах (17) и (18) использовали тот же самый инициирующий раствор как и в примере (13)-(16). Термогазохимический бинарный состав готовили с использованием сульфата аммония и нитрита натрия. 20,15 г - 0,15 моль - сульфата аммония растворили в 26 мл воды. К раствору сульфата добавили 20,7 г нитрита натрия и после растворения нитрита при 16,5°С добавили инициирующий раствор. Результаты приведены в таблице 5.
Пример 19
В эксперименте использовали водный раствор глиоксаля, приготовленный разбавлением 40%-ного глиоксаля водой до концентрации 3,85% мас. Термогазохимический состав готовили смешением 49,92 г нитрата аммония с 15 мл воды и 41,55 нитрита натрия. К полученной суспензии добавили 0,5 мл раствора глиоксаля, содержащего 3,85% альдегида, при температуре -10°С. В автотермическом режиме тепловыделение завершается подъемом температуры до 137°С в течение 191 мин.
Пример 20
В эксперименте для инициирования тепло- и газовыделения использовали раствор формальдегида, предварительно разбавленный водой до 10%. 49,92 г нитрата аммония смешивали с 15 мл воды и добавляли 41,54 г нитрита натрия, к полученной суспензии добавляли 0,47 мл 10%-ного формальдегида. В автотермическом режиме температура суспензии достигла 137°С после 114 мин. Температура окружающей среды составляла 18,5°С.
Проведенные лабораторно-стендовые эксперименты были систематизированы и оформлены в виде примеров и таблиц, анализ которых позволил сделать следующие выводы:
- определены оптимальные соотношения бинарных смесей и инициирующих растворов водных, спиртовых, ацетоновых растворов формальдегида, глиоксаля и других - от 0,5:1 до 2:1, которые обеспечивают запуск процесса температурного разложения бинарных смесей и позволяют получить индукционный период развития реакций тепло- и газовыделения в пределах от 20 до 180 минут;
- определены молярные соотношения между альдегидом, содержащимся в инициирующем растворе, и аммониевой солью в термогазохимическом бинарном составе, которые соответствуют соотношениям от 1:40 до 1:250;
- установлены оптимальные концентрации бинарных смесей (40-85%), которые рекомендуются к применению на добывающих и нагнетательных газонефтяных скважинах.
Для практического применения предлагается способ обработки призабойной и удаленной зон нефтегазоносного пласта, включающий закачку в пласт растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующем раствором, причем смешивание их производится на поверхности в режиме интенсивного перемешивания, до начала закачки термогазохимического бинарного состава в нефтегазоносный пласт, при этом температура водного раствора аммониевых солей минеральных кислот и нитритов щелочных металлов перед смешением с инициирующим раствором предлагается в пределах от -10 до +30°С.
Испытание термогазохимического бинарного состава проводилось на стендовой установке в герметичных условиях.
Моделирование поведения термогазохимического бинарного состава в условиях, наиболее приближенных к реальным условиям, существующих на большой глубине залегания нефтегазоносной породы (1500-3000 м), осуществляли с использованием стенда, основным элементом которого является металлическая труба-реактор диаметром 76 мм и длиной 1500 мм. Подача термогазохимического бинарного состава (водный раствор смеси солей и инициирующий раствор) осуществляется с помощью дозирующего насоса, способного развивать давление до 200 кг/см2, производительностью 2,5 л/мин и осуществляющего подачу бинарного состава через один из торцевых герметизирующих фланцев.
Контроль процессов тепловыделения осуществлялся дистанционными температурными датчиками с диапазонами измерений от 0 до 600°С. Датчики устанавливали в 3 точках: в центре трубы и в торцевых герметизирующих фланцах, которые герметизируют металлическую трубу-реактор. Давление образующихся газов контролируется дистанционным датчиком давления, установленным в торцевом герметизирующем фланце.
Перед началом испытаний металлическая труба-реактор заполнялась гранулированным порошком (пропантом), моделирующим состав нефтегазоносной породы в призабойной зоне (AL2O3 - 65%, Fe2O3 - 7%, SiO2 - 22-26%, CaO - 1,5%, TiO - 1,5%, Na2O до 100%). Количество гранулированного порошка (пропанта), загруженного в трубу-реактор, составляло 7,0-8,0 кг на одно испытание.
Термогазохимический бинарный состав готовили следующим образом: 934 г (11,67 моль) нитрата аммония растворяли в 1160 мл воды, при этом температура раствора понижалась до -6°С. К холодному гомогенному раствору селитры добавляли 806 г (11,68 моль) нитрита натрия и перемешивали до полного растворения (10-15 мин). К холодному -1°С - -2°С раствору добавили инициирующий раствор, приготовленный накануне (к 10 мл 40%-ного водного глиоксаля (12,28 г), содержащего 4,91 г (0,085 моль) глиоксаля, добавляли 6,8 мл (5,36 г) ацетона).
Состав полученного инициирующего раствора был следующим:
- глиоксаль 27,84%, ацетон 30,4%, вода 44,76%.
Молярное соотношение нитрат аммония/глиоксаль 137:1. Инициирующий раствор в количестве 16,9 г - содержание глиоксаля 4,7 г (0,081 моль) добавляли в раствор солей и перемешивали непосредственно перед заливкой в напорный бачок, откуда дозировочным насосом закачивали в металлическую трубу-реактор. Регистрация давления газов и температур во всех точках металлической трубы-реактора осуществлялась дистанционно с записью на регистраторе.
На фиг. 1 и фиг. 2 представлен процесс термогазохимического разложения бинарного состава в металлической трубе-реакторе, который зарегистрировали три температурных датчика и датчик давления. Целью подобных экспериментов являлось определение максимальных давления, температуры и время задержки начала реакции - индукционный период реакции - термогазохимического разложения бинарных составов. Работа на стенде позволила уточнить зависимости термогазовыделения бинарных составов при различной концентрации солей, инициирующего раствора и гранулированного порошка (пропанта). Установлено, что термогазохимические бинарные составы с равной концентрацией солей и инициирующего раствора имеют различную задержку начала реакции (индукционный период реакции), которая может отличаться от индукционного периода, наблюдающегося в лабораторных экспериментах. Основное отличие результатов в трубе-реакторе от результатов лабораторных испытаний состоит в использовании пропанта (7,5 кг). Наличие пропанта в трубе-реакторе увеличивает индукционный период из-за расхода значительного количества тепла на нагрев пропанта. Индукционный период 46-210 минут вполне достаточен для безопасной закачки в нефтегазоносный пласт термогазохимического бинарного состава вместе с инициирующим раствором.
На фиг. 1 представлены результаты закачки бинарного состава вместе с инициирующим раствором. Они показали, что рост температуры начинается одновременно во всех точках трубы-реактора, достигает максимума при давлении 130 кг/см2, после чего произошел сброс давления из-за открытия предохранительного клапана. Максимальная температура достигала 200-210°С.
На фиг. 2 представлена последовательная закачка, без предварительного смешивания, тех же количеств компонентов 2900 г раствора солей и 100 мл инициирующего раствора, обнаруживается только очень слабый и медленный подъем температуры до 48-50°С в центральной части трубы-реактора. Температура у фланцев трубы-реактора изменяется при этом незначительно, едва повышаясь до 30-32°С. Такая большая разница тепло- и газовыделения объясняется плохим смешиванием реагирующих растворов в гранулированном порошке (пропанте), где диффузионные процессы очень сильно замедляются из-за мелкого размера пор между частицами гранулированного порошка (пропанта).
Сопоставление молярных количеств прореагировавшего нитрата аммония 934 г (11,67 моль) и глиоксаля (инициирующего раствора) 4,7 г (0,081 моль) показывает, что одного моля глиоксаля было достаточно для конверсии 144 молей нитрата аммония.
Это испытание демонстрирует принципиально различную реакционную способность одинаковых по соотношению солей и инициирующего раствора в термогазохимических бинарных составах в случае изменения последовательности закачки его (состава) в реакционную зону.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭНЕРГОГАЗООБРАЗУЮЩИЙ СОСТАВ И ТЕХНОЛОГИЯ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПРОДУКТИВНОГО ПЛАСТА | 2014 |
|
RU2615543C2 |
| Термогазохимический состав и способ его применения при обработке призабойной и удаленной зоны продуктивного пласта (варианты) | 2022 |
|
RU2803463C1 |
| Способ добычи высоковязкой нефти и термогазохимический состав для его осуществления | 2021 |
|
RU2778919C1 |
| Способ добычи высоковязкой нефти с внутрискважинной тепловой активацией бинарного раствора | 2023 |
|
RU2812996C1 |
| Способ добычи высоковязкой нефти с внутрискважинной тепловой активацией бинарного раствора | 2023 |
|
RU2812385C1 |
| ТЕРМОГАЗОХИМИЧЕСКИЙ СОСТАВ И СПОСОБ ПРИМЕНЕНИЯ ДЛЯ ОБРАБОТКИ ПРИЗАБОЙНОЙ И УДАЛЕННОЙ ЗОНЫ ПРОДУКТИВНОГО ПЛАСТА | 2012 |
|
RU2525386C2 |
| Способ добычи высоковязкой нефти с внутрискважинной тепловой активацией бинарного раствора | 2023 |
|
RU2812983C1 |
| Способ обработки нефтяного пласта | 2021 |
|
RU2766283C1 |
| Способ термогазохимической и ударно-волновой обработки нефтеносных пластов | 2018 |
|
RU2717151C1 |
| Способ добычи высоковязкой нефти с внутрискважинной тепловой активацией бинарного раствора | 2023 |
|
RU2812985C1 |


Группа изобретений относится к нефтяной и газодобывающей промышленности. Технический результат - повышение эффективности обработки призабойной и удаленной зон нефтегазоносного пласта, безопасности процесса, уменьшение сырьевых затрат. Термогазохимический бинарный состав для обработки призабойной и удаленной зон нефтегазоносного пласта содержит эквимолярные растворы аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором, в качестве инициирующего раствора используют растворы альдегидов, содержащие спирты или ацетон, превращающие альдегидные группировки в полуацетали, которые обладают пониженной реакционной способностью, что обеспечивает индукционный период, достаточный для безопасной закачки исходных реагентов в нефтегазоносный пласт. Способ для обработки призабойной и удаленной зон нефтегазоносного пласта включает закачку в пласт термогазохимического бинарного состава - растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором. Смешение растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором производят в режиме интенсивного перемешивания до начала закачки термогазохимического бинарного состава в нефтегазоносный пласт. 2 н. и 4 з.п. ф-лы, 2 ил., 5 табл., 20 пр.
1. Термогазохимический бинарный состав для обработки призабойной и удаленной зон нефтегазоносного пласта, содержащий эквимолярные растворы аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором, отличающийся тем, что в качестве инициирующего раствора используют растворы альдегидов, содержащие спирты или ацетон, превращающие альдегидные группировки в полуацетали, которые обладают пониженной реакционной способностью, что обеспечивает индукционный период, достаточный для безопасной закачки исходных реагентов в нефтегазоносный пласт.
2. Термогазохимический бинарный состав по п. 1, отличающийся тем, что инициирующий раствор, обеспечивающий индукционный период развития реакций тепло- и газовыделения от 20 до 180 минут, состоит из смеси водных растворов алифатических альдегидов с алифатическими спиртами или ацетоном в молярном соотношении от 0,5:1 до 2:1.
3. Термогазохимический бинарный состав по п. 1, отличающийся тем, что молярное соотношение между альдегидом, содержащимся в инициирующем растворе, и аммониевой солью в термогазохимическом бинарном составе используют в пределах от 1:40 до 1:250.
4. Термогазохимический бинарный состав по п. 1, отличающийся тем, что смесь аммониевых солей минеральных кислот и нитритов щелочных металлов в водном растворе используют в пределах от 40 до 85 мас.%.
5. Способ для обработки призабойной и удаленной зон нефтегазоносного пласта, включающий закачку в пласт термогазохимического бинарного состава - растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором, отличающийся тем, что смешение растворов аммониевых солей минеральных кислот и нитритов щелочных металлов с инициирующим раствором производят в режиме интенсивного перемешивания до начала закачки термогазохимического бинарного состава в нефтегазоносный пласт, а в качестве инициирующего раствора используют растворы альдегидов, содержащие спирты или ацетон, превращающие альдегидные группировки в полуацетали, которые обладают пониженной реакционной способностью, что обеспечивает индукционный период, достаточный для безопасной закачки исходных реагентов в нефтегазоносный пласт.
6. Способ по п. 5, отличающийся тем, что температура водного раствора аммониевых солей минеральных кислот и нитритов щелочных металлов перед смешением с инициирующим раствором применяется в пределах от -10 до +30°С.
| ТЕРМОГАЗОХИМИЧЕСКИЙ СОСТАВ И СПОСОБ ПРИМЕНЕНИЯ ДЛЯ ОБРАБОТКИ ПРИЗАБОЙНОЙ И УДАЛЕННОЙ ЗОНЫ ПРОДУКТИВНОГО ПЛАСТА | 2012 |
|
RU2525386C2 |
| Способ термохимической обработки призабойной зоны пласта | 1977 |
|
SU640023A1 |
| СПОСОБ ТЕРМОХИМИЧЕСКОЙ ОБРАБОТКИ НЕФТЯНОГО ПЛАСТА | 2009 |
|
RU2401941C1 |
| Способ и устройство для термохимической обработки продуктивного пласта | 2002 |
|
RU2224103C1 |
| СПОСОБ ТЕРМОХИМИЧЕСКОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА | 1997 |
|
RU2126084C1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
Авторы
Даты
2017-12-01—Публикация
2015-12-28—Подача