ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к соединениям, которые модулируют функцию LRRK2 и полезны для лечения LRRK2-опосредованных заболеваний и состояний, таких как болезнь Паркинсона.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Нейродегенеративные заболевания, такие как болезнь Паркинсона, деменция с тельцами Леви и болезнь Гентингтона, поражают миллионы людей. Болезнь Паркинсона представляет собой хроническое, прогрессирующее двигательное расстройство, которое поражает приблизительно одного из каждой 1000 человек, при этом наследственная болезнь Паркинсона наблюдается у 5-10% всех пациентов. Причиной болезни Паркинсона является прогрессирующая потеря дофаминовых нейронов среднего мозга, приводящая к нарушению у пациентов способности управлять своими движениями и осуществлять над ними контроль. Первичными симптомами болезни Паркинсона являются дрожь, ригидность, замедленность движений и нарушение равновесия. Многие пациенты с болезнью Паркинсона также испытывают другие симптомы, такие как эмоциональные изменения, потеря памяти, речевые проблемы и расстройства сна.
Ген, кодирующий белок - обогащенную лейциновыми повторами киназу 2 (leucine-rich repeat kinase 2; LRRK2), был идентифицировали совместно с наследственной болезнью Паркинсона (Paisan-Ruiz et al., Neuron, Vol. 44 (4), 2004, pp. 595-600; Zimprich et al., Neuron, Vol. 44 (4), 2004, 601-607). Исследования in vitro показывают, что ассоциированная с болезнью Паркинсона мутация вызывает увеличение киназной активности LRRK2 и уменьшение скорости гидролиза ГТФ по сравнению с диким типом (Guo et al., Experimental Cell Research, Vol. 313 (16), 2007, pp. 3658-3670). Антитела к LRRK2 были использованы для "мечения" телец Леви ствола головного мозга, ассоциированных с болезнью Паркинсона, и наличие кортикальных антител, ассоциированных с деменцией с тельцами Леви, позволяет высказать предположение, что LRRK2 может играть важную роль в образовании и патогенезе телец Леви, ассоциированных с этими заболеваниями (Zhou et al., Molecular Degeneration, 2006, 1: 17 doi: 10.1186/1750-1326-1-17). Ген LRRK2 также был идентифицирован как ген, потенциально ассоциированный с повышенной предрасположенностью к болезни Крона и предрасположенностью к лепре (Zhang et al., New England J. Med., Vol. 361 (2009), pp. 2609-2618).
LRRK2 также ассоциирована с перерождением умеренной когнитивной недостаточности в болезнь Альцгеймера (WO 2007/149789); с L-допа-индуцированной дискинезией (Hurley et al., Eur. J. Neurosci., Vol. 26, 2007, pp. 171-177); расстройствами центральной нервной системы (ЦНС), связанными с дифференцировкой предшественников нейронов (Milosevic et al., Neurodegen., Vol. 4, 2009, p. 25); случаями рака, такого как рак почки, молочной железы, предстательной железы, крови, легкого и острый миелогенный лейкоз (WO 2011/038572); папиллярным раком почки и раком щитовидной железы (Looyenga et al., www.pnas.org/cgi/doi/10.1073/pnas.1012500108); множественной миеломой (Chapman et al., Nature, Vol. 471, 2011, pp. 467-472); боковым амиотрофическим склерозом (Shtilbans et al., Amyotrophic Lateral Sclerosis, "Early Online, 2011, pp. 1-7); ревматоидным артритом (Nakamura et al., DNA Res. Vol. 13 (4), 2006, pp. 169-183) и анкилозирующим спондилитом (Danoy et al., PLoS Genetics, Vol. 6 (12), 2010, e1001195, pp. 1-5).
Соответственно, используя соединения и композиции, эффективные при модулировании активности LRRK2, можно проводить лечение нейродегенеративных заболеваний, таких как болезнь Паркинсона и деменция с тельцами Леви, расстройств ЦНС, таких как болезнь Альцгеймера и L-допа-индуцированная дискинезия, случаев рака, такого как рак почки, молочной железы, предстательной железы, крови, папиллярный рак и рак легкого, острый миелогенный лейкоз и множественная миелома, и воспалительных заболеваний, таких как лепра, болезнь Крона, боковой амиотрофический склероз, ревматоидный артрит и анкилозирующий спондилит. В частности, существует потребность в соединениях с аффинностью к LRRK2, которые селективны в отношении LRRK2, а не других киназ, таких как JAK2 (janus kinase - янус-киназа), и на основе которых могут быть разработаны эффективные лекарственные средства для лечения нейродегенеративных расстройств, таких как болезнь Паркинсона (Parkinson's disease; PD).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Согласно изобретению предложены соединения формулы I:
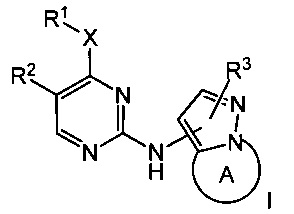
или их фармацевтически приемлемая соль,
где:
X представляет собой: -NRa- или -О-, где Ra представляет собой водород или С1-6алкил;
R1 представляет собой: С1-6алкил; С2-6алкенил; С2-6алкинил; галоген-С1-6алкил; С1-6алкокси-С1-6алкил; гидрокси-С1-6алкил; амино-С1-6алкил; С1-6алкилсульфонил-С1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз C1-6алкилом; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз С1-6алкилом; гетероциклил, возможно, замещенный один или более раз группой R5; или гетероциклил-С1-6алкил, возможно, замещенный один или более раз группой R5;
или X и R1 вместе образуют С1-6алкил; С1-6алкокси-С1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4;
или R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать трех-шестичленное гетероциклическое кольцо, возможно, замещенное один или более раз группой R5;
R2 представляет собой: С1-6алкил; атом галогена; С1-6алкокси; циано; С2-6алкинил; С2-6алкенил; галоген-С1-6алкил; галоген-С1-6алкокси; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; -ORb, где Rb представляет собой C1-6алкил, С3-6циклоалкил, возможно, замещенный один или более раз группой R4, или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; или -C(O)-Rc, где Rc представляет собой С1-6алкил, С1-6алкокси, амино или гетероциклил, возможно, замещенный один или более раз группой R5;
R3 представляет собой: водород; С1-6алкил; атом галогена; циано; галоген-С1-6алкил; С2-6алкенил; С2-6алкинил; С1-6алкокси; С1-6алкокси-С1-6алкил; гидрокси-С1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; или -Y-C(O)-Rd;
Y представляет собой С2-6алкилен или связь;
Rd представляет собой С1-6алкил, С1-6алкокси, амино, С1-6алкиламино, ди-С1-6алкиламино, галоген-С1-6алкиламино, дигалоген-С1-6алкиламино, галоген-С1-6алкил, гидрокси-С1-6алкил, гидрокси, С1-6алкокси-С1-6алкил, циано-С1-6алкил, C1-6алкилсульфонилС1-6алкил, амино-С1-6алкил, С3-6циклоалкил, возможно, замещенный один или более раз группой R4, С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4, гетероциклил, возможно, замещенный один или более раз группой R5, или гетероциклил-С1-6алкил, гетероциклильная часть которого, возможно, замещена один или более раз группой R5;
каждый R4 независимо представляет собой: С1-6алкил; галоген-С1-6алкил; C1-6алкокси; оксо; циано; атом галогена или -Y-C(O)-Rd;
каждый R5 независимо представляет собой: С1-6алкил; галоген-С1-6алкил; атом галогена; оксо; С1-6алкокси; С1-6алкилсульфонил; С1-6алкокси-С1-6алкил; циано; -Y-C(O)-Rd; гетероциклил; гетероциклил-С1-6алкил; С3-6циклоалкил; С3-6циклоалкил-С1-6алкил или С3-6циклоалкилсульфонил;
А представляет собой пяти- или шестичленное ненасыщенное или насыщенное карбоциклическое кольцо, которое, возможно, может содержать гетероатом, выбранный из О, N и S, и которое может быть замещено один или более раз группой R6; и
каждый R6 независимо представляет собой: оксо; С1-6алкил; галоген-С1-6алкил; С1-6алкокси; С1-6алкокси-С1-6алкил; циано; циано-С1-6алкил; -Y-C(O)-Rd; С3-6циклоалкил, гетероциклил или С3-6циклоалкил-С1-6алкил.
Согласно изобретению также предложены фармацевтические композиции, содержащие эти соединения, способы применения соединений и способы получения соединений.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Если не указано иное, следующие термины, использованные в этой заявке, в том числе в описании и формуле изобретения, имеют приведенные ниже определения. Необходимо отметить, что, как использовано в описании и прилагаемой формуле изобретения, формы единственного числа (по англ. выражаемые артиклями "a", "an" и "the") включают объекты в форме множественного числа, если контекст ясно не предусматривает иное.
"Алкил" означает одновалентный линейную или разветвленную насыщенную углеводородную группировку, состоящую исключительно из атомов углерода и водорода, имеющую от одного до двенадцати атомов углерода. "Низший алкил" относится к алкильной группе, содержащей от одного до шести атомов углерода, т.е. С1-6алкилу. Примеры алкильных групп включают, но не ограничиваются этим, метил, этил, пропил, изопропил, изобутил, втор-бутил, трет-бутил, пентил, н-гексил, октил, додецил и тому подобное.
"Алкенил" означает линейный одновалентный углеводородный радикал из двух-шести атомов углерода или разветвленный одновалентный углеводородный радикал из трех-шести атомов углерода, содержащий по меньшей мере одну двойную связь, например, этенил, пропенил и тому подобное.
"Алкинил" означает линейный одновалентный углеводородный радикал из двух-шести атомов углерода или разветвленный одновалентный углеводородный радикал из трех-шести атомов углерода, содержащий по меньшей мере одну тройную связь, например, этинил, пропинил и тому подобное.
"Алкилен" означает линейный насыщенный двухвалентный углеводородный радикал, содержащий от одного до шести атомов углерода, или разветвленный насыщенный двухвалентный углеводородный радикал из трех-шести атомов углерода, например, метилен, этилен, 2,2-диметилэтилен, пропилен, 2-метилпропилен, бутилен, пентилен и тому подобное.
Термины "алкокси" и "алкилокси", которые могут быть использованы взаимозаменяемо, означают группировку формулы -OR, где R представляет собой алкильную группировку, которая определена в данном описании. Примеры алкоксигруппировок включают, но не ограничиваются этим, метокси, этокси, изопропокси и тому подобное.
"Алкоксиалкил" означает группировку формулы Ra-O-Rb-, где Ra представляет собой алкил, a Rb представляет собой алкилен, как определено в данном описании. Типичные алкоксиалкильные группы включают, в качестве примера, 2-метоксиэтил, 3-метоксипропил, 1-метил-2-метоксиэтил, 1-(2-метоксиэтил)-3-метоксипропил и 1-(2-метоксиэтил)-3-метоксипропил.
"Алкоксиалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен, a R' представляет собой алкокси, как определено в данном описании.
"Алкилкарбонил" означает группировку формулы -C(O)-R, где R представляет собой алкил, определенный в данном описании.
"Алкоксикарбонил" означает группу формулы -C(O)-R, где R представляет собой алкокси, определенный в данном описании.
"Алкилкарбонилалкил" означает группу формулы -R-C(O)-R', где R представляет собой алкилен, a R' представляет собой алкил, как определено в данном описании.
"Алкоксикарбонилалкил" означает группу формулы -R-C(O)-R', где R представляет собой алкилен, a R' представляет собой алкокси, как определено в данном описании.
"Алкоксикарбонилалкокси" означает группу формулы -O-R-C(O)-R', где R представляет собой алкилен, a R' представляет собой алкокси, как определено в данном описании.
"Гидроксикарбонилалкокси" означает группу формулы -O-R-C(O)-OH, где R представляет собой алкилен, определенный в данном описании.
"Алкиламинокарбонилалкокси" означает группу формулы -O-R-C(O)-NHR', где R представляет собой алкилен, a R' представляет собой алкил, как определено в данном описании.
"Диалкиламинокарбонилалкокси" означает группу формулы -O-R-C(O)-NR'R'', где R представляет собой алкилен, a R' и R'' представляют собой алкил, как определено в данном описании.
"Алкиламиноалкокси" означает группу формулы -O-R-NHR', где R представляет собой алкилен, a R' представляет собой алкил, как определено в данном описании.
"Диалкиламиноалкокси" означает группу формулы -O-R-NR'R'', где R представляет собой алкилен, a R' и R'' представляют собой алкил, как определено в данном описании.
"Алкилсульфонил" означает группировку формулы -SO2-R, где R представляет собой алкил, определенный в данном описании.
"Алкилсульфонилалкил" означает группировку формулы -R'-SO2-R'', где R' представляет собой алкилен, a R'' представляет собой алкил, как определено в данном описании.
"Алкилсульфонилалкокси" означает группу формулы -O-R-SO2-R', где R представляет собой алкилен, a R' представляет собой алкил, как определено в данном описании.
"Амино" означает группировку формулы -NRR', где каждый R и R' независимо представляет собой водород или алкил, определенный в данном описании. Так, термин "амино" включает в себя "алкиламино" (один из R и R' представляет собой алкил, а другой представляет собой водород) и "диалкиламино" (где R и R' оба представляют собой алкил).
"Аминокарбонил" означает группу формулы -C(O)-R, где R представляет собой амино, определенный в данном описании.
"Алкоксиамино" означает группировку формулы -NR-OR', где R представляет собой водород или алкил, a R' представляет собой алкил, определенный в данном описании.
"Алкилсульфанил" означает группировку формулы -SR, где R представляет собой алкил, определенный в данном описании.
"Аминоалкил" означает группу -R-R', где R' представляет собой амино, a R представляет собой алкилен, как определено в данном описании. "Аминоалкил" включает аминометил, аминоэтил, 1-аминопропил, 2-аминопропил и тому подобное. Аминогруппировка "аминоалкила" может быть замещена один или два раза алкилом с получением "алкиламиноалкила" и "диалкиламиноалкила", соответственно. "Алкиламиноалкил" включает метиламинометил, метиламиноэтил, метиламинопропил, этиламиноэтил и тому подобное. "Диалкиламиноалкил" включает диметиламинометил, диметиламиноэтил, диметиламинопропил, N-метил-N-этиламиноэтил и тому подобное.
"Аминоалкокси" означает группу -OR-R', где R' представляет собой амино, a R представляет собой алкилен, как определено в данном описании.
"Алкилсульфониламидо" означает группировку формулы -NR'SO2-R, где R представляет собой алкил, a R' представляет собой водород или алкил.
"Аминокарбонилоксиалкил" или "карбамилалкил" означает группу формулы -R-O-C(O)-NR'R'', где R представляет собой алкилен, а каждый из R' и R'' независимо представляет собой водород или алкил, как определено в данном описании.
"Алкинилалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен, a R' представляет собой алкинил, как определено в данном описании.
"Арил" означает одновалентную циклическую ароматическую углеводородную группировку, состоящую из моно-, би- или трициклического ароматического кольца. Арильная группа, возможно, может быть замещена так, как определено в данном описании. Примеры арильных группировок включают, но не ограничиваются этим, фенил, нафтил, фенантрил, флуоренил, инденил, пенталенил, азуленил, оксидифенил, бифенил, метилендифенил, аминодифенил, дифенилсульфидил, дифенилсульфонил, дифенилизопропилиденил, бензодиоксанил, бензофуранил, бензодиоксилил, бензопиранил, бензоксазинил, бензоксазинонил, бензопиперидинил, бензопиперазинил, бензопирролидинил, бензоморфолинил, метилендиоксифенил, этилендиоксифенил и тому подобное, в том числе их частично гидрированные производные, при этом каждый из них, возможно, замещен.
"Арилалкил" и "аралкил", которые могут быть использованы взаимозаменяемо, означают радикал -RaRb, где Ra представляет собой алкиленовую группу, a Rb представляет собой арильную группу, как определено в данном описании; например, примерами арилалкила являются фенилалкилы, такие как бензил, фенилэтил, 3-(3-хлорфенил)-2-метилпентил и тому подобное.
"Арилсульфонил" означает группу формулы -SO2-R, где R представляет собой арил, определенный в данном описании.
"Арилокси" означает группу формулы -O-R, где R представляет собой арил, определенный в данном описании.
"Аралкилокси" означает группу формулы -O-R-R', где R представляет собой алкилен, a R' представляет собой арил, как определено в данном описании.
"Карбокси" или "гидроксикарбонил", которые могут быть использованы взаимозаменяемо, означают группу формулы -С(O)-ОН.
"Цианоалкил" означает группировку формулы -R'-R'', где R' представляет собой алкилен, определенный в данном описании, a R'' представляет собой циано или нитрил.
"Циклоалкил" означает одновалентную насыщенную карбоциклическую группировку, состоящую из моно- или бициклических колец. Конкретный цикпоалкил является незамещенным, или он замещен алкилом. Циклоалкил, возможно, может быть замещен одним или более заместителями, при этом каждый заместитель независимо представляет собой гидрокси, алкил, алкокси, атом галогена, галогеналкил, амино, моноалкиламино или диалкиламино, если конкретно не указано иное. Примеры циклоалкильных группировок включают, но не ограничиваются этим, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и тому подобное, в том числе их частично ненасыщенные (циклоалкенильные) производные.
"Циклоалкилалкил", означает группировку формулы -R'-R'', где R' представляет собой алкилен, a R'' представляет собой циклоалкил, определенный в данном описании.
"Циклоалкилалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен, a R' представляет собой циклоалкил, как определено в данном описании.
"Гетероалкил" означает алкильный радикал, определенный в данном описании, где один, два или три атома водорода заменены на заместитель, независимо выбранный из группы, состоящей из -ORa, -NRbRc и -S(O)nRd (где n представляет собой целое число от 0 до 2), при этом понимается, что местом присоединения гетероалкильного радикала будет атом углерода, где Ra представляет собой атом водорода, ацил, алкил, циклоалкил или циклоалкилалкил; каждый из Rb и Rc независимо друг от друга представляет собой атом водорода, ацил, алкил, циклоалкил или циклоалкилалкил; и в том случае, когда n равно 0, Rd представляет собой атом водорода, алкил, циклоалкил или циклоалкилалкил, и когда n равно 1 или 2, Rd представляет собой алкил, циклоалкил, циклоалкилалкил, амино, ациламино, моноалкиламино или диалкиламино. Репрезентативные примеры включают, но не ограничиваются этим, 2-гидроксиэтил, 3-гидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксипропил, 1-гидроксиметилэтил, 3-гидроксибутил, 2,3-дигидроксибутил, 2-гидрокси-1-метилпропил, 2-аминоэтил, 3-аминопропил, 2-метилсульфонилэтил, аминосульфонилметил, аминосульфонилэтил, аминосульфонилпропил, метиламиносульфонилметил, метиламиносульфонилэтил, метиламиносульфонилпропил и тому подобное.
"Гетероарил" означает моноциклический или бициклический радикал из 5-12 атомов в кольце, имеющий по меньшей мере одно ароматическое кольцо, содержащее один, два или три гетероатома в кольце, выбранных из N, О или S, причем остальными атомами в кольце являются атомы С, при этом понимается, что местом присоединения гетероарильного радикала будет ароматическое кольцо. Гетероарильное кольцо, возможно, может быть замещено так, как определено в данном описании. Примеры гетероарильных группировок включают, но не ограничиваются этим, возможно, замещенный имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, пиразинил, тиенил, бензотиенил, тиофенил, фуранил, пиранил, пиридинил, пирролил, пиразолил, пиримидил, хинолинил, изохинолинил, бензофурил, бензотиофенил, бензотиопиранил, бензимидазолил, бензооксазолил, бензооксадиазолил, бензотиазолил, бензотиадиазолил, бензопиранил, индолил, изоиндолил, триазолил, триазинил, хиноксалинил, пуринил, хиназолинил, хинолизинил, нафтиридинил, птеридинил, карбазолил, азепинил, диазепинил, акридинил и тому подобное, в том числе их частично гидрированные производные, при этом каждый из них, возможно, замещен.
"Гетероарилалкил" или "гетероаралкил" означает группу формулы -R-R', где R представляет собой алкилен, и R' представляет собой гетероарил, как определено в данном описании.
"Гетероарилсульфонил" означает группу формулы -SO2-R, где R представляет собой гетероарил, как определено в данном описании.
"Гетероарилокси" означает группу формулы -O-R, где R представляет собой гетероарил, как определено в данном описании.
"Гетероаралкилокси" означает группу формулы -O-R-R'', где R представляет собой алкилен, и R' представляет собой гетероарил, как определено в данном описании.
Термины "галоген", "атом галогена" и "галогенид", которые могут быть использованы взаимозаменяемо, относятся к заместителю - атому фтора, хлора, брома или йода.
"Галогеноалкил" означает алкил, определенный в данном описании, в котором один или более атомов водорода заменены на одинаковые или разные атомы галогена. Типичные галогеналкилы включают -CH2Cl, -CH2CF3, -CH2CCl3, перфторалкил (например, -CF3) и тому подобное.
"Галогеналкокси" означает группировку формулы -OR, где R представляет собой галогеналкильную группировку, как определено в данном описании. Типичным галогеналкокси является дифторметокси.
"Гетероциклоамино" означает насыщенное кольцо, где по меньшей мере один атом в кольце представляет собой N, NH или N-алкил, а остальны атомы в кольце образуют алкиленовую группу.
"Гетероциклил" означает одновалентную насыщенную группировку, состоящую из одного-трех колец, включающих в себя один, два или три либо четыре гетероатома (выбранных из атома азота, кислорода или серы). Гетероциклильное кольцо, возможно, может быть замещено так, как определено в данном описании. Примеры гетероциклильных группировок включают, но не ограничиваются этим, возможно, замещенный пиперидинил, пиперазинил, гомопиперазинил, азепинил, пирролидинил, пиразолидинил, имидазолинил, имидазолидинил, пиридинил, пиридазинил, пиримидинил, оксазолидинил, изоксазолидинил, морфолинил, тиазолидинил, изотиазолидинил, хинуклидинил, хинолинил, изохинолинил, бензимидазолил, тиадиазолидинил, бензотиазолидинил, бензоазолилидинил, дигидрофурил, тетрагидрофурил, дигидропиранил, тетрагидропиранил, тиоморфолинил, тиаморфолинилсульфоксид, тиаморфолинилсульфонил, дигидрохинолинил, дигидроизохинолинил, тетрагидрохинолинил, тетрагидроизохинолинил и тому подобное.
"Гетероциклилалкил" означает группировку формулы -R-R', где R представляет собой алкилен, a R' представляет собой гетероциклил, как определенно в данном описании.
"Гетероциклилокси" означает группировку формулы -OR, где R представляет собой гетероциклил, определенный в данном описании.
"Гетероциклилалкокси" означает группировку формулы -OR-R', где R представляет собой алкилен, a R' представляет собой гетероциклил, как определено в данном описании.
"Гидроксиалкокси" означает группировку формулы -OR, где R представляет собой гидроксиалкил, определенный в данном описании.
"Гидроксиалкиламино" означает группировку формулы -NR-R', где R представляет собой водород или алкил, a R' представляет собой гидроксиалкил, как определено в данном описании.
"Гидроксиалкиламиноалкил" означает группировку формулы -R-NR'-R'', где R представляет собой алкилен, R' представляет собой водород или алкил, a R'' представляет собой гидроксиалкил, как определено в данном описании.
"Гидроксикарбонилалкил" или "карбоксиалкил" означает группу формулы -R-(CO)-OH, где R представляет собой алкилен, определенный в данном описании.
"Гидроксикарбонилалкокси" означает группу формулы -O-R-C(O)-OH, где R представляет собой алкилен, определенный в данном описании.
"Гидроксиалкилоксикарбонилалкил" или "гидроксиалкоксикарбонилалкил" означает группу формулы -R-C(O)-O-R-OH, где каждый R представляет собой алкилен, и они могут быть одинаковыми или разными.
"Гидроксиалкил" означает алкильную группировку, определенную в данном описании, замещенную одной или более, например, одной, двумя или тремя группами гидрокси, при условии, что один и тот же атом углерода не несет более одной гидроксигруппы. Репрезентативные примеры включают, но не ограничиваются этим, гидроксиметил, 2-гидроксиэтил, 2-гидроксипропил, 3-гидроксипропил, 1-(гидроксиметил)-2-метилпропил, 2-гидроксибутил, 3-гидроксибутил, 4-гидроксибутил, 2,3-дигидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксибутил, 3,4-дигидроксибутил и 2-(гидроксиметил)-3-гидроксипропил.
"Гидроксициклоалкил" означает циклоалкильную группировку, определенную в данном описании, где один, два или три атома водорода в циклоалкильном радикале заменены на заместитель гидрокси. Репрезентативные примеры включают, но не ограничиваются этим, 2-, 3- или 4-гидроксициклогексил и тому подобное.
"Алкоксигидроксиалкил" и "гидроксиалкоксиалкил", которые могут быть использованы взаимозаменяемо, означает алкил, определенный в данном описании, который замещен по меньшей мере один раз группой гидрокси и по меньшей мере один раз группой алкокси. Таким образом, "алкоксигидроксиалкил" и "гидроксиалкоксиалкил" охватывают, например, 2-гидрокси-3-метокси-пропан-1-ил и тому подобное.
Группа "мочевины" или "уреидо" означает группу формулы -NR'-C(O)-NR''R''' где каждый из R', R'' и R''' независимо представляет собой водород или алкил.
"Карбамат" означает группу формулы -O-C(O)-NR'R'', где каждый из R' и R'' независимо представляет собой водород или алкил.
"Карбокси" означает группу формулы -O-С(O)-ОН.
"Сульфонамидо" означает группу формулы -SO2-NR'R'', где каждый из R' и R'' независимо представляет собой водород или алкил.
"Возможно замещенный", при использовании вместе с "арилом", "фенилом", "гетероарилом", "циклоалкилом" или "гетероциклилом", означает арил, фенил, гетероарил, циклоалкил или гетероциклил, который, возможно, независимо замещен одним-четырьмя заместителями, например одним или двумя заместителями, выбранными из алкила, циклоалкила, циклоалкилалкила, гетероалкила, гидроксиалкила, атома галогена, нитро, циано, гидрокси, алкокси, амино, ациламино, моно-алкиламино, ди-алкиламино, галогеналкила, галогеналкокси, гетероалкила, -COR, -SO2R (где R представляет собой водород, алкил, фенил или фенилалкил), -(CR'R'')n-COOR (где n представляет собой целое число от 0 до 5, R' и R'' независимо представляют собой водород или алкил, и R представляет собой водород, алкил, циклоалкил, циклоалкилалкил, фенил или фенилалкил) или -(CR'R'')n-CONRaRb (где n представляет собой целое число от 0 до 5, R' и R'' независимо представляют собой водород или алкил, и Ra и Rb независимо друг от друга представляют собой водород, алкил, циклоалкил, циклоалкилалкил, фенил или фенилалкил). Некоторые конкретные возможные заместители для "арила", "фенила", "гетероарила", "циклоалкила" или "гетероциклила" включают алкил, атом галогена, галогеналкил, алкокси, циано, амино и алкилсульфонил. В одном из воплощений заместителями являются метил, атом фтора, хлора, трифторметил, метокси, амино и метансульфонил.
"Уходящая группа" означает группу, имеющую значение, традиционно ассоциируемое с ней в синтетической органической химии, т.е. атом или группу, замещаемые в условиях реакции замещения. Примеры уходящих групп включают, но не ограничиваются этим, атом галогена, алкан- или ариленсульфонилокси, такой как метансульфонилокси, этансульфонилокси, тиометил, бензолсульфонилокси, тозилокси и тиенилокси, дигалогенфосфиноилокси, возможно, замещенный бензилокси, изопропилокси, ацилокси и тому подобное.
"Модулятор" означает молекулу, которая взаимодействует с мишенью. Во взаимодействия включены, но не ограничиваются этим, агонист, антагонист и тому подобное, определенные в данном описании.
Термин "возможный" или "возможно" означает, что описываемое впоследствии событие или обстоятельство может иметь место, но происходит не обязательно, и что данное описание включает случаи, когда это событие или обстоятельство происходит, и случаи, в которых это не так.
"Заболевание" и "болезненное состояние" означает любое заболевание, состояние, симптом, расстройство или показание.
"Инертный органический растворитель" или "инертный растворитель" означает растворитель, являющийся инертным в условиях реакции, описываемой в связи с ним, включая например, бензол, толуол, ацетонитрил, тетрагидрофуран, N,N-диметилформамид, хлороформ, метиленхлорид или дихлорметан, дихлорэтан, диэтиловый эфир, этилацетат, ацетон, метилэтилкетон, метанол, этанол, пропанол, изопропанол, трет-бутанол, диоксан, пиридин и тому подобное. Если не указано иное, растворители, использованные в реакциях по настоящему изобретению, представляют собой инертные растворители.
"Фармацевтически приемлемый" означает то, что полезно при изготовлении фармацевтической композиции, то есть, как правило, является безопасным, нетоксичным и не является нежелательным ни в биологическом, ни в каком-либо ином отношении, и включает в себя то, что приемлемо для использования в производстве фармацевтических продуктов для ветеринарии, а также для людей.
Термин "фармацевтически приемлемые соли" соединения означает соли, которые являются фармацевтически приемлемыми, как определено в данном описании, и которые обладают желаемой фармакологической активностью исходного соединения.
Следует понимать, что все ссылки на фармацевтически приемлемые соли в случае одной и той же соли присоединения кислоты включают формы присоединения растворителя (сольваты) или кристаллические формы (полиморфы), которые определены в данном описании.
"Защищающая группа" или "защитная группа" означает группу, которая избирательно блокирует один из реакционно-способных центров в многофункциональном соединении, в связи с чем химическая реакция может избирательно протекать по другому незащищенному реакционно-способному центру, то есть группу, имеющую традиционно связываемое с ней значение в синтетической органической химии. Некоторые способы по данному изобретению основаны на том, что в реагентах имеются защищающие группы для блокирования реакционно-способных атомов азота и/или кислорода. Например, термины "амино-защитная группа" и "азот-защитная группа" используются в данном описании взаимозаменяемо и относятся к тем органическим группам, которые предназначены для защиты атома азота от нежелательных реакций во время процедур синтеза. Типичные азот-защитные группы включают, но не ограничиваются этим, трифторацетил, ацетамидо, бензил (Bn), бензилоксикарбонил (карбобензилокси, CBZ), п-метоксибензилоксикарбонил, п-нитробензилокси-карбонил, трет-бутоксикарбонил (ВОС) и тому подобное. Специалисту в данной области техники будет известно, как выбрать группу, удаление которой осуществляется легко и которая обладает способностью быть устойчивой в последующих реакциях.
Термин "сольваты" означает формы присоединения растворителя, которые содержат или стехиометрические, или нестехиометрические количества растворителя. Некоторые соединения в кристаллическом твердом состоянии имеют тенденцию захватывать молекулы растворителя в фиксированном молярном соотношении с образованием таким образом сольвата. Если растворителем является вода, то образованный сольват представляет собой гидрат, в том случае, когда растворителем является спирт, образованный сольват представляет собой алкоголят. Гидраты образуются путем объединения одной или более молекул воды с одним из веществ, в комбинации с которым вода сохраняет свое молекулярное состояние в виде H2O, при этом в результате такого объединения может образовываться один или более чем один гидрат.
"Болезнь Паркинсона" означает дегенеративное расстройство центральной нервной системы, при котором ухудшаются двигательные навыки, речевая и/или когнитивная функция. Симптомы болезни Паркинсона могут включать, например, мышечную ригидность, тремор, замедление физических движений (брадикинезию) и отсутствие физических движений (акинезию).
"Болезнь с тельцами Леви (Lewie или Lewy)", также называемая "деменцией с тельцами Леви", "болезнью диффузных телец Леви", "кортикальной деменцией с тельцами Леви", означает нейродегенеративное расстройство, морфологически характеризующееся присутствием телец Леви в головном мозге.
"Субъект" относится к млекопитающим и не млекопитающим. Термин "млекопитающие" означает любого представителя класса млекопитающих, включая, но не ограничиваясь этим, людей; не являющихся людьми приматов, таких как шимпанзе и другие обезьяны и виды макак; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы и свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, в том числе грызунов, таких как крысы, мыши и морские свинки; и им подобных. Примеры немлекопитающих включают, но не ограничиваются этим, птиц и им подобных. Термин "субъект" не указывает на конкретный возраст или пол.
"Терапевтически эффективное количество" означает количество соединения, которое при введении субъекту для лечения болезненного состояния, является достаточным для осуществления такого лечения в отношении данного болезненного состояния. "Терапевтически эффективное количество" будет варьировать в зависимости от соединения, подвергаемого лечению болезненного состояния, тяжести или подвергаемого лечению заболевания, возраста и относительного состояния здоровья субъекта, пути и формы введения, проницательности лечащего врача или ветеринара и других факторов.
Термины "те, которые описаны выше" и "те, которые определены в данном описании", когда они имеют отношение к переменной величине, включают посредством ссылки широкое определение для данной переменной, а также конкретные определения, если таковые имеются.
Термин "подвергание лечению" или "лечение" болезненного состояния включает в себя, помимо прочего, подавление болезненного состояния, т.е. приостановку развития болезненного состояния или его клинических симптомов, и/или облегчение болезненного состояния, т.е. вызывание временной или постоянной ремиссии болезненного состояния или его клинических симптомов.
Термины "обработка", "приведение в контакт" и "подвергание взаимодействию", когда они имеют отношение к химической реакции, означают добавление или смешивание двух или более реагентов в соответствующих условиях с получением указанного и/или желаемого продукта. Должно быть очевидно, что реакция, после выполнения которой получается указанный и/или желаемый продукт, не обязательно должна быть результатом непосредственного объединения двух реагентов, которые были добавлены первоначально, т.е. могут присутствовать одно или более промежуточных соединений, которые образуются в данной смеси, что в конечном итоге приводит к образованию указанного и/или желаемого продукта.
Номенклатура и структуры
В общем случае, использованная в этой заявке номенклатура основывается на компьютеризированной системе института Бейльштейна AUTONOM™, v.4.0, для создания систематической номенклатуры IUPAC (International Union of Pure and Applied Chemistry - Международный союз по теоретической и прикладной химии). Химические структуры, показанные в данном описании, получали с использованием ISIS®, версии 2.2. Любая свободная валентность, показанная на атоме углерода, кислорода, серы или азота, в приведенных в данном описании структурах указывает на присутствие атома водорода, если не указано иное. Если азот-содержащее гетероарильное кольцо показано со свободной валентностью на атоме азота, и на этом гетероарильном кольце отмечены переменные, как например, Ra, Rb или Rc, то такие переменные могут быть связаны с азотом, имеющим свободную валентность, или присоединены к нему. Если в структуре существуют один или более хиральных центров, но для этих хиральных центров никакой конкретной стереохимии не показано, то данной структурой охватываются оба энантиомера, ассоциированные с каждым таким хиральным центром. Если структура, показанная в данном описании, может существовать во множественных таутомерных формах, то все такие таутомеры охватываются данной структурой. Подразумевается, что атомы, представленные в данном описании в таких структурах, охватывают все природные изотопы таких атомов. Так, например, подразумевается, что атомы водорода, представленные в данном описании, включают дейтерий и тритий, и подразумевается, что атомы углерода включают изотопы С13 и С14.
Соединения по изобретению
Согласно изобретению предложены соединения формулы I:
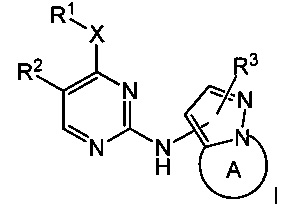
или их фармацевтически приемлемая соль,
где:
X представляет собой: -NRa- или -О-, где Ra представляет собой водород или С1-6алкил;
R1 представляет собой: С1-6алкил; С2-6алкенил; С2-6алкинил; галоген-С1-6алкил; С1-6алкокси-С1-6алкил; гидрокси-С1-6алкил; амино-С1-6алкил; С1-6алкилсульфонил-С1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз С1-6алкилом; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз С1-6алкилом; гетероциклил, возможно, замещенный один или более раз группой R5; или гетероциклил-C1-6алкил, возможно, замещенный один или более раз группой R5;
или X и R1 вместе образуют С1-6алкил; С1-6алкокси-С1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4;
или R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать трех-шестичленное гетероциклическое кольцо, возможно, замещенное один или более раз группой R5;
R2 представляет собой: С1-6алкил; атом галогена; С1-6алкокси; циано; С2-6алкинил; С2-6алкенил; галоген-С1-6алкил; галоген-С1-6алкокси; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; -ORb, где Rb представляет собой С1-6алкил, С3-6циклоалкил, возможно, замещенный один или более раз группой R4, или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; или -C(O)-Rc, где Rc представляет собой С1-6алкил, С1-6алкокси, амино или гетероциклил, возможно, замещенный один или более раз группой R5;
R3 представляет собой: водород; С1-6алкил; атом галогена; циано; галоген-C1-6алкил; С2-6алкенил; С2-6алкинил; С2-6алкокси; С1-6алкокси-С1-6алкил; гидрокси-C1-6алкил; С3-6циклоалкил, возможно, замещенный один или более раз группой R4; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4; или -Y-C(O)-Rd;
Y представляет собой С2-6алкилен или связь;
Rd представляет собой С1-6алкил, C1-6алкокси, амино, С1-6алкиламино, ди-C1-6алкиламино, галоген-С1-6алкиламино, дигалоген-С1-6алкиламино, галоген-C1-6алкил, гидрокси-С1-6алкил, гидрокси, С1-6алкокси-С1-6алкил, циано-С1-6алкил, С1-6алкилсульфонилС1-6алкил, амино-С1-6алкил, С3-6циклоалкил, возможно, замещенный один или более раз группой R4, С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4, гетероциклил, возможно, замещенный один или более раз группой R5, или гетероциклил-С1-6алкил, гетероциклильная часть которого, возможно, замещена один или более раз группой R5;
каждый R4 независимо представляет собой: C1-6алкил; галоген-С1-6алкил; С1-6алкокси; оксо; циано; атом галогена или -Y-C(O)-Rd;
каждый R5 независимо представляет собой: C1-6алкил; галоген-С1-6алкил; атом галогена; оксо; С1-6алкокси; С1-6алкилсульфонил; С1-6алкокси-С1-6алкил; циано; -Y-C(O)-Rd; гетероциклил; гетероциклил-С1-6алкил; С3-6циклоалкил; С3-6циклоалкил-С1-6алкил или С3-6циклоалкилсульфонил;
А представляет собой пяти- или шестичленное ненасыщенное или насыщенное карбоциклическое кольцо, которое, возможно, может содержать гетероатом, выбранный из О, N и S, и которое может быть замещено один или более раз группой R6; и
каждый R6 независимо представляет собой: оксо; С1-6алкил; галоген-C1-6алкил; С1-6алкокси; С1-6алкокси-С1-6алкил; циано; циано-С1-6алкил; -Y-C(O)-Rd; С3-6циклоалкил, гетероциклил или С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях согласно изобретению предложены соединения формулы I или их фармацевтически приемлемая соль, где X представляет собой NH, R1 представляет собой метил, и R2 представляет собой CF3.
В некоторых воплощениях согласно изобретению предложены соединения формулы I или их фармацевтически приемлемая соль, где X представляет собой NH, R1 представляет собой этил, и R2 представляет собой CF3.
В некоторых воплощениях согласно изобретению предложены соединения формулы I или их фармацевтически приемлемая соль, где X представляет собой NH, R1 представляет собой циклопропил, и R2 представляет собой CF3.
В некоторых воплощениях согласно изобретению предложены соединения формулы IIA или формулы IIB:
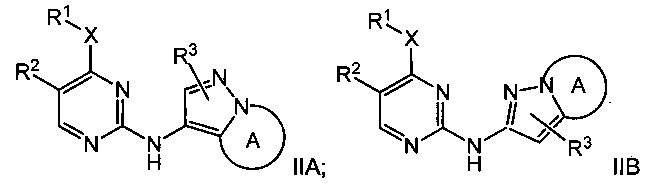
или их фармацевтически приемлемая соль,
где X, R1, R2, R3 и А являются такими, как определено в данном описании.
В некоторых воплощениях соединения представляют собой соединения формулы IIA.
В некоторых воплощениях соединения представляют собой соединения формулы IIB.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -NRa- или -О-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -NRa.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -О-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -NH- или -О-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -NH-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X представляет собой -О-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Ra представляет собой водород.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Ra представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: С1-6алкил; С2-6алкенил; С2-6алкинил; галоген-С1-6алкил; С1-6алкокси-С1-6алкил; гидрокси-С1-6алкил; амино-С1-6алкил; С1-6алкилсульфонил-С1-6алкил; С3-6циклоалкил, возможно, замещенный С1-6алкилом; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом; гетероциклил или гетероциклил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: С1-6алкил; галоген-С1-6алкил; С1-6алкокси-С1-6алкил; амино-С1-6алкил; С1-6алкилсульфонил-С1-6алкил; С3-6циклоалкил или С3-6циклоалкил-C1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: С1-6алкил; С3-6циклоалкил, возможно, замещенный С1-6алкилом; или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: С1-6алкил; галоген-С1-6алкил; C1-6алкокси-С1-6алкил; амино-С1-6алкил; С1-6алкилсульфонил-С1-6алкил; тетрагидрофуранил; тетрагидрофуранил-С1-6алкил; оксетанил или оксетан-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: С1-6алкил; галоген-С1-6алкил; С1-6алкокси-С1-6алкил; амино-С1-6алкил или С1-6алкилсульфонил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С1-6алкил или галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С1-6алкокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой амино-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С1-6алкилсульфонил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С3-6циклоалкил, возможно, замещенный С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена C1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой гетероциклил или гетероциклил-С1-6алкил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R1 представляет собой гетероциклил или гетероциклил-С1-6алкил, такой гетероциклил может представлять собой пиперидинил, пиперазинил, морфолинил, тетрагидропиранил, пирролидинил, тетрагидрофуранил или оксетанил, каждый из которых, возможно, замещен так, как определено в данном описании.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R1 представляет собой гетероциклил или гетероциклил-С1-6алкил, такой гетероциклил может представлять собой тетрагидропиранил, пиперидинил, тетрагидрофуранил или оксетанил, каждый из которых, возможно, замещен так, как определено в данном описании.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой тетрагидрофуранил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой тетрагидропиранил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой тетрагидрофуранил-С1-6алкил или оксетанил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой тетрагидрофуранил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой оксетанил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой оксетан-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопропил; циклобутил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил; циклопропилэтил; метоксиэтил; оксетанил; тетрагидропиранил; 2,2-дифторэтил или тетрагидрофуранил метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил; циклопропилэтил; метоксиэтил; оксетанил; тетрагидропиранил; 2,2-дифторэтил или тетрагидрофуранилметил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопентил; циклогексил; циклопентилметил; метоксиэтил; оксетанил; тетрагидропиранил или тетрагидрофуранилметил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой 2,2-дифторэтил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: метил; этил; н-пропил; изопропил или изобутил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой метил, этил или циклопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой метил или этил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой этил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: циклопропил; циклобутил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил или циклопропилэтил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой: циклопентил; циклогексил или циклопентилметил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 представляет собой циклопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать трех-шестичленное гетероциклическое кольцо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать трехчленное гетероциклическое кольцо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать четырехчленное гетероциклическое кольцо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать пятичленное гетероциклическое кольцо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R1 и Ra вместе с атомами, к которым они присоединены, могут образовывать шестичленное гетероциклическое кольцо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X и R1 вместе образуют С1-6алкил; С3-6циклоалкил, возможно, замещенный С1-6алкилом; или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X и R1 вместе образуют С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X и R1 вместе образуют С3-6циклоалкил, возможно, замещенный C1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB X и R1 вместе образуют С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: С1-6алкил; атом галогена; С1-6алкокси; циано; С2-6алкинил; С2-6алкенил; галоген-С1-6алкил; галоген-С1-6алкокси; С3-6циклоалкил, возможно, замещенный С1-6алкилом; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом; -ORb, где Rb представляет собой С1-6алкил, С3-6циклоалкил, возможно, замещенный C1-6алкилом, или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом; или -C(O)-Rc.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена; С1-6алкокси; галоген-C1-6алкил; галоген-С1-6алкокси; С3-6циклоалкил, возможно, замещенный С1-6алкилом; С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6алкил; оксетанил или оксетан-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена; С1-6алкокси; галоген-С1-6алкил; циано; С2-6алкинил; С2-6алкенил; С3-6циклоалкил или С3-6циклоалкил-C1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена; С1-6алкокси; галоген-С1-6алкил; циано; С3-6циклоалкил или С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена; С1-6алкокси; галоген-С1-6алкил; С3-6циклоалкил или С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена; галоген-С1-6алкил или циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом фтора; брома; хлора; иода; трифторметил или циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом хлора; трифторметил или циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой: атом галогена или галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой галоген-С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С3-6циклоалкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой тетрагидрофуранил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой тетрагидрофуранил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой оксетанил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой оксетан-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом фтора, хлора или брома.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом хлора.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом фтора.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом брома.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой атом йода.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой трифторметил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой метокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С2-6алкинил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой С2-6алкенил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R2 представляет собой -ORb, где Rb представляет собой С1-6алкил, С3-6циклоалкил, возможно, замещенный C1-6алкилом, или С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом.
В некоторых воплощениях соединений формулы I R2 представляет собой -C(O)-Rc, где Rc представляет собой С1-6алкил, С1-6алкокси, амино или гетероциклил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; С1-6алкил; атом галогена; циано; галоген-С1-6алкил; С2-6алкенил; С2-6алкинил; С1-6алкокси; С1-6алкокси-С1-6алкил; гидрокси-С1-6алкил; С3-6циклоалкил или С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; С1-6алкил; галоген-С1-6алкил; С3-6циклоалкил или С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; С1-6алкил или С3-6циклоалкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; С1-6алкил; атом галогена или С3-6циклоалкил, возможно, замещенный С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой водород или C1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой водород.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С1-6алкокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой гидрокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С3-6циклоалкил, возможно, замещенный С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой водород или метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена С1-6алкилом.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой -C(O)-Rc, где Rc представляет собой С1-6алкил, С1-6алкокси, амино или гетероциклил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой -C(O)-Rc, где Rc представляет собой гетероциклил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где Rc представляет собой гетероциклил, такой гетероциклил может представлять собой пирролидинил, пиперидинил, пиперазинил или морфолинил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где Rc представляет собой гетероциклил, такой гетероциклил может представлять собой пиперидинил, пиперазинил или морфолинил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; метил; изопропил; циклопропил; атом хлора или морфолин-4-ил-карбонил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой: водород; метил; изопропил; циклопропил или атом хлора.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой изопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой циклопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой атом хлора.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой морфолин-4-ил-карбонил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой 2-фтор-этил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С3-6циклоалкил, возможно, замещенный один или более раз или один или два раза группой R4.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз или один или два раза группой R6.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R3 представляет собой -Y-C(O)-Rd.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой связь.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой С2-6алкилен.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой изопропилидин.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой метилен.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой этилен.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой -С(СН3)2-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой -СН2-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой -СН(СН3)-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой -СН2-С(СН3)2-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Y представляет собой -С(СН3)2-СН2-.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С1-6алкил, С1-6алкокси, амино или гетероциклил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой амино.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой гидрокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С1-6алкокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой циано-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С1-6алкилсульфонилС1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой амино-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С3-6циклоалкил, возможно, замещенный один или более раз группой R4.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой С3-6циклоалкил-С1-6алкил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R4.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой гетероциклил, возможно, замещенный один или более раз группой R5.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой гетероциклил-С1-6алкил, гетероциклильная часть которого, возможно, замещена один или более раз группой R5.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой 1-метил-циклопропил; метиламино; диметиламино; пирролидин-1-ил; метокси; циклопропил-метил; этил; 2,2,2-трифтор-этил; трет-бутил или изопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой 1-метил-циклопропил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой метиламино.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой диметиламино.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой пирролидин-1-ил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой метокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой циклопропил-метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой этил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой 2,2,2-трифтор-этил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой трет-бутил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB Rd представляет собой изопропил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где Rd представляет собой гетероциклил или гетероциклил-С1-6алкил, такой гетероциклил может представлять собой пиперидинил, пиперазинил, морфолинил, тетрагидропиранил, пирролидинил, азетидинил, тетрагидрофуранил или оксетанил, каждый из которых, возможно, замещен один или более раз или один или два раза группой R5, определенной в данном описании.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где Rd представляет собой гетероциклил, такая гетероциклильная группировка может представлять собой пиперидинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил, каждый из которых не замещен или замещен один или более раз группой R5.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где Rd представляет собой гетероциклил-С1-6алкил, такая гетероциклильная группировка может представлять собой пиперидинил, пиперазинил, морфолинил, тиоморфолинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил, каждый из которых не замещен или замещен один или более раз группой R5.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой С1-6алкил; галоген-С1-6алкил; С1-6алкокси или атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой С1-6алкил; галоген-С1-6алкил или атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой -Y-C(O)-Rd.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R4 представляет собой оксо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB каждый R5 независимо представляет собой С1-6алкил; галоген-С1-6алкил; атом галогена; С1-6алкилсульфонил; С1-6алкокси-С1-6алкил; циано; гетероциклил или С3-6циклоалкилсульфонил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R6.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB каждый R5 независимо представляет собой С1-6алкил; галоген-С1-6алкил или атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой C1-6алкилсульфонил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С1-6алкокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой -Y-C(O)-Rd.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой гетероциклил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С3-6циклоалкилсульфонил, С3-6циклоалкильная часть которого, возможно, замещена один или более раз группой R6.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой оксо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой гетероциклил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С3-6циклоалкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R5 представляет собой С3-6циклоалкил-С1-6алкил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R5 представляет собой гетероциклил, такая гетероциклильная группировка может представлять собой пиперидинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R5 представляет собой гетероциклил-С1-6алкил, такая гетероциклильная группировка может представлять собой пиперидинил, пиперазинил, морфолинил, тиоморфолинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А представляет собой пятичленное кольцо.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А представляет собой шестичленное кольцо.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А является насыщенным.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А является ненасыщенным.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А является карбоциклическим.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А содержит гетероатом, выбранный из О, N и S.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А содержит гетероатом О.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А содержит гетероатом N.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А содержит гетероатом S.
В воплощениях соединений формулы I, формулы IIA или формулы IIB, кольцо А замещено по меньшей мере один раз группой R6.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А замещено по меньшей мере один раз группой R6.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А замещено один, два или три раза группой R6.
В воплощениях соединений формулы I, формулы IIA или формулы IIB кольцо А замещено один, два, три или четыре раза группой R6.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой оксо.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой метил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой галоген-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой атом галогена.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С1-6алкилсульфонил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С1-6алкокси.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С1-6алкокси-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой циано.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой циано-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой -Y-C(O)-Rd.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С3-6циклоалкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой С3-6циклоалкил-С1-6алкил.
В некоторых воплощениях соединений формулы I, формулы IIA или формулы IIB R6 представляет собой гетероциклил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой гетероциклил, такая гетероциклильная группировка может представлять собой пиперидинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой С3-6циклоалкил или гетероциклил, такой С3-6циклоалкил или гетероциклил может быть присоединен к кольцу А либо: (а) посредством одинарной связи с атомом кольца А; либо (b) посредством двух связей с одним и тем же атомом углерода в кольце А, в геминальном положении (т.е. кольцо А и гетероциклил или С3-6циклоалкил, присоединенный к нему, образуют "спиро"-бициклическую структуру); либо (с) посредством двух связей, каждая из которых присоединяется к соседним атомам углерода в кольце А в вицинальном положении (т.е. кольцо А и гетероциклил или С3-6циклоалкил, присоединенный к нему, являются "конденсированными").
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой С3-6циклоалкил или гетероциклил, такой С3-6циклоалкил или гетероциклил присоединен к кольцу А посредством одинарной связи с атомом кольца А.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой С3-6циклоалкил или гетероциклил, такой С3-6циклоалкил или гетероциклил присоединен к кольцу А посредством двух связей с одним и тем же атомом углерода в кольце А, в геминальном положении (т.е. кольцо А и гетероциклил или С3-6циклоалкил, присоединенный к нему, образуют "спиро"-бициклическую структуру).
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой С3-6циклоалкил или гетероциклил, такой С3-6циклоалкил или гетероциклил присоединен к кольцу А посредством двух связей, каждая из которых присоединяется к соседним атомам углерода в кольце А в вицинальном положении (т.е. кольцо А и гетероциклил или С3-6циклоалкил, присоединенный к нему, являются "конденсированными").
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой гетероциклил, такая гетероциклильная группировка может представлять собой пиперидинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил.
В тех воплощениях соединений формулы I, формулы IIA или формулы IIB, где R6 представляет собой гетероциклил-С1-6алкил, такая гетероциклильная группировка может представлять собой пиперидинил, пиперазинил, морфолинил, тиоморфолинил, пирролидинил, оксетанил, тетрагидропиранил, тетрагидрофуранил, азетидинил, [1,3]диоксоланил или тетрагидротиопиранил.
В некоторых воплощениях согласно изобретению предложены соединения формулы III:
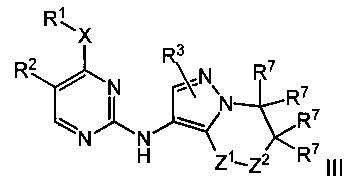
или их фармацевтически приемлемая соль, где:
один из Z1 и Z2 представляет собой -О- или -NR7-, а другой представляет собой -C(R7)2-;
или оба Z1 и Z2 представляют собой -C(R7)2-;
каждый R7 независимо представляет собой: водород или C1-6алкил;
или две группы из групп R7 вместе с атомом или атомами, к которым они присоединены, могут образовывать четырех-семичленное ненасыщенное кольцо, которое является карбоциклическим или которое включает гетероатом, выбранный из О, N и S; и
R1, R2 и R3 являются такими, как определено в данном описании.
В некоторых воплощениях соединений формулы III Z1 представляет собой -О-, a Z2 представляет собой -C(R7)2-.
В некоторых воплощениях соединений формулы III Z1 представляет собой -NR7-, a Z2 представляет собой -C(R7)2-.
В некоторых воплощениях соединений формулы III Z2 представляет собой -О-, a Z1 представляет собой -C(R7)2-.
В некоторых воплощениях соединений формулы III Z2 представляет собой -NR7-, a Z1 представляет собой -C(R7)2-.
В некоторых воплощениях соединений формулы III Z1 и Z2 представляют собой -C(R7)2-.
В некоторых воплощениях соединений формулы III по меньшей мере одна группа из групп R7 представляет собой С1-6алкил.
В некоторых воплощениях соединений формулы III одна или две группы из групп R7 представляют собой С1-6алкил.
В некоторых воплощениях соединений формулы III одна, две или три группы из групп R7 представляют собой С1-6алкил.
В некоторых воплощениях соединений формулы III две группы из групп R7 вместе с атомом или атомами, к которым они присоединены, образуют четырех-семичленное ненасыщенное кольцо, которое является карбоциклическим или которое включает гетероатом, выбранный из О, N и S.
В некоторых воплощениях соединений формулы III две группы из групп R7 вместе с атомом или атомами, к которым они присоединены, образуют четырех-семичленное ненасыщенное карбоциклическое кольцо.
В некоторых воплощениях соединений формулы III две группы из групп R7 вместе с атомом или атомами, к которым они присоединены, образуют четырех-семичленное ненасыщенное кольцо, которое включает гетероатом, выбранный из О, N и S.
В тех воплощениях соединений формулы III, где две группы из групп R7 образуют кольцо, такие группы R7 могут быть либо: (а) связаны с одним и тем же атомом углерода в кольце А, в геминальном положении (т.е. кольцо А и кольцо, образованное группами R7, присоединенное к нему, образуют "спиро"-бициклическую структуру); либо (b) связаны с соседними атомами в кольце А в вицинальном положении (т.е. кольцо А и кольцо, образованное группами R7, присоединенное к нему, являются "конденсированными"); либо (с) связаны с отдельными несоседними атомами в кольце А.
В тех воплощениях соединений формулы III, где две группы из групп R7 образуют кольцо, такие R7 связаны с одним и тем же атомом углерода в кольце А, в геминальном положении (т.е. кольцо А и кольцо, образованное группами R7, присоединенное к нему, образуют "спиро"-бициклическую структуру).
В тех воплощениях соединений формулы III, где две группы из групп R7 образуют кольцо, такие группы R7 связаны с соседними атомами в кольце А в вицинальном положении (т.е. кольцо А и кольцо, образованное группами R7, присоединенное к нему, являются "конденсированными").
В тех воплощениях соединений формулы III, где две группы из групп R7 образуют кольцо, такие группы R7 связаны с отдельными несоседними атомами в кольце А.
Согласно изобретению также предложен способ лечения заболевания или состояния, опосредованного или иным образом ассоциированного с рецептором LRRK2, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по изобретению.
Заболевание может представлять собой нейродегенеративное заболевание, такое как болезнь Паркинсона, болезнь Гентингтона или деменция с тельцами Леви.
Заболевание может представлять собой расстройство ЦНС, такое как болезнь Альцгеймера или L-допа-индуцированная дискинезия.
Заболевание может представлять собой рак или пролиферативное расстройство, такое как рак почки, молочной железы, предстательной железы, крови, папиллярный рак или рак легкого, острый миелогенный лейкоз или множественная миелома.
Заболевание может представлять собой воспалительное заболевание, такое как лепра, болезнь Крона, боковой амиотрофический склероз, ревматоидный артрит или анкилозирующий спондилит.
Согласно изобретению также предложен способ улучшения когнитивной памяти, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по изобретению.
В воплощениях по изобретению предложено соединение, описанное в данной заявке, для применения в качестве терапевтически активного вещества.
В воплощениях по изобретению предложено соединение, описанное в данной заявке, для применения в качестве терапевтически активного вещества для терапевтического и/или профилактического лечения болезни Паркинсона.
В воплощениях по изобретению предложено применение соединения, описанного в данной заявке, при терапевтическом и/или профилактическом лечении болезни Паркинсона.
Репрезентативные соединения, соответствующие способам по изобретению, показаны в экспериментальных примерах ниже.
Синтез
Соединения по настоящему изобретению могут быть получены разными способами, представленными на иллюстративных схемах реакций синтеза, показанных и описанных ниже.
Исходные вещества и реагенты, используемые при получении этих соединений, обычно либо приобретают у коммерческих поставщиков, таких как Aldrich Chemical Co., либо получают способами, известными специалистам в данной области техники, следуя методикам, изложенным в таких ссылках, как Fieser L.F. and Fieser М. Reagents for Organic Synthesis; Wiley & Sons: New York, 1991, Volumes 1-15; Rodd (ed.) Chemistry of Carbon Compounds, Elsevier Science Publishers, 1989, Volumes 1-5 and Supplemental; и Organic Reactions, Wiley & Sons: New York, 1991, Volumes 1-40. Приведенные далее схемы реакций синтеза являются лишь иллюстрацией некоторых способов, согласно которым могут быть синтезированы соединения по изобретению, и могут быть выполнены различные модификации этих схем реакций синтеза, и они будут предложены специалисту в данной области со ссылкой на описание, содержащееся в этой заявке.
Исходные вещества и промежуточные соединения, приведенные на схемах реакций синтеза, при желании могут быть выделены и очищены с использованием традиционных методов, включая, но не ограничиваясь этим, фильтрацию, дистилляцию, кристаллизацию, хроматографию и им подобные. Такие вещества могут быть охарактеризованы с использованием традиционных средств, включая данные о физических константах и спектральные данные.
Если не указано иное, реакции, изложенные в данном описании, можно проводить в атмосфере инертного газа при атмосферном давлении в диапазоне температур реакции от примерно -78°С до примерно 150°С, например, от примерно 0°С до примерно 125°С или в целях удобства при температуре приблизительно комнатной (или температуре окружающей среды), например, при приблизительно 20°С.
Приведенная ниже схема А иллюстрирует одну из методик синтеза, используемых для получения конкретных соединений формулы I, где X, R1, R2, R3, R4 и R5 являются такими, как определено в данном описании.
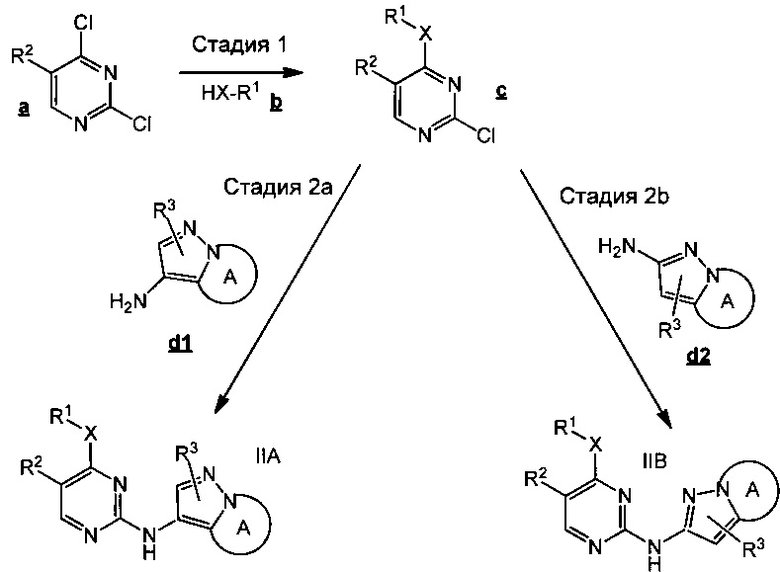
СХЕМА А
На стадии 1 схемы А дихлорпиримидиновое соединение а приводят во взаимодействие с реагентом b, получая пиримидиновое соединение с. Реакция на стадии 1 может протекать в условиях полярного растворителя. В тех воплощениях изобретения, где X представляет собой -О- (реагент b представляет собой спирт), реакция на стадии 1 может быть осуществлена в присутствии основания.
После стадии 1 осуществляют одну из стадий 2а или 2b. На стадии 2а пиримидиновое соединение с подвергают взаимодействию с 4-аминопиразоловым соединением d1, получая аминопиримидиновое соединение формулы IIa. На стадии 2b пиримидиновое соединение с приводят во взаимодействие с 5-аминопиразоловым соединением d2, получая аминопиримидиновое соединение формулы IIb. Реакция на стадиях 2а и 2b может протекать в полярном протонном растворителе и в присутствии кислоты, такой как HCl.
Возможно существование многих вариантов методики со схемы А, и они будут предложены специалистам в данной области техники. Конкретные детали получения соединений по изобретению описаны в приведенных ниже примерах.
Введение и фармацевтическая композиция
Изобретение включает фармацевтические композиции, содержащие по меньшей мере одно соединение по настоящему изобретению или один индивидуальный изомер, одну рацемическую или нерацемическую смесь изомеров или их фармацевтически приемлемые соль или сольват вместе по меньшей мере с одним фармацевтически приемлемым носителем и, возможно, другими терапевтическими и/или профилактическими ингредиентами.
В общем случае соединения по изобретению будут введены в терапевтически эффективном количестве любым из способов введения, приемлемых для средств, используемых при аналогичных состояниях. Подходящие диапазоны дозировок обычно составляют 1-500 мг один раз в сутки, например 1-100 мг один раз в сутки и в некоторых воплощениях 1-30 мг один раз в сутки в зависимости от многочисленных факторов, таких как тяжесть подлежащего лечению заболевания, возраст и относительное состояние здоровья субъекта, эффективность используемого соединения, путь и форма введения, показание, в отношении которого направлено такое введение, а также предпочтения и опыт лечащего врача. Средний специалист в области лечения таких заболеваний будет способен, без излишнего экспериментирования и руководствуясь персональными знаниями и описанием этой заявки, определить терапевтически эффективное количество соединений по настоящему изобретению, необходимое для данного заболевания.
Соединения по изобретению могут быть введены в виде фармацевтических композиций, включая композиции, подходящие для перорального (в том числе трансбуккального и сублингвального), ректального, назального, местного, легочного, вагинального или парентерального (в том числе внутримышечного, интраартериального, интратекального, подкожного и внутривенного) введения, или в форме, подходящей для введения посредством ингаляции или инсуффляции. Конкретным способом введения обычно является пероральный с использованием удобного режима введения один раз в сутки, который может быть откорректирован в соответствии с тяжестью заболевания.
Соединение или соединения по изобретению вместе с одним или более чем одним традиционным адъювантом, носителем или разбавителем могут быть представлены в форме фармацевтических композиций и стандартных лекарственных форм. Фармацевтические композиции и стандартные лекарственные формы могут содержать традиционные ингредиенты в обычных пропорциях с добавлением или без добавления дополнительных активных соединений или действующих начал, и стандартные лекарственные формы могут содержать любое подходящее эффективное количество активного ингредиента в соответствии с предполагаемым диапазоном суточных дозировок, который будет применен. Фармацевтические композиции могут быть использованы в виде твердых веществ, таких как таблетки или заполненные капсулы, полутвердых веществ, порошков, композиций с длительным высвобождением или жидкостей, таких как растворы, суспензии, эмульсии, эликсиры или заполненные капсулы для перорального применения; или в форме суппозиториев для ректального или вагинального введения; или в форме стерильных инъекционных растворов для парентерального применения. Соответственно, композиции, содержащие примерно один (1) миллиграмм активного ингредиента или, в более широком диапазоне, от примерно 0,01 до примерно ста (100) миллиграммов на одну таблетку, представляют собой подходящие репрезентативные стандартные лекарственные формы.
На основе соединений по настоящему изобретению могут быть изготовлены разнообразные лекарственные формы для перорального введения. Фармацевтические композиции и лекарственные формы в качестве активного компонента могут содержать соединение или соединения по настоящему изобретению или их фармацевтически приемлемые соли. Фармацевтически приемлемые носители могут быть или в твердой, или в жидкой форме. Препараты в твердой форме включают порошки, таблетки, пилюли, капсулы, облатки, суппозитории и диспергируемые гранулы. Твердым носителем может быть одно или более веществ, которые также могут действовать в качестве разбавителей, корригентов, солюбилизаторов, смазывающих веществ, суспендирующих агентов, связующих веществ, консервантов, разрыхлителей для таблеток или инкапсулирующего материала. Носитель в порошках обычно является тонкоизмельченным твердым веществом, которое представляет собой смесь вместе с тонкоизмельченным активным компонентом. Активный компонент в таблетках обычно смешан в подходящих пропорциях с носителем, обладающим необходимой связывающей способностью, и скомпактизован до желаемых формы и размера. Порошки и таблетки могут содержать от примерно одного (1) до примерно семидесяти (70) процентов активного соединения. Подходящие носители включают, но не ограничиваются этим, карбонат магния, стеарат магния, тальк, сахар, лактозу, пектин, декстрин, крахмал, желатин, трагакант, метилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, легкоплавкий воск, масло какао и тому подобное. Подразумевается, что термин "препарат" включает в себя композицию активного соединения с инкапсулирующим материалом в качестве носителя, обеспечивающим получение капсулы, в которой активный компонент с носителями или без них окружен носителем, который оказывается ассоциированным с ним. Аналогичным образом включены облатки и пастилки для рассасывания. Таблетки, порошки, капсулы, пилюли, облатки и пастилки для рассасывания могут быть в виде твердых форм, подходящих для перорального введения.
Другие формы, подходящие для перорального введения, включают препараты в жидкой форме, в том числе эмульсии, сиропы, эликсиры, водные растворы, водные суспензии или препараты в твердой форме, предназначенные для преобразования их в препараты в жидкой форме незадолго до применения. Эмульсии могут быть приготовлены в растворах, например, в водно-пропиленгликолиевых растворах, или могут содержать такие эмульгирующие агенты, как лецитин, моноолеат сорбитана или аравийская камедь. Водные растворы могут быть приготовлены путем растворения активного компонента в воде и добавления подходящих красителей, корригентов, стабилизаторов и загустителей. Водные суспензии могут быть приготовлены путем диспергирования тонкоизмельченного активного компонента в воде с вязким веществом, таким как природные или синтетические камеди, смолы, метил целлюлоза, натриевая соль карбоксиметилцеллюлозы и другие хорошо известные суспендирующие агенты. Препараты в жидкой форме включают растворы, суспензии и эмульсии и могут содержать помимо активного компонента красители, корригенты, стабилизаторы, буферы, искусственные и природные подсластители, диспергирующие вещества, загустители, солюбилизирующие агенты и тому подобное.
На основе соединений по настоящему изобретению могут быть изготовлены композиции для парентерального введения (например, путем инъекции, например болюс-инъекции или непрерывной инфузии), которые могут быть представлены в стандартной лекарственной форме в ампулах, предварительно заполненных шприцах, капельницах небольшого объема или в контейнерах для многократного введения с добавленным консервантом. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных разбавителях, например, растворы в водном полиэтиленгликоле. Примеры масляных или неводных носителей, разбавителей, растворителей или наполнителей включают пропиленгликоль, полиэтиленгликоль, растительные масла (например, оливковое масло) и инъекционные органические сложные эфиры (например, этилолеат) и могут содержать такие входящие в состав композиции агенты, как консерванты, увлажняющие, эмульгирующие или суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в порошковой форме, полученной в результате выделения стерильного твердого вещества в асептических условиях или в результате лиофилизации из раствора, для повторного разведения подходящим разбавителем, например стерильной апирогенной водой, перед применением.
На основе соединений по настоящему изобретению могут быть изготовлены композиции для местного введения в эпидермис в виде мазей, кремов или лосьонов или в виде трансдермального пластыря. Мази и кремы могут быть изготовлены, например, с использованием водной или масляной основы с добавлением подходящих загущающих и/или желатинизирующих агентов. Лосьоны могут быть изготовлены с использованием водной или масляной основы и в общем случае также будут содержать один или более эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, загустителей или красителей. Композиции, подходящие для местного введения в ротовую полость, включают пастилки для рассасывания, содержащие активные агенты в корригентной основе, обычно сахарозе и аравийской или трагакантовой камеди; пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин или сахароза и аравийская камедь; и жидкости для полоскания рта, содержащие активный ингредиент в подходящем жидком носителе.
На основе соединений по настоящему изобретению могут быть изготовлены композиции для введения в виде суппозиториев. Сначала расплавляют легкоплавкий воск, такой как смесь глицеридов жирных кислот или масло какао, и в нем гомогенно диспергируют активный компонент, например, путем перемешивания. Расплавленную гомогенную смесь затем выливают в формы удобного размера, оставляют охладиться и отвердеть.
На основе соединений по настоящему изобретению могут быть изготовлены композиции для вагинального введения. Пессарии, тампоны, кремы, гели, пасты, пенки или спреи содержат помимо активного ингредиента такие носители, которые известны в данной области как приемлемые.
На основе соединений, являющихся предметом изобретения, могут быть изготовлены композиции для назального введения. Растворы или суспензии вводят непосредственно в носовую полость традиционными способами, например, с использованием капельницы, пипетки или спрея. Композиции могут быть представлены в лекарственной форме для однократного или многократного приема. В последнем случае с использованием капельницы или пипетки этого можно достичь путем введения пациентом соответствующего, предварительно заданного объема раствора или суспензии. В случае спрея этого можно достичь, например, посредством дозирующего мелкодисперсно распыляющего насоса.
На основе соединений по настоящему изобретению могут быть изготовлены композиции для аэрозольного способа введения, в частности в респираторный тракт, и в том числе для интраназального введения. Как правило, частицы, содержащие данное соединение будут иметь размер, соответствующий мелким частицам, например порядка пяти (5) микрон или меньше. Такого размера частиц можно добиться средствами, известными в данной области техники, например путем микронизации. Активный ингредиент представлен в находящейся под давлением упаковке вместе с подходящим пропеллентом, таким как хлорфторуглерод (CFC), например, дихлордифторметан, трихлорфторметан или дихлортетрафторэтан, либо двуокись углерода или другой подходящий газ. Удобно, если аэрозоль также может содержать поверхностно-активное вещество, такое как лецитин. Дозу лекарственного средства можно контролировать посредством дозирующего клапана. Альтернативно, активные ингредиенты могут быть представлены в форме сухого порошка, например порошковой смеси соединения в подходящей порошковой основе, такой как лактоза, крахмал, производные крахмала, например, в гидроксипропилметилцеллюлозе и поливинилпирролидоне (PVP). Порошковый носитель будет образовывать гель в носовой полости. Порошковая композиция может быть представлена в стандартной лекарственной форме, например в капсулах или картриджах из, например желатина, или блистерных упаковках, из которых находящийся там порошок можно вводить посредством ингалятора.
При желании композиции могут быть изготовлены с энтеросолюбильными покрытиями, адаптированными для введения активного ингредиента посредством длительного или регулируемого высвобождения. Например, на основе соединений по настоящему изобретению могут быть изготовлены устройства для трансдермальной или подкожной доставки лекарственных средств. Такие системы доставки имеют преимущество тогда, когда необходимо длительное высвобождение соединения и когда соблюдение больным режима и схемы лечения является принципиальным. Соединения в трансдермальных системах доставки часто нанесены на приклеиваемую к коже твердую подложку. Представляющее интерес соединение также может быть в комбинации с усилителем проницаемости, например, азоном (1-додецилазациклогептан-2-оном). Системы доставки с длительным высвобождением вводят подкожно в субдермальный слой путем хирургической манипуляции или инъекции. В подкожных имплантатах соединение заключено в липидорастворимую оболочку, например, из силиконового каучука или биоразлагаемого полимера, например, полимолочной кислоты.
Фармацевтические препараты предпочтительно находятся в стандартных лекарственных формах. Препарат в такой форме подразделен на стандартные дозы, содержащие соответствующие количества активного компонента. Стандартная лекарственная форма может представлять собой упакованный препарат, при этом такая упаковка содержит дискретные количества препарата, как например упакованные таблетки, капсулы и порошки во флаконах или ампулах. Кроме того, стандартная лекарственная форма может представлять собой только одну капсулу, таблетку, облатку или пастилку, или это может быть соответствующее количество любой из них в упакованной форме.
Другие подходящие фармацевтические носители и их составы описаны в Remington: The Science and Practice of Pharmacy, 1995, под редакцией E.W. Martin, Mack Publishing Company, 19-е издание, Easton, Pennsylvania. Репрезентативные фармацевтические композиции, содержащие соединение по настоящему изобретению, описаны ниже.
Полезность
Соединения по изобретению полезны для лечения LRRK2-опосредованных заболеваний или состояний, включая нейродегенеративные заболевания, такие как болезнь Паркинсона, деменция с тельцами Леви и болезнь Гентингтона, и для улучшения когнитивной памяти обычно у субъектов, нуждающихся в этом.
Примеры
Далее приведены подготовительные примеры и примеры, дающие возможность специалистам в данной области более четко понимать и применять на практике настоящее изобретение. Их не следует рассматривать как ограничивающие объем данного изобретения, а только как иллюстрирующие и характеризующие его.
Если не указано иное, все температуры, включая точки плавления (т.е. т.пл.), приведены в градусах по Цельсию (°С). Должно быть очевидно, что реакция, после выполнения которой получается указанный и/или желаемый продукт, не обязательно должна быть результатом непосредственного объединения двух реагентов, которые были добавлены первоначально, т.е. могут присутствовать одно или более промежуточных соединений, которые образуются в данной смеси, что в конечном итоге приводит к образованию указанного и/или желаемого продукта. В разделах "Подготовительные примеры" и "Примеры" могут быть использованы следующие сокращения.
Сокращения
АсОН уксусная кислота,
AIBN 2,2'-азобис(2-метилпропионитрил),
ат. атмосфера,
(ВОС)2O ди-трет-бутилдикарбонат,
dba трис(дибензилиденацетон),
DCM дихлорметан/метиленхлорид,
DIAD диизопропилазодикарбоксилат,
DIPEA диизопропилэтиламин,
DMAP 4-диметиламинопиридин,
DME 1,2-диметоксиэтан,
DMF N,N-диметилформамид,
DMSO диметилсульфоксид,
DPPF 1,1'-бис(дифенилфосфино)ферроцен,
Et2O диэтиловый эфир,
EtOH этанол/этиловый спирт,
EtOAc этилацетат,
HATU 2-(1Н-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония
гексафторфосфат метанаминий,
HBTU O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония гексафторфосфат,
НОВТ 1-гидроксибензотриазол,
HPLC жидкостная хроматография высокого давления,
RP HPLC обращенно-фазовая жидкостная хроматография высокого
давления,
i-PrOH изопропанол/изопропиловый спирт,
LCMS жидкостная хроматография/масс-спектроскопия,
МеОН метанол/метиловый спирт,
MW микроволновое излучение,
NBS N-бромсукцинимид,
NMP 1-метил-2-пирролидинон,
ф/кв. дюйм фунт на квадратный дюйм,
КТ комнатная температура,
SFC сверхкритическая жидкостная хроматография,
TBDMS трет-бутилдиметилсилил,
TFA трифторуксусная кислота,
THF тетрагидрофуран,
TLC тонкослойная хроматография,
Xphos 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил.
Жидкостная хроматография-масс-спектрометрия, метод А
LC-MS проводили на жидкостном хроматографе (LC) серии Agilent 1200, соединенном с квадрупольным масс-спектрометром Agilent 6140, используя колонку Agilent SD-C18 (1,8 мкм; 2,1×30 мм) с линейным градиентом смеси 3-95% ацетонитрил/вода (с 0,05% трифторуксусной кислоты в каждой подвижной фазе) в пределах 8,5 минуты и выдерживанием при 95% в течение 2,5 минуты.
Жидкостная хроматография-масс-спектрометрия, метод В
LC-MS проводили на HPLC-системе 2795 Alliance НТ от Waters с диодным матричным детектором 2996 от Waters, соединенным с Micromass ZQ, квадрупольным масс-спектрометром с одиночной фокусировкой, используя колонку Luna С18 (2) от Phenomenex (5 мкм, 100×4,6 мм плюс защитный картридж) с линейным градиентом смеси 5-95% ацетонитрил/вода (с 0,1% муравьиной кислоты в каждой подвижной фазе) в пределах 3,5 минуты и выдерживанием при 95% в течение 2,0 минуты.
Жидкостная хроматография-масс-спектрометрия, метод С
LC-MS проводили на HPLC-системе 2795 Alliance НТ от Waters с диодным матричным детектором 2996 от Waters, соединенным с Micromass ZQ, квадрупольным масс-спектрометром с одиночной фокусировкой, используя колонку Xterra MS С18 от Waters (5 мкм, 100×4,6 мм плюс guard картридж), которую сначала выдерживали в 5%-ном ацетонитриле в воде (с 10 мМ бикарбонатом аммония в водной подвижной фазе) в течение 0,5 минуты, после чего применяли линейный градиент 5-95% в пределах 3,5 минуты и затем выдерживали при 95% в течение 1,5 минуты.
Аналитические методы
Спектроскопию 1Н-ядерного магнитного резонанса (ЯМР) выполняли на приборе Bruker, работающем при 400 или 500 МГц, используя указанный растворитель при температуре примерно комнатной, если не указано иное. Во всех случаях, данные ЯМР находились в соответствии с предполагаемыми структурами. Характерные химические сдвиги (δ) приведены в миллионных долях с использованием традиционных сокращений для обозначения основных пиков: например s, синглет; d, дублет; t, триплет; q, квартет; dd, дублет дублетов; dt, дублет триплетов; br, уширенный. В случае применения тонкослойной хроматографии (TLC) речь идет о TLC на силикагеле с использованием пластинок силикагеля MK6F 60 Å, Rf представляет собой расстояние, на которое перемещается соединение, поделенное на расстояние, на которое перемещается растворитель на TLC-пластинке. Флэш-хроматография относится к хроматографии на силикагеле, и ее осуществляют с использованием системы для MPLC (жидкостная хроматография умеренного давления) SP4 или Isolara 4 (производства Biotage); предварительно упакованных силикагелевых картриджей (поставляемых Biotage); или с использованием традиционной хроматографии на стеклянных колонках.
Получение соединений
В тех случаях, когда получение исходных веществ не описано, их приобретают путем закупок, они известны из литературы или могут быть легко получены специалистами в данной области техники с использованием стандартных методик. Если указано, что соединения были получены аналогично соединениям из приведенных ранее примеров или аналогично промежуточным соединениям, то специалисту будет очевидно, что продолжительность реакции, количество эквивалентов реагентов и температура могут быть изменены для каждой конкретной реакции и что может быть необходимо или желательно использовать другие методы обработки и очистки. В тех случах, когда реакции осуществляют с применением облучения микроволнами, используют микроволновой реактор Initiator 60, поставляемый Biotage. Прикладываемую эффективную мощность варьируют в ходе реакции для поддержания постоянной температуры.
Данные для соединений, полученных в следующих далее примерах, суммированы в приведенных ниже таблицах, где показаны значения аффинности в отношении LRRK2 (Ki, микромолярная концентрация) для репрезентативных соединений вместе со значениями, полученными по LCMS-методу (М), т.е. с временем удерживания (retention time; RT) при LC в минутах и значениями m/z (молекулярная масса) при масс-спектрометрии.
Промежуточное соединение 1: 2-хлор-N-метил-5-(трифторметил)-пиримидин-4-амин
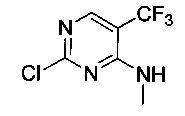
К охлажденному (-10°С) раствору 2,4-дихлор-5-трифторметилпиримидина (20 г; 0,089 моль) в метаноле (100 мл) добавляли триэтиламин (12,5 мл; 0,089 моль) и 2 М раствор метиламина в метаноле (45 мл). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь концентрировали и перерастворяли в этилацетате. Раствор промывали насыщ. NaHCO3, рассолом, сушили над MgSO4, фильтровали и концентрировали. Неочищенный продукт очищали колоночной хроматографией (5-25% EtOAc в гептане), получая 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амин (8,6 г; 45%). 1Н-ЯМР (DMSO): δ 8.37 (s, 1Н), 7.90 (s, 1Н), 2.90 (s, 3Н).
Дополнительные промежуточные соединения, полученные с использованием способов, аналогичных описанным выше, приведены в ТАБЛИЦЕ 1, ниже.
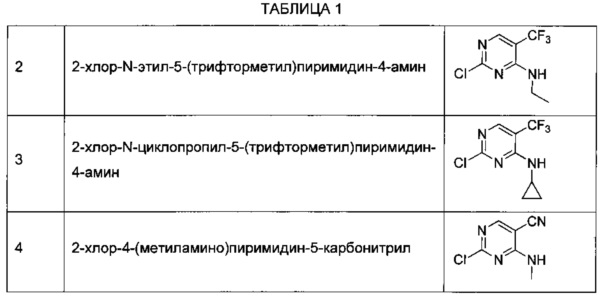
Промежуточное соединение 5: 6,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
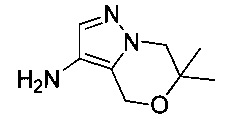
Стадия 1 - 1-(бензилокси)-2-метилпропан-2-ол
К раствору 2,2-диметилоксирана (15,0 мл; 168 ммоль) и фенилметанола (4,8 мл) в толуоле (40 мл) добавляли 50%-ный водн. NaOH (12 мл). Смесь перемешивали при 100°С в течение 30 ч. Добавляли воду и смесь экстрагировали этилацетатом. Органические слои объединяли, промывали рассолом, сушили над Na2SO4 и концентрировали. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (5/1), получая указанное в заголовке соединение (9,36 г; 99%) в виде желтого масла. 1Н ЯМР (500 МГц, CDCl3) δ 7.30-7.38 (m, 5Н), 4.58 (s, 2Н), 3.31 (s, 2Н), 2.05 (s, 1Н), 1.23 (s, 6Н).
Стадия 2 - ((2-метил-2-(проп-2-инилокси)пропокси)метил)бензол
К смеси NaH (5,0 г) в THF (50 мл) при 0°С по каплям добавляли 1-(бензилокси)-2-метилпропан-2-ол (9,36 г; 51,9 ммоль). После перемешивания при комнатной температуре в течение 0,5 ч медленно добавляли 3-бромпроп-1-ин (12,4 г; 104 ммоль) при 0°С. Затем смесь перемешивали при температуре дефлегмации в течение ночи. Реакцию гасили добавлением насыщ. NH4Cl. Полученную смесь экстрагировали этилацетатом (30 мл × 3). Органический слой объединяли, сушили над Na2SO4 и концентрировали. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (20/1), получая указанное в заголовке соединение (9,72 г; 86%) в виде бледно-желтого масла. 1Н ЯМР (500 МГц, CDCl3) δ 7.34-7.35 (m, 5Н), 4.56 (s, 2Н), 4.18 (d, J=2,0 Гц, 2Н), 3.38 (s, 2Н), 2.34 (t, J=2,0 Гц, 1Н), 1.25 (s, 6Н).
Стадия 3 - 3-((1-(бензилокси)-2-метилпропан-2-илокси)метил)-1Н-пиразол
Смесь ((2-метил-2-(проп-2-инилокси)пропокси)метил)бензола (1,00 г; 4,58 ммоль) и (диазометил)триметилсилана (2,29 мл) перемешивали при 135°С с использованием облучения микроволнами в течение 1 ч. После удаления растворителя получали указанное в заголовке соединение (1,19 г; 80%). LC-MS (ESI (electrospray ionization - электрораспылительная ионизация)): m/z=261,2 (М+Н)+.
Стадия 4 - 2-((1Н-пиразол-3-ил)метокси)-2-метилпропан-1-ол
Смесь 3-((1-(бензилокси)-2-метилпропан-2-илокси)метил)-1Н-пиразола (5,5 г; 21 ммоль) и 10%-ного Pd(OH)2/C (2,2 г) в EtOH (100 мл) перемешивали при 100°С в атмосфере H2 (4 ат; 392,3 кПа) в течение 12 ч. Нерастворенное вещество отфильтровывали и фильтрат концентрировали, получая указанное в заголовке соединение (3,0 г; 83%). LC-MS (ESI): m/z=171,1 (М+Н)+.
Стадия 5 - 2-((4-бром-1Н-пиразол-3-ил)метокси)-2-метилпропан-1-ол
К раствору 2-((1Н-пиразол-3-ил)метокси)-2-метилпропан-1-ола (3,00 г; 17,6 ммоль) в ацетонитриле (30 мл) добавляли NBS (3,45 г; 19,4 ммоль) в виде одной порции. После перемешивания в течение ночи смесь концентрировали. Остаток очищали обращенно-фазовой комби-флэш-хроматографией, получая указанное в заголовке соединение (1,8 г; 41%). LC-MS (ESI): m/z=249,1 (М+Н)+.
Стадия 6 - 2-метил-2-((4-нитро-1Н-пиразол-5-ил)метокси)пропилнитрат
В охлажденную (0°С) колбу с 2-((4-бром-1Н-пиразол-3-ил)метокси)-2-метилпропан-1-олом (300 мг; 1,2 ммоль) добавляли дымящую азотную кислоту (3,0 мл). После перемешивания в течение 1 ч при 0°С реакцию гасили, используя лед. Смесь экстрагировали этилацетатом (25 мл × 3). Органические слои промывали водой и рассолом, сушили над сульфатом натрия и концентрировали в вакууме, получая указанное в заголовке соединение (260 мг; 52%, чистота 69%). LC-MS (ESI): m/z=261,2 (М+Н)+.
Стадия 7 - 6,6-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин
К охлажденному (0°С) раствору 2-метил-2-((4-нитро-1Н-пиразол-5-ил)метокси)-пропилнитрата (580 мг; 1,12 ммоль) в DMF (15 мл) добавляли NaH (89,0 мг; 2,23 ммоль). Смесь перемешивали в течение ночи. Эту реакцию гасили, используя лед, и смесь экстрагировали этилацетатом (30 мл × 3). Органические слои промывали водой и рассолом, сушили над Na2SO4 и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (от 20/1 до 5/1), получая указанное в заголовке соединение (43,5 мг; 20%). LC-MS (ESI): m/z=198,3 (М+Н)+.
Стадия 8 - 6,6-диметил-6.7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
К охлажденному (0°С) раствору 6,6-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазина (35,0 мг; 0,177 ммоль) в THF/MeOH (3 мл/3 мл) добавляли Ni Ренея (100 мг) и гидразина гидрат (1 мл). После перемешивания в течение 16 ч нерастворенное вещество отфильтровывали. Фильтрат концентрировали в вакууме, получая указанное в заголовке соединение (26 мг; 89%). LC-MS (ESI): m/z=168,1 (М+Н)+.
Промежуточное соединение 6: 4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-амин
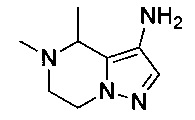
Стадия 1 - 4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол
К раствору 4-нитро-1 Н-пиразола (5650 мг; 50,00 ммоль) и PTSA (п-толуолсульфоновая кислота) (860 мг; 5,00 ммоль) в DCM (50 мл) при 0°С по каплям добавляли раствор DHP (дигидропиран) (5040 мг; 60,00 ммоль) в DCM (10 мл). После перемешивания при комнатной температуре в течение 20 ч смесь концентрировали. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (5/1), получая указанное в заголовке соединение (8,5 г; 86%). LC-MS (ESI): m/z=198 (М+Н)+.
Стадия 2 - 5-хлор-4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол
К раствору 4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1 Н-пиразола (7880 мг; 40,00 ммоль) в THF (100 мл) при -70°С добавляли LHMDS (гексаметилдисилазид лития) (1 н. в THF; 44 мл) в атмосфере N2 в течение 40 мин. После перемешивания при -30°С в течение 30 мин смесь снова охлаждали до -70°С. При этой температуре добавляли раствор C2Cl6 (10,5 г; 44,0 ммоль) в THF (60 мл). Смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 2 ч. Реакцию гасили H2O (2 мл). После концентрирования остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (8/1), получая указанное в заголовке соединение (7,5 г; 81%) в виде желтого твердого вещества. LC-MS (ESI): m/z=232 (М+Н)+.
Стадия 3 - 5-(1-этоксивинил)-4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол
Смесь 5-хлор-4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1 Н-пиразола (6,93 г; 30,0 ммоль), трибутил-(1-этоксивинил)станнана (11,9 г; 33,0 ммоль) и Pd(PPh3)4 (1,74 г; 1,50 ммоль) в диоксане (100 мл) кипятили с обратным холодильником в атмосфере N2 в течение 20 ч. После охлаждения добавляли KF (1,0 г). Нерастворенное вещество отфильтровывали и фильтрат концентрировали. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (10/1), получая указанное в заголовке соединение (6,5 г; 80%) в виде белого твердого вещества. LC-MS (ESI): m/z=268 (М+Н)+.
Стадия 4 - 1-(4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)этанон
К раствору 5-(1-этоксивинил)-4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразола (2,67 г; 10,0 ммоль) в метаноле (20 мл) добавляли смесь 2 н. HCl/метанол (10 мл). Смесь перемешивали в течение 10 ч. После концентрирования остаток очищали колоночной хроматографией на силикагеле с элюированием смесью петролейный эфир/этилацетат (5/1), получая указанное в заголовке соединение (1,5 г; 63%) в виде масла. LC-MS (ESI): m/z=240 (М+Н)+.
Стадия 5 - 2-(метил(1-(4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)этил)амино)этанол
Смесь 1-(4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)этанона (1,2 г; 5,0 ммоль), 2-(метиламино)этанола (450 мг; 6,00 ммоль), NaBH3CN (630 мг; 10,0 ммоль) и ZnCl2 (68 мг; 0,50 ммоль) в метаноле (20 мл) кипятили с обратным холодильником в течение 2 ч. После охлаждения смесь концентрировали. Остаток очищали обращенно-фазовой комби-флэш-хроматографией, получая указанное в заголовке соединение (820 мг; 88%) в виде желтого твердого вещества. LC-MS (ESI): m/z=299 (М+Н)+.
Стадия 6 - 2-(метил(1-(4-нитро-1Н-пиразол-5-ил)этил)амино)этанол
Раствор 2-(метил(1-(4-нитро-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)этил)амино)этанола (750 мг; 2,50 ммоль) и SOBr2 (1,04 г; 5,00 ммоль) в толуоле (10 мл) перемешивали при комнатной температуре в течение 2 ч. После концентрирования остаток очищали обращенно-фазовой комби-флэш-хроматографией, получая указанное в заголовке соединение (460 мг; 85%) в виде белого твердого вещества. LC-MS (ESI): m/z=215 (М+Н)+.
Стадия 7 - 4,5-диметил-3-нитро-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин
К раствору 2-(метил(1-(4-нитро-1Н-пиразол-5-ил)этил)амино)этанола (430 мг; 2,00 ммоль) и PPh3 (786 мг; 3,00 ммоль) в THF (10 мл) при 0°С добавляли DIAD (606 мг; 3,00 ммоль). После перемешивания при 50°С в течение 2 ч смесь концентрировали. Остаток очищали обращенно-фазовой комби-флэш-хроматографией, получая указанное в заголовке соединение (260 мг; 66%) в виде белого твердого вещества. LC-MS (ESI): m/z=197 (М+Н)+.
Стадия 8 - 4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-амин
К раствору 4,5-диметил-3-нитро-4,5,6,7-тетрагидропиразоло[1,5-а]пиразина (260 мг; 1,30 ммоль) в метаноле (5 мл) добавляли Ni Ренея (50 мг) и гидразина гидрат (2 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. Нерастворенное вещество отфильтровывали и фильтрат концентрировали, получая указанное в заголовке соединение (200 мг; 91%) в виде белого твердого вещества. LC-MS (ESI): m/z=167 (M+H)+.
Промежуточное соединение 7: (6R)-4,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
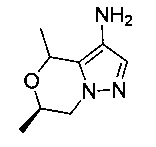
Стадия 1 - (((2R)-2-(бут-3-ин-2-илокси)пропокси)метил)бензол
К суспензии гидрида натрия (60 масс. %-ная дисперсия в минеральном масле; 1380 мг; 34,6 ммоль) в тетрагидрофуране (100 мл), охлажденной до 0°С, по каплям добавляли (2R)-1-бензилоксипропан-2-ол (5,00 г; 30,1 ммоль). Раствор перемешивали при 0°С в течение 1 ч, затем по каплям добавляли 1-метилпроп-2-инилметансульфонат (4780 мг; 32,3 ммоль) и реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь гасили, добавляя насыщ. водн. раствор хлорида аммония, и экстрагировали EtOAc. Объединенные органические экстракты промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный остаток адсорбировали на диоксиде кремния и очищали колоночной хроматографией (0-20% EtOAc в гептане), получая указанное в заголовке соединение в виде желтого масла (2,36 г; 36%; смесь диастереомеров).
Стадия 2 - 5-(1-(((R)-1-(бензилокси)пропан-2-ил)окси)этил)-1Н-пиразол
Во флакон для микроволнового реактора, содержащий [(2R)-2-(1-метилпроп-2-инокси)пропокси]метилбензол (1000 мг; 4,58 ммоль), добавляли (триметилсилил)диазометан (2,0 моль/л в гексанах; 2,9 мл; 5,73 ммоль). Флакон закрывали и нагревали до 135°С в микроволновом реакторе в течение 40 мин. Реакционную смесь концентрировали в вакууме, адсорбировали на диоксиде кремния и очищали колоночной флэш-хроматографией (0-100% EtOAc в гептане), получая указанное в заголовке соединение в виде желтого масла (1,04 г; 87%; смесь диастереомеров). LC-MS (ESI): m/z=261,2 (М+Н)+.
Стадия 3 - (2R)-2-(1-(1Н-пиразол-5-ил)этокси)пропан-1-ол
В круглодонную колбу, оборудованную обратным холодильником, содержащую 5-[1-[(1R)-2-бензилокси-1-метил-этокси]этил]-1Н-пиразол (1040 мг; 4,00 ммоль), добавляли этанол (35 мл), затем гидроксид палладия на угле (20 масс. %-ный; 281 мг; 0,40 ммоль). Сначала через раствор барботировали азот, затем барботировали водород, каждый в течение 5 мин. После этого раствор нагревали до температуры дефлегмации (80°С) в течение ночи. Реакционную смесь охлаждали до комнатной температуры и фильтровали через целит, элюируя дихлорметаном. Фильтрат концентрировали в вакууме, получая указанное в заголовке соединение (674 мг; 99%; смесь диастереомеров). LC-MS (ESI): m/z=171,1 (М+Н)+.
Стадия 4 - (2R)-2-(1-(4-нитро-1Н-пиразол-5-ил)этокси)пропилнитрат
К раствору (2R)-2-[1-(1Н-пиразол-5-ил)этокси]пропан-1-ола (674 мг; 3,96 ммоль) в серной кислоте (15,0 мл; 276 ммоль), охлажденному до 0°С, по каплям добавляли дымящую азотную кислоту (15,0 мл). Реакционную смесь перемешивали при 0°С и оставляли медленно нагреваться до комнатной температуры в течение ночи. Гашение осуществляли, выливая в 100 мл ледяной воды, и медленно порциями добавляли твердый карбонат натрия (внимание: энергичная реакция!), пока вся кислота не была погашена. Реакционную смесь выливали в делительную воронку и экстрагировали EtOAc. Объединенные органические экстракты промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме, получая указанное в заголовке соединение в виде темно-оранжевого масла (952 мг; 92%; смесь диастереомеров).
Стадия 5 - (6R)-4,6-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин
К раствору [(2R)-2-[1-(4-нитро-1Н-пиразол-5-ил)этокси]пропил]нитрата (952 мг; 3,66 ммоль) в N,N-диметилформамиде (30 мл; 387 ммоль), охлажденному до 0°С, добавляли 60%-ный гидрид натрия в масле (176 мг; 4,39 ммоль). Реакционную смесь оставляли медленно нагреваться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь гасили, выливая в ледяную воду, и экстрагировали EtOAc. Объединенные органические экстракты промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток адсорбировали на диоксиде кремния и очищали колоночной хроматографией (0-100% EtOAc в гептане), получая указанное в заголовке соединение (408 мг; 57%; смесь диастереомеров). LC-MS (ESI): m/z=198,0 (М+Н)+.
Стадия 6 - (6R)-4,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
В круглодонную колбу добавляли (6R)-4,6-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин (408 мг; 2,07 ммоль). Колбу продували азотом и добавляли этанол (35 мл; 575 ммоль), затем 10%-ный палладий на угле (220 мг; 0,21 ммоль). Подсоединяли баллон с водородом и водород барботировали через реакционную смесь в течение 5 мин. Реакционную смесь перемешивали в течение ночи при комнатной температуре, затем разбавляли дихлорметаном, фильтровали через целит с элюированием дихлорметаном и концентрировали в вакууме, получая указанное в заголовке соединение (344 мг; 99%; смесь диастереомеров). LC-MS (ESI): m/z=168,1 (М+Н)+.
Промежуточное соединение 8: (6S)-4,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
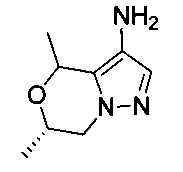
(6S)-4,6-Диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин получали способом, аналогичным получению (6R)-4,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амина, исходя из (2S)-1-бензилоксипропан-2-ола.
Промежуточное соединение 9: 5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-амин
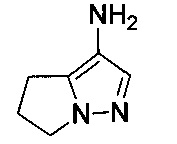
Стадия 1 - 5,6-дигидро-4Н-пирроло[1,2-с][1,2,3]оксадиазол-7-ий-3-олат
К раствору L-пролина (1000 мг; 8,69 ммоль) и нитрита натрия (845 мг; 12,2 ммоль) в воде (2,00 мл), охлажденному до 0°С, медленно добавляли концентрированную соляную кислоту (1,0 мл; 11,6 ммоль). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь разбавляли водой и экстрагировали МТВЕ, сушили над сульфатом натрия и концентрировали в вакууме. Затем неочищенный остаток переносили в толуол (4,00 мл) и охлаждали до 0°С. Далее добавляли трифторуксусный ангидрид (1,81 мл; 13,0 ммоль) и реакционную смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали в вакууме, адсорбировали на диоксиде кремния и очищали колоночной хроматографией (0-10% МеОН в DCM), получая указанное в заголовке соединение в виде коричневого масла (0,807 г; 74%) 1Н ЯМР (400 МГц, CDCl3) δ 4.43 (t, J=7,6 Гц, 2Н), 2.96-2.86 (m, 2Н), 2.85-2.73 (m, 2Н). LC-MS (ESI): m/z=127,0 (М+Н)+.
Стадия 2 - этил 5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-карбоксилат
Смесь 5,6-дигидро-4Н-пирроло[1,2-с]оксадиазол-7-ий-3-олата (355,4 мг; 2,82 ммоль) и этилпропиолата (0,87 мл; 8,46 ммоль) в ксилоле (10 мл) в круглодонной колбе, оборудованной холодильником, нагревали до 125°С в течение ночи. Реакционную смесь концентрировали в вакууме, адсорбировали на диоксиде кремния и очищали колоночной хроматографией (0-100% EtOAc в гептане), получая указанное в заголовке соединение в виде желтого масла (161 мг; 32%; более полярный региоизомер). 1Н ЯМР (400 МГц, CDCl3) δ 7.90 (s, 1Н), 4.27 (q, J=7,1 Гц, 2Н), 4.16 (t, J=7,3 Гц, 2Н), 3.09 (t, J=7,4 Гц, 2Н), 2.70-2.60 (m, 2Н), 1.33 (t, J=7,1 Гц, 3Н). LC-MS (ESI): m/z=181,1 (М+Н)+.
Стадия 3 - 5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-карбоновая кислота
Во флакон, содержащий этил-5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-карбоксилат (171 мг; 0,95 ммоль), добавляли воду (5 мл), затем гидроксид калия (266,20 мг; 4,74 ммоль). Флакон закрывали облицованной тефлоном крышкой и нагревали до 80°С в течение 3 ч. Продукт подкисляли концентрированной HCl и концентрировали в вакууме. Неочищенный остаток переносили в EtOAc и фильтровали. Фильтрат концентрировали в вакууме, получая указанное в заголовке соединение в виде белого твердого вещества (89 мг; 62%). 1Н ЯМР (400 МГц, CDCl3) δ 7.18 (s, 1Н), 4.05 (t, J=7,2 Гц, 2Н), 2.84-2.75 (m, 2Н), 2.70 (s, 2Н), 2.63-2.49 (m, 2Н). 1Н ЯМР (400 МГц, DMSO) δ 12.06 (s, 1Н), 7.75 (s, 1Н), 4.12-4.06 (m, 2Н), 3.00-2.92 (m, 2Н), 2.61-2.52 (m, 2Н). LC-MS (ESI): m/z=153,0 (М+Н)+.
Стадия 4 - бензил (5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-ил)карбамат
К раствору 5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-карбоновой кислоты (24,2 мг; 0,159 ммоль) в диоксане (2,0 мл) и бензиловом спирте (0,0333 мл; 0,318 ммоль) добавляли N,N-диизопропилэтиламин (0,0834 мл; 0,477 ммоль) и дифенилфосфорилазид (0,0354 мл; 0,159 ммоль). Затем смесь нагревали до 110°С в течение 2 часов. Реакционную смесь концентрировали в вакууме и очищали обращенно-фазовой HPLC, получая указанное в заголовке соединение вместе с неидентифицированным побочным продуктом. Это вещество использовали непосредственно на следующей стадии.
Стадия 5 - 5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-амин
К раствору бензил-N-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-ил)карбамата (42,8 мг; 0,166 ммоль) в этаноле (5 мл; 82,2 ммоль) добавляли палладий на активированном угле (10 масс. %; 17,7 мг; 0,0166 ммоль). Через эту смесь в течение 5 мин барботировали азот, затем в течение 5 мин через раствор барботировали водород. Реакционную смесь перемешивали в атмосфере водорода в течение 2 ч. Реакционную смесь фильтровали через целит, элюируя DCM, и концентрировали в вакууме. Остаток адсорбировали на диоксиде кремния и очищали колоночной флэш-хроматографией (0-10% МеОН в DCM), получая указанное в заголовке соединение (7,8 мг; 39% за две стадии). 1Н ЯМР (400 МГц, CDCl3) δ 7.18 (s, 1H), 4.05 (t, J=7,2 Гц, 2H), 2.84-2.75 (m, 2H), 2.70 (s, 2H), 2.63-2.49 (m, 2H).
Промежуточное соединение 10: 5-метил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-амин
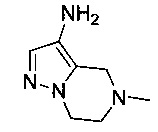
Стадия 1 - 2-(метил((4-нитро-1Н-пиразол-5-ил)метил)амино)этанол
К раствору (4-нитро-1Н-пиразол-5-ил)метанола (550 мг; 3,85 ммоль) и четырехбромистого углерода (1,40 г; 4,23 ммоль) в безводном DCM (30 мл) при 0°С по каплям в течение 20 мин добавляли раствор трифенилфосфина (1,12 г; 4,23 ммоль) в DCM (10 мл). После перемешивания смеси при 0°С в течение 1 ч добавляли N-метилэтаноламин (0,34 мл; 4,23 ммоль), затем DIPEA (0,85 мл; 4,81 ммоль). После перемешивания в холодной водяной бане (примерно 10°С) в течение 1 ч смесь концентрировали. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью DCM/10% MeOH/NH3 (от 100/0 до 0/100), получая указанный в заголовке продукт в виде янтарного масла (0,79 г; 100%). 1Н ЯМР (400 МГц, CDCl3) δ 8.14 (s, 1Н), 4.11 (s, 2Н), 3.80 (t, J=4,8 Гц, 2Н), 3.49 (s, 1Н), 2.70 (t, J=4,8 Гц, 2Н), 2.46 (s, 3Н). LC-MS (ESCI (electrospray and atmospheric pressure chemical ionization электрораспылительная ионизация с возможностью переключения на химическую ионизацию при атмосферном давлении)): m/z=201 (М+Н)+.
Стадия 2 - 5-метил-3-нитро-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин
К раствору 2-(метил((4-нитро-1Н-пиразол-5-ил)метил)амино)этанола (0,79 г; 3,95 ммоль) и трифенилфосфина (3,1 г; 11,85 ммоль) в безводном THF (25 мл) при 0°С по каплям в течение 5 мин добавляли диэтилазодикарбоксилат (1,86 мл; 11,85 ммоль). Смесь оставляли перемешиваться и нагреваться до комнатной температуры в течение 72 ч. Смесь разбавляли этилацетатом (50 мл) и водой (30 мл). Слои разделяли и водную фазу промывали этилацетатом (2×30 мл). Добавляли водный 2 М HCl и проводили разделение слоев. Водную фазу подщелачивали 2 М водным раствором гидроксида натрия и экстрагировали DCM. Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток очищали на SCX-картридже с элюированием метанолом, затем смесью 7 н. NH3/MeOH, получая указанное в заголовке соединение в виде беловатого твердого вещества (122 мг; 17%). 1Н ЯМР (400 МГц, CDCl3) δ 8.08 (s, 1Н), 4.24 (t, J=5,5 Гц, 2Н), 4.01 (s, 2Н), 2.94 (t, J=5,5 Гц, 2Н), 2.57 (s, 3Н). LC-MS: m/z=183 (М+Н)+.
Стадия 3 - 5-метил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-амин
К раствору 5-метил-3-нитро-4,5,6,7-тетрагидропиразоло[1,5-а]пиразина (122 мг; 0,67 ммоль) в этаноле (10 мл) добавляли палладий на угле (25 мг; 10 масс. %). Смесь продували азотом и встряхивали в атмосфере водорода (40 ф/кв. дюйм (275,8 кПа)) в течение 3 ч. Смесь фильтровали через картридж с целитом и фильтрат концентрировали, получая указанное в заголовке соединение в виде темно-зеленого смолообразного вещества (120 мг; колич.). 1Н ЯМР (400 МГц, CDCl3) δ 7.16 (s, 1Н), 4.13 (t, J=5,7 Гц, 2Н), 3.56 (s, 2Н), 3.48 (s, 2Н), 2.86 (t, J=5,7 Гц, 2Н), 2.52 (s, 3Н): LC-MS (ESCI): m/z=153 (M+H)+.
Промежуточное соединение 11: 1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразол
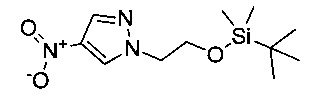
К смеси 4-нитропиразола (904 мг; 8 ммоль) и карбоната калия (3,3 г; 24 ммоль) в DMF (10 мл) добавляли (2-бромэтокси)(трет-бутил)диметилсилан (0,6 мл; 2,9 ммоль) и смесь нагревали до 50°С в течение 2 ч. Добавляли дополнительное количество (2-бромэтокси)(трет-бутил)диметилсилана (1,4 мл; 6,7 ммоль) и смесь нагревали до 50°С в течение 4 ч. Растворитель удаляли в вакууме и остаток распределяли между DCM (10 мл) и водой (10 мл). Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью изогексан/этилацетат (от 100/0 до 0/100), получая указанное в заголовке соединение (2,15 г; 99%) в виде белого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 8.20 (s, 1Н), 8.08 (s, 1Н), 4.24 (t, J=4,9 Гц, 2Н), 3.95 (t, J=4,9 Гц, 2Н), 0.84 (s, 9Н), -0.04 (s, 6Н). LC-MS (ESCI): m/z=272 (М+Н)+.
Промежуточное соединение 12: 6',7'-дигидроспиро[оксетан-3,4'-пиразоло[5,1-с][1,4]оксазин]-3'-амин

Стадия 1 - 3-(1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразол-5-ил)оксета н-3-ол
К раствору 1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразола (542 мг; 2 ммоль) в THF (2 мл) при -78°С по каплям в течение 10 мин добавляли бис(триметилсилил)амид лития (8 мл; 1 M в THF; 8 ммоль). Смесь оставляли перемешиваться при -78°С в течение 25 мин и затем оставляли медленно нагреваться до -45°С. Затем смесь повторно охлаждали до -78°С и по каплям добавляли оксетан-3-он (187 мг; 2,6 ммоль) в THF (2,5 мл). Смесь оставляли перемешиваться при -78°С в течение 1 ч и затем гасили, добавляя насыщенный водный раствор хлорида аммония (10 мл). Смесь оставляли нагреваться до комнатной температуры и затем добавляли DCM (20 мл). Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью изогексан/этилацетат (от 100/0 до 0/100), получая указанное в заголовке соединение (338 мг; 49%) в виде беловатого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 8.16 (s, 1Н), 5.18-5.15 (m, 2Н), 4.93-4.90 (m, 2Н), 4.35 (s, 1Н), 4.03 (s, 4Н), 0.83 (s, 9Н), 0.04 (s, 6Н). LC-MS (ESCI): m/z=344 (М+Н)+.
Стадия 2 - 3-(1-(2-гидроксиэтил)-4-нитро-1Н-пиразол-5-ил)оксетан-3-ол
К раствору 3-(1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразол-5-ил)оксетан-3-ола (338 мг; 0,98 ммоль) в THF (6 мл) добавляли фторид тетрабутиламмония (3 мл; 1 М в THF; 3 ммоль). Смесь оставляли перемешиваться при комнатной температуре в течение 3 ч. Добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и DCM (10 мл) и органическую фазу пропускали через гидрофобную фритту. Остаток очищали колоночной хроматографией на силикагеле, элюируя смесью изогексан/этилацетат/10%-ный МеОН в DCM (от 100/0/0 до 0/100/0, затем до 0/0/100), получая указанное в заголовке соединение (171 мг; 76%) в виде беловатого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 8.14 (s, 1Н), 5.14-5.11 (m, 2Н), 4.92-4.89 (m, 2Н), 4.11-4.03 (m, 4Н), 3.49 (s, 1Н). LC-MS (ESCI): m/z=230 (М+Н)+.
Стадия 3 - 3'-нитро-6',7'-дигидроспиро[оксетан-3,4'-пиразоло[5,1-с][1,4]оксазин]
К раствору 3-(1-(2-гидроксиэтил)-4-нитро-1Н-пиразол-5-ил)оксетан-3-ола (160 мг; 0,7 ммоль) в DCM (7 мл) добавляли DMAP (1 мг; 0,01 ммоль), затем раствор тозилхлорида (153 мг; 0,8 ммоль) в DCM (1 мл). Смесь охлаждали до 0°С и затем добавляли триэтиламин (0,44 мл; 3,5 ммоль). Смесь перемешивали при комнатной температуре в течение 3 ч и затем добавляли воду (10 мл). Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток растворяли в THF (5 мл) и добавляли гидрид натрия (28 мг; 60%-ный в масле; 0,7 ммоль). Смесь перемешивали при комнатной температуре в течение 8 ч. Добавляли воду (50 мл) и DCM (50 мл) и органическую фазу пропускали через гидрофобную фритту. Растворитель удаляли в вакууме и остаток очищали колоночной хроматографией на силикагеле с элюированием смесью изогексан/этилацетат (от 100/0 до 0/100), получая указанное в заголовке соединение (86 мг; 58%) в виде беловатого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 8.18 (s, 1Н), 5.31 (d, J=7,1 Гц, 2Н), 4.73 (d, J=7,1 Гц, 2Н), 4.25 (предпол. dd, J=5,5; 4,7 Гц, 2Н), 4.14 (предпол. dd, J=5,5; 4,7 Гц, 2Н). LC-MS (ESCI): m/z=212 (М+Н)+.
Стадия 4 - 6',7'-дигидроспиро[оксетан-3,4'-пиразоло[5,1-с][1,4]оксазин]-3'-амин
К раствору 3'-нитро-6',7'-дигидроспиро[оксетан-3,4'-пиразоло[5,1-с][1,4]оксазина] (86 мг; 0,41 ммоль) в смеси этанола (10 мл) и этилацетата (5 мл) добавляли палладий на угле (25 мг; 10 масс. %). Смесь продували азотом и встряхивали в атмосфере водорода (30 ф/кв. дюйм (207 кПа)) в течение 6 ч. Смесь фильтровали через целит и целит промывали этанолом. Растворитель удаляли в вакууме, получая указанное в заголовке соединение (73 мг; 98%) в виде желтого масла. 1Н ЯМР (400 МГц, CDCl3) δ 7.20 (s, 1Н), 4.98-4.91 (m, 4Н), 4.10-4.06 (m, 2Н), 4.01-3.97 (m, 2Н), 3.33 (br s, 2Н). LC-MS (ESCI): m/z=182 (М+Н)+.
Промежуточное соединение 13: 4,4-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
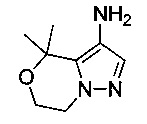
Стадия 1 - 2-(1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразол-5-ил)пропан-2-ол
К раствору 1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразола (1 г; 3,68 ммоль) в THF (4 мл) при -78°С по каплям в течение 10 мин добавляли бис(триметилсилил)амид лития (14,7 мл; 1 М в THF; 14,7 ммоль). Смесь оставляли перемешиваться при -78°С в течение 25 мин и затем оставляли медленно нагреваться до -45°С. Затем смесь повторно охлаждали до -78°С и по каплям добавляли ацетон (0,35 мл; 4,8 ммоль) в THF (5 мл). Смесь оставляли перемешиваться при -78°С в течение 1 ч и затем гасили, добавляя насыщенный водный раствор хлорида аммония (10 мл). Смесь оставляли нагреваться до комнатной температуры и затем добавляли DCM (20 мл). Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью изогексан/этилацетат (от 100/0 до 0/100) и затем еще раз с элюированием смесью изогексан/диэтиловый эфир (от 100/0 до 0/100), получая указанное в заголовке соединение (LC-MS (ESCI): m/z=330 (М+Н)+) в виде смеси с 1-(2-(трет-бутилдиметилсилилокси)этил)-4-нитро-1Н-пиразолом.
Стадия 2 - 2-(1-(2-гидроксиэтил)-4-нитро-1Н-пиразол-5-ил)пропан-2-ол
Смесь продуктов со стадии 1 растворяли в THF (20 мл) и добавляли фторид тетрабутиламмония (10 мл; 1 М в THF; 10 ммоль). Смесь оставляли перемешиваться при комнатной температуре в течение 3 ч. Добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и DCM (10 мл) и органическую фазу пропускали через гидрофобную фритту. Остаток очищали колоночной хроматографией на силикагеле с элюированием смесью DCM/10%-ный МеОН в DCM (от 100/0 до 0/100), получая указанное в заголовке соединение (MS (ESCI): m/z=216 (М+Н)+) в виде смеси с 2-(4-нитро-1Н-пиразол-1-ил)этанолом.
Стадия 3 - 4,4-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин
Смесь продуктов со стадии 2 растворяли в DCM (35 мл), добавляли DMAP (6 мг; 0,05 ммоль), затем раствор тозилхлорида (801 мг; 4,2 ммоль) в DCM (5 мл). Смесь охлаждали до 0°С и затем добавляли триэтиламин (2,6 мл; 18,4 ммоль). Смесь перемешивали при комнатной температуре в течение 3 ч и затем добавляли воду (50 мл). Органическую фазу пропускали через гидрофобную фритту и растворитель удаляли в вакууме. Остаток растворяли в THF (200 мл) и добавляли гидрид натрия (147 мг; 60%-ный в масле; 3,68 ммоль). Смесь перемешивали при комнатной температуре в течение 24 ч. Добавляли воду (200 мл) и DCM (200 мл) и органическую фазу пропускали через гидрофобную фритту. Растворитель удаляли в вакууме и остаток очищали колоночной хроматографией на силикагеле с элюированием смесью изогексан/этилацетат (от 100/0 до 0/100), получая указанное в заголовке соединение (52 мг; 7% за три стадии) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 8.13 (s, 1Н), 4.21-4.17 (m, 2Н), 4.13-4.09 (m, 2Н), 1.75 (s, 6Н). LC-MS (ESCI): m/z=198 (М+Н)+.
Стадия 4 - 4,4-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин
К раствору 4,4-диметил-3-нитро-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазина (52 мг; 0,26 ммоль) в смеси этанола (10 мл) и этилацетата (5 мл) добавляли палладий на угле (25 мг; 10 масс. %-ный). Смесь продували азотом и встряхивали в атмосфере водорода (30 ф/кв. дюйм (207 кПа)) в течение 18 ч. Смесь фильтровали через целит и целит промывали этанолом. Растворитель удаляли в вакууме, получая указанное в заголовке соединение (44 мг; колич.) в виде беловатого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 7.13 (s, 1Н), 4.06 (s, 4H), 2.62 (br s, 2H), 1.57 (s, 6H). LC-MS (ESCI): m/z=168 (M+H)+.
Промежуточное соединение 13: 6,7-дигидро-4H-пиразоло[5,1-с][1,4]оксазин-2-амин
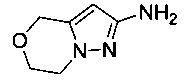
Указанное в заголовке соединение получали согласно методике, описанной в WO 2011/112995.
Промежуточное соединение 14: 5-метил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-2-амин
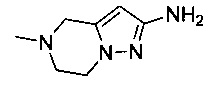
Указанное в заголовке соединение получали согласно методике, описанной в WO 2012/020008.
Промежуточное соединение 15: 1-метил-2,3-дигидро-1Н-имидазо[1,2-b]пиразол-7-амин
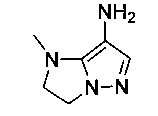
Стадия 1 - 7-нитро-2,3-дигидро-1Н-имидазо[1,2-b]пиразол
7-Нитро-2,3-дигидро-1Н-имидазо[1,2-b]пиразол получали согласно методике, описанной в WO 2004/039814.
Стадия 2 - 1-метил-7-нитро-2.3-дигидро-1H-имидазо[1,2-b]пиразол
К раствору 7-нитро-2,3-дигидро-1H-имидазо[1,2-b]пиразола (140 мг; 0,91 ммоль) в THF (10 мл) добавляли гидрид натрия (110 мг; 2,73 ммоль). Полученную смесь перемешивали в течение 30 мин и затем добавляли подметан (0,125 мл; 2 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 36 ч и затем гасили водой (10 мл). THF удаляли при пониженном давлении и остаток далее переносили в DCM и промывали водой. Водную фазу экстрагировали DCM (×3). Объединенные органические фракции сушили над сульфатом магния, фильтровали и концентрировали в вакууме, получая указанное в заголовке соединение (150 мг; 99%). 1Н ЯМР (400 МГц, CDCl3) δ 7.82 (s, 1Н), 4.19 (t, J=7,2 Гц, 2Н), 3,97 (t, J=7,2 Гц, 2Н), 3.34 (s, 3Н).
Стадия 3 - 1-метил-2.3-дигидро-1Н-имидазо[1,2-b]пиразол-7-амин
К раствору 1-метил-7-нитро-2,3-дигидро-1Н-имидазо[1,2-b]пиразола (150 мг; 0,89 ммоль) в этаноле (15 мл) добавляли палладий на угле (20 мг; 10 масс. %-ный). Смесь продували азотом и перемешивали в атмосфере водорода (1 ат (98,1 кПа)) в течение 18 ч. Реакционную смесь фильтровали через целит и целит промывали метанолом. Растворитель удаляли в вакууме, получая указанное в заголовке соединение (120 мг; 98%). 1Н ЯМР (400 МГц, CDCl3) δ 7.27 (s, 1Н), 4.05 (t, J=7,6 Гц, 2Н), 3.62 (t, J=7,6 Гц, 2Н), 2.91 (s, 3Н), 2.22 (brs, 2Н).
Пример 1: N2-(6,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин
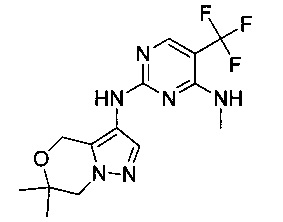
Во флакон для микроволнового реактора, оборудованного магнитной мешалкой, загружали 6,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-амин (13 мг; 0,078 ммоль), 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амин (20 мг; 0,095 ммоль) и трет-BuOH (0,5 мл). Смесь нагревали при 100°С с использованием облучения микроволнами в течение 15 мин. После концентрирования остаток очищали препаративной HPLC, получая указанное в заголовке соединение (9,5 мг; 36%). 1Н ЯМР (500 МГц, CDCl3) δ 8.09 (s, 1Н), 7.67 (s, 1Н), 6.79 (s, 1Н), 5.18 (s, 1Н), 4.83 (s, 2Н), 3.93 (s, 2Н), 3.00 (d, J=4,5 Гц, 3Н), 1.63 (s, 6Н). LC-MS (метод В): m/z=343,3 (М+Н)+; 4,77 мин, чистота 98,2%.
Пример 2: N4-метил-N2-(1-метил-2,3-дигидро-1Н-имидазо[1,2-b]пиразол-7-ил)-5-(трифторметил)пиримидин-2,4-диамин
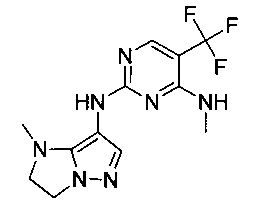
Смесь 1-метил-2,3-дигидро-1Н-пиразоло[1,5-а]имидазол-7-амина (91 мг; 0,66 ммоль), 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амина (90 мг; 0,44 ммоль), карбоната цезия (287 мг; 0,88 ммоль), ацетата палладия (2 мг; 0,009 ммоль) и BrettPhos (7 мг; 0,013 ммоль) в 1,4-диоксане (1,5 мл) продували, барботируя через смесь азот в течение 5 мин. Реакционную пробирку герметично закрывали и смесь нагревали до 100°С в течение 18 ч. Смесь охлаждали, разбавляли этилацетатом (5 мл) и промывали водой (2×5 мл). Водные промывки объединяли и экстрагировали EtOAc (5 мл). Органические экстракты объединяли и фильтровали через гидрофобную фритту. Растворитель удаляли в вакууме и остаток очищали препаративной HPLC, получая указанное в заголовке соединение (19 мг; 14%).1Н ЯМР (400 МГц, DMSO) δ 8.64† (br s, 1Н), 8.32* (br s, 1H), 8.05 (s, 1H), 7.30† (br s, 1H), 7.11* (br s, 1H), 6.91 (s, 1H), 4.06 (t, J=7,6 Гц, 2H), 3.65 (t, J=7,6 Гц, 2H), 2.86 (d, J=4,4 Гц, 3Н), 2.69 (s, 3Н). † и * относятся к разным ротомерам (определенным произвольно). LC-MS (метод С): m/z=314 (М+Н)+; 2,78 мин, чистота 98,7%.
Соединения, полученные с использованием указанных выше методик, показаны ниже в ТАБЛИЦЕ 2 вместе с приведенными для отдельных соединений данными по масс-спектрометрии низкого разрешения (М+Н), протонного ЯМР и Ki (микромолярная концентрация) в отношении LRRK2, определенными в описанном ниже анализе.
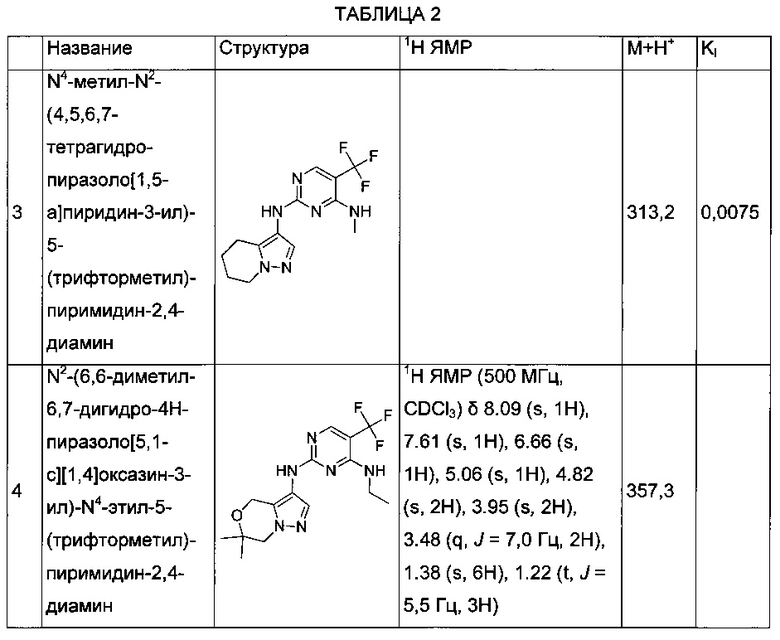
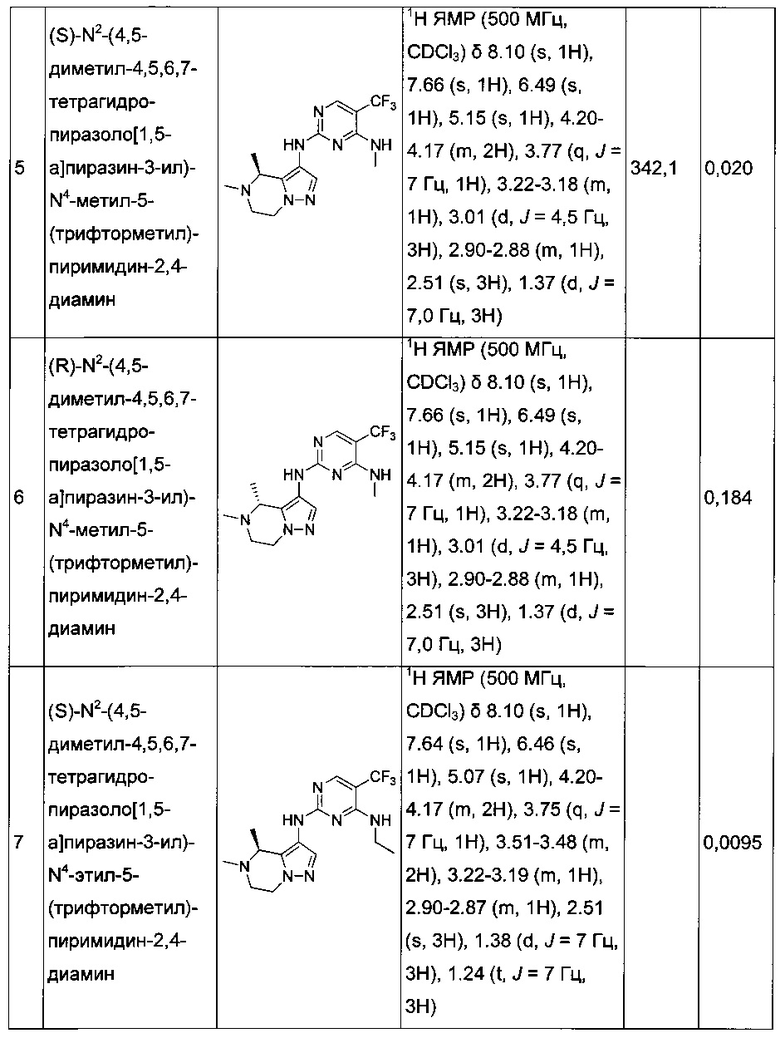
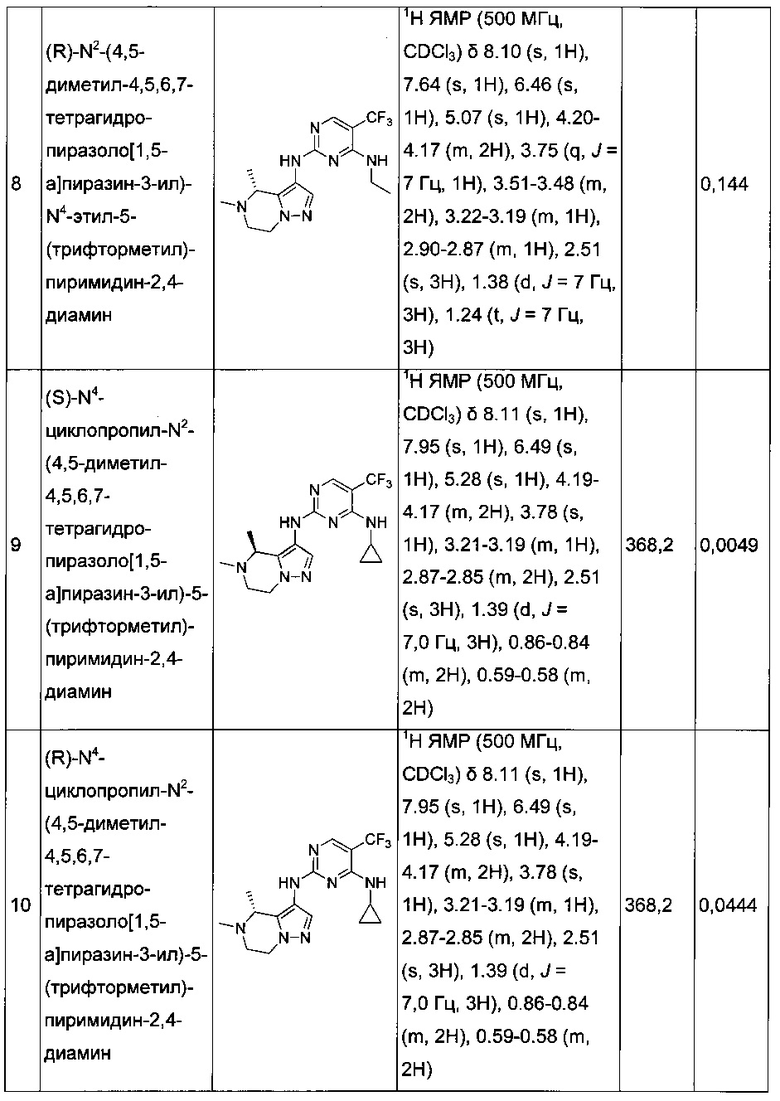
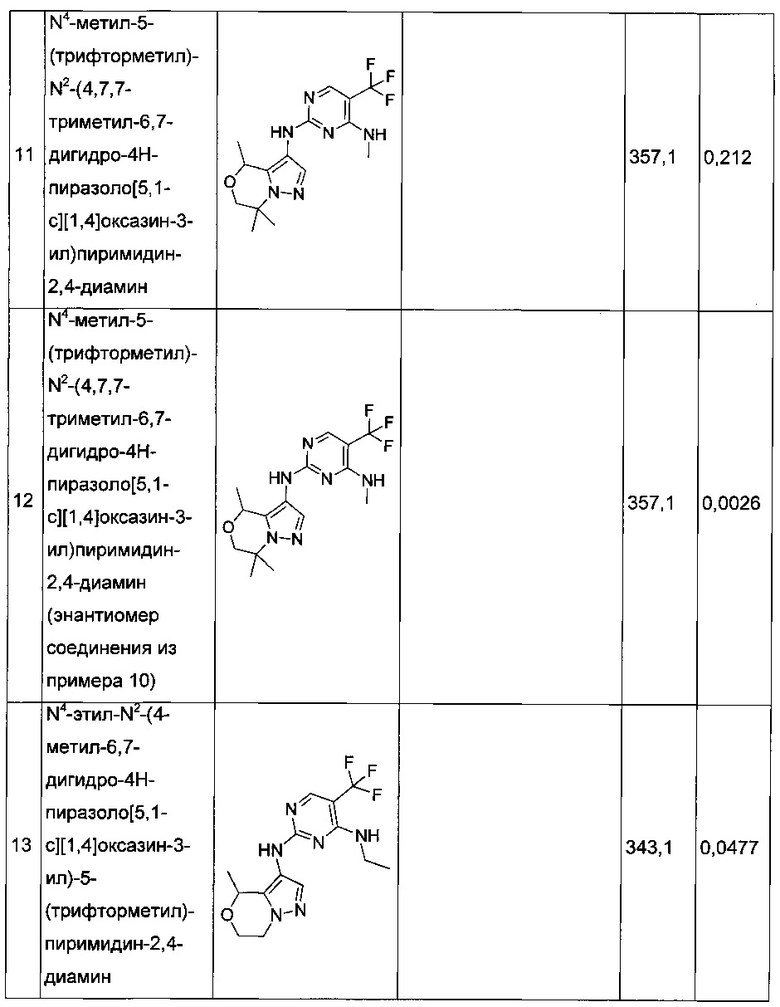
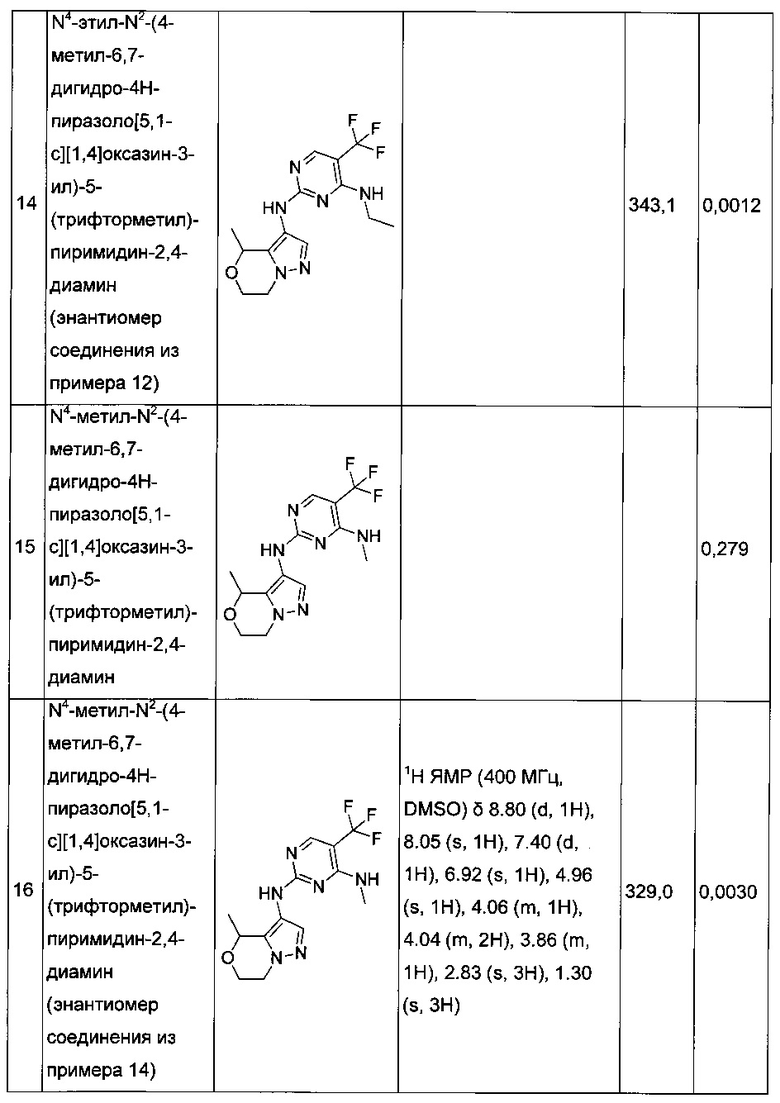
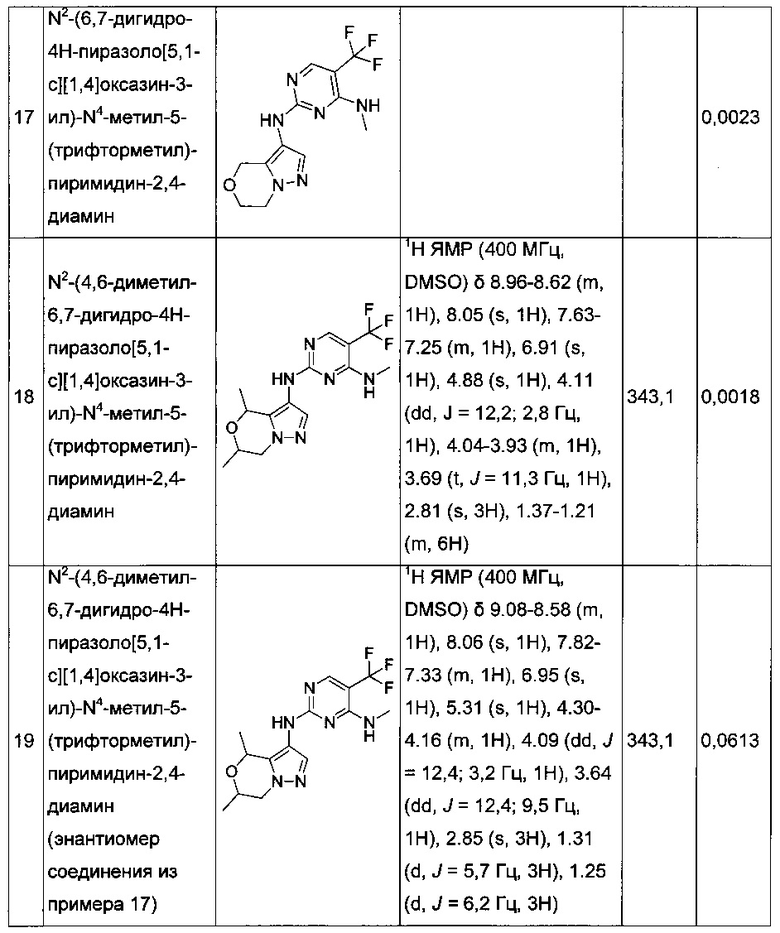
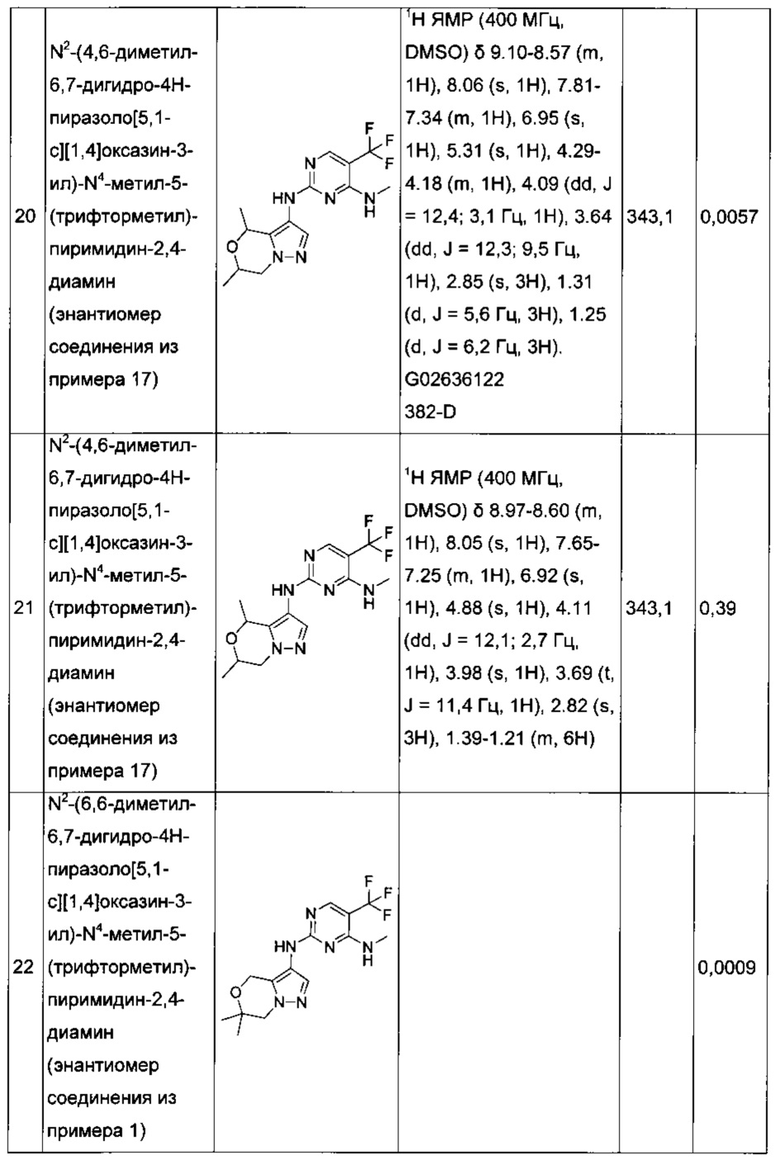
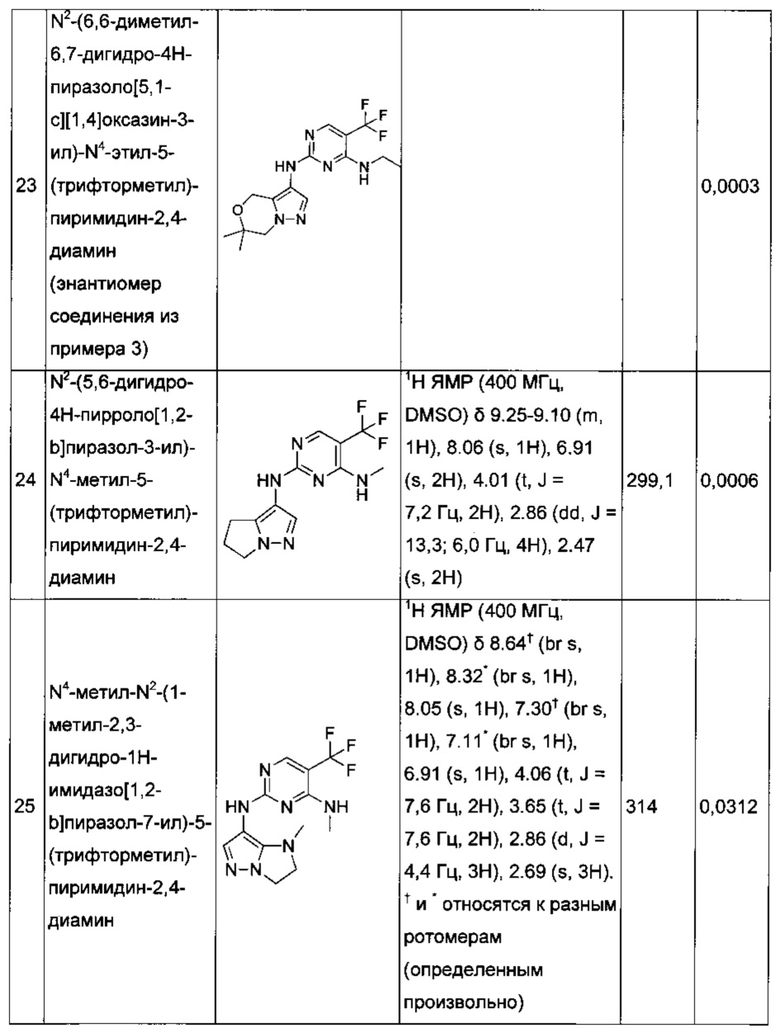
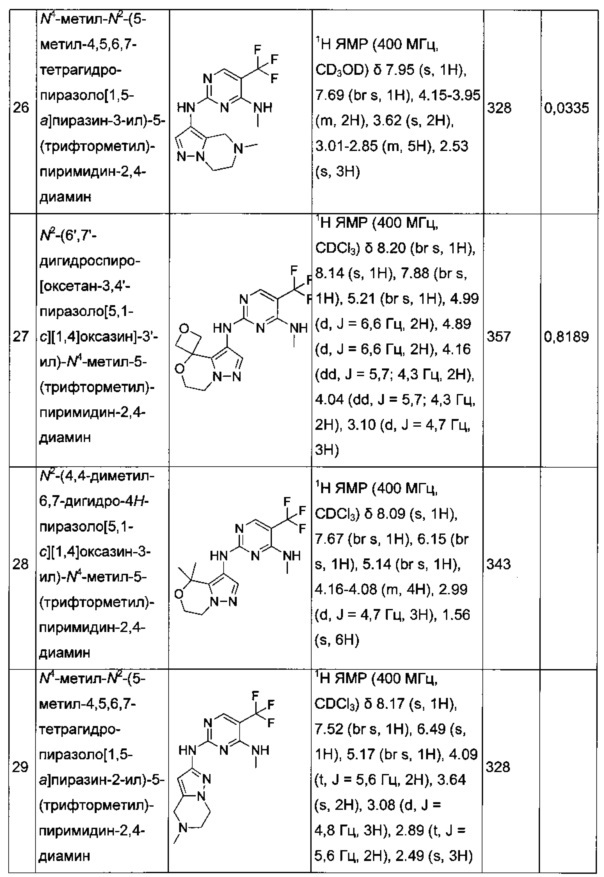
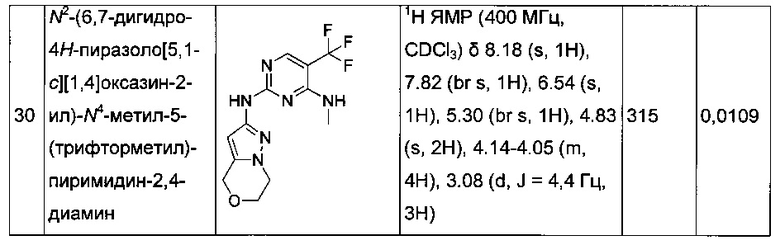
Пример 51. Связывание in vitro с LRRK2 в анализе LanthaScreen
Этот анализ использовали для оценки эффективности соединений в отношении ингибирования активности LRRK2 путем определения величин Kiкаж, IC50 или процента ингибирования. В 384-луночных черных планшетах ProxiPlates F с мелкими лунками совместно инкубировали LRRK2, Eu-антитело к GST (glutathione S-transferase - глутатион-S-трансфераза), конъюгированный с Alexa Fluor® индикатор киназной активности 236 и тестируемое соединение.
Детектирование связывания Alexa Fluor®-"индикатора" с киназой осуществляли, добавляя Eu-меченное антитело к GST. В результате связывания индикатора и антитела с киназой наблюдается высокая степень FRET (fluorescence resonance energy transfer - резонансный перенос энергии флуоресценции), в то время как замена индикатора на ингибитор киназы приводит к затуханию FRET.
При проведении анализа использовали приведенные ниже условия и материалы.


Подготовка планшета с соединениями
Выполнить серийные разведения тестируемых соединений (из 10 мМ концентрированных растворов) в соотношении 1:3,16 (20 мкл + 43,2 мкл) в 100%-ном DMSO для получения кривой по 12 точкам. Каждую концентрацию разбавить в соотношении 1:33,3 (3 мкл + 97 мкл) в реакционном буфере. Внести по 5 мкл в анализируемый планшет. Конечная максимальная тестируемая концентрация составляет 100 мкМ.
Подготовка общих и холостых проб
В лунки для общих и холостых проб (total and blank wells) добавляли по 5 мкл DMSO (3%) и в лунки для холостой пробы добавляли по 5 мкл Eu-меченного антитела к GST (6 нМ), все в реакционном буфере. В содержащие соединения и в "общие" лунки добавить по 5 мкл смеси LRRK2 (30 нМ)/Eu-меченное антитело к GST (6 нМ).
Процедура анализа
Во все лунки добавить по 5 мкл индикатора киназной активности (25,5 нМ). Инкубирование планшетов осуществить при комнатной температуре в течение 1 часа на планшетном шейкере (слабое встряхивание). Считать протокол анализа гомогенной флуоресценции с разрешением по времени (homogeneous time-resolved fluorescence; HTRF) на ридере EnVision от Perkin Elmer.
Обработка данных
Выполнить расчет соотношения: (665/620)⋅10000. Из данных для всех точек вычесть средние значения для фона (значения в лунках холостой пробы). Рассчитать % от контроля для каждой тестируемой величины. Построить график зависимости % от контроля от концентрации соединения. Рассчитать величину Ki (аппроксимация кривой с помощью уравнения Моррисона с использованием программы XLfit). Результаты выражены в виде Ki в мкМ. Уравнение для Ki:
Y=V0⋅(1-((x+Ki⋅(1+S/Km)+Et)/(2⋅Et)-(((x+Ki⋅(1+S/Km)+Et)^2-(4⋅Et⋅x)^0,5)/(2*Et))),
где Et составляет 4 нМ,
kd (индикатор) составляет 8,5 нМ,
концентрация индикатора (S) составляет 8,5 нМ.
Пример 32. Анализ LRRK2 in vitro
Этот анализ использовали для оценки эффективности соединений в отношении ингибирования активности LRRK2 путем определения величин Kiкаж, IC50 или процента ингибирования. В полипропиленовом планшете инкубировали совместно LRRK2, меченный флуоресцентной меткой пептидный субстрат, АТФ и тестируемое соединение. С использованием LabChip 3000 (Caliper Life Sciences) по окончании реакции проводили разделение субстрата капиллярным электрофорезом на две разновидности: фосфорилированный и нефосфорилированный субстрат. Относительные количества каждого из них количественно определяли по интенсивности флуоресценции. Значение Ki в отношении LRRK2 определяли согласно уравнению:
Y=V0⋅(1-((x+Ki⋅(1+S/Km)+Et)/(2⋅Et)-(((x+Ki⋅(1+S/Km)+Et)^2-(4⋅Et⋅x))^0,5)/(2⋅Et))).
Величины Ki в ТАБЛИЦЕ 2 и где-либо еще в данном описании приведены в мкМ.
При проведении анализа использовали приведенные ниже условия и материалы.


Подготовка планшета с соединениями
Для проведения серийных разведений в колонки 3-24 добавляли по 34,6 мкл DMSO. Для контролей в анализе в колонки 1 и 2 рядов А и Р добавляли по 37,5 мкл DMSO. В колонки 1 и 2, ряд В, добавляли a, d и по 50 мкл 25 мкМ G-028831 (стауроспорина). В отношении образцов: для инициирования реакции при 100 мкМ в колонки 1 и 2 добавляли по 37,5 мкл DMSO, затем по 12,5 мкл 10 мМ раствора соединения; для инициирования реакции при 10 мкМ в колонки 1 и 2 добавляли по 78 мкл DMSO, затем по 2 мкл 10 мМ раствора соединения; и для инициирования реакции при 1 мкМ в пустые колонки 1 и 2 добавляли 25 мкМ раствор соединения (2 мкл 10 мМ раствора соединения + 798 мкл DMSO). Для выполнения серийных разведений 1:3,16 ("PLK_BM_serial_halflog") использовали точный прибор.
Подготовка АТФ
Раствор АТФ разбавляли до 282,1 мкМ в полном буфере для киназной реакции (конечная концентрация составляла 130 мкМ).
Подготовка общих и холостых проб
Субстрат разбавляли в полном реакционном буфере до концентрации 4 мкМ. Объединяли равные объемы полного реакционного буфера и 4 мкМ раствора субстрата, получая холостую пробу. Объединяли равные объемы полного реакционного буфера и 4 мкМ раствор субстрата и к объединенному раствору добавляли LRRK2 в 2 × конечной концентрации.
Процедура анализа
В лунки полипропиленового планшета с объемом лунок 50 мкл, предназначенные для холостых проб, добавляли вручную буфер/субстрат из расчета 5 мкл/лунка. Для инициирования киназной реакции ("PLK SAR 23 АТР") использовали Biomek FX. В соответствующие лунки добавляли следующее:
2 мкл соединения + 23 мкл АТФ;
соединение/АТФ из расчета 5 мкл/лунка в анализируемый планшет;
киназу/субстрат из расчета 5 мкл/лунка в анализируемый планшет;
Планшет инкубировали в течение 2 часов в темноте. Для остановки киназной реакции ("PLK Stop") использовали Biomek FX и в анализируемый планшет добавляли стоп-раствор из расчета 10 мкл/лунка. Результаты прочитывали на LabChip 3000.
Протокол для LabChip 3000
Работу на LabChip 3000 проводили, используя программу "LRRK2 IC50" со следующими рабочими настройками:


Пример 33. Мышиная модель болезни Паркинсона
Болезнь Паркинсона можно воспроизвести у мышей и у приматов путем введения 1-метил-4-фенилтетрагидропиридина (МРТР), селективного нигростриального дофаминергического нейротоксина, который вызывает потерю маркера нервных окончаний - дофамина (DA) в стриатуме. Оценку соединений по изобретению на предмет эффективности в лечении болезни Паркинсона можно провести с использованием МРТР-индуцированной нейродегенерации, в целом следуя протоколу, описанному в Saporito et al., J. Pharmacology (1999) Vol. 288, pp. 421-427.
Кратко, МРТР растворяют в PBS (забуференный фосфатом физиологический раствор) в концентрациях 2-4 мг/мл и мышам (самцам С57 весом 20-25 г) делают подкожную инъекцию в дозе 20-40 мг/кг. Соединения по изобретению солюбилизируют, используя гидроксистеарат полиэтиленгликоля, и растворяют в PBS. Мышам вводят подкожной инъекцией раствор соединения в дозе 10 мл/кг за 4-6 ч до введения МРТР и затем один раз в сутки в течение 7 суток. В день последней инъекции мышей умерщвляют и средний мозг блокируют и далее фиксируют в параформальдегиде. Полосатые тела отсекают, взвешивают и хранят при -70°С.
Собранные таким образом полосатые тела оценивают на предмет содержания дофамина и его метаболитов дигидроксифенилуксусной кислоты и гомованилиновой кислоты посредством HPLC с использованием электрохимических методов детекции, как описано в Sonsalla et al., J. Pharmacol. Exp. Ther. (1987) Vol. 242, pp. 850-857. Оценку полосатых тел также можно осуществить, используя анализ тирозингидроксилазы из Okunu et al., Anal. Biochem. (1987) Vol. 129, pp. 405-411 путем измерения выделения 14CO2, ассоциированного с тирозингидроксилаза-опосредуемым превращением меченного тирозина в L-допу. Кроме того, оценку полосатых тел можно осуществить с использованием анализа моноаминоксидазы-В, который описан в White et al., Life Sci. (1984), Vol. 35, pp. 827-833, и путем мониторинга захвата дофамина, как описано в Saporito et al. (1992) Vol. 260, pp. 1400-1409.
Несмотря на то, что настоящее изобретение описано со ссылкой на конкретные его воплощения, специалистам в данной области техники следует понимать, что могут быть внесены различные изменения и могут быть сделаны замены на эквиваленты без отклонения от истинной сущности и объема изобретения. Помимо этого могут быть сделаны многочисленные модификации с целью адаптации конкретной ситуации, вещества, композиции объекта (изобретения), способа, стадии или стадий способа к объективной сущности и действительному объему настоящего изобретения. Подразумевается, что все модификации включены в объем формулы изобретения, прилагаемой к заявке.
Изобретение относится к соединениям формулы (I) или к их фармацевтически приемлемым солям, где X, R1, R2, R3 и А являются такими, как определено в формуле изобретения. Соединения формулы (I) являются модуляторами обогащенной лейциновыми повторами киназы 2 (LRRK2). Изобретение также относится к фармацевтической композиции, содержащей эти соединения, их применению для лечения заболеваний, ассоциированных с рецептором LRRK2, таких как болезнь Паркинсона, и к способу лечения болезни Паркинсона. 4 н. и 16 з.п. ф-лы, 2 табл., 53 пр.
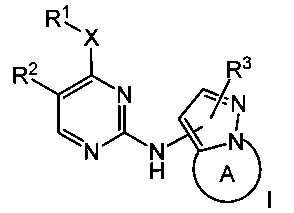
1. Соединение формулы I:
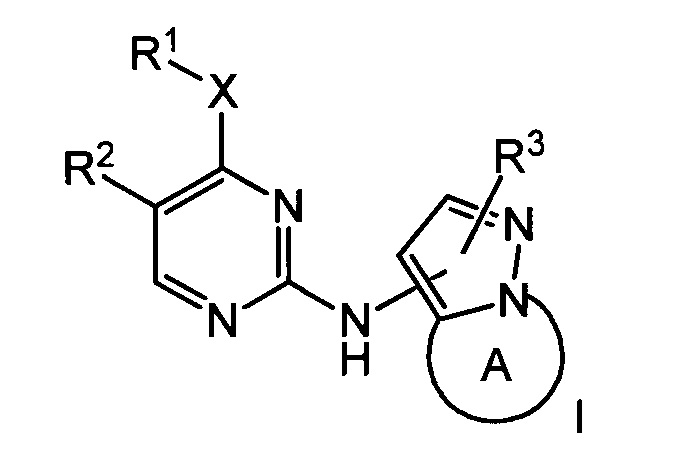
или его фармацевтически приемлемая соль,
где
X представляет собой: -NRa-, где Ra представляет собой водород или С1-6алкил;
R1 представляет собой: С1-6алкил или С3-6циклоалкил;
R2 представляет собой: атом галогена или галоген-С1-6алкил;
R3 представляет собой: водород или С1-6алкил;
А представляет собой пяти- или шестичленное ненасыщенное или насыщенное карбоциклическое кольцо, которое, возможно, может содержать гетероатом, выбранный из О, N и S, и которое может быть замещено один или более раз группой R6;
где каждый R6 независимо представляет собой: C1-6алкил; или R6 представляет собой оксетанил, спироконденсированный с кольцом А.
2. Соединение по п. 1, где X представляет собой -NH-.
3. Соединение по п. 1, где R1 представляет собой метил, этил или циклопропил.
4. Соединение по п. 1, где R2 представляет собой галоген-С1-6алкил.
5. Соединение по п. 1, где R3 представляет собой водород.
6. Соединение по п. 1, где кольцо А представляет собой пятичленное кольцо.
7. Соединение по п. 1, где кольцо А представляет собой шестичленное кольцо.
8. Соединение по п. 1, где кольцо А является насыщенным.
9. Соединение по п. 1, где кольцо А является карбоциклическим.
10. Соединение по п. 1, где кольцо А содержит гетероатом, выбранный из О, N и S.
11. Соединение по п. 1, где кольцо А замещено по меньшей мере один раз группой R6.
12. Соединение по п. 1, представляющее собой соединение формулы IIA или формулы IIB:
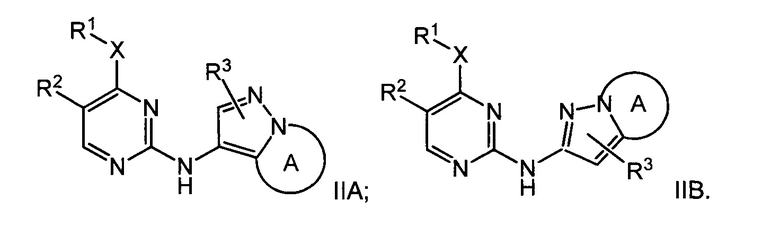
13. Соединение по п. 1, представляющее собой соединение формулы III:
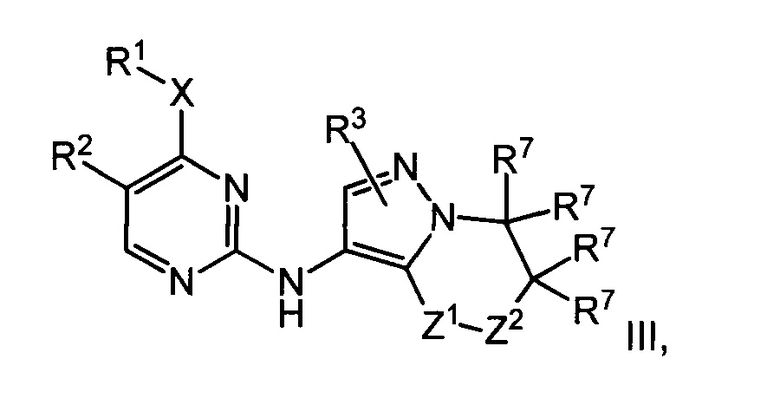
где
один из Z1 и Z2 представляет собой -О- или -NR7-, а другой представляет собой -C(R7)2-;
или оба Z1 и Z2 представляют собой -C(R7)2-;
где каждый R7 независимо представляет собой водород или С1-6алкил;
или две группы из групп R7 вместе с атомом или атомами, к которым они присоединены, могут образовывать спироконденсированный оксетанил; и
R1, R2 и R3 являются такими, как указано в п. 1.
14. Соединение по п. 13, где по меньшей мере один из R7 представляет собой С1-6алкил.
15. Соединение по п. 1, выбранное из:
N4-метил-N2-(4,5,6,7-тетрагидропиразоло[1,5-а]пиридин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N2-(6,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-этил-5-(трифторметил)пиримидин-2,4-диамина;
(S)-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
(R)-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
(S)-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-N4-этил-5-(трифторметил)пиримидин-2,4-диамина;
(R)-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-N4-этил-5-(трифторметил)пиримидин-2,4-диамина;
(S)-N4-циклопропил-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
(R)-N4-циклопропил-N2-(4,5-диметил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N4-метил-5-(трифторметил)-N2-(4,7,7-триметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)пиримидин-2,4-диамина;
N4-этил-N2-(4-метил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N4-метил-N2-(4-метил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N2-(6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N2-(4,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N2-(6,6-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N2-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N4-метил-N2-(1-метил-2,3-дигидро-1Н-имидазо[1,2-b]пиразол-7-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N4-метил-N2-(5-метил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-3-ил)-5-(трифторметил)пиримидин-2,4-диамина;
N2-(6',7'-дигидроспиро[оксетан-3,4'-пиразоло[5,1-с][1,4]оксазин]-3'-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N2-(4,4-диметил-6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-3-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина;
N4-метил-N2-(5-метил-4,5,6,7-тетрагидропиразоло[1,5-а]пиразин-2-ил)-5-(трифторметил)пиримидин-2,4-диамина и
N2-(6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазин-2-ил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамина
или фармацевтически приемлемой соли указанных соединений.
16. Фармацевтическая композиция, обладающая аффинностью к обогащенной лейциновыми повторами киназе 2 (LRRK2), содержащая:
(a) фармацевтически приемлемый носитель; и
(b) соединение или его фармацевтически приемлемую соль по любому из пп. 1-15.
17. Способ лечения болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп. 1-15.
18. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-15 для применения в качестве терапевтически активного вещества для ингибирования активности LRRK2.
19. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-15 для применения в качестве терапевтически активного вещества для терапевтического и/или профилактического лечения болезни Паркинсона.
20. Применение соединения или его фармацевтически приемлемой соли по любому из пп. 1-15 в терапевтическом и/или профилактическом лечении болезни Паркинсона.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| ЕА 200970670 А1, 26.02.2010. | |||
Авторы
Даты
2017-12-08—Публикация
2013-04-30—Подача