Данная заявка заявляет приоритет Европейской Патентной Заявки № ЕР 12163319.2, поданной 5 апреля 2012 года, и Международной Патентной заявки № РСТ/ЕР 2011/067604, поданной 7 октября 2011 года, раскрытие каждой из которых, таким образом, включено в полном объеме посредством ссылки.
Настоящее изобретение относится к способам и составам для терапевтического и диагностического применения в лечении заболеваний и расстройств, которые вызваны или связаны с нейрофибриллярными сплетениями. В частности, изобретение относится к антителам, которые специфично распознают и связываются с патологическими фосфорилированными конформерами белка тау, и к способам и составам, содержащим указанные антитела, для терапевтического и диагностического применения в лечении таупатий, в том числе, болезни Альцгеймера (БА).
Нейрофибриллярные сплетения и нейропильные нити (НН) представляют собой основные невропатологические признаки болезни Альцгеймера (БА). Они состоят из связанного с микротрубочками белка тау, который подвергается посттрансляционным модификациям, в том числе, фосфорилированию, дезамидированию и изомеризации, при аспарагинильных или аспартильных остатках. Они образуются в результате агрегации гиперфосфорилированного белка тау и его конформеров. Данная патология объединяет БА со многими нейродегенеративными таупатиями, в особенности, с некоторыми видами фронтотемпоральной деменции (ФТД).
Белок Тау представляет собой легко растворимый, «развернутый от природы» белок, который авидно связывается с микротрубочками (МТ), способствуя их сборке и стабильности. МТ очень важен для цитоскелетной целостности нейронов - и, таким образом, для надлежащего образования и функционирования нейронных цепей, т.е., для обучения и памяти. Связывание тау с МТ контролируется динамическим фосфорилированием и дефосфорилированием, что продемонстрировано, в основном, in vitro и в клетках, не относящихся к нейроналу. За счет большого количества возможных сайтов фосфорилирования (>80), точный вклад каждого из них и идентификация ответственных киназ in vivo остается в значительной степени неопределенным.
В мозге больного БА, патология тау развивается позже, и, вероятно, в ответ на амилоидную патологию, что составляет сущность гипотезы амилоидного каскада. Она основывается на исследованиях с участием больных БА и синдромом Дауна и подтверждается исследованиями на трансгенных мышах с комбинированной амилоидной и тау патологией (Lewis et al., 2001; Oddo et al., 2004; Ribe et al., 2005; Muyllaert et al, 2006; 2008; Terwel et al, 2008).
Точное протекание во времени обеих патологий у пациентов-людей с БА, а также механизмы, которые связывают амилоидную и тау патологии, остаются в значительной степени неясными, но предполагается, что они включают активацию нейронала, путей проведения сигнала, которые воздействуют на или посредством GSK3 и cdk5 как основных «тау-киназ» (см. обзор в Muyllaert et al, 2006, 2008).
Гипотеза о том, что таупатия не является невинным побочным эффектом, а является основным патологическим фактором при БА, основана на очевидных генетических, патологических и экспериментальных наблюдениях, которые полностью подтверждают друг друга:
- в семейных случаях раннего возникновения БА, которые являются результатом мутаций прекурсора амилоидного белка (ПАБ) или пресенилина, облигатной патогенной причиной является аккумуляция амилоида, но неизменно патология включает коллатеральную таупатию, идентичную наблюдаемой в спорадических случаях позднего возникновения БА;
- тяжесть когнитивной дисфункции и деменции коррелирует с таупатией, а не с амилоидной патологией, примером чего явилось несколько недавно проведенных клинических испытаний фазы 1&2, которые включали PIB-PET визуализацию амилоида и идентифицировали множество «ложноположительных» случаев - индивидуумов с нормальной когнитивной функцией и высоким содержанием амилоида в мозге;
- при семейной ФТД, таупатия провоцируется мутантным тау и вызывает нейродегенерацию непосредственно, без амилоидной патологии;
- на экспериментальной мышиной модели когнитивные дефекты, вызванные амилоидной патологией, практически полностью исчезают в отсутствие белка тау (Roberson et al, 2007).
Сочетанные аргументы поддерживают гипотезу о том, что белок тау играет ведущую роль в наследственной передаче когнитивной дисфункции при БА и сопутствующих нейродегенеративных таупатиях.
Новый многообещающий способ лечения БА состоит в пассивной иммунотерапии специфичными антителами (mAb) с целью удаления амилоидных пептидов и их агрегатов, для которых предполагается нейротоксичность или синаптотоксичность.
Предусматривается, что иммунотерапия, нацеленная на патологию тау, как раскрывается в данном описании, будет противодействовать патологическим конформерам белка тау, которые доказанно или постулированно вызывают синаптическую дисфункцию и нейродегенерацию.
Другие терапевтические подходы, нацеленные на белок тау, малочисленны и включают, главным образом:
- ингибиторы киназ, предположительно, увеличивающих фосфорилирование тау до патологических уровней;
- соединения, которые блокируют цитоплазматическую агрегацию гиперфосфорилированного белка тау.
Указанные подходы с точки зрения специфичности и эффективности содержат различные изъяны - проблема, которая объединяет их с попытками модифицировать метаболизм ПАБ и амилоида, и все это подчеркивает важность продолжения поиска дополнительных возможностей лечения, в том числе, иммунотерапии против тау. Действительно, нацеленная на амилоид иммунотерапия продемонстрировала дополнительное влияние на патологию тау на доклинической мышиной модели с сочетанной БА-подобной патологией, хотя агрегаты тау присутствовали (Oddo et al., 2004).
Некоторые сомнения касаются осуществимости иммунотерапевтического подхода к внутриклеточному белку тау. Им противостоят недавние экспериментальные исследования на модели таупатии у мышей (Asuni et al., 2007). Они продемонстрировали уменьшение патологических сплетений и функциональное улучшение в результате вакцинации полученным из белка тау фосфо-пептидом. Эти данные подтверждают предыдущие отчеты относительно иммунотерапии, нацеленной на α-синуклеин на моделях болезни Паркинсона (БП) и деменции с тельцами Леви (Masliah et al., 2005, 2011) и супероксиддисмутазу в модели амиотрофного латерального склероза (АЛС) (Urushitiani et al., 2007). Указаные заболевания представляют собой примеры, в которых внутриклеточные белки приводят к синаптическим дефектам и нейродегенерации по механизмам, пока до конца не ясным.
Существует неудовлетворенная потребность в пассивной и/или активной иммунотерапии, противодействующей патологическим конформерам белка, которые доказанно или предположительно вызывают нейродегенеративные расстройства, такие как амилоидная патология при БА, вызванная, например, внутринейрональными агрегатами гиперфосфорилированного белка тау, которые так же типичны для БА, как и амилоид.
Настоящее изобретение направлено на указанную неудовлетворенную потребность и раскрывает связывающиеся белки, которые распознают и связываются с основными патологическими фосфо-эпитопами белка тау. В частности, в настоящем изобретении раскрываются специфичные антитела против линейных и конформационных, простых и сложных фосфо-эпитопов на белке тау, конкретно на агрегированном белке тау, который считается ответственным за синапто- и нейро-токсичность при таупатиях, включая БА.
Соответственно, настоящее изобретение в одном из вариантов реализации относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно к моноклональному антителу или его функциональной части, причем связывающийся пептид или белок или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с фосфо-эпитопом на агрегированном белке Тау, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, конкретно в мозге, конкретно с константой диссоциации по меньшей мере 10 нМ, конкретно по меньшей мере 8 нМ, конкретно по меньшей мере 5 нМ, конкретно по меньшей мере 2 нМ, конкретно по меньшей мере 1 нМ, конкретно по меньшей мере 500 пМ, конкретно по меньшей мере 400 пМ, конкретно по меньшей мере 300 пМ, конкретно по меньшей мере 200 пМ, конкретно по меньшей мере 100 пМ, конкретно по меньшей мере 50 пМ.
В частности, константа диссоциации находится в интервале от 2 нМ до 80 нМ, конкретно от 2 нМ до 40 нМ, конкретно от 2 нМ до 10 нМ.
В определенном аспекте данного описания предложено антитело или его функциональный фрагмент, причем указанное антитело или фрагмент антитела связывается с фосфо-эпитопом, имеющим или содержащим последовательность аминокислот VYKSPVVSGDTSPRHL (SEQ ID NO: 62) (Tay aa 393-408 SEQ ID NO: 67, например, раскрытую в Табл. 1), содержащую фосфорилированный Ser в положениях 396 (pS396) и 404 (pS404).
Во втором варианте настоящее изобретение относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Tay млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, и при этом, указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, а также демонстрирует константу скорости ассоциации 104 М-1 с-1 или более, конкретно в интервале 3-5×104 М-1 с-1 или более, конкретно 10-5 М-1 с-1 или более; конкретно 2-9×105 М-1 с-1 или более; конкретно 106 М-1 c-1 или более, конкретно 1-4×106 М-1 с-1 или более, конкретно 107 М-1 с-1 или более.
В частности, константа скорости ассоциации находится в интервале от 1,6×103 до 5×105, конкретно в интервале от 2,4×104 до 5×105, в интервале от 3×103 до 5×105.
В третьем варианте реализации настоящее изобретение относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, а также обладает высокой аффинностью связывания, с константой диссоциации по меньшей мере 4 нМ и константой скорости ассоциации 105 М-1 с-1 или более, конкретно константой диссоциации по меньшей мере 3 нМ и константой скорости ассоциации 106 М-1 с-1 или более, конкретно константой диссоциации по меньшей мере 2 нМ и константой скорости ассоциации 104 М-1 с-1 или более, конкретно константой диссоциации по меньшей мере 1 нМ и константой скорости ассоциации 105 М-1 с-1 или более, конкретно константой диссоциации по меньшей мере 200 пМ и константой скорости ассоциации 105 М-1 с-1 или более, конкретно константой диссоциации по меньшей мере на 100 пМ и константой скорости ассоциации 10 М-1 с-1 или более.
В частности, константа диссоциации находится в интервале от 2 нМ до 80 нМ, и константа скорости ассоциации находится в интервале от 1,6×103 до 5×105, конкретно константа диссоциации находится в интервале от 2 нМ до 40 нМ, и константа скорости ассоциации находится в интервале от 2,4×104 до 5×105, конкретно константа диссоциации находится в интервале от 2 нМ до 10 нМ, и константа скорости ассоциации находится в интервале от 3×103 до 5×105.
Один из вариантов реализации (4) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, как представлено в SEQ ID NO: 67, выбранным из группы, состоящей из Тау аа 393-401, содержащего фосфорилированный Ser в положении 396 (pS396), Tay aa 396-401 содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 394-400 содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 402-406 содержащего фосфорилированный Ser в положении 404 (pS404) и Тау аа 393-400 содержащего фосфорилированный Ser в положении 396 (pS396).
Один из вариантов реализации (5) относится к связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем указанный пептид связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, и конкретно на белке Тау человека, показанном в SEQ ID NO: 67, который содержит Тау аа 393-401, содержащий фосфорилированный Ser в положении 396 (pS396).
Один из вариантов реализации (6) относится к связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем указанный пептид связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, и конкретно на белке Тау человека, показанном в SEQ ID NO: 67, который содержит Тау аа 396-401, содержащий фосфорилированный Ser в положении 396 (pS396).
Один из вариантов реализации (7) относится к связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем указанный пептид связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, и конкретно на белке Тау человека, показанном в SEQ ID NO: 67, который содержит Тау аа 394-400, содержащий фосфорилированный Ser в положении 396 (pS396).
Один из вариантов реализации (8) относится к связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем указанный пептид связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, и конкретно на белке Тау человека, показанном в SEQ ID NO: 67, который содержит Тау аа 402-406, содержащий фосфорилированный Ser в положении 404 (pS404).
Один из вариантов реализации (9) относится к связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем указанный пептид связывается с эпитопом на белке млекопитающего, конкретно на белке Тау человека, и конкретно на белке Тау человека, показанном в SEQ ID NO: 67, который содержит Тау аа 393-400, содержащий фосфорилированный Ser в положении 396 (pS396).
Один из вариантов реализации (10) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 73, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 74, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 75, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей, и/или второй домен связывания, который содержит последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 70, или последовательность аминокислот по меньшей мере на 95%, конкретно 98%, конкретно 99% идентичную ей, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 71, или последовательность аминокислот по меньшей мере на 94%, 95%, 96%, 97%, 98%, или 99% идентичную ей, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 72, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей.
В одном из аспектов данного описания раскрыто антитело или его функциональный фрагмент, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, и при этом, указанное антитело или его фрагмент содержит:
(а) первый домен связывания, содержащий CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 73, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 74, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 75; и/или
(б) второй домен связывания, который содержит последовательность аминокислот, содержащую CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 70, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 71, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 72.
Один из вариантов реализации (11) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 81, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 82, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 83, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей, и/или второй домен связывания, который содержит последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 78, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 79, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 80, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей.
В одном из аспектов данного описания раскрыто антитело или его функциональный фрагмент, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, притом, что указанное антитело или его фрагмент содержит:
(а) первый домен связывания, содержащий CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 81, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 82, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 83; и/или
(б) второй домен связывания, который содержит последовательность аминокислот, содержащую CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 78, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 79, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 80.
Один из вариантов реализации (12) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 93, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 94, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 95, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR, и/или второй домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 12, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 90, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 91, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%», конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR.
В определенном аспекте данного описания раскрыто антитело или его функциональная часть, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, и при этом, указанное антитело или его фрагмент содержит:
(а) первый домен связывания, содержащий CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 93, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 94, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 95; и/или
(б) второй домен связывания, который содержит последовательность аминокислот, содержащую CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 12, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 90, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 91.
Один из вариантов реализации (13) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 101, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 102, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 103, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR, и/или второй домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 98, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 99, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 100, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR.
В одном из аспектов данного описания раскрыто антитело или его функциональный фрагмент, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, и при этом, указанное антитело или его фрагмент содержит:
(а) первый домен связывания, содержащий CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 101, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 102, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 103; и/или
(б) второй домен связывания, который содержит последовательность аминокислот, содержащую CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 98, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 99, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 100.
Один из вариантов реализации (14) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 106, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 107, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 108, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR, и/или второй домен связывания, содержащий последовательность CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 89, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 115, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 91, или последовательность аминокислот по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную любому из упомянутых выше CDR.
В конкретном аспекте данного описания раскрыто антитело или его функциональный фрагмент, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, притом, что указанное антитело или его фрагмент содержит:
(а) первый домен связывания, содержащий CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 106, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 107, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 108; и/или
(б) второй домен связывания, который содержит последовательность аминокислот, содержащую CDR1, который содержит последовательность аминокислот, представленную в SEQ ID NO: 89, CDR2, который содержит последовательность аминокислот, представленную в SEQ ID NO: 115, и CDR3, который содержит последовательность аминокислот, представленную в SEQ ID NO: 91.
В конкретном варианте реализации первый домен связывания антитела или фрагмента антитела, раскрытого в данном описании, представляет собой вариабельный участок легкой цепи, и второй домен связывания антитела или фрагмента антитела, раскрытого в данном описании, представляет собой вариабельный участок тяжелой цепи.
В другом варианте реализации (15), настоящее изобретение относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 69, 77, 116/92, 118, 97, 105, или последовательность аминокислот, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей, и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 68, 76, 88, 96, 104, или последовательность аминокислот по меньшей мере на 80%, конкретно по меньшей мере на 85%, конкретно по меньшей мере на 86%, конкретно по меньшей мере на 87%, конкретно по меньшей мере на 88%, конкретно по меньшей мере на 89%, конкретно по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, конкретно по меньшей мере на 95%, конкретно по меньшей мере на 96%, конкретно по меньшей мере на 97%, конкретно по меньшей мере на 98%, конкретно по меньшей мере на 99% или 100% идентичную ей.
Один из вариантов реализации (16) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 69, или последовательность аминокислот по меньшей мере на 98% или 99% идентичную ей; и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 68, или последовательность аминокислот по меньшей мере на 90%, 91%, 92% или 93% идентичную ей.
Один из вариантов реализации (17) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 77, или последовательность аминокислот по меньшей мере на 93%, 94% или 95% идентичную ей; и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 76, или последовательность аминокислот по меньшей мере на 88%, 89% или 90% идентичную ей.
Один из вариантов реализации (18) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 116, 92 или 118, или последовательность аминокислот по меньшей мере на 93%, 94% или 95% идентичную ей; и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 88 или последовательность аминокислот по меньшей мере на 90%, 91%, 92% или 93% идентичную ей.
Один из вариантов реализации (19) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 97 или последовательность аминокислот по меньшей мере на 99% идентичную ей; и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 96, или последовательность аминокислот по меньшей мере на 86%, 87%, 88% или 90% идентичную ей.
Один из вариантов реализации (20) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 105, или последовательность аминокислот по меньшей мере на 98% или 99% идентичную ей; и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 104, или последовательность аминокислот по меньшей мере на 88%, 89% или 90% идентичную ей.
Один из вариантов реализации (21) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, притом, что указанный связывающийся пептид или антитело содержит первый домен связывания, последовательность аминокислот, представленную в SEQ ID NO: 69, или последовательность аминокислот по меньшей мере на 99% идентичную ей; и/или второй домен связывания, который содержит последовательность аминокислот, представленную в SEQ ID NO: 68, или последовательность аминокислот по меньшей мере на 93% идентичную ей.
Один из вариантов реализации (22) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, притом, что указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 77, или последовательность аминокислот по меньшей мере на 95% идентичную ей, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 76, или последовательность аминокислот по меньшей мере на 90% идентичную ей.
Один из вариантов реализации (23) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, притом, что указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 116, 92 или 118, или последовательность аминокислот по меньшей мере на 93-95% идентичную ей; и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 88, или последовательность аминокислот по меньшей мере на 93% идентичную ей.
Один из вариантов реализации (24) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, притом, что указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 97, или последовательность аминокислот по меньшей мере на 99% идентичную ей; и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 96, или последовательность аминокислот по меньшей мере на 90% идентичную ей.
Один из вариантов реализации (25) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, притом, что указанный связывающийся пептид или антитело содержит первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 105, или последовательность аминокислот по меньшей мере на 98% или 99% идентичную ей; и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 104, или последовательность аминокислот по меньшей мере на 90% идентичную ей.
Один из вариантов реализации (26) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, в соответствии с вариантом реализации (16), причем указанный первый домен связывания содержит CDR, как представлено в SEQ ID NO: 73-75, и указанный второй домен связывания содержит CDR, как представлено в SEQ ID NO: 70-72.
Один из вариантов реализации (27) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, в соответствии с вариантом реализации (17), причем указанный первый домен связывания содержит CDR, как представлено в SEQ ID NO: 81-83, и указанный второй домен связывания содержит CDR, как представлено в SEQ ID NO: 78-80.
Один из вариантов реализации (28) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, в соответствии с вариантом реализации (18), причем указанный первый домен связывания содержит CDR, как представлено в SEQ ID NO: 93-95, и указанный второй домен связывания содержит CDR, как представлено в SEQ ID NO: 12, 90-91.
Один из вариантов реализации (29) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, в соответствии с вариантом реализации (19), причем указанный первый домен связывания содержит CDR, как представлено в SEQ ID NO: 101-103, и указанный второй домен связывания содержит CDR, как представлено в SEQ ID NO: 98-100.
Один из вариантов реализации (30) настоящего изобретения относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, в соответствии с вариантом реализации (18), причем указанный первый домен связывания содержит CDR, как представлено в SEQ ID NO: 89, 115 и 91, и указанный второй домен связывания содержит CDR, как представлено в SEQ ID NO: 106-108.
Еще в одном варианте реализации (31) настоящее изобретение относится к связывающемуся пептиду или белку или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, конкретно связывающемуся пептиду или антителу в соответствии с любым из предыдущих вариантов реализации, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания с растворимым, олигомерным и нерастворимым фосфорилированным белком Тау и способен обнаруживать и/или модулировать уровни растворимого, олигомерного и нерастворимого фосфорилированного белка Тау in vivo, и при этом, указанный связывающийся пептид или антитело содержит:
а. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 69, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 68; или
б. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 77, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 76; или
в. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 116, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 88; или;
г. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 92, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 88; или
д. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 97, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 96; или
е. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 105, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 104.
ж. первый домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 118, и/или второй домен связывания, содержащий последовательность аминокислот, представленную в SEQ ID NO: 88
В одном из вариантов реализации (32) изобретения связывающийся пептид в соответствии с любым из предыдущих вариантов реализации представляет собой антитело, конкретно антитело изотипа IgG2a, IgG2b или IgG3, конкретно поликлональное антитело, моноклинальное антитело, химерное антитело, гуманизированное антитело или полностью человеческое антитело.
Один из вариантов реализации (33) изобретения относится к полинуклеотиду, кодирующему связывающийся пептид в соответствии с любым из предыдущих вариантов реализации.
В одном из вариантов реализации (34) указанный полинуклеотид содержит молекулу нуклеиновой кислоты, выбранную из группы, состоящей из
а. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, кодирующую полипептид, который содержит последовательность аминокислот, как представлено в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
б. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по меньшей мере на 85% идентичную последовательности, представленной в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
в. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по меньшей мере на 90% идентичную последовательности, представленной в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
г. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по меньшей мере на 95% идентичную последовательности, представленной в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
д. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по меньшей мере на 98% идентичную последовательности, представленной в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
е. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по меньшей мере на 99% идентичную последовательности, представленной в SEQ ID NO: 84-87, SEQ ID NO: 109-114, 117 и 119;
ж. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, комплементарная цепь которой гибридизуется с молекулой нуклеиновой кислоты в по любому из а)-е);
з. молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, отклоняющуюся от нуклеотидной последовательности, определенной в любом из а)-ж), вырождением генетического кода,
причем указанная молекула нуклеиновой кислоты, раскрытая в любом из а)-з), распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно на белке Тау человека, как представлено в SEQ ID NO: 67, выбранном из группы, состоящей из Тау аа 393-401, содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 396-401 содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 394-400 содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 402-406 содержащего фосфорилированный Ser в положении 404 (pS404), и Тау аа 393-400 содержащего фосфорилированный Ser в положении 396 (pS396), и при этом, в одном из вариантов реализации указанный связывающийся пептид обладает высокой аффинностью связывания, с константой диссоциации по меньшей мере 10 нМ, конкретно по меньшей мере 8 нМ, конкретно по меньшей мере 5 нМ, конкретно по меньшей мере 2 нМ, конкретно по меньшей мере 1 нМ, конкретно по меньшей мере 500 пМ, конкретно по меньшей мере 400 пМ, конкретно по меньшей мере 300 пМ, конкретно по меньшей мере 200 пМ, конкретно по меньшей мере 100 пМ, конкретно по меньшей мере 50 пМ и/или демонстрирует константу скорости ассоциации 104 М-1 с-1 или более, конкретно в интервале 3-5×104 М- с-1 или более, конкретно 105 М-1 с-1 или более; конкретно 6-9×105 М-1 с-1 или более; конкретно 106 М-1 с-1 или более, конкретно 1-4×106 М-1 с-1 или более, конкретно 107 М-1 с-1 или более, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами.
В различных вариантах реализации (35) изобретения раскрыт связывающийся пептид или его функциональная часть, конкретно антитело, конкретно моноклональное антитело или его функциональная часть, или полинуклеотид, в соответствии в любым из предыдущих вариантов реализации, или их комбинация, который способен специфично распознавать и связываться с фосфо-эпитопом на белке млекопитающего, конкретно на белке Тау человека, конкретно связанном с микротрубочкой белке тау, конкретно связанном с микротрубочкой агрегированном и гиперфосфорилированном белке тау, таком как присутствует в спаренных спиральных нитях (ССН), которые являются доминирующими структурами в нейрофибриллярных сплетениях, нейропильных нитях и при дистрофических невритах, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами.
В конкретном варианте реализации (36) изобретения человеческий белок тау представляет собой человеческий белок Тау, как представлено в SEQ ID NO: 67.
Связывающиеся пептиды и антитела в соответствии с любым из предыдущих вариантов реализации могут, таким образом, применяться (37) для снижения уровней общего растворимого белка тау, конкретно растворимого фосфорилированного белка тау, в мозге, конкретно в коре мозга и/или гиппокампе млекопитающего или человека, где присутствуют повышенные уровни растворимого белка тау и/или растворимого фосфорилированного белка тау.
Связывающиеся пептиды и антитела в соответствии с любым из предыдущих вариантов реализации могут также применяться (38) для снижения уровней спаренных спиральных нитей, содержащих гиперфосфорилированный белок тау (ССН pTau) в мозге, конкретно в коре мозга и/или гиппокампе, млекопитающего или человека, у которого присутствуют повышенные уровни указанных спаренных спиральных нитей pTau.
Снижение уровня общего растворимого белка тау и/или растворимого фосфорилированного белка тау и/или спаренных спиральных нитей pTau в мозге, конкретно в коре мозга и/или гиппокампе, млекопитающего или человека, у которого присутствует повышенные уровни указанных вариантов белка тау, способствующие связанным с белком тау заболеваниям, расстройствам или состояниям у указанного млекопитающего или человека, может приводить к улучшению и/или облегчению симптомов, ассоциирующихся с такими связанными с белком тау заболеваниями, расстройствами или состояниями (39).
Связывающиеся пептиды и антитела в соответствии с любым из предыдущих вариантов реализации, таким образом, могут применяться (40) в лечении, конкретно в лечении человека, для замедления или остановки прогрессирования связанного с белком тау заболевания, расстройства или состояния.
Связывающиеся пептиды и антитела в соответствии с любым из предыдущих вариантов реализации дополнительно могут применяться (41) в лечении, конкретно в лечении человека, для улучшения или облегчения симптомов, сопутствующих связанным с белком тау заболеваниями расстройствам или состояниям, например, таким как нарушение или утрата когнитивных функций, включая обоснование, принятие ситуативных решений, емкость памяти, обучение, специальную навигацию, и т.п.
В одном из вариантов реализации (42) изобретение относится к связывающимся пептидам и антителам, в соответствии с любым из предыдущих вариантов реализации, для применения в лечении, конкретно для применения в лечении таупатий, группы связанных с белком тау заболеваний и расстройств, или для облегчения симптомов, связанных с таупатиями.
В одном из вариантов реализации (43) изобретение относится к связывающимся пептидам и антителам, в соответствии с любым из предыдущих вариантов реализации, для сохранения или увеличения емкости когнитивной памяти у млекопитающего, страдающего таупатией.
В другом конкретном варианте реализации (44) изобретения, связывающиеся пептиды и антитела, содержащие по меньшей мере один или все CDR легкой цепи антител ACI-35-2А1-Ab1; ACI-35-2А1-Ab2; ACI-35-4А6-Ab2; ACI-35-4A6-Ab2; ACI-35-1D2-Ab1; ACI-35-2G5-Ab1; ACI-35-2G5-Ab2; ACI-35-2G5-Ab3; как представлено в SEQ ID NO: 73-75, 81-83, 93-95, 101-103, 106-108, и/или по меньшей мере один или все CDR тяжелой цепи антител ACI-35-2А1-Ab1; ACI-35-2А1-Ab2; ACI-35-4А6-Ab1; ACI-35-4А6-Ab2; ACI-35-1D2-Ab1; ACI-35-2G5-Ab1; ACI-35-2G5-Ab2; ACI-35-2G5-Ab3; как представлено в SEQ ID NO: 70-72, 78-80, (12, 90-91), 98-100, (89, 115, 91), применяются в лечении, конкретно в лечении человека, для улучшения или облегчения симптомов, сопутствующих связанным с белком тау заболеваниями расстройствам или состояниям, например, таким как нарушение или утрата когнитивных функций, включая обоснование, принятие ситуативных решений, память, обучение, специальную навигацию, и т.п.
В другом конкретном варианте реализации (45) изобретения, связывающиеся пептиды и антитела, содержащие по меньшей мере один или все CDR легкой цепи антител ACI-35-2G5-Ab2; ACI-35-2G5-Ab3, как представлено в SEQ ID NO: 106-108, и/или по меньшей мере один или все CDR тяжелой цепи антител ACI-35-2G5-Ab2; ACI-35-2G5-Ab3; как представлено в SEQ ID NO: 89, 115 и 91, применяются в лечении, конкретно в лечении человека, для улучшения или облегчения симптомов, сопутствующих связанным с белком тау заболеваниями расстройствам или состояниям, например, таким как нарушение или утрата когнитивных функций, включая обоснование, принятие ситуативных решений, память, обучение, специальную навигацию, и т.п.
Связывающиеся пептиды или антитела, в соответствии с предыдущими вариантами, против сплетений тау и pTau в мозге, могут быть определены с применением анализов иммунореактивности белка в выбранных отделах мозга и Вестерн-блоттингом гомогенатов мозга, соответственно, как описано в Примерах.
В другом варианте реализации (46) настоящего изобретения раскрывается фармацевтический состав, содержащий связывающийся пептид или его функциональную часть, конкретно антитело, конкретно моноклональное антитело или его функциональную часть, или полинуклеотид, в соответствии с любым из предыдущих вариантов реализации, или их комбинацию, в терапевтически эффективном количестве, вместе с фармацевтически приемлемым носителем.
В одном из вариантов реализации (47) связывающийся пептид или его функциональная часть, конкретно антитело, конкретно моноклональное антитело или его функциональная часть, или полинуклеотид, или фармацевтический состав, в соответствии с любым из предыдущих вариантов реализации, или их комбинация применяется в лечении, конкретно в лечении человека, с целью лечения или облегчения симптомов связанных с белком тау заболеваний или расстройств, включая нейродегенеративные расстройства, такие как таупатии.
Связывающиеся пептиды, антитела и/или фармацевтические составы в соответствии с любым из предыдущих вариантов реализации, таким образом, могут применяться (48) для замедления или остановки прогрессирования связанного с белком тау заболевания, расстройства или состояния, путем введения указанных связывающихся пептидов, антител и/или фармацевтических составов животному, конкретно млекопитающему, конкретно человеку, страдающему таким заболеванием или состоянием.
Связывающиеся пептиды, антитела и/или фармацевтические составы в соответствии с любым из предыдущих вариантов реализации дополнительно могут применяться (49) для улучшения или облегчения симптомов, сопутствующих связанным с белком тау заболеваниями расстройствам или состояниям, например, таких как нарушение или утрата когнитивных функций, включая обоснование, принятие ситуативных решений, емкость памяти, обучение, специальную навигацию, и т.п., путем введения указанных связывающихся пептидов, антител и/или фармацевтических составов животному, конкретно млекопитающему, конкретно человеку, страдающему таким заболеванием или состоянием.
В одном из вариантов реализации (50), связывающийся пептид или его функциональная часть, конкретно антитело, конкретно моноклональное антитело или его функциональная часть, или полинуклеотид или фармацевтический состав, в соответствии с любым из предыдущих вариантов реализации, или их комбинация, применяется в лечении заболеваний и расстройств, которые вызваны или связаны с образованием нейрофибриллярных повреждений, доминирующей патологии мозга при таупатии, включающих гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, при которых проявляются патологии и амилоидные патологии, в том числе, не ограничиваясь ими, болезнь Альцгеймера, болезнь Крейтцфельда - Якоба, деменция боксеров, синдром Дауна, болезнь Герстманна – Штреусслера - Шейнкера, миозит с тельцами включения и вызванная прионными белками амилоидная ангиопатия мозга, травматическое повреждение мозга, и дополнительные заболевания или расстройства, при которые не проявляется явная амилоидная патология, в том числе, не ограничиваясь ими, комплекс амиотрофный латеральный склероз/паркинсонизм-деменция Гуама, негуамские заболевания двигательных нейронов с нейрофибриллярными сплетениями, деменция с аргирофильными шарами, кортикобазальная дегенерация, диффузные нейрофибриллярные сплетения с кальцификацией, фронтотемпоральная деменция с паркинсонизмом, связанным с хромосомой 17, болезнь Галлервордена - Шпатца, множественная системная атрофия, болезнь Ниманна - Пика, тип С, паллидо-понто-нигральная дегенерация, синдром Пика, прогрессирующий подкорковый глиоз, прогрессирующий супрануклеарный паралич, подострый склерозирующий панэнцефалит, лимбическая деменция, постэнцефалитный паркинсонизм, миотоническая дистрофия.
В одном из вариантов реализации (51) связывающийся пептид или его функциональная часть, конкретно антитело, конкретно моноклональное антитело или его функциональная часть, или полинуклеотид или фармацевтический состав в соответствии с любым из предыдущих вариантов реализации, или их комбинация, применяется в лечении болезни Альцгеймера.
В одном из вариантов реализации (52) изобретения раскрыт способ обнаружения и/или модулирования уровней растворимого и/или олигомерного и/или нерастворимого фосфорилированного белка Тау, конкретно in vivo, конкретно в мозге, конкретно в коре мозга и/или гиппокампе животного, конкретно млекопитающего или человека, включающий введение указанному животному, конкретно указанному млекопитающему или человеку, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В одном из аспектов модуляция связана со снижением уровней растворимого белка тау, конкретно растворимого фосфорилированного белка тау, в мозге, конкретно в коре мозга и/или гиппокампе животного, конкретно млекопитающего или человека, у которого присутствуют повышенные уровни растворимого белка тау и/или растворимого фосфорилированного белка тау.
В одном из вариантов реализации (53) изобретения раскрыт способ снижения уровней нерастворимого белка тау, конкретно спаренных спиральных нитей, содержащих гиперфосфорилированный белок тау (ССН pTau), в мозге, конкретно в коре мозга и/или гиппокампе животного, конкретно млекопитающего или человека, у которого присутствуют повышенные уровни нерастворимого белка тау, конкретно спаренных спиральных нитей pTau (ССН pTau), включающий введение указанному животному, конкретно указанному млекопитающему или человеку, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В одном из вариантов реализации (54) настоящее изобретение относится к способу замедления или остановки прогрессирования связанного с белком тау заболевания, расстройства или состояния у животного, конкретно млекопитающего или человека, включающему введение указанному животному, конкретно указанному млекопитающему или человеку, страдающему таким заболеванием или состоянием, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В одном из вариантов реализации (55) настоящее изобретение относится к способу улучшения или облегчения симптомов, ассоциирующихся со связанными с белком тау заболеваниями, расстройствами или состояниями, например, таких как нарушение или утрата когнитивных функций, включая обоснование, принятие ситуативных решений, емкость памяти, обучение, специальную навигацию, и т.п., у животного, конкретно млекопитающего или человека, причем указанный способ включает введение указанному животному, конкретно указанному млекопитающему или человеку, страдающему таким заболеванием или состоянием, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В одном из вариантов реализации (56), настоящее изобретение относится к способу сохранения или увеличения емкости когнитивной памяти у млекопитающего, страдающего таупатией.
В другом варианте реализации (57) изобретения раскрыт способ лечения связанного с белком тау заболевания или расстройства, в том числе, нейродегенеративного заболевания или расстройства, такого как таупатия, включающий введение животному, конкретно млекопитающему, и конкретно человеку, страдающему таким заболеванием или расстройством, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В одном из вариантов реализации (58) изобретения раскрыт способ лечения заболеваний и расстройств, вызванных или связанных с образованием нейрофибриллярных повреждений, доминирующей патологии мозга при таупатии, которые включают гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, при которых проявляются патологии и амилоидные патологии, включая, без ограничений, болезнь Альцгеймера, болезнь Крейтцфельда-Якоба, деменцию боксеров, синдром Дауна, болезнь Герстманна – Штреусслера - Шейнкера, миозит с тельцами включения и вызванную прионными белками амилоидную ангиопатию мозга, травматическое повреждение мозга, и дополнительные заболевания или расстройства, при которые не проявляется явная амилоидная патология, включая, без ограничений, комплекс амиотрофный латеральный склероз/паркинсонизм-деменция Гуама, негуамские заболевания двигательных нейронов с нейрофибриллярными сплетениями, деменция с аргирофильными шарами, кортикобазальную дегенерацию, диффузные нейрофибриллярные сплетения с кальцификацией, фронтотемпоральную деменцию с паркинсонизмом, связанным с хромосомой 17, болезнь Галлервордена - Шпатца, множественную системную атрофию, болезнь Ниманна - Пика, тип С, паллидо-понто-нигральную дегенерацию, синдром Пика, прогрессирующий подкорковый глиоз, прогрессирующий супрануклеарный паралич, подострый склерозирующий панэнцефалит, лимбическую деменцию, постэнцефалитный паркинсонизм, миотоническую дистрофию, причем указанный способ включает введение животному, конкретно млекопитающему, и конкретно человеку, страдающему таким заболеванием или расстройством, связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
В другом варианте реализации (59) изобретения раскрыт способ индукции пассивной иммунной реакции у животного, конкретно млекопитающего или человека, страдающего нейродегенеративным расстройством, таким как таупатия, путем введения указанному животному или человеку связывающегося пептида или его функциональной части, конкретно антитела, конкретно моноклонального антитела или его функциональной части, или полинуклеотида, или фармацевтического состава, в соответствии с любым из предыдущих вариантов реализации, или их комбинации.
Еще в одном варианте реализации (60) изобретения раскрыт способ диагностики связанного с белком тау заболевания, расстройства или состояния у больного, включающий обнаружение иммуноспецифичного связывания связывающегося пептида или его активного фрагмента, конкретно антитела, конкретно моноклонального антитела или его функциональной части, в соответствии с любым из предыдущих вариантов реализации, с эпитопом белка тау, в образце или in situ, который включает стадии
а. приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт со связывающимся пептидом или его фрагментом, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, по любому из предыдущих пунктов, притом, что указанный связывающийся пептид или антитело или его фрагмент связывается с эпитопом белка тау;
б. период времени, достаточный для связывания указанного связывающегося пептида, конкретно указанного антитела, конкретно указанного моноклонального антитела или его функциональной части, с белком тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса; и
г. установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке.
Еще в одном варианте реализации (61) изобретения раскрыт способ диагностики предрасположенности к связанному с белком тау заболеванию, расстройству или состоянию у больного, включающий обнаружение иммуноспецифичного связывания связывающегося пептида или его активного фрагмента, конкретно антитела, конкретно моноклонального антитела или его функциональной части, в соответствии с любым из предыдущих вариантов реализации, с эпитопом белка тау, в образце или in situ, который включает стадии:
а. приведение образца или конкретной части тела или участка тела, где предполагается содержание антигена тау, в контакт со связывающимся пептидом или его активным фрагментом, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, в соответствии с любым из предыдущих вариантов реализации, причем пептид или его фрагмент связывается с эпитопом белка тау;
б. период времени, достаточный для связывания указанного связывающегося пептида, конкретно указанного антитела, конкретно указанного моноклонального антитела или его функциональной части, с белком тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса; и
г. установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке.
д. сравнение содержания указанного иммунологического комплекса с контрольным нормальным значением;
притом, что повышение содержания указанного агрегата, по сравнению с контрольным нормальным значением, указывает на то, что указанный больной страдает от или подвержен риску развития связанного с белком тау заболевания или состояния.
В одном из вариантов реализации (62) изобретения раскрыт способ мониторинга минимального остаточного заболевания у больного после лечения связывающимся пептидом или его функциональной частью, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, или полинуклеотидом, или фармацевтическим составом, в соответствии с любым из предыдущих вариантов реализации, причем указанный способ включает:
а. приведение образца или конкретной части тела или участка тела, где предполагается содержание антигена тау, в контакт со связывающимся пептидом или его функциональной частью, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, в соответствии с любым из предыдущих вариантов реализации, притом, что пептид или его фрагмент связывается с эпитопом белка тау;
б. создание возможности для указанного связывающегося пептида, конкретно указанного антитела, конкретно указанного моноклонального антитела или его функциональной части, связаться с антигеном тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса; и
г. установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием антигена тау в образце или конкретной части тела или участке.
д. сравнение содержания указанного иммунологического комплекса с контрольным нормальным значением;
и при этом, повышение содержания указанного агрегата, по сравнению с контрольным нормальным значением, указывает на то, что указанный больной все еще страдает от минимального остаточного заболевания.
В одном из вариантов реализации (63) раскрыт способ прогнозирования ответа больного на лечение связывающимся пептидом или его функциональной частью, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, или полинуклеотидом или фармацевтическим составом, в соответствии с любым из предыдущих вариантов реализации, включающий:
а. приведение образца или конкретной части тела или участка тела, где предполагается содержание антигена тау, в контакт со связывающимся пептидом или его активным фрагментом, конкретно антителом, конкретно моноклональным антителом или его функциональной частью, в соответствии с любым из предыдущих вариантов реализации, причем пептид или его фрагмент связывается с эпитопом белка тау;
б. создание возможности для указанного связывающегося пептида, конкретно указанного антитела, конкретно указанного моноклонального антитела или его функциональной части, связаться с антигеном тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса; и
г. установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием антигена тау в образце или конкретной части тела или участке.
д. сравнение содержания указанного иммунологического комплекса до и после начала лечения;
притом, что снижение содержания указанного агрегата показывает, что у указанного больного присутствует высокий потенциал ответа на лечение.
Анти-Тау антитела и их фрагменты могут применяться в упомянутых выше способах по изобретению. В упомянутых выше способах образец, содержащий антитело или его фрагмент, может быть иммунообогащен, с целью повышения концентрации белка Тау в образце, путем приведения образца в контакт с анти-Тау антителом или его фрагментом, присоединенным к твердой подложке.
До начала стадии (а), проводят иммунообогащение образца, с целью повышения концентрации белка Тау в образце, путем приведения образца в контакт с анти-Тау антителом или его фрагментом, присоединенным к твердой подложке
В другом варианте реализации (64) изобретение относится к диагностическому набору для обнаружения и диагностики связанных с белком тау заболеваний, расстройств или состояний, содержащему связывающийся пептид или его активный фрагмент, конкретно антитело, конкретно моноклональное антитело или его функциональную часть, в соответствии с любым из предыдущих вариантов реализации.
В одном из вариантов реализации (65) указанный диагностический набор содержит емкость, содержащую один или больше связывающихся пептидов или их активных фрагментов, конкретно антител, конкретно моноклональных антител или их функциональных частей, в соответствии с любым из предыдущих вариантов реализации, и инструкцию по применению связывающихся пептидов или антител для целей связывания с антигеном тау с образованием иммунологического комплекса и обнаружения образования иммунологического комплекса, таким образом, что присутствие или отсутствие иммунологического комплекса коррелирует с присутствием или отсутствием антигена тау.
Еще в одном варианте реализации (66) настоящее изобретение относится к эпитопу на белке Тау млекопитающего, конкретно человека, как представлено в SEQ ID NO: 67, выбранному из группы, состоящей из Тау аа 393-401, содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 396-401 содержащего фосфорилированный Ser в положении 396 (pS396), Тау аа 394-400 содержащего фосфорилированный Ser в положении 396 (pS396), Tay aa 402-406 содержащего фосфорилированный Ser в положении 404 (pS404) и Tay aa 393-400 содержащего фосфорилированный Ser в положении 396 (pS396).
В одном из вариантов реализации (67) указанный эпитоп состоит из Tay aa 393-401, содержащего фосфорилированный Ser в положении 396 (pS396).
В одном из вариантов реализации (68) указанный эпитоп состоит из Tay aa 396-401, содержащего фосфорилированный Ser в положении 396 (pS396).
В одном из вариантов реализации (69) указанный эпитоп состоит из Tay aa 394-400, содержащего фосфорилированный Ser в положении 396 (pS396).
В одном из вариантов реализации (70) указанный эпитоп состоит из Tay aa 402-406, содержащего фосфорилированный Ser в положении 404 (pS404).
В одном из вариантов реализации (71) указанный эпитоп состоит из Tay aa 393-400, содержащего фосфорилированный Ser в положении 396 (pS396).
В другом варианте реализации (72) изобретение относится к линии клеток, вырабатывающей связывающийся пептид или его активный фрагмент, конкретно антитело, конкретно моноклональное антитело или его функциональную часть в соответствии с любым из предыдущих вариантов реализации.
В одном из вариантов реализации (73), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы А4-4А6-48, депонированную 30 августа 2011 года как DSM ACC3136.
В одном из вариантов реализации (74), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы A6-2G5-30, депонированную 30 августа 2011 года как DSM ACC3137.
В одном из вариантов реализации (75), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы A6-2G5-41, депонированную 30 августа 2011 года как DSM ACC3138.
В одном из вариантов реализации (76), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы А4-2А1-18, депонированную 30 августа 2011 года как DSM ACC3139.
В одном из вариантов реализации (77), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы А4-2А1-40, депонированную 30 августа 2011 года как DSM ACC3140.
В одном из вариантов реализации (78), изобретение относится к линии клеток, которая представляет собой линию клеток гибридомы A6-1D2-12, депонированную 6 сентября 2011 года как DSM ACC3141.
В одном из вариантов реализации (79) изобретение относится к моноклональному антителу или его функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), который кодируется полинуклеотидом, расположенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы А4-2А1-18, депонированной 30 августа 2011 года как DSM ACC3139, с использованием:
а. пары праймеров, содержащей 5'-праймер SEQIDNO: 149 и 3'-праймер SEQ ID NO: 51 для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO:120, 123, 124, 136, 137, 138, 139 и 140, и 3'-праймер, выбранный из группы, состоящей из SEQ ID NO: 131, 134 и 141-148, для амплификации второго домена связывания.
В одном из вариантов реализации (80) изобретение относится к моноклональному антителу или его функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), кодируемый полинуклеотидом, расположенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы A6-2G5-30, депонированной 30 августа 2011 года как DSM АСС3137, с использованием:
а. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ IDNO: 51 и 169-174, и 3'-праймер SEQ IDNO: 51, для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQIDNO: 124, 127 и 150-158, и 3'-праймер, выбранный из группы, состоящей из SEQ ID NO: 130 и 159-168, для амплификации второго домена связывания.
В одном из вариантов реализации (81) изобретение относится к моноклональному антителу или его функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), кодируемый полинуклеотидом, размещенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы А4-2А1-40, депонированной 30 августа 2011 года как DSM АСС3140, с использованием:
а. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO: 178, 179 и 180, и 3'-праймер SEQ ID NO: 51, для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO: 121, 127, 139, 154, 155 и 175, и 3'-праймер, выбранный из группы, состоящей из SEQ ID NO: 128, 129, 147, 176 и 177, для амплификации второго домена связывания.
В одном из вариантов реализации (82) изобретение относится к моноклональному антителу или функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), кодируемый полинуклеотидом, размещенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы A6-2G5-41, депонированной 30 августа 2011 года как DSM АСС3138, с использованием:
а. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ IDNO: 51 и 188-192, и 3'-праймер SEQ IDNO: 51, для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ IDNO: 120, 124, 126, 181, 182 и 183, и 3'-праймер, выбранный из группы, состоящей из SEQ ID NO:144, 145 и 184-187, для амплификации второго домена связывания.
В одном из вариантов реализации (83), изобретение относится к моноклональному антителу или его функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), кодируемый полинуклеотидом, размещенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы А4-4А6-48, депонированной 30 августа 2011 года как DSM АСС3136, с использованием:
а. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO: 50 и 201-204, и 3'-праймер SEQ ID NO: 51, для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO: 121, 137, 151 и 193-197, и 3'-праймер, выбранный из группы, состоящей из SEQ IDNO: 131, 141, 144, 166, 198, 199 и 200, для амплификации второго домена связывания.
В одном из вариантов реализации (84) изобретение относится к моноклональному антителу или его функциональной части, содержащей домен легкой цепи (VL) и/или тяжелой цепи (VH), кодируемый полинуклеотидом, размещенным на нуклеотидном фрагменте, который может быть получен ПЦР амплификацией ДНК линии клеток гибридомы A6-1D2-12, депонированной 6 сентября 2011 года как DSM АСС3141, с использованием:
а. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ ID NO:209-214 и 219-221, 3'-праймер SEQIDNO:215, для амплификации первого домена связывания; и/или
б. смеси праймеров, содержащей 5'-праймер, выбранный из группы, состоящей из SEQ Ю NO:216, 217 и 218, и 3'-праймер SEQ ID NO: 208, для амплификации второго домена связывания.
В одном из вариантов реализации (85), антитело в соответствии с любым из предыдущих вариантов реализации может представлять собой поликлональное антитело, моноклональное антитело, химерное антитело, гуманизированное антитело, человеческое антитело, верблюжье антитело, диатело, или модифицированное или сконструированное антитело.
В одном из вариантов реализации (86) изобретения раскрыт способ получения связывающихся пептидов или антител в соответствии с любым из предыдущих вариантов реализации, включающий стадию культивирования линии клеток в соответствии с любым из предыдущих вариантов реализации в пригодной среде культивирования и, необязательно, очистки связывающихся пептидов или антител из линии клеток или среды культивирования.
В другом варианте реализации (87) настоящего изобретения раскрыт способ обнаружения мультимеров фосфо-Тау (pTau) в образца мозга, включающий:
а. приведение образца в контакт с антителом или его фрагментом по любому из предыдущих пунктов, причем пептид или его фрагмент связывается с эпитопом белка фосфо-Тау;
б. обеспечение возможности для антитела связаться с белком тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса, конкретно с помощью анализа ТИФА.
В частности, в конкретном варианте реализации (88) изобретение относится к способу посмертного обнаружения мультимера фосфо-Тау (pTau) в гомогенатах мозга субъекта, предположительно страдающего связанным с тау заболеванием или расстройством, и здорового контрольного субъекта, который включает:
а. приведение образцов гомогената мозга обоих субъектов в контакт с антителом или его фрагментом по любому из предыдущих пунктов, причем пептид или его фрагмент связывается с эпитопом белка фосфо-Тау;
б. обеспечение возможности для антитела связаться с белком тау, с образованием иммунологического комплекса;
в. обнаружение образования иммунологического комплекса, конкретно с помощью анализа ТИФА, и
г. сравнение количества или интенсивности иммунологического комплекса в образце, полученном от субъекта, предположительно страдающего связанным с тау заболеванием, или субъекта из контрольной выборки,
притом, что повышение содержания или интенсивности указанного иммунологического комплекса, по сравнению с контрольным значением, показывает, что указанный больной страдал от минимального остаточного заболевания.
В одном из вариантов реализации (89) наблюдаемое в тестовом образце повышение, по сравнению с контрольной выборкой, находится в интервале от 30% до 50%, конкретно в интервале от 35% до 45%.
В одном из вариантов реализации (90) изобретения раскрыт связывающийся пептид или белок или его функциональная часть, конкретно антитело, конкретно моноклональное антитело или его функциональная часть, в соответствии с любым из предыдущих вариантов реализации, причем антитело или фрагмент демонстрирует благоприятный профиль рК. В частности, указанное антитело или фрагмент демонстрирует высокую концентрацию в сыворотке до 10 дней после введения, что указывает на фармакокинетический профиль (ФК), благоприятствующий применению указанных антител в качестве терапевтического антитела. (Deng et al., Expert Opin Drug Metab Toxicol, 2012, 8(2) 141-60; Putman et al., Trends Biotech, 2010 (28) 509-516; Bai, S. Clin Pharmacokinet 2012; 51 (2): 119-135).
КРАТКОЕ ОПИСАНИЕ ФИГУР И ПОСЛЕДОВАТЕЛЬНОСТЕЙ
ФИГУРЫ
Фиг. 1 иллюстрирует результаты обнаружения мультимеров фосфорилированного Тау ACI-35-2А1-Ab1 (левая панель), ACI-35-2G5-Ab3 (средняя панель) и контрольного антитела (НТ7; правая панель) в гомогенатах мозга человека, полученных от контрольных и БА субъектов.
Фиг. 2 (2А и 2В) иллюстрирует обнаружение общего и pTau с помощью коммерческих антител в гомогенатах мозга человека.
Фиг. 3 (ЗА, 3В, 3С) иллюстрирует обнаружение фосфо-Тау ACI-35-2А1-Ab1 (А), ACI-35-1D2-Ab1 (В) и ACI-35-2G5-Ab3 (С) в гомогенатах мозга человека.
Фиг. 4 (4А, 4В, 4С) иллюстрирует результаты обнаружения Tay-pS396 в мозге больного БА и контрольного субъекта (Контроль) с помощью антител ACI-35-2А1-Ab1 (А), ACI-35-lD2-Ab1 (В) и ACI-35-2G5-Ab3 (С), с применением AlphaLISA. ****р<0,0001, **р<0,01, тест Манна-Уитни.
Фиг. 5 (5А и 5В) иллюстрирует результаты окрашивания методом ИГА Тау-рТ231 (ATI 80) в миндалевидной железе (А) и гиппокампе (В), после лечения ACI-35-2G5-Ab3 мышей с трансгенным Тау.
Фиг. 6 (6А и 6В) иллюстрирует результаты окрашивания ИГА общего Тау (НТ7) в миндалевидной железе (А) и гиппокампе (В), после лечения ACI-35-2G5-Ab3 мышей с трансгенным Тау.
Фиг. 7 иллюстрирует SDS-PAGE для Tay-pS396, полученного с применением различных условий GSK3p, и блоттинг мембран с использованием антитела ACI-35-2G5-Ab3.
Фиг. 8 иллюстрирует специфичные условия анализа AlphaLISA с использованием антител ACI-35-2G5-Ab3-BT и Таи-13.
Фиг. 9 иллюстрирует обнаружение Tay-pS396 во фракции мозга S1 человека от одного донора БА; сравнение сигнала, полученного от образцов, обогащенных иммунопреципитацией (ИП), и образцов без ИП.
Фиг. 10 иллюстрирует результаты обнаружения Tay-pS396 в СМЖ больного БА и контрольного субъекта (Ctrl) с помощью антитела ACI-35-2G5-Ab3, с применением ИП, с последующим AlphaLISA. ***p=0,0003, тест Манна-Уитни.
ПОСЛЕДОВАТЕЛЬНОСТИ
SEQ ID NO: 46-57 представляют нуклеотидные последовательности прямых и обратных праймеров VH/VK.
SEQ ID NO: 62 представляет последовательность аминокислот антигена Тау, пептид Т3 (см. Табл. 1).
SEQ ID NO: 67 представляет последовательность аминокислот самой длинной изоформы тау человека (441 аа), которая также носит название Таи40.
SEQ ID NO: 68 представляет последовательность аминокислот вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-4А6-Ab1, вырабатываемого линией клеток гибридомы А4-4А6-18.
SEQ ID NO: 69 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab1, вырабатываемого линией клеток гибридомы А4-4А6-18.
SEQ ID NO: 70 представляет последовательность аминокислот CDR1 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO:71 представляет последовательность аминокислот CDR2 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO: 72 представляет последовательность аминокислот CDR3 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO: 73 представляет последовательность аминокислот CDR1 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO: 74 представляет последовательность аминокислот CDR2 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO: 75 представляет последовательность аминокислот CDR3 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab1.
SEQ ID NO: 76 представляет последовательность аминокислот вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-1D2-Ab1, вырабатываемого линией клеток гибридомы A6-1D2-12.
SEQ ID NO: 77 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-lD2-Abl, вырабатываемого линией клеток гибридомы A6-1D2-12.
SEQ ID NO: 78 представляет последовательность аминокислот CDR1 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO: 79 представляет последовательность аминокислот CDR2 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO: 80 представляет последовательность аминокислот CDR3 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO:81 представляет последовательность аминокислот CDR1 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO: 82 представляет последовательность аминокислот CDR2 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO: 83 представляет последовательность аминокислот CDR3 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-1D2-Ab1.
SEQ ID NO: 84 представляет нуклеотидную последовательность вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-4А6-Ab1, вырабатываемого линией клеток гибридомы А4-4А6-18.
SEQ ID NO: 85 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab1, вырабатываемого линией клеток гибридомы А4-4А6-18.
SEQ ID NO: 86 представляет нуклеотидную последовательность вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-1D2-Ab1, вырабатываемого линией клеток гибридомы A6-1D2-12.
SEQ ID NO: 87 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-1D2-Ab1, вырабатываемого линией клеток гибридомы A6-1D2-12.
SEQ ID NO: 88 представляет последовательность аминокислот вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2А1-Ab1, ACI-35-2A1-Ab2 и ACI-35-4А6-Ab2, соответственно, вырабатываемого линией клеток гибридомы А4-2А1-18, А4-2А1-40 и А4-4А6-48, соответственно.
SEQ ID NO: 89 представляет последовательность аминокислот CDR1 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-Ab2 и ACI-35-2G5-Ab3, соответственно.
SEQ ID NO: 90 представляет последовательность аминокислот CDR2 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2А1-Ab1, ACI-35-2А1-Ab2 и ACI-35-4А6-Ab2, соответственно.
SEQ ID NO: 91 представляет последовательность аминокислот CDR3 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2А1-Ab1, ACI-35-2А1-Ab2, ACI-35-4A6-Ab2, ACI-35-2G5-Ab2 и ACI-35-2G5-Ab3, соответственно.
SEQ ID NO: 92 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab2, вырабатываемого линией клеток гибридомы А4-2А1-40
SEQ ID NO: 93 представляет последовательность аминокислот CDR1 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab2.
SEQ ID NO: 94 представляет последовательность аминокислот CDR2 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab2.
SEQ ID NO: 95 представляет последовательность аминокислот CDR3 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab2.
SEQ ID NO: 96 представляет последовательность аминокислот вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-Ab1, вырабатываемого линией клеток гибридомы A6-2G5-08.
SEQ ID NO: 97 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-Ab1, вырабатываемого линией клеток гибридомы A6-2G5-08.
SEQ ID NO: 98 представляет последовательность аминокислот CDR1 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 99 представляет последовательность аминокислот CDR2 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 100 представляет последовательность аминокислот CDR3 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 101 представляет последовательность аминокислот CDR1 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 102 представляет последовательность аминокислот CDR2 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 103 представляет последовательность аминокислот CDR3 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-Ab1.
SEQ ID NO: 104 представляет последовательность аминокислот вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-АВЗ, соответственно, вырабатываемого линией клеток гибридомы A6-2G5-30 и А6-2G5-41, соответственно.
SEQ ID NO: 105 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-АВ3, соответственно, вырабатываемого линией клеток гибридомы A6-2G5-30 и А6-2G5-41, соответственно.
SEQ ID NO: 106 представляет последовательность аминокислот CDR1 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3, соответственно.
SEQ ID NO: 107 представляет последовательность аминокислот CDR2 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3, соответственно.
SEQ ID NO: 108 представляет последовательность аминокислот CDR3 вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3, соответственно.
SEQ ID NO: 109 представляет нуклеотидную последовательность вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2А1-Ab1, ACI-35-2A1-Ab2 и ACI-35-4А6-Ab2, соответственно, вырабатываемого линией клеток гибридомы А4-2А1-18, А4-2А1-40 и А4-4А6-48, соответственно.
SEQ ID NO: 110 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab2, вырабатываемого линией клеток гибридомы А4-2А1-40.
SEQ ID NO: 111 представляет нуклеотидную последовательность вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-AB1, вырабатываемого линией клеток гибридомы A6-2G5-08.
SEQ ID NO: 112 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB1, вырабатываемого линией клеток гибридомы A6-2G5-08.
SEQ ID NO: 113 представляет нуклеотидную последовательность вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3, соответственно, вырабатываемого линией клеток гибридомы A6-2G5-30 и А6-2G5-41, соответственно.
SEQ ID NO: 114 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3, соответственно, вырабатываемого линией клеток гибридомы A6-2G5-30 и Аб-2G5-41, соответственно.
SEQ ID NO:115 представляет последовательность аминокислот CDR2 вариабельного участка тяжелой цепи (VH) моноклонального антитела ACI-35-2G5-AB2 и ACI-35-2G5-AB3.
SEQ ID NO: 116 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab1, вырабатываемого линией клеток гибридомы А4-2А1-18.
SEQ ID NO: 117 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-2А1-Ab1, вырабатываемого линией клеток гибридомы А4-2А1-18.
SEQ ID NO: 118 представляет последовательность аминокислот вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4Аб-Ab2, вырабатываемого линией клеток гибридомы А4-4А6-48.
SEQ ID NO: 119 представляет нуклеотидную последовательность вариабельного участка легкой цепи (VK) моноклонального антитела ACI-35-4А6-Ab2, вырабатываемого линией клеток гибридомы А4-4А6-48.
SEQ ID NO: 120-221 представляет нуклеотидные последовательности прямых и обратных праймеров VH/VK.
Определение терминов
Термины «полипептид», «пептид» и «белок» в данном описании являются равнозначными и определены как обозначающие биомолекулу, состоящую из аминокислот, связанных пептидной связью.
Термины «пептиды» или «связывающийся пептид» используются в данном описании равнозначно и обозначают цепи аминокислот (обычно L-аминокислот), в которых альфа-атомы углерода соединены посредством пептидных связей, образованных в ходе реакции конденсации между карбоксильной группой альфа-атома углерода одной аминокислоты и аминогруппой альфа-атома углерода другой аминокислоты. Концевая аминокислота на одном конце цепи (т.е., амино-концевая) содержит свободную аминогруппу, тогда как концевая аминокислота на другом конце цепи (т.е., карбокси-концевая) содержит свободную карбоксильную группу. Таким образом, термин «аминный конец» (сокращено N-конец) обозначает свободную альфа-аминогруппу на аминокислоте, находящейся на аминном конце пептида, или альфа-аминогруппу (иминогруппу в случае участия в пептидной связи) аминокислоты в любом другом положении в пределах пептида. Кроме того, термин «карбоксильный конец» (сокращено С-конец) обозначает свободную карбоксильную группу на аминокислоте на карбоксильном конце пептида, или карбоксильную группу аминокислоты в любом другом положении в пределах пептида. Связывающийся пептид может составлять антитела, такие как поликлональные или моноклональные антитела, человеческие или гуманизированные антитела, диатела, верблюжьи антитела, и т.п., или их функциональные части, раскрытые определено в данном описании.
Термины «его фрагмент» или «фрагмент» в данном описании в контексте пептида обозначают функциональный фрагмент пептида, который обладает по существу такой же (биологической) активностью, что и интактный пептид, определенный в данном описании. В случае использования в данном описании в контексте антитела, термины обозначают фрагмент антитела, содержащий часть интактного антитела, которая содержит антигенсвязывающий или вариабельный участок интактного антитела. Примеры фрагментов антитела включают Fab, Fab', F(ab')2 и Fv фрагменты; диатела; молекулы одноцепочечных антител, в том числе, молекулы одноцепочечных Fv (scFv); и антитела с двойной и полиспецифичностью, и/или фрагменты антител.
Обычно, аминокислоты, из которых состоит пептид, нумеруются в порядке по возрастанию, начиная с аминного конца, и по направлению к карбоксильному концу пептида. Таким образом, если указано, что одна аминокислота «следует» за другой, то первая аминокислота расположена ближе к карбоксильному концу пептида, чем вторая аминокислота.
Термин «остаток» в данном описании применяется для обозначения аминокислоты, введенной в состав пептида посредством амидной связи. Как таковая, аминокислота может быть природной аминокислотой, или, если нет других ограничений, может включать известные аналоги природных аминокислот, которые функционируют до некоторой степени подобно природным аминокислотам (т.е., миметики аминокислот). Кроме того, миметик амидной связи включает модификации пептидного скелета, хорошо известные специалистам из уровня техники.
Выражение «по существу состоящий из» применяется в данном описании для исключения любых элементов, которые в существенной мере изменили бы значимые свойства пептидов, о которых говорится в выражении. Поэтому, описание пептида как «по существу состоящего из…» исключает любые замены, добавления или делеции аминокислот, которые значительно изменили бы биологическую активность указанного пептида.
Кроме того, специалисту будет понятно, что индивидуальные замены, делеции или добавления, которые модифицируют, добавляют или удаляют одинарную аминокислоту или небольшой процент аминокислот (обычно менее 5%, чаще менее 1%) в кодируемой последовательности, как упомянуто выше, представляют собой консервативные модификации, при которых изменения ведут к замене аминокислоты химически сходной аминокислотой. Таблицы консервативных замен, раскрывающие функционально подобные аминокислоты, хорошо известны из уровня техники. Каждая из приведенных ниже 6 групп содержит аминокислоты, которые являются консервативными заменами друг для друга:
1) Аланин (А), Серин (S), Треонин (Т);
2) Аспарагиновая кислота (D), Глутаминовая кислота (Е);
3) Аспарагин (N), Глутамин (Q);
4) Аргинин (R), Лизин (К);
5) Изолейцин (I), Лейцин (L), Метионин (М), Валин (V); и
6) Фенилаланин (F), Тирозин (Y), Триптофан (W).
Выражения «выделенные» или «биологически чистые» обозначают материал, который в существенной мере или по существу свободен от компонентов, обычно сопровождающих его в природном состоянии. Таким образом, пептиды, раскрытые в данном описании, не содержат материалов, обычно ассоциирующихся с их окружением in situ. Обычно, выделенные иммуногенные пептиды, раскрытые в данном описании, являются чистыми по меньшей мере приблизительно на 80%, обычно по меньшей мере приблизительно на 90%, и предпочтительно по меньшей мере приблизительно на 95%, по данным интенсивности полосы на окрашенном серебром геле.
Чистота или гомогенность белка может быть доказана с помощью целого ряда методов, хорошо известных из уровня техники, таких как электрофорез образца белка на полиакриламидном геле, с визуализацией после окрашивания. Для некоторых целей понадобится высокое разрешение, поэтому применяют ВЭЖХ или подобные методы очистки.
Если иммуногенные пептиды относительно короткие (т.е., менее чем приблизительно 50 аминокислот), их часто синтезируют с применением стандартных химических способов синтеза пептидов.
Твердофазный синтез, в ходе которого С-концевую аминокислоту последовательности присоединяют к нерастворимой подложке, с последующим добавлением остальных аминокислот последовательности, является предпочтительным способом химического синтеза иммуногенных пептидов, раскрытых в данном описании. Методы твердофазного синтеза известны специалистам из уровня техники, Альтернативно, иммуногенные пептиды, раскрытые в данном описании, синтезируют с применением методологии рекомбинантной нуклеиновой кислоты. В общем, она включает создание последовательности нуклеиновой кислоты, кодирующей пептид, размещение нуклеиновой кислоты в кассете экспрессии под контролем конкретного промотора, экспрессию пептида в организме хозяина, выделение экспрессированного пептида или полипептида и, при необходимости, рефолдинг пептида. В литературе можно найти методики, достаточные для осуществления таких процедур специалистом.
После экспрессии, рекомбинантные пептиды могут быть очищены согласно стандартным методикам, в том числе осаждение сульфатом аммония, аффинные колонки, колоночная хроматография, гель-электрофорез, и т.п. В существенной мере чистые композиции с гомогенностьют от приблизительно 50% до 95% являются предпочтительными, и с гомогенностью от 80% до 95% или более являются наиболее предпочтительными для применения в качестве терапевтических агентов.
Специалисту в данной области будет понятно, что после химического синтеза, биологической экспрессии или очистки, иммуногенные пептиды могут находиться в конформации, которая значительно отличается от природной конформации природных пептидов. В таком случае, часто существует необходимость в денатурации и выделении антипролиферативного пептида, с последующим рефолдингом пептида в предпочтительную конформацию. Способы выделения и денатурации белков, а также индукции рефолдинга хорошо известны специалистам в данной области.
Антигенность очищенного белка может быть подтверждена, например, демонстрацией реакции с иммунной сывороткой или с антисыворотками, полученными непосредственно против белка.
Термины «a», «an» и «the» (единственное число существительного) в данном описании подразумевают «один или больше» и включают множественное число, если это не противоречит контексту.
Термины «обнаружение» или «обнаружимый» в данном описании подразумевают применение известных способов обнаружения биологических молекул, таких как иммунохимические или гистологические способы, и обозначают качественное или количественное определение присутствия или концентрации биомолекулы в условиях испытания.
Под «выделенной» подразумевается биологическая молекула, свободная по меньшей мере от некоторых из компонентов, с которыми она найдена в природе.
Термины «антитело» или «антитела» или «его(их) функциональные части» в данном описании представляют собой признанный в уровне техники термин, и их следует понимать как обозначающие молекулы или активные фрагменты молекул, которые связываются с известными антигенами, конкретно с молекулами иммуноглобулинов и иммунологически активными частями молекул иммуноглобулинов, т.е., молекул, которые содержат сайт связывания, иммуноспецифично связывающийся с антигеном. Иммуноглобулин по изобретению может относится к любому типу (IgG, IgM, IgD, IgE, IgA и IgY) или классу (IgGI, IgG2, IgG3, IgG4, IgA1 и IgA2) или подклассам молекул иммуноглобулина.
«Антитела» в контексте настоящего изобретения включают моноклональные антитела, поликлональные, химерные, одноцепочечные антитела, антитела с двойной специфичностью, симианизированные, человеческие и гуманизированные антитела. верблюжьи антитела, диатела, а также их функциональные части или активные фрагменты. Примеры активных фрагментов молекул, которые связываются с известными антигенами, включают фрагменты Fab и Р(ab')2, в том числе, продукты экспрессии библиотеки иммуноглобулинов и фрагментов связывания с эпитопом любого из антител и фрагментов, упомянутых выше.
Такие активные фрагменты могут быть получены из антитела по настоящему изобретению целым рядом способов. Например, очищенные моноклональные антитела могут быть расщеплены ферментом, таким как пепсин, и обработаны ВЭЖХ гель-фильтрацией. Соответствующая фракция, содержащая фрагменты Fab, далее может быть собрана и концентрирована мембранной фильтрацией, и т.п. Дополнительное описание общих методов выделения активных фрагментов антител, см., например, в Khaw, В.A. et al. J. Nucl. Med. 23:1011-1019 (1982); Rousseaux et al. Methods Enzymo1ogy, 121:663-69, Academic Press (1986).
«Гуманизированное антитело» обозначает тип генно-инженерного антитела, которое содержит участки CDR, происходящие из нечеловеческого донорского иммуноглобулина, притом, что остальные части молекулы иммуноглобулина происходят от одного (или более) иммуноглобулина(ов) человека.
Гуманизированное антитело дополнительно может обозначать антитело, содержащее вариабельный участок, в котором один или больше каркасных участков содержат аминокислоты человека или приматов. Кроме того, поддерживающие каркас остатки могут быть модифицированы таким образом, чтобы сохранить сродство связывания. Способы получения «гуманизированных антител» хорошо известны специалистам в данной области (см., например. Queen et al., Proc. Natl Acad Sci USA, 86:10029-10032 (1989), Hodgson et al., Bio/Technoloy, 9:421 (1991)).
Кроме того, «гуманизированное антитело» может быть получено с помощью современного генно-инженерного подхода, который позволяют продуцирование поликлональных человекоподобных антител созревшей аффинности в организме крупных животных, например, таких как кролики (http://www.rctech.com/bioventures/therapeutic.php).
Термин «полностью человеческое антитело» или «человеческое» антитело обозначает антитело, полученное от трансгенных мышей, несущих гены антител человека, или из клеток человека. Для иммунной системы человека, однако, разница между «полностью человеческими», «человеческими» и «гуманизированными» антителами может быть незначительной или отсутствовать, и таким образом, все три могут обладать равной эффективностью и безопасностью.
Термин «моноклональное антитело» также хорошо известен в уровне техники и обозначает антитело, массово произведенное в лаборатории из единственного клона, которое распознает только один антиген. Моноклональные антитела обычно получают путем слияния В-клетки с нормальной, т.е., короткой продолжительностью жизни, вырабатывающей антитело, с быстрорастущей клеткой, такой как раковая клетка (иногда обозначается как «бессмертная» клетка). Полученная гибридная клетка или гибридома быстро размножается, образуя клон, который вырабатывает большие количества антитела.
Термин «антиген» обозначает молекулу или ее фрагмент, который может вызывать иммунный ответ в организме, конкретно животного, более конкретно млекопитающего, включая человека. Термин включает иммуногенные средства и участки, ответственные за антигенность, или антигенные детерминанты.
В данном описании термин «растворимый» обозначает частичное или полное растворение в водном растворе.
В данном описании термин «иммуногенный» обозначает субстанции, которые вызывают или увеличивают выработку антител, Т-клеток и других реактивных иммунных клеток, направленных против иммуногенного агента, и способствуют иммунному ответу у человека или животного.
Иммунная реакция возникает, когда индивидуум вырабатывает достаточно антител, Т-клеток и других реактивных иммунных клеток против иммуногенных композиций, которые вводят по настоящему изобретению для модуляции или облегчения расстройства, которое лечат.
Термин «гибридома» признан в уровне техники и понятен средним специалистам в данной области, как обозначающий клетку, полученную слиянием вырабатывающей антитело клетки и бессмертной клетки, например, клетки множественной миеломы. Указанная гибридная клетка способна непрерывно вырабатывать запас антитела. См. определение «моноклонального антитела» выше и Примеры ниже относительно более подробного описания способа слияния.
Термин «носитель» в данном описании обозначает структуру, в которую может быть введен антигенный пептид или супрамолекулярный конструкт или с которой он может быть связан, таким образом, презентуя или приводя в контакт антигенные пептиды или часть пептида с иммунной системой человека или животного. Любая частица, которая может соответствующим образом применяться в лечении животного или человека, например, такая как везикула, частица или сыпучее вещество, пригодна в качестве носителя в контексте настоящего изобретения.
Термин «носитель» дополнительно включает способы доставки, в которых композиции супрамолекулярного антигенного конструкта, содержащие антигенный пептид, могут быть доставлены к желательным участкам с помощью механизмов доставки. В одном из примеров такой системы используются коллоидные металлы, например,коллоидное золото.
Белки-носители, которые могут применяться в композициях супрамолекулярного антигенного конструкта по настоящему изобретению, включают, не ограничиваясь ими, связывающийся с мальтозой пептид «СМП»; альбумин телячьей сыворотки «АТС»; гемоцианин фиссуреловых «ГЦФ»; овальбумин; флагеллин; тироглобулин; альбумин сыворотки любого вида; гаммаглобулин любого вида; сингенные клетки; сингенные клетки, несущие антигены Ia; и полимеры D- и/или L-аминокислот.
Кроме того, термин «терапевтически эффективное количество» или «фармацевтически эффективное количество» обозначает количество связывающегося пептида, которое при введении человеку или животному является достаточным для оказания терапевтического воздействия на организм указанного человека или животного. Эффективное количество легко определяется средним специалистом в данной области с помощью шаблонных методик.
Выражения «ССН pTau», «CCH» и «спаренные спиральные нити» используются в данном описании синонимически и обозначают пары нитей размером приблизительно 10 нм, свитые в спирали с периодичностью 160 нм, которые можно визуализировать с помощью электронного микроскопа. Ширина варьирует в интервале от 10 до 22 нм. ССН являются доминирующими структурами в нейрофибриллярных сплетениях при болезни Альцгеймера (БА) и нейропильных нитях. ССН также можно наблюдать при некоторых, но не всех случаях дистрофических нефритов, связанных с невритными бляшками. Основным компонентом ССН является гиперфосфорилированная форма связанного с микротрубочками белка тау. ССН состоят из соединенных дисульфидными связями антипараллельных гиперфосфорилированных белков тау. ССН тау может быть укорочен на 20 остатков аминокислот на С-конце. Базовые механизмы образования ССН неясны, но гиперфосфорилирование тау может высвобождать его из микротрубочек, увеличивая растворимый пул тау.
В контексте настоящего изобретения продемонстрировано, что вызванный антителом ответ на антигенную композицию по изобретению в значительной степени независим от Т-клеток. С этой целью использовали модель на голых мышах, причем голых мышей вакцинировали, и ответ в форме антител измеряли для оценки ответа в форме Аβ-специфичных антител, вызванного антигенной композицией по изобретению у иммунизированных голых мышей. Голые мыши несут мутацию Foxnlnu и, следовательно, у них снижена функция Т-клеток в результате отсутствия функционирующего тимуса.
«Фармацевтически эффективное количество» в данном описании обозначает дозу активного ингредиента в фармацевтическом составе, соответствующую излечению, или по меньшей мере частичной остановке симптомов заболевания, расстройства или состояния, которое следует лечить, или любых связанных с ним осложнений.
В настоящем изобретении раскрыты связывающиеся пептиды, которые распознают и связываются с основными патологическими фосфо-эпитопами белка тау. В частности, настоящее изобретение раскрывает специфичные антитела против линейных и конформационных, простых и сложных фосфо-эпитопов на белке тау, которые считаются ответственными за синапсо- и нейротоксичность при таупатиях, включая БА.
Соответственно, в одном из вариантов реализации настоящее изобретение относится к связывающемуся пептиду или его функциональной части, конкретно к антителу, конкретно моноклональному антителу или его функциональной части, причем связывающийся пептид или антитело распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего, конкретно человека, или на его фрагменте, конкретно с патологическим конформером белка тау, но в одном из вариантов реализации не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами, притом, что указанный связывающийся пептид или антитело обладает высокой аффинностью связывания, с константой диссоциации по меньшей мере 10 нМ, конкретно по меньшей мере 8 нМ, конкретно по меньшей мере 5 нМ, конкретно по меньшей мере 2 нМ, конкретно по меньшей мере 1 нМ, конкретно по меньшей мере 500 пМ, конкретно по меньшей мере 400 пМ конкретно по меньшей мере 300 пМ, конкретно по меньшей мере 200 пМ, конкретно по меньшей мере 100 пМ, конкретно по меньшей мере 50 пМ.
«Растворимый белок тау» в данном описании обозначает белки, состоящие из двух полностью солюбилизированных мономеров белок Тау/пептид или Тау-подобные пептиды/белки или модифицированных или укороченных пептидов/белков Тау, или других производных пептидов/мономеров белка Тау, и олигомеров белка Тау. «Растворимый Тау» конкретно исключает нейрофибриллярные сплетения (НФС).
«Нерастворимый Тау» в данном описании обозначает множественные агрегированные мономеры пептидов или белков Тау, или Тау-подобных пептидов/белков, или модифицированных или укороченных пептидов/белков Тау или других производных пептидов/белков Тау, образующих олигомерные или полимерные структуры, которые нерастворимы в водной среде in vitro и in vivo в организме млекопитающего или человека, более конкретно в мозге, и конкретно множественные агрегированные мономеры Тау или модифицированные или укороченные пептиды/белки Тау или их производные, которые нерастворимы в организме млекопитающего или человека, более конкретно в мозге, соответственно. «Нерастворимый Тау» конкретно включает нейрофибриллярные сплетения (НФС).
«Мономерный Тау» или «мономер Тау» в данном описании обозначает полностью солюбилизированные белки Тау без агрегированных комплексов в водной среде.
«Агрегированный Тау», «олигомерный Тау» и «олигомер Тау» обозначают множественные агрегированные мономеры пептидов или белков Тау, Тау-подобных пептидов/белков или модифицированных или укороченных пептидов/белков Тау или других производных пептидов/белков Тау, образующих олигомерные или полимерные структуры, которые нерастворимы или растворимы в водной среде т vitro и в организме млекопитающего или человека in vivo, более конкретно в мозге, и конкретно множественные агрегированные мономеры Тау, модифицированных или укороченных пептидов/белков Тау или их производных, которые нерастворимы или растворимы в организме млекопитающего или человека, более конкретно, в мозге, соответственно.
«Модулирующее антитело» обозначает антитело или его функциональный фрагмент, как описано в различных вариантах реализации настоящего изобретения, которые также могут регулировать вверх (например, активизировать или стимулировать), регулировать вниз (например, ингибировать или подавлять) или иным способом изменять функциональное свойство, биологическую активность или уровень растворимого и/или нерастворимого и/или олигомерного белка Тау, конкретно растворимого фосфорилированного белка тау, in vivo, конкретно в мозге, конкретно в коре мозга и/или гиппокампе, животного, конкретно млекопитающего или человека, у которого присутствуют повышенные уровни растворимого белка тау и/или растворимого фосфорилированного белка тау. Модулирующее антитело или его функциональный фрагмент может действовать таким образом, чтобы модулировать белок тау или полипептид, кодирующий указанный белок тау, прямо или косвенно. В некоторых вариантах, модулирующее антитело или его функциональный фрагмент снижает уровни растворимого и/или нерастворимого и/или олигомерного, конкретно растворимого и нерастворимого белка тау, конкретно растворимого и нерастворимого и олигомерного белка тау. В одном из аспектов, растворимый и/или нерастворимый и/или олигомерный белок тау представляет собой фосфорилированный белок тау, конкретно растворимый фосфорилированный белок тау, в мозге, конкретно в коре мозга и/или гиппокампе животного, конкретно млекопитающего или человека, у которого присутствуют повышенные уровни белка тау и/или фосфорилированного белка тау, конкретно растворимого белка тау и/или растворимого фосфорилированного белка тау.
В одном из вариантов реализации настоящего изобретения раскрывается фармацевтический состав, содержащий связывающийся пептид или его функциональную часть, конкретно антитело, конкретно моноклональное антитело или его функциональную часть, или полинуклеотид, содержащий последовательность нуклеиновой кислоты, кодирующую указанный связывающийся пептид или антитело, согласно любому из вариантов реализации, раскрытых и заявленных в данном изобретении, или их комбинация, в терапевтически эффективном количестве, вместе с фармацевтически приемлемым носителем.
Пригодные фармацевтические носители, разбавители и/или вспомогательные вещества хорошо известны в данной области и включают, например, буферизованные фосфатом солевые растворы, воду, эмульсии, такие как эмульсии масло/вода, различные виды увлажняющих агентов, стерильные растворы, и т.п.
Связывающиеся пептиды по изобретению, в том числе, антитела, конкретно моноклональные антитела и их активные фрагменты, могут быть введены в физиологически приемлемый состав, который может содержать фармацевтически приемлемый носитель, разбавитель и/или вспомогательное вещество, с помощью известных методов. Например, связывающиеся пептиды по изобретению и как описано в данном описании, в том числе, любые функционально эквивалентные связывающиеся пептиды или их функциональные части, в частности, моноклональные антитела по изобретению, включая любые функционально эквивалентные антитела или их функциональные части, объединяют с фармацевтически приемлемьм носителем, разбавителем и/или вспомогательным веществом, чтобы получить терапевтический состав. Пригодные фармацевтические носители, разбавители и/или вспомогательные вещества хорошо известны в данной области и включают, например, буферизованные фосфатом солевые растворы, воду, эмульсии, такие как эмульсии масло/вода, различные виды увлажняющих агентов, стерильные растворы, и т.п.
Препарат фармацевтического состава по изобретению может быть получен в соответствии со стандартной методологией, известной среднему специалисту в данной области из уровня техники.
Составы по настоящему изобретению могут вводиться субъекту в форме твердого вещества, жидкости или аэрозоля в подходящей, фармацевтически эффективной дозе. Примеры твердых составов включают пилюли, кремы и имплантируемые лекарственные формы. Пилюли могут вводиться перорально. Терапевтические кремы могут применяться местно. Имплантируемые лекарственные формы могут вводиться в определенном месте, например, в месте опухоли, или могут быть имплантированы для системного высвобождения терапевтического состава, например, подкожно. Примеры жидких композиций включают составы, адаптированные для внутримышечной, подкожной, внутривенной, внутриартериальной инъекции, и препараты для местного и внутриглазного применения. Примеры аэрозольных составов включают составы для ингалятора, вводимые в легкое.
Составы могут вводиться стандартными способами введения. В целом, состав может применяться местно, вводиться перорально, ректально, интраназально, внутрикожно, внутрибрюшинно или парентерально (например, внутривенно, подкожно или внутримышечно).
Кроме того, состав может быть введен в матрицы замедленного высвобождения, например, поддающиеся биологическому разложению полимеры, полимеры, имплантируемые в непосредственной близости от того места, куда желательно произвести доставку, например, в месте опухоли. Способ включает введение единичной дозы, введение нескольких доз через предварительно определенные промежутки времени, и непрерывное введение в течение предварительно определенного периода времени.
Матрица замедленного высвобождения в данном описании представляет собой матрицу, изготовленную из материалов, обычно полимерных, которые разлагаются ферментным или кислотным/основным гидролизом или растворением. После введения в организм, на матрицу действуют ферменты и жидкости биологического происхождения. Матрицу замедленного высвобождения желательно выбирать из биосовместимых материалов, таких как липосомы, полилактиды (полимолочная кислота), полигликолид (полимер гликолевой кислоты), полилактид со-гликолид (сополимеры молочной кислоты и гликолевой кислоты), полиангидриды, поли(орто)эфиры, полипептиды, гиалуроновая кислота, коллаген, хондроитина сульфат, карбоновые кислоты, жирные кислоты, фосфолипиды, полисахариды, нуклеиновые кислоты, полиаминокислоты, аминокислоты, такие как фенилаланин, тирозин, изолейцин, полинуклеотиды, поливинилпропилен, поливинилпирролидон и силикон. Предпочтительная биоразлагаемая матрица представляет собой матрицу из полилактида, полигликолида или полилактида со-гликолида (сополимеры молочной кислоты и гликолевой кислоты).
Среднему специалисту в данной области хорошо известно, что дозировка композиции будет зависеть от различных факторов, например, таких как требующее лечения состояние, конкретный применяемый состав и другие клинические факторы, например, масса тела, размеры, пол и общее состояние здоровья больного, площадь поверхности тела, конкретное соединение или состав для введения, другие лекарственные средства, которые вводят параллельно, и способ введения.
Состав по изобретению можно вводить в комбинации с другими составами, содержащими биологически активную субстанцию или соединение, например, такое как известное соединение, применяемое в лечении таупатий и/или амилоидозов, группы заболеваний и расстройств, связанных с амилоидом или амилоид-подобным белком, таким как амилоидный β белок, принимающий участие в болезни Альцгеймера.
Другая биологически активная субстанция или соединение может оказывать свое биологическое воздействие по такому же или сходному механизму, как терапевтическая вакцина по изобретению, или неродственному механизму действия, или множеству родственных и/или неродственных механизмов действия.
В целом, другое биологически активное соединение может включать усилители нейтронной передачи, психотерапевтические лекарственные средства, ингибиторы ацетилхолинэстеразы, блокаторы кальциевых каналов, биогенные амины, бензодиазепиновые транквилизаторы, активаторы синтеза, хранения или высвобождения ацетилхолина, постсинаптические агонисты рецепторов ацетилхолина, или ингибиторы моноаминоксидазы А или В, антагонисты рецептора N-метил-D-аспартатглутамата, нестероидные противовоспалительные препараты, антиоксиданты и антагонисты серотонинергического рецептора.
В частности, биологически активный агент или соединение может включать по меньшей мере одно соединение, выбранное из группы, состоящей из соединений, противостоящих окислительному стрессу, анти-апоптотических соединений, образующих комплексы с металлами хелатных агентов, ингибиторов восстановления ДНК, таких как пирензепин и метаболиты, 3-амино-1-пропансульфоновой кислоты (3АПС), 1,3-пропандисульфоната (1,3ПДС), активаторов секретазы, ингибиторов [бета]- и 7-секретазы, белков тау, нейромедиаторов, дробителей 3-листов, противовоспалительных молекул, «атипичных антипсихотических средств», таких как клозапин, зипразидон, рисперидон, арипипразол или оланзапин, или ингибиторов холинэстеразы (ИХЭ), таких как такрин, ривастигмин, донепезил и/или галантамин, и других лекарственных средств и биологически активных добавок, например, таких как витамин В12, цистеин, прекурсор ацетилхолина, лецитин, холин, Ginkgo biloba, ацетил-L-карнитин, идебенон, пропентофиллин или производное ксантина, вместе со связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, и, необязательно, фармацевтически приемлемый носитель и/или разбавитель и/или вспомогательное вещество, и инструкции по лечению заболеваний.
В другом варианте реализации состав по изобретению может содержать ниацин или мемантин, вместе со связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, и, необязательно, фармацевтически приемлемый носитель и/или разбавитель и/или вспомогательное вещество.
Еще в одном варианте реализации изобретения раскрыт состав, содержащий «атипичные антипсихотические средства», такие как клозапин, зипразидон, рисперидон, арипипразол или оланзапин, для лечения галлюцинаций, в том числе, позитивных и негативных психотических симптомов, иллюзий, расстройств мышления (которые проявляются очевидной бессвязностью, соскальзыванием, тангенциальность мышления), странного или дезорганизованного поведения, а также ангедонии, притупленного аффекта, апатичности и социальной изоляции, вместе со связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, и, необязательно, фармацевтически приемлемый носитель и/или разбавитель и/или вспомогательное вещество.
Другие соединения, которые могут применяться в составах в дополнение к связывающемуся пептиду по изобретению, раскрыты, например, в WO 2004/058258 (конкретно см. стр. 16 и 17), включая мишени терапевтических лекарственных средств (стр. 36-39), алкансульфоновые кислоты и алканосерные кислоты (стр. 39-51), ингибиторы холинэстеразы (стр. 51-56), антагонисты рецептора N-метил-D-аспартата (стр. 56-58), эстрогены (стр. 58-59), нестероидные противовоспалительные лекарственные средства (стр. 60-61), антиоксиданты (стр. 61-62), агонисты рецепторов, активируемых пролифератором пероксисом (PPAR), гипохолестеринемические агенты (стр. 68-75); ингибиторы амилоида (стр. 75-77), ингибиторы образования амилоида (стр. 77-78), хелатные агенты, образующие комплексы с металлами (стр. 78-79), антипсихотические средства и антидепрессанты (стр. 80-82), биологически активные добавки (стр. 83-89), а также соединения, повышающие доступность биологически активных субстанций в мозге (см. стр. 89-93) и пролекарства (стр. 93 и 94), причем указанный документ включен в данное описание посредством ссылки, и конкретно соединения, упомянутые на страницах, приведенных выше.
Белковое фармацевтически активное вещество может присутствовать в количествах в интервале от 1 нг до 10 мг на дозу. В общем, схема введения должна включать интервал от 0,1 мкг до 10 мг антитела по изобретению, конкретно интервал от 1,0 мкг до 1,0 мг, и более конкретно, интервал от 1,0 мкг до 100 мкг, причем все индивидуальные значения в пределах указанных интервалов также являются частью изобретения. Если введение проводят путем непрерывной инфузии, более подходящие дозы могут находиться в интервале от 0,01 мкг до 10 мг на килограмм массы тела в час, причем все индивидуальные значения в пределах указанных интервалов также являются частью изобретения.
В общем, введение будет парентеральным, например, внутривенным или подкожным. Препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Неводные растворители включают, не ограничиваясь ими, пропиленгликоль, полиэтиленгликоль, масло, например, оливковое масло, и инъекционные органические эфиры, например, этилолеат. Водные растворители могут быть выбраны из группы, состоящей из воды, спиртовых/водных растворов, эмульсий или суспензий, включая солевые и буферизованные среды. Растворитель для парентерального введения включает раствор натрия хлорида, раствор Рингера с глюкозой, глюкозу и натрия хлорид, раствор Рингера с лактатом или нелетучие масла. Растворитель для внутривенного введения включает средства для восполнения дефицита жидкости и питательных веществ, средства для восполнения дефицита электролитов (например, на основе раствора Рингера с глюкозой), и др. Консерванты также могут присутствовать, например, такие как противомикробные средства, антиоксиданты, хелатные агенты, инертные газы, и т.п.
Фармацевтический состав дополнительно может содержать белковые носители, такие как альбумин сыворотки или иммуноглобулин, конкретно человеческого происхождения. Кроме того, биологически активные агенты могут присутствовать в фармацевтическом составе по изобретению, в зависимости от его запланированного применения.
Если мишень связывания находится в мозге, некоторые варианты реализации изобретения предусматривают связывающийся пептид по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, для проникновения сквозь гематоэнцефалический барьер. Некоторые нейродегенеративные заболевания связаны с повышением проницаемости гематоэнцефалического барьера, и таким образом, связывающийся пептид по изобретению, включая антитела, конкретно моноклональные антитела или их активный фрагмент, может быть легко введен в мозг. Если гематоэнцефалический барьер остается интактным, в уровне техники известно несколько подходов для переноса молекул сквозь него, в том числе, без ограничений, физические способы, основанные на липидах способы, и основанные на рецепторах и каналах способы.
Физические способы переноса связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела или их активный фрагмент, сквозь гематоэнцефалический барьер включают, не ограничиваясь ими, полный обход гематоэнцефалического барьера или создание прохода в гематоэнцефалическом барьере. Способы обхода включают, не ограничиваясь ими, прямую инъекцию в мозг (см., например, Papanastassiou et al., Gene Therapy 9: 398-406 (2002)) и имплантацию в мозг устройства для доставки (см., например. Gill et al., Nature Med. 9: 589-595 (2003); и Gliadel Wafers(TM), Guildford Pharmaceutical). Способы создания проходов в барьере включают, не ограничиваясь ими, ультразвук (см., например. Патентную публикацию США №2002/0038086), осмотическое давление (например, введение гипертонического раствора маннита (Neuwelt, E.A., Implication of the Blood-Brain Barrier and its Manipulation, Vols 1 & 2, Plenum Press, N.Y. (1989)), повышение проницаемости, например, с помощью брадикинина или пермеабилизатора А-7 (см., например, патенты США №№5112596, 5268164, 5506206 и 5686416), и трансфекцию нейронов, располагающихся по обе стороны гематоэнцефалического барьера, векторами, которые содержат гены, кодирующие связывающийся пептид или фрагмент связывания с антигеном (см., например, Патентную публикацию США №2003/0083299).
Основанные на липидах способы транспортировки связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела, или их активный фрагмент, сквозь гематоэнцефалический барьер включают, не ограничиваясь или, инкапсуляцию связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела, или их активный фрагмент, в липосомы, которые связаны с их активными фрагментами, связывающимися с рецепторами на сосудистом эндотелии гематоэнцефалического барьера (см., например. Публикацию Патентной заявки США №20020025313), и покрытие связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела, или их активный фрагмент, частицами липопротеина низкой плотности (см., например. Публикацию Патентной заявки США №20040204354) или аполипопротеина Е (см., например, Публикацию Патентной заявки США №20040131692).
Основанные на рецепторах и каналах способы переноса связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела, или их активный фрагмент, сквозь гематоэнцефалический барьер включают, не ограничиваясь ими, применение блокаторов глюкокортикоида с целью повышения проницаемости гематоэнцефалического барьера (см., например, Публикацию Патентных заявок США №№2002/0065259, 2003/0162695 и 2005/0124533); активацию калиевых каналов (см., например, Публикацию Патентной заявки США №2005/0089473), ингибирующие АВС переносчики лекарственных средств (см., например. Публикацию Патентной заявки США №2003/0073713); покрытие антител трансферрином и модулирование активности одного или более рецепторов трансферрина (см., например, Публикацию Патентной заявки США №2003/0129186), и катионизацию антитела (см., например, патент США №5004697).
Однократные или многократные дозы связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела, или их активный фрагмент, или фармацевтического состава по изобретению могут быть введены субъекту в течение длительного периода времени. Продолжительность введения может находиться в интервале от 1 недели до 12 месяцев или более. В течение данного времени связывающийся пептид, антитело или фармацевтический состав может вводиться 1 раз в неделю, 1 раз в 2 недели, 3 недели, 4 недели, и т.д, или с большей или меньшей частотой, в зависимости от потребностей субъекта, который получает лечение.
В другом варианте реализации настоящего изобретения раскрыты способы и наборы для обнаружения и диагностики связанных с белком тау заболеваний, расстройств или состояний, в том числе, нейродегенеративных заболеваний или расстройств, таких как таупатии, включающие гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, которые демонстрируют присутствие как патологии тау, так и амилоидной патологии, в том числе, без ограничений, болезнь Альцгеймера, болезнь Крейтцфельда - Якоба, деменция боксеров, синдром Дауна, болезнь Герстманна – Штреусслера - Шейнкера, миозит с тельцами включения и вызванная прионными белками амилоидная ангиопатия мозга, травматическое повреждение мозга и другие заболевания или расстройства, которые не демонстрируют явной амилоидной патологии, в том числе, без ограничений, комплекс амиотрофный латеральный склероз/паркинсонизм-деменция Гуама, негуамское заболевание моторных нейронов с нейрофибриллярными сплетениями, деменция с аргирофильными шарами, кортикобазальная дегенерация, диффузные нейрофибриллярные сплетения с кальцификацией, фронтотемпоральная деменция с паркинсонизмом, связанным с хромосомой 17, фронтотемпоральная деменция, болезнь Галлервордена - Шпатца, множественная системная атрофия, болезнь Ниманна - Пика, тип С, паллидо-понто-нигральная дегенерация, синдром Пика, прогрессирующий подкорковый глиоз, прогрессирующий супрануклеарный паралич, подострый склерозирующий панэнцефалит, лимбическая деменция, постэнцефалитный паркинсонизм и миотоническая дистрофия. Патологическая аномалия может быть вызвана или связана с образованием нейрофибриллярных повреждений, доминирующей патологии мозга при таупатии.
Кроме того, настоящее изобретение раскрывает способы и наборы для диагностики предрасположенности к связанным с белком тау заболеваниям, расстройствам или состояниям, в том числе, нейродегенеративным заболеваниям или расстройствам, таким как таупатии, включающие гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, при которых одновременно проявляются патологии тау и амилоидные патологии, или для мониторинга минимального остаточного заболевания у больного, или для прогнозирования реакции больного на лечение связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, или составом по изобретению, и как описано в данном описании. Указанные способы включают известные иммунологические способы, обычно применяемые для обнаружения или количественного определения субстанций в биологических образцах или в условиях in situ.
Постановка диагноза связанного с белком тау заболевания или состояния, или предрасположенности к связанному с белком тау заболеванию или состоянию у субъекта, нуждающегося в этом, конкретно млекопитающего, более конкретно, человека, в том числе нейродегенеративных заболеваний или расстройств, таких как таупатии, включающие гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, при которых проявляются патологии тау и амилоидные патологии, может быть осуществлена путем обнаружения иммуноспецифичного связывания связывающегося пептида по изобретению, конкретно антитела, конкретно моноклонального антитела или его активного фрагмента, с эпитопом белка тау, в образце или in situ, что включает приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт с антителом, которое связывается с эпитопом белка тау, обеспечение возможности для антитела связаться с белком тау, с образованием иммунологического комплекса, обнаружение образования иммунологического комплекса, и установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке, с необязательным сравнением количества иммунологического комплекса с контрольным нормальным значением, притом, что повышение содержания иммунологического комплекса, по сравнению с контрольным нормальным значением, указывает на то, что субъект страдает от или подвержен риску развития связанного с белком тау заболевания или состояния.
Мониторинг минимального остаточного заболевания у субъекта, конкретно млекопитающего, более конкретно, человека, после лечения связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, или составом по изобретению, может быть осуществлен путем обнаружения иммуноспецифичного связывания связывающегося пептида по изобретению, конкретно антитела, конкретно моноклонального антитела или его активного фрагмента, с эпитопом белка тау, в образце или in situ, что включает приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт со связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, который связывается с эпитопом белка тау, создание возможности для связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, связаться с белком тау, с образованием иммунологического комплекса, обнаружение образования иммунологического комплекса, и установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке, с необязательным сравнением количества указанного иммунологического комплекса с контрольным нормальным значением, притом, что повышение содержания указанного иммунологического комплекса, по сравнению с контрольным нормальным значением, указывает на то, что субъект может все еще страдать минимальным остаточным заболеванием.
Прогнозирование ответа субъекта, конкретно млекопитающего, более конкретно, человека, на лечение связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, или составом по изобретению, может быть осуществлено путем обнаружения иммуноспецифичного связывания связывающегося пептида, конкретно моноклонального антитела или его активного фрагмента, с эпитопом белка тау, в образце или in situ, что включает приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт со связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, который связывается с эпитопом белка тау, создание возможности для связывающегося пептида по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, связаться с белком тау, с образованием иммунологического комплекса, обнаружение образования иммунологического комплекса и установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке, с необязательным сравнением количества указанного иммунологического комплекса до и после начала лечения, притом, что снижение содержания указанного иммунологического комплекса указывает на то, что у указанного больного присутствует высокий потенциал ответа на лечение.
Биологические образцы, которые могут применяться для диагностики связанного с белком тау заболевания или состояния, для диагностики предрасположенности к связанному с белком тау заболеванию или состоянию, в том числе, нейродегенеративным заболеваниям или расстройствам, таким как таупатии, включающие гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболеваний или расстройств, при которых проявляются патологии и амилоидные патологии, или для мониторинга минимального остаточного заболевания у больного или для прогнозирования ответа больного на лечение связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты или состав по изобретению, и как описано в данном описании, представляют собой, например, жидкости, такие как сыворотка, плазма, слюна, желудочный секрет, слизь, спинномозговая жидкость, лимфатическая жидкость, и т.п., или образцы тканей или клеток, полученные из организма, например, ткань нервов, мозга, сердца или сосудов. Для определения присутствия или отсутствия белка тау в образце, может применяться любой иммуноанализ, известный среднему специалисту из уровня техники, например, такой как анализы, в которых применяются косвенные способы обнаружения, с использованием вторичных реактивов для обнаружения, ТИФА и анализы иммунопреципитации и агглютинации. Подробное описание таких анализов приведено, например, в Harlow and Lane, Antibodies: A Laboratory Manual (Cold Spring Harbor Laboratory, New York 1988 555-612, WO 96/13590, заявители Maertens и Stuyver, Zrein с соавт. (1998) и WO 96/29605.
Для диагностики in situ, связывающийся пептид по изобретению, включая антитела по изобретению, конкретно моноклональные антитела и их активные фрагменты или любую их активную и функциональную часть, может быть введен в организм, для которого следует провести диагностику, способами, известными из уровня техники, например, такими как внутривенная, подкожная, интраназальная, внутрибрюшинная, интрацеребральная, внутриартериальная инъекция, таким образом, что может происходить специфичное связывание между антителом по изобретению и участком эпитопа на амилоидном белке. Комплекс связывающийся пептид/антиген традиционно может быть обнаружен с помощью метки, присоединенной к связывающемуся пептиду по изобретению, включая антитела, конкретно моноклональные антитела или их функциональный фрагмент, или любым другим известным из уровня техники способом обнаружения.
Иммуноанализы, применяемые с целью диагностики связанного с белком тау заболевания или состояния или предрасположенности к нему, включая нейродегенеративные заболевания или расстройства, например, таупатии, включающие гетерогенную группу нейродегенеративных заболеваний или расстройств, в том числе, заболевания или расстройства, при которых проявляются патологии и амилоидные патологии, или для мониторинга минимального остаточного заболевания у больного, или для прогнозирования ответа больного на лечение связывающимся пептидом по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, или составом по изобретению, и как описано в данном описании, обычно основаны на меченных антигенах, связывающихся пептидах, или вторичных реактивах для обнаружения. В такие белки или реактивы могут быть введены метки в виде соединений, известных среднему специалисту из уровня техники, включая ферменты, радиоизотопы и флуоресцентные, люминесцентные и хромогенные субстанции, и включая, без ограничений, окрашенные частицы, такие как коллоидное золото и латексные гранулы. Из перечисленного, радиоактивная метка может применяться почти для всех видов анализов и с большинством вариаций. Конъюгированные с ферментом метки особенно пригодны в тех случаях, когда радиоактивности следует избегать, или когда необходимо быстро получить результаты. Флуорохромы, хотя и требуют дорогостоящего оборудования для их применения, предлагают высокочувствительный способ обнаружения. Пригодные для таких анализов связывающиеся пептиды раскрыты и заявлены в настоящем изобретении, в том числе, антитела, конкретно моноклональные антитела, поликлональные антитела и поликлональные антитела очищенной аффинности.
Альтернативно, в связывающийся пептид по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, метка может быть введена косвенно, путем реакции с содержащими метку субстанциями, которые обладают аффинностью в отношении иммуноглобулина, такими как Белок А или G, или вторичные антитела. Связывающийся пептид по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, может быть конъюгирован со второй субстанцией и обнаружен с помощью меченной третьей субстанции, обладающей аффиностью в отношении второй субстанции, конъюгированной с антителом. Например, связывающийся пептид по изобретению, включая антитела, конкретно моноклональные антитела и их активные фрагменты, может быть конъюгирован с биотином и связывающимся конъюгатом пептид/биотин, обнаружимым с помощью меченного авидина или стрептавидина. Кроме того, связывающийся пептид может быть конъюгирован с гаптеном, и конъюгат связывающийся пептид/гаптен обнаружен с помощью меченного анти-гаптенового связывающегося пептида.
Среднему специалисту из уровня техники будут известны перечисленные и другие пригодные метки, которые могут применяться в соответствии с настоящим изобретением. Присоединение таких меток к связывающимся пептидам или их фрагментам может быть осуществлено с применением стандартных способов, обычно известных среднему специалисту в данной области. Типичные методы описаны Kennedy, J. H., et al., 1976 (Clin. Chim. Acta 70:1-31), и Schurs, A. H. W. M., et al. 1977 (Clin. Chim Acta 57:1-40). Методики сочетания, упомянутые в последнем источнике, представляют собой глутаральдегидный способ, перйодатный способ, дималеинимидный способ и другие, все из которых включены в данное описание посредством ссылки.
В существующих иммуноанализах применяется метод двойного антитела для обнаружения присутствия анализируемого вещества, в котором метку в антитело вводят косвенно, посредством реакции со вторым антителом, которое содержит обнаружимую метку. Второе антитело предпочтительно является таким, которое связывается с антителами животного, от которого получено моноклональное антитело. Другими словами, если моноклональное антитело представляет собой антитело мыши, то второе, меченное антитело представляет собой анти-мышиное антитело. В случае антитела, которое применяется в анализе, раскрытом в настоящем описании, такая метка предпочтительно представляет собой покрытую антителом гранулу, конкретно магнитную гранулу. В случае антитела, которое применяется в иммуноанализе, раскрытом в данном описании, метка предпочтительно представляет собой обнаружимую молекулу, такую как радиоактивная, флуоресцентная или электрохемилюминесцентная субстанция.
Альтернативные системы двойного антитела, часто называемые системами быстрого формата, поскольку они адаптированы к быстрому определению наличия анализируемого вещества, также могут применяться в контексте настоящего изобретения. Система требует высокой аффинности между антителом и анализируемым веществом. В соответствии с одним из вариантов реализации настоящего изобретения, присутствие амилоидного белка определяют, используя пару антител, каждое из которых специфично в отношении амилоидного белка. Одно из указанной пары антител здесь и в дальнейшем носит название «антитело-детектор», и другое из указанной пары антител здесь и в дальнейшем носит название «антитело захвата». Моноклональное антитело по настоящему изобретению может применяться в качестве антитела захвата или антитела-детектора. Моноклональное антитело по настоящему изобретению также может применяться в качестве антитела захвата и антитела-детектора одновременно в одном анализе. В одном из вариантов реализации настоящего изобретения, таким образом, применяется способ двойного «сандвича» антител для обнаружения амилоидного белка в образце биологической жидкости. В данном способе, анализируемое вещество (амилоидный белок) располагается между антителом-детектором и антителом захвата, притом, что антитело захвата необратимо иммобилизировано на твердой подложке. Антитело-детектор должно содержать обнаружимую метку для идентификации присутствия «сандвича» антитело-анализируемое вещество и, таким образом, присутствия анализируемого вещества.
Примеры твердофазных субстанций включают, не ограничиваясь ими, планшеты для микротитрования, пробирки из полистирола, магнитные пластмассовые или стеклянные гранулы и покровные стекла, которые хорошо известны в области радиоиммуноанализа и иммуноферментного анализа. Способы присоединения антител к твердым фазам также хорошо известны среднему специалисту из уровня техники. Позже, целый ряд пористых материалов, таких как нейлон, нитроцеллюлоза, ацетат целлюлозы, стекловолокно и другие пористые полимеры нашли применение в качестве твердых подложек.
Настоящее изобретение также относится к диагностическому набору для обнаружения белка тау в биологическом образце, содержащему состав, раскрытый выше. Кроме того, настоящее изобретение относится к указанному диагностическому набору, который в дополнение к составу, раскрытому выше, также содержит реактив для обнаружения, раскрытый выше. Термин «диагностический набор» в общем обозначает любой диагностический набор, известный в данной области. Более конкретно, данный термин обозначает диагностический набор, как описано в Zrein с соавт. (1998).
Еще одним объектом настоящего изобретения являются новые иммунозонды и аналитические наборы для обнаружения и диагностики связанных с белком тау заболеваний и состояний, содержащие связывающиеся пептиды по настоящему изобретению. В случае иммунозондов, связывающиеся пептиды прямо или косвенно присоединяются к подходящей репортерной молекуле, например, ферменту или радионуклиду. Аналитический набор содержит контейнер, содержащий один или больше связывающихся пептидов по настоящему изобретению, и инструкции по применения связывающихся пептидов для связывания с антигеном тау, с образованием иммунологического комплекса, и обнаружения образования иммунологического комплекса, таким образом, что присутствие или отсутствие иммунологического комплекса коррелирует с присутствием или отсутствием белка тау.
ПРИМЕРЫ
ПРИМЕР 1: Генерация и скрининг гибридом и антител
Задача данного исследования состояла в генерации и скрининге анти-Тау mAb (моноклональные антитела). Гибридомы генерировали слиянием иммунизированных вакциной тау клеток селезенки мыши с линией клеток миеломы. Гибридомы оценивали на предмет реактивности против фосфорилированного и нефосфорилированного полноразмерного белка Тау, а также фосфорилированных и нефосфорилированных антигенных пептидов Тау, используемых для получения вакцины. Скрининг гибридомы также проводили на предмет реактивности супернатанта гибридом с тау сплетениями, с применением иммуногистохимии на срезах мозга мышей с трансгенным Тау.
1.1 Методы
1.1.1 Слияние
Мышь C57BL/6 дикого типа, иммунизированную ACI-35 (Тау393-408 [р8396, pS404]), использовалась для получения гибридомы. Мыши вводили бустерную дозу вакцины ACI-35 на 0-й день, затем на 4-й день, и слияние осуществляли на 7-й день.
Осуществляли слияние 6×107 (ACI-35) спленоцитов от иммунизированной мыши с 2×107 клеток миеломы SP2-O-Ag14 в соотношении 3 спленоцита/1 клетка миеломы.
Слияние давало 8×96-луночных планшетов, и клонам были присвоены названия в соответствии с планшетом (1-8), затем рядом (A-G), и, наконец, колонкой (1-12).
1.1.2 Способ скрининга для отбора клонов
Сначала дважды проводили скрининг 8×96-луночных планшетов на предмет экспрессии IgG. Затем положительные, экспрессирующие клоны переносили на 24-луночные планшеты, и клеточные супернатанты (=клоны) культивируемых клеток анализировали скринингом ТИФА Тау и иммуногистохимическим скринингом TAUPIR. Супернатанты, которые продемонстрировали положительный результат в анализе ТИФА и/или TAUPIR, переносили в колбы Т25, и снова проводили скрининг клонов на предмет экспрессии IgG методом скрининга ТИФА Тау и скрининга TAUPIR.
1.1.3 Скрининг IgG
Планшеты ТИФА (Costar; Sigma) покрывали 50 мкл/лунку анти-мышиного IgG антитела (AbD Serotec, Дюссельдорф, Германия) в буфере покрытия в течение 16 час при 4°С. После промывания планшетов ФБР/Твин, лунки блокировали 100 мкл/лунку блокирующего раствора в течение 1 час при температуре окружающей среды. Неразведенные супернатанты гибридомы (50 мкл на лунку) инкубировали в течение 1 час при температуре окружающей среды. После промывания, смесь анти-мышиного IgG1, IgG2a, IgG2b, IgG3 или IgM, конъюгированного с пероксидазой хрена (ПХ) (AbD Serotec) добавляли на 1 час при температуре окружающей среды. После окончательного промывания, выполняли обнаружение с помощью субстрата ПХ (ТМБ; 3-3',5,5'-тетраметилбензидин), и планшеты считывали на длине волны 405 нм с помощью устройства для считывания микропланшетов. Результаты выражали как оптическую плотность (O.D.).
1.1.4 Скрининг гибридом ТИФА Тау
Скрининг гибридом ТИФА выполняли на пептиде pTau (ACI-35, T3.5: Тау393-408 [pS396/pS404; PolyPeptide Laboratories, Хиллеред, Дания), соответствующем нефосфорилированном пептиде Тау (Т3.6: Тау393-408, PolyPeptide Laboratories), полноразмерном фосфорилированном белке (441аа) Тау (белок pTau, Vandebroek с соавт., 2005) и полноразмерном (441аа) белке Тау (белок Тау, SignalChem, Ричмонд, Канада). И, наконец, альбумин телячьей сыворотки (АТС) применяли в качестве отрицательного контроля.
Планшеты покрывали 10 мкг/мл соответствующего пептида Тау и 1 мкг/мл соответствующего белка Тау на протяжении ночи при 4°С. После промывания каждой лунки ФБР-0,05% Твина 20 и блокирования 1% АТС в ФБР-0,05% Твина 20, неразбавленный супернатант гибридомы или отрицательный контроль добавляли на планшеты и инкубировали при 37°С в течение 2 час. После промывания планшеты инкубировали с конъюгированным со щелочной фосфатазой (ЩФ) общим антимышиным IgG антителом (Jackson Laboratories, Балтимор, Филадельфия, США) в течение 2 час при 37°С. После промывания планшеты инкубировали с пНФФ (п-нитро-фенилфосфат), субстратом ЩФ, и считывали на длине волны 405 нм с помощью устройства для считывания планшетов ТИФА. Результаты выражали как O.D. (оптическая плотность).
1.1.5 Скрининг гибридом ИГА: связывание анти-Тау антител со сплетениями в секциях мозга трансгенных мышей (TAUPIR)
Эксперименты TAUPIR проводили согласно протоколу из Примера 3.1.2.
1.1.6 Скрининг IgG в колбах Т25
Планшеты ТИФА покрывали 5 мкг/мл анти-мышиного IgG антитела, специфичного в отношении фрагмента F(ab')2 (Jackson Laboratories, Балтимор, Филадельфия, США) в карбонатно-бикарбонатном буфере покрытия, рН 9,6 (Sigma, Букс, Швейцария) на протяжении ночи при 4°С. После промывания планшетов, неразведенный супернатант гибридомы, положительный контроль антитело IgG1 (6E10 в концентрации 1 мкг/мл: Covance, Эмеривилль, Калифорния, США) или отрицательный контроль (только среда культивирования) инкубировали в течение 1 час при комнатной температуре. После стадии промывания, вторичное козье антимышиное антитело IgG (подклассы 1+2а+2b+3), специфичное в отношении фрагмента Fey, конъюгированное с ЩФ (Jackson Laboratories, Балтимор, Филадельфия, США) инкубировали на планшетах в течение 2 час при 37°С. После завершающего промывания, проводили обнаружение с использованием пНФФ (п-нитро-фенилфосфат), субстрата ЩФ, и планшеты считывали на длине волны 405 нм с помощью устройства для считывания планшетов ТИФА. Результаты выражали как O.D. (оптическая плотность).
1.2 Результаты
Был проведен скрининг супернатантов клеток с 8×96-луночных планшетов, полученных в результате слияния, на предмет выработки IgG. Из 768 проанализированных лунок (8×96 лунок), 48 лунок с положительным результатом были отобраны на основании наилучших результатов связывания с фосфо-пептидом вакцины и полноразмерным фосфо-Тау. Селекция основывалась на связывании с пептидом и полноразмерным белком фосфо-Тау по данным ТИФА, а также на селективности по сравнению с не-фосфо-пептидом и полноразмерным не-фосфо-белком Тау. 24 отобранные гибридомы субклонировали путем высевания по 2 планшета на гибридому в количестве 1 клетка/лунку и 1 планшет в количестве 0,5 клетки/лунку. Супернатанты повторно анализировали на предмет связывания с фосфо-пептидом и фосфо-белком, чтобы верифицировать профиль связывания, после чего стабильность оценивали в 6-недельной культуре. Далее были отобраны 8 стабильных клонов и проанализирован их изотип и связывание с применением ТИФА и TAUPIR, как описано в Методах.
1.3. Заключение
Генерируемые антитела продемонстрировали высокую специфичность в отношении пептидов pTau, при пограничном связывании с нефосфорилированными пептидами.
Всего 8 клонов были отобраны для дальнейшего субклонирования и секвенированы (см. Табл. 6 и Табл. 7), и 6 клонов были депонированы в DSMZ (см. Табл. 10).
Положительные материнские клоны, упомянутые выше, дополнительно культивировали на 96-луночных планшетах, затем 24-луночных планшетах и, наконец, в колбах Т25. На каждой стадии, проводили скрининг супернатантов клонов гибридомы методами ТИФА, TAUPIR и Вестерн-блоттинга.
ПРИМЕР 2: Клонирование вариабельных участков легкой цепи и тяжелой цепи антител
Гены вариабельного участка тяжелой и легкой цепей антитела из клеток гибридомы клонировали, ДНК секвенировали, и определяли расположение определяющих комплементарность участков (CDR), а также характеристики связывания антител.
Общую РНК получали из 3×106 клеток гибридомы (1 флакон), с использованием мининабора Qiagen RNeasy (кат. №74104). РНК элюировали 50 мкл воды и тестировали на 1,2% геле агарозы.
кДНК VH и VK получали с использованием обратной транскриптазы с IgG и праймерами константного участка каппа. Первую цепь кДНК амплифицировали с помощью ПЦР, с применением большого набора праймеров сигнальной последовательности. Амплифицированную ДНК очищали на геле и клонировали в вектор pGem® Т Easy (Promega). Проводили скрининг полученных клонов VH и VK на предмет вставок ожидаемого размера. Последовательность ДНК отобранных клонов определяли в обоих направлениях путем автоматизированного секвенирования ДНК. Расположение определяющих комплементарность участков (CDR) в последовательностях определяли со ссылкой на другие последовательности антител (Kabat EA et al., 1991).
ПРИМЕР 3: Исследование связывания I
Задача состояла в измерении связывания фосфо-Тау (pTau) антител, сгенерированных субклонированными гибридомами, которые были получены от мышей, иммунизированных липосомальными вакцинами тау. Для данного исследования применяли твердофазный иммуноферментный анализ (ТИФА), чтобы измерить связывание очищенных антител с фосфорилированным и нефосфорилированным полноразмерным белком Тау, а также с фосфорилированными и нефосфорилированными антигенными пептидами Тау, которые используются для получения липосомальной вакцины.
Скрининг завершали двумя другими способами. Проводили иммуногистохимический анализ (ИГА) на срезах мозга трансгенного животного Тау (TAUPIR) с применением анти-тау антитела в качестве первичного антитела. Дополнительно, проводили Вестерн-блоттинг (ВБ) на гомогенате белков мозга мышей с трансгенным Тау, с применением анти-тау антитела в качестве блоттинг-антитела.
3.1 Методы
3.1.1. ТИФА: анализ связывания с фосфо-Тау
Для исследования связывания очищенных антител с Тау и pTau применяли анализ ТИФА. Если коротко, 96-луночные планшеты Nunc MaxiSorp (Nunc, Роскилле, Дания) покрывали 1 мкг/мл полноразмерного (441 аа) белка Тау (SignalChem, Ричмонд, Канада) или полноразмерного (441 аа) фосфорилированного белка Тау (Vandebroek с соавт., 2005). Дополнительно, планшеты покрывали 10 мкг/мл пептида полученной вакцины Тау, Тау393-408 (фосфорилированный в положениях S396 и S404 или нефосфорилированный). Для проверки на перекрестную реактивность с Тау и последовательностями pTau различных эпитопов pTau, которые не применялись для получения вакцины, планшеты покрывали 10 мкг/мл следующих пептидов: Тау393-408 (фосфорилированный или нефосфорилированный в положениях S396 и S404), Покрытие осуществляли на протяжении ночи в фосфатном буферном растворе (ФБР) при 4°С. Планшеты тщательно промывали 0,05% Твина 20/ФБР, а затем блокировали 1% альбумином телячьей сыворотки (АТС) сыворотки в 0,05% Твин 20/ФБР в течение 1 час при 37°С. Затем добавляли исследуемое антитело в сериях по 8 или 16 двукратных разведении в интервале от 20 до 0 мкг/мл, и инкубировали в течение 2 час при 37°С. Далее планшеты промывали, как было описано выше, и добавляли конъюгированное с ЩФ вторичное анти-мышиное антитело IgG (Jackson ImmunoResearch Laboratories, Суффолк, Великобритания) в разведении 1:6000 в 0,05% Твина 20/ФБР в течение 2 час при 37°С. После промывания, планшеты инкубировали с раствором субстрата фосфатазы п-нитрофенилфосфат динатрия гексагидрата (пНФФ; Sigma-Aldrich, Букс, Швейцария), и считывали на длине волны 405 нм после периода инкубации 30 минут, 1, 2 или 16 часов, с помощью устройства для считывания планшетов ТИФА.
3.1.2. TAUPIR и Вестерн-блоттинг: связывание анти-Тау антитела в Тау сплетениях в срезах мозга трансгенного животного Тау (TAUPIR)
Для окрашивания TAUPIR получали срезы мозга мышей TPLH (трансгенные мыши, экспрессирующие самую длинную изоформу (441аа) hTayP301L), старых (возраст >18 недель) мышей с двойным трансгенным biGT (трансгенные мыши GSK-3β, скрещенные с TPLH) и мышей с двойным трансгенным biAT (трансгенные мыши hAPPV717I, скрещенные с TPLH). В качестве отрицательного контроля, использовали срезы мышей с инактивированным Тау (ТКО; возраст 6 месяцев). Срезы мозга промывали в течение 5 минут ФБР, затем инкубировали в течение 15 минут при комнатной температуре в смеси ФБР/МеОН (1:1, 1,5% H2O2), чтобы блокировать активность эндогенной пероксидазы. После троекратного промывания срезов ФБРТ (ФБР/0,1% Тритона X100) их инкубировали в течение 30 минут при комнатной температуре в блокирующем растворе - ФБРТ, содержащем 10% СТЭ (сыворотка телячьего эмбриона). Инкубацию с исследуемым анти-Тау антителом проводили в течение ночи при 4°С, с использованием следующих концентраций антитела: ACI-35-2А1-Ab1 в концентрации 0,0053 мкг/мл, ACI-35-2А1-Ab2 в концентрации 0,0048 мкг/мл, ACI-35-4А6-Ab1 в концентрации 0,015 мкг/мл, ACI-35-1D2-Ab1 в концентрации 0,0047 мкг/мл, ACI-35-2G5-AM в концентрации 0,0055 мкг/мл, ACI-35-2G5-Ab2 и ACI-35-2G5-Ab3 в концентрации 0,01 мкг/мл в ФБРТ/10% СТЭ. Далее срезы трижды промывали ФБРТ перед инкубацией с конъюгированным с ПХ вторичным козьим анти-мышиным антителом (приобретено у Dako, Глоструп, Дания) в ФБРТ/10% СТЭ в течение 1 часа при комнатной температуре. Перед обнаружением, срезы трижды промывали ФБРТ и инкубировали в 50 мМ Трис/HCl, рН 7,6 в течение 5 минут. Обнаружение проводили, инкубируя срезы в течение 3 минут в диаминобензидине (ДАБ: 1 таблетка в 10 мл 50 мМ Трис.HCl + 3 мкл 30% H2O2; MP Biomedicals, Solon, Огайо, США). Реакцию останавливали троекратным промыванием срезов ФБРТ. Далее срезы переносили на силанизированные стеклянные планшеты и сушили в потоке воздуха на теплой плите при температуре 50°С в течение 2 часов. Контрастное окрашивание осуществляли путем инкубации с гематоксилином Майера (Fluka Chemie, Букс, Швейцария) в течение 1 минуты, с последующей стадией промывания проточной водой в течение 4 минут. Срезы обезвоживали погружением в баню с 50%, 70%, 90% этанолом и дважды в 100% этанол, затем дважды в ксилол на 1 минуту. В конце, срезы фиксировали для визуализации с помощью DePeX (BDH Chemicals Ltd., Пул, Великобритания) под стеклянными покровными стеклами.
Дополнительное окрашивание (Вестерн-блоттинг) проводили методом SDS-PAGE (10%) на отдельных гомогенатах белков мозга мышей дикого типа (FVB), мышей с трансгенным Тау (TPLH и biGT) или мышей с инактивированным Тау (ТКО). Для Вестерн-блоттинга использовались антитела в следующих концентрациях: ACI-35-2А1-Ab1 в концентрации 0,53 мкг/мл, ACI-35-2А1-Ab2 в концентрации 0,48 мкг/мл, ACI-35-4А6-Ab1 в концентрации 0,5 мкг/мл, ACI-35-1D2-Ab1 в концентрации 0,47 мкг/мл, ACI-35-2G5-Ab1 в концентрации 0,55 мкг/мл, ACI-35-2G5-Ab2 в концентрации 0,33 мкг/мл и ACI-35-2G5-Ab3 в концентрации 0,5 мкг/мл.
3.2 Результаты
Антитела ACI-35-2А1-Ab1, ACI-35-2A1-Ab2, ACI-35-1D2-Ab1, ACI-35-2G5-Ab2 и ACI-35-2G5-Ab3 продемонстрировали высокую активность связывания и специфичность в отношении фосфорилированного человеческого белка Тау (Табл. 2), более конкретно, антигенного пептида фосфо-Тау, используемого в соответствующей вакцине. Не наблюдалось перекрестной реактивности с нефосфорилированным Тау или с другими фосфорилированными и нефосфорилированными пептидами, полученными из Тау. Антитело ACI-35-4А6-Ab1, как и при отборе, продемонстрировало высокую активность связывания только с антигенным фосфо-Тау пептидом, используемым для получения вакцины. Низкая перекрестная реактивность была обнаружена в отношении не-фосфо-двойника антигенного пептида, используемого для получения вакцины, как и ожидалось на основании селекции клона. Антитело ACI-35-2G5-Ab1 продемонстрировало высокую активность связывания только с антигенным фосфо-Тау пептидом, используемым для получения вакцины. Слабая перекрестная реактивность наблюдалась в отношении фосфо-пептида Т4.5, содержащего часть антигенной последовательности пептида, используемого в вакцине.
TAUPIR и ВБ применяли с целью анализа связывания с Тау сплетениями в мозге мышей с поздними стадиями таупатии (biGT>18 месяцев) и полноразмерным Тау в денатурированных гомогенатах, полученных от указанных мышей. Различные участки мозга были проанализированы: кора и СА1, СА3 и часть зубчатой фасции (ЗФ) гиппокампа. Антитела ACI-35-2А1-Ab1 и ACI-35-2A1-Ab2 продемонстрировали лучшие результаты в анализе TAUPIR с плотным окрашиванием цитоплазмы и прозрачными нейропильными нитями, особенно в участках СА1 и СА3 гиппокампа. Антитело ACI-35-4А6-Ab1 продемонстрировало отрицательный результат в анализе TAUPIR, со слабым спорадическим окрашиванием сходных со сплетениями структур. Антитело ACI-35-1D2-Ab1 продемонстрировало эффективное цитоплазматическое окрашивание TAUPIR, с нейропильнми нитями на участке СА1. Антитело ACI-35-2G5-Ab1 продемонстрировало отрицательные результаты в анализе TAUPIR с окрашиванием ядер, и только слабое окрашивание сплетений. И, наконец, антитела ACI-35-2G5-Ab2 и ACI-35-2G5-Ab3 продемонстрировали сходные положительные результаты в анализе TAUPIR с окрашиванием цитоплазмы и нейропильными нитями, наблюдаемыми в СА1 и СА3 гиппокампа. Рейтинг качества окрашивания показан знаками «+» или «-» в Табл. 2. Гомогенаты мозга мышей с трансгенным Тау анализировали блоттингом, демонстрируя, что все антитела надлежащим образом связывались с ожидаемыми полосами Тау (Табл. 2, рейтинг «+»), причем ACI-35-1D2-Ab1 и ACI-35-2G5-Ab1 также продемонстрировали дополнительное неспецифическое связывание («-/+»).
ПРИМЕР 4: Исследование связывания II
4,1 Методы
4.1.1 Анализ связывания методом резонанса поверхностного плазмона (РПП)
Все эксперименты РПП проводили на приборе Biacore X (Healthcare GE). Сенсорный чип SA (дериватизированный стрептавидином карбоксиметилдекстран) приобретали у Healthcare GE. Буфер анализа представлял собой ФБР (ФБР Дульбекко, Sigma D8537). Нековалентно связанный стрептавидин вначале удаляли с сенсорной поверхности путем инъекции 8 импульсов (каждый ~1 мкл) 16 мМ NaOH (водн.). Далее пептид фосфо-тау солюбилизировали в ФБР для получения конечной концентрации пептида 1 мкМ, а затем инъекционно вводили (35 мкл) над проточной кюветой (пк) 2 сенсорного чипа со скоростью 5 мкл/мин. После сочетания был достигнут конечный уровень иммобилизации 130ЕР. Для изучения связывания антител с поверхностью чипа, несколько концентраций антител были приготовлены путем двукратного серийного разведения в буфере анализа. Инъекции осуществляли над пк 1 и 2 со скоростью потока 50 мкл/мин в течение 120 с.Проточная кювета 1 не была дериватизированной, и ответ пк 1 вычитали из пк 2 для коррекции с учетом шума прибора и массового изменения преломления. После каждой инъекции, поверхности немедленно промывали буфером анализа в течение 100 с. Для удаления любого остатка связанного антитела с чипа, выполняли регенерацию поверхности путем инъекции 1 мкл 10 мМ глицина-HCl, рН 1,7. Кинетические анализы выполняли, применяя алгоритмы цифровой интеграции и глобального анализа, с помощью BIAevaluation 3.0. Сенсограммы, полученные для инъекций антитела в различных концентрациях, накладывали, и осуществляли коррекцию начальных значений до нуля. Для аппроксимации кривой, все данные одновременно аппроксимировали к однородной модели 1:1 (Ленгмюра).
Используемые пептиды
4,2 Результаты
Связывание анти-тау антител с фосфорилированным пептидом Тау контролировали в реальном времени с использованием РПП. Анализы фаз ассоциации и диссоциации связывания антитела могут применяться для определения константы скорости ассоциации (ka), константы скорости диссоциации (kd), а также константы диссоциации KD.
Все антитела продемонстрировали специфичное связывание с пептидом Т3.30 над недериватизированной карбоксиметилдекстрановой поверхностью в интервале 46-+734 нМ исследуемого антитела (или 11,5→184 нМ для ACI-35-4А6-Ab1). Кинетические анализы сенсограмм определили константу диссоциации KD для взаимодействия связывания между различными антителами и Т3.30 в интервале от 2 до 82 нМ. Таким образом, результаты анализа демонстрируют, что антитела распознают фосфопептид Т3.30 с очень высокой аффинностью (Табл. 3).
ПРИМЕР 5: Исследование связывания III методом ТИФА на образцах мозга человека (ТИФА для обнаружения мультимеров фосфорилированного Тау)
5.1 Методы
5.1.1. Образцы тканей человека: подготовка образцов мозга человека, используемых в анализах, раскрытых в настоящем изобретении
Посмертные образцы височной области коры 10 больных болезнью Альцгеймера (БА) и 10 контрольных субъектов такого же возраста были получены из Банка образцов мозга Университета Майами. Средний возраст смерти для больных БА (7 женщин, 3 мужчин) составил 81,1±7,3 года и для контрольных субъектов (отсутствие неврологических симптомов; 9 женщин, 1 мужчина) составил 87,0±5,8 (незначимое отличие от больных БА согласно t-критерию Стьюдента). Все субъекты были кавказского происхождения. Образцы БА были охарактеризованы на предмет стадии заболевания по Braak (Braak and Braak (1991) Neuropathological stageing of Alzheimer-related changes. Acta Neuropathol 82:239-259), как показано в Табл. 4.
Посмертные образцы височной области коры 10 больных БА и 10 контрольных субъектов были гомогенизированы согласно следующему протоколу. Фрагменты мозга взвешивали и гомогенизировали в 9 объемах 25 мМ Трис-HCl, рН 7,4, 150 мМ NaCl, 1 мМ ЭДТА, 1 мМ ЭГТА, содержащего ингибиторы фосфатаз (30 мМ NaF, 0,2 мМ Na3VO4, 1 нМ окадаиковой кислоты, 1 мМ фенилметилсульфонилфторида (ФМСФ), 5 мМ Na4P2O7) и ингибиторы протеаз (Complete Mini; Roche, Швейцария). Гомогенизацию проводили на льду, с помощью стеклянного гомогенизатора. Получали фракцию полного гомогената (ОГ). Концентрацию белка измеряли с помощью реактива Bradford (Sigma).
5.1.2. Условия 1 ТИФА: условия 1 анализа ТИФА для обнаружения присутствия мультимеров фосфорилированного Тау в посмертных гомогенатах коры мозга человека, полученных от пораженных БА индивидуумов и контрольных субъектов соответствующего возраста
Многоярусные 96-луночные планшеты покрывали антителами на протяжении ночи при 4°С в концентрации 5 мкг/мл в карбонатном/бикарбонатном буфере. После 4-хкратного промывания ФБР/Твин, планшеты насыщали ФБР/Твин, содержащим 10% АТС, в течение 1 часа при 37°С. Затем гомогенаты мозга помещали в лунки в концентрации 100 нг/мкл в 50 мкл ФБР, и инкубировали в течение 2 часов при 37°С. После промывания планшеты инкубировали с таким же антителом, которое использовали для покрытия, но биотинилированным, в течение 1 часа при 37°С при конечной концентрации 5 мкг/мл. Планшеты промывали, и, после добавления авидин-пероксидазы (набор Vectastain ABC, Vector Laboratories) и ее субстрата (ABTS, Roche 10881420), планшеты считывали в различных точках времени. Значения выражены как среднее значение OD ± стандартное отклонение для 10 больных БА и 10 контрольных субъектов.
5.2 Результаты
Антитела ACI-35-2А1-Ab1 и ACI-35-2G5-Ab3 изучали на предмет способности обнаруживать мультимеры фосфо-Тау (pTau) в гомогенатах мозга, полученных от больных БА и контрольных субъектов, с использованием фосфо- и мультимер-специфичных Условий 1 ТИФА. Мы наблюдали высокую степень значимости различий (р<0,001) между БА и контрольными субъектами соответствующего возраста (n=10) в данном испытании для обоих антител (Фиг. 1). С использованием посмертных гомогенатов коры мозга больных БА и контрольных образцов мозга субъектов соответствующего возраста, мы продемонстрировали способность антител ACI-35-2A1-Ab1 и ACI-35-2G5-Ab3 анти-pTau обнаруживать мультимеры Tay-pS396 в посмертных человеческих образцах мозга.
ПРИМЕР 6: Исследование Связывания IV - Вестерн-блоттинг на образцах мозга человека.
6.1 Методы
6.1.1. Образцы мозга человека: Способ подготовки образцов тканей человека такой же, как описано в Способе 5.1.1.
6.1.2. Вестерн-блоттинг: Анализ методом Вестерн-блоттинга для обнаружения присутствия фосфорилированного Тау в посмертных гомогенатах коры мозга человека, полученных от пораженных БА индивидуумов и контрольных субъектов соответствующего возраста
Антитела против Тау человека, применяемые в данном исследовали, представляли собой мышиные ACI-35-2A1-Ab1, ACI-35-1D2-Ab1, и ACI-35-2G5-Ab3, все направлены против Tay-pS396. Мышиное моноклональное антитело TAU-13 (Abeam ab24636), направленное против общего Тау человека, и кроличье моноклональное антитело Е178, направленное против Tay-pS396 (Abeam ab32057), применяли в качестве контроля. По 20 мкг каждого из полных гомогенатов наносили на дорожку сборного 10% Бис-Трис полиакриламидного геля (Nupage Novex 10% Bis-TRIS Midi Gel, Invitrogen). Белки разделяли согласно рекомендациям производителя в буфере анализа NuPAGE 3-М-морфолинпропансульфоновая кислота/натрия додецилсульфат (Invitrogen NP0001). Блоттинг белка осуществляли в течение 3 час в буфере, содержащем 25 мМ Трис, рН 8,6, 190 мМ глицина, 20% метанола, на льду на ПВДФ мембранах (Immobilon-FL, Millipore IPFL00010). Мембраны блокировали в течение 1 час в блокирующем буфере Licor (Odyssey), разбавленном ФБР в соотношении 1:3. Мембраны инкубировали на протяжении ночи с первичными антителами в следующих концентрациях: TAU-13 в концентрации 0,6 мкг/мл, Е178 в разведении 1:5000, ACI-35-2А1-Ab1 в концентрации 0,53 мкг/мл, ACI-35-1D2-Ab1 в концентрации 0,47 мкг/мл, и ACI-35-2G5-Ab3 в концентрации 0,5 мкг/мл, разведенное в соотношении 1:3 буфером Licor и 2:3 ФБР, содержащим 0,1% Твина-20 (ФБР-Т). После 4-хкратного промывания ФБРТ, мембраны инкубировали с козьим анти-мышиным антителом, конъюгированным с красителем LICOR 800 (козье анти-мышиное IRDye 800 CW, Odyssay), в течение 1 час при комнатной температуре, снова промывали 4 раза ФБРТ, и сканировали для воспроизведения изображения с использованием системы LICOR.
6.2 Результаты
Антитела ACI-35-2А1-Ab1, ACI-35-1D2-AM и ACI-35-2G5-Ab3 были исследованы на предмет способности обнаруживать фосфо-Тау (pTau) в гомогенатах мозга больных БА и контрольных субъектов, с применением фосфо-специфичных Вестерн-блотов. Все посмертные образцы коры мозга человека сначала характеризовали с помощью коммерческих антител против человеческого Тау: антитело против общего Тау (TAU-13) и анти-р8396 Тау антитело (Е178). Как показано на Фиг. 2А, с помощью антитела TAU-13 мы обнаружили во всех образцах характерную лесенку Тау, соответствующую различным изоформам Тау в интервале 50-70 кДа. Интересно, что в гомогенатах мозга больных БА мы также наблюдали относительный сдвиг характера миграции Тау, как ожидалось в присутствии гиперфосфорилированного Тау в мозге больных БА. В подтверждение данной гипотезы, коммерческие анти-р8396 Тау антитела очень эффективно различали контрольных субъектов и больных БА (Фиг. 2В). Действительно, анти-р8396 Тау антитело выявило три основных иммунореактивных полосы, соответствующих (гипер)-фосфорилированным изоформам Тау в полных гомогенатах мозга больных БА, с очень слабой интенсивностью или отсутствующие у здоровых контрольных субъектов. Кроме того, образцы больных БА продемонстрировали высокомолекулярное иммунореактивное пятно TAU-13, вероятно отображающее присутствие агрегированного Тау (Фиг. 2А).
Вестерн-блоттинг с использованием ACI-35-2А1-Ab1 выявил присутствие двух иммунореактивных полос белка ожидаемого размера для фосфо-Тау в гомогенатах мозга больных БА, но не контрольных субъектов (Фиг. 3А). Слабая иммунореактивность Вестерн-блота с применением ACI-35-2А1-Ab1 может быть объяснена присутствием двух основных неспецифичных полос ~35 и ~40 кДа. Вестерн-блоттинг с применением ACI-35-1D2-Ab1 обнаружил присутствие двух иммунореактивных полос белка ожидаемого размера для фосфо-Тау в гомогенатах мозга больных БА, но не контрольных субъектов (Фиг. 3В). Слабая иммунореактивность Вестерн-блота с применением ACI-35-1D2-Ab1 может быть объяснена присутствием неспецифичных полос ~40 и ~50 кДа, а также 4 неспецифичных полос в интервале от 80 кДа до 150кДа. Вестерн-блоттинг с использованием ACI-2G5-Ab3 обнаружил присутствие трех основных иммунореактивных групп, соответствующих изоформам (гипер)-фосфорилированного Тау в полных гомогенатах мозга больных БА, отсутствующих у здоровых контрольных субъектов, за исключением одного контрольного субъекта (С22) с семейным анамнезом БА (Фиг. 3С). Данный отчет демонстрирует, что ACI-35-2А1-Ab1, ACI-35-1D2-Ab1, и ACI-35-2G5-Ab3 могут различать образцы больных БА и контрольных субъектов соответствующего возраста на предмет присутствия pS396 Тау в коре человека посмертно, и, таким образом, указанные моноклональные антитела распознают связанные с БА патологические изоформы Тау.
ПРИМЕР 7: Исследование связывания V - Условия 1 (ТИФА на образцах мозга человека)
7.1 Методы
7.1.1. Образцы мозга человека. Способ подготовки образцов мозга человека такой же, как описано в Способе 5.1.1, за исключением последней стадии, получения фракции S1.
7.7.2. Фракция белка Тау S1: Субфракционирование фракции полного гомогената для получения растворимых белков Тау и фосфо-Тау.
Для получения растворимой фракции Тау (S1), используемой в анализе AlphaLISA, половину объема фракции ОГ разделили на аликвоты и хранили при -80°С. Остаток фракции ОГ дополнительно обрабатывали путем добавления Тритона Х-100 до конечной концентрации 0,4%. Образцы тщательно перемешивали и несколько раз обрабатывали вихревым перемешиванием, после чего центрифугировали со скоростью 5000 об/мин в течение 5 минут при 4°С. Супернатант составляет фракцию S1. Образцы разделили на аликвоты и хранили при -80°С. Концентрацию белка измеряли с помощью реактива Bradford.
7.1.3. AlphaLISA: Анализ AlphaLISA для обнаружения присутствия фосфорилированного Тау в посмертных гомогенатах коры мозга человека, полученных от пораженных БА индивидуумов и контрольных субъектов соответствующего возраста.
Антитела ACI-35-2А1-Ab1, ACI-35-1D2-Ab1 и ACI-35-2G5-Ab3, все направленные против Tay-pS396, биотинилировали с использованием EZ-Link Micro Sulfo-NHS-LC-Biotinylation Kit (Thermo Scientific), согласно инструкциям производителя. 20-кратный молярный избыток биотина по сравнению с антителом использовали в реакции введения метки. После биотинилирования, избыток свободного биотина удаляли диализом против ФБР с помощью S1ide-A-Lyzer MINI Dia1ysis Devices, 10K MWCO (Thermo Scientific). Биотинилированные антитела обозначены как ACI-35-2А1-Ab1-ВТ, ACI-35-1D2-Ab1-BT и ACI-35-2G5-Ab3-BT. Антитело Tau-13 конъюгируют с активированными гранулами Альфа Акцептора (Perkin Elmer), согласно следующему протоколу: раствор 0,1 мг антитела Tau-13 (очищенный на колонке Белка А) смешивали с 1 мг гранул Акцептора AlphaLISA и добавляли 0,13 М фосфатный буфер (рН 8,0) до конечного объема реакции 200 мкл. Далее, добавляли 1,25 мкл 10% Твина-20 и 10 мкл 25 мг/мл раствора NaBH3CN, и пробирку инкубировали в течение 48 часов при 37°С с легким вращением (7 об/мин). После реакции сочетания, активные сайты на гранулах блокируют добавлением 10 мкл раствора карбокси-метоксиламина, и дополнительно инкубировали при 37°С в течение 1 часа. В конце, гранулы дважды промывали по 200 мкл 0,1 М Трис-HCl (рН 8,0) и хранили при 4°С в 200 мкл буфера для хранения (ФБР, содержащий 0,05% Проклина-300), что давало конечную концентрацию гранул Акцептора AlphaLISA 5 мг/мл.
AlphaLISA представляет собой гомогенный анализ, основанный на бесконтактной хемилюминесценции гранул. Если гранулы Альфа Донора и Акцептора находятся в непосредственной близости, при возбуждении лазером, каскад химических реакций генерирует усиленный сигнал. При возбуждении на длине волны 680 нм, фотосенсибилизатор, содержащийся в гранулах Донора, превращает кислород окружающей среды в более реакционноспособные атомарные формы кислорода. Такие атомарные формы диффундируют (до 200 нм, в пределах периода полураспада 4 мс) и вызывают хемилюминесцентную реакцию в гранулах Акцептора, приводящую к эмиссии света. Условия анализа были такими, как указано ниже.
Образцы S1 предварительно разбавляли буфером анализа Альфа (Perkin Elmer AL000C) до получения концентрации 20 мкг/мл. Следующие реактивы добавляли на 384-луночный белый OptiPlate (Perkin Elmer) до конечного объема 50 мкл: гомогенат мозга S1 (5 мкл), 10 мкл ACI-35-2А1-Ab1-ВТ, ACI-35-1D2-Ab1-BT или ACI-35-2G5-Ab3-BT до конечной концентрации антитела 0,2 нМ, 0,5 нМ или 0,5 нМ, соответственно, и 10 мкл конъюгата гранул Акцептора-Tau13 до конечной концентрации гранул 2,5 мкг/мл. Реакционную смесь инкубировали в течение 1 час при комнатной температуре, добавляли 25 мкл гранул Донора Стрептавидина, и дополнительно инкубировали в течение 2 часов при комнатной температуре в темноте. Считывание данных проводили с помощью прибора EnSpire Alpha, и анализировали с помощью EnSpire Workstation, версия 3.00. Статистический анализ данных выполняли с помощью программного обеспечения GraphPad Prism. Результаты представлены как единицы Альфа ± стандартное отклонение.
7.2 Результаты
Анализ AlphaLISA применяли для изучения способности антител ACI-35-2A1-Ab1, ACI-35-1D2-Ab1 и ACI-35-2G5-Ab3 обнаруживать Tay-pS396 в посмертных гомогенатах мозга человека и различать образцы больных БА и контрольных субъектов соответствующего возраста. Все антитела обнаруживали Tay-pS396 (Фиг. 4А, 4В, 4С). Разница в обнаружении сигнала между БА и контрольными субъектами (n=10) также была высоко значимой для всех антител, с демонстрацией усиленного сигнала для мозга больных БА; ACI-35-2A1-Ab1 (р<0,0001), ACI-35-1D2-Ab1 (р<0,0001) и ACI-35-2G5-Ab3 (р=0,002). В заключение, технология AlphaLISA применялась с целью демонстрации способности ACI-35-2А1-Ab1, ACI-35-1D2-Ab1 и ACI-35-2G5-Ab3 обнаруживать pS396-Tau в мозге субъекта БА и проводить дифференциацию между больными БА донорами и контрольными субъектами.
ПРИМЕР 8: Эффективность антитела ACI-35-2G5-Ab3 in vivo
8.1 Методы
8.1.1. Условия исследования: Влияние in vivo лечения путем введения 2-х доз анти-pTau антитела ACI-35-2G5-Ab3 трансгенным мышам Тау
Самкам и самцам мышей с трансгенным Тау (ТМНТ) с базовым генотипом C57BL/6×DBA в возрасте 6-7 месяцев вводили внутрибрюшинной инъекцией 3 или 10 мг/кг ACI-35-2G5-Ab3, или дважды вводили контрольный растворитель (ФБР), с интервалом 1 неделя. На 14-й день животных умерщвляли эвтаназией, мозг извлекали и обрабатывали иммуногистохимическим (ИГА) методом. Для определения патологии Тау в гиппокампе и миндалевидной железе осуществляли введение метки для 5 срезов (по 1 для каждого уровня) на мозг, с применением антител ATI 80 (для Тау-рТ231) и НТ7 (для общего Тау человека), и затем оценивали иммунореактивную область с помощью программного обеспечения Image Pro Plus (версия 6.2). Иммунореактивные объекты измеряли при условии превышения порогового ограничения (30 мкм в миндалевидной железе, 7 мкм2 в гиппокампе) и порога динамической интенсивности. Общая площадь и интенсивность объектов, а также индивидуальный порог устанавливались автоматически. Динамический порог, если он применялся, был определен как средняя интенсивность в пределах зоны интенсивности (ЗИ) плюс кратность фактора стандартного отклонения интенсивности пикселей в пределах ЗИ. Размер участка измеряли путем разграничения области гиппокампа и миндалевидной железы вручную. Данные области ИК ATI 80 и НТ7 были нормализованы к участку (в гиппокампе) или размеру ЗИ (в миндалевидной железе).
8.2 Результаты
Антитело AT 180 pTau обнаруживает эндогенный и человеческий pTau (дважды фосфорилированный при Thr231 и Ser235). Для мышей с трансгенным Тау, используемых в данном исследовании, гистологические измерения ATI 80 были сосредоточены на нейронах гиппокампа и миндалевидной железы. Мыши, получавшие ACI-35-2G5-Ab3, продемонстрировали значительное снижение средней интенсивности и интенсивности нормализованной суммы AT 180 соматического введения метки в миндалевидной железе и гиппокампе (Фиг. 5А и 5В), демонстрируя снижение общего соматического АТ180-положительного pTau у леченных мышей.
Для общего человеческого Тау (трансгенный) применяли антитело НТ7. НТ7 распознает нормальный человеческий Тау в интервале между остатками 159 и 163. Гистологические измерения были сосредоточены на иммунореактивных сомах нейронов гиппокампа и миндалевидной железы. У мышей, получавших ACI-35-2G5-Ab3, сокращалась иммунореактивная зона НТ7, а также уменьшалась суммарная и средняя интенсивность иммунореактивности НТ7 в миндалевидной железе (Фиг. 6А). В гиппокампе наблюдался такой же эффект для средней интенсивности (Фиг. 6В). Однако, наблюдалось повышение содержания метки НТ7 в иммунореактивной области и суммарной интенсивности в гиппокампе мышей, получавших дозу 10 мг/кг. Такое увеличение, наблюдаемое в гиппокампе, по большей части было результатом показателей 3 мышей из общего количества 8 мышей в исследовании.
Лечение ACI-35-2G5-Ab3 значительно снижало уровни иммунореактивного pTau AT180 в исследуемых участках и сомах нейронов гиппокампа и миндалевидной железы. В миндалевидной железе суммарная интенсивность метки была снижена для AT 180 иммунореактивного pTau и НТ7 иммунореактивного общего Тау человека. Лечение дозой 3 мг/кг также значительно снижало среднюю интенсивность НТ7 в обоих участках. Однако, при дозе 10 мг/кг средняя площадь иммунореактивной зоны НТ7 и суммарная интенсивность в гиппокампе увеличивались, по сравнению с контрольной группой мышей, наводя на мысль о том, что лечение ACI-35-2G5-Ab3 приводит к сдвигу от патологического pTau.
ПРИМЕР 9: Картирование эпитопа анти-pTau антител
9.1 Методы
Картирование эпитопа мышиных моноклональных анти-фосфо-Тау антител выполняли методом ТИФА с использованием различных библиотек фосфо- и не-фосфопептидов. Последовательности аминокислот используемой библиотеки пептидов ТЗ показаны в Табл. НА. Каждая библиотека состояла из коротких биотинилированных пептидов, содержащих фосфо- и не-фосфо-последовательности, присутствующие в пептидной вакцине. Дополнительно, генерировали библиотеку пептидов, заменяя каждый остаток последовательности пептида, которая связывается с антителом, аланином (Ala), как показано в Табл. 11В и 11С. Каждая библиотека состояла из коротких биотинилированных пептидов, содержащих фосфо- и не-фосфо-последовательности, присутствующие в пептидной вакцине. Библиотеки пептидов были приобретены у ANAWA Trading SA. Библиотеки пептидов были приобретены у ANAWA Trading SA. Картирование эпитопа осуществляли согласно инструкциям производителя (Mimotopes). Если коротко, покрытые стрептавидином планшеты (NUNC) блокировали 0,1% АТС в фосфатном буферном растворе (ФБР) на протяжении ночи при 4°С. После промывания ФБР/0,05% Твина 20, планшеты покрывали в течение 1 часа при комнатной температуре различными пептидами из каждой библиотеки, разведенными в ФБР, содержащем 0,1% АТС и 0,1% натрия азида, до конечной концентрации 10 мкМ. После промывания, планшеты инкубировали в течение 1 часа при комнатной температуре с исследуемым антителом, разведенным до 40 нг/мл ФБР, содержащим 2% АТС и 0,1% натрия азида. Планшеты снова промывали и инкубировали с вторичным анти-мышиным IgG антителом, конъюгированным со ЩФ (Jackson ImmunoResearch Laboratories, Суффолк, Великобритания) в разведении 1:6000 в течение 1 час при комнатной температуре. После завершающего промывания, планшеты инкубировали с раствором субстрата фосфатазы, п-нитрофенилфосфата динатрия гексагидрата (пНФФ; Sigma-Aldrich, Букс, Швейцария), и считывали на длине волны 405 нм после инкубации в течение 2 час, с помощью устройства для считывания планшетов ТИФА. Связывание считалось положительным, если оптическая плотность (O.D.) по меньшей мере в 2 раза превышала фоновое значение O.D.
9.2 Результаты
В результате экспериментов по картированию эпитопа, могут быть идентифицированы эпитопы, в том числе, необходимый фосфорилированный остаток аминокислоты (см. Табл. 5), с которым специфично связываются антитела, раскрытые в данном описании.
- Тауаа 393-401, с требованием р8396 (ACI-35-2А1-Ab1; ACI-35-2A1-Ab2)
- Тауаа 396-401, с требованием р8396 (ACI-35-4А6-Ab1)
- Тау аа 394-400, с требованием pS396 (ACI-35-1D2-Ab1)
- Тау аа 402-406, с требованием pS404 (ACI-35-2G5-Ab1)
- Тау аа 393-400, с требованием р396 (ACI-35-2G5-Ab2; ACI-35-2G5-Ab3)
ПРИМЕР 10: Фосфорилирование Тау в положении серина 396 (pS396) с применением GSK3β киназы и метода SDS-PAGE/Вестерн-блоттинга
10.1 Методы
Самую длинную изоформу человеческого полноразмерного Тау (TAU441; SignalChem) в конечной концентрации 16 мкМ (20 мкг Тау/25 мкл реакционной смеси) инкубировали с 0,018 Ед GSK-3β/пмоль Тау в буфере фосфорилирования, содержащем HEPES, рН 7,64 (40 мМ), ЭГТА (5 мМ), MgCl2 (3 мМ) и АТФ (2 мМ) в течение 1, 6 или 20 час при 4, 30 или 37°С. Одна единица GSK3R определена производителем (New England BioLabs) как количество фермента, которое будет переносить 1 пмоль фосфата с АТФ на фосфопептид CREB (KRREILSRRPpSYR) за 1 минуту при 30°С. Тау, фосфорилированный с помощью GSK3β (pTau-GSK3β), зондировали антителами, направленными против Тау, фосфорилированного в положениях серина 202, 396, 404, 409, треонина 181, 205 и 231, и общего Тау, анализ методом прямого ТИФА и Вестерн-блоттинга (ВБ), чтобы оптимизировать и верифицировать активность и специфичность киназы (данные не показаны). Дополнительно, пятна зондировали на предмет присутствия GSK3P с применением анти-CSK3α/β антитела (BioSource Invitrogen). Для всех ВБ, pTau-GSK3β разбавляли добавлением равного объема буфера А образца (125 мМ Трис-HCl, рН 6,8, 4% [масс/об] натрия додецилсульфата [НДС], 20% глицерина, 0,01% бромфенольного голубого, 5% β-меркаптоэтанола), и образцы нагревали до 95°С, выдерживая при этой температуре в течение 10 минут. 30 мкг образца наносили на 4-12% Бис-Трис гель (Invitrogen) и анализировали в буфере 3-N-морфолинпропансульфоновой кислоты/натрия додецилсульфата (Invitrogen). Белки переносили на ПВДФ мембрану с размером пор 0,45 мкм в буфере переноса (25 мМ Трис, рН 8,6, 190 мМ глицина, 20% метанола). Для верификации переноса белка, мембраны окрашивали понсо S в течение 5 минут. Далее мембраны промывали, а затем блокировали в течение 1 часа в блокирующем буфере (5% АТС в ТБР [50 мМ Трис-HCl, рН 7,6, 150 мМ NaCl]). Блоттинг мембран проводили на протяжении ночи при 4°С с первичными антителами в блокирующем буфере, содержащем 0,1% Твина. Блоттинг с ACI-35-2G5-Ab3 осуществляли при концентрации антитела 0,5 мкг/мл.
10.2 Результаты
Обработка Тау GSK3R приводила к высокой степени фосфорилирования серина 396 Тау (Tau-pS396), что подтверждено с применением антител, специфичных в отношении различных остатков фосфо-серина и -треонина Тау (данные не показаны). Фиг. 7 иллюстрирует SDS-PAGE для Tau-pS396, сегенерированного с применением различных условий GSK3β, и мембрану, обработанную блоттингом с применением антитела ACI-35-2G5-Ab3. Антитело ACI-35-2G5-Ab3, специфичное в отношении Tau-pS396, продемонстрировало интенсивный сигнал для Tau-pS396, причем наблюдаемые полосы также наводят на мысль о том, что оно связывается с димерами Tau-pS396 (Фиг. 7, дорожки 11 и 13). Без обработки GSK3p полосы не наблюдались (дорожки 6-8 и 14-15).
ПРИМЕР 11: Обнаружение фосфорилирования Тау (pSer396) в образцах спинномозговой жидкости (СМЖ) человека
11.1 Методы
11.1.1 Образцы тканей человека - посмертные образцы мозга Посмертный образец височной области коры донора AD19, страдающего болезнью Альцгеймера (БА), был получен из Банка образцов мозга Университета Майами. Мы выражаем признательность Банку образцов мозга Университета Майами за предоставление образцов для данного исследования. Демографические данные донора приведены в Табл. 12 ниже, в которой также указана стадия заболевания по Braak (Braak and Braak (1991) Neuropathological stageing of Alzheimer-related changes. Acta Neuropathol 82: 239-259).

11.1.2. Получение фракции S1 посмертного гомогената мозга
Посмертный образец височной области коры донора AD19 был гомогенизирован согласно следующему протоколу. Фрагменты мозга взвешивали и гомогенизировали в 9 объемах 25 мМ Трис-HCl, рН 7,4, 150 мМ NaCl, 1 мМ ЭДТА, 1 мМ ЭГТА, содержащего ингибиторы фосфатаз (30 мМ NaF, 0,2 мМ Na3VO4, 1 нМ окадаиковой кислоты, 1 мМ ПМСФ, 5 мМ Na4P2O7) и ингибиторы протеаз (Complete Mini, Roche 04 693 124 001). Гомогенизацию проводили на льду с помощью стеклянного гомогенизатора. Получали фракцию полного гомогената (ОГ). Половину объема фракции ОГ разделили на аликвоты и хранили при -80°С. Остаток фракции ОГ дополнительно обрабатывали путем добавления Тритона Х-100 до конечной концентрации 0,4%. Образцы тщательно перемешивали и несколько раз обрабатывали вихревым перемешиванием, после чего центрифугировали со скоростью 5000 об/мин в течение 5 минут при 4°С. Супернатант составляет фракцию S 1. Образцы разделили на аликвоты и хранили при -80°С. Концентрацию белка измеряли с помощью реактива Bradford (Sigma B6916-500).
11.1.3 Образцы СМЖ человека
Образцы спинномозговой жидкости (СМЖ) больных клинически подтвержденной болезнью Альцгеймера (БА) легкой или средней степени тяжести и контрольных доноров - здоровых добровольцев (Контроль) были предоставлены Благотворительной Школой медицины Берлина. Мы выражаем признательность Благотворительной Школе медицины Берлина за предоставление образцов для данного исследования. Образцы разделили на аликвоты, хранили при -80°С и использовали без дальнейшей обработки. Демографическая и клиническая информация доноров образцов СМЖ приведена в Табл. 13 ниже.
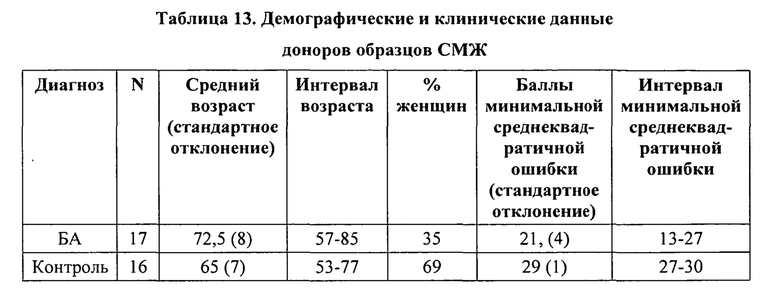
11.1.4 Иммунообогащение СМЖ Тау
11.1.4.1 Сочетание антитела
Для иммунообогащения СМЖ Тау применяли коммерческое антитело человека против Тау (клон НТ7, Thermo Scientific MN 1000). С целью сочетания НТ7 с Dynabeads Белка G (Life Technologies 10004D), для каждого образца 1,5 мг (50 мкл) Dynabeads Белка G ресуспендировали путем вихревого перемешивания и переносили в пробирку Maximum Recovery емкостью 1,7 мл (Axygen MCT-175-L-C). Пробирки помещали на магнитную подложку (DynaMag, Life Technologies 123.21D) для концентрации гранул на стенке пробирки и удаления буфера. Связывание 1 мкг НТ7 в 200 мкл ФБР с Dynabeads Белка G осуществляли с использованием Hula Mixer (Life Technologies) со скоростью 10/20 об/мин, 25°/отклонение 10, 5°/2 вибро в течение 10 минут, после чего пробирки помещали на магнит, буфер удаляли, и пробирки промывали 1 раз, путем аккуратного переноса пипеткой 200 мкл ФБР/0,02% Твина 20, и 2 раза по 200 мкл буфера конъюгации (20 мМ Na фосфата, 150 мМ NaCl, свежеприготовленный). Промывочные буферы всегда удаляли с помощью магнита. Для поперечного сшивания НТ7 с Dynabeads Белка G, НТ7-гранулы ресуспендировали в 250 мкл 5 мМ раствора BS3 (Sigma-Aldrich S5799), растворяли в буфере конъюгации и инкубировали с вращением (такие же условия, как описано выше) в течение 30 минут при комнатной температуре, реакцию останавливали добавлением 12,5 мкл гасящего буфера (1 М Трис-HCl рН 7,5) в течение 15 минут, с последующим трехкратным промыванием по 200 мкл ФБР/0,02% Твина 20.
11.1.4.2 Иммунообогащение СМЖ Тау
СМЖ использовали в неразведенном виде, причем 1 мл СМЖ от каждого донора переносили в пробирку, содержащую поперечно-сшитые гранулы НТ7, и инкубировали в течение 1 час при 4°С и непрерывном вращении (10 об/мин). После удаления несвязанного материала на магните, гранулы промывали 200 мкл ФБР/0,02% Твина 20, и Тау элюировали 20 мкл 1% раствора натрия додецилсульфата (НДС) в ФБР при 70°С в течение 10 минут. Во избежание осаждения гранул, содержимое пробирок кратковременно перемешивали (300 об/мин в нагретом горизонтальном миксере, в течение 5 с каждую минуту). После инкубации, образцы элюата собирали, помещая пробирку на магнит.
В качестве положительного контроля, Тау был также обогащен из гомогенатов мозга человека. Для этого готовили серийные разведения фракции S1 мозга человека, полученной от донора AD19, в ФБР (0,5 мкг/мл, 0,17 мкг/мл, 0,056 мкг/мл, 0,019 мкг/мл, 0,006 мкг/мл, 0,002 мкг/мл, 0,0007 мкг/мл). Затем каждый образец (1 мл) обрабатывали, как описано выше, и элюировали 25 мкл 1% раствора НДС.
11.1.5 AlphaLISA.
11.1.5.1 Описание анализа AlphaLISA
AlphaLISA представляет собой гомогенный анализ, в котором применяется основанная на гранулах технология Альфа. AlphaLISA был выбран как технологическая платформа за его чувствительность и минимальное количество стадий. Если коротко, анализ основан на бесконтактном взаимодействии гранул. При возбуждении на длине волны 680 нм, фотосенсибилизатор, содержащийся в гранулах Донора, превращает кислород окружающей среды в более реакционноспособные атомарные формы кислорода, которые диффундируют (до 200 нм, в пределах периода полураспада 4 мс) и вызывают хемилюминесцентную реакцию в гранулах Акцептора, приводящую к эмиссии света.
Условия анализа в наших экспериментах были следующими (см. также Фиг. 8):
- Пан-Тау антитело Таи-13 (Abeam ab24636), присоединенное к гранулам Акцептора Альфа, связывается с Тау человека, присутствующим в образце, и образует комплекс «белок Тау-антитело Tau-13-гранулы Акцептора»
- Антитело обнаружения ACI-35-2G5-Ab3-BT связывается с pS396 человеческого Тау и позволяет связывание покрытых стрептавидином (SAv) гранул Донора Альфа с комплексом.
После ввода всех реактивов в реакцию, хемилюминесцентный сигнал считывают с помощью устройства для считывания EnSpire Alpha 2390.
11.1.5.2 Биотинилирование антитела ACI-35-2G5-Ab3
Для использования в анализе AlphaLISA, антитело ACI-35-2G5-Ab3 биотинилировали с использованием набора EZ-Link Micro Sulfo-NHS-LC-Biotinylation Kit (Thermo Scientific 21935), согласно инструкциям производителя. 25-кратный молярный избыток биотина по сравнению с антителом использовали в реакции введения метки. После биотинилирования, избыток свободного биотина удаляли 4-хкратным промыванием антитела ФБР с помощью концентратора 50'000 MWCO Spin-X UF 500 (Coming 431480). Биотинилированное антитело ACI-35-2G5-Ab3 обозначено как ACI-35-2G5-Ab3-BT.
11.1.5.3 Сочетание антитела Tau-13 с гранулами Акцептора AlphaLISA. Для использования в анализе AlphaLISA, антитело Тау-13 конъюгировали с активированными гранулами Альфа Акцептора (Perkin Elmer 6772001). Применяли следующий протокол сочетания: раствор 0,1 мг антитела Тау-13 (очищенный на колонке Белка А) смешивали с 1 мг гранул Акцептора AlphaLISA и добавляли 0,13 М фосфатный буфер (рН 8,0) до конечного объема реакции 200 мкл. Далее, добавляли 1,25 мкл 10% Твина-20 и 10 мкл 25 мг/мл раствора NaBH3CN, и пробирку инкубировали в течение 48 часов при 37°С с легким вращением (7 об/мин). После реакции сочетания, активные сайты на гранулах блокировали добавлением 10 мкл раствора карбокси-метоксиламина, и дополнительно инкубировали при 37°С в течение 1 часа. В конце, гранулы дважды промывали по 200 мкл 0,1 М Трис-HCl, рН 8,0, и хранили при 4°С в 200 мкл буфера для хранения (ФБР, содержащий 0,05% Проклина-300), с получением конечной концентрации гранул Акцептора AlphaLISA 5 мг/мл.
11.1.5.4 Лимит обнаружения при использовании pS396-Tau мозга Для данного эксперимента использовали иммунообогащенные образцы мозга Тау, образцы фракции мозга S1 и холостые буферы. Каждый образец анализировали в конечном объеме 50 мкл, с использованием 384-луночного белого OptiPlate (Perkin Elmer 6007291). Разведения всех реактивов готовили в буфере анализа Альфа (Perkin Elmer AL000C).
- 5 мкл образца (1/10 конечного объема, т.е., конечная концентрация белка в анализе соответствует 1/10 концентрации образца).
- Добавляли 10 мкл 0,5% НДС для образцов фракции мозга S1 или 10 мкл холостого буфера для иммунообогащенных образцов Тау мозга.
- 15 мкл антитела ACI-35-2G5-Ab3-BT (конечная концентрация: 5 нМ) смешивали с конъюгатом Таи 13-гранулы Акцептора (конечная концентрация гранул: 2,5 мкг/мл).
- Инкубация при комнатной температуре в течение 1 часа
- 20 мкл гранул Донора Стрептавидина (конечная концентрация гранул: 25 мкг/мл).
- Инкубация при комнатной температуре в течение 30 минут (в защищенном от света месте).
- Считывание на приборе EnSpire Alpha и анализ с помощью EnSpire Workstation, версия 3.00.
11.1.5.5 Определение иммунообогащенного pS396-Tau в СМЖ Каждый образец анализируют в конечном объеме 50 мкл с использованием 384-луночного белого OptiP1ate (Perkin Elmer 6007291). Разведения всех реактивов готовят в буфере анализа Альфа (Perkin Elmer AL000C).
- 5 мкл иммунопреципитированного элюата от каждого донора
- 20 мкл антитела ACI-35-2G5-Ab3-BT (конечная концентрация: 5 нМ), смешанного с конъюгатом гранулы Таи 13-Акцептор (конечная концентрация гранул: 2,5 мкг/мл)
- Инкубация при комнатной температуре в течение 1 часа
- 25 мкл гранул Донора Стрептавидина (конечная концентрация гранул: 25 мкг/мл)
- Инкубация при комнатной температуре в течение 30 минут (в защищенном от света месте).
- Считывание на приборе EnSpire Alpha и анализ с помощью EnSpire Workstation, версия 3.00.
11.1.6 Статистический анализ
Статистический анализ данных выполняли с помощью программного обеспечения GraphPar Prism.
11.2 Результаты
Предварительные эксперименты продемонстрировали, что содержание pS396, присутствующего в СМЖ человека, было слишком низким для обнаружения. По этой причине был разработан протокол иммунообогащения в сочетании с иммунообнаружением с высокой чувствительностью. Протокол иммунообогащения сначала валидировали с использованием посмертного материала мозга человека, страдающего БА. Параллельное сравнение необработанных образцов гомогената мозга с иммунообогащенными образцами Тау выявило, что, при эквивалентных концентрациях, предел обнаружения в анализе Tay13/ACI-35-2G5-Ab3 AlphaLISA был достигнут на уровне 0,5 мкг/мл для необработанных образцов и в интервале 0,002-0,006 мкг/мл дыля иммунообогащенных образцов, что соответствует 100-кратному обогащению (Фиг. 9).
Далее, протокол иммунообогащения был применен к образцам СМЖ живых доноров (n=17 больных БА легкой или средней степени тяжести, и n=16 здоровых добровольцев соответствующего возраста). Полученные данные (Фиг. 10) демонстрируют следующее: а) после иммунообогащения протокол Tay13/ACI-35-2G5-Ab3 AlphaLISA обнаруживает pS396-Tau во всех образцах СМЖ человека; и б) что более важно, наблюдается значительное повышение содержания pS396-Tau в СМЖ БА, по сравнению с контролем (р=0,0003, тест Манна-Уитни).
В заключение, был разработан протокол иммунообогащения/иммунообнаружения, который позволяет обнаружить pS396-Tau в СМЖ человека. Повышение содержания pS396-Tau в СМЖ больных БА легкой или умеренной степени тяжести свидетельствует, что данный способ может с успехом применяться в клинических исследованиях биомаркеров, чтобы оценить прогрессирование заболевания, стратификацию пациентов и эффективность лечения. Антитело ACI-35-2G5-Ab3 обнаруживало pS396-Tau во всех образцах СМЖ человека, и, что более важно, антитело способно отличать БА СМЖ, по сравнению с контролем.

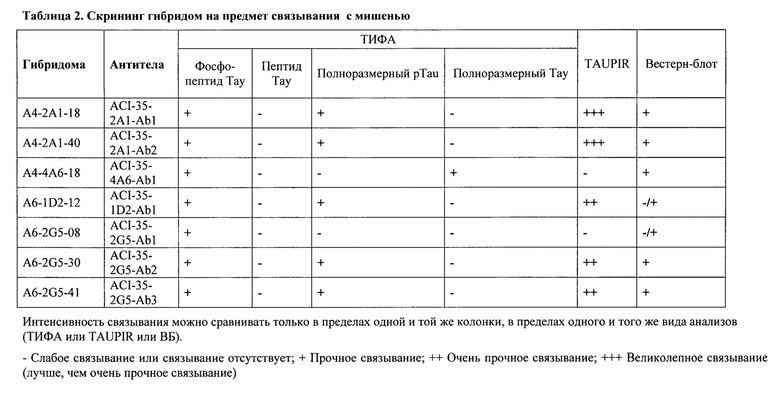
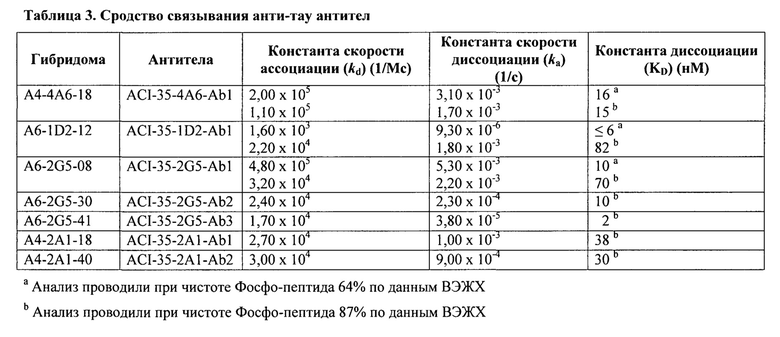
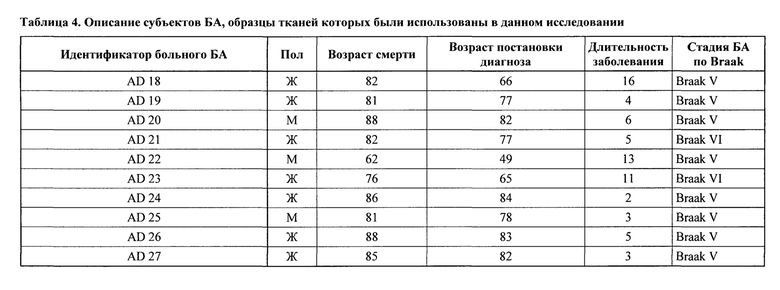
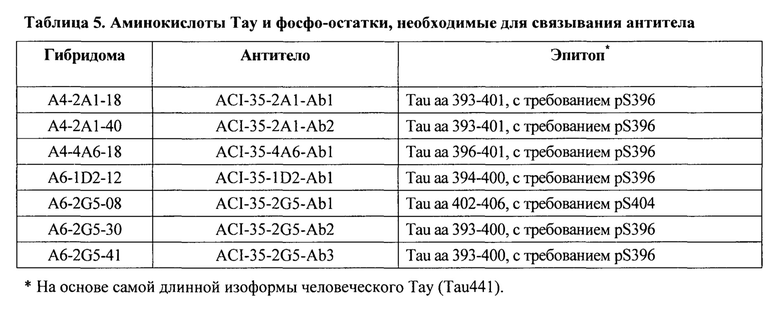
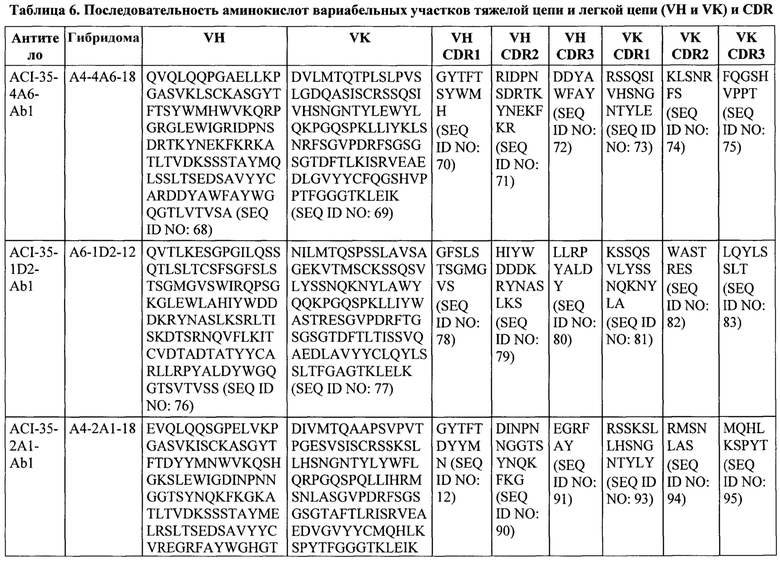
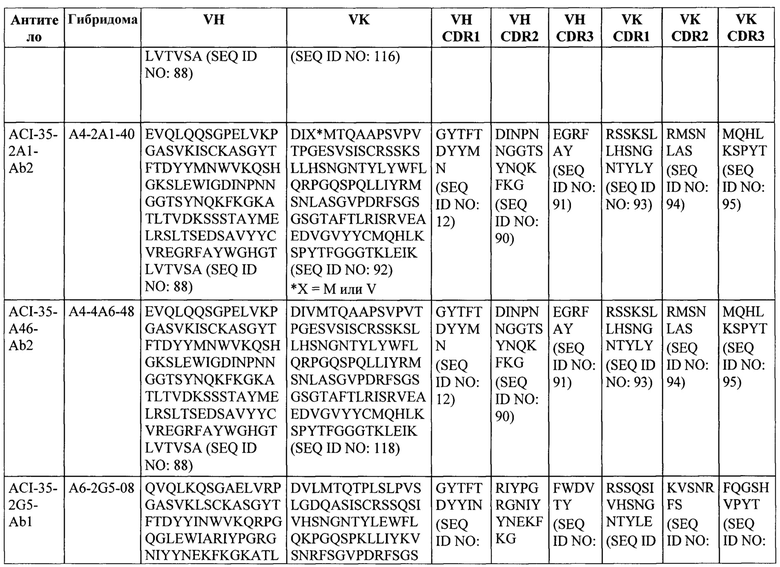
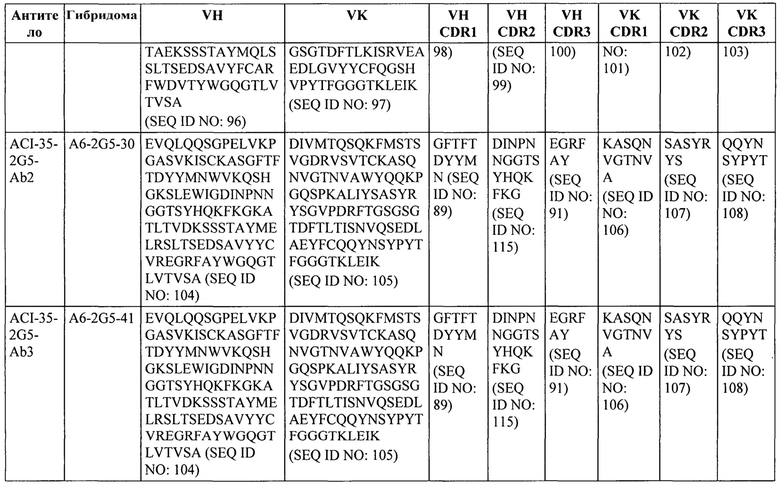




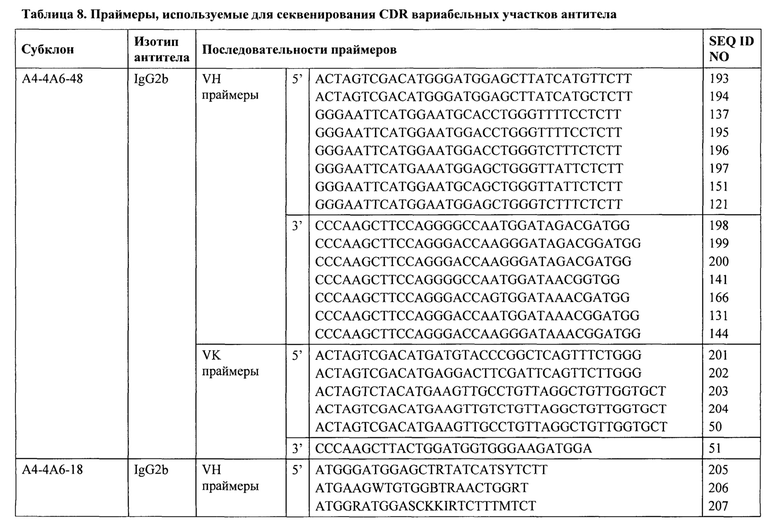
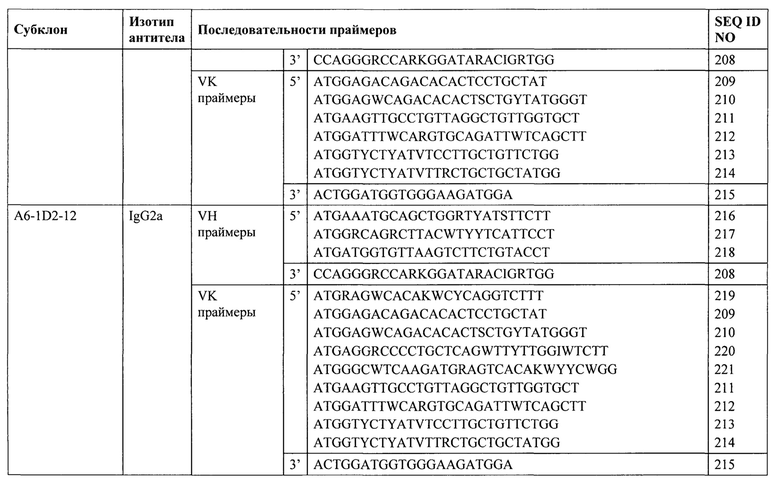

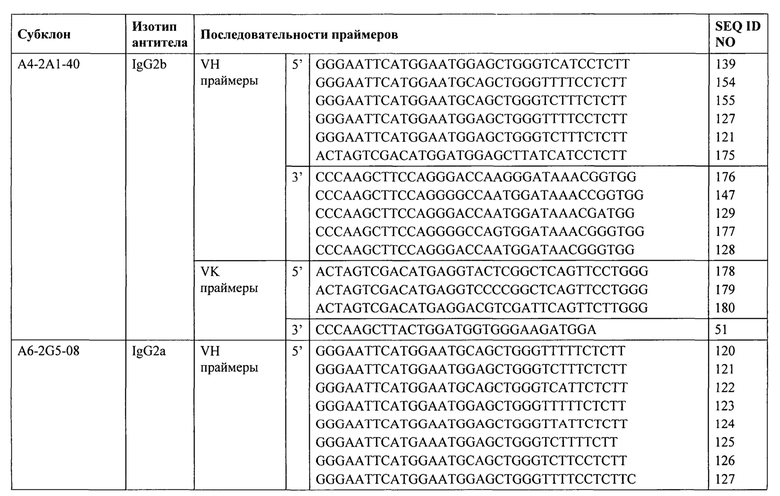
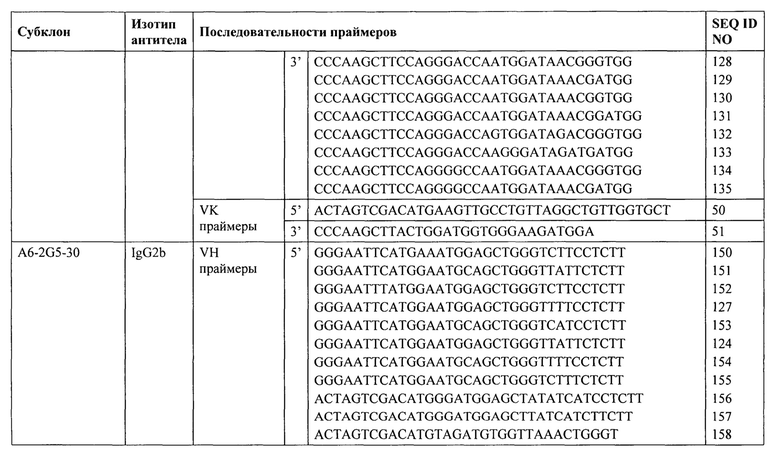
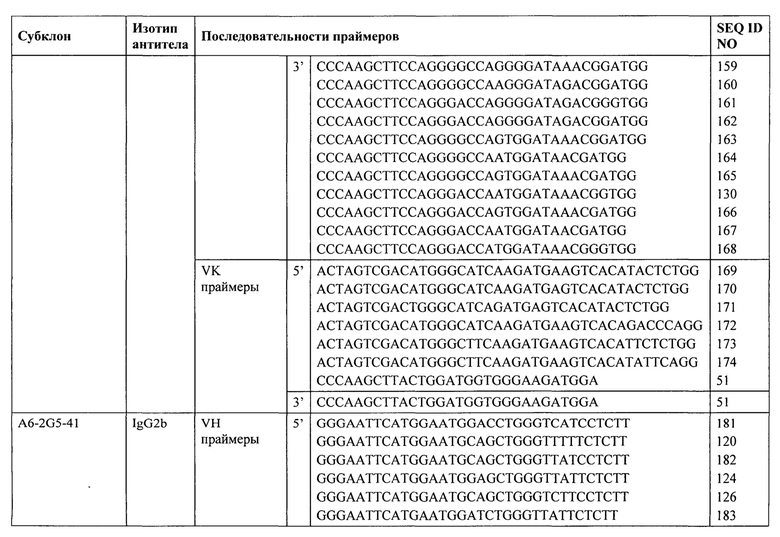
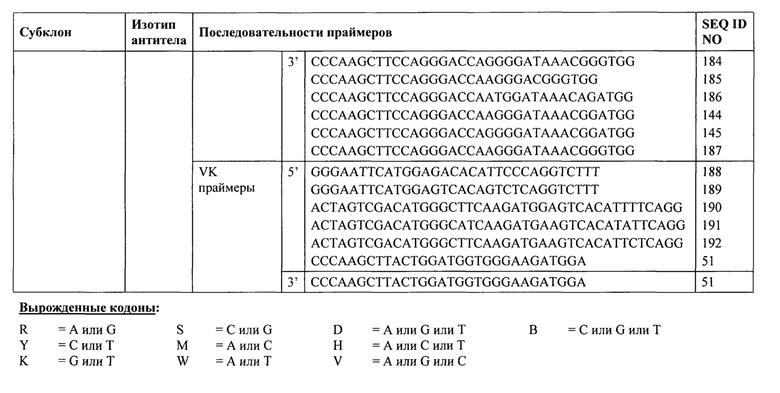

Депозиты:
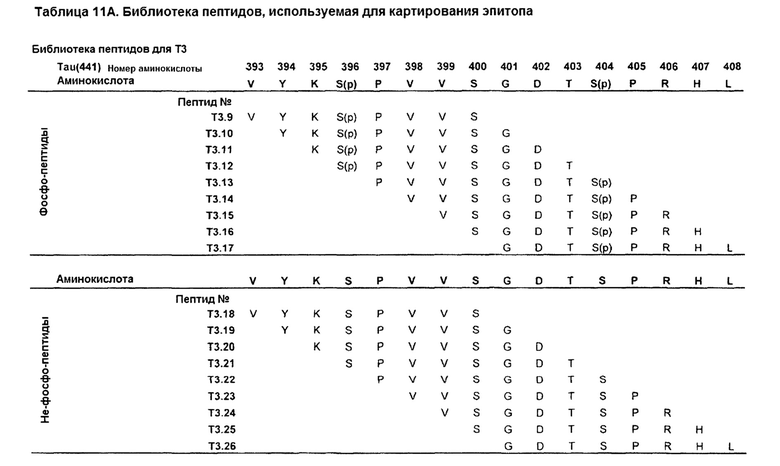

ЛИТЕРАТУРА
Alonso A.D., et al. (1997), Proc. Natl. Acad. Sci. U.S.A., 94, 298-303
Alving et al. (1992) Infect. Immun. 60:2438-2444
Asuni et al. (2007) J Neurosc. 27 (34), 9115-29
Braak and Braak (1991) Neuropathological stageing of Alzheimer-related changes. Acta Neuropathol 82:239-259)
Braak H., et al. (1993), Eur. Neurol., 33, 403-408
Gill et al., Nature Med. 9: 589-595 (2003)
Greenberg S.G., et al. (1992), J Biol. Chem., 267, 564-569.
Harlow and Lane, Antibodies: A Laboratory Manual (Cold Spring Harbor Laboratory, New York 1988 555-612
Hodgson et al. (1991) Bio/Technoloy, 9:421
Hoffmann R., et al. (1997), Biochemistry, 36, 8114-8124.
Kabat EA, Wu TT, Perry HM, Gottesman K.S, Foeller C. Sequences of proteins of Immunological Interest, US Department of Health and Human Services, 1991
Kennedy, J. H., et al., 1976 (Clin. Chim. Acta 70:1-31)
Khaw, B. A. et al. (1982) J. Nucl. Med. 23:1011-1019
Lewis et al. (2000) Nature Genetics, 25:402-405] Masliah et al. (2005) Neuron, 46(6), 857-68
Masliah et al. (2011) PLoS ONE, Volume 6(4), e19338, pp - 1-17
Muhs et al. (2007) Proc Natl Acad Sci USA, 104(23), 9810-5
Muyllaert et al. (2006) Rev Neurol, 162(10), 903-907
Muyllaert et al. (2008) Genes Brain Behav., Suppl. 1, 57-66
Neuwelt, E.A., Implication of the Blood-Brain Barrier and its Manipulation, Vols 1 & 2, Plenum Press, N.Y. (1989))
Nicolau et. al. (2002) Proc Natl. Acad. Sci USA 99, 2332-2337
Nicoll et al. (2003) Nature Med, 9, 448-452
Oddo et al. (2004) Neuron, 43, 321-332
Queen et al. (1989) Proc. Natl Acad Sci USA, 86:10029-10032
Papanastassiou et al., Gene Therapy 9: 398-406 (2002)
Reig S., et al. (1995), Acta Neuropathol., 90, 441-447
Ribe et al. (2005) Neurobiol Dis, 20(3), 814-22
Roberson et al. (2007) Science, 316 (5825), 750-4
Rosenmann et al. (2006) Arch Neurol, 63(10), 1459-67
Rousseaux et al. Methods Enzymology, (1986), Academic Press 121:663-69
Schurs, A. H. W. M., et al. (1977) Clin. Chim Acta 57:1-40
Terwel et al. (2006) J Biol Chem, 280, 3963-3973
Terwel et al. (2008) Am J pathol., 172(3), 786-98
Urushitiani et al. (2007) Proc. Natl Acad Sci USA, 104(79, 2495-500
Vandebroek et al., "Phosphorylation and Aggregation of Protein Tau in Humanized Yeast Cells and in Transgenic Mouse Brain"; 7th International Conference on A1zheimer's and Parkinson's Disease, Sorrento, Italy, March 9-13, 2005, pp 15-19
Wagner et al (2002) Journa1 of Liposome Research Vol 12(3), pp 259-270
WO 2004/058258
WO 96/13590
WO 96/29605
Патентная публикация США №2002/0038086
Патентная публикация США №2003/0083299
Патентная публикация США №2002/0025313
Патентная публикация США №2004/0204354
Патентная публикация США №2004/0131692
Патентная публикация США №2002/0065259
Патентная публикация США №2003/0162695
Патентная публикация США №2005/0124533
Патентная публикация США №2005/0089473.
Патентная публикация США №2003/0073713
Патентная публикация США №2003/0129186
Патент США №5112596
Патент США №5268164
Патент США №5506206
Патент США №5686416
Патент США №5004697
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2603078C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2582916C2 |
| ГУМАНИЗИРОВАННОЕ ТАУ-АНТИТЕЛО | 2013 |
|
RU2644242C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ГИПЕРФОСФОРИЛИРОВАННОМУ ТАУ-БЕЛКУ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2727911C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ГИПЕРФОСФОРИЛИРОВАННОМУ ТАУ-БЕЛКУ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2760875C1 |
| МОНОКЛОНАЛЬНОЕ ТЕЛО ПРОТИВ АМИЛОИДА БЕТА | 2008 |
|
RU2571856C2 |
| ТЕРАПИЯ И ДИАГНОСТИКА НА ОСНОВЕ БЕЛКОВ ТАУ-ОПОСРЕДУЕМОЙ ПАТОЛОГИИ ПРИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2012 |
|
RU2645259C2 |
| АНТИТЕЛА К ТАУ И СПОСОБЫ ПРИМЕНЕНИЯ | 2014 |
|
RU2661111C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ИЛИ ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ПРОТИВ ДЕМЕНЦИИ | 2013 |
|
RU2657438C2 |
| ПРИМЕНЕНИЕ АНТИТЕЛА ПРОТИВ АМИЛОИДА БЕТА ПРИ ГЛАЗНЫХ ЗАБОЛЕВАНИЯХ | 2008 |
|
RU2604181C2 |


































































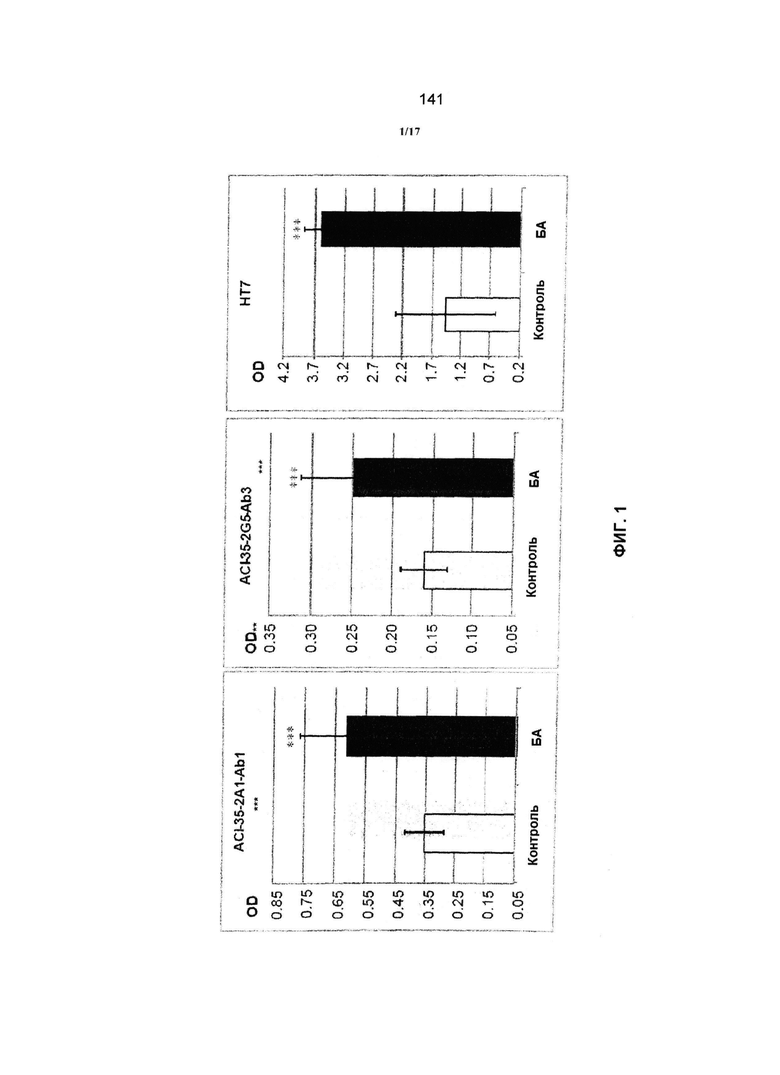
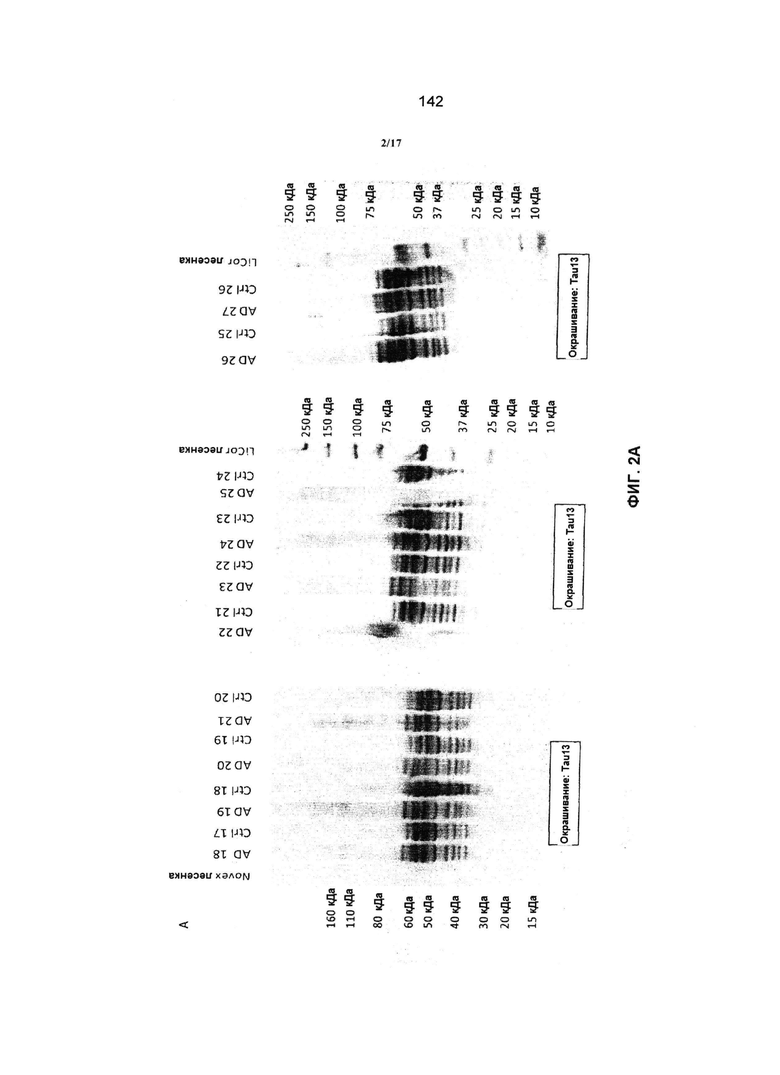
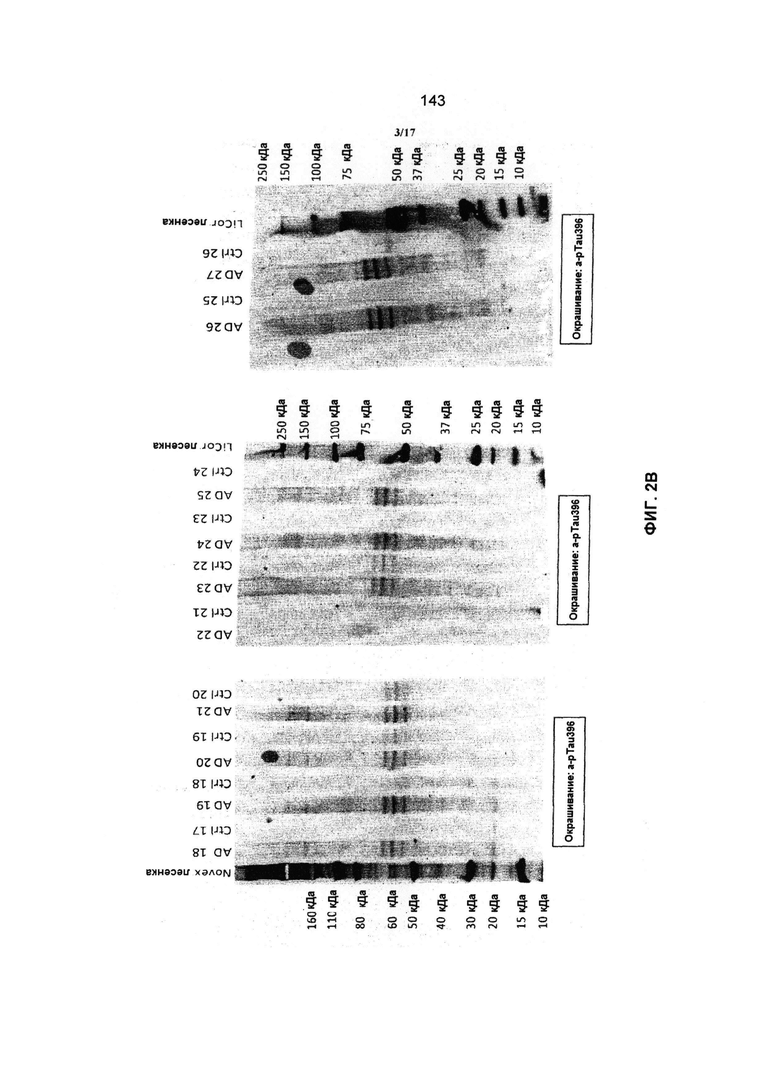
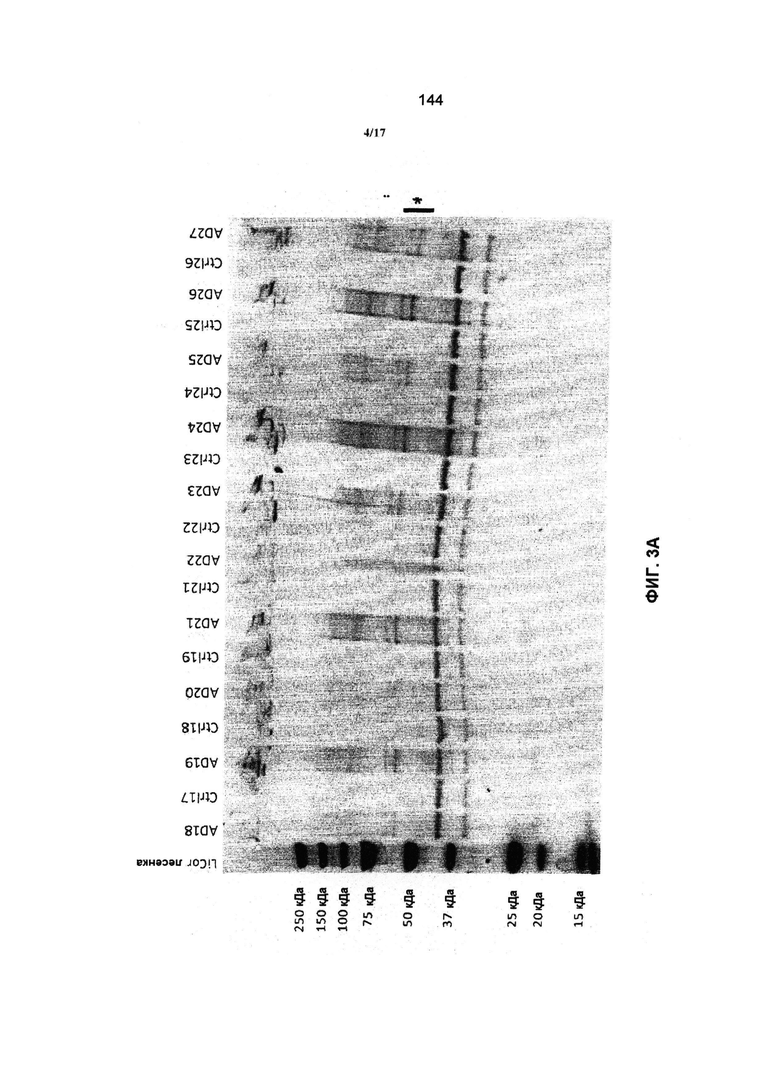
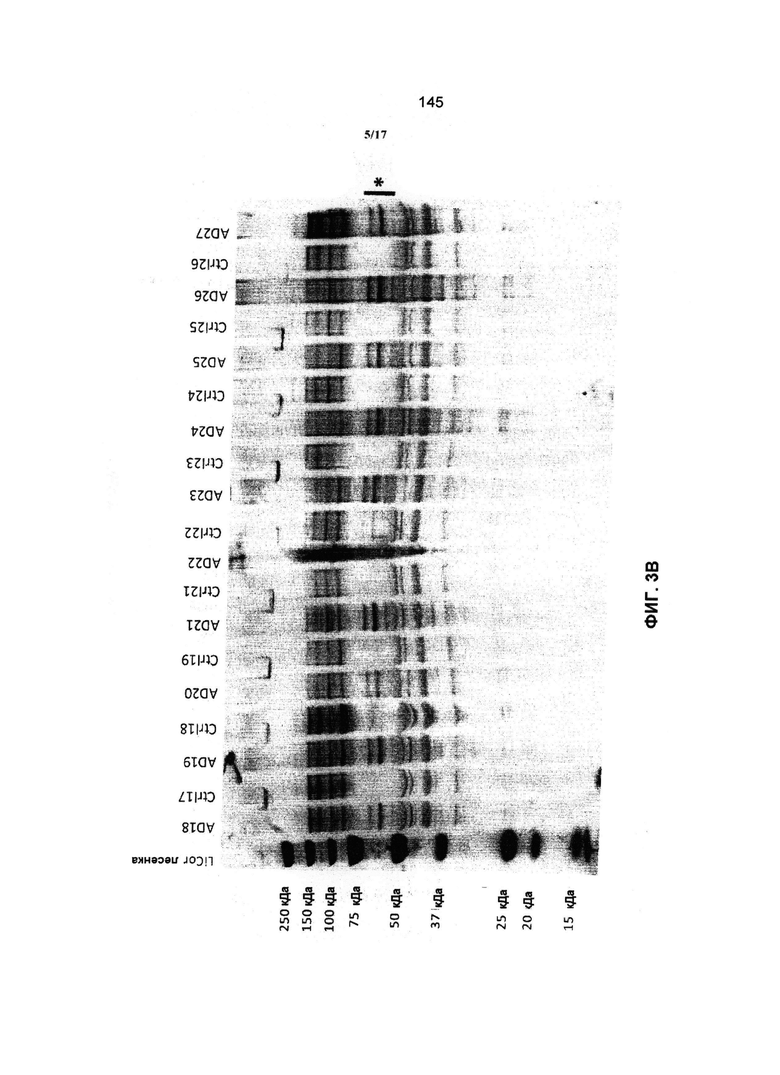
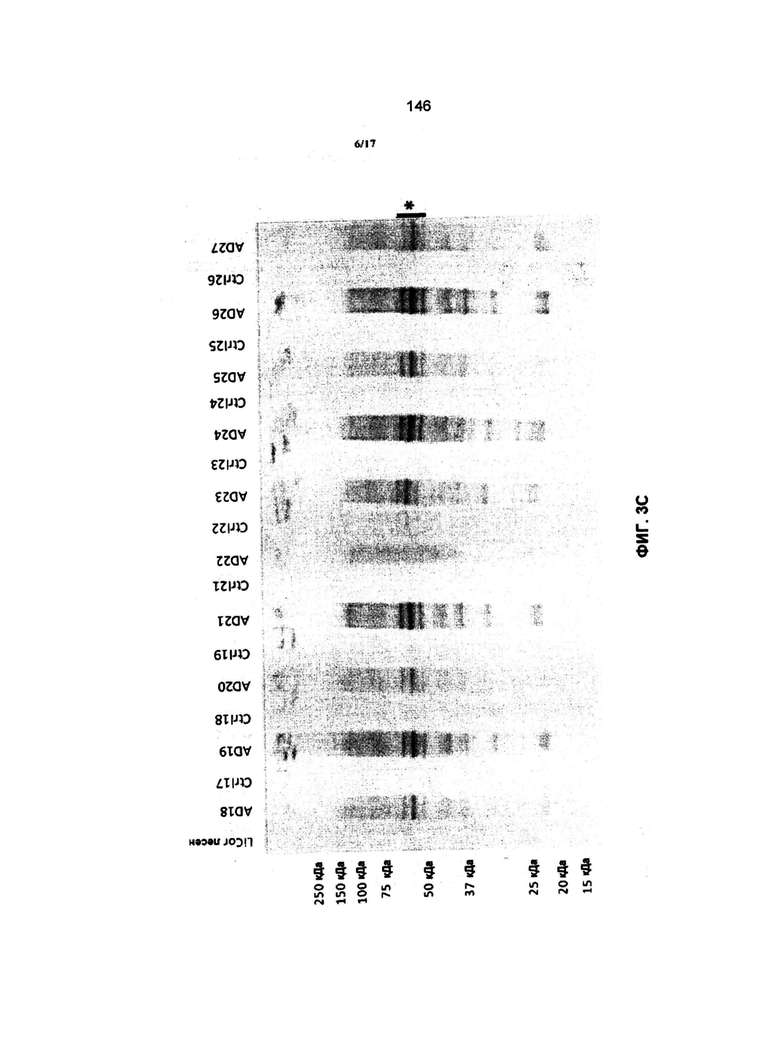
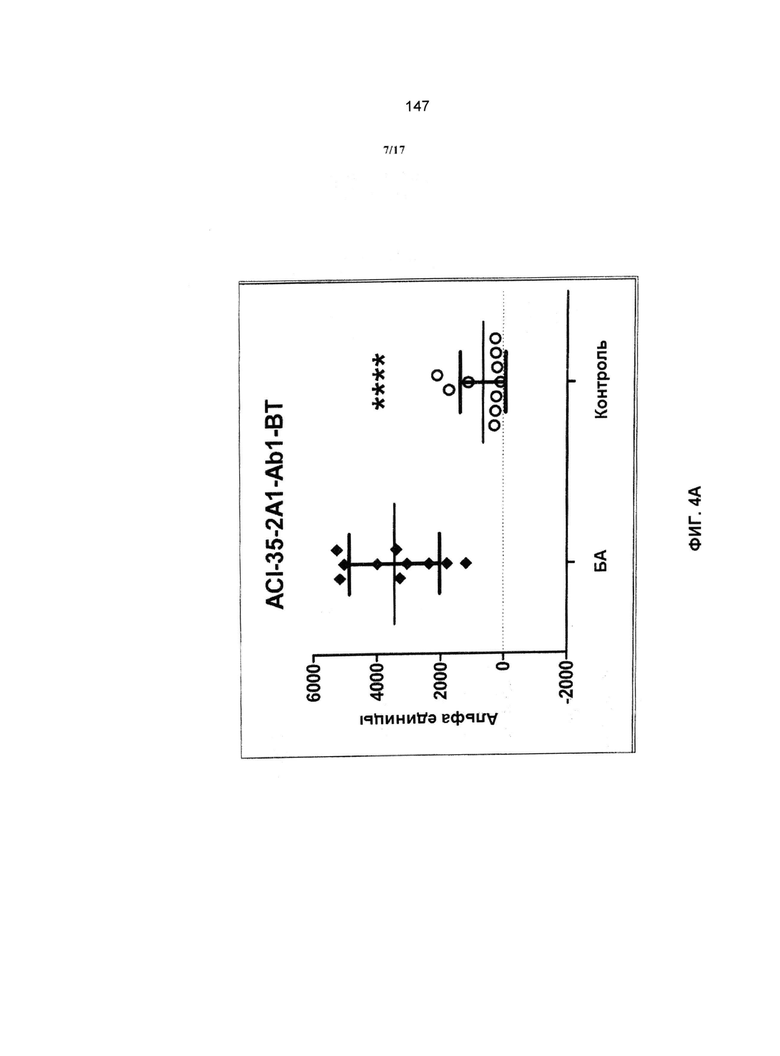
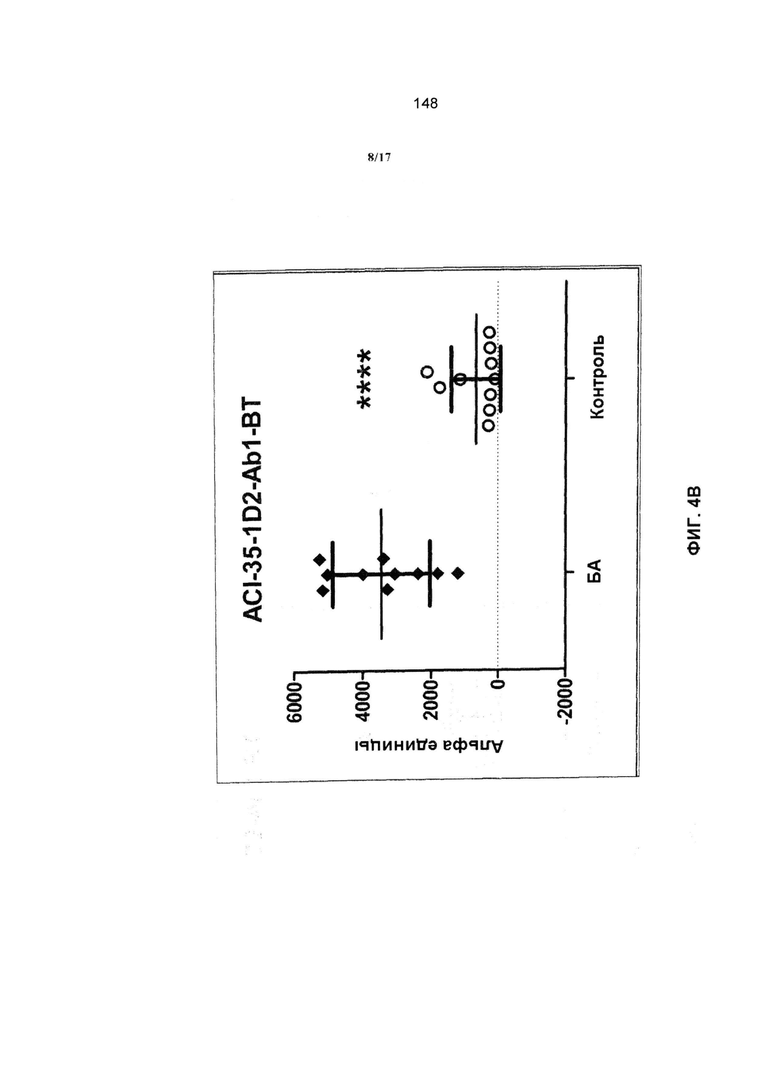
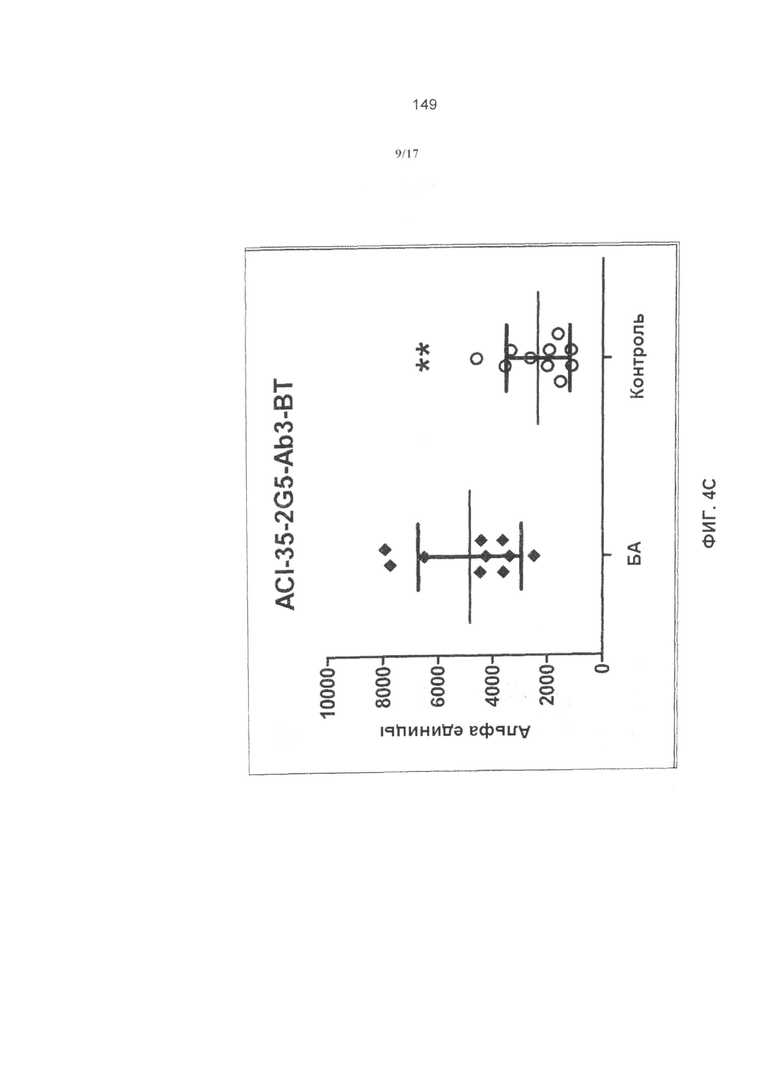
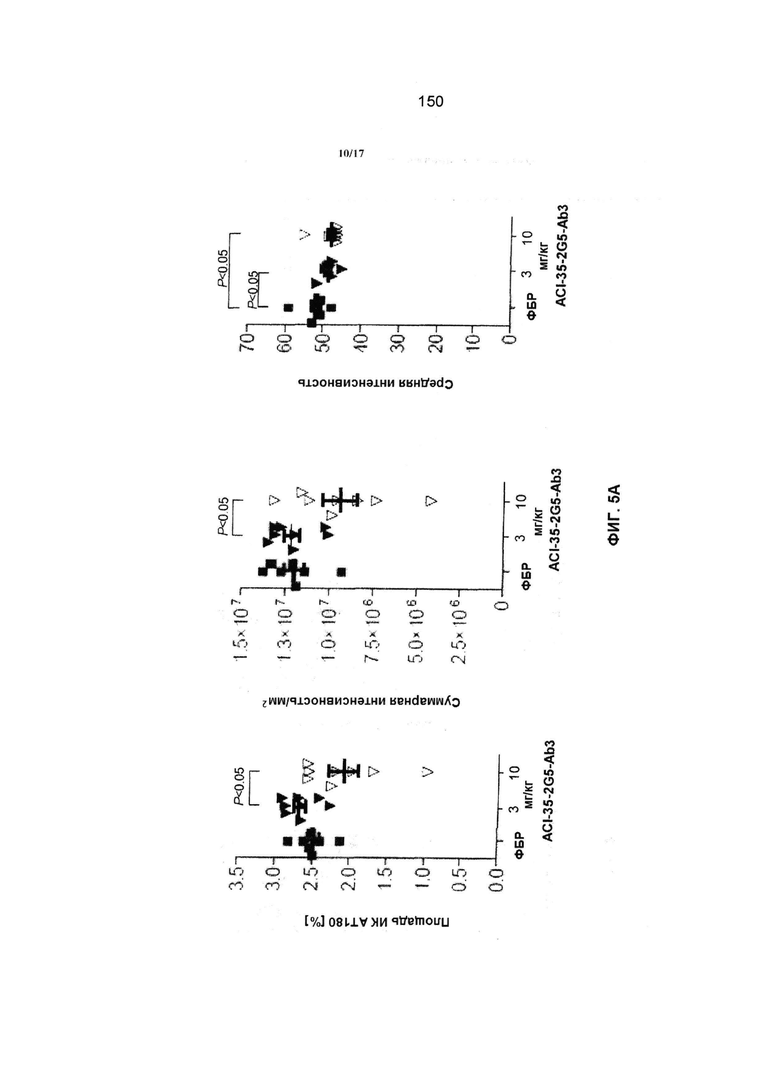
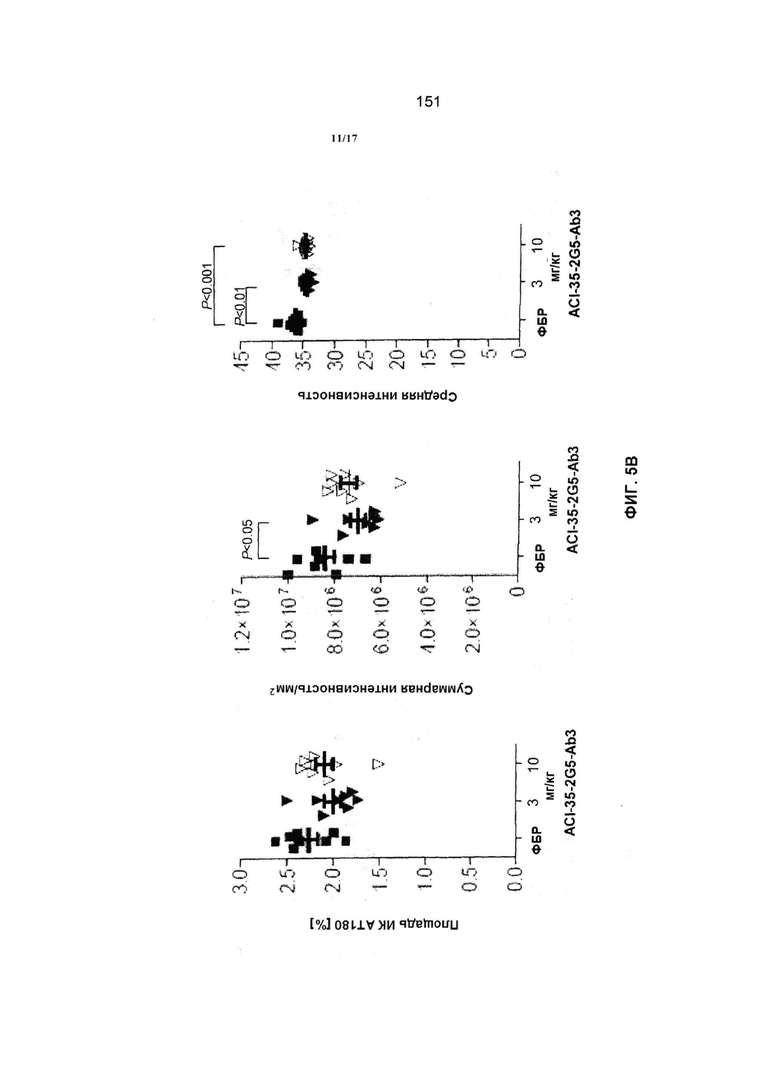
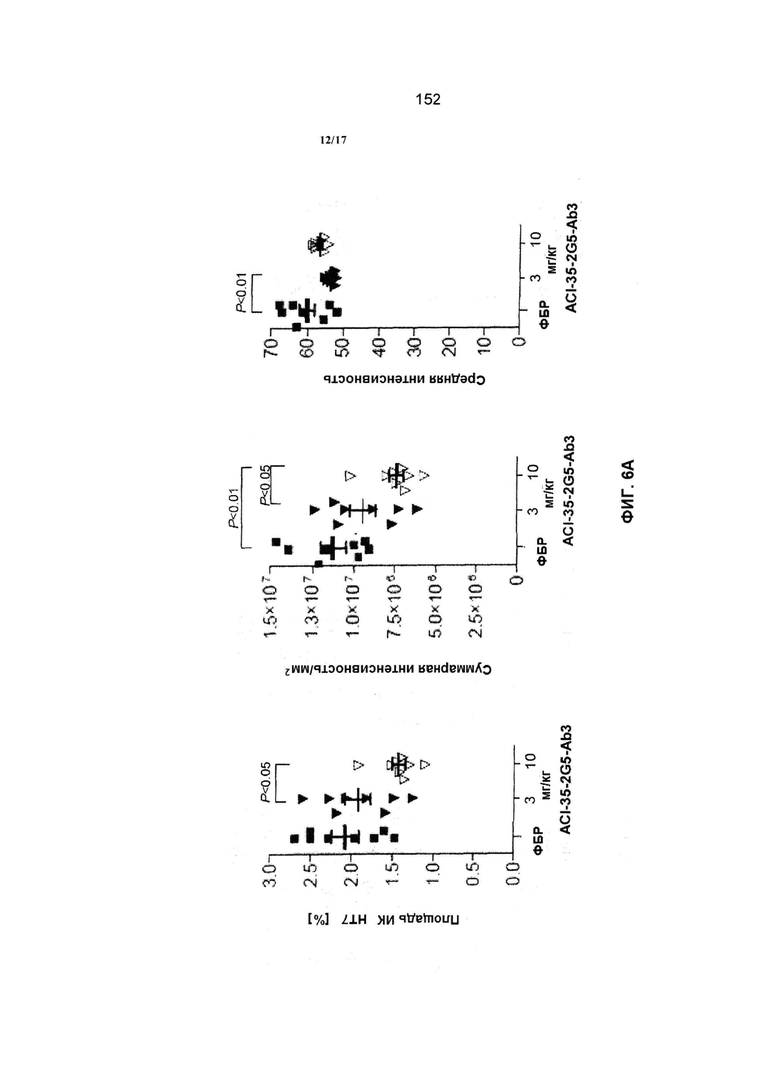
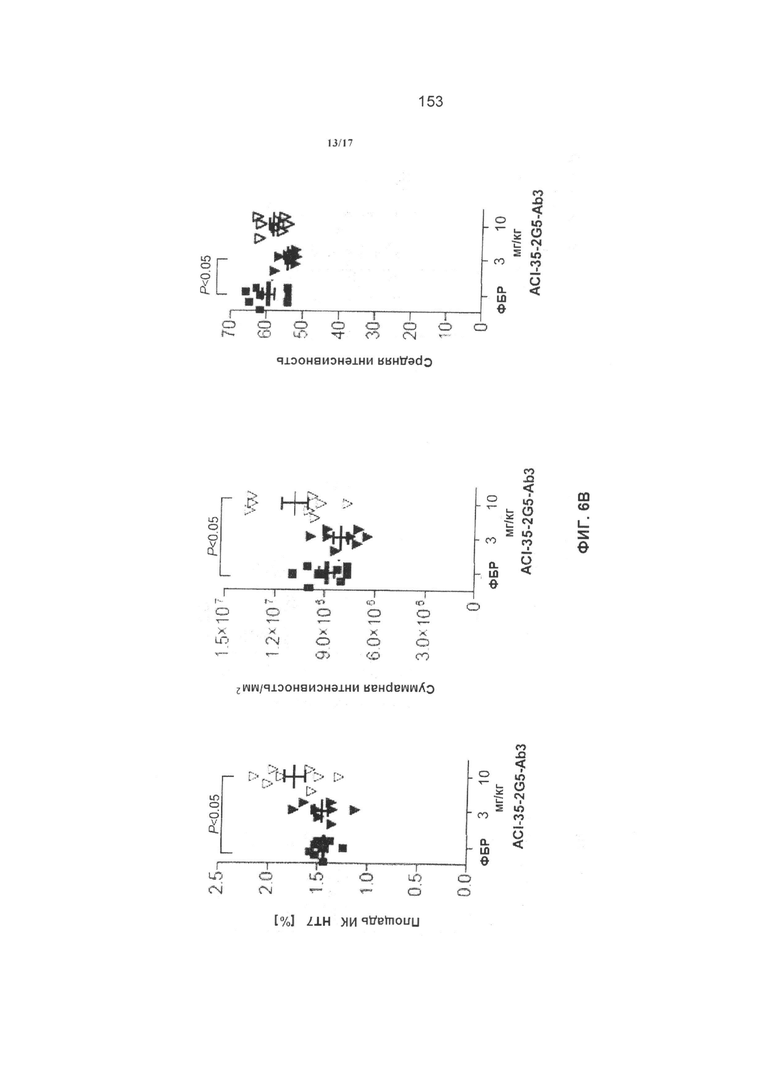
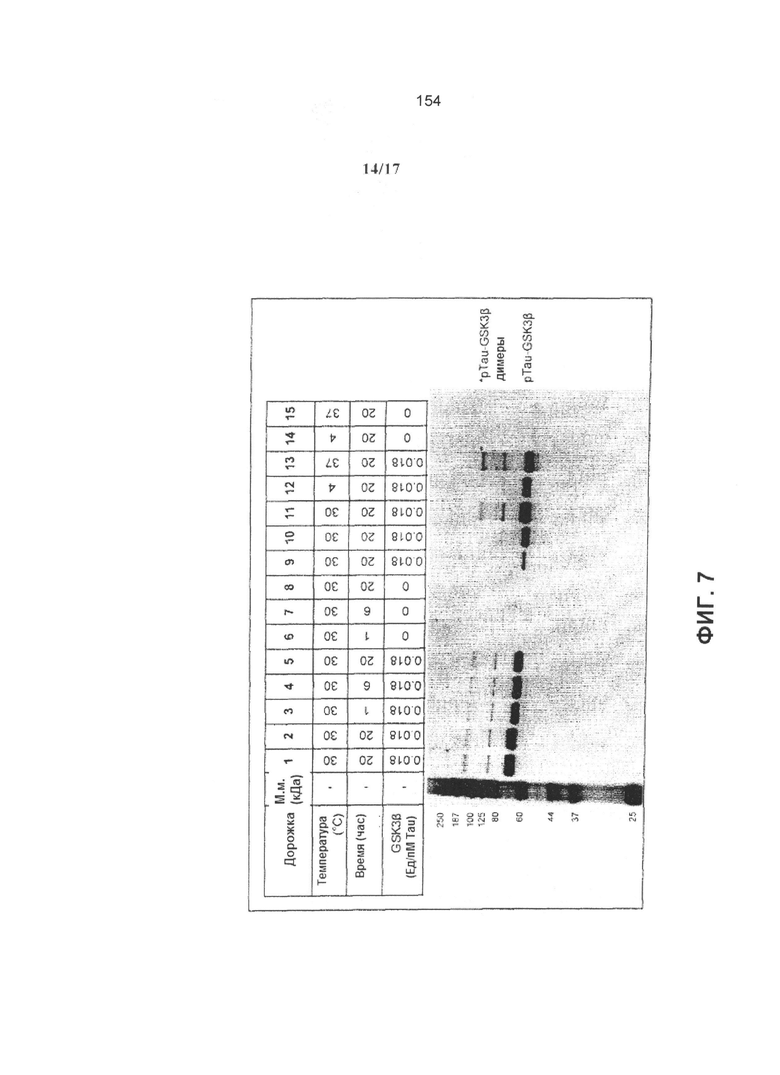
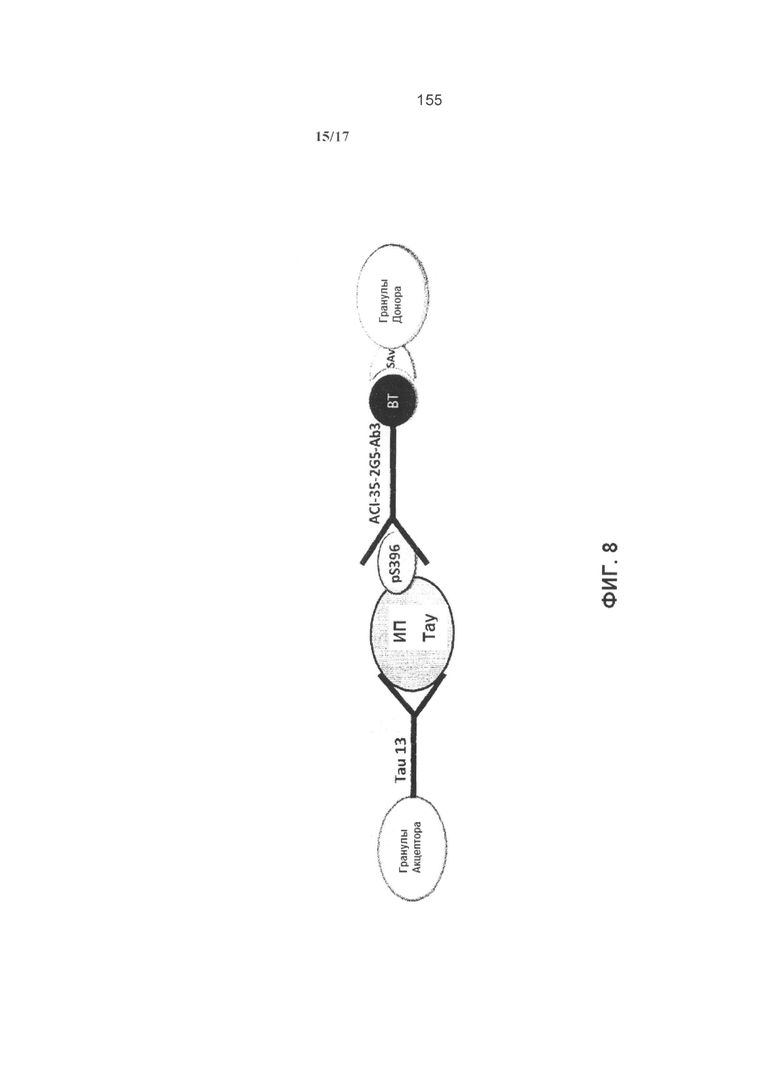


Настоящее изобретение относится к иммунологии. Предложены антитело и его фрагмент, которые связываются с фосфо-эпитопом на белке Тау, а также кодирующие их полинуклеотиды; линии клеток, продуцирующие антитела; вектор, содержащая его клетка-хозяин и способ получения антитела и его функционального фрагмента. Кроме того, предложены фармацевтический состав, способ лечения, облегчения или защиты от таупатии; способ индукции пассивной иммунной реакции у животного; способ диагностики связанного с белком тау заболевания, расстройства или состояния или предрасположенности к связанному с белком тау заболеванию; способ мониторинга минимального остаточного заболевания у пациента после лечения антителом против тау; способ прогнозирования ответа больного на лечение антителом против тау; способы обнаружения мультимеров фосфо-Тау (pTau) в образце мозга, в том числе посмертного обнаружения; диагностический набор. Данное изобретение может найти дальнейшее применение в диагностике и терапии заболеваний, связанных с Тау-белком. 19 н. и 23 з.п. ф-лы, 10 ил., 15 табл., 11 пр.
1. Антитело или его функциональный фрагмент, который распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, притом что указанное антитело или фрагмент антитела содержит:
(a) вариабельную область легкой цепи, содержащую CDR1 с аминокислотной последовательностью SEQ ID NO: 106, CDR2 с аминокислотной последовательностью SEQ ID NO: 107 и CDR3 с аминокислотной последовательностью SEQ ID NO: 108, и вариабельную область тяжелой цепи, содержащую CDR1 с аминокислотной последовательностью SEQ ID NO: 89, CDR2 с аминокислотной последовательностью SEQ ID NO: 115 и CDR3 с аминокислотной последовательностью SEQ ID NO: 91; или
(b) вариабельную область легкой цепи, содержащую CDR1 с аминокислотной последовательностью SEQ ID NO: 93, CDR2 с аминокислотной последовательностью SEQ ID NO: 94 и CDR3 с аминокислотной последовательностью SEQ ID NO: 95, и вариабельную область тяжелой цепи, содержащую CDR1 с аминокислотной последовательностью SEQ ID NO: 12, CDR2 с аминокислотной последовательностью SEQ ID NO: 90 и CDR3 с аминокислотной последовательностью SEQ ID NO: 91.
2. Антитело или его функциональный фрагмент по п. 1, притом что указанное антитело или фрагмент антитела связывается с фосфо-эпитопом, имеющим или содержащимся в последовательности аминокислот VYKSPVVSGDTSPRHL (SEQ ID NO: 62) (Тау аа 393-408 SEQ ID NO: 67), содержащей фосфорилированный Ser в положениях 396 (pS396) и 404 (pS404).
3. Антитело или его функциональный фрагмент по п. 1, где антитело или его функциональный фрагмент специфично связывает растворимый, олигомерный и нерастворимый фосфорилированный белок тау.
4. Антитело или его функциональный фрагмент по п. 1, где антитело или его функциональный фрагмент специфично связывает фосфорилированный белок тау с константой диссоциации в диапазоне от 2 нМ до 80 нМ.
5. Антитело или его функциональный фрагмент по п. 1, где антитело или его функциональный фрагмент специфично связывает фосфорилированный белок тау с константой скорости ассоциации в диапазоне от 1.6×102 М-1с-1 до 5×105 М-1с-1.
6. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или фрагмент антитела представляет собой модулирующее антитело, которое модулирует уровни растворимого и/или нерастворимого Тау в мозгу млекопитающего.
7. Антитело или его функциональный фрагмент по п. 6, отличающееся тем, что указанное антитело или фрагмент антитела модулирует уровни растворимого и/или нерастворимого Тау в коре мозга и/или гиппокампе.
8. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или фрагмент антитела снижает уровни общего растворимого и/или нерастворимого белка тау.
9. Антитело или его функциональный фрагмент по п. 8, отличающееся тем, что указанный белок тау представляет собой фосфорилированный белок тау.
10. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или фрагмент антитела снижает уровни спаренных спиральных нитей, содержащих гиперфосфорилированный белок тау.
11. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или фрагмент антитела снижает уровни общего растворимого белка тау, растворимого фосфорилированного белка тау и спаренных спиральных нитей pTau.
12. Антитело или его функциональный фрагмент по п. 6, отличающееся тем, что указанное млекопитающее является человеком.
13. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или фрагмент антитела связывается с эпитопом, выбранным из группы, состоящей из:
a) VYKSPVVSG (Тау аа 393-401 SEQ ID NO: 67), содержащего фосфорилированный Ser в положении 396 (pS396), и
b) VYKSPVVS (Тау аа 393-400 SEQ ID NO: 67), содержащего фосфорилированный Ser в положении 396 (pS396).
14. Антитело или его функциональный фрагмент по п. 1, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, отличающееся тем, что указанное антитело или его фрагмент содержит вариабельную область легкой цепи, содержащую CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 93, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 94, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 95, и вариабельную область тяжелой цепи, содержащую CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 12, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 90, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 91.
15. Антитело или его функциональный фрагмент по п. 1, причем указанное антитело или его фрагмент распознает и специфично связывается с фосфо-эпитопом на белке Тау млекопитающего или на его фрагменте, отличающееся тем, что указанное антитело или его фрагмент содержит вариабельную область легкой цепи, содержащую CDR1 с последовательностью аминокислот, представленной в SEQ ID NO: 106, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 107, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 108, и вариабельную область тяжелой цепи, содержащую CDR1 с последовательностью аминокислот, представленной в SEQ ID NО: 89, CDR2 с последовательностью аминокислот, представленной в SEQ ID NO: 115, и CDR3 с последовательностью аминокислот, представленной в SEQ ID NO: 91.
16. Антитело или его функциональный фрагмент по п. 1, содержащий:
a) вариабельную область легкой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 116, и/или вариабельную область тяжелой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 88; или
b) вариабельную область легкой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 92, и/или вариабельную область тяжелой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 88; или
c) вариабельную область легкой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 105, и/или вариабельную область тяжелой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 104, или
d) вариабельную область легкой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 118, и/или вариабельную область тяжелой цепи, содержащую последовательность аминокислот, представленную в SEQ ID NO: 88.
17. Антитело или его функциональный фрагмент по п. 1, причем указанное антитело является поликлональным антителом, моноклональным антителом, химерным антителом, гуманизированным антителом или его функциональным фрагментом.
18. Антитело или его функциональный фрагмент по п. 17, изотип которого представляет собой IgG2b, IgG2a или IgG3.
19. Антитело или его функциональный фрагмент по п. 1, отличающееся тем, что указанное антитело или его фрагмент связывается с патологическим конформером белка Тау, но не связывается с соответствующим нефосфорилированным эпитопом и/или неродственными эпитопами.
20. Полинуклеотид, кодирующий антитело его функциональный фрагмент по п. 1.
21. Полинуклеотид по п. 20, отличающийся тем, что содержит молекулу нуклеиновой кислоты, выбранную из группы, состоящей из:
а) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, по меньшей мере на 85% идентичную последовательности, представленной в SEQ ID NO: 109, 110, 113, 114, 117 или 119;
б) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, по меньшей мере на 90% идентичную последовательности, представленной в SEQ ID NO: 109, 110, 113, 114, 117 или 119;
в) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, по меньшей мере на 95% идентичную последовательности, представленной в SEQ ID NO: 109, 110, 113, 114, 117 или 119;
г) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, по меньшей мере на 98% идентичную последовательности, представленной в SEQ ID NO: 109, 110, 113, 114, 117 или 119;
д) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, по меньшей мере на 100% идентичную последовательности, представленной в SEQ ID NO: 109, 110, 113, 114, 117 или 119;
е) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, комплементарная цепь которой гибридизуется с молекулой нуклеиновой кислоты по любому из а)-г); или
ж) молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, которая отклоняется от нуклеотидной последовательности, определенной в любом из а)-д) вырождением генетического кода.
22. Фармацевтический состав для лечения, облегчения или защиты от таупатии, содержащий антитело или его функциональный фрагмент по любому из пп. 1-19 или их комбинацию в терапевтически эффективном количестве вместе с фармацевтически приемлемым носителем.
23. Способ лечения, облегчения или защиты от таупатии, включающий введение млекопитающему, страдающему таким заболеванием или расстройством, антитела или его функционального фрагмента по любому из пп. 1-19.
24. Способ по п. 23, отличающийся тем, что таупатия выбрана из группы, состоящей из болезни Альцгеймера, болезни Крейтцфельда - Якоба, деменции боксеров, синдрома Дауна, болезни Герстманна – Штреусслера - Шейнкера, миозита с тельцами включения и вызванной прионными белками амилоидной ангиопатии мозга, травматического повреждения мозга, комплекса амиотрофный латеральный склероз/паркинсонизм-деменция Гуама, негуамских заболеваний двигательных нейронов с нейрофибриллярными сплетениями, деменции с аргирофильными шарами, кортикобазальной дегенерации, диффузных нейрофибриллярных сплетений с кальцификацией, фронтотемпоральной деменции с паркинсонизмом, связанным с хромосомой 17, фронтотемпоральной деменции, болезни Галлервордена - Шпатца, множественной системной атрофии, болезни Ниманна - Пика, тип С, паллидо-понто-нигральной дегенерации, синдрома Пика, прогрессирующего подкоркового глиоза, прогрессирующего супрануклеарного паралича, подострого склерозирующего панэнцефалита лимбической деменции, постэнцефалитного паркинсонизма, миотонической дистрофии.
25. Способ по п. 24, отличающийся тем, что млекопитающее является человеком.
26. Способ индукции пассивной иммунной реакции у животного, конкретно млекопитающего или человека, страдающего таупатией, путем введения указанному животному или человеку антитела или его функционального фрагмента по любому из пп. 1-19.
27. Способ диагностики связанного с белком тау заболевания, расстройства или состояния или предрасположенности к связанному с белком тау заболеванию, расстройству или состоянию у пациента, включающий:
а) приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт с антителом или его функциональным фрагментом по п. 1, причем указанное антитело или его функциональный фрагмент связывается с эпитопом белка тау;
б) обеспечение возможности для антитела связаться с белком тау с образованием иммунологического комплекса;
в) обнаружение образования иммунологического комплекса и
г) установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке тела,
притом что повышение содержания указанного агрегата по сравнению с контрольным нормальным значением указывает на то, что указанный больной страдает от или подвержен риску развития связанного с белком тау заболевания или состояния.
28. Способ мониторинга минимального остаточного заболевания у пациента после лечения антителом против тау, причем указанный способ включает:
а) приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт с антителом или его функциональным фрагментом по п. 1, причем антитело или его функциональный фрагмент связывается с эпитопом белка тау;
б) обеспечение возможности для антитела связаться с белком тау с образованием иммунологического комплекса;
в) обнаружение образования иммунологического комплекса и
г) установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке тела,
притом что повышение содержания указанного иммунологического комплекса по сравнению с контрольным нормальным значением указывает на то, что указанный больной все еще страдает минимальным остаточным заболеванием.
29. Способ прогнозирования ответа больного на лечение антителом против тау, включающий:
а) приведение образца или конкретной части тела или участка тела, где предполагается содержание белка тау, в контакт с антителом или его функциональным фрагментом по п. 1, причем антитело или его функциональный фрагмент связывается с эпитопом белка тау;
б) обеспечение возможности для антитела связаться с белком тау с образованием иммунологического комплекса;
в) обнаружение образования иммунологического комплекса и
г) установление корреляции присутствия или отсутствия иммунологического комплекса с присутствием или отсутствием белка тау в образце или конкретной части тела или участке тела,
д) сравнение количества указанного иммунологического комплекса до и после начала лечения,
притом что снижение содержания указанного иммунологического комплекса указывает на то, что указанный больной демонстрирует высокий потенциал ответа на лечение.
30. Способ посмертного обнаружения мультимеров фосфо-Тау (pTau) в образце мозга субъекта, предположительно страдающего связанным с тау заболеванием или расстройством, причем указанный способ включает:
а) приведение образца мозга субъекта в контакт с антителом или его функциональным фрагментом по п. 2, причем антитело или его функциональный фрагмент связывается с эпитопом белка фосфо-Тау;
б) обеспечение возможности для антитела связаться с белком тау с образованием иммунологического комплекса;
в) обнаружение образования иммунологического комплекса и
г) сравнение содержания или интенсивности иммунологического комплекса в образце, полученном от субъекта, с содержанием или интенсивностью иммунологического комплекса, полученного от здорового контрольного субъекта с применением таких же условий,
притом что повышение содержания или интенсивности указанного иммунологического комплекса по сравнению с контрольным значением указывает на то, что указанный больной страдал от связанного с тау заболевания или расстройства.
31. Диагностический набор для обнаружения и диагностики связанных с белком тау заболеваний, расстройств или состояний, содержащий емкость, вмещающую антитело или его функциональный фрагмент по п. 1, и инструкции по применению антитела или его функционального фрагмента для связывания белка тау с формированием иммунологического комплекса и обнаружения образования иммунологического комплекса, где присутствие или отсутствие иммунологического комплекса коррелирует с присутствием или отсутствием белка тау.
32. Линия клеток, продуцирующая антитело или его функциональный фрагмент по п. 1, которая представляет собой линию клеток гибридомы А4-4А6-48, депонированную от 30 августа 2011 г. под номером DSM АСС3136.
33. Линия клеток, продуцирующая антитело или его функциональный фрагмент по п. 1, которая представляет собой линию клеток гибридомы A6-2G5-30, депонированную от 30 августа 2011 г. под номером DSM АСС3137.
34. Линия клеток, продуцирующая антитело или его функциональный фрагмент по п. 1, которая представляет собой линию клеток гибридомы A6-2G5-41, депонированную от 30 августа 2011 г. под номером DSM АСС3138.
35. Линия клеток, продуцирующая антитело или его функциональный фрагмент по п. 1, которая представляет собой линию клеток гибридомы А4-2А1-18, депонированную от 30 августа 2011 г. под номером DSM АСС3139.
36. Линия клеток, продуцирующая антитело или его функциональный фрагмент по п. 1, которая представляет собой линию клеток гибридомы А4-2А1-40, депонированную от 30 августа 2011 г. под номером DSM АСС3140.
37. Вектор для экспрессии антитела по п. 1, содержащий полинуклеотид по п. 20, причем указанный полинуклеотид является функционально связанным.
38. Клетка-хозяин для получения антитела по п. 1, содержащая вектор по п. 37.
39. Клетка-хозяин по п. 38, которая является клеткой млекопитающего.
40. Клетка-хозяин по п. 38, которая является клеткой яичника китайского хомяка.
41. Способ получения антитела или его функционального фрагмента по п. 1, включающий культивирование клетки-хозяина по п. 38 в условиях, пригодных для экспрессии антитела или его функционального фрагмента, и выделение антитела или фрагмента.
42. Способ обнаружения мультимеров фосфо-Тау (pTau) в образце мозга, включающий:
а) приведение образца в контакт с антителом или его функциональным фрагментом по п. 1, причем антитело или его функциональный фрагмент связывается с эпитопом белка фосфо-Тау;
б) обеспечение возможности для антитела или его фрагмента связаться с белком тау с образованием иммунологического комплекса и
в) обнаружение образования иммунологического комплекса.
| OTVOS L | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| BUÉE-SCHERER V | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| КОНФОРМАЦИОННО АНОМАЛЬНЫЕ ФОРМЫ БЕЛКОВ ТАУ И СПЕЦИФИЧЕСКИЕ АНТИТЕЛА К НИМ | 2002 |
|
RU2299889C2 |
Авторы
Даты
2017-12-21—Публикация
2012-10-05—Подача