Изобретение относится к области нанотехнологии и пищевой промышленности.
Ранее были известны способы получения микрокапсул лекарственных препаратов. Так, в пат. 2092155 (МПК A61K 047/02, A61K 009/16, опубликован 10.10.1997, Российская Федерация) предложен метод микрокапсулирования лекарственных средств, основанный на применении специального оборудования с использованием облучения ультрафиолетовыми лучами.
Недостатками данного способа являются длительность процесса и применение ультрафиолетового излучения, что может оказывать влияние на процесс образования микрокапсул.
В пат. 2095055 (МПК A61K 9/52, A61K 9/16, A61K 9/10, Российская Федерация, опубликован 10.11.1997) предложен способ получения твердых непористых микросфер включает расплавление фармацевтически неактивного вещества-носителя, диспергирование фармацевтически активного вещества в расплаве в инертной атмосфере, распыление полученной дисперсии в виде тумана в замораживающей камере под давлением, в инертной атмосфере, при температуре от -15 до -50°C, и разделение полученных микросфер на фракции по размерам. Суспензия, предназначенная для введения путем парентеральной инъекции, содержит эффективное количество указанных микросфер, распределенных в фармацевтически приемлемом жидком векторе, причем фармацевтически активное вещество микросферы нерастворимо в указанной жидкой среде.
Недостатки предложенного способа: сложность и длительность процесса, применение специального оборудования.
В пат. 2091071 (МПК А61К 35/10, Российская Федерация, опубликован 27.09.1997) предложен способ получения препарата путем диспергирования в шаровой мельнице с получением микрокапсул.
Недостатками способа являются применение шаровой мельницы и длительность процесса.
В пат. 2076765 (МПК B01D 9/02, Российская Федерация, опубликован 10.04.1997) предложен способ получения дисперсных частиц растворимых соединений в микрокапсулах посредством кристаллизации из раствора, отличающийся тем, что раствор диспергируют в инертной матрице, охлаждают и, изменяя температуру, получают дисперсные частицы.
Недостатком данного способа является сложность исполнения: получение микрокапсул путем диспергирования с последующим изменением температур, что замедляет процесс.
В пат. 2101010 (МПК А61К 9/52, А61К 9/50, А61К 9/22, А61К 9/20, А61К 31/19, Российская Федерация, опубликован 10.01.1998) предложена жевательная форма лекарственного препарата со вкусовой маскировкой, обладающая свойствами контролируемого высвобождения лекарственного препарата, содержит микрокапсулы размером 100-800 мкм в диаметре и состоит из фармацевтического ядра с кристаллическим ибупрофеном и полимерного покрытия, включающего пластификатор, достаточно эластичного, чтобы противостоять жеванию. Полимерное покрытие представляет собой сополимер на основе метакриловой кислоты.
Недостатки изобретения: использование сополимера на основе метакриловой кислоты, так как данные полимерные покрытия способны вызывать раковые опухоли; получение микрокапсул методом суспензионной полимеризации; сложность исполнения; длительность процесса.
В пат. 2139046 (МПК А61К 9/50, А61К 49/00, А61К 51/00, Российская Федерация, опубликован 10.10.1999) предложен способ получения микрокапсул следующим образом. Эмульсию масло-в-воде готовят из органического раствора, содержащего растворенный моно-, ди-, триглицерид, предпочтительно трипальмитин или тристеарин и, возможно, терапевтически активное вещество, и водного раствора, содержащего поверхностно-активное вещество, возможно выпаривают часть растворителя, добавляют редиспергирующий агент и смесь подвергают сушке вымораживанием. Подвергнутую сушке вымораживанием смесь затем снова диспергируют в водном носителе для отделения микрокапсул от остатков органических веществ и полусферические или сферические микрокапсулы высушивают.
Недостатками предложенного способа являются сложность и длительность процесса, использования высушивания вымораживанием, что занимает много времени и замедляет процесс получения микрокапсул.
В пат. 2159037 (МПК A01N 25/28, A01N 25/30, Российская Федерация, опубликован 20.11.2000) предложен способ получения микрокапсул реакцией полимеризации на границе раздела фаз, содержащие твердый агрохимический материал 0,1-55 мас. %, суспендированный в перемешивающейся с водой органической жидкости, 0,01-10 мас. % неионного диспергатора, активного на границе раздела фаз и не действующего как эмульгатор.
Недостатки предложенного метода: сложность, длительность, использование высокосдвигового смесителя.
В пат. 2173140 (МПК А61К 009/50, А61К 009/127, Российская Федерация, опубликован 10.09.2001) предложен способ получения кремнийорганолипидных микрокапсул с использованием роторно-кавитационной установки, обладающей высокими сдвиговыми усилиями и мощными гидроакустическими явлениями звукового и ультразвукового диапазона для диспергирования.
Недостатком данного способа является применение специального оборудования - роторно-квитационной установки, которая обладает ультразвуковым действием, что оказывает влияние на образование микрокапсул и при этом может вызывать побочные реакции в связи с тем, что ультразвук разрушающе действует на полимеры белковой природы, поэтому предложенный способ применим при работе с полимерами синтетического происхождения.
В пат. 2359662 (МПК А61К 009/56, A61J 003/07, B01J 013/02, A23L 001/00, опубликован 27.06.2009, Российская Федерация) предложен способ получения микрокапсул с использованием распылительного охлаждения в распылительной градирне Niro при следующих условиях: температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 оборотов/мин. Микрокапсулы по изобретению обладают улучшенной стабильностью и обеспечивают регулируемое и/или пролонгированное высвобождение активного ингредиента.
Недостатками предложенного способа являются длительность процесса и применение специального оборудования, комплекс определенных условий (температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 оборотов/мин).
В пат. WO/2010/076360 ES (МПК B01J 3/00; А61К 9/14; А61К 9/10; А61К 9/12, опубликован 08.07.2010) предложен новый способ получения твердых микро- и наночастиц с однородной структурой с размером частиц менее 10 мкм, где обработанные твердые соединения имеют естественное кристаллическое, аморфное, полиморфное и другие состояния, связанные с исходным соединением. Метод позволяет получить твердые микро- и наночастицы с существенно сфероидальной морфологией.
Недостатком предложенного способа является сложность процесса, что приводит к получению капсул с плавающим выходом.
В пат. WO/2010/119041 ЕР (МПК A23L 1/00, опубликован 21.10.2010) предложен способ получения микрошариков, содержащих активный компонент, инкапсулированный в гель-матрице сывороточного протеина, включающего денатурированный белок, сыворотку и активные компоненты. Изобретение относится к способу получения микрошариков, которые содержат такие компоненты, как пробиотические бактерии. Способ получения микрошариков включает стадию производства микрошариков в соответствии с методом изобретения и последующее отверждение микрошариков в растворе анионный полисахарид с pH 4,6 и ниже в течение не менее 10, 30, 60, 90, 120, 180 минут. Примеры подходящих анионных полисахаридов: пектины, альгинаты, каррагинаны. В идеале, сывороточный протеин является теплоденатурирующим, хотя и другие методы денатурации также применимы, например денатурация индуцированным давлением. В предпочтительном варианте сывороточный белок денатурирует при температуре от 75°С до 80°С, надлежащим образом в течение от 30 минут до 50 минут. Как правило, сывороточный протеин перемешивают при тепловой денатурации. Соответственно, концентрация сывороточного белка составляет от 5 до 15%, предпочтительно от 7 до 12%, а в идеале от 9 до 11% (вес/объем). Как правило, осуществление процесса осуществляется путем фильтрации через множество фильтров с постепенным снижением размера пор. В идеале, фильтр тонкой очистки имеет субмикронных размеров поры, например от 0,1 до 0,9 микрон. Предпочтительным способом получения микрошариков является способ с применением вибрационных инкапсуляторов (Inotech, Швейцария) и машин производства Nisco Engineering AG. Как правило, форсунки имеют отверстия 100 и 600 мкм, а в идеале около 150 микрон.
Недостатком данного способа является применение специального оборудования (вибрационных инкапсуляторов (Inotech, Швейцария)), получение микрокапсул посредством денатурации белка, сложность выделения полученных данным способом микрокапсул - фильтрация с применением множества фильтров, что делает процесс длительным.
В пат. WO/2011/003805 ЕР МПК B01J 13/18; B65D 83/14; C08G 18/00 описан способ получения микрокапсул, которые подходят для использования в композициях, образующих герметики, пены, покрытия или клеи.
Недостатком предложенного способа является применение центрифугирования для отделения от технологической жидкости, длительность процесса, а также применение данного способа не в фармацевтической промышленности.
В пат. 20110223314 МПК B05D 7/00 20060101 B05D 007/00, В05С 3/02 20060101 В05С 003/02; В05С 11/00 20060101 В05С 011/00; B05D 1/18 20060101 B05D 001/18; B05D 3/02 20060101 B05D 003/02; B05D 3/06 20060101 B05D 003/06 от 10.03.2011 US описан способ получения микрокапсул методом суспензионной полимеризации, относящийся к группе химических методов с применением нового устройства и ультрафиолетового облучения.
Недостатком данного способа являются сложность и длительность процесса, применение специального оборудования, использование ультрафиолетового облучения.
В пат. WO/2011/150138 US (МПК C11D 3/37; B01J 13/08; C11D 17/00, опубликован 01.12.2011) описан способ получения микрокапсул твердых растворимых в воде агентов методом полимеризации.
Недостатками данного способа являются сложность исполнения и длительность процесса.
В пат. WO/2011/127030 US (МПК А61К 8/11; B01J 2/00; B01J 13/06; C11D 3/37; C11D 3/39; C11D 17/00, опубликован 13.10.2011) предложено несколько способов получения микрокапсул: межфазной полимеризацией, термоиндуцированным разделением фаз, распылительной сушкой, выпариванием растворителя и др. Недостатками предложенных способов является сложность, длительность процессов, а также применение специального оборудования (фильтр (Albet, Dassel, Германия), распылительной сушилки для сбора частиц (Spray-4M8 Сушилка от ProCepT, Бельгия)).
Недостатками предложенных способов является сложность, длительность процессов, а также применение специального оборудования (фильтр (Albet, Dassel, Германия), распылительной сушилки для сбора частиц (Spray-4М8 Сушилка от ProCepT, Бельгия)).
Наиболее близким методом является способ, предложенный в пат. 2134967 (МПК A01N 53/00, A01N 25/28, опубликован 27.08.1999, Российская Федерация). В воде диспергируют раствор смеси природных липидов и пиретроидного инсектицида в весовом отношении 2-4:1 в органическом растворителе, что приводит к упрощению способа микрокапсулирования.
Недостатком метода является диспергирование в водной среде, что делает предложенный способ неприменимым для получения микрокапсул водорастворимых препаратов в водорастворимых полимерах.
Техническая задача - упрощение и ускорение процесса получения нанокапсул сухого экстракта топинамбура в каррагинане, уменьшение потерь при получении нанокапсул (увеличение выхода по массе).
Решение технической задачи достигается способом получения нанокапсул сухого экстракта топинамбура, отличающимся тем, что в качестве оболочки нанокапсул используется каррагинан, а также получение нанокапсул физико-химическим способом осаждения нерастворителем с использованием осадителя - толуола.
Отличительной особенностью предлагаемого метода является использование в качестве оболочки нанокапсул сухого экстракта топинамбура каррагинана, а также получение нанокапсул физико-химическим способом осаждения нерастворителем с использованием осадителя - толуола.
Результатом предлагаемого метода являются получение нанокапсул сухого экстракта топинамбура в каррагинане при 25°С в течение 15 минут. Выход нанокапсул составляет 100%.
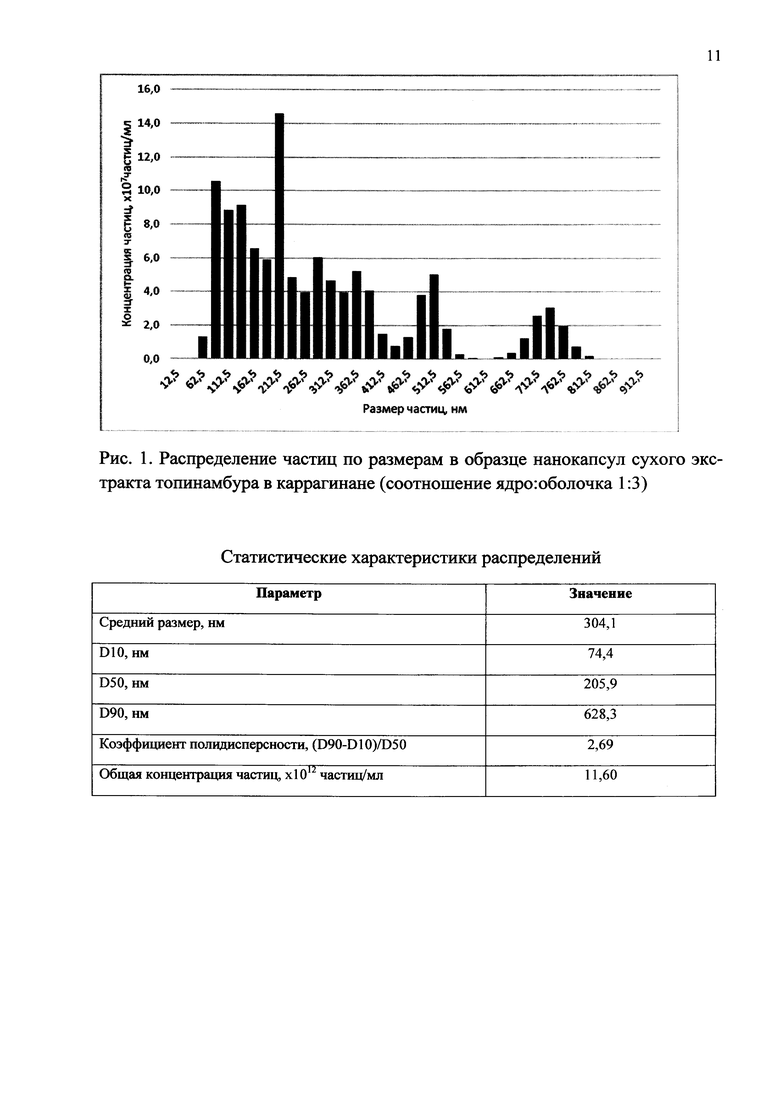
ПРИМЕР 1. Получение нанокапсул сухого экстракта топинамбура, соотношение ядро:оболочка 1:3
К 3 г суспензии каррагинана в бутаноле и 0,01 г препарата Е472с в качестве поверхностно-активного вещества. Полученную смесь ставят на магнитную мешалку и включают перемешивание. 1 г сухого экстракта топинамбура медленно порциями добавляют в суспензию каррагинана в бутаноле. Затем добавляют 5 мл толуола. Полученную суспензию нанокапсул отфильтровывают на фильтре, промывают толуолом, сушат.
Получено 4 г кремового порошка. Выход составил 100%.
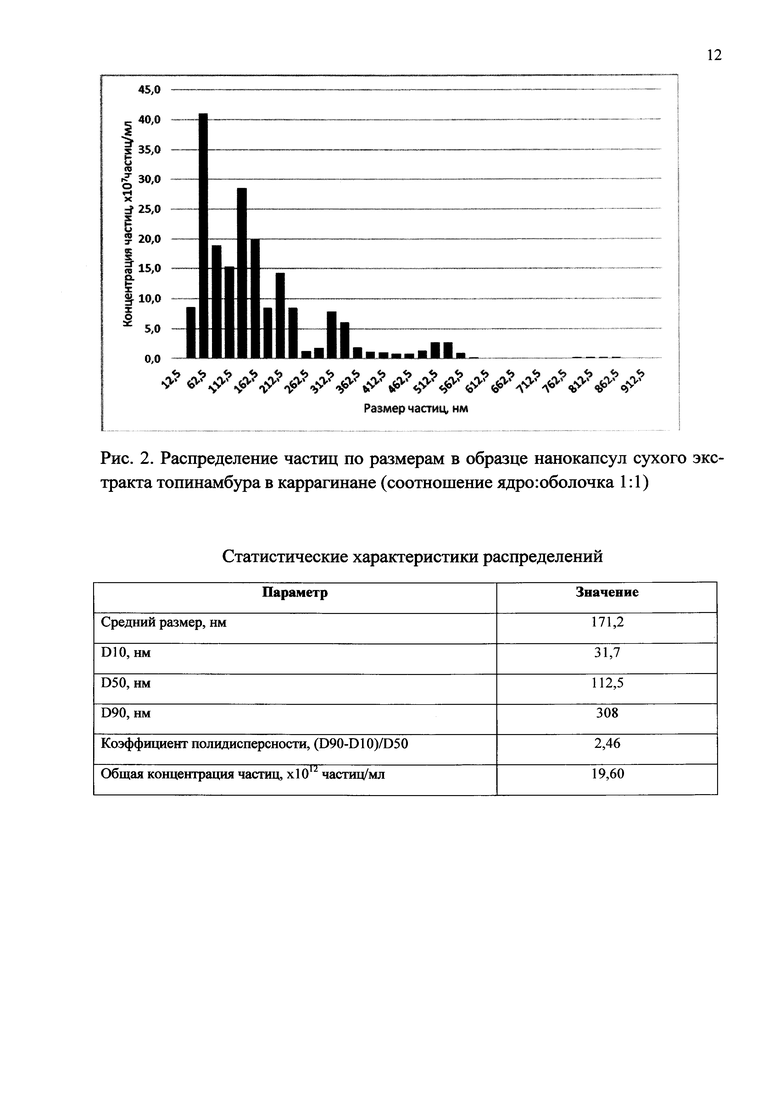
ПРИМЕР 2. Получение нанокапсул сухого экстракта топинамбура, соотношение ядро:оболочка 1:1
К 1 г суспензии каррагинана в бутаноле и 0,01 г препарата Е472с в качестве поверхностно-активного вещества. Полученную смесь ставят на магнитную мешалку и включают перемешивание. 1 г сухого экстракта топинамбура переносят в суспензию каррагинана в бутаноле. После этого добавляют 5 мл толуола. Полученную суспензию нанокапсул отфильтровывают на фильтре, промывают толуолом, сушат.
Получено 2 г с кремовым оттенком порошка. Выход составил 100%.
ПРИМЕР 3Получение нанокапсул сухого экстракта топинамбура, соотношение ядро:оболочка 1:5
К 5 г суспензии каррагинана в бутаноле и 0,01 г препарата Е472с в качестве поверхностно-активного вещества. Полученную смесь ставят на магнитную мешалку и включают перемешивание. 1 г сухого экстракта топинамбура переносят в суспензию каррагинана в бутаноле. После этого добавляют 10 мл толуола. Полученную суспензию нанокапсул отфильтровывают на фильтре, промывают толуолом, сушат.
Получено 6 г с кремовым оттенком порошка. Выход составил 100%.
ПРИМЕР 4. Получение нанокапсул сухого экстракта топинамбура, соотношение ядро:оболочка 5:1
К 1 г суспензии каррагинана в бутаноле и 0,01 г препарата Е472с в качестве поверхностно-активного вещества. Полученную смесь ставят на магнитную мешалку и включают перемешивание. 5 г сухого экстракта топинамбура переносят в суспензию каррагинана в бутаноле. После этого добавляют 10 мл толуола. Полученную суспензию нанокапсул отфильтровывают на фильтре, промывают толуолом, сушат.
Получено 6 г с кремовым оттенком порошка. Выход составил 100%.
ПРИМЕР 5. Определение размеров нанокапсул методом NTA.
Измерения проводили на мультипараметрическом анализаторе наночастиц Nanosight LM0 производства Nanosight Ltd (Великобритания) в конфигурации HS-BF (высокочувствительная видеокамера Andor Luca, полупроводниковый лазер с длиной волны 405 нм и мощностью 45 мВт). Прибор основан на методе анализа траекторий наночастиц (Nanoparticle Tracking Analysis, NTA), описанном bASTM E2834.
Оптимальным разведением для разведения было выбрано 1:100. Для измерения были выбраны параметры прибора: Camera Level=16, Detection Threshold=10 (multi), Min Track Length: Auto, Min Expected Size: Auto. Длительность единичного измерения 215s, использование шприцевого насоса.
Препарат Е472с - сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота как трехосновная может быть этерифицирована другими глицеридами и как оксокислота - другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием.
Получены нанокапсулы сухого экстракта топинамбура в каррагинане физико-химическим методом осаждения нерастворителем с использованием толуола в качестве нерастворителя. Процесс прост в исполнении и длится в течение 15 минут,
Предложенная методика пригодна для косметической и фармацевтической промышленности вследствие минимальных потерь, быстроты, простоты получения и выделения микрокапсул сухого экстракта топинамбура в каррагинане.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения нанокапсул сухого экстракта топинамбура | 2016 |
|
RU2626821C1 |
| Способ получения нанокапсул сухого экстракта топинамбура в ксантановой камеди | 2016 |
|
RU2632428C1 |
| Способ получения нанокапсул сухого экстракта топинамбура | 2016 |
|
RU2640130C2 |
| Способ получения нанокапсул сухого экстракта топинамбура | 2016 |
|
RU2634256C2 |
| Способ получения нанокапсул сухого экстракта топинамбура в пектине | 2017 |
|
RU2641190C1 |
| Способ получения нанокапсул сухого экстракта шпината | 2016 |
|
RU2622752C1 |
| Способ получения нанокапсул сухого экстракта топинамбура в геллановой камеди | 2016 |
|
RU2640490C2 |
| Способ получения нанокапсул стрептоцида в каппа-каррагинане | 2017 |
|
RU2657767C1 |
| Способ получения нанокапсул антибиотиков в геллановой камеди | 2014 |
|
RU2619328C2 |
| Способ получения нанокапсул сульфата глюкозамина в альгинате натрия | 2016 |
|
RU2647439C1 |

Изобретение относится к области нанотехнологии, в частности к способу получения нанокапсул, и описывает способ получения нанокапсул сухого экстракта топинамбура. Способ характеризуется тем, что к суспензии, содержащей каррагинан в бутаноле и препарат Е472с в качестве поверхностно-активного вещества, добавляют сухой экстракт топинамбура, после этого добавляют толуол, полученную суспензию нанокапсул отфильтровывают, промывают толуолом, сушат, при этом соотношение ядро:оболочка составляет 1:1, 1:3, 1:5 или 5:1. Способ обеспечивает упрощение и ускорение процесса получения нанокапсул, уменьшение потерь при получении нанокапсул и может быть использован в пищевой промышленности. 3 ил., 5 пр.
Способ получения нанокапсул сухого экстракта топинамбура, который характеризуется тем, что к суспензии, содержащей каррагинан в бутаноле и препарат Е472с в качестве поверхностно-активного вещества, добавляют сухой экстракт топинамбура, после этого добавляют толуол, полученную суспензию нанокапсул отфильтровывают, промывают толуолом, сушат, при этом соотнощение ядро:оболочка составляет 1:1, 1:3, 1:5 или 5:1.
| NAGAVARMA B | |||
| V | |||
| N | |||
| Different techniques for preparation of polymeric nanoparticles, Asian Journal Pharm Clin Res, vol.5, suppl 3, 2012, стр.16-23 | |||
| WO 2004064544 A1, 05.08.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ | 2012 |
|
RU2496483C1 |
| Биологический энциклопедический словарь | |||
| Гл | |||
| ред | |||
| М | |||
| С | |||
| Гиляров; Редкол.: А | |||
| А | |||
| Бабаев, Г | |||
| Г | |||
| Винберг, Г | |||
| А | |||
| Заварзин и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| — М.: Сов | |||
| Энциклопедия, 1986 | |||
| ЧУЕШОВ В.И | |||
| Промышленная технология лекарств | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Передвижная комнатная печь | 1922 |
|
SU383A1 |
Авторы
Даты
2017-12-26—Публикация
2016-04-18—Подача