ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к области конъюгатов терапевтически активных одноцепочечных антисмысловых LNA-олигонуклеотидов (LNA-закрытая нуклеиновая кислота). В изобретении предложены терапевтически активные конъюгаты углевода и LNA-олигонуклеотида, обладающие повышенной эффективностью, увеличенным терапевтическим индексом и пониженной токсичностью.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Конъюгаты олигонуклеотидов интенсивно изучали с целью их использования в миРНК, поскольку они считаются незаменимыми для обеспечения надлежащей эффективности in vivo. Например, WO 2004/044141 относится к модифицированным олигомерным соединениям, изменяющим экспрессию генов за счет РНК-интерференции. Олигомерные соединения включают одну или несколько конъюгатных группировок, способных модифицировать или улучшать фармакокинетические или фармакодинамические свойства связанных с ними олигомерных соединений.
WO 2012/083046 описывает кластер галактозы - компонент для адресной доставки миРНК.
В отличие от этого, одноцепочечные антисмысловые олигонуклеотиды в целях терапии обычно вводят без конъюгирования или включения в состав композиций. Основными тканями-мишенями для антисмысловых олигонуклеотидов являются печень и почки, хотя антисмысловые нуклеотиды могут воздействовать и на другие ткани, включая лимфоузлы, селезенку и костный мозг.
Согласно van Poelgeest et al. (American Journal of Kidney Disease, в печати) введение антисмысловых олигонуклеотидов LNA в клинических исследованиях могло приводить к острому почечному повреждению у человека. Согласно Swayze et al, NAR, Dec. 2006 (онлайн публикация) антисмысловые олигонуклеотиды, содержащие закрытые нуклеиновые кислоты, более эффективны, однако обладают выраженной гепатотоксичностью у животных.
WO 2004/087931 описывает олигонуклеотиды, содержащие кислотолабильный гидрофильный полимерный конъюгат (ПЭГ).
WO 2005/086775 описывает адресную доставку лекарственных средств к определенным органам с применением терапевтически активного химического компонента, расщепляемого линкера и метки. Расщепляемые линкеры, например, могут представлять собой дисульфидную группу, пептид или расщепляемый рестрикционным ферментом олигонуклеотидный домен.
WO 2011/126937 описывает адресную доставку внутрь клеток олигонуклеотидов, конъюгированных с низкомолекулярными лигандами.
WO 2009/025669 описывает полимерные линкеры (полиэтилен гликоля), содержащие пиридил дисульфид. См. также Zhao et al., Bioconjugate Chem. 2005 16 758-766.
Chaltin et al., Bioconjugate Chem. 2005 16 827-836 описывает модифицированные холестерином моно-, ди- и тетрамерные олигонуклеотиды, используемые для включения антисмысловых олигонуклеотидов в катионные липосомы, для получения дендримерных систем доставки. Холестерин конъюгирован с олигонуклеотидом при помощи лизинового линкера.
Другие нерасщепляемые конъюгаты холестерина используют для адресной доставки в печень миРНК и антагомир, см., например, Soutscheck et al., Nature 2004 vol. 432 173-178 и Krützfeldt et al., Nature 2005 vol 438, 685-689. Применение холестерина в качестве компонента, обеспечивающего адресную доставку в печень, принципиально важно для активности частично тиофосфорилированных миРНК и антагомиров in vivo.
Bhat et al. (AASLD, 7-11 ноября 2013, постер) представили данные доклинических исследований о применении конъюгата анти-миРНК с GalNac, RG-101, блокирующего миРНК-122. Информация о том, что представляет собой RG-101, отсутствует.
Данное изобретение основано на том, что конъюгация LNA-олигонуклеотидов с углеводным конъюгатом, таким как конъюгат GalNAc, позволяет значительно улучшить активность, биораспределение и терапевтический индекс одноцепочечных антисмысловых LNA-олигонуклеотидов.
РОДСТВЕННЫЕ ЗАЯВКИ
В данной заявке испрашивается приоритет заявок ЕР 13153296.2 (подана 2013-01-30), ЕР 13157237.2 (подана 2013-02-28), ЕР 13174092.0 (подана 2013-06-27), ЕР 13192938.2 (подана 2013-11-14), ЕР 13192931.7 (подана 2013-11-14), ЕР 13192930.9 (подана 2013-11-14), РСТ/ЕР2013/073859 (подана 2013-11-14) и РСТ/ЕР2013/073859 (подана 2013-11-14), содержание которых включено путем ссылки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В изобретении предложен антисмысловой LNA-олигомер (который в данном документе может обозначаться как сегмент А), содержащий антисмысловой олигомер и конъюгатную группировку, обеспечивающий адресное взаимодействие с асиалогликопротеиновым рецептором, такой как GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С).
В изобретении предложен антисмысловой LNA-олигомер (который в данном документе может обозначаться сегментом А), содержащий антисмысловой олигомер и компонент GalNAc, например, тривалентный компонент GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С).
В изобретении предложен антисмысловой LNA-олигомер гэпмер (который в данном документе может обозначаться сегментом А), содержащий антисмысловой LNA-олигомер гэпмер и конъюгатную группировку, обеспечивающий адресное взаимодействие с асиалогликопротеиновым рецептором, такой как GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С). Мишенью антисмыслового LNA-олигомера гэпмера может быть, например, мРНК или вирусная РНК.
В изобретении предложен антисмысловой LNA-олигомер миксмер (который в данном документе может обозначаться сегментом А), содержащий антисмысловой LNA-олигомер миксмер и конъюгатную группировку, обеспечивающую адресное взаимодействие с асиалогликопротеиновым рецептором, такой как GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С). Мишенью антисмыслового LNA-олигомера миксмера может быть, например, мРНК или сайт сплайсинга мРНК или микроРНК.
В изобретении предложен антисмысловой LNA-олигомер тоталмер (totalmer) (который в данном документе может обозначаться сегментом А), содержащий антисмысловой LNA-олигомер тоталмер и конъюгатную группировку, обеспечивающую адресное взаимодействие с асиалогликопротеиновым рецептором, такой как GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С). Мишенью антисмыслового LNA-олигомера миксмера может быть, например, микроРНК.
Антисмысловой LNA-олигомер может быть длиной от 7 до 30, например, от 8 до 26, или, в некоторых воплощениях, от 8 до 18 нуклеозидов и может содержать по меньшей мере одно LNA-звено (нуклеозид). Таким образом, в изобретении предложен конъюгат антисмыслового LNA-олигомера, содержащий антисмысловой олигомер и конъюгатную группировку, обеспечивающую адресное взаимодействие с асиалогликопротеиновым рецептором, такой как GalNAc, который может быть частью другого сегмента (обозначаемого сегментом С).
В изобретении предложен антисмысловой LNA-олигомер, ковалентно присоединенный к (например, связанный с) углеводному компоненту (не являющемуся нуклеозидом), такому как конъюгированный углеводный компонент. В некоторых воплощениях углеводный компонент не является линейным углеводным полимером. При этом углеводный компонент может быть мультивалентным, например, к олигомеру могут быть ковалентно присоединены 2, 3, 4 или 4 идентичных или неидентичных углеводных компонента, возможно, посредством линкера или линкеров.
В изобретении предложен антисмысловой LNA-олигомер (конъюгат), содержащий антисмысловой олигомер и конъюгатную группировку, содержащую углевод, такой как конъюгированный углеводный компонент.
В изобретении предложена фармацевтическая композиция, содержащая олигомерное LNA-соединение по изобретению, а также фармацевтически приемлемый разбавитель, носитель, соль или адъювант.
В изобретении предложено олигомерное соединение по изобретению для применения с целью ингибирования в клетке нуклеиновой кислоты-мишени. В некоторых воплощениях применение представляет собой применение in vitro. В некоторых воплощениях применение представляет собой применение in vivo.
В изобретении предложено олигомерное соединение по изобретению для применения в медицине, например, для применения в качестве лекарственного средства. В изобретении предложено олигомерное соединение по изобретению для применения в лечении заболевания или нарушения.
В изобретении предложено применение олигомерного соединения по изобретению в изготовлении лекарственного средства для лечения заболевания или нарушения, например, метаболического заболевания или нарушения.
В изобретении также предложен LNA-олигомер, содержащий сегмент из 8-24 смежных нуклеозидов, связанных фосфоротиоатными связями, а также содержащий от 1 до 6 ДНК-нуклеозидов, смежных с LNA-олигомером, при этом связи, расположенные между ДНК-нуклеозидами и/или рядом с ДНК-нуклеозидом(ами), являются лабильными в физиологических условиях, например, такими как фосфодиэфирные связи. Такие LNA-олигомеры могут находиться в форме конъюгата, как описано в данном документе. В этом случае конъюгат может, например, представлять собой углевод, такой как конъюгат GalNac, кластер GalNac, например, триGalNac, или другой конъюгат, согласно данному описанию.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1: Стадия конъюгации LNA-олигонуклеотида и GalNac.
Фиг. 2: Количество белка FVII.
Фиг. 3: Количество мРНК FVII.
Фиг. 4а-d: Пример 3 - количество FVII в сыворотке.
Фиг. 5а-d: Пример 3 - уровень мРНК FVII в печени.
Фиг. 6: Пример 3 - содержание олигонуклеотидов в печени и почках.
Фиг. 7a и b: Подавление экспрессии мРНК АроВ in vivo с использованием различных конъюгатов моноGalNAc. Мыши получали различные конъюгаты АроВ моно-GalNAc, либо не содержащие биорасщепляемого линкера, либо содержащие дитио-линкер (SS), либо ДНК/РО-линкер (РО) (А), а также проводили сравнение моноGalNAc с ДНК/РО-линкером с кластером GalNAc (В). РНК выделяли из образцов печени (А) и почек (В) и исследовали на предмет снижения экспрессии мРНК АроВ. Приведены данные в сравнении с физиологическим раствором (=1).
Фиг. 8: Пример 5 - экспрессия мРНК АроВ.
Фиг. 9: Пример 5 - общий холестерин сыворотки.
Фиг. 10: Пример 5 - содержание олигонуклеотидов в печени и почках.
Фиг. 11: Пример 6 - количество FVII в сыворотке.
Фиг. 12: Пример 6 - количество мРНК FVII в печени.
Фиг. 13: Примеры соединений и конъюгатных группировок, использованных в Примерах.
Фиг. 14: Примеры конъюгатов три-GalNac, которые можно использовать. Конъюгаты 1-4 являются примерами 4 подходящих конъюгированных компонентов GalNac, а конъюгаты 1а-4а представляют те же конъюгаты с дополнительным линкерным компонентом (Y), который используют для связывания конъюгата с олигомером (сегмент А) или с биорасщепляемым линкером (таким как сегмент В). Волнистой линией обозначена ковалентная связь с олигомером.
Фиг. 15: Экспрессия Kim-1 при исследовании безопасности на крысах (см. Пример 10).
Фиг. 16: Уровни АроВ и холестерина липопротеидов низкой плотности (LDL-C) у мышей, получавших соединения с последовательностью SEQ ID NO 32 или 17 в дозе 1 или 2,5 мг/кг однократно.
Фиг. 17: Подавление экспрессии миР-122 в печени мышей с использованием миниатюрных LNA, спаривающихся с последовательностью т.н. "seed region" (сайт узнавания мишени) (seed-targeting tiny LNA). (а) Нозерн-блот-анализ РНК печени мышей, получавших внутривенно 3 дозы по 20 мг/кг миниатюрных анти-миР-122, пентадекамера анти-миР-122 или рандомизированных контрольных LNA или физиологический раствор.
Фиг. 18: Исследование общего холестерина перед введением, на 4 и 7 сутки. Холестерин повышен вследствие снижения миР-122.
Фиг. 19: Экспрессию Aldo А и Bckdk исследовали с помощью стандартной TaqMan Q-PCR. Уровень мРНК этих генов повышен вследствие снижения миРНК-122.
Фиг. 20: АЛТ определяли в сыворотке, полученной в конце эксперимента (на 7 сутки) для оценки переносимости соединений.
Фиг. 21: Для оценки антивирусного эффекта LNA-соединений с последовательностями SEQ ID 55 и SEQ ID 56 исследовали репликацию вируса в печени мышей Balb/C через 7 дней после гидродинамической инъекции в хвостовую вену pAAV2/HBV. Соединения вводили в/в однократно за 24 ч до гидродинамической инъекции, в той же дозе, что и препарат сравнения энтекавир, который вводили ежедневно перорально, начиная через 24 ч после гидродинамической инъекции. Количественное определение ДНК HBV выполняли с помощью qPCR и результаты выражали в виде геномных эквивалентов на 100 нг ДНК печени.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Изобретение относится к соединениям LNA-олигомеров, таким как антисмысловые LNA-олигонуклеотиды, ковалентно связанным с ненуклеотидными конъюгированными группами углеводов.
Олигомер
В изобретении предложен конъюгат антисмыслового олигомера закрытых нуклеиновых кислот (LNA-олигомера), содержащий антисмысловой LNA-олигомер и конъюгатную группировку, содержащую углевод, такой как конъюгированный углеводный компонент, ковалентно связанный с антисмысловым LNA-олигомером.
Данное изобретение относится к соединениям LNA-олигомеров (также обозначаемым как LNA-олигомеры или LNA-олигонуклеотиды) для применения с целью модулирования, например, ингибирования в клетке нуклеиновой кислоты-мишени. LNA-олигомер содержит по меньшей мере один LNA-нуклеозид (от англ. Locked Nucleic Acid, закрытая (замкнутая, запертая) нуклеиновая кислота), например, нуклеозид, содержащий ковалентный мостик (также обозначаемый радикалом) между атомами во 2' и 4' положениях (связь 2'-4'). LNA-нуклеозиды также обозначают «бициклическими нуклеозидами». LNA-олигомер обычно представляет собой одноцепочечный антисмысловой олигонуклеотид.
В некоторых воплощениях LNA-олигомер содержит или представляет собой гэпмер. В некоторых воплощениях LNA-олигомер содержит или представляет собой миксмер. В некоторых воплощениях LNA олигомер содержит или представляет собой тоталмер.
В некоторых воплощениях все аналоги нуклеозидов, присутствующие в олигомере, представляют собой LNA, а олигомер необязательно может также содержать РНК или ДНК, например, ДНК-нуклеозиды (например, в составе гэпмера или миксмера).
В различных воплощениях соединение по изобретению не содержит (звенья) РНК. В некоторых воплощениях олигомер имеет последовательность смежных нуклеотидов, которые представляют собой линейную молекулу или синтезируются в виде линейной молекулы. Олигомер, таким образом, может быть одноцепочечной молекулой. В некоторых воплощениях олигомер не содержит коротких сегментов, например, по меньшей мере из 3, 4 или 5 смежных нуклеотидов, которые комплементарны гомологичным сегментам в составе самого олигомера (т.е. дуплексов). В некоторых воплощениях олигомер может (по существу) не быть двуцепочечным. Олигомер по существу не является двуцепочечным, так же как и миРНК. В некоторых воплощениях олигомерное соединение не находится в форме дуплекса с (по существу) комплементарным олигонуклеотидом - т.е. не является миРНК.
Длина
Термин «олигомер» в контексте данного изобретения обозначает молекулу, образованную путем ковалентного связывания двух или более нуклеотидов (т.е. олигонуклеотид). В данном документе одиночный нуклеотид (звено) может также обозначаться мономером или звеном. В некоторых воплощениях термины «нуклеозид», «нуклеотид», «звено» и «мономер» используют взаимозаменяемо. Считается, что при упоминании последовательности нуклеотидов или мономеров имеют в виду последовательность оснований, таких как А, Т, G, С или U.
Олигомер может содержать или состоять из последовательности смежных нуклеотидов длиной приблизительно от 7 до 30, например, от 7 до 26 или от 8 до 25, например, длиной 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 нуклеотидов, например, длиной от 10 до 20 нуклеотидов. В некоторых воплощениях длина олигомера LNA составляет 10-16 нуклеотидов, например, 12, 13 или 14 нуклеозидов. В некоторых воплощениях, олигомер LNA имеет 7, 8, 9 нуклеозидов в длину, как, например, миниатюрные LNA ("Tiny" LNA).
В некоторых воплощениях олигомеры также содержат или состоят из последовательности смежных нуклеотидов общей длиной от 10 до 22, например, от 12 до 18, например, от 13 до 17 или от 12 до 16, например, 13, 14, 15, 16 смежных нуклеотидов.
В некоторых воплощениях олигомеры также содержат или состоят из последовательности смежных нуклеотидов общей длиной 10, 11, 12, 13 или 14 смежных нуклеотидов.
В некоторых воплощениях олигомер по изобретению состоит не более чем из 22 нуклеотидов, например, не более чем из 20 нуклеотидов, например, не более чем из 18 нуклеотидов, например, из 15, 16 или 17 нуклеотидов. В некоторых воплощениях олигомер по изобретению содержит менее 20 нуклеотидов. Считается, что когда длина олигомера или последовательности смежных нуклеотидов выражена в виде диапазона, она включает нижний и верхний пределы диапазона, например, диапазон от 10 до 30 (или между 10 и 30) включает как 10, так и 30.
В некоторых воплощениях применение конъюгатов углеводов по изобретению оказалось особенно подходящим для коротких LNA-олигомеров, включая короткие гэпмеры, миксмеры или тоталмеры (миниатюрные LNA), таких как LNA-олигомеры из менее чем 20, например, менее 18, менее 16 нуклеотидов или менее 15 или 14 нуклеотидов или менее.
Межнуклеозидные связи
В некоторых воплощениях межнуклеозидные связи LNA-олигомеров содержат по меньшей мере одну межнуклеозидную связь, отличную от фосфодиэфирной, например, по меньшей мере одна, например, по меньшей мере 50%, например, по меньшей мере 75%, например, по меньшей мере 90%, например, по меньшей мере 100% межнуклеозидных связей в сегменте А отличаются от фосфодиэфирных. В некоторых воплощениях отличные от фосфодиэфирных межнуклеозидные связи представляют собой серосодержащие межнуклеозидные связи, такие как фосфоротиоатная, фосфородитиоатная, такие как фосфоротиоатная.
В некоторых воплощениях LNA-олигомер может содержать по меньшей мере одну фосфоротиоатную межнуклеозидную связь, например, по меньшей мере две, три или четыре фосфоротиоатных связи, а в некоторых воплощениях по меньшей мере 50% межнуклеозидных связей могут быть фосфоротиоатными, например, по меньшей мере 75%, по меньшей мере 90% или все межнуклеозидные связи (кроме тех, что могут присутствовать в отщепляемом линкере) могут быть фосфоротиоатными. В некоторых воплощениях межнуклеозидные связи между двумя концевыми нуклеозидами на 5' конце, на 3' конце или на 5' и на 3' концах (кроме связей в сегменте В, если таковой существует) представляют собой серосодержащие межнуклеозидные связи, такие как фосфоротиоатные. В некоторых воплощениях олигомер содержит по меньшей мере один сегмент последовательно расположенных ДНК-нуклеозидов, например, сегмент из 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 последовательно расположенных ДНК-нуклеозидов, в котором межнуклеозидные связи между ДНК-нуклеозидами представляют собой серосодержащие межнуклеозидные связи, такие как фосфоротиоатные. В некоторых воплощениях в центральном сегменте гэпмера (Y), который обычно содержит сегмент последовательно расположенных ДНК-нуклеозидов, между нуклеозидами имеются серосодержащие межнуклеозидные связи, такие как фосфоротиоатные, например, между последовательно расположенными ДНК-нуклеозидами и/или между ДНК-нуклеозидами и аналогами нуклеозидов, такими как нуклеозиды с модифицированными углеводами, обозначаемыми в данном документе LNA.
Другие примеры межнуклеозидных связей, которые могут использоваться в олигомерах, включают метилфосфонатную (СН3Р=O) и метилтионофосфатную (CH3P=S) и боранофосфатную.
Нуклеозиды закрытых нуклеиновых кислот (LNA)
Бициклические аналоги нуклеозидов (LNA-нуклеозиды) включают аналоги нуклеозидов, которые обычно содержат мостик (или бирадикал), соединяющий второй и четвертый атом углерода в кольце рибозы (мостик С4*-С2* или бирадикал). Наличие бирадикала между 2 и 4 углеродом запирает рибозу в 3' эндо-конформации, и поэтому бициклические аналоги нуклеозидов, содержащие С4*-С2* бирадикал, часто обозначают закрытыми нуклеиновыми кислотами (от англ. Locked nucleic acid, LNA) или бициклическими нуклеиновыми кислотами (от англ. bicyclic nucleic acids, BNA). Термины LNA и BNA в данном документе используют взаимозаменяемо.
В некоторых воплощениях некоторые или все нуклеозиды в составе LNA-олигомера могут быть модифицированными нуклеозидами, которые в данном документе также обозначают аналогами, например, аналогами с модифицированными углеводами, например, бициклическими аналогами нуклеозидов (например, LNA) и/или 2' замещенными аналогами нуклеозидов. В некоторых воплощениях все аналоги нуклеозидов, присутствующие в составе олигомера, содержат одинаково модифицированные углеводы, например, все являются бициклическими аналогами нуклеозидов, и могут быть (возможно, независимо) выбраны из группы, состоящей из бета-D-X-LNA или альфа-L-X-LNA (где X обозначает окси, амино или тио), или другими LNA, описанными в данном документе, включая (R/S) сЕТ, сМОЕ или 5'-Me-LNA, но не ограничиваясь ими.
В некоторых воплощениях, олигомер может содержать по меньшей мере один бициклический нуклеозид (LNA) и по меньшей мере еще один аналог нуклеозида, например, один или несколько 2'замещенных нуклеозидов. В некоторых воплощениях некоторые или все нуклеозиды в олигомере могут быть модифицированными нуклеозидами, которые в данном документе также обозначают аналогами нуклеозидов.
В некоторых воплощениях первый сегмент содержит по меньшей мере один, например, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24 или 25 аналогов нуклеозидов. В некоторых воплощениях аналоги нуклеозидов (возможно, независимо) выбирают из группы, состоящей из бициклических аналогов нуклеозидов (таких как LNA) и/или 2'замещенных аналогов нуклеозидов, например, (возможно, независимо) выбранных из группы, состоящей из звеньев 2'-O-алкил-РНК, звеньев 2'-ОМе-РНК, звеньев 2'-амино-ДНК, 2'-АР, 2'-FANA, 2'-(3-гидрокси)пропил и звеньев 2'-фтор-ДНК и/или других (возможно) аналогов нуклеозидов с модифицированным углеводом, таких как морфолино, пептидно-нуклеиновые кислоты (PNA, от англ. peptide nucleic acid), CeNA, раскрытые нуклеиновые кислоты (UNA, от англ. unlocked nucleic acid), гексит-нуклеиновые кислоты (HNA, от англ. hexitol nucleic acid), бицикло-HNA (см., например, WO 2009/100320). В некоторых воплощениях аналоги нуклеозидов повышают аффинность первого сегмента к его нуклеиновой кислоте-мишени (или комплементарной последовательности ДНК или РНК). Различные аналоги нуклеозидов описаны в публикациях Freier & Altmann; Nucl. Acid Res., 1997, 25, 4429-4443 и Uhlmann; Curr. Opinion in Drug Development, 2000, 3(2), 293-213, содержание которых включено путем ссылки.
В некоторых воплощениях меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, например, все аналоги нуклеозидов, содержащиеся в составе LNA-олигомера (или все нуклеозиды, содержащиеся в составе тоталмера), являются бициклическими аналогами нуклеозидов, такими как LNA, например, бета-D-X-LNA или альфа-L-X-LNA (где X обозначает окси, амино или тио) или другими LNA, описанными в данном документе, включая (R/S) сЕТ, сМОЕ или 5'-Me-LNA, но не ограничиваются ими. В некоторых воплощениях LNA олигомер содержит ДНК и аналоги нуклеозидов с модифицированными углеводами, такие как бициклические аналоги нуклеозидов и/или 2' замещенные аналоги нуклеозидов. В некоторых воплощениях олигомер содержит звенья нуклеозидов ДНК и LNA.
WO 05/013901, WO 07/027775, WO 07027894 описывают олигомеры, в которых каждый нуклеозид является 2' замещенным, например, 2'-O-МОЕ. В некоторых воплощениях первый сегмент олигомера может содержать 2' замещенные нуклеозиды. WO 07/027775 также описывает миксмеры МОЕ, LNA, ДНК для адресного взаимодействия с микроРНК.
Мишень
Конъюгаты LNA-олигомеров по изобретению обычно применяют для адресного взаимодействия с нуклеиновой кислотой-мишенью, обозначаемой в данном документе мишенью. В некоторых воплощениях олигомер по изобретению применяют, например, для модулирования нуклеиновой кислоты (т.е. мишени), выбранной из группы, состоящей из мРНК, микроРНК, длинной некодирующей рНК (IncPHK, от англ. long non-coding РНК), малой ядерной РНК (snРНК, от англ. small nuclear РНК), малой ядрышковой РНК (snoРНК, от англ. small nucleolar РНК) и вирусной РНК.
В некоторых воплощениях мишенью олигомера является РНК, экспрессируемая в печени, например, экспрессируемая в печени мРНК или микроРНК. В некоторых воплощениях мишенью антисмыслового LNA-олигомера является мРНК, выбранная из группы, состоящей из фактора VII, PCSK9, АроВ, GCGR, CRP, DGAT2, GCCR, PTEN, РТР1В, SGLT2 и SOD1 (см., например, WO 2007/146511, содержание которого включено путем ссылки. В частности, в данный документ включена Таблица из WO'511, приведенная на с. 42-43). В некоторых воплощениях мишень может быть выбрана из группы, состоящей из: АроВ человека NM 000384.1, АроВ мыши ХМ 137955.5, натрий-глюкозного котранспортера 2 типа, или SGLT2 (от англ. sodium-glucose cotransporter 2) человека NM 003041.1, пропротеиновой конвертазы субтилизин-кексинового типа 9, или PCSK9 (от англ. proprotein convertase subtilisin/kexin type 9) человека NM 174936.2, супероксиддисмутазы, или SODI (от англ. superoxide dismutase) человека Х02317, С-реактивного белка, или CRP (от англ. C-reactive protein) человека NM 000567.1, глюкагонового рецептора, или GCCR (от англ. glucagon receptor) мыши ВС031885.1, GCGR человека NM 000160.1, диацилглицерин ацилтрансферазы 2 типа, или DGAT2 (от англ. Diacylglycerol O-Acyltransferase 2) человека NM 032564.2, протеиновой тирозинфосфатазы типа 1В, или PTPIB (от англ. protein tyrosine phosphatase IB) человека NM 002827.2, фосфатазы и гомолога тензина, или PTEN (от англ. Phosphatase and tensin homolog) мыши U92437.1, PTEN человека NM 000314.4 (приведенные ссылки представляют учетные номера в базе данных GENBANK), коагуляционного фактора VII, С6 компонента комплемента и транстиретина, или TTR (от англ. transthyretin). Нуклеотидная последовательность, кодирующая фактор VII, включает: Последовательность с учетным номером GENBANK NM 000131.3, последовательность с учетным номером GENBANK NM 019616.2, нуклеотиды с 1255000 по 5 1273000 в последовательности с учетным номером GENBANK NT 027140.6, последовательность с учетным номером GENBANK NM 010172.3 и нуклеотиды с 10024000 по 10037000 в последовательности с учетным номером GENBANK NT 039455.6, но не ограничивается ими. Нуклеотидные последовательности компонента комплемента С6 включают ВС035723.1, J05024.1 GI: 187824 и J05064.1 GI: 179703. См. также ЕР 2320925 А2, где изложены LNA-олигонуклеотиды, мишенью которых является С6 компонент комплемента. Нуклеотидные последовательности TTR (транстиретина) включают ВС020791.1 GI:18089144 и ВС005310.1 GI:13529049.
Примеры LNA-олигомеров, мишенью которых является PCSK9, приведены в WO 2008/043753 и WO 2001/009697, содержание которых включено путем ссылки.
Примеры LNA-олигомеров, мишенью которых является АроВ, приведены в WO 2010014280 и WO 2008/113830, содержание которых включено путем ссылки.
В некоторых воплощениях мишень может представлять собой мРНК Bcl2 - см. WO 2005/061710, где описаны LNA-олигомеры, мишенью которых является Bcl2 (например, М13994.1 GI: 179366).
Мишень может представлять собой РНК, которая экспрессируется в печени. Мишень может представлять собой мишень, экспрессируемую в печени, связанную с заболеванием или нарушением. С печенью связаны различные метаболические нарушения, и в некоторых воплощениях их можно лечить с применением соединений по изобретению. Мишени ассоциированных с печенью метаболических заболеваний или нарушений включают, например, Аро-В (высокий уровень холестерина ЛПНП, острый коронарный синдром), ApoCIII (повышенный уровень триглицеридов сыворотки), АроА (сердечно-сосудистые заболевания), FGFR4 (ожирение), GCCR (диабет 2 типа), GCGR (диабет 2 типа), РТР1В (диабет 2 типа), DGAT2 (неалкогольный стеатогепатит), PCSK9 (гиперлипидемия и родственные ей нарушения), MtGPAT, миР-122 (высокий уровень холестерина) и миР-33 (метаболический синдром, атеросклероз).
Мишень может представлять собой вирусную нуклеиновую кислоту, например, вирусную РНК. Примеры включают вирусы гепатита, например, вирус гепатита В и гепатита С (HCV). Вирусные гепатиты включают гепатиты А, В, С, D и Е. Антисмысловые LNA-олигомеры, мишенью которых является HCV, описаны, например, в публикации Laxton et al., Antimicrobial Agents and Chemotherapy 2011 Vol 55 3105-3114.
Таким образом, олигомер может найти применение в лечении связанных (или ассоциированных) с печенью метаболических заболеваний, которые в данном документе обозначают метаболическими заболеваниями печени. Связанные с печенью метаболические заболевания включают, например, метаболический синдром, ожирение, гиперлипидемию, атеросклероз, нарушение соотношения ЛПВП и ЛПНП, дислипидемии, например, семейную комбинированную гиперлипидемию (СКГЛ), приобретенную гиперлипидемию, резистентную к терапии статинами гиперхолестеринемию, сердечно-сосудистые заболевания, атеросклеротическую болезнь сердца и ишемическую болезнь сердца (ИБС), атеросклероз, болезни сердца, диабет (1 и/или 2 типа), неалкогольный стеатогепатит, острый коронарный синдром (ОКС). В некоторых воплощениях связанное или ассоциированное с печенью заболевание или нарушение ассоциировано с экспрессией, например, повышенной экспрессией нуклеиновой кислоты-мишени в печени.
В некоторых воплощениях, например, когда мишенью является микроРНК-122, заболевание может представлять собой вирусное заболевание, такое как гепатит, включая гепатит В и гепатит С, или метаболическое заболевание, связанное с повышением холестерина, такое как атеросклероз и гиперлипидемия и родственные им нарушения. Олигомеры, мишенями которых является миР-122, также могут применяться для улучшения функции печени (см., например, РСТ/ЕР2012/071934), для лечения некротического воспаления, для улучшения концентрации биомаркеров функции печени в сыворотке, для предупреждения потери (или замедления нарушения) функции печени у человека, инфицированного или не инфицированного HCV и имеющего риск нарушения функции печени, для улучшения функции печени у человека, инфицированного или не инфицированного HCV, нуждающегося в улучшении функции печени. Заболевание печени может представлять собой заболевание или нарушение, выбранное из группы, состоящей из неалкогольной жировой болезни печени (НЖАБП) и неалкогольного стеатогепатита; или из группы, состоящей из заболевания или нарушения, выбранного из группы, состоящей из цитомегаловирусной инфекции, шистосомоза и лептоспироза.
В некоторых воплощениях мишенью олигомера по изобретению является экспрессируемая в печени микроРНК, например, миР-122. Олигомеры, мишенью которых является миРНК-122, описаны в WO 2007/112754, WO 2007/112753, WO 2009/043353, и могут представлять собой миксмеры, такие как SPC3649, также известный под названием миравирсен (miravirsen, имеет последовательность 5'-CcAttGTcaCaCtCC-3' (SEQ ID NO 57), где заглавные буквы обозначают бета-D-окси LNA, строчные буквы обозначают ДНК, в которых все связи являются фосфоротиоатными, а цитозины LNA представляют собой 5-метилцитозин), или миниатюрные LNA, такие как описанные в WO 2009/043353 (например, 5'-АСАСТСС-3', 5'-САСАСТСС-3', 5''-ТСАСАСТСС-3', SEQ ID NOs 58, 59&33) где заглавные буквы обозначают LNA (возможно, бета-D_окси), в которых все связи являются фосфоротиоатными, а цитозины LNA могут представлять собой 5-метилцитозин). В некоторых воплощениях длина олигомеров, мишенью которых является миР-122, составляет 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18 нуклеотидов. В некоторых воплощениях последовательность олигомеров, мишенью которых является миР-122, полностью комплементарна миР-122 на всем протяжении олигомера и, предпочтительно, включает последовательность 5'-САСАСТСС-3'. Согласно базе данных miRBase, зрелая микроРНК-122 имеет последовательность 5' uggagugugacaaugguguuugu 3' (SEQ ID NO 34). В некоторых воплощениях олигомер, мишенью которого является микроРНК, например, миР-122, является комплементарным соответствующему сегменту микроРНК на всем протяжении олигомера и в некоторых воплощениях 3' нуклеозид олигомера комплементарен (т.е. спаривается) с первым, вторым, третьим или четвертым 5' нуклеотидом микроРНК, такой как миР-122, например, со вторым 5' нуклеотидом микроРНК, такой как миР-122.
В некоторых воплощениях мишенью олигомера по изобретению является экспрессируемая в печени микроРНК, например, миР-33 (миР-33a и/или миР-33b), что может использоваться в лечении метаболических заболеваний, таких как атеросклероз (см., например, WO 2010/120508). Олигомер, мишенью которого является миР-33a/b, может содержать последовательность нуклеотидов, выбранную из группы, состоящей из: 5'-TACAATGCA-3', 5'-ACAATGCAC-3', 5'-ACAATGCA-3' и 5'-CAATGCA-3' (SEQ ID Nos 35-38), конкретными примерами олигомеров, мишенью которых является миР-33a/b, могут быть 5'-TACAATGCA-3', 5'-ACAATGCA-3' и 5'-CAATGCA-3', где заглавные буквы обозначают (возможно, бета-D_окси) LNA, где все связи являются фосфоротиоатными, а цитозины LNA возможно представляют собой 5-метилцитозин. Согласно базе данных miRBase, зрелая микроРНК-33a имеет последовательность 5'-GUGCAUUGUAGUUGCAUUGCA-3' (SEQ ID NO 39), а миРНК-33b - 5' GUGCAUUGCUGUUGCAUUGC-3' (SEQ ID NO 40).
В некоторых воплощениях мишенью олигомера по изобретению является экспрессируемая в печени микроРНК, например, миР-21, что можно использовать в лечении таких заболеваний, как фиброз печени или гепатоцеллюлярная карцинома. Олигомеры, мишенью которых является миР-21, могут содержать последовательность нуклеотидов, выбранную из группы, состоящей из: 5'-TGATAAGCT-3', 5'-GATAAGCT-3', 5'-ATAAGCT-3' (SEQ ID Nos 41-43), конкретными примерами олигомеров, мишенью которых является миР-21 могут быть: 5'-TGATAAGCT-3', 5'-GATAAGCT-3', 5'-ATAAGCT-3' или 5' TcAGtCTGaTaAgCT 3' (SEQ ID NO 44) где заглавные буквы обозначают (возможно, бета-D_окси) LNA, строчные буквы обозначают ДНК, в которых все связи являются фосфоротиоатными, а цитозины LNA возможно представляют собой 5-метилцитозин. LNA-олигомер с фосфоротиоатными связями (например, бета-D-окси-LNA) с последовательностью 5-GATAAGCT-3' (LNA С представляет собой 5-метилцитозин) широко использовали для ингибирования миР-21 in vivo (SEQ ID NO 51). Согласно базе данных miRBase, зрелая микроРНК-21 имеет последовательность 5'-UAGCUUAUCAGACUGAUGUUGA-3' (SEQ ID NO 45).
В некоторых воплощениях мишенью олигомера по изобретению является экспрессируемая в печени микроРНК, например, миР-221, что можно использовать в лечении, например, гепатоцеллюлярной карциномы. Олигомер, мишенью которого является миР-221, может содержать последовательность нуклеиновых оснований, выбранную из группы, состоящей из: 5'-CAATGTAGC-3', 5'-AATGTAGC-3' и 5'-ATGTAGC-3' (SEQ ID NO 46-48) конкретные примеры олигомеров, мишенью которых является миР-221, включают 5'-CAATGTAGC-3', 5'-AATGTAGC-3' и 5'-ATGTAGC-3', где заглавные буквы обозначают (возможно, бета-D_окси) LNA, все связи являются фосфоротиоатными, а цитозины LNA возможно представляют собой 5-метилцитозин). Согласно базе данных miRBase, зрелая микроРНК-221 имеет последовательность 5' AGCUACAUUGUCUGCUGGGUUUC 3' (SEQ ID NO 49).
Другие микроРНК мишени и соединения, специфически взаимодействующие с ними, которые можно использовать в качестве олигонуклеотидов по изобретению или последовательности смежных нуклеотидов или их части, изложены в WO 2007/112754, например, представлены в Таблице 2 и Примере 29 из WO 2007/112754, содержание которого включено путем ссылки. Другие микроРНК мишени и соединения, специфически взаимодействующие с ними, которые можно использовать в качестве олигонуклеотидов по изобретению или последовательности смежных нуклеотидов или их части, изложены в WO 2009/043353, например, представлены в Таблице 1 из WO 2009/043353, содержание которого включено путем ссылки.
В некоторых воплощениях, олигомер по изобретению способен понижать (например, уменьшать или устранять) экспрессию мишени (например, нуклеиновой кислоты-мишени). В этой связи олигомер по изобретению может влиять на ингибирование мишени. В некоторых воплощениях олигомеры по изобретению связывают нуклеиновую кислоту-мишень и ингибируют экспрессию по меньшей мере на 10% или 20% по сравнению с нормальным уровнем экспрессии, более предпочтительно по меньшей мере на 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95% по сравнению с нормальным уровнем экспрессии (таким, как уровень экспрессии в отсутствие олигомера(ов) или конъюгата(ов)). В некоторых воплощениях такие изменения наблюдаются при применении соединения по изобретению в концентрации от 0,04 до 25 нМ, например, от 0,8 до 20 нМ. В том же или другом воплощении ингибирование экспрессии составляет менее 100%, например, менее 98% ингибирования, менее 95% ингибирования, менее 90% ингибирования, менее 80% ингибирования, менее 70% ингибирования. Изменение уровня экспрессии можно оценивать по уровню белка, например, с помощью таких методов, как электрофорез в полиакриламидном геле с додецилсульфатом натрий (ДСН-ПААГ) с последующим вестрен-блоттингом с использованием подходящих антител, направленных против белка-мишени. В альтернативном случае, изменение уровня экспрессии оценивают по уровню мРНК, например, с использованием нозерн-блоттинга или количественной полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). В некоторых воплощениях при использовании соответствующей концентрации, например, от 0,04 до 25 нМ, например, от 0,8 до 20 нМ, происходит снижение экспрессии до 10%-20% от нормального уровня в отсутствие соединения, конъюгата или композиции по изобретению, при оценке по уровню мРНК.
Таким образом, в изобретении предложен способ подавления или ингибирования экспрессии мишени в клетке, экспрессирующей мишень, указанный способ включает введение олигомера или конъюгата по изобретению в указанную клетку с целью подавления или ингибирования экспрессии мишени в указанной клетке. Соответствующая клетка представляет собой клетку млекопитающих, например, клетку человека. В некоторых воплощениях введение осуществляют in vitro. В некоторых воплощениях введение осуществляют in vivo.
Соединения по изобретению, такие как олигомеры и их конъюгаты, могут специфически взаимодействовать с различными мишенями, такими как мРНК или микроРНК или другими нуклеиновыми кислотами-мишенями, экспрессируемыми в печени (ссылки на гены в базе данных NCBI Genbank приведены в качестве примеров последовательностей, которые могут служить мишенями для соединений по изобретению, последовательности Genbank/NCBI включены путем ссылки).
АроВ
В некоторых воплощениях первый сегмент (или первый и второй сегмент) образуют единую последовательность смежных нуклеотидов, которая комплементарна соответствующей области целевой мРНК АроВ (т.е. специфически взаимодействует с ней), например, АроВ-100 (NCBI Genbank ID NM_000384.2 GI: 105990531, включен путем ссылки). Соединения по изобретению, мишенями которых является АроВ, могут найти применение в лечении острого коронарного синдрома (см. WO 20100076248). Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является АроВ, для применения в лечении острого коронарного синдрома. В изобретении также предложен способ лечения острого коронарного синдрома, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
Соединения по изобретению, мишенями которых является АроВ, могут найти применение в лечении атеросклероза. Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является АроВ100, для применения в лечении атеросклероза. В изобретении также предложен способ лечения атеросклероза, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
Соединения по изобретению, мишенями которых является АроВ, могут найти применение в лечении гиперхолестеринемии или гиперлипидемии. Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является АроВ100, для применения в лечении гиперхолестеринемии или гиперлипидемии. В изобретении также предложен способ лечения гиперхолестеринемии или гиперлипидемии, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
В изобретении предложен способ in vivo или in vitro ингибирования АроВ в клетке, экспрессирующей АроВ, указанный способ включает введение олигомера или конъюгата или фармацевтической композиции по изобретению в указанную клетку для ингибирования АроВ в указанной клетке.
Примеры LNA-олигомеров, которые могут применяться в качестве первого сегмента олигомеров/конъюгатов по изобретению, включают, например, описанные в WO 2007/031081, WO 2008/113830, WO 2007131238 и WO 2010142805, содержание которых включено путем ссылки. Конкретные предпочтительные соединения включают следующие:
5'-GsmCsaststsgsgstsastsTsmCsA-3' (SEQ ID NO 12)
5'-GsTstsgsascsascstsgsTsmC-3' (SEQ ID NO 50)
Где заглавные буквы обозначают звенья бета-D-окси LNA (нуклеозиды), строчные буквы обозначают звенья ДНК, подстрочный индекс s обозначает фосфоротиоатную связь, а надстрочный индекс m перед заглавной С означает, что все цитозины LNA представляют собой 5-метилцитозин. Соединения по изобретению, мишенью которых является АроВ, могут быть конъюгированы с конъюгатом, обеспечивающим адресную доставку олигомера в печень, описанным в данном документе, например, конъюгатом углевода или липофильным конъюгатом, таким как конъюгат GalNac или конъюгат стерина (например, холестерина или токоферола). Конъюгат может быть присоединен, например, к 5' концу или 3' концу олигомерного соединения (в некоторых воплощениях, через сегмент В). Другие олигомеры, мишенью которых является АроВ, изложены в WO 03/011887, WO 04/044181, WO 2006/020676, WO 2007/131238, WO 2007/031081 и WO 2010142805.
PCSK9
В некоторых воплощениях первый сегмент (или первый и второй сегменты) образуют единую последовательность смежных нуклеиновых оснований, комплементарную соответствующей области мишени мРНК PCSK9 (т.е. специфически взаимодействующую с ней), например, мРНК PCSK9 человека: NCBI Genbank ID NM_174936.3 GI:299523249, которая включена путем ссылки.
В изобретении предложен олигомер по изобретению, мишенью которого является PCSK9, для применения в качестве лекарственного средства, например, средства для лечения гиперхолестеринемии или родственного ей нарушения, такого как нарушение, выбранное из группы, состоящей из атеросклероза, гиперлипидемии, гиперхолестеринемии, семейной гиперхолестеринемии, например, мутации PCSK9 с приобретением функции, нарушения соотношения ЛПВП и ЛПНП, дислипидемии, например, семейной гиперлипидемии (семейной комбинированной гиперхолестеринемии), приобретенной гиперлипидемии, резистентной к терапии статинами гиперхолестеринемии, атеросклеротической болезни сердца и ишемической болезни сердца (ИБС).
В изобретении предложено применение олигомера по изобретению, мишенью которого является PCSK9, для изготовления лекарственного средства для лечения гиперхолестеринемии или родственного ей нарушения, такого как нарушение, выбранное из группы, состоящей из атеросклероза, гиперлипидемии, гиперхолестеринемии, семейной гиперхолестеринемии, например, мутации PCSK9 с приобретением функции, нарушения соотношения ЛПВП и ЛПНП, дислипидемии, например, семейной гиперлипидемии (семейной комбинированной гиперхолестеринемии), приобретенной гиперлипидемии, резистентной к терапии статинами гиперхолестеринемии, атеросклеротической болезни сердца и ишемической болезни сердца (ИБС).
В изобретении предложен способ лечения гиперхолестеринемии или родственного ей нарушения, такого как нарушение, выбранное из группы, состоящей из атеросклероза, гиперлипидемии, гиперхолестеринемии, семейной гиперхолестеринемии, например, мутации PCSK9 с приобретением функции, нарушения соотношения ЛПВП и ЛПНП, дислипидемии, например, семейной гиперлипидемии (семейной комбинированной гиперхолестеринемии), приобретенной гиперлипидемии, резистентной к терапии статинами гиперхолестеринемии, атеросклеротической болезни сердца и ишемической болезни сердца (ИБС), указанный способ включает введение эффективного количества олигомера по изобретению, мишенью которого является PCSK9, пациенту, страдающему или предположительно страдающему гиперхолестеринемией или родственным ей нарушением.
В изобретении предложен способ ингибирования in vivo или in vitro PCSK9 в клетке, экспрессирующей PCSK9, указанный способ включает введение олигомера по изобретению, мишенью которого является PCSK9, в указанную клетку для ингибирования PCSK9 в указанной клетке.
Ниже представлен олигомер, мишенью которого является мРНК PCSK9 человека, который может применяться в соединениях по изобретению в качестве сегмента А.
5'-TsGsmCstsascsasasasascsmCsmCsA-3' (SEQ ID NO 22)
Где заглавные буквы обозначают звенья бета-D-окси LNA (нуклеозиды), строчные буквы обозначают звенья ДНК, подстрочный индекс s обозначает фосфоротиоатную связь, а надстрочный индекс m перед заглавной С означает, что все цитозины LNA представляют собой 5-метилцитозин. Соединения по изобретению, мишенью которых является PCSK9, могут быть конъюгированы с конъюгатом, обеспечивающим адресную доставку олигомера в печень, описанным в данном документе, например, конъюгатом углевода или липофильным конъюгатом, таким как конъюгат GalNac или конъюгат стерина (например, холестерина или токоферола). Конъюгат может быть присоединен, например, к 5' концу или 3' концу олигомерного соединения (в некоторых воплощениях, через сегмент В).
Другие олигомеры, мишенью которых является PCSK9, приведены в Примерах, а также описаны в WO 2008/043753, WO 2011/009697, WO 08/066776, WO 07/090071, WO 07/146511, WO 07/143315, WO 09/148605, WO 11/123621 и WO 11133871, содержание которых включено путем ссылки. Другие соединения, мишенями которых является PCSK9, которые можно использовать в соединениях по изобретению, приведены в Примерах.
миР-122
В некоторых воплощениях первый сегмент (или первый и второй сегменты) образуют единую последовательность смежных нуклеиновых оснований, комплементарную соответствующей области микроРНК-122, такой как миР-122а (т.е. мишени), например, последовательности hsa-miR-122: (20 версия miRBase: MI0000442), такой как:

миР-122 играет роль при инфицировании HCV, это существенный фактор организма-хозяина, необходимый для поддержания инфекции. Следовательно, ингибиторы миРНК-122 могут найти применение в лечении гепатита С.
Соединения по изобретению, мишенями которых является миР-122, могут найти применение в лечении гепатита С. Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является миРНК-122, для применения в лечении инфекции, вызванной HCV. В изобретении также предложен способ лечения инфекции, вызванной HCV, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
Таким образом, в изобретении предложено применение олигомера по изобретению, мишенью которого является миР-122, для изготовления лекарственного средства для лечения инфекции, вызванной HCV.
В изобретении предложен способ лечения инфекции, вызванной HCV, указанный способ включает введение эффективного количества олигомера по изобретению, мишенью которого является миР-122, пациенту, инфицированному HCV.
В изобретении предложен способ ингибирования in vivo или in vitro миРНК-122 в клетке, экспрессирующей миРНК-122, например, в клетке, инфицированной HCV, или клетке, экспрессирующей репликон HCV, указанный способ включает введение олигомера или конъюгата или фармацевтической композиции по изобретению в указанную клетку для ингибирования миР-122 в указанной клетке.
миР-122 также задействована в метаболизме холестерина, предполагают, что ингибирование миР-122 может найти применение в терапии с целью снижения уровня холестерина в плазме (Esau, Cell Metab. 2006 Feb; 3(2):87-98).
Следовательно, ингибиторы миР-122 могут найти применение в терапии для снижения уровня холестерина в плазме или в терапии метаболических нарушений, сопровождающихся повышением уровня холестерина (ассоциированных нарушений), показания к применению выбирают из группы, состоящей из стеатоза печени, атеросклероза, гиперлипидемии, гиперхолестеринемии, семейной гиперхолестеринемии, дислипидемий, атеросклеротической болезни сердца и ишемической болезни сердца (ИБС).
Соединения по изобретению, мишенями которых является миР-122, могут найти применение в лечении повышенного уровня холестерина или ассоциированных нарушений. Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является миР-122, для применения в лечении повышенного уровня холестерина или ассоциированных нарушений. В изобретении также предложен способ лечения повышенного уровня холестерина или ассоциированных нарушений, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
В изобретении предложено применение олигомера по изобретению, мишенью которого является миР-122, для изготовления лекарственного средства для лечения повышенного уровня холестерина или ассоциированных нарушений.
В изобретении предложен способ лечения повышенного уровня холестерина или ассоциированных нарушений, указанный способ включает введение эффективного количества олигомера по изобретению, мишенью которого является миР-122, пациенту, страдающему указанным нарушением.
В изобретении предложен способ ингибирования in vivo или in vitro миР-122 в клетке, экспрессирующей миР-122, например, в клетке, инфицированной HCV, или клетке, экспрессирующей репликон HCV, указанный способ включает введение олигомера или конъюгата или фармацевтической композиции по изобретению в указанную клетку для ингибирования миР-122 в указанной клетке.
Олигомеры, мишенью которых является миР-122, описаны в WO 2007/112754, WO 2007/112753, и могут представлять собой миксмеры, такие как SPC3649, также известный под названием миравирсен (miravirsen, см. ниже), или миниатюрные LNA, такие как описанные в WO 2009/043353, WO 2009/043353 (например, 5'-АСАСТСС-3', 5'-САСАСТСС-3', 5'-ТСАСАСТСС-3', (SEQ ID NOs 58, 64&33) где заглавные буквы обозначают бета-D-окси LNA, где все связи являются фосфоротиоатными, а цитозины LNA представляют собой 5-метилцитозин). В некоторых воплощениях длина олигомеров, мишенью которых является миР-122, составляете, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18 (или 19, 20, 21, 22 или 23) нуклеотидов. В некоторых воплощениях последовательность олигомеров, мишенью которых является миР-122, полностью комплементарна миР-122 на всем протяжении олигомера и, предпочтительно, включает последовательность 5'-САСАСТСС-3'. В некоторых воплощениях олигомер, мишенью которого является микроРНК, например, миР-122, является комплементарным соответствующему сегменту микроРНК на всем протяжении олигомера и в некоторых воплощениях 3' нуклеозид олигомера комплементарен (т.е. спаривается) с первым, вторым, третьим или четвертым 5' нуклеотидом микроРНК, такой как миР-122, например, со вторым 5' нуклеотидом микроРНК, такой как миР-122.
Ниже представлен олигомер, мишенью которого является hsa-miR-122 (миР-122 человека), который может применяться в качестве сегмента А в соединениях по изобретению.
Миравирсен: 5'-mCscsAststsGsTscsasmCsasmCstsmCsmC-3' (SEQ ID NO 57)
Другие соединения, мишенью которых является миР-122, которые могут применяться в контексте данного изобретения (сегмент А), описаны в WO 2007/027894, WO 2007/027775.
MtGPAT: (база данных NCBI ген ID 57678 - хромосома: 10; NC_000010.10(113907971..113975153, комплемент). Митохондриальная глицерол-3-фосфат ацилтрансфераза (ЕС 2.3.1.15, также обозначаемая GPAT1, mtGPATI, GPAM, mtGPAM, от англ. Mitochondrial glycerol-3-phosphate acyltransferase 1) играет главную роль в биосинтезе триглицеридов в печени, при этом высокий уровень активности mtGPATI вызывает накопление жира в печени (гепатостеатоз), тогда как следствием отсутствия mtGPATI является низкий уровень триглицеридов печени и интенсивное окисление жирных кислот (см. WO 2010/000656, описывающий олигомеры, мишенями которых является mtGPAT). Соединения по изобретению, мишенями которых является MtGPAT, могут найти применение в лечении таких состояний, как избыточный вес, ожирение, жировая инфильтрация печени, гепатостеатоз, неалкогольная жировая болезнь печени (НАЖБП), неалкогольный стеатогепатит (НАСГ), инсулинорезистентность, диабет, такой как инсулин-независимый сахарный диабет (ИНСД).
Данный олигомер (SEQ ID NO 60), мишенью которого является mTGPAt, можно применять в качестве олигомерного сегмента (первого сегмента) в составе соединений по изобретению, заглавные буквы обозначают LNA, например, бета-D-окси-LNA, прописные буквы обозначают ДНК, нижний индекс s означает фосфоротиоатную связь. Цитозины LNA могут представлять собой 5-метилцитозин.
AsTsTscscscstsgscscstsGsTsG-3'
Фактор VII (база данных NCBI ген ID 2155, NCBI J02933.1 GI:180333, или EU557239.1 GI:182257998). Мишенью олигомера или конъюгата по изобретению может быть фактор VII, таким образом, возможно ингибировать образование фактора VII, ключевого компонента внешнего пути свертывания крови. Соединения по изобретению, мишенью которых является фактор VII, могут найти применение в лечении или профилактике тромботических заболеваний (как правило, не вызывая кровоточивости), таких как инфаркт миокарда, инсульт, тромбозы, или воспалительных заболеваний. WO 2013/119979 и WO 2012/174154, содержание которых включено путем ссылки, описывают соединения олигонуклеотидов, мишенью которых является FVII, которые могут входить в состав конъюгатов по данному изобретению.
Фактор XI (база данных NCBI ген ВС122863.1 GI:114108211) - фактор XI, коагуляционный фактор, синтезируемый в печени. Высокий уровень фактора XI связывают с инфарктом миокарда, инсультом и тромбообразованием. WO 2013/070771, содержание которого включено путем ссылки, описывает соединения олигонуклеотидов, мишенью которых является FXI, которые могут входить в состав конъюгатов по данному изобретению. Соединения по изобретению, мишенью которых является фактор XI, могут найти применение в лечении или профилактике тромботических заболеваний, таких как инфаркт миокарда, инсульт, тромбозы, или воспалительных заболеваний, таких как артрит и колит.
ApoCIII (база данных NCBI ген ВС027977.1 GI:20379764) белок, регулирующий метаболизм триглицеридов в крови. Высокий уровень ApoCIII связывают с воспалением, высоким уровнем триглицеридов, атеросклерозом и метаболическим синдромом. Соединения по изобретению, мишенью которых является ApoCIII, могут найти применение для снижения уровня триглицеридов сыворотки или в лечении, например, синдрома семейной хиломикронемии и повышенного уровня триглицеридов, как в виде монотерапии, так и в комбинации с другими агентами, снижающими уровень триглицеридов. WO 11085271, содержание которого включено путем ссылки, описывает соединения олигонуклеотидов, мишенью которых является ApoCIII, которые могут входить в состав конъюгатов по данному изобретению.
Аро(а) (база данных NCBI ген NM_005577.2 GI:116292749) ингибирует биосинтез аро(а) в печени и обеспечивает возможность непосредственного снижения Lp(a), независимого фактора риска сердечно-сосудистых заболеваний. Высокий уровень Lp(a) связывают с повышенным риском атеросклероза, ишемической болезни сердца, инфаркта миокарда и инсульта. Lp(a) способствует раннему формированию бляшек, или атеросклеротическому повреждению артерий. Соединения по изобретению, мишенями которых является Аро(а), могут найти применение в лечении, например, атеросклероза и ишемической болезни сердца. WO 05000201 и WO 03014307, содержание которых включено путем ссылки, описывают соединения олигонуклеотидов, мишенью которых является аполипопротеин (а), которые могут входить в состав конъюгатов по данному изобретению.
Вирус гепатита В (HBV, от англ. Hepatitis В virus) (см., например, NCBI D23684.1 GI: 560092; D23683.1 GI: 560087; D23682.1 GI: 560082; D23681.1 GI: 560077; D23680.1 GI: 560072; D23679.1 GI: 560067; D23678.1 GI: 560062; D23677.1 GI: 560057; содержание которых включено путем ссылки).
Олигомеры, мишенью которых является HBV, хорошо известны в области техники, см., например, WO 96/03152, WO 97/03211, WO 2011/052911, WO 2012/145674, WO 2012/145697, WO 2013/003520 и WO 2013/159109.
Соединения по изобретению, мишенями которых является HBV, могут найти применение в лечении инфекции, вызванной HBV. Таким образом, в изобретении предложен олигомер по изобретению, мишенью которого является HBV, для применения в лечении HBV. В изобретении также предложен способ лечения инфекции, вызванной HBV, указанный способ включает введение олигомера по изобретению субъекту, нуждающемуся в указанном лечении.
В изобретении предложен олигомер или конъюгат по изобретению, мишенью которого является вирус гепатита В (HBV) для применения в качестве лекарственного средства, например, для лечения инфекции, вызванной вирусом гепатита В или ассоциированного заболевания.
В изобретении предложен олигомер или конъюгат или фармацевтическая композиция по изобретению, мишенью которых является вирус гепатита В (HBV) для изготовления лекарственного средства для лечения инфекции, вызванной вирусом гепатита В или родственного заболевания. В изобретении предложен способ лечения инфекции, вызванной вирусом гепатита В, или родственного заболевания, указанный способ включает введение эффективного количества олигомера или конъюгата по изобретению, мишенью которого является HBV, пациенту, инфицированному вирусом гепатита В.
В изобретении предложен способ ингибирования in vivo или in vitro репликации HBV в клетке, инфицированной HBV, указанный способ включает введение олигомера или конъюгата по изобретению, мишенью которого является HBV, в указанную клетку для ингибирования репликации HBV. Ниже приведен пример LNA-олигомера, мишенью которого является HBV (согласно WO 2011/47312), который можно использовать в качестве олигомера (участка А) по изобретению 5'-GsAsGsGscsastsasgscsasgsmCsAsGsG-3'. Другие соединения приведены в Таблице 1 документа WO 2011/47312, а также в WO 2011/052911, WO 2012/145674, WO 2012/145697, WO 2013/003520 и WO 2013/159109, содержание которых включено путем ссылки.
RG-101 представляет собой соединение, мишенью которого является миР-122, содержащее конъюгат Galnac, разработанное для лечения HCV компанией Regulus Therapeutics.
ANGPTL3 (например, NCBI ВС007059.1 GI: 14712025 или ВС058287.1 GI: 34849466) Ангиопоэтин-подобный 3 белок регулирует обмен липидов, глюкозы и энергетический обмен. У людей с повышенным уровнем ANGPTL3 отмечается гиперлипидемия, ассоциированная с повышенным риском развития инфаркта миокарда в молодом возрасте, утолщения стенки артерий и множественных метаболических нарушений, таких как инсулинорезистентность. Напротив, у людей с низким уровнем ANGPTL3 наблюдается низкий уровень холестерина ЛПНП и триглицеридов и сниженный риск сердечно-сосудистых заболеваний. Соединения по изобретению, мишенями которых является ANGPTL3, могут найти применение в лечении, например, гиперлипидемии и связанных с ней заболеваний, метаболических нарушений, атеросклероза, ишемической болезни сердца или инсулинорезистентности. WO 11085271, включенный путем ссылки, описывает соединения олигонуклеотидов, мишенью которых является ANGPTL3, которые могут входить в состав конъюгатов по данному изобретению.
Глюкагоновый рецептор, или GCGR (от англ. Glucagon receptor) (ВС112041.1 GI: 85567507; L20316.1 GI: 405189): Глюкагон представляет собой гормон, являющийся антагонистом инсулина и стимулирующий образование глюкозы в печени, в частности, при диабете 2 типа. У пациентов с выраженным диабетом неконтролируемое действие глюкагона вызывает значительное повышение уровня глюкозы в крови. Таким образом, подавление глюкагона может приводить к существенному понижению глюкозы у пациентов, страдающих тяжелым диабетом. Кроме того, снижение GCGR приводит к образованию более активного глюкагон-подобного пептида, или GLP-1, гормона, стимулирующего функцию поджелудочной железы и усиливающего секрецию инсулина. Соединения по изобретению, мишенями которых является GCGR, могут найти применение в лечении, например, инсулинорезистентности, гипергликемии, диабета, например, диабета 1 или 2 типа, для сохранения функции поджелудочной железы и контролирования уровня глюкозы в крови. WO 2007/134014 описывает соединения олигонуклеотидов, мишенью которых является GCGR, которые могут входить в состав конъюгатов по данному изобретению.
Рецептор фактора роста фибробластов 4, или FGFR4 (от англ. Fibroblast growth factor receptor 4) (база данных NCBI ген 2264 - NC_000005.9 (176513906..176525143) FGFR4 экспрессируется в печени и жировой ткани, понижает способность организма накапливать жир, одновременно усиливая сжигание жира и энергетические затраты. Многие лекарственные препараты для борьбы с ожирением действуют на головной мозг, подавляя аппетит, и часто вызывают побочные эффекты со стороны ЦНС. Соединения по изобретению, мишенями которых является FGFR4, могут найти применение, например, в терапии инсулинорезистентности, гипергликемии, диабета, например, диабета 1 или 2 типа, для предупреждения ожирения (например, при использовании в комбинации с препаратом, подавляющим аппетит), снижения веса тела и улучшения чувствительности к инсулину, облегчения симптомов диабета, например, диабета 1 или 2 типа, и контролирования уровня глюкозы крови. WO 09046141 и WO 12174476 содержание которых включено путем ссылки, описывают соединения олигонуклеотидов, мишенью которых является FGFR4, которые могут входить в состав конъюгатов по данному изобретению.
Диацилглицерин ацилтрансфераза-2, или DGAT-2 (от англ. Diacylglycerol acyltransferase-2) (база данных NCBI ген ID 84649): ключевой компонент в синтезе триглицеридов. Ингибирование DGAT может уменьшить аккумулирование жира в печени пациентов, страдающих неалкогольным стеатогепатитом (NASH), а также использоваться в лечении диабета 2 типа и инсулинорезистентности. Соединения по изобретению, мишенью которых является DGAT-2, могут применяться для лечения NASH, уменьшения накопления жира в печени, лечения диабета, например, диабета 2 типа и лечения инсулинорезистентности. WO 05019418 и WO 2007136989, содержание которых включено путем ссылки, описывают соединения олигонуклеотидов, мишенью которых является DGAT-2, которые могут входить в состав конъюгатов по данному изобретению.
Рецептор глюкокортикоидов, или GCCR (от англ. Glucocorticoid receptor) (ВС150257.1 GI: 152013043): Глюкокортикоидные гормоны влияют на различные процессы в организме, а избыточная концентрация глюкокортикоидных гормонов может оказывать негативное влияние на многие ткани и органы. Синдром Кушинга представляет собой редкое заболевание, которое развивается, когда организм в течение длительного времени подвергается воздействию высоких уровней глюкокортикоидов. В отсутствие лечения у пациентов с синдромом Кушинга может развиваться гипертензия, диабет, нарушение функций иммунной системы и повышаться риск ранней смерти. Несмотря на успехи в лечении синдрома Кушинга, существующие препараты обладают выраженным побочным действием, в частности, приводят к развитию гипертензии и диабета, поэтому существует необходимость в разработке новых терапевтических средств для таких пациентов. Соединения по изобретению, мишенью которых является GCCR-2, могут применяться в лечении синдрома Кушинга и связанных с ним состояний (таких, которые перечислены выше). WO 07035759 и WO 2007136988, содержание которых включено путем ссылки, описывают соединения олигонуклеотидов, мишенью которых является GCCR, которые могут входить в состав конъюгатов по данному изобретению.
С5 компонент комплемента (М57729.1 GI: 179982): Система комплемента играет центральную роль в поддержании иммунитета, являясь защитным механизмом организма, и нарушение ее регуляции приводит к серьезным осложнениям различных заболеваний, которые могут представлять угрозу жизни, среди них можно упомянуть пароксизмальную ночную гемоглобинурию, атипический гемолитико-уремический синдром, миастению гравис, нейромиелит зрительного нерва. Соединения по изобретению, мишенью которых является С5 компонент комплемента, могут применяться в лечении одного или нескольких перечисленных нарушений. С5 представляет собой мишень, значимость которой подтверждена генетически и клинически; мутации с потерей функции у человека связаны с нарушением иммунной защиты против некоторых инфекций; при ряде заболеваний с вовлечением комплемента показана клиническая эффективность и переносимость внутривенного введения моноклонального антитела, направленного против С5. Трансмембранная протеаза, серии 6 (Tmprss6) для лечения бета-талассемии и нарушений с перенасыщением железом.
Альфа-1 антитрипсин (ААТ): (М11465.1 GI: 177826) ассоциирован с заболеваниями печени. WO 13142514 содержание которого включено путем ссылки, описывает соединения олигонуклеотидов, мишенью которых является ААТ, которые могут входить в состав конъюгатов по данному изобретению. Соединения по изобретению, мишенью которых является ААТ, могут найти применение в способах снижения экспрессии мРНК и белка ААТ у нуждающегося в этом индивида для лечения, улучшения, профилактики, замедления прогрессирования или остановки прогрессирования фиброза, например, заболеваний печени с вовлечением альфа-1 антитрипсина и заболеваний легких, например, заболеваний легких с вовлечением альфа-1 антитрипсина.
Транстиретин - TTR (от англ. Transthyretin) (ВС005310.1 GI: 13529049): Олигомеры по изобретению, мишенью которых является TTR, могут найти применение в лечении транстиретинового амилоидоза, или TTR амилоидоза, редко встречающегося тяжелого генетического заболевания, при котором пациент наследует мутантный ген, продуцирующий неправильно свернутую форму TTR, которая постепенно накапливается в тканях. У пациентов, страдающих TTR амилоидозом, как нормальная, так и мутантная формы TTR могут образовывать фибриллы в тканях, в том числе в сердце, периферических нервах и желудочно-кишечном тракте. Наличие фибрилл TTR мешает нормальному функционированию этих тканей, увеличение фибрилл, образованных белком TTR, усиливает повреждение тканей и усугубляет течение заболевания. TTR является транспортным белком, переносящим тиреоидный гормон и ретинол в крови. У пациентов, страдающих TTR амилоидозом, как нормальная, так и мутантная формы TTR могут образовывать фибриллы в тканях. Соединения по изобретению, мишенью которых является TTR, могут применяться в лечении амилоидоза. См. Benson et al., Amyloid. 2010 Jun; 17(2):43-9, and Ackermann et al., Amyloid. 2012 Jun; 19 Suppl 1:43-4.). Антисмысловые соединения, мишенью которых является TTR, которые могут применяться в составе олигомеров или конъюгатов по изобретению, описаны в WO 2007/031081, WO 2008/113830, WO 11139917 и WO 10017509, содержание которых включено путем ссылки.
Аминолевулинат синтаза-1 (от англ. Aminolevulinate synthase-1, ALAS-1) (ВС011798.2 GI: 33877783; AK312566.1 GI: 164690365; NM_199166.2 GI: 362999012; NM_000688.5 GI: 362999011). ALAS1 является важной мишенью при лечении порфирии, например, лечении печеночной порфирии, включающей острую интермиттирующую (перемежающуюся) порфирию (ОПП). Соединения по изобретению, мишенью которых является ALAS-1, могут найти применение в лечении указанных нарушений.
Фактор роста сосудистого эндотелия, или VEGF (от англ. Vascular endothelial growth factor) (ген ID 7422, у человека находится на хромосоме: 6; NC_000006.11 (43737946..43754224)). VEGF является мишенью при злокачественных новообразованиях. Соединения по изобретению, мишенью которых является VEGF, могут найти применение в лечении нарушений, характеризующихся гиперпролиферацией, таких как злокачественные новообразования, например, злокачественные новообразования печени.
В Таблице 3 приведена группа присутствующих в печени мишеней, с которыми могут специфически взаимодействовать соединения по изобретению, а также медицинские показания к применению/нарушения, для лечения которых могут применяться указанные соединения (например, у лиц, имеющих ассоциированное заболевание) (см. Sehgal et al., Liver as a target for oligonucleotide therapeutics, J. of Hepatology 2013, в печати).


Последовательности
В некоторых воплощениях олигомер или его первый сегмент содержит последовательность смежных нуклеотидов, которая соответствует обратному комплементу нуклеотидной последовательности, присутствующей в составе нуклеиновой кислоты-мишени (т.е. последовательности, являющейся мишенью олигомера). В Таблице 3 приведена группа мРНК и миРНК, которые служат мишенями в доклинических и клинических исследованиях с применением олигонуклеотидных соединений по соответствующим показаниям, и следовательно, являются подходящими мишенями для соединений по данному изобретению.
В некоторых воплощениях мишень выбрана из группы, состоящей из: миРНК-122, АроВ-100, ApoCIII, PCSK9, CRP, KSP, VEGF, PLK1, миРНК-34, FGFR4, фактора IXa, фактора XI, TTR, GCCR, PTP-1В, GCGR, ААТ, ALDH2, компонентов пути НАМР, миРНК-33, Аро(а), миР-7, миР-378, миР-21, Myc, миР-122, таких сегментов генома HCV, как HCV 5'UTR или HCV NS5B РНК или NS3 РНК, TMPRSS6, антитромбина III, ApoCIII, ANGPLT3, МТР, DGAT2, ALAS1, антитромбина III, сывороточного амилоида А и фактора VII.
В некоторых воплощениях последовательность смежных нуклеотидов, гибридизуемая с последовательностью мишени, содержит не более одного некомплементарного основания. При этом, сегмент В может быть некомплементарным и, не обязательно учитывается при определении степени комплементарности.
При определении степени «комплементарности» между олигомером по изобретению (или его сегментами) и целевым сегментом нуклеиновой кислоты, описанными в данном документе, степень «комплементарности» (а также «гомологии» или «идентичности») выражают как процент идентичности (или процент гомологии) между последовательностью олигомера (или его сегмента) и последовательностью целевого сегмента (или обратного комплемента целевого сегмента), с которым достигается наилучшее выравнивание. Процент вычисляют, путем подсчета количества выровненных оснований, идентичных между двумя последовательностями, деления общего количества смежных мономеров в составе олигомера и умножения на 100. При выполнении данного сравнения предпочтительно заменять пробелом (разрывом, гэпом) сами несовпадения, а не области, в которых число мономеров внутри гэпа различалось бы между олигомером по изобретению и целевым сегментом.
В данном документе термины «гомологичный» и «гомология» используются взаимозаменяемо с терминами «идентичный» и «идентичность».
Термины «соответствующий» и «соответствует» относятся к сравнению нуклеотидной последовательности олигомера (т.е. последовательности оснований, или нуклеиновых оснований) или последовательности смежных нуклеотидов (первого сегмента) с эквивалентной последовательностью смежных нуклеотидов последовательности, выбранной из i) части последовательности обратного комплемента нуклеиновой кислоты-мишени. Аналоги нуклеотидов сравнивают непосредственно с их эквивалентами или соответствующими нуклеотидами. Первая последовательность, соответствующая другой последовательности из категории i) или и) обычно идентична указанной последовательности на всем протяжении первой последовательности (например, последовательности смежных нуклеотидов) или, как описано в данном документе, в некоторых воплощениях может быть по меньшей мере на 80% гомологична соответствующей последовательности, например, гомологична по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, например, гомологична на 100% (идентична).
Термины «соответствующий нуклеотидный аналог» и «соответствующий нуклеотид» указывают, что нуклеотид в нуклеотидном аналоге и нуклеотид естественного происхождения идентичны. Например, если в составе нуклеотида 2-дезоксирибоза связана с аденином, то «соответствующий аналог нуклеотида» (в отличие от 2-дезоксирибозы) содержит пентозу, связанную с аденином.
Термины "обратный комплемент", "обратно комплементарный" и "обратная комплементарность" в данном документе используют взаимозаменяемо с терминами «комплемент», «комплементарный» и «комплементарность».
Таким образом, последовательность смежных нуклеиновых оснований олигомера может быть комплементарна мишени, например, такой, которая указана в данном документе.
Нуклеозиды и аналоги нуклеозидов
Термин «нуклеотид» в данном документе обозначает гликозид, содержащий углеводный компонент (или его аналог), азотистое основание и ковалентную связь (связывающую группу), например, фосфатную или фосфоротиоатную межнуклеотидную связь, и охватывает как нуклеотиды естественного происхождения, такие как ДНК-нуклеотиды или РНК-нуклеотиды, или нуклеотиды искусственного происхождения, содержащие модифицированный углеводный компонент или модифицированное основание, которые в данном документе обозначают «аналогами нуклеотидов». В данном документе одиночный нуклеотид (звено) может также обозначаться мономером или звеном нуклеиновой кислоты.
В контексте данного изобретения термины нуклеозид и нуклеотид обозначают как нуклеотиды/нуклеозиды естественного происхождения, например, ДНК- или РНК-нуклеотиды/нуклеозиды, так и аналоги нуклеотидов/нуклеозидов.
В биохимии термин «нуклеозид» обычно обозначает гликозид, содержащий углеводный компонент и азотистое основание, и, таким образом, может использоваться для обозначения нуклеотидных звеньев в составе олигомера, ковалентно связанных межнуклеозидными связями. В биотехнологии термин «нуклеотид» обычно обозначает мономер или звено нуклеиновой кислоты, и применительно к олигонуклеотиду может обозначать его остов - «нуклеотидную последовательность», как правило, при упоминании последовательности нуклеиновых оснований подразумевают наличие углеводного скелета и межнуклеозидных связей. Аналогично, в отношении олигонуклеотидов, у которых модифицирована одна или несколько межнуклеозидных связей, термин «нуклеотид» может обозначать «нуклеозид», например, термин «нуклеотид» может использоваться даже для указания наличия или природы связей между нуклеозидами.
Для специалиста в области техники очевидно, что 5' концевой нуклеотид в составе олигонуклеотида не содержит 5' межнуклеотидной связи, хотя при этом может содержать или не содержать 5' концевую группу. Нуклеотиды искусственного происхождения включают нуклеотиды, имеющие модифицированный углеводный компонент, такие как бициклические нуклеотиды или 2' модифицированные нуклеотиды, например, 2' замещенные нуклеотиды.
«Аналоги нуклеотидов» представляют собой варианты нуклеотидов естественного происхождения, например, ДНК- или РНК-нуклеотидов, имеющие модификации углеводного компонента и/или азотистого основания. Аналоги могут быть «молчащими», или «эквивалентами» нуклеотидов естественного происхождения, т.е. не оказывать функционального влияния на ингибирование экспрессии гена-мишени олигонуклеотида. Тем не менее, такие «эквивалентные» аналоги, могут оказаться полезными, например, если их легче или дешевле получать, или если они более стабильны в условиях хранения или производства, или если они имеют таг или метку. Однако предпочтительны аналоги, которые оказывают функциональное влияние на ингибирование экспрессии гена-мишени олигонуклеотида; например, повышают аффинность при связывании с мишенью и/или повышают устойчивость к внутриклеточным нуклеазам и/или облегчают транспорт внутрь клетки. Конкретные примеры аналогов нуклеозидов описаны, например, в публикации Freier & Altmann; Nucl. Acid Res., 1997, 25, 4429-4443 and Uhlmann; Curr. Opinion in Drug Development, 2000, 3(2), 293-213, и приведены на схеме 1:

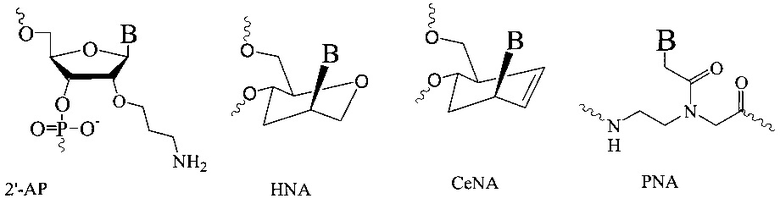
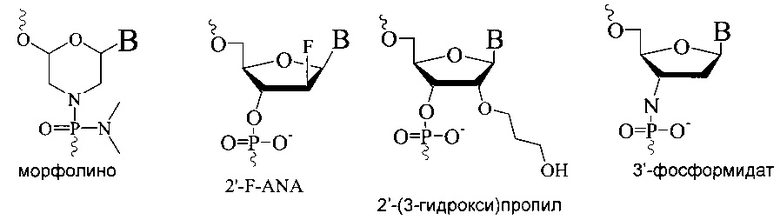
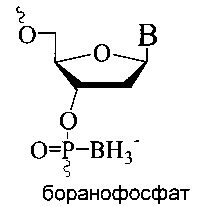
Схема 1
Таким образом, олигомер может содержать или состоять из простой последовательности нуклеотидов естественного происхождения предпочтительно 2'-дезоксинуклеотидов (обычно обозначаемых в данном документе «ДНК»), а также возможно, рибонуклеотидов (обычно обозначаемых в данном документе «РНК») или комбинации таких нуклеотидов естественного происхождения с одним или несколькими нуклеотидами искусственного происхождения, т.е. аналогами нуклеотидов. Такие аналоги нуклеотидов могут повышать аффинность олигомера к целевой последовательности.
Примеры подходящих и предпочтительных аналогов нуклеотидов приведены в WO 2007/031091 или в документах, на которые он ссылается. Другие аналоги нуклеотидов, которые могут применяться в составе олигомеров по изобретению, включают трициклические нуклеиновые кислоты, см., например, WO 2007/031081, WO 2008/113830, WO 2013154798 и WO 2013154798, содержание которых включено путем ссылки.
Олигомерные соединения, такие как антисмысловые олигонуклеотиды, например, упомянутые в данном документе соединения, имеющие в своем составе сегмент А, а в некоторых воплощениях, сегмент В, могут содержать один или несколько нуклеозидов, у которых модифицирована углеводная группа. Такие нуклеозиды с модифицированными углеводами (аналоги нуклеозидов) могут придавать антисмысловым соединениям повышенную устойчивость к нуклеазам, повышенную аффинность связывания или некоторые другие полезные биологические свойства. В некоторых воплощениях нуклеозид содержит химически модифицированное рибофуранозное кольцо.
В некоторых воплощениях олигомер или его первый сегмент содержит по меньшей мере один, например, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24 или 25 аналогов нуклеозидов, например, аналогов нуклеозидов с модифицированным углеводом.
В некоторых воплощениях аналоги нуклеозидов (возможно, независимо) выбирают из группы, состоящей из бициклических аналогов нуклеозидов (таких как LNA) и/или 2'замещенных аналогов нуклеозидов, например, (возможно, независимо) выбранных из группы, состоящей из звеньев 2'-O-алкил-РНК, звеньев 2'-ОМе-РНК, звеньев 2'-амино-ДНК, 2'-АР, 2'-FANA, 2'-(3-гидрокси)пропил и звеньев 2'-фтор-ДНК и/или других аналогов нуклеозидов (возможно) с модифицированным углеводом, таких как морфолино, пептидо-нуклеиновые кислоты (PNA), нуклеиновые кислоты с конформационно ограниченным этилом (CeNA), раскрытые нуклеиновые кислоты (UNA), гексит-нуклеиновые кислоты (HNA), бициклические гексит-нуклеиновые кислоты (bicyclo-HNA) (см., например, WO 2009/100320). В некоторых воплощениях аналоги нуклеозидов повышают аффинность первого сегмента к его нуклеиновой кислоте-мишени (или комплементарной последовательности ДНК или РНК).
В некоторых воплощениях олигомер может содержать по меньшей мере один бициклический аналог нуклеотида, такой как LNA. В некоторых воплощениях первый сегмент содержит по меньшей мере один бициклический аналог нуклеозидов (например, LNA) и/или 2' замещенный аналог нуклеозидов. В некоторых все воплощениях аналоги нуклеозидов, присутствующие в составе олигомера, содержат одинаковым образом модифицированный углеводный компонент. В некоторых воплощениях по меньшей мере один аналог нуклеозида, находящийся в первом сегменте, представляет собой бициклический аналог нуклеозида, например, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, например, все аналоги нуклеозидов (за исключением ДНК и РНК нуклеозидов сегмента В), являются аналогами нуклеозидов с модифицированными углеводами, например, бициклическими аналогами нуклеозидов, такими как LNA, например, бета-D-X-LNA или альфа-L-X-LNA (где X обозначает окси, амино или тио) или другими LNA, описанными в данном документе, включая (R/S) сЕТ, сМОЕ или 5'-Me-LNA, но не ограничиваясь ими.
Примеры химически модифицированного рибофуранозного кольца включают добавление замещающих групп (включая 5' и 2' замещающие группы); связывание мостиком разных атомов кольца с формированием бициклических нуклеиновых кислот (BNA, от англ. bicyclic nucleic acids), замещение атома кислорода рибозильного кольца S, N(R) или C(R1)(R2) (где R представляет собой Н, С1-С2 алкил или защитную группу) и их комбинации, но не ограничиваются ими. Примеры химически модифицированных углеводов включают 2'-F-5'-метил замещенные нуклеозиды (другие 5', 2'-бис замещенные нуклеозиды описаны в заявке на международный WO 2008/101157, опубликованной 8/21/08), замещение атома кислорода в рибозильном кольце атомом S с дальнейшим замещением в положении 2' (см. заявку на патент US 2005/0130923, опубликованную 16 июня 2005), или, в альтернативном случае, 5'-замещенные BNA (см. заявку на международный патент WO 2007/134181, опубликованную 11/22/07, где LNA замещена, например, 5'-метильной или 5'-винильной группой).
Примеры нуклеозидов с модифицированными углеводными компонентами включают нуклеозиды, содержащие 5'-винильную, 5'-метильную (R или S), 4'-S, 2'-F, 2'-ОСН3 и 2'-O(СН2)2ОСН3 замещающие группы. Заместитель, находящийся в положении 2' может также быть выбран из аллила, амино, азидо, тио, О-аллила, О-С1-С10 алкила, OCF3, О(CH2)2SCH3, О(СН2)2-О-N(Rm)(Rn) и О-СН2-С(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой Н или замещенный или незамещенный С1-С10 алкил.
В данном документе «бициклические нуклеозиды" обозначают модифицированные нуклеозиды, содержащие бициклический углеводный компонент. Примеры бициклических нуклеозидов включают нуклеозиды, содержащие мостик между 4' и 2' атомами рибозильного кольца, но не ограничиваются ими. В некоторых воплощениях предложенные соединения включают один или несколько бициклических нуклеозидов, в которых мостик находится в положении 4'-2' бициклического нуклеозида. Примеры подобных 4'-2' бициклических нуклеозидов включают один из нуклеозидов формулы: 4'-(СН2)-О-2' (LNA); 4'-(CH2)-S-2'; 4-(СН2)2-О-2' (ENA); 4'-СН(СН3)-О-2' и 4'-СН(СН2ОСН3)-O-2*, и их аналоги (см. патент US 7,399,845, выданный 15 июля 2008); 4'-С(СН3)(СН3)-O-2', и его аналоги (см. заявку на международный патент WO 2009/006478, опубликованную 8 января 2009); 4'-CH2-N(OCH3)-2', и его аналоги (см. заявку на международный патент WO 2008/150729, опубликованную 11 декабря 2008); 4'-CH2-O-N(CH3)-2' (см. заявку на патент US 2004/0171570, опубликованную 2 сентября 2004); 4'-CH2-N(R)-О-2', где R представляет собой Н, С1-С10 алкил или защитную группу (см. патент US 7,427,672, выданный 23 сентября 2008); 4'-СН2-С(Н)(СН3)-2' (см. Chattopadhyaya, et al, J. Org. Chem., 2009, 74, 118-134) и 4'-CH2-C(=CH2)-2', и его аналоги (см. заявку на международный патент WO 2008/154401, опубликованную 8 декабря 2008), но не ограничиваются ими). Другие примеры приведены в публикациях Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Wahlestedt et al., Proc. Natl. Acad. Sci. U.S.A., 2000, 97, 5633-5638; Kumar et al., Bioorg. Med. Chem. Lett, 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; Srivastava et al., J. Am. Chem. Soc, 129(26) 8362-8379 (Jul. 4, 2007); Elayadi et al., Curr. Opinion Invens. Drugs, 2001, 2, 558-561; Braasch etal., Chem. Biol, 2001, 8, 1-7; Oram et al, Curr. Opinion Mol. Then, 2001, 3, 239-243; U.S. Patent Nos U.S. 6,670,461, 7,053,207, 6,268,490, 6,770,748, 6,794,499, 7,034,133, 6,525,191, 7,399,845; опубликованные заявки на международные патенты WO 2004/106356, WO 94/14226, WO 2005/021570, и WO 2007/134181; публикации US 2004/0171570, US 2007/0287831 и US 2008/0039618; и патенты США US 12/129,154, 60/989,574, 61/026,995, 61/026,998, 61/056,564, 61/086,231, 61/097,787 и 61/099,844; заявки на международные патенты PCT/US2008/064591, PCT/US2008/066154 и PCT/US2008/068922. Каждый из вышеупомянутых бициклических нуклеозидов может содержать углеводы в одной или нескольких стереохимических конфигурациях, включая, например, a-L-рибофуранозу и бета-D-рибофуранозу (см. заявку РСТ DK98/00393, опубликованную 25 марта 1999, а также WO 99/14226).
В некоторых воплощениях бициклические углеводные компоненты BNA-нуклеозидов включают соединения, имеющие по меньшей мере один мостик между атомами в 4' и 2' положении пентафуранозильного углеводного компонента, но не ограничиваются ими, при этом данные мостики независимо содержат 1 или от 2 до 4 присоединенных групп, независимо выбранных из -[CiRaXRb)]-, -C(Ra)=C(Rb)-, -C(Ra)=N-, -C(=NRa)-, -C(=O)-, -C(=S)-, -O-, -Si(Ra)2-, -S(=O)x- и -N(Ra)-; где: x представляет собой 0, 1 или 2; n представляет собой 1, 2, 3 или 4; каждый Ra и Rb независимо представляет собой Н, защитную группу, гидроксил, С1-С12 алкил, замещенный С1-С12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, С2-С12 алкинил, замещенный С2-С12 алкинил, С5-С20 арил, замещенный С5-С20 арил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, С5-С7 алициклический радикал, замещенный С5-С7 эпициклический радикал, галоген, OJ1, NJ1J2, SJ1, N3, COOJ1 ацил (С(=O)-Н), замещенный ацил, CN, сульфонил (S(=O)2-J1) или сульфоксил (S(=O)-J1); а каждый J1 и J2 независимо представляет собой, Н, С1-С6 алкил, замещенный С1-С12 алкил, С2-С12 алкенил, замещенный С2-C12 алкенил, С2-С12 алкинил, замещенный С2-С12 алкинил, С5-С20 арил, замещенный С5-С20 арил, ацил (С(=O)-Н), замещенный ацил, гетероциклический радикал, замещенный гетероциклический радикал, С1-С12 аминоалкил, замещенный С1-С12 аминоалкил или защитную группу.
В некоторых воплощениях мостик бициклического углеводного компонента представляет собой -[C(Ra)(Rb)]n-, -[C(Ra)(Rb)]n-О-, -C(RaRb)-N(R)-О- или -C(RaRb)-О-N(R)-. В некоторых воплощениях мостик представляет собой 4'-СН2-2', 4'-(СН2)2-2', 4'-(СН2)3-2', 4'-СН2-О-2', 4*-(СН2)2-О-2', 4'-СН2-О-N(R)-2' и 4'-CH2-N(R)-О-2'-, где каждый R независимо представляет собой, Н, защитную группу или С1-С12 алкил.
В некоторых воплощениях бициклические нуклеозиды также характеризуются изомерной конфигурацией. Например, нуклеозид, содержащий мостик 4'-2' метиленокси, может находиться в а-L конфигурации или в бета-D конфигурации. Ранее, a-L-метиленокси (4'-СН2-O-2') BNA включали в состав антисмысловых олигонуклеотидов, обладающих антисмысловой активностью (Frieden et al., Nucleic Acids Research, 2003, 21, 6365- 6372).
В некоторых воплощениях бициклические нуклеозиды включают (А) a-L-метиленокси (4'-СН2-O-2') BNA, (В) бета-D-метиленокси (4'-СН2-O-2') BNA, (С) этиленокси (4'-(СН2)2-O-2') BNA, (D) аминоокси (4'-CH2-O-N(R)-2') BNA, (Е) оксиамино (4'-CH2-N(R)-O-2') BNA, (F), метил(метиленокси) (4'-СН(СН3)-O-2') BNA, (G) метилен-тио (4'-CH2-S-2') BNA, (H) метилен-амино (4'-CH2-N(R)-2') BNA, (I) метил карбоциклические (4'-CH2-CH(CH3)-2') BNA и (J) пропилен карбоциклические (4'-(СН2)3-2') BNA, как показано ниже, но не ограничиваются ими.
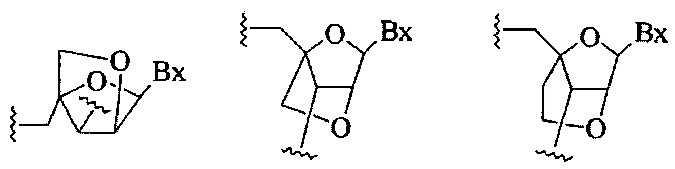


где Вх является основанием, a R независимо представляет собой Н, защитную группу или С1-С2 алкил.
В некоторых воплощениях бициклический нуклеозид имеет Формулу I:

где:
Вх представляет собой гетероциклическое основание;
-Qa-Qb-Qc- is -CH2-N(Rc)-CH2-, -C(=O)-N(Rc)-CH2-, -CH2-O-N(Rc)-, -CH2-N(Rc)-O- или -N(Rc)-O-CH2;
Rc представляет собой C1-C12 алкил или группу, защищающую аминогруппу; и
Ta и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем.
В некоторых воплощениях бициклический нуклеозид имеет формулу II:
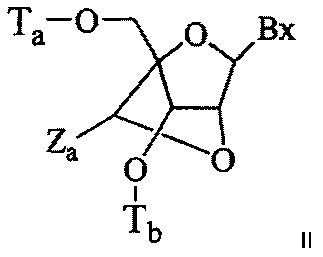
где:
Вх представляет собой гетероциклическое основание;
Ta и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем; Za представляет собой С1-С6 алкил, С2-С6 алкенил, С2-С6 алкинил, замещенный С1-С6 алкил, замещенный С2-С6 алкенил, замещенный С2-С6 алкинил, ацил, замещенный ацил, замещенный амид, тиол или замещенную тиогруппу.
В некоторых воплощениях каждая из замещенных групп независимо является моно- или полизамещенной и содержит один или несколько заместителей, независимо выбранных из галогена, оксо, гидроксила, OJc, NJd, SJC, N3, OC(=X)Jc и NJeC(=X)NJcJd, где каждый Jc, Jd и Je независимо представляет собой, Н, С1-С6 алкил или замещенный С1-С6 алкил, а X представляет собой О или NJC.
В некоторых воплощениях бициклический нуклеозид имеет формулу III:

где:
Вх представляет собой гетероциклическое основание;
Ta и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем;
Rd представляет собой С1-С6 алкил, С2-С6 алкенил, С2-С6 алкинил, замещенный С1-С6 алкил, замещенный С2-С6 алкенил, замещенный С2-С6 алкинил или замещенный ацил (С(=O)-).
В некоторых воплощениях бициклический нуклеозид имеет формулу IV:
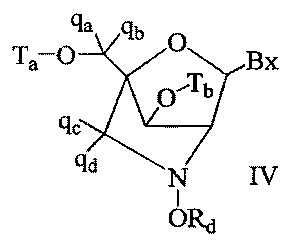
где:
Вх представляет собой гетероциклическое основание;
Та и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем;
Rd представляет собой С1-С6 алкил, замещенный С1-С6 алкил, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил, замещенный С2-С6 алкинил; каждый qb, qc и qd независимо представляет собой, Н, галоген, С1-С6 алкил, замещенный С1-С6 алкил, С2-Се алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил, С1-С6 алкоксил, замещенный Q-С6 алкоксил, ацил, замещенный ацил, С1-С6 аминоалкил или замещенный С1-С6 аминоалкил;
В некоторых воплощениях бициклический нуклеозид имеет формулу V:

где:
Вх представляет собой гетероциклическое основание;
Ta и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем; qa, qb, qc и qf каждый, независимо, представляет собой водород, галоген, C1-C12 алкил, замещенный С1-С12 алкил, С2-С12 алкенил, замещенный С2-C12 алкенил, С2-С12 алкинил, замещенный С2-С12 алкинил, С1-С12 алкокси, замещенный С1-С12 алкокси, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk or N(H)C(=S)NJjJk; или qe и qf вместе представляют собой =C(qg)(qh); qg и qh каждый, независимо, представляют собой Н, галоген, C1-С12 алкил или замещенный С1-С12 алкил.
Синтез и получение мономеров метиленокси (4'-СН2-O-2') BNA аденина, цитозина, гуанина, 5-метил-цитозина, тимина и урацила, наряду с их олигомеризацией и способностью распознавать нуклеиновые кислоты описаны ранее (см., например, Koshkin et al., Tetrahedron, 1998, 54, 3607-3630). BNA и их получение также описаны в WO 98/39352 и WO 99/14226.
Также получены аналоги метиленокси (4'-СН2-O-2') BNA, метиленокси (4'-СН2-O-2') BNA и 2'-тио-BNA (см. например, Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222). Также описано получение закрытых аналогов нуклеозидов, содержащих дуплексы олигодезоксирибонуклеотидов, в качестве субстратов для полимераз нуклеиновых кислот (см., например, Wengel et al., WO 99/14226). Кроме того, в области техники известен синтез 2'-амино-BNA, нового конформационно ограниченного высокоаффинного аналога (см., например, Singh et al., J. Org. Chem., 1998, 63, 10035-10039). Кроме того, получены 2'-амино- и 2'-метиламино-BNA и опубликованы данные о термостабильности их дуплексов с комплементарными цепями РНК и ДНК.
В некоторых воплощениях бициклический нуклеозид имеет формулу VI:
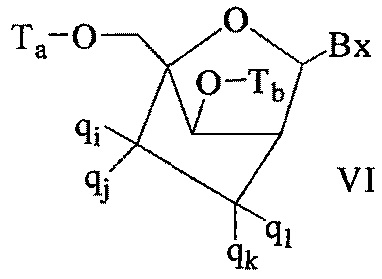
где:
Вх представляет собой гетероциклическое основание;
Ta и Tb каждый, независимо, представляет собой Н, группу, защищающую гидроксил, конъюгированную группу, реактивную фосфорсодержащую группу, фосфорсодержащий компонент или ковалентную связь с иммобилизирующим носителем; каждый qj, qj, qk и ql независимо представляет собой, Н, галоген, С1-С12 алкил, замещенный С1-С12 алкил, С2-С12 алкенил, замещенный С2-С12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, С1-С12 алкоксил, замещенный С2-С12 алкоксил, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk или (H)C(=S)NJjJk; a qi и qj или ql и qk вместе образуют =C(qg)(qh), где qg и qh каждый, независимо, представляют собой Н, галоген, С1-С12 алкил или замещенный С1-С6 алкил.
Описан один карбоциклический бициклический нуклеозид, имеющий 4'-(СН2)3-2' мостик и мостик-аналог алкенила 4'-СН=СН-СН2-2' (см., например, Freier et al., Nucleic Acids Research, 1997, 25(22), 4429- 4443 and Albaek et al., J. Org. Chem., 2006, 71, 7731-77 '40). Также описан синтез и получение карбоциклических бициклических нуклеозидов, а также их олигомеризация и опубликованы данные биохимических исследований (см., например, Srivastava et al, J. Am. Chem. Soc. 2007, 129(26), 8362-8379).
В данном документе "4'-2' бициклический нуклеозид" обозначает бициклический нуклеозид, содержащий фуранозное кольцо, содержащее мостик, соединяющий атом углерода в положении 2' и атом углерода в положении 4'.
В данном документе "моноциклические нуклеозиды" обозначают нуклеозиды, содержащие модифицированные углеводные компоненты, которые не являются бициклическими углеводными компонентами. В некоторых воплощениях углеводный компонент и аналог углеводного компонента нуклеозида могут быть модифицированы или замещены в любом положении.
В данном документе "2'-модифицированный углевод" обозначает фуранозильный углевод, модифицированный в положении 2'. В некоторых воплощениях такие модификации включают заместители, выбранные из: галогенида, включая замещенный и незамещенный алкокси, замещенный и незамещенный тиоалкил, замещенный и незамещенный аминоалкил, замещенный и незамещенный алкил, замещенный и незамещенный аллил, а также замещенный и незамещенный алкинил, но не ограничиваются ими. В некоторых воплощениях 2' модификации выбраны из заместителей, включающих: O[(CH2)nO]mCH3, O(CH2)„NH2, O(СН2)„СН3, O(CH2)„ONH2, OCH2C(=O)N(H)CH3 и O(CH2)nON[(CH2)nCH3]2, где n и m составляют от 1 до приблизительно 10. Другие 2'- заместители могут быть выбраны из: C1-C12 алкила; замещенного алкила; алкенила; алкинила; алкарила; аралкила; О-алкарила или О-аралкила; SH; SCH3; OCN; Cl; Br; CN; CF3; OCF3; SOCH3; SO2CH3; ONO2; NO2; N3; NH2; гетероциклоалкила; гетероциклоалкарила; аминоалкиламино; полиалкиламино; замещенного силила; расщепляющей РНК группы; репортерной группы; интеркалятора; группы, улучшающей фармакокинетические свойства; группы, улучшающей фармакодинамическические свойства антисмыслового соединения, и других заместителей, имеющих схожие свойства, но не ограничиваются ими. В некоторых воплощениях модифицированные нуклеозиды, в качестве боковой цепи содержащие 2'-метоксиэтил (2'-МОЕ, от англ. methoxyethyl) (см., например, Baker et al., J. Biol. Chem., 1997, 272, 1 1944-12000). Показано, что данное замещение 2'-МОЕ улучшает аффинность связывания по сравнению с немодифицированными нуклеозидами и другими модифицированными нуклеозидами, такими как 2'-О-метил, О-пропил и О-аминопропил. Также было показано, что олигонуклеотиды, имеющие заместитель 2-МОЕ, являются антисмысловыми ингибиторами экспрессии генов и обладают свойствами, делающими их перспективными для применения in vivo (см., например, Martin, Р., He/v. Chim. Acta, 1995, 78, 486-504; Altmann et al., Chimia, 1996, 50, 168-176; Altmann et al., Biochem. Soc. Trans., 1996, 24, 630-637; and Altmann et al., Nucleotides, 1997, 16, 917-926).
В данном документе "модифицированный тетрагидропираном нуклеозид" или "модифицированный ТНР нуклеозид" обозначает нуклеозид, имеющий шестичленный тетрагидропирановый "углевод" (суррогат углевода), вместо пентафуранозильного остатка обычных нуклеозидов. Модифицированные ТНР нуклеозиды включают гексит-нуклеиновые кислоты (HNA), альтрит-нуклеиновые кислоты (ANA), маннит-нуклеиновые кислоты (MNA) (см. Leumann, CJ. Bioorg. and Med. Chem. (2002) 10:841-854), фтор-HNA (F-HNA) или соединения, имеющие формулу X:
формула X,
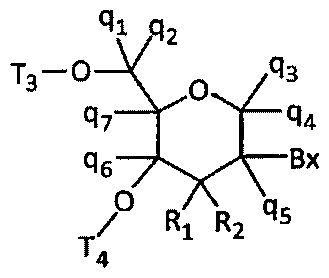
где независимо для каждого по меньшей мере одного тетрагидропиранового аналога нуклеозида формулы X:
Вх представляет собой гетероциклическое основание;
Т3 и Т4 каждый, независимо, представляют собой межнуклеозидную связывающую группу, соединяющую тетрагидропирановый аналог нуклеозида с антисмысловым соединением или один из Т3 и Т4, представляют собой межнуклеозидную связывающую группу, соединяющую тетрагидропирановый аналог нуклеозида с антисмысловым соединением, а другой из Т3 и Т4 представляет собой Н, группу, защищающую гидроксил, присоединенную конъюгированную группу или 5' или 3'-концевую группу; каждый из q1 q2 q3 q4 q5, q6 и q7 и q7 независимо представляет собой Н, С1-С6 алкил, замещенный C1-C6 алкил, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил; и один из R1 и R2 представляет собой водород, а другой выбран из галогена, замещенного или незамещенного алкокси, NJ, J2, SJ,, N3, OC(=X)J1, OC(=X)NJ1J2, NJ3C(=X)NJ1J2 и CN, где X представляет собой О, S или NJ1, а каждый J1, J2 и J3 независимо представляет собой Н или С1-С6 алкил.
В некоторых воплощениях предложены модифицированные ТНР нуклеозиды формулы X, где каждый из qm, qn, qp, qr, qs, qt, и qu представляет собой H. В некоторых воплощениях по меньшей мере один из qm, qn, qp, qr, qs, qt и qu не является H. В некоторых воплощениях по меньшей мере один из qm, qn, qp, qr, qs, qt и qu представляет собой метил. В некоторых воплощениях предложены ТНР нуклеозиды формулы X, где один из R1 и R2 представляет собой F. В некоторых воплощениях R1 представляет собой фтор, a R2 представляет собой Н, R1 представляет собой метокси, a R2 представляет собой Н, R1 представляет собой метоксиэтокси, a R2 представляет собой Н.
В данном документе "2'-модифицированный" или "2'-замещенный" обозначает нуклеозид, содержащий углевод, содержащий в положении 2' заместитель, отличный от Н или ОН. 2'-модифицированные нуклеозиды включают нуклеозиды с немостиковыми 2' заместителями, такими как аллил, амино, азидо, тио, О-аллил, O-C1-С10 алкил, -OCF3, O-(СН2)2-O-СН3, 2'-O(CH2)2SCH3, O-(СН2)2-O-N(Rm)(Rn) или O-CH2-C(=O)-N(Rm)(Rn), где каждый Rm и R„ независимо представляет собой, Н или замещенный или незамещенный С1-С10 алкил, но не ограничиваются ими. 2'-модифицированные нуклеозиды могут также иметь другие модификации, например, в других положениях углевода и/или нуклеинового основания.
В данном документе "2'-F" обозначает углевод, содержащий атом фтора (фтор-группу) в положении 2'.
В данном документе "2'-ОМе" или "2'-ОСН3" или "2'-O-метил" каждый обозначает нуклеозид, содержащий углевод, содержащий группу -ОСН3 в положении 2' углеводного кольца.
В данном документе "олигонуклеотид" обозначает соединение, содержащее множество связанных нуклеозидов.
В некоторых воплощениях один или несколько из множества нуклеозидов модифицированы. В некоторых воплощениях олигонуклеотид содержит один или несколько рибонуклеозидов (РНК) и/или дезоксирибонуклеозидов (ДНК).
В области техники известны многие другие бициклические и трициклические кольцевые системы суррогатов углеводов, которые могут применяться для модификации нуклеозидов для включения в состав антисмысловых соединений (см., например, обзор Leumann, J.С., Bioorganic and Medicinal Chemistry, 2002, 10, 841-854). Для повышения активности в данные кольцевые системы можно вводить различные дополнительные замены. Способы получения модифицированных углеводов хорошо известны специалистам в данной области. Нуклеиновые основания (естественные, модифицированные или их комбинации), входящие в составе нуклеотидов, имеющих модифицированный углеводный компонент, обеспечивают гибридизацию с соответствующей нуклеиновой кислотой - мишенью.
В некоторых воплощениях антисмысловые соединения содержат один или несколько нуклеотидов, имеющих модифицированные углеводные компоненты. В некоторых воплощениях модифицированный углеводный компонент представляет собой 2'-МОЕ. В некоторых воплощениях модифицированные 2'-МОЕ нуклеотиды входят в состав гэпмера. В некоторых воплощениях модифицированный углеводный компонент представляет собой cEt (от англ. constrained ethyl, конформационно ограниченный этил). В некоторых воплощениях модифицированные cEt нуклеотиды расположены на «лопастях» гэпмера.
В некоторых воплощениях R4* и R2* в составе BNA (LNA) вместе обозначают бирадикал -O-СН(СН2ОСН3)- (2'О-метоксиэтил бициклическую нуклеиновую кислоту - Seth at al., 2010, J. Org. Chem), находящийся в R- или S-конфигурации.
В некоторых воплощениях R4* и R2* в составе BNA (LNA) вместе обозначают бирадикал -O-СН(СН2СН3)- (2'О-этил бициклическую нуклеиновую кислоту - Seth at al., 2010, J. Org. Chem), находящийся в R- или S-конфигурации.
В некоторых воплощениях R4* и R2* в составе BNA (LNA) вместе обозначают бирадикал-O-СН(СН3)-, находящийся в R- или S- конфигурации. В некоторых воплощениях R4* и R2* вместе обозначают бирадикал -O-СН2-O-СН2- - (Seth at al., 2010, J. Org. Chem).
В некоторых воплощениях R4* и R2* в составе BNA (LNA) вместе обозначают бирадикал -O-NR-CH3- - (Seth at al., 2010, J. Org. Chem).
В некоторых воплощениях звенья LNA имеют структуру, выбранную из следующей группы:

При исследовании нефротоксичности сЕТ соединения (использовали (S)-сЕТ соединение (6/411847 из WO 2009/12495), которое сравнивали с бета-D-окси LNA соединением (6/392063 из WO 2009/12495)) обнаружено, что сЕТ соединения проявляют неожиданно высокую нефротоксичность по сравнению с бета-D-окси LNA, которые использовали в качестве контроля. Данное исследование представляло собой исследование с однократным введением, после которого через 3 дня выполняли эвтаназию (методы описаны в ЕР 1984381 Пример 41, использовали мышей линии NMRI). Нефротоксичность оценивали с помощью гистологического анализа. Признаки нефротоксичности отмечались при более низких дозах сЕТ соединения, чем повышение АЛТ в сыворотке, что указывало на то, что нефротоксичность соединений сЕТ может представлять особые трудности. Таким образом, применение конъюгатов по данному изобретению, таких как тривалентные конъюгаты GalNAc, может оказаться особенно предпочтительным для снижения нефротоксичности соединений LNA, таких как сЕТ соединения.
Таким образом, олигомер может содержать или состоять из простой последовательности нуклеотидов естественного происхождения предпочтительно 2'-дезоксинуклеотидов (обычно обозначаемых в данном документе «ДНК»), а также возможно, рибонуклеотидов (обычно обозначаемых в данном документе «РНК») или комбинации таких нуклеотидов естественного происхождения с одним или несколькими нуклеотидами искусственного происхождения, т.е. аналогами нуклеотидов. Такие аналоги нуклеотидов могут повышать аффинность олигомера к целевой последовательности.
Включение в состав олигомера аналогов нуклеотидов, увеличивающих аффинность, например, таких как BNA, LNA или 2'-замещенные углеводы, позволит уменьшить размеры специфически связывающегося олигомера, а также понизить верхний предел размеров олигомера, ниже которых происходит неспецифическое или некорректное связывание.
В некоторых воплощениях олигомер содержит по меньшей мере один аналог нуклеозида. В некоторых воплощениях олигомер содержит по меньшей мере два аналога нуклеотида. В некоторых воплощениях олигомер содержит 3-8 аналогов нуклеотидов, например, 6 или 7 аналогов нуклеотидов. В большинстве предпочтительных воплощений по меньшей мере один указанный аналог нуклеотида представляет собой BNA, например, закрытую нуклеиновую кислоту (LNA); например, по меньшей мере 3 или по меньшей мере 4, или по меньшей мере 5, или по меньшей мере 6, или по меньшей мере 7 или 8 аналогов нуклеотидов могут представлять собой BNA, например, LNA. В некоторых воплощениях все аналоги нуклеотидов могут представлять собой BNA, например, LNA.
При упоминании предпочтительного мотива нуклеотидной последовательности или нуклеотидной последовательности, состоящих только из нуклеотидов, следует иметь в виду, что олигомеры по изобретению, характеризуемые данной последовательностью, вместо одного или нескольких нуклеотидов, присутствующих в указанной последовательности, могут содержать соответствующий аналог нуклеотида, например, звенья BNA или другие аналоги нуклеотидов, которые повышают стабильность дуплекса/Tm дуплекса олигомера и мишени (т.е. аналоги нуклеотидов, повышающие аффинность).
Предпочтительным аналогом нуклеотида является LNA, например, окси-LNA (например, бета-D-окси-LNA и альфа-L-окси-LNA) и/или амино-LNA (например, бета-D-амино-LNA и альфа-L-амино-LNA) и/или тио-LNA (например, бета-D-тио-LNA и альфа-L-тио-LNA) и/или ENA (например, бета-D-ENA и альфа-L-ENA).
В некоторых воплощениях аналоги нуклеотидов, присутствующие в составе олигомера по изобретению, независимо выбраны, например, из: звеньев 2'-O-алкил-РНК, звеньев 2'-амино-ДНК, звеньев 2'-фтор-ДНК, звеньев BNA, например, звеньев LNA, звеньев ANA (арабино-нуклеиновой кислоты), звеньев 2'-фтор-ANA, звеньев HNA, звеньев INA (интеркалирующей нуклеиновой кислоты - Christensen, 2002. Nucl. Acids. Res. 2002 30: 4918-4925, содержание публикации включено путем ссылки) и звеньев 2'МОЕ. В некоторых воплощениях в состав олигомера по изобретению, например, его первого сегмента или последовательности смежных нуклеотидов, входит только один из перечисленных выше типов аналогов нуклеотидов.
В некоторых воплощениях дополнительные аналоги нуклеотидов представляют собой 2'-O-метоксиэтил-РНК (2'МОЕ), мономеры 2'-фтор-ДНК или аналоги LNA-нуклеотидов, и, таким образом, олигонуклеотид по изобретению может включать аналоги нуклеотидов, независимо выбранные из указанных трех типов аналогов или может содержать только один тип аналогов, выбранный из трех указанных типов. В некоторых воплощениях по меньшей мере один из указанных аналогов нуклеотидов представляет собой 2'-МОЕ-РНК, например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидных звеньев 2'-МОЕ-РНК. В некоторых воплощениях по меньшей мере один из указанных аналогов нуклеотидов представляет собой 2'-фтор-ДНК, например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидных звеньев 2'-фтор-ДНК.
Олигомер по изобретению содержит по меньшей мере одно звено BNA, например, звено LNA (закрытой нуклеиновой кислоты), например, 1, 2, 3, 4, 5, 6, 7 или 8 звеньев BNA/LNA, например, 3-7 или от 4 до 8 звеньев BNA/LNA или 3, 4, 5, 6 или 7 звеньев BNA/LNA. В некоторых воплощениях все аналоги нуклеотидов представляют собой BNA, например, LNA. В некоторых воплощениях олигомер может содержать как бета-D-окси-LNA, так и один или несколько следующих звеньев LNA: тио-LNA, амино-LNA, окси-LNA и/или ENA, находящиеся в бета-D или в альфа-L конфигурации, или их комбинации. В некоторых воплощениях все цитозины звеньев BNA, например, LNA, представляют собой 5'метил-цитозин. В некоторых воплощениях изобретения олигомер (например, первый и, возможно, второй сегмент) может содержать как звенья BNA и LNA, так и звенья ДНК. В некоторых воплощениях общее количество звеньев LNA и ДНК составляет 10-25, например, 10-24, предпочтительно 10-20, например, 10-18, например, 12-16. В некоторых воплощениях изобретения нуклеотидная последовательность олигомера, его первого сегмента, например, последовательность смежных нуклеотидов, содержит по меньшей мере одно звено BNA, например, LNA, а остальные нуклеотидные звенья представляют собой звенья ДНК. В некоторых воплощениях олигомер или его первый сегмент содержит только аналоги нуклеотидов, представляющие собой BNA, например, LNA, и нуклеотиды естественного происхождения (например, РНК- или ДНК-, наиболее предпочтительно ДНК-нуклеотиды), возможно, с модифицированными межнуклеотидными связями, например, фосфоротиоатными.
Термин "нуклеиновое основание" обозначает основной компонент нуклеотида и охватывает как варианты естественного происхождения, так и искусственного происхождения. Таким образом, "нуклеиновое основание" охватывает не только известные пуриновые и пиримидиновые гетероциклы, но и гетероциклические аналоги и их таутомеры. Считается, что ДНК- или РНК-нуклеозиды в сегменте В могут быть нуклеиновыми основаниями естественного и/или искусственного происхождения, например, нуклеиновыми основаниями ДНК, независимо выбранными из группы А, С, Т и G или из группы С, Т и G.
Примеры нуклеиновых оснований включают аденин, гуанин, цитозин, тимидин, урацил, ксантин, гипоксантин, 5-метилцитозин, изоцитозин, псевдоизоцитозин, 5-бромурацил, 5-пропинилурацил, 6-аминопурин, 2-аминопурин, инозин, диаминопурин и 2-хлор-6-аминопурин, но не ограничиваются ими. В некоторых воплощениях нуклеиновые основания могут быть независимо выбраны из группы, состоящей из аденина, гуанина, цитозина, тимидина, урацила, 5-метилцитозина. В некоторых воплощениях нуклеиновые основания могут быть независимо выбраны из группы, состоящей из аденина, гуанина, цитозина, тимидина и 5-метилцитозина.
В некоторых воплощениях по меньшей мере одно из нуклеиновых оснований, присутствующих в составе олигомера, представляет собой модифицированное нуклеиновое основание, выбранное из группы, состоящей из 5-метилцитозина, изоцитозина, псевдоизоцитозина, 5-бромурацила, 5-пропинилурацила, 6-аминопурина, 2-аминопурина, инозина, диаминопурина и 2-хлор-6-аминопурина.
LNA
Термин "LNA" обозначает бициклический аналог нуклеозида, который содержит бирадикал С2*-С4* (мостик) и известен под названием "закрытая нуклеиновая кислота". Он может обозначать мономер LNA, или, при упоминании в контексте "LNA олигонуклеотида", LNA обозначает олигонуклеотид, содержащий один или несколько таких бициклических аналогов нуклеотидов. В некоторых аспектах бициклические аналоги нуклеозидов представляют собой LNA нуклеотиды, и данные термины могут использоваться взаимозаменяемо, и в указанных воплощениях те и другие характеризуются наличием линкерной группы (например, мостика) между С2' и С4' кольцевыми атомами углевода рибозы.
В некоторых воплощениях LNA, используемый в составе олигонуклеотидных соединений по изобретению, предпочтительно имеет структуру общей формулы II:
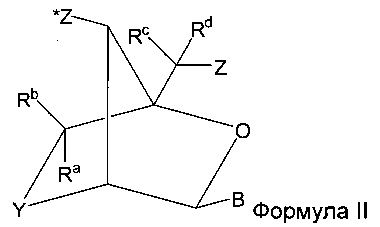
где Y выбран из группы, состоящей из -О-, -CH2O-, -S-, -NH-, N(Re) и/или -СН2-; Z и Z* независимо выбраны из межнуклеотидной связи, RH, концевой группы или защитной группы; В образует основной компонент нуклеотида естественного или искусственного происхождения (нуклеиновое основание), и RH выбран из водорода и С1-4-алкила; Ra, Rb Rc, Rd и Re, возможно, независимо, выбраны из группы, состоящей из водорода, возможно замещенного С1-12-алкила, возможно замещенного С2-12-алкенила, возможно замещенного С2-12-алкинила, гидрокси, C1-12-алкокси, С2-12-алкоксиалкила, С2-12-алкенилокси, карбокси, С1-12-алкоксикарбонила, С1-12-алкилкарбонила, формила, арила, арилокси-карбонила, арилокси, арилкарбонила, гетероарила, гетероарилокси-карбонила, гетероарилокси, гетероарилкарбонила, амино, моно- и ди(С1-6-алкил)амино, карбамоила, моно- и ди(С1-6-алкил)-амино-карбонила, амино-С1-6-алкил-аминокарбонила, моно- и ди(C1-6-алкил)амино-С1-6-алкил-аминокарбонила, C1-6-алкил-карбониламино, карбамидо, С1-6-алканоилокси, сульфоно, C1-6-алкилсульфонилокси, нитро, азидо, сульфанила, C1-6-алкилтио, галогена, интеркаляторов ДНК, фотохимически активных групп, термохимически активных групп, хелатирующих групп, репортерных групп и лигандов, где арил и гетероарил могут быть возможно замещенными, и где два геминальных заместителя Ra и Rb вместе могут обозначать возможно замещенный метилен (=СН2); a RH выбран из водорода и C1-4-алкила. В некоторых воплощениях Ra, Rb Rc, Rd и Re возможно, независимо выбраны из группы, состоящей из водорода и С1-6 алкила, например, метила. Для всех хиральных центров, асимметричные группы могут находиться как в R так и в S ориентации, например, два приведенных в качестве примера стереохимических изомера включают бета-D и альфа-L изоформы, которые можно представить следующим образом:

Некоторые примеры звеньев LNA приведены ниже:



Термин "тио-LNA" включает в себя закрытые нуклеотиды, в которых Y в общей формуле, приведенной выше, выбран из S или -CH2-S-. Тио-LNA могут находиться как в бета-D, так и в альфа-L-конфигурации.
Термин "амино-LNA" включает в себя закрытые нуклеотиды, в которых Y в общей формуле, приведенной выше, выбран из -N(H)-, N(R)-, CH2-N(H)- и -СН2-N(R)-, где R выбран из водорода и C1-4-алкила. Амино-LNA могут находиться как в бета-D, так и в альфа-L-конфигурации.
Термин "окси-LNA" включает в себя закрытые нуклеотиды, в которых Y в общей формуле, приведенной выше, обозначает -О-. Окси-LNA могут находиться как в бета-D, так и в альфа-L-конфигурации.
Термин "ENA" (от англ. ethylene-bridged nucleic acids, нуклеиновые кислоты с этиленовым мостиком) включает в себя закрытые нуклеотиды, в которых Y в общей формуле, приведенной выше, представляет собой -СН2-O- (где атом кислорода в составе -СН2-O- присоединен в 2'-положении относительно основания В). Re представляет собой водород или метил.
В некоторых приведенных в качестве примера воплощениях LNA выбраны из бета-D-окси-LNA, альфа-L-окси-LNA, бета-D-амино-LNA и бета-D-тио-LNA, в частности, бета-D-окси-LNA.
Рекрутирование РНКазы
Считается, что функция олигомерного соединения может реализоваться путем деградации мРНК-мишени, не опосредованной РНКазой, например, за счет создания стерических препятствий при трансляции или другими способами, в некоторых воплощениях олигомеры по изобретению способны рекрутировать эндорибонуклеазу (РНКазу), например, РНКазу Н.
Предпочтительно, такие олигомеры, например, сегмент А или последовательность смежных нуклеотидов, содержит сегмент, состоящий по меньшей мере из 6, например, по меньшей мере из 7 последовательных нуклеотидных звеньев, например, по меньшей мере из 8 или по меньшей мере из 9 последовательных нуклеотидных звеньев (остатков), включая 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 последовательных нуклеотидов, которые при образовании дуплекса с комплементарной РНК-мишенью способны рекрутировать РНКазу. Последовательность смежных нуклеотидов, способная рекрутировать РНКазу, может представлять собой сегмент Y' в составе гэпмера, описанного в данном документе. В некоторых воплощениях размер последовательности смежных нуклеотидов, способной рекрутировать РНКазу, например, сегмента Y', может быть больше, например, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 нуклеотидных звеньев.
ЕР 1222309 предлагает способы определения активности РНКазы Н in vitro, которые можно применять для определения способности рекрутировать РНКазу Н. Считается, что олигомер способен рекрутировать РНКазу Н, если в присутствии комплементарной РНК-мишени, начальная скорость, выраженная в пмоль/л/мин, составляет по меньшей мере 1%, например, по меньшей мере 5%, например, по меньшей мере 10% или более 20% от начальной скорости, измеренной согласно методике, описанной в Примерах 91-95 публикации ЕР 1222309 с использованием ДНК-олигонуклеотидов, имеющих ту же последовательность оснований, но включающих только ДНК-мономеры, не имеющие 2' замен, причем все мономеры в составе олигонуклеотида соединены фосфоротиоатными связями.
В некоторых воплощениях олигомер считается по существу неспособным рекрутировать РНКазу Н, если в присутствии комплементарной РНК-мишени и РНКазы Н начальная скорость РНКазы Н, выраженная в пмоль/л/мин, составляет менее 1%, например, менее 5%, например, менее 10% или менее 20% от начальной скорости, измеренной согласно методике, описанной в Примерах 91-95 публикации ЕР 1222309, с использованием аналогичного олигонуклеотида, состоящего только из звеньев ДНК, не имеющего 2' замен, причем все нуклеотиды в составе олигонуклеотида соединены фосфоротиоатными связями.
В других воплощениях олигомер считается способным рекрутировать РНКазу Н, если в присутствии комплементарной РНК-мишени и РНКазы Н начальная скорость РНКазы Н, выраженная в пмоль/л/мин, составляет по меньшей мере 20%, например, по меньшей мере 40%, например, по меньшей мере 60%, например, по меньшей мере 80% от начальной скорости, измеренной согласно методике, описанной в Примерах 91-95 публикации ЕР 1222309, с использованием аналогичного ДНК олигонуклеотида, не имеющего 2' замен, причем все нуклеотиды в составе олигонуклеотида соединены фосфоротиоатными связями.
Обычно сегмент олигомера, образующий последовательно расположенные нуклеотидные звенья, которые при образовании дуплекса с комплементарной РНК-мишенью способны рекрутировать РНКазу, состоит из нуклеотидных звеньев, образующих с РНК мишенью ДНК/РНК-подобный дуплекс. Олигомер по изобретению, например, первый сегмент, может содержать нуклеотидную последовательность, которая содержит как нуклеотиды, так и аналоги нуклеотидов, и может быть представлен, например, в форме гэпмера (gapmer), хедмера (headmer) или миксмера (mixmer).
"Хедмер" (headmer) обозначает олигомер, который содержит сегмент X' и смежный с ним сегмент Y', при этом 5'-мономер сегмента Y' связан с 3'-мономером сегмента X'. Сегмент X' содержит сегмент смежных аналогов нуклеозидов, не рекрутирующих РНКазу, а сегмент Y' содержит ряд смежных ДНК-мономеров или мономеров аналогов нуклеозидов, которые распознаются и расщепляются РНКазой (например, по меньшей мере 7 последовательно расположенных мономеров).
"Тейлмер" (tailmer) обозначает олигомер, который содержит сегмент X' и смежный с ним сегмент Y', при этом 5'-мономер сегмента Y' связан с 3'-мономером сегмента X'. Сегмент X' содержит ряд смежных ДНК-мономеров или мономеров аналогов нуклеозидов, которые распознаются и расщепляются РНКазой (например, по меньшей мере из 7 последовательно расположенных мономеров), а сегмент X' содержит ряд смежных аналогов нуклеозидов, не рекрутирующих РНКазу.
Другие "химерные" олигомеры, обозначаемые "миксмеры" (mixmers), представляют собой чередующиеся сочетания (i) ДНК-мономеров или мономеров аналогов нуклеозидов, которые распознаются и расщепляются РНКазой, и (ii) мономеров аналогов нуклеозидов, не рекрутирующих РНКазу.
В некоторых воплощениях помимо усиления аффинности олигомера к целевому сегменту, некоторые аналоги нуклеозидов также опосредуют связывание РНКазы (например, РНКазы Н) и расщепление. Поскольку мономеры α-L-LNA (BNA) в некоторой степени рекрутируют РНКазу Н, в некоторых воплощениях гэп-области олигомеров (например, обозначаемые в данном документе сегментом Y'), включающие в себя α-L-LNA мономеры, состоят из меньшего количества мономеров, распознаваемых и расщепляемых РНКазой Н, за счет чего конструкции миксмеров придается большая подвижность.
Строение гэпмеров
В некоторых воплощениях олигомер по изобретению, например, первый сегмент, содержит или представляет собой гэпмер. Гэпмер представляет собой олигомер, который содержит ряд смежных нуклеотидов, способных рекрутировать РНКазу, например, РНКазу Н, например, сегмент по меньшей мере из 6 или 7 ДНК-нуклеотидов, обозначаемый в данном документе сегментом Y' (Y'), причем сегмент Y' фланкирован на 5' и 3' концах сегментами аналогов нуклеотидов, увеличивающих аффинность, например, 1-6 аналогами нуклеотидов, расположенными в направлении 5' и 3' относительно ряда смежных нуклеотидов, способных рекрутировать РНКазу - данные сегменты обозначают сегментами X' (X') и Z' (Z'), соответственно. Примеры гэпмеров описаны в WO 2004/046160, WO 2008/113832 и WO 2007/146511.
В некоторых воплощениях мономеры, способные рекрутировать РНКазу, выбраны из группы, состоящей из ДНК-мономеров, альфа-L-LNA мономеров, С4' алкилированных ДНК-мономеров (см. РСТ/ЕР2009/050349 и Vester et al., Bioorg. Med. Chem. Lett. 18 (2008) 2296-2300, содержание которых включено путем ссылки) и UNA-нуклеотидов (от англ. unlocked nucleic acid, «раскрытые» нуклеиновые кислоты) (см. публикацию Fluiter et al., Mol. Biosyst., 2009, 10, 1039 содержание которой включено путем ссылки). UNA представляют собой «незакрытые» нуклеиновые кислоты, обычно такие, в которых удалена С-С связь между С2 и С3 атомами рибозы, в результате чего образуется незакрытый "углеводный" остаток. Предпочтительно, гэпмер содержит (поли)нуклеотидную последовательность формулы (5'→3'), X'-Y'-Z', где сегмент X' (X') (5' сегмент) содержит или состоит по меньшей мере из одного аналога нуклеотида, например, по меньшей мере одного звена BNA (например, LNA), например, из 1-6 аналогов нуклеотидов, например, звеньев BNA (например, LNA), а сегмент Y' (Y') содержит или состоит по меньшей мере из пяти последовательно расположенных нуклеотидов, которые способны рекрутировать РНКазу (при образовании дуплекса с молекулой комплементарной РНК, например, целевой мРНК), например, ДНК-нуклеотидов, а сегмент Z' (Z') (3' сегмент) содержит или состоит по меньшей мере из одного аналога нуклеотида, например, по меньшей мере одного звена BNA (например, звена LNA), например, из 1-6 аналогов нуклеотидов, например, звеньев BNA (например, LNA).
В некоторых воплощениях сегмент X' состоит из 1, 2, 3, 4, 5 или 6 аналогов нуклеотидов, например, звеньев BNA (например, LNA), например, из 2-5 аналогов нуклеотидов, например, из 2-5 звеньев LNA, например, из 3 или 4 аналогов нуклеотидов, например, из 3 или 4 звеньев LNA; и/или сегмент Z' состоит из 1, 2, 3, 4, 5 или 6 аналогов нуклеотидов, например, звеньев BNA (например, LNA), например, из 2-5 аналогов нуклеотидов, например, 2-5 звеньев BNA (например, LNA), например, из 3 или 4 аналогов нуклеотидов, например, из 3 или 4 звеньев BNA (например, LNA).
В некоторых воплощениях Y содержит или состоит из 5, 6, 7, 8, 9, 10, 11 или 12 последовательно расположенных нуклеотидов, которые способны рекрутировать РНКазу, или из 6-10 или из 7-9, например, из 8 последовательно расположенных нуклеотидов, которые способны рекрутировать РНКазу. В некоторых воплощениях сегмент Y' представляет собой или содержит по меньшей мере одно звено ДНК-нуклеотида, например, 1-12 звеньев ДНК, предпочтительно 4-12 звеньев ДНК, более предпочтительно, 6-10 звеньев ДНК, например, 7-10 звеньев ДНК, наиболее предпочтительно 8, 9 или 10 звеньев ДНК.
В некоторых воплощениях сегмент X' состоит из 3 или 4 аналогов нуклеотидов, например, BNA (например, LNA), сегмент X' состоит из 7, 8, 9 или 10 звеньев ДНК, и сегмент Z' состоит из 3 или 4 аналогов нуклеотидов, например, BNA (например, LNA). Такое строение включает (X'-Y'-Z') 3-10-3, 3-10-4, 4-10-3, 3-9-3, 3-9-4, 4-9-3, 3-8-3, 3-8-4, 4-8-3, 3-7-3, 3-7-4, 4-7-3.
Гэпмеры другого строения описаны в WO 2004/046160, содержание которого включено путем ссылки. WO 2008/113832, где испрашивается приоритет предварительной заявки на патент US 60/977,409, содержание которой включено путем ссылки, относится к гэпмерам, представляющим собой короткие олигомеры 'шортмеры' (shortmer). В некоторых воплощениях представленные олигомеры могут быть такими короткими гэпмерами - шортмерами.
В некоторых воплощениях олигомер, например, сегмент X', включает в себя последовательность смежных нуклеотидов из 10, 11, 12, 13 или 14 нуклеотидных звеньев, где последовательность смежных нуклеотидов содержит или представляет собой последовательность формулы (5'-3'), X'-Y'-Z' где; X' состоит из 1, 2 или 3 звеньев аналогов нуклеотидов, например, звеньев BNA (например, LNA); Y' состоит из 7, 8 или 9 последовательно расположенных звеньев нуклеотидов, которые способны рекрутировать РНКазу при образовании дуплекса с молекулой комплементарной РНК (например, целевой мРНК); и Z' состоит из 1, 2 или 3 звеньев аналогов нуклеотидов, например, звеньев BNA (например, LNA).
В некоторых воплощениях X' состоит из 1 звена BNA (например, LNA). В некоторых воплощениях X' состоит из 2 звеньев BNA (например, LNA). В некоторых воплощениях X' состоит из 3 звеньев BNA (например, LNA). В некоторых воплощениях Z' состоит из 1 звена BNA (например, LNA). В некоторых воплощениях Z' состоит из 2 звеньев BNA (например, LNA). В некоторых воплощениях Z' состоит из 3 звеньев BNA (например, LNA). В некоторых воплощениях Y' состоит из 7 нуклеотидных звеньев. В некоторых воплощениях Y' состоит из 8 нуклеотидных звеньев. В некоторых воплощениях Y' состоит из 9 нуклеотидных звеньев. В некоторых воплощениях сегмент Y' состоит из 10 мономеров нуклеозидов. В некоторых воплощениях сегмент Y' содержит или состоит из 1-10 мономеров ДНК. В некоторых воплощениях Y' содержит от 1 до 9 звеньев ДНК, например, 2, 3, 4, 5, 6, 7, 8 или 9 звеньев ДНК. В некоторых воплощениях Y' состоит из звеньев ДНК. В некоторых воплощениях Y' содержит по меньшей мере одно звено BNA, которое находится в альфа-L конфигурации, например, 2, 3, 4, 5, 6, 7, 8 или 9 звеньев LNA в альфа-L-конфигурации. В некоторых воплощениях Y' содержит по меньшей мере одно звено альфа-L-окси BNA/LNA или где все звенья LNA в альфа-L-конфигурации представляют собой звенья альфа-L-окси LNA. В некоторых воплощениях число нуклеотидов, входящих в состав X'-Y'-Z', выбрано из группы, состоящей из (звенья аналогов нуклеотидов - сегмент Y' - звенья аналогов нуклеотидов): 1-8-1, 1-8-2, 2-8-1, 2-8-2, 3-8-3, 2-8-3, 3-8-2, 4-8-1, 4-8-2, 1-8-4, 2-8-4, or; 1-9-1, 1-9-2, 2-9-1, 2-9-2, 2-9-3, 3-9-2, 1-9-3, 3-9-1, 4-9-1, 1-9-4, or; 1-10-1, 1-10-2, 2-10-1, 2-10-2, 1-10-3, 3-10-1. В некоторых воплощениях число нуклеотидов в составе X'-Y'-Z' выбрано из группы, состоящей из: 2-7-1, 1-7-2, 2-7-2, 3-7-3, 2-7-3, 3-7-2, 3-7-4 и 4-7-3. В некоторых воплощениях каждый из сегментов X' и Y' состоит из трех мономеров BNA (например, LNA), а сегмент Y' состоит из 8 или 9 или 10 мономеров нуклеозидов, предпочтительно из мономеров ДНК. В некоторых воплощениях как X', так и Z' состоят из двух звеньев BNA (например, LNA), a Y состоит из 8 или 9 звеньев нуклеотидов, предпочтительно звеньев ДНК. В различных воплощениях гэпмеры другого строения включают такие, в которых сегменты X' и/или Z' состоят из 3, 4, 5 или 6 аналогов нуклеозидов, например, мономеров, содержащих углевод 2'-O-метоксиэтил-рибозу (2'-МОЕ), или мономеров, содержащих углевод 2'-фтор-дезоксирибозу, а сегмент Y' состоит из 8, 9, 10, 11 или 12 нуклеозидов, например, мономеров ДНК, где сегменты X'-Y'-Z' имеют 3-9-3, 3-10-3, 5-10-5 или 4-12-4 мономеров. Гэпмеры другого строения описаны в WO 2007/146511А2, содержание которого включено путем ссылки.
Гэпмеры BNA и LNA: термины BNA и LNA используются взаимозаменяемо. Гэпмер BNA представляет собой олигомер гепмер (сегмент А), который содержит по меньшей мере один BNA нуклеотид. Гэпмер LNA представляет собой олигомер гэпмер (сегмент А), который содержит по меньшей мере один LNA нуклеотид.
Переключающие сплайсинг олигомеры
В некоторых воплощениях антисмысловой олигонуклеотид представляет собой переключающий сплайсинг олигомер - т.е. олигомер, мишенью которого является пре-мРНК, вызывающий альтернативный сплайсинг пре-мРНК.
Мишени переключающих сплайсинг олигомеров могут включать рецептор TNF, например, переключающие сплайсинг олигомеры могут представлять собой один или несколько из переключающих сплайсинг TNFR олигомеров, описанных в WO 2007/058894, WO 08051306 А1 и РСТ/ЕР2007/061211, содержание которых включено путем ссылки.
Переключающие сплайсинг олигомеры обычно (по существу) не способны рекрутировать РНКазу Н и такие конструкции, как гэпмеры, тейлмеры или хедмеры, обычно нежелательны. Однако такие конструкции, как миксмеры и тоталмеры, являются подходящими конструкциями для переключающих сплайсинг олигомеров.
Переключающие сплайсинг олигомеры также применяли для устранения дефицита дистрофина при мышечной дистрофии Дюшенна.
Миксмеры
Большинство антисмысловых олигонуклеотидов представляют собой соединения, которые предназначены для рекрутирования фермента РНКазы (например, РНКазы Н) для деградации их мишеней. Такие соединения включают ДНК олигонуклеотиды с фосфоротиоатными связями, а также гэпмеры, хедмеры и тейлмеры. Данные соединения обычно содержат сегмент по меньшей мере из 5 или 6 ДНК нуклеотидов, а в случае гэпмеров фланкированы с каждой стороны аналогами нуклеотидов, повышающими аффинность.
Механизм действия олигомеров по данному изобретению может быть независимым от РНКаз (например, РНКазы Н). Примерами олигомеров, механизм действия которых не связан с РНКазой Н (или с РНКазами) являются миксмеры и тоталмеры.
Термин "миксмеры" обозначает олигомеры, которые содержат нуклеотиды естественного и искусственного происхождения, которые, в отличие от гэпмеров, тейлмеров и хедмеров не содержат последовательности смежных нуклеотидов более чем из 5, а в некоторых воплощениях более чем из 4, например, более чем из 3 последовательно расположенных нуклеотидов естественного происхождения, например, звеньев ДНК. В некоторых воплощениях миксмеры не содержат более 5 последовательно расположенных аналогов нуклеозидов, например, BNA (LNA), а в некоторых воплощениях более 4, например, более трех последовательно расположенных аналогов нуклеозидов, например, BNA (LNA). Остальные нуклеозиды в таких миксмерах могут, например, быть ДНК нуклеозидами, и/или небициклическими аналогами нуклеозидов, например, указанными в данном документе, например, 2' замещенными аналогами нуклеозидов, например, 2'-O-МОЕ и/или 2'фтор.
Олигомеры по изобретению могут быть миксмерами - миксмеры различного строения могут успешно применяться в качестве олигомера или его первого сегмента, в частности, когда их мишенью являются микроРНК (анти-миР), сайты связывания микроРНК на мРНК (Blockmirs), или в качестве переключающих сплайсинг олигомеров (SSO, от англ. splice switching oligomers). См., например, WO 2007/112754 (LNA-AntimiRs™), WO 2008/131807 (LNA олигомеры, переключающие сплайсинг).
В некоторых воплощениях олигомер или миксмер может содержать BNA и 2' замещенные аналоги нуклеозидов, возможно, с ДНК нуклеозидами - см., например, WO 07027894 и WO 2007/112754, содержание которых включено путем ссылки. Конкретными примерами являются олигомеры или первые сегменты, содержащие LNA, 2'-O-МОЕ и ДНК, LNA, 2'фтор и 2'-O-МОЕ, 2'-O-МОЕ и 2'фтор, 2'-O-МОЕ и 2'фтор и LNA или LNA и 2'-O-МОЕ и LNA и ДНК.
В некоторых воплощениях олигомер или миксмер содержит или состоит из последовательности смежных нуклеотидов с повторяющейся комбинацией аналогов нуклеотидов и нуклеотидов естественного происхождения или аналогов нуклеотидов первого типа и аналогов нуклеотидов второго типа. Например, каждый второй или каждый третий нуклеотид в повторяющейся комбинации может быть аналогом нуклеотида, например, BNA (LNA), а остальные нуклеотиды могут быть нуклеотидами естественного происхождения, например, ДНК, или 2'замещенными аналогами нуклеотида, например, обозначаемыми в данном документе 2'МОЕ или 2'фтор аналогами, или, в некоторых воплощениях могут быть выбраны из группы аналогов нуклеотидов, указанных в данном документе. Считается, что повторяющаяся комбинация аналогов нуклеотидов, например, звеньев LNA, может содержать аналоги нуклеотидов в фиксированных положениях - например, на 5' или 3' концах.
В некоторых воплощениях первый нуклеотид олигомера или миксмера, начиная с 3' конца, представляет собой аналог нуклеотида, например, LNA-нуклеотид.
В некоторых воплощениях, которые могут быть одинаковыми или различными, второй нуклеотид олигомера или миксмера, начиная с 3' конца, представляет собой аналог нуклеотида, например, LNA-нуклеотид.
В некоторых воплощениях, которые могут быть одинаковыми или различными, седьмой и/или восьмой нуклеотид олигомера или миксмера, а в некоторых воплощениях, девятый и/или десятый нуклеотид олигомера или миксмера, начиная с 3' конца, представляет собой аналог нуклеотида, например, LNA нуклеотид.
В некоторых воплощениях, которые могут быть одинаковыми или различными, 5' концевой нуклеотид олигомера или миксмера представляет собой аналог нуклеотида, например, LNA-нуклеотид.
В некоторых воплощениях указанные выше особенности строения могут быть присущи строению миксмеров, например, миксмеров анти-миР.
В некоторых воплощениях олигомер или миксмер не содержит сегмента более чем из 4 последовательно расположенных звеньев ДНК-нуклеотидов или 3 последовательно расположенных звеньев ДНК-нуклеотидов. В некоторых воплощениях миксмер не содержит сегмента более чем из 2 последовательно расположенных звеньев ДНК-нуклеотидов.
В некоторых воплощениях олигомер или миксмер содержит по меньшей мере один сегмент, состоящий по меньшей мере из двух последовательно расположенных звеньев аналогов нуклеотидов, например, по меньшей мере из двух последовательно расположенных звеньев LNA.
В некоторых воплощениях олигомер или миксмер содержит по меньшей мере один сегмент, состоящий по меньшей мере из трех последовательно расположенных звеньев аналогов нуклеотидов, например, по меньшей мере из трех последовательно расположенных звеньев LNA.
В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 7 последовательно расположенных звеньев аналогов нуклеотидов, например, звеньев LNA. В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 6 последовательно расположенных звеньев аналогов нуклеотидов, например, звеньев LNA. В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 5 последовательно расположенных звеньев аналогов нуклеотида, например, звеньев LNA. В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 4 последовательно расположенных звеньев аналогов нуклеотида, например, звеньев LNA. В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 3 последовательно расположенных звеньев аналогов нуклеотида, например, звеньев LNA. В некоторых воплощениях олигомер или миксмер по изобретению не содержит сегмента из более чем 2 последовательно расположенных звеньев аналогов нуклеотида, например, звеньев LNA.
Следующие воплощения могут касаться таких олигомеров, как миксмеры или тоталмеры (например, сегмента А):
Олигомер (например, сегмент А) по изобретению в некоторых воплощениях может содержать по меньшей мере две чередующиеся области LNA и не-LNA нуклеотидов (например, ДНК-нуклеотидов или 2'-замещенных аналогов нуклеотидов).
Олигомер по изобретению в некоторых воплощениях может содержать последовательность смежных нуклеотидов формулы: 5' ([LNA нуклеотид]1-5 и [не-LNA нуклеотид]1-4)2-12. 3'.
В некоторых воплощениях 5' нуклеотид последовательности смежных нуклеотидов (или олигомер) представляет собой LNA нуклеотид.
В некоторых воплощениях 3' нуклеотид последовательности смежных нуклеотидов представляет собой аналог нуклеотида, например, LNA, или 2, 3, 4, 5 3' нуклеотидов представляют собой аналоги нуклеотидов, например, LNA нуклеотиды или другие аналоги нуклеотидов, которые придают олигомеру повышенную стабильность в сыворотке.
В некоторых воплощениях последовательность смежных нуклеотидов олигомера имеет формулу 5' ([LNA нуклеотид]1-5 - [не-LNA нуклеотид]1-4)2-11 - [LNA нуклеотид]1-5 3'.
В некоторых воплощениях последовательность смежных нуклеотидов олигомера имеет 2, 3 или 4 сегмента смежных LNA и не-LNA нуклеотидов - например, содержит последовательность формулы 5' ([LNA нуклеотид]1-5 и [не-LNA нуклеотид]1-4)2-3, за которой, возможно, следует 3' LNA сегмент: [LNA нуклеотид]1-5.
В некоторых воплощениях последовательность смежных нуклеотидов олигомера содержит последовательность 5' ([LNA нуклеотид]1-3 и [не-LNA нуклеотид]1-3)2-5, за которой, возможно, следует 3' LNA сегмент: [LNA нуклеотид]1-3.
В некоторых воплощениях последовательность смежных нуклеотидов олигомера содержит последовательность 5' ([LNA нуклеотид]1-3 и [не-LNA нуклеотид]1-3)3, за которой, возможно, следует 3' LNA сегмент: [LNA нуклеотид]1-3.
В некоторых воплощениях все не-LNA нуклеотиды представляют собой ДНК-нуклеотиды.
В некоторых воплощениях не-LNA нуклеотиды независимо или зависимо друг от друга выбраны из группы, состоящей из звеньев ДНК, звеньев РНК, звеньев 2'-O-алкил-РНК, звеньев 2'-OMe-РНК, звеньев 2'-амино-ДНК и звеньев 2'-фтор-ДНК.
В некоторых воплощениях не-LNA нуклеотиды (возможно, независимо друг от друга) выбраны из группы, состоящей из 2'-замещенных аналогов нуклеозидов, например, (возможно, независимо) выбраны из группы, состоящей из звеньев 2'-O-алкил-РНК, звеньев 2'-ОМе-РНК, звеньев 2'-амино-ДНК, 2'-АР, 2'-FANA, 2'-(3-гидрокси)пропил и звеньев 2'-фтор-ДНК и/или других аналогов нуклеозидов (возможно) с модифицированным углеводом, например, морфолино-аналогов, аналогов нуклеозидов пептидо-нуклеиновых кислот (PNA), CeNA, раскрытых нуклеиновых кислот (UNA), гексит-нуклеиновых кислот (HNA), бициклических HNA (см., например, WO 2009/100320), в некоторых воплощениях аналоги нуклеозидов повышают аффинность первого сегмента к его нуклеиновой кислоте-мишени (или комплементарной последовательности ДНК или РНК). Различные аналоги нуклеозидов описаны публикациях Freier & Altmann; Nucl. Acid Res., 1997, 25, 4429-4443 и Uhlmann; Curr. Opinion in Drug Development, 2000, 3(2), 293-213, содержание которых включено путем ссылки.
В некоторых воплощениях не-LNA нуклеотиды представляют собой ДНК-нуклеотиды. В некоторых воплощениях олигомер или последовательность смежных нуклеотидов содержит LNA-нуклеотиды и, возможно, другие аналоги нуклеотидов (например, аналоги нуклеотидов, перечисленные среди не-LNA нуклеотидов), которые могут представлять собой аналоги нуклеотидов, повышающие аффинность, и/или аналоги нуклеотидов, повышающие стабильность в сыворотке.
В некоторых воплощениях олигомер или его последовательность смежных нуклеотидов включает в себя последовательность смежных аналогов нуклеотидов, указанных выше.
В некоторых воплощениях олигомер или его последовательность смежных нуклеотидов включает в себя последовательность смежных LNA нуклеотидов.
В некоторых воплощениях олигомер или последовательность смежных нуклеотидов имеет длину 8-12, например, 8-10 или 10-20, например, 12-18 или 14-16 нуклеотидов.
В некоторых воплощениях олигомер или последовательность смежных нуклеотидов способна образовывать дуплекс с комплементарной молекулой одноцепочечной РНК, содержащей фосфодиэфирные межнуклеозидные связи, где Tm дуплекса составляет по меньшей мере приблизительно 60°С, например, по меньшей мере 65°С.
Пример определения Tm: олигонуклеотид: дуплексы олигонуклеотида и РНК-мишени (РО) разводят до концентрации 3 мМ в 500 мл свободной от РНКаз воды и смешивают с 500 мл 2х Tm-буфера (200 мМ NaCl, 0,2 мМ EDTA, 20 мМ Na фосфат, pH 7,0). Раствор нагревают до 95°С в течение 3 мин, а затем оставляют для отжига при комнатной температуре в течение 30 мин. Температуру плавления дуплекса (Tm) измеряют с помощью спектрофотометра Lambda 40 UV/VIS, снабженного температурным контроллером Пелтье РТР6 с использованием программного обеспечения РЕ Templab (Perkin Elmer). Температуру повышают от 20°С до 95°С, а затем снижают до 25°С, регистрируя абсорбцию при 260 нм. Для оценки Тт дуплекса используют первую производную и локальные максимумы при плавлении и отжиге.
Тоталмеры
Тоталмер представляет собой одноцепочечный олигомер, который содержит только нуклеозиды искусственного происхождения, например, аналоги нуклеозидов с модифицированными углеводами.
Согласно изобретению, первый сегмент может представлять собой тоталмер - тоталмеры различного строения могут успешно применяться в качестве олигомера или его первого сегмента, в частности, когда их мишенью являются микроРНК (анти-миР), или в качестве переключающих сплайсинг олигомеров (SSO). В некоторых воплощениях тоталмер содержит или состоит по меньшей мере из одного мотива XYX или YXY, например, повторяющейся последовательности XYX или YXY, где X представляет собой LNA, a Y представляет собой альтернативный (т.е. отличный от LNA) аналог нуклеотида, например, звено 2'-O-МОЕ РНК и звено 2'-фтор ДНК. В некоторых воплощениях указанные выше мотивы могут представлять собой, например, XXY, XYX, YXY или YYX.
В некоторых воплощениях тоталмер может содержать или состоять из последовательности смежных нуклеотидов длиной 7-16 нуклеотидов, например, из 9, 10, 11, 12, 13, 14 или 15 нуклеотидов, например, из 7-12 нуклеотидов.
В некоторых воплощениях последовательность смежных нуклеотидов тоталмера содержит по меньшей мере 30%, например, по меньшей мере 40%, например, по меньшей мере 50%, например, по меньшей мере 60%, например, по меньшей мере 70%, например, по меньшей мере 80%, например, по меньшей мере 90%, например, 95%, например, 100% звеньев BNA (LNA). Остальные звенья могут быть выбраны из не-LNA аналогов нуклеотидов, приведенных в данном документе, например, выбранных из группы, состоящей из звена 2'-O_алкил-РНК, звена 2'-ОМе-РНК, звена 2'-амино-ДНК, звена 2'-фтор-ДНК, звена LNA, звена PNA, звена HNA, звена INA и звена 2'МОЕ-РНК или из группы, состоящей из звена 2'-ОМе-РНК и звена 2'-фтор-ДНК.
В некоторых воплощениях тоталмер представляет собой или состоит из последовательности смежных нуклеотидов, которая состоит только из звеньев LNA. В некоторых воплощениях тоталмер, например, LNA тоталмер, имеет длину 7-12 нуклеозидных звеньев. В некоторых воплощениях мишенью тоталмера (олигомера или его первого сегмента) может быть микроРНК (т.е. он может представлять собой анти-миР) - как описано в WO 2009/043353, содержание которого включено путем ссылки.
В некоторых воплощениях олигомер или последовательность смежных нуклеотидов содержит LNA-нуклеотиды и, возможно, другие аналоги нуклеотидов, которые могут быть аналогами нуклеотидов, повышающими аффинность, и/или аналогами нуклеотидов, повышающими стабильность в сыворотке.
В некоторых воплощениях олигомер или его последовательность смежных нуклеотидов включает в себя непрерывную нуклеотидную последовательность указанных аналогов нуклеотидов.
В некоторых воплощениях олигомер или его последовательность смежных нуклеотидов включает в себя непрерывную нуклеотидную последовательность LNA-нуклеотидов.
Регуляция микроРНК с помощью олигомеров по изобретению
В некоторых воплощениях олигомер или его первый сегмент представляет собой олигомер, например, LNA-antimiR® (LNA миксмер или тоталмер), который содержит или состоит из последовательности смежных нуклеотидов, соответствующей или полностью комплементарной последовательности микроРНК, например, зрелой микроРНК или ее части. Применение данного изобретения для контролирования активности микроРНК in vivo имеет исключительную важность, поскольку микроРНК обычно регулируют множество мРНК индивидуума. Следовательно, инактивация используемых в терапевтических целях анти-миР крайне актуальна.
Различные микроРНК связаны с рядом заболеваний - см., например, WO 2009/043353. В некоторых воплощениях мишенью олигомера может быть микроРНК, т.е. олигомер содержит или состоит из последовательности смежных нуклеотидов, полностью комплементарной микроРНК (или ее соответствующему сегменту). МикроРНК может представлять собой микроРНК, которая экспрессируется в печени, например, микроРНК-21, микроРНК-221, миР-122 или миР-33 (миР-33a и миР-33b).
Так, в некоторых аспектах изобретение относится к лечению заболеваний, связанных с экспрессией микроРНК. В некоторых воплощениях олигомер по изобретению или его первый сегмент содержит или состоит из последовательности смежных нуклеотидов, которая соответствует или является полностью комплементарной последовательности микроРНК, например, последовательности зрелой микроРНК, например, микроРНК человека, последовательность которой опубликована в базе miRBase (http://microrna.sanger.ac.uk/cgi-bin/sequences/mirna_summary.pl?org=hsa). В некоторых воплощениях микроРНК является вирусной микроРНК. На момент составления заявки в базе miRbase 19 находятся 1600 последовательностей предшественников и 2042 последовательности зрелых миРНК, все из которых включены путем ссылки, в том числе и последовательности зрелой микроРНК каждой микроРНК человека. В некоторых воплощениях олигомер по изобретению содержит или состоит из последовательности смежных нуклеотидов, которая соответствует или является полностью комплементарной hsa-miR122 (NR_029667.1 GI:262205241), например, зрелой hsa-miR-122. В некоторых воплощениях олигомер по изобретению содержит или состоит из последовательности смежных нуклеотидов, которая соответствует или является полностью комплементарной hsa-miR122 (NR_029667.1 GI:262205241), например, зрелой hsa-miR-122 по всей длине олигомера.
В некоторых воплощениях, когда мишенью олигомера или его первого сегмента является миР-122, олигомер применяют для лечения инфекции, вызванной вирусом гепатита С.
В некоторых воплощениях, когда мишенью олигомера является hsa-miR-33, например, hsa-miR-33a (GUGCAUUGUAGUUGCAUUGCA) или hsa-miR-33b (GUGCAUUGCUGUUGCAUUGC), его применяют для лечения метаболического заболевания, например, метаболического синдрома, атеросклероза, гиперхолестеринемии и ассоциированных нарушений. См. Najafi-Shoushtar et al, Science 328 1566-1569, Rayner et al., Science 328 (1570-1573), Horie et al., J Am Heart Assoc. 2012, Dec 1(6). Другие экспрессируемые в печени микроРНК, которые могут быть мишенями при лечении метаболических заболеваний, включают miR-758, miR-10b, miR-26 и miR-106b, известные своей способностью непосредственно модулировать транспорт холестерина (см. Davalos & Fernandez-Hernando, Pharmacol Res. 2013 Feb). Таким образом, мишенью может быть микроРНК, выбранная из группы, состоящей из miR-122 (MIMAT0004590), miR-33 (MIMAT0000091, MIMAT0003301), miR-758 (MIMAT0003879), miR-10b (MIPF0000033), miR-26a (MIMAT0000082) и miR-106b (MIMAT0004672). Указаны ссылки на микроРНК в базе miRBase 19.
Анти-миР олигомеры
Строение предпочтительного "анти-миР" олигомера или его первого сегмента изложено в WO 2007/112754, WO 2007/112753, PCT/DK2008/000344 и предварительных заявках на патент US 60/979217 и 61/028062, содержание которых включено путем ссылки. В некоторых воплощениях олигомер или его первый сегмент представляют собой анти-миР, который представляет собой миксмер или тоталмер. Таким образом, термин анти-миР можно заменить термином олигомер.
Олигомеры анти-миР представляют собой олигомеры, которые содержат или состоят из последовательности смежных нуклеотидов, полностью комплементарной или по существу комплементарной (т.е., возможно, содержащей один или два некомплементарных основания) последовательности микроРНК или соответствующей части ее последовательности. В этом случае считается, что анти-миР может содержать последовательность смежных нуклеотидов, которая комплементарна или по существу комплементарна всей зрелой микроРНК, или анти-миР может содержать последовательность смежных нуклеотидов, которая комплементарна или по существу комплементарна части последовательности зрелой микроРНК или пре-микроРНК - такая часть последовательности (а следовательно, соответствующая последовательность смежных нуклеотидов) обычно имеет длину по меньшей мере 8 нуклеотидов, например, от 8 до 25 нуклеотидов, например, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 нуклеотидов, например, 10-17 или 10-16 нуклеотидов, например, 12-15 нуклеотидов.
Известны анти-миР различного строения, обычно анти-миР, используемые в терапевтических целях, или их последовательность смежных нуклеотидов содержат одно или несколько звеньев аналогов нуклеотидов.
В некоторых воплощениях анти-миР могут иметь структуру гэпмеров, как в данном описании. Однако, согласно WO 2007/112754 и WO 2007/112753, предпочтительным может быть другое строение, например, миксмеры или тоталмеры.
В WO 2007/112754 и WO 2007/112753, содержание которых включено путем ссылки, описаны анти-миР олигомеры и строение анти-миР олигомеров, где олигомеры комплементарны зрелой микроРНК.
В некоторых воплощениях часть последовательности анти-миР соответствует последовательности сайта узнавания мишени, т.н. «seed region» миРНК. В некоторых воплощениях первое или второе нуклеиновое основание 3' конца олигомера соответствует второму нуклеотиду 5' конца последовательности микроРНК.
В некоторых воплощениях с 1 по 6 (включительно) нуклеиновые основания олигомера, считая с 3' конца олигомера, комплементарны последовательности «seed region» микроРНК.
В некоторых воплощениях с 1 по 7 (включительно) нуклеиновые основания олигомера, считая с 3' конца олигомера, комплементарны последовательности «seed region» микроРНК.
В некоторых воплощениях со 2 по 7 (включительно) нуклеиновые основания олигомера, считая с 3' конца олигомера, комплементарны последовательности «seed region» микроРНК.
В некоторых воплощениях анти-миР олигомер содержит по меньшей мере один аналог нуклеотида, например, по меньшей мере одно звено LNA, в положении, которое находится в составе сегмента, комплементарного «seed region» миРНК. В некоторых воплощениях анти-миР олигомер содержит от 1 до 6 или от 1 до 7 звеньев аналогов нуклеотида, например, от 1 до 6 и от 1 до 7 звеньев LNA, в положениях, которые находятся в составе области, комплементарной «seed region» миРНК.
В некоторых воплощениях анти-миР по изобретению имеет длину 7, 8 или 9 нуклеотидов и содержит последовательность смежных нуклеотидов, которая комплементарна «seed region» микроРНК человека или вируса, где по меньшей мере 80%, например, 85%, например, 90%, например, 95%, например, 100% нуклеотидов представляют собой LNA.
В некоторых воплощениях анти-миР по изобретению имеет длину 7, 8 или 9 нуклеотидов и содержит последовательность смежных нуклеотидов, которая комплементарна «seed region» микроРНК человека или вируса, где по меньшей мере 80% нуклеотидов представляют собой LNA, где по меньшей мере 80%, например, 85%, например, 90%, например, 95%, например, 100% межнуклеотидных связей представляют собой фосфоротиоатные связи.
В некоторых воплощениях анти-миР содержит одно или два звена LNA в положениях 3-8, считая с 3' конца. Это предпочтительно для стабильности А-спирали, образованной дуплексом олигонуклеотид : микроРНК, который напоминает по структуре дуплекс РНК : РНК.
Примеры олигомеров анти-микроРНК (т.е. анти-миР, которые могут представлять собой олигомер или его первый сегмент), приведены в таблице WO 2007/112754 на с. 48 стр. 15 - с. 51 стр. 9, которая включена путем ссылки.
Миметики микроРНК
В некоторых воплощениях олигомер или его первый сегмент находятся в форме миметика миРНК, который может быть введен в клетку для подавления экспрессии одной или нескольких РНК-мишеней. Миметики миРНК обычно полностью комплементарны всей последовательности миРНК. Миметики миРНК представляют собой соединения, содержащие последовательность смежных нуклеотидов, которая гомологична соответствующему сегменту одной или нескольких последовательностей миРНК, указанных или процитированных в данном документе. Миметики миРНК или анти-миР могут найти применение для (возможно) дальнейшего подавления мРНК-мишеней или для подавления (супрессии) миРНК, и следовательно, ингибирования функции эндогенных миРНК, вызывая дерепрессию и повышение экспрессии мРНК-мишени.
Аптамеры
В некоторых воплощениях олигомер или его первый сегмент может представлять собой используемый в терапевтических целях аптамер, шпигельмер (spiegelmer). Следует отметить, что аптамеры также могут быть лигандами, например, лигандами рецепторов, и таким образом, применяться в качестве компонента, обеспечивающего адресное взаимодействие (т.е. дополнительного конъюгата). Аптамеры (например, шпигельеры) в контексте данного изобретения представлены нуклеиновыми кислотами длиной от 20 до 50 нуклеотидов, выбранными в основном по их конформационной структуре, а не последовательности нуклеотидов - они проявляют свое терапевтическое действие, непосредственно связываясь с белком-мишенью in vivo и, следовательно, они не содержат обратный комплемент своей мишени, поскольку их мишень является не нуклеиновой кислотой, а белком. Конкретные аптамеры, которые могут представлять собой олигомер или его первый сегмент, включают Macugen (OSI Pharmaceuticals) или ARC1779, (Archemix, Cambridge, MA). В некоторых воплощениях олигомер или его первый сегмент не являются аптамером. В некоторых воплощениях олигомер или его первый сегмент не являются аптамером или шпигельмером.
Межнуклеотидные связи
Нуклеозиды, представляющие собой мономеры, входящие в состав олигомеров (т.е. первого и второго сегмента), описанные в данном документе, связаны друг с другом при помощи (межнуклеозидных) связующих групп. Соответственно, каждый мономер связан с соседним 3' мономером при помощи связующей группы.
Для специалиста в области техники очевидно, что в контексте данного изобретения мономер, находящийся на 5' конце олигомера не имеет связующей группы на 5' конце, хотя при этом он может содержать или не содержать 5' концевую группу.
Термины "связующая группа" или "межнуклеотидная связь" обозначают группу, способную ковалентно связывать два нуклеотида. Конкретные предпочтительные примеры включают фосфатные группы и фосфоротиоатные группы.
Нуклеотиды олигомера по изобретению или их последовательность смежных нуклеотидов связаны друг с другом при помощи связующей группы. Соответственно, каждый нуклеотид связан с соседним 3' нуклеотидом при помощи связующей группы.
Подходящие межнуклеотидные связи включают те, которые перечислены в WO 2007/031091, например, межнуклеотидные связи, приведенные в первом параграфе на с. 34 WO 2007/031091, (содержание которого включено путем ссылки).
В некоторых воплощениях, предпочтительно модифицировать межнуклеотидные связи, представляющие собой обычные фосфодиэфирные связи, за исключением фосфодиэфирных связей сегмента В, заменяя их более устойчивыми к действию нуклеаз, например, фосфоротиоатными или боранофосфатными, которые могут расщепляться РНКазой Н, что дает возможность подавлять экспрессию генов-мишеней при помощи антисмысловой технологии.
Предпочтительными межнуклеотидными связями могут быть связи, содержащие серу (S), такие как фосфоротиоатная или фосфодитиоатная, описанные в данном документе. Например, в гэпмерах, миксмерах, переключающих сплайсинг олигомерах анти-миР и тоталмерах предпочтительны фосфоротиоатные межнуклеотидные связи, особенно для первого сегмента.
В случае гэпмеров, межнуклеотидные связи в составе олигомеров могут, например, быть фосфоротиоатными или боранофосфатными, что обеспечивает расщепление РНК-мишени под действием РНКазы Н. Фосфоротиоатные связи предпочтительны по той причине, что они повышают устойчивость к нуклеазам, а также по другим причинам, например, простоте получения.
В одном аспекте, за исключением фосфодиэфирных связей между первым и вторым сегментом и, возможно, связей в составе сегмента В, все остальные межнуклеозидные связи в составе олигомера по изобретению, при помощи которых нуклеотиды и/или аналоги нуклеотида связаны друг с другом, образованы фосфоротиоатными группами. В некоторых воплощениях по меньшей мере 50%, например, по меньшей мере 70%, например, по меньшей мере 80%, например, по меньшей мере 90%, например, все межнуклеозидные связи между нуклеозидами в составе первого сегмента отличны от фосфодиэфирных (фосфатных), например, выбраны из группы, состоящей из фосфоротиоатной, фосфородитиоатной или боранофосфатной. В некоторых воплощениях по меньшей мере 50%, например, по меньшей мере 70%, например, по меньшей мере 80%, например, по меньшей мере 90%, например, все межнуклеозидные связи между нуклеозидами в составе первого сегмента являются фосфоротиоатными.
WO 09124238 относится к олигомерным соединениям, имеющим по меньшей мере один бициклический нуклеозид, присоединенный к 3' или 5' концу при помощи нейтральной межнуклеозидной связи. Таким образом, олигомеры по изобретению могут иметь по меньшей мере один бициклический нуклеозид, присоединенный к 3' или 5' концу при помощи нейтральной межнуклеозидной связи, например, такой как фосфотриэфирная, метилфосфонатная, MMI, амид-3, формацетальная или тиоформацетальная. Остальные связи могут быть фосфоротиоатными.
Конъюгаты, компоненты, обеспечивающие адресное взаимодействие, и блокирующие группы
Термин "конъюгат" обозначает гетерогенную молекулу, образованную ковалентным присоединением ("конъюгированием") олигомера, описанного в данном документе, к одному или нескольким компонентам, отличным от нуклеотида или отличным от полинуклеотида.
Конъюгаты, содержащие углеводы
В некоторых воплощениях конъюгатная группировка представляет собой углеводный компонент.
В некоторых воплощениях конъюгат представляет собой или может содержать углевод или содержит углеводную группу. В некоторых воплощениях углевод выбран из группы, состоящей из галактозы, лактозы, n-ацетилгалактозамина, маннозы и маннозо-6-фосфата. В некоторых воплощениях конъюгированная группа представляет собой или может содержать маннозу и маннозо-6-фосфат. Конъюгаты, содержащие углеводы, могут применяться для улучшения доставки или активности в различных тканях, например, печени и/или мышцах. См. Например, ЕР 1495769, WO 99/65925, Yang et al., Bioconjug Chem (2009) 20(2): 213-21. Zatsepin & Oretskaya Chem Biodivers. (2004) 1(10): 1401-17.
Кроме того, олигомер может также включать один или несколько дополнительных конъюгатных группировок, среди которых наибольший интерес представляют липофильные или гидрофобные компоненты. Например, они могут играть роль модуляторов фармакокинетики и могут быть ковалентно связаны либо с углеводным конъюгатом, с линкером, соединяющим углеводный конъюгат с олигомером, либо с линкером, соединяющим множество углеводных конъюгатов (мультивалентным), либо с олигомером, возможно через линкер, например, биорасщепляемый линкер.
Модуляторы фармакокинетики
Соединение по изобретению может также включать один или несколько дополнительных конъюгатных группировок, из которых наибольший интерес представляют липофильные или гидрофобные компоненты, например, когда конъюгированная группа представляет собой углеводный компонент. Такие липофильные или гидрофобные компоненты могут модулировать фармакокинетику и могут быть ковалентно присоединены либо к углевод-содержащему конъюгату, либо к линкеру, соединяющему углевод-содержащий конъюгат с олигомером, либо к линкеру, соединяющему конъюгат, имеющий множество углеводных компонентов (мультивалентный), либо к олигомеру, возможно через линкер, например, биорасщепляемый линкер.
Таким образом, олигомер или конъюгатная группировка может содержать модулятор фармакокинетики, такой как липофильный или гидрофобный компонент. Такие компоненты описаны в составе конъюгатов миРНК в WO 2012/082046. Гидрофобный компонент может содержать С8-С36 жирную кислоту, которая может быть насыщенной или ненасыщенной. В некоторых воплощениях могут применяться С10, С12, С14, С16, С18, С20, С22, С24, С26, С28, С30, С32 и С34 жирные кислоты. Гидрофобная группа может иметь 16 или более атомов углерода. Примеры подходящих гидрофобных групп могут быть выбраны из группы, включающей стерин, холестерин, пальмитоил, гексадек-8-еноил, олеил, (9Е, 12Е)-октадека-9,12-диеноил, диоктаноил и С16-С20 ацил. Согласно WO'346, гидрофобные группы, имеющие менее 16 атомов углерода, менее эффективны в обеспечении адресного взаимодействия полинуклеотидов, но для повышения эффективности их можно использовать в нескольких копиях (например, по 2, например, 2х С8 или С10, С12 или С14). Модуляторы фармакокинетики, которые могут найти применение в качестве компонентов, обеспечивающих адресное взаимодействие нуклеотидов, могут быть выбраны из группы, состоящей из: холестерина, алкильной группы, алкенильной группы, алкинильной группы, арильной группы, аралкильной группы, аралкенильной группы и аралкинильной группы, каждая из которых может быть линейной, разветвленной или циклической. Модуляторы фармакокинетики предпочтительно представляют собой углеводороды, содержащие только атомы углерода и водорода. Однако допускается присутствие заместителей или гетероатомов, поддерживающих гидрофобность, например, фтора.
Неожиданно было обнаружено, что конъюгаты GalNac, используемые с LNA олигомерами, не требуют модуляторов фармакокинетики, в связи с этим, в некоторых воплощениях конъюгаты GalNac не являются ковалентно присоединенными к липофильному или гидрофобному компоненту, например, описанным в данном документе, например, не содержат С8-С36 жирной кислоты или стерина. Таким образом, в изобретении также предложены GalNac конъюгаты LNA-олигомеров, которые не содержат липофильного или гидрофобного модулятора фармакокинетики или конъюгатной группировки.
Конъюгаты GalNAc
В изобретении предложены антисмысловые LNA-олигонуклеотиды, конъюгированные с группировкой, направленной на асиалогликопротеиновый рецептор. В некоторых воплощениях конъюгатная группировка (такая как третий сегмент, или сегмент С) содержит компонент, обеспечивающий адресное взаимодействие с асиалогликопротеиновым рецептором, например, галактозу, галактозамин, N-формил-галактозамин, N-ацетилгалактозамин, N-пропионил-галактозамин, N-n-бутаноил-галактозамин и N-изобутаноил-галактозамин. В некоторых воплощениях конъюгат представляет содержит кластар галактозы, например, тример N-ацетилгалактозамина. В некоторых воплощениях конъюгатная группировка содержит GalNAc (N-ацетилгалактозамин), например, моновалентный, дивалентный, тривалентный или тетравалентный GalNAc. Конъюгаты, содержащие тривалентный GalNAc, могут найти применение для направленной доставки соединения в печень. Конъюгаты GalNAc использовали с олигонуклеотидами, содержащими метилфосфонатные связи, и с антисмысловыми PNA олигонуклеотидами (см. US 5,994517 and Hangeland et al., Bioconjug Chem. 1995 Nov-Dec; 6(6):695-701) и миРНК (например, WO 2009/126933, WO 2012/089352 & WO 2012/083046). Публикации, в которых упоминается GalNAc и конкретные конъюгаты, используемые с ними, включены путем ссылки. Другие компоненты, содержащие конъюгаты GalNAc, могут включать, например, олигосахариды и кластеры углеводов, такие как Tyr-Clu-Glu-(аминогексил GalNAc)3 (YEE(ahGalNAc)3; гликотрипептид, который связывается с рецепторами Gal/GalNAc на гепатоцитах, см., например, Duff, et al., Methods Enzymol, 2000, 313, 297); кластеры галактозы на основе лизина (например, L3G4; Biessen, et al., Cardovasc. Med., 1999, 214) и кластеры галактозы на основе холана (например, углеводный мотив, распознаваемый асиалогликопротеиновым рецептором). Другие подходящие конъюгаты могут включать олигосахариды, которые способны связываться с доменами, распознающими углевод (CRD, от англ. carbohydrate recognition domains), которые обнаруживаются у асиалогликопротеинового рецептора (ASGP-R, от англ. asiologlycoprotein-receptor). Примеры конъюгированных компонентов, содержащих олигосахариды и/или углеводные комплексы, приведены в патенте США US 6,525,031, содержание которого включено во всей полноте путем ссылки.
WO 2012/083046 описывает миРНК, конъюгированные с GalNAc-содержащими компонентами, которые содержат расщепляемый модулятор фармакокинетики, подходящий для применения в данном изобретении, предпочтительными фармакокинетическими модуляторами являются С16 гидрофобные группы, такие как пальмитоил, гексадек-8-еноил, олеил, (9Е, 12Е)-октадека-9,12-диеноил, диоктаноил и С16-С20 ацил. Описанный в патенте '046 расщепляемый модулятор фармакокинетики может также представлять собой холестерин.
Обеспечивающий адресное взаимодействие компонент (конъюгатная группировка) может быть выбран из группы, состоящей из: галактозы, галактозамина, N-формил-галактозамина, N-ацетилгалактозамина, N-пропионил-галактозамина, N-n-бутаноил-галактозамина, N-изо-бутаноил-галактозамина, кластера галактозы и тримера N-ацетилгалактозамина, и может иметь модулятор фармакокинетики, выбранный из группы, состоящей из: гидрофобной группы, имеющей 16 или более атомов углерода, гидрофобной группы, имеющей 16-20 атомов углерода, пальмитоила, гексадек-8-еноила, олеила, (9Е, 12Е)-октадека-9,12-диеноила, диоктаноила и С16-С20 ацила и холестерина. Некоторые кластеры GalNac, изложенные в патенте '046, включают: (Е)-гексадек-8-еноил (С16), олеил (С18), (9,Е,12Е)-октадека-9,12-диеноил (С18), октаноил (С8), додеканоил (С12), С-20 ацил, С24 ацил, диоктаноил (2хС8). Обеспечивающий адресное взаимодействие компонент и модулятор фармакокинетики могут быть связаны с полинуклеотидом при помощи лабильной в физиологических условиях связи или, например, дисульфидной связи, или ПЭГ линкера. Изобретение также касается применения фосфодиэфирных линкеров, таких как линкеры, представляющие собой ДНК, имеющие фосфодиэфирные связи, расположенные между олигомером и конъюгированной группой (в данном документе они обозначаются сегментом В и находятся между LNA-олигомером и углеводной конъюгированной группой).
Предпочтительным лигандом для направленной доставки к гепатоцитам печени, обеспечивающим адресное взаимодействие, является кластер галактозы.
Кластер галактозы содержит молекулу, имеющую, например, содержащую от двух до четырех концевых производных галактозы. В данном документе термин производное галактозы включает как галактозу, так и производные галактозы, имеющие аффинность к асиалогликопротеиновому рецептору, равную или превышающую аффинность галактозы. Концевое производное галактозы присоединено к молекуле через С-I атом углерода. Асиалогликопротеиновый рецептор (ASGPr) обнаруживается только на гепатоцитах и связывает разветвленные гликопротеины с концевыми остатками галактозы. Предпочтительный кластер галактозы имеет три концевых остатка галактозамина или производных галактозамина, каждый из которых имеет аффинность к асиалогликопротеиновому рецептору. Более предпочтительный кластер галактозы имеет три концевых остатка N-ацетилгалактозамина. Другими терминами, распространенными в области техники, являются трехантенная галактоза, трехвалентная галактоза и тример галактозы. Известно, что кластеры трехантенных производных галактозы связываются с ASGPr с более высокой аффинностью, чем двухантенные или моноантенные структуры производных галактозы (Baenziger and Fiete, 1980, Cell, 22, 611-620; Connolly et al., 1982,1. Biol. Chern., 257,939-945). Мультивалентность необходима для достижения аффинности нМ масштаба. Согласно WO 2012/083046 присоединение единственного производного галактозы, обладающего аффинностью к асиалогликопротеиновому рецептору, не обеспечивает функцию доставки полинуклеотида RNAi к гепатоцитам in vivo при совместном введении с полимером, обеспечивающим доставку.
Кластер галактозы может содержать два или предпочтительно три производных галактозы, каждое из которых присоединено к центральной точке ветвления. Производные галактозы присоединены к центральной точке ветвления С-I углеродными атомами сахаридов. Предпочтительно, производные галактозы присоединены к центральной точке ветвления при помощи линкеров или спейсеров. Предпочтительный спейсер представляет собой гибкий гидрофильный спейсер (патент US Patent 5885968; Biessen et al. J. Med. Chern. 1995 Vol. 39 p. 1538-1546). Предпочтительный гибкий спейсер представляет собой ПЭГ спейсер. Предпочтительный ПЭГ спейсер представляет собой ПЭГЗ спейсер. Точкой ветвления может быть любая небольшая молекула, позволяющая присоединять три производных галактозы и также позволяющая присоединять олигомер. Примером группы, служащей точкой ветвления, может быть ди-лизин. Молекула ди-лизина содержит три аминогруппы, через которые могут присоединяться три производных галактозы, и реакционноспособную карбоксильную группу, через которую ди-лизин может быть присоединен к олигомеру. Точка ветвления может присоединяться к олигомеру через линкер или спейсер. Предпочтительный спейсер представляет собой гибкий гидрофильный спейсер. Предпочтительный гибкий спейсер представляет собой ПЭГ спейсер. Предпочтительный ПЭГ спейсер представляет собой ПЭГЗ спейсер (три звена этилена). Кластер галактозы может быть присоединен к 3' или 5' концу олигомера способами, известными в области техники.
Предпочтительным производным галактозы является N-ацетилгалактозамин (GalNAc). Другие сахариды, обладающие аффинностью к асиалогликопротеиновому рецептору, могут быть выбраны из группы, включающей: галактозамин, N-n-бутаноилгалактозамин и N-изо-бутаноилгалактозамин. Аффинность различных производных галактозы к асиалогликопротеиновому рецептору изучена ранее (см., например: Jobst, S.T. and Drickamer, K. JB.C. 1996, 271, 6686) или легко определяется способами, известными в области техники.

Одно воплощение кластера галактозы
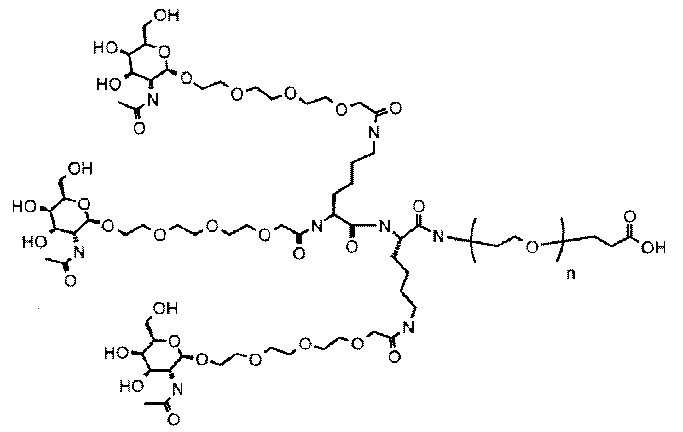
Кластер галактозы с ПЭГ-спейсером между точкой ветвления и нуклеиновой кислотой
Конъюгат GalNac приведен на Фиг. 1. Другие примеры конъюгатов по изобретению приведены ниже:




Таким образом, углеводный конъюгат (например, GalNAc) может быть связан с олигомером посредством линкера, такого как (поли)этиленгликолевый (ПЭГ) линкер, такой как ди, три, тетра, пента, гекса-этиленгликолевый линкер.
Таким образом, углеводный конъюгат (например, GalNAc) может быть связан с олигомером посредством биорасщепляемого линкера, такого как сегмент В, и возможно, сегмента Y, который на приведенных выше диаграммах обозначен как ди-лизин.
При этом наличие гидрофобного или липофильного (или иного конъюгированного) компонента (т.е. модулятора фармакокинетики) в указанном кластере GalNac является необязательным при использовании BNA или LNA-олигомеров, таких как антисмысловые олигонуклеотиды.
На фигурах изображены конкретные кластеры Galnac, использованные в данном исследовании, конъюгаты 1, 2, 3, 4 и 1а, 2а, 3а и 4а (которые показаны с необязательным линкером С6, соединяющим кластер Galnac с олигомером).
Таким образом, каждый углеводный компонент кластера (например, GalNAc) может быть присоединен к олигомеру посредством линкера, такого как (поли)этиленгликолевый (ПЭГ) линкер, такой как ди, три, тетра, пента, гекса-этиленгликолевый линкер. Как показано выше, компонент ПЭГ образует спейсер между углеводным компонентом галактозой и пептидным линкером (показан трилизин).
Углеводный конъюгат (например, Galnac) или компонент углевод-линкер (например, компонент углевод-ПЭГ) может быть ковалентно связан с олигомером (присоединен) через точку ветвления, такую как аминокислота или пептид, которые соответственно содержат две или более аминогруппы (например, 3, 4 или 5), такие как лизин, ди-лизин или три-лизин или тетра-лизин. Молекула три-лизина содержит четыре аминогруппы, через которые могут присоединяться три группы углеводных конъюгатов, таких как галактоза и ее производные (например, GalNAc) и дополнительная конъюгированная группа, такая как гидрофобная или липофильная группа/компонент, а также реакционноспособную карбоксильную группу, через которую три-лизин может быть присоединен к олигомеру. Дополнительная конъюгированная группа, например, гидрофобный или липофильный компонент может быть присоединен к остатку лизина, присоединенного к олигомеру.
В некоторых воплощениях кластер GalNac содержит пептидный линкер, например, трипептид Tyr-Asp(Asp) или дипептид Asp(Asp), который присоединен к олигомеру (или к сегменту Y или к сегменту В) через линкер-бирадикал, например, кластер GalNac может содержать следующие линкеры-бирадикалы:
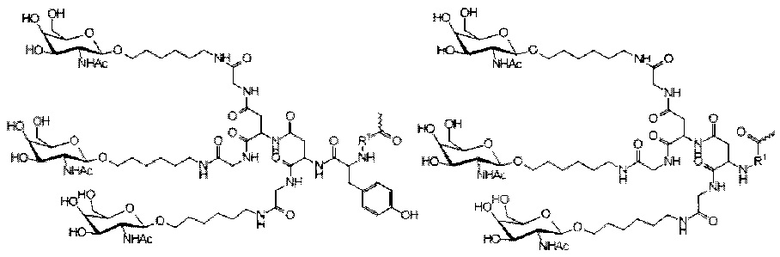
R1 представляет собой бирадикал, предпочтительно выбранный из -С2Н4-, -С3Н6-, -С4Н8-, -С5Н10-, -С6Н12-, 1,4-cyclohexyl (-С6Н10-), 1,4-phenyl (-С6Н4-), -С2Н4ОС2Н4-, -С2Н4(ОС2Н4)2- или -С2Н4(ОС2Н4)3-, С(O)СН2-, -С(O)С2Н4-, -С(O)С3Н6-, -С(O)С4Н8-, -С(О)С5Н10-, -C(O)C6H12-, 1,4-циклогексил (-С(О)С6Н10-), 1,4-фенил (-С(O)С6Н4-), -С(O)С2Н4ОС2Н4-, -С(O)С2Н4(ОС2Н4)2- или -С(O)С2Н4(ОС2Н4)3-. В некоторых воплощениях R1 представляет собой бирадикал, предпочтительно выбранный из -С2Н4-, -С3Н6-, -С4Н8-, -С5Н10-, -С6Н12-, 1,4-циклогексил (-С6Н10-), 1,4-фенил (-С6Н4-), -С2Н4ОС2Н4-, -С2Н4(ОС2Н4)2- или -С2Н4(ОС2Н4)3-.
Аминоалкильные промежуточные соединения
В изобретении также предложены промежуточные соединения LNA олигомеров, содержащие антисмысловой LNA олигомер, содержащий (например, 5' или 3' концевую) аминоалкильную группу, например, С2-С36 аминоалкильную группу, включая, например, С6 и С12 аминоалкильные группы. Аминоалкильная группа может быть добавлена к LNA олигомеру в ходе стандартного синтеза олигонуклеотидов, например, при использовании (например, защищенного) аминоалкил фосфорамидита. Связующая группа между аминоалкилом и LNA олигомером может быть, например, фосфоротиоатной или фосфодиэфирной, или одной из связующих нуклеозиды групп, которые указаны в данном документе. Аминоалкильная группа может быть ковалентно присоединена, например, к 5' или 3' концу LNA олигомера, например, при помощи нуклеозидной связующей группы, например, при помощи фосфоротиоатной или фосфодиэфирной связи.
В изобретении также предложен способ синтеза LNA олигомера, включающий последовательный синтез LNA олигомера, например, твердофазный синтез олигонуклеотидов, включающий этап добавления аминоалкильной группы к олигомеру, например, в ходе первой или последней стадии синтеза олигонуклеотидов. Способ синтеза может также включать стадию реакции углеводного конъюгата с аминоалкил-LNA олигомером (этап конъюгирования). Углеводный конъюгат может содержать подходящие линкеры и/или точки ветвления, и возможно, дополнительные конъюгированные группы, например, гидрофобные или липофильные группы, описанные в данном документе. Стадия конъюгирования может выполняться во время, когда олигомер связан с твердым носителем (например, после синтеза олигонуклеотида, но до элюирования олигомера с твердого носителя) или после (т.е. после элюирования). В изобретении предложено применение аминоалкильного линкера для синтеза олигомера по изобретению.
В изобретении предложен способ синтеза (или получения) олигомерного соединения, например, олигомерного соединения по изобретению, указанный способ включает стадию (последовательного) олигонуклеотидного синтеза первого сегмента (А) и (возможно, при наличии) второго сегмента (В), при этом за стадией синтеза следует стадия добавления третьего сегмента (содержащего фосфорамидит), содержащего углеводную конъюгированную группу, описанную в данном документе (X или X-Y вместе с линкером), например, такую как конъюгат GalNAc, такую как тривалентный GalNAc (например, конъюгат, выбранный из группы, состоящей из Конъюгата 1, Конъюгата 2, Конъюгата 3, Конъюгата 4, Конъюгата 1а, Конъюгата 2а, Конъюгата 3а и Конъюгата 4а, или другого тривалентного конъюгата GalNAc, описанного в данном документе), с последующим отщеплением олигомерного соединения от (твердофазного) носителя.
При этом считается, что конъюгированный сегмент (например, X или X-Y) может быть добавлен после отщепления от твердого носителя. В альтернативном случае, способ синтеза может включать стадию синтеза первого (А) и возможно, второго сегмента (В), с последующим отщеплением олигомера от носителя, за чем следует стадия добавления к олигомеру третьего сегмента, такого как группа X или X-Y. Добавление третьего сегмента можно произвести, например, путем добавления звена амино фосфорамидита на последней стадии синтеза олигомера (на носителе), который после отщепления от носителя можно использовать для присоединения к группе X или X-Y, возможно через активную группу на группе X или Y (если таковая существует). В воплощениях, в которых расщепляемый линкер не является нуклеотидным сегментом, сегмент В может представлять собой ненуклеотидный расщепляемый линкер, например, пептидный линкер, который может составлять часть сегмента X (также обозначаемого сегментом С) или сегмента Y (или его части).
В некоторых воплощениях способа сегмент X (например, С) или (X-Y), например, конъюгат (например, конъюгат GalNAc) содержит активную группу (активированную функциональную группу), а в способе синтеза активированный конъюгат (или сегмент X или X-Y) добавляют к первому и второму сегментам, например, к олигомеру с присоединенной аминогруппой. Аминогруппа может быть добавлена к олигомеру при помощи стандартного фосфорамидитного метода, например, на последней стадии синтеза олигомера (что обычно приводит к получению олигомера с аминогруппой на 5' конце). Например, на последней стадии синтеза олигонуклеотидов используют защищенный амино-алкил фосфорамидит, например, TFA-аминоС6 фосфорамидит (6-(трифторацетиламино)-гексил-(2-цианоэтил)-(N,N-диизопропил)-фосфорамидит). Аминогруппу можно добавить к олигомеру, например, на первой стадии синтеза олигомера (что обычно приводит к получению олигомера с аминогруппой на 3' конце). Например, при использовании твердого носителя с N-(6-(O-(4,4''-диметокситритил))-гексил)-(2-карбоксамид)-фталимидилом.
Сегмент X (также обозначаемый в данном документе сегментом С), например, конъюгат (например, конъюгат GalNac) можно активировать через образование NHS эфира, а затем добавить олигомер с присоединенной аминогруппой. Например, в качестве активной группы для сегмента X (или участка С, например, конъюгата, такого как конъюгатная группировка GalNac) можно использовать N-гидроксисукцинимид (NHS).
Липофильные конъюгаты
Олигомер может также содержать другой конъюгат, например, липофильный конъюгат (например, модулятор фармакокинетики). Репрезентативные конъюгированные компоненты могут включать липофильные молекулы (ароматические и неароматические), включая молекулы стероидов; белки (например, антитела, ферменты, белки сыворотки); пептиды; витамины (водорастворимые или жирорастворимые); полимеры (водорастворимые или жирорастворимые); низкомолекулярные соединения, включая лекарства, токсины, репортерные молекулы и лиганды рецепторов; углеводные комплексы; комплексы, расщепляющие нуклеиновые кислоты; хелаторы металлов (например, порфирины, тексафирины, краун-эфиры и т.д.); интеркаляторы, включая гибриды фотонуклеазы и интеркалятора; образующие сшивки агенты (например, фотоактивные, редокс-активные) и их комбинации и производные. Различные подходящие конъюгированные компоненты, их получение и связывание с олигомерными соединениями описано, например, в WO 93/07883 и патенте US 6,395,492, содержание которых включено во всей полноте путем ссылки. Конъюгаты олигонуклеотидов и их синтез также описан в подробных обзорах Manoharan in Antisense Drug Technology, Principles, Strategies, and Applications, ST. Crooke, ed., Ch. 16, Marcel Dekker, Inc., 2001 и Manoharan, Antisense and Nucleic Acid Drug Development, 2002, 12, 103, содержание которых включено во всей полноте путем ссылки. Липофильные конъюгированные компоненты можно применять, например, чтобы скомпенсировать гидрофильность олигомерного соединения и улучшить проникновение в клетки. Липофильные компоненты включают, например, стероиды и родственные им соединения, такие как холестерин (патент US 4,958,013 and Letsinger et al., Proc. Natl. Acad. Sci. USA, 1989, 86, 6553), ланостерин, копростанол, стигмастерол, эргостерол, кальциферол, холевую кислоту, дезоксихолевую кислоту, эстрон, эстрадиол, эстратриол, прогестерон, стильбэстрол, тестостерон, андростерон, дезоксикортикостерон, кортизон, 17-гидроксикортикостерон, их производные и т.п.
Другие липофильные конъюгированные компоненты включают алифатические группы, например, линейные, разветвленные и циклические алкилы, алкенилы и алкинилы. Алифатические группы могут иметь, например, приблизительно от 5 до 50, приблизительно от 6 до 50, приблизительно от 8 до 50 или приблизительно от 10 до 50 атомов углерода. Примеры алифатических групп включают ундецил, додецил, гексадецил, гептадецил, октадецил, нонадецил, терпены, борнил, адамантил, их производные и т.п. В некоторых воплощениях один или более атомов углерода в алифатической группе могут быть замещены гетероатомом, таким как О, S или N (например, геранилоксигексил). Другие подходящие липофильные конъюгированные компоненты включают алифатические производные глицерола, такие как алкилглицерол, бис(алкил)глицерол, трис(алкил)глицерол, моноглицериды, диглицериды и триглицериды. В некоторых воплощениях липофильный конъюгат представляет собой ди-гексилдецил-рац-глицерол или 1,2-ди-О-гексилдецил-рац-глицерол (Manoharan et al., Tetrahedron Lett., 1995, 36, 3651; Shea, et al., Nuc. Acids Res., 1990, 18, 3777) или его фосфонаты. В качестве липофильных конъюгированных компонентов могут также выступать насыщенные и ненасыщенные алифатические функциональные группы, например, такие как жирные кислоты, жирные спирты, жирные эфиры и жирные амины. В некоторых воплощениях алифатические функциональные группы могут содержать приблизительно от 6 до 30 атомов углерода или приблизительно от 8 до 22 атомов углерода. Примеры жирных кислот включают каприновую, каприловую, пальмитиновую, миристиновую, стеариновую, олеиновую, линолевую, линоленовую, арахидоновую, эйкозановую кислоты и т.п.
В других воплощениях липофильные конъюгированные группы могут представлять собой полициклические ароматические группы, имеющие приблизительно от 6 до 50, приблизительно от 10 до 50 или приблизительно от 14 до 40 атомов углерода. Примеры полициклических ароматических групп включают пирены, пурины, акридины, ксантены, флуорены, фенантрены, антрацены, хинолины, изохинолины, нафталены, их производные и т.п. Другие подходящие липофильные конъюгированные компоненты включают ментолы, тритилы (например, диметокситритил (ДМТ)), феноксазины, липоевую кислоту, фосфолипиды, эфиры, тиоэфиры (например, гексил-S-тритилтиол), их производные и т.п. Получение липофильных конъюгатов олигомерных соединений подробно описано в области техники, например, Saison-Behmoaras et al, EMBO J., 1991, 10, 1111; Kabanov et al., FEBSLett., 1990, 259, 327; Svinarchuk et al, Biochimie, 1993, 75, 49; (Mishra et al., Biochim. Biophys. Acta, 1995, 1264, 229, and Manoharan et al., Tetrahedron Lett., 1995, 36, 3651.
Олигомерные соединения, содержащие конъюгированные компоненты с аффинностью к липопротеинам низкой плотности (ЛПНП), могут способствовать получению эффективной системы адресной доставки. Высокий уровень экспрессии рецепторов к ЛПНП на опухолевых клетках делает ЛПНП удобным носителем для селективной доставки лекарств в эти клетки (Rump, et al., Bioconjugate Chem., 1998, 9, 341; Firestone, Bioconjugate Chem., 1994, 5, 105; Mishra, et al., Biochim. Biophys. Acta, 1995, 1264, 229). Компоненты, обладающие аффинностью к ЛПНП, включают многие липофильные группы, такие как стероиды (например, холестерин), жирные кислоты, их производные и комбинации. В некоторых воплощениях конъюгированные компоненты, обладающие аффинностью к ЛПНП, могут представлять собой диолеиловые эфиры холевых кислот, например, хенодезоксихолевой и литохолевой кислот.
В некоторых воплощениях конъюгированная группа представляет собой или может содержать липофильный компонент, например, стерол (например, холестерин, холестерил, холестанол, стигмастерол, холановую кислоту и эргостерол). В некоторых воплощениях конъюгат представляет собой или может содержать холестерин. См., например, Soutschek et al., Nature (2004) 432, 173; Krutzfeldt Nature 2005, NAR 2007.
В некоторых воплощениях конъюгат представляет собой или может содержать липид, фосфолипид или липофильный спирт, например, катионные липиды, нейтральные липиды, сфинголипиды и жирные кислоты, такие как стеариновая, олеиновая, элаидиновая кислота, линолевая кислота, транс-транс-линолевая, линоленовая и миристиновая кислоты. В некоторых воплощениях жирная кислота содержит С4-С30 насыщенную или ненасыщенную алкильную цепь. Алкильная цепь может быть линейной или разветвленной.
В некоторых воплощениях липофильные конъюгаты могут представлять собой или содержать биотин. В некоторых воплощениях липофильные конъюгаты могут представлять собой или содержать глицерид или сложный эфир глицерида.
Липофильные конъюгаты, такие как холестерин или перечисленные в данном документе, можно применять для улучшения доставки олигонуклеотидов, например, в печень (обычно, к гепатоцитам).
Следующие ссылки относятся к применению липофильных конъюгатов: Kobylanska et al., Acta Biochim Pol. (1999); 46(3): 679-91. Felber et al,. Biomaterials (2012) 33(25): 599-65); Grijalvo et al., J Org Chem (2010) 75(20): 6806-13. Koufaki et al., Curr Med Chem (2009) 16(35): 4728-42. Godeau et al J. Med. Chem. (2008) 51(15): 4374-6.
В некоторых воплощениях конъюгатная группировка является гидрофильной. В некоторых воплощениях конъюгированная группа не содержит липофильной замещающей группы, например, замещающей группы, представленной жирной кислотой, например, С8-С26, например, замещающей группы, представленной пальмитоиловой кислотой, или не содержит стерола, например, замещающей группы, представленной холестерином. Таким образом, часть изобретения основана на неожиданном наблюдении, что LNA-олигомеры, содержащие конъюгаты GalNAC, обладают исключительными фармакокинетическими свойствами даже без использования модуляторов фармакокинетики, таких как замещающие группы, представленные жирными кислотами (например, жирными кислотами >С8 или >С16).
Линкеры
Линкер представляет собой связующее звено между двумя атомами, соединяющее одну химическую группу или сегмент, представляющий интерес, с другой химической группой или сегментом, представляющим интерес, при помощи одной или нескольких ковалентных связей. Конъюгированные компоненты (или обеспечивающие адресную доставку или блокирующие компоненты) могут быть присоединены к олигомерному соединению напрямую или через линкерный компонент (линкер или связующее звено) - линкер. Линкеры представляют собой бифункциональные компоненты, служащие для ковалентного присоединения третьего сегмента, например, конъюгированного компонента, к олигомерному компоненту (такому как сегмент В). В некоторых воплощениях линкер содержит цепочку или олигомер, состоящие из повторяющихся звеньев, например, таких как звенья этиленгликоля или звенья аминокислот. Линкер может иметь по меньшей мере две функциональные группы, одна из которых служит для присоединения олигомерного соединения, а другая для присоединения конъюгированного компонента. Примерами функциональных групп линкеров могут быть электрофильные, вступающие в реакцию с нуклеофильными группами олигомера или конъюгированного компонента, или нуклеофильные, вступающие в реакцию с электрофильными группами. В некоторых воплощениях функциональные группы линкеров включают аминогруппу, гидроксил, карбоновую кислоту, тиол, фосфорамидат, фосфат, фосфит, ненасыщенные связи (двойные или тройные связи) и т.п. Некоторые примеры линкеров включают 8-амино-3,6-диоксаоктановую кислоту (ADO), сукцинимидил 4-(N-малеимидометил)циклогексан-I-карбоксилат (SMCC), 6-аминогексановую кислоту (АНЕХ или AHA), 6-аминогексилокси, 4-аминобутировую кислоту, 4-аминоциклогексилкарбоновую кислоту, сукцинимидил 4-(N-малеимидометил)циклогексан-1-карбокси-(6-амидо-капроат) (LCSMCC), сукцинимидил m-малеимидо-бензилат (MBS), сукцинимидил N-e-малеимидо-каприлат (EMCS), сукцинимидил 6-(бета-малеимидо-пропионамидо)гексанат (SMPH), сукцинимидил N-(а-малеимидо ацетат) (AMAS), сукцинимидил 4-(р-малеимидофенил)бутират (SMPB), бета-аланин (бета-ALA), фенилглицин (PHG), 4-аминоциклогексановую кислоту (АСНС), бета-(циклопропил) аланин (бета-CYPR), аминододекановую кислоту (ADC), алкилен диолы, полиэтиленгликоли, аминокислоты и т.п.
В области техники известно множество других линкерных групп, которые можно применять для присоединения конъюгированных компонентов к олигомерным соединениям. Обзор многих подходящих линкерных групп приведен, например, в публикации Antisense Research and Applications, S.Т. Crooke and B. Lebleu, Eds., CRC Press, Boca Raton, Fla., 1993, p. 303-350. Дисульфидную связь использовали для присоединения 3' конца олигонуклеотида к пептиду (Corey, et al., Science 1987, 238, 1401; Zuckermann, et al, J Am. Chem. Soc. 1988, 110, 1614; and Corey, et al., J Am. Chem. Soc. 1989, 111, 8524). Nelson, et al., Nuc. Acids Res. 1989, 17, 7187 описывает сшивающий реагент для присоединения биотина к 3'-концу олигонуклеотида. Данный реагент, N-Fmoc-O-DMT-3-амино-1,2-пропандиол выпускается фирмой Clontech Laboratories (Palo Alto, Calif.) под названием 3'-амин. Он также выпускается фирмой Glen Research Corporation (Sterling, Va.) под названием 3'-амино-модифицирующий реагент. Данный реагент также использовали для связывания пептида с олигонуклеотидом, согласно описанию Judy, et al., Tetrahedron Letters 1991, 32, 879. 5'-Amino-Modifier C6 представляет собой аналогичный имеющийся в продаже реагент для соединения с 5'-концом олигонуклеотида. Данные реагенты выпускаются фирмой Glen Research Corporation (Sterling, Va.). Krieg, et al, Antisense Research and Development 1991, 1, 161 использовали данные соединения или их аналоги для присоединения флуоресцеина к 5'-концу олигонуклеотида. Другие соединения, такие как акридин, присоединяли к 3'-концевой фосфатной группе олигонуклеотида посредством полиметиленовой связи (Asseline, et al., Proc. Natl. Acad. Sci. USA 1984, 81, 3297). Любую из перечисленных выше групп можно использовать в качестве единственного линкера или в комбинации с одним или несколькими дополнительными линкерами.
Линкеры и их применение для получения конъюгатов олигомерных соединений описано в области техники, например, в WO 96/11205 и WO 98/52614 и патентах US 4,948,882; 5,525,465; 5,541,313; 5,545,730; 5,552,538; 5,580,731; 5,486,603; 5,608,046; 4,587,044; 4,667,025; 5,254,469; 5,245,022; 5,112,963; 5,391,723; 5,510475; 5,512,667; 5,574,142; 5,684,142; 5,770,716; 6,096,875; 6,335,432 и 6,335,437, WO 2012/083046 каждый из которых включен во всей полноте путем ссылки.
В данном документе лабильная в физиологических условиях связь (также обозначаемая расщепляемым линкером) представляет собой лабильную связь, которая расщепляется в условиях, обычно встречающихся или аналогичных тем, которые встречаются в организме млекопитающего. Лабильные в физиологических условиях линкерные группы выбирают таким образом, чтобы при нахождении в определенных физиологических условиях они подвергались химической трансформации (например, отщеплению). Условия внутри клеток млекопитающих включают такие химические параметры, как pH, температура, окислительные или восстановительные условия или агенты, концентрация соли, которые встречаются или аналогичны тем, которые встречаются в клетках млекопитающих. Условия внутри клеток млекопитающих включают также наличие ферментативной активности, обычно существующей в клетках млекопитающих, например, присущей протеолитическим или гидролитическим ферментам. В некоторых воплощениях расщепляемый линкер чувствителен к нуклеазам, которые, например, могут экспрессироваться в клетке-мишени, и соответственно, согласно данному описанию, линкер может представлять собой короткую последовательность нуклеозидов (например, 1-10), связанных фосфодиэфирными связями, например, ДНК-нуклеозидов.
Химическая трансформация (расщепление лабильной связи) может начаться при добавлении к клетке фармацевтически приемлемого агента или может произойти спонтанно при попадании молекулы, содержащей лабильную связь, в соответствующее внутри- и/или внеклеточное окружение. Например, pH-лабильная связь может расщепляться при попадании молекулы в кислую среду эндосом. Таким образом, pH-лабильную связь можно считать связью, расщепляемой в эндосомах. Расщепляемые ферментами связи могут расщепляться под воздействием ферментов, например, таких, которые присутствуют в эндосомах или лизосомах или в цитоплазме. Дисульфидная связь может расщепляться, когда молекула попадает в более восстанавливающие условия в цитоплазме клеток. Таким образом, дисульфидную связь можно считать связью, расщепляемой в цитоплазме. В данном документе pH-лабильная связь представляет собой лабильную связь, которая подвергается избирательному расщеплению в кислых условиях (pH<7). Такие связи могут также обозначаться лабильными в эндосомах, поскольку pH клеточных эндосом и лизосом ниже 7.
Линкеры (например, сегмент Y)
Линкер представляет собой связующее звено между двумя атомами, соединяющее одну химическую группу или сегмент, представлящий интерес, с другой химической группой или сегментом, представляющим интерес, при помощи одной или нескольких ковалентных связей. Конъюгированные компоненты (или обеспечивающие адресную доставку или блокирующие компоненты) могут быть присоединены к олигомерному соединению напрямую или через линкерный компонент (линкер или связующее звено) - линкер. Линкеры представляют собой бифункциональные компоненты, служащие для ковалентного присоединения третьего сегмента, например, конъюгированного компонента, к олигомерному компоненту (такому как сегмент В). В некоторых воплощениях линкер содержит цепочку или олигомер, состоящие из повторяющихся звеньев, например, таких как звенья этиленгликоля или звенья аминокислот. Линкер может иметь по меньшей мере две функциональные группы, одна из которых служит для присоединения олигомерного соединения, а другая для присоединения конъюгированного компонента. Примерами функциональных групп линкеров могут быть электрофильные, вступающие в реакцию с нуклеофильными группами олигомера или конъюгированного компонента, или нуклеофильные, вступающие в реакцию с электрофильными группами. В некоторых воплощениях функциональные группы линкеров включают аминогруппу, гидроксил, карбоновую кислоту, тиол, фосфорамидат, фосфат, фосфит, ненасыщенные связи (двойные или тройные связи) и т.п. Некоторые примеры линкеров включают 8-амино-3,6-диоксаоктановую кислоту (ADO), сукцинимидил 4-(N-малеимидометил)циклогексан-I-карбоксилат (SMCC), 6-аминогексановую кислоту (АНЕХ или AHA), 6-аминогексилокси, 4-аминобутировую кислоту, 4-аминоциклогексилкарбоновую кислоту, сукцинимидил 4-(N-малеимидометил)циклогексан-I-карбокси-(6-амидо-капроат) (LCSMCC), сукцинимидил m-малеимидо-бензилат (MBS), сукцинимидил N-e-малеимидо-каприлат (EMCS), сукцинимидил 6-(бета-малеимидо-пропионамидо)гексанат (SMPH), сукцинимидил N-(а-малеимидо ацетат) (AMAS), сукцинимидил 4-(р-малеимидофенил)бутират (SMPB), бета-аланин (бета-ALA), фенилглицин (PHG), 4-аминоциклогексановую кислоту (АСНС), бета-(циклопропил) аланин (бета-CYPR), аминододекановую кислоту (ADC), алкилен диолы, полиэтиленгликоли, аминокислоты и т.п.
В области техники известно множество других линкерных групп, которые можно применять для присоединения конъюгированных компонентов к олигомерным соединениям. Обзор многих подходящих линкерных групп приведен, например, в публикации Antisense Research and Applications, S.Т. Crooke and B. Lebleu, Eds., CRC Press, Boca Raton, Fla., 1993, p. 303-350. Дисульфидную связь использовали для присоединения 3' конца олигонуклеотида к пептиду (Corey, et al., Science 1987, 238, 1401; Zuckermann, et al, J Am. Chem. Soc. 1988, 110, 1614; and Corey, et al., J Am. Chem. Soc. 1989, 111, 8524). Nelson, et al., Nuc. Acids Res. 1989, 17, 7187 описывает сшивающий реагент для присоединения биотина к 3'-концу олигонуклеотида. Данный реагент, N-Fmoc-O-DMT-3-амино-1,2-пропандиол выпускается фирмой Clontech Laboratories (Palo Alto, Calif.) под названием 3'-амин. Он также выпускается фирмой Glen Research Corporation (Sterling, Va.) под названием 3'-амино-модифицирующий реагент. Данный реагент также использовали для связывания пептида с олигонуклеотидом, согласно описанию Judy, et al., Tetrahedron Letters 1991, 32, 879. 5'-Amino-Modifier C6 представляет собой аналогичный имеющийся в продаже реагент для соединения с 5'-концом олигонуклеотида. Данные реагенты выпускаются фирмой Glen Research Corporation (Sterling, Va.). Krieg, et al, Antisense Research and Development 1991, 1, 161 использовали данные соединения или их аналоги для присоединения флуоресцеина к 5'-концу олигонуклеотида. Другие соединения, такие как акридин, присоединяли к 3'-концевой фосфатной группе олигонуклеотида посредством полиметиленовой связи (Asseline, et al., Proc. Natl. Acad. Sci. USA 1984, 81, 3297). Любую из перечисленных выше групп можно использовать в качестве единственного линкера или в комбинации с одним или несколькими дополнительными линкерами.
Линкеры и их применение для получения конъюгатов олигомерных соединений описано в области техники, например, в WO 96/11205 и WO 98/52614 и патентах US 4,948,882; 5,525,465; 5,541,313; 5,545,730; 5,552,538; 5,580,731; 5,486,603; 5,608,046; 4,587,044; 4,667,025; 5,254,469; 5,245,022; 5,112,963; 5,391,723; 5,510475; 5,512,667; 5,574,142; 5,684,142; 5,770,716; 6,096,875; 6,335,432 и 6,335,437, Wo 2012/083046 каждый из которых включен во всей полноте путем ссылки.
В данном документе лабильная в физиологических условиях связь (также обозначаемая расщепляемым линкером) представляет собой лабильную связь, которая расщепляется в условиях, обычно встречающихся или аналогичных тем, которые встречаются в организме млекопитающего. Лабильные в физиологических условиях линкерные группы выбирают таким образом, чтобы при нахождении в определенных физиологических условиях они подвергались химической трансформации (например, отщеплению). Условия внутри клеток млекопитающих включают такие химические параметры, как pH, температура, окислительные или восстановительные условия или агенты, концентрация соли, которые встречаются или аналогичны тем, которые встречаются в клетках млекопитающих. Условия внутри клеток млекопитающих включают также наличие ферментативной активности, обычно существующей в клетках млекопитающих, например, присущей протеолитическим или гидролитическим ферментам. В некоторых воплощениях расщепляемый линкер чувствителен к нуклеазам, которые, например, могут экспрессироваться в клетке-мишени, и соответственно, согласно данному описанию, линкер может представлять собой короткую последовательность нуклеозидов (например, 1-10), связанных фосфодиэфирными связями, например, ДНК-нуклеозидов.
Химическая трансформация (расщепление лабильной связи) может начаться при добавлении к клетке фармацевтически приемлемого агента или может произойти спонтанно при попадании молекулы, содержащей лабильную связь, в соответствующее внутри- и/или внеклеточное окружение. Например, pH-лабильная связь может расщепляться при попадании молекулы в кислую среду эндосом. Таким образом, pH-лабильную связь можно считать связью, расщепляемой в эндосомах. Расщепляемые ферментами связи могут расщепляться под воздействием ферментов, например, таких, которые присутствуют в эндосомах или лизосомах или в цитоплазме. Дисульфидная связь может расщепляться, когда молекула попадает в более восстанавливающие условия в цитоплазме клеток. Таким образом, дисульфидную связь можно считать связью, расщепляемой в цитоплазме. В данном документе pH-лабильная связь представляет собой лабильную связь, которая подвергается избирательному расщеплению в кислых условиях (pH<7). Такие связи могут также обозначаться лабильными в эндосомах, поскольку клеточные эндосомы и лизосомы имеют pH ниже 7.
Биорасщепляемые конъюгаты, связанные с олигомерами
Олигомерное соединение может содержать второй сегмент (сегмент В), который располагается между олигомером (обозначаемым как сегмент А) и конъюгатом (обозначаемым как сегмент С). Сегмент В может представлять собой линкер, например, расщепляемый линкер (также обозначаемый лабильным в физиологических условиях линкером).
Для определения, является ли линкер биорасщепляемым или лабильным в физиологических условиях, определяют его чувствительность к расщеплению способами, проиллюстрированными в Примере 9.
Биорасщепляемые линкеры по данному изобретению относятся к линкерам, которые чувствительны к расщеплению в ткани-мишени (т.е. лабильны в физиологических условиях), например, в печени и/или почках. Предпочтительно, чтобы скорость расщепления в ткани-мишени превышала таковую в сыворотке крови. Соответствующие способы определения степени расщепления (%) в ткани (например, в печени или почках) и в сыворотке приведены в Примере 9. В некоторых воплощениях биорасщепляемый линкер, входящий в соединение по изобретению (также обозначаемый лабильным в физиологических условиях линкером или чувствительным к нуклеазам линкером), например, сегмент В, расщепляется в гомогенате печени или почек по меньшей мере на 20%, например, по меньшей мере приблизительно на 30%, например, по меньшей мере приблизительно на 40%, например, по меньшей мере приблизительно на 50%, например, по меньшей мере приблизительно на 60%, например, по меньшей мере приблизительно на 70%, например, по меньшей мере приблизительно на 75%, при исследовании, описанном в Примере 9. В некоторых воплощениях расщепление (%) в сыворотке, определяемое согласно Примеру 9, составляет менее чем приблизительно 30%, менее чем приблизительно 20%, например, менее чем приблизительно 10%, например, менее чем приблизительно 5%, например, менее чем приблизительно 1%.
В некоторых воплощениях, которые могут быть одинаковыми или различными, биорасщепляемый линкер, входящий в соединение по изобретению (также обозначаемый лабильным в физиологических условиях линкером или чувствительным к нуклеазам линкером), например, сегмент В, подвержен расщеплению нуклеазой S1. Чувствительность к расщеплению нуклеазой S1 можно оценивать, как показано в Примере 9 в исследовании с использованием нуклеазы S1. В некоторых воплощениях биорасщепляемый линкер (также обозначаемый лабильным в физиологических условиях линкером или чувствительным к нуклеазам линкером), например, сегмент В соединения по изобретению расщепляется по меньшей мере на 30%, например, по меньшей мере приблизительно на 40%, например, по меньшей мере приблизительно на 50%, например, по меньшей мере приблизительно на 60%, например, по меньшей мере приблизительно на 70%, например, по меньшей мере приблизительно на 80%, например, по меньшей мере приблизительно на 90%, например, по меньшей мере приблизительно на 95% при инкубации в течение 120 мин в с нуклеазой S1 в исследовании, описанном в Примере 9.
Чувствительные к нуклеазам связи, лабильные в физиологических условиях
Олигомерное соединение может содержать второй сегмент (сегмент В), который располагается между LNA-олигомером (обозначаемым как сегмент А) и углеводным конъюгатом (обозначаемым как сегмент С). Сегмент В может представлять собой линкер, например, расщепляемый линкер (также обозначаемый лабильным в физиологических условиях линкером).
В некоторых воплощениях сегмент В содержит от 1 до 10 нуклеотидов, которые ковалентно связаны с 5' или 3' нуклеотидом первого сегмента, например, при помощи межнуклеозидной связующей группы, такой как фосфодиэфирная связь, где:
a. межнуклеозидная связь между первым и вторым сегментом представляет собой фосфодиэфирную связь, а нуклеозид второго сегмента (например, непосредственно) примыкающий к первому сегменту, представляет собой ДНК- или РНК-нуклеозид; и/или
b. по меньшей мере 1 нуклеозид второго сегмента представляет собой ДНК- или РНК-нуклеозид, присоединенный посредством фосфодиэфирной связи.
В некоторых воплощениях сегмент А и сегмент В образуют единую непрерывную нуклеотидную последовательность длиной 8-35 нуклеотидов. В некоторых аспектах межнуклеотидная связь между первым и вторым сегментом может считаться частью второго сегмента.
В некоторых воплощениях между вторым и третьим сегментом находится фосфор-содержащая связующая группа. Фосфор-содержащая связующая группа может быть, например, фосфатной (фосфодиэфирной), фосфоротиоатной, фосфородитиоатной или боранофосфатной группой. В некоторых воплощениях фосфор-содержащая связующая группа находится между вторым сегментом и линкерным сегментом, который присоединен к третьему сегменту. В некоторых воплощениях, фосфатная группа представляет собой фосфодиэфир.
Таким образом, в некоторых аспектах олигомерное соединение содержит по меньшей мере две фосфодиэфирных группы, где по меньшей мере одна является такой, как указано выше, а другая находится между вторым и третьим сегментами, возможно между линкерной группой и вторым сегментом.
В некоторых воплощениях третий сегмент представляет собой активную группу, например, активную группу, применяемую для конъюгирования. В данном аспекте изобретения также предложены активированные олигомеры, содержащие сегмент А и В и активную группу, например, промежуточное соединение, подходящее для последующего присоединения третьего сегмента, например, подходящее для конъюгирования.
В некоторых воплощениях третий сегмент представляет собой реакционноспособную группу, например, реакционноспособную группу, применяемую для конъюгирования. В данном аспекте изобретения также предложены олигомеры, содержащие сегмент А и В и реакционноспособную группу, например, промежуточные соединения, подходящие для последующего присоединения третьего сегмента, например, подходящие для конъюгирования. Реакционноспособная группа в некоторых воплощениях может содержать амин спиртовой группы, например, аминогруппу.
В некоторых воплощениях сегмент А содержит по меньшей мере одну, например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 межнуклеозидные связи, отличные от фосфодиэфирной, например, межнуклеозидные связи, которые (возможно независимо) выбраны из группы, состоящей из фосфоротиоатной, фосфородитиоатной и боранофосфатной, а также метил фосфонатной, например, фосфоротиоатной. В некоторых воплощениях сегмент А содержит по меньшей мере одну фосфоротиоатную связь. В некоторых воплощениях по меньшей мере 50%, например, по меньшей мере 75%, например, по меньшей мере 90%, например, все межнуклеозидные связи в составе сегмента А отличны от фосфодиэфирных, например, являются фосфоротиоатными связями. В некоторых воплощениях все межнуклеозидные связи сегмента А отличны от фосфодиэфирной.
В некоторых воплощениях олигомерное соединение содержит антисмысловой олигонуклеотид, например, конъюгат антисмыслового олигонуклеотида. Антисмысловой олигонуклеотид может представлять собой или может содержать первый сегмент и, возможно, второй сегмент. Соответственно, в некоторых воплощениях сегмент В может быть частью последовательности смежных нуклеиновых оснований, комплементарной (нуклеиновой кислоте) мишени. В другом воплощении сегмент В может не быть комплементарен мишени.
В альтернативном случае, в некоторых воплощениях изобретения предложен олигонуклеотид (например, антисмысловой олигонуклеотид), связанный нефосфодиэфирными связями, например, фосфоротиоатными связями, имеющий по меньшей мере один концевой (5' и/или 3') ДНК или РНК нуклеозид, связанный с соседним нуклеозидом олигонуклеотида посредством фосфодиэфирной связи, где концевой ДНК или РНК нуклеозид далее ковалентно присоединен к конъюгированному компоненту, компоненту, обеспечивающему адресное взаимодействие, или блокирующему компоненту, возможно, посредством линкерного компонента.
Первый сегмент ковалентно связан со вторым сегментом, например, при помощи 5' концевой или 3' концевой межнуклеозидной связи, такой как фосфодиэфирная связь. Таким образом, фосфодиэфирная связь может располагаться между нуклеозидом, находящимся в крайнем 5' положении сегмента А, и нуклеозидом, находящимся в крайнем 3' положении сегмента В, и/или между нуклеозидом, находящимся в крайнем 3' положении сегмента А и нуклеозидом, находящимся в крайнем 5' положении сегмента В. Соответственно, в некоторых воплощениях может существовать два сегмента В, ковалентно связанных с сегментом А, один из которых находится на 5' конце сегмента А, а другой - на 3' конце сегмента А. Два сегмента В могут быть одинаковыми или различными, могут быть ковалентно присоединены к одному и тому же или к различным третьим сегментам, возможно, независимо, опосредовано через линкер (Y).
Олигомеры могут быть длиной 8-35 нуклеотидов и содержать первый сегмент, например, из 7-25 смежных нуклеотидов и второй сегмент из 1-10 смежных нуклеотидов, где, например, межнуклеозидная связь между первым и вторым сегментом является фосфодиэфирной, связанной с первым (или единственным) ДНК или РНК-нуклеозидом второго сегмента, или сегмент В содержит по меньшей мере один ДНК или РНК нуклеозид, связанный фосфодиэфирной связью.
В некоторых воплощениях второй сегмент может содержать дополнительные ДНК или РНК-нуклеозиды, которые могут быть связаны фосфодиэфирными связями. Второй сегмент ковалентно связан с третьим сегментом, который может, например, представлять собой или содержать конъюгированный компонент.
Второй сегмент может содержать или состоять по меньшей мере из одного ДНК или РНК-нуклеозида, связанного с первым сегментом посредством фосфодиэфирной связи. В некоторых аспектах межнуклеотидная связь между первым и вторым сегментом считается частью сегмента В.
В некоторых воплощениях второй сегмент содержит или представляет собой по меньшей мере от 1 до 10 связанных нуклеозидов, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 связанных ДНК или РНК- нуклеотидов. Хотя сегмент связанных фосфодиэфирными связями ДНК/РНК-нуклеозидов имеет важное значение для расщепляемого линкера, сегмент В также может содержать аналоги нуклеозидов с модифицированными углеводами, например, такие, которые упоминаются в данном документе при описании первого сегмента. Однако в некоторых воплощениях нуклеозиды сегмента В (возможно, независимо) выбраны из группы, состоящей из ДНК и РНК-нуклеозидов. Считается, что нуклеозиды сегмента В могут содержать нуклеиновые основания естественного происхождения или искусственного происхождения. Сегмент В содержит по меньшей мере один ДНК или РНК-нуклеозид, связанный фосфодиэфирными связями (который в некоторых воплощениях может представлять собой первый нуклеозид, примыкающий к сегменту А). Если сегмент В содержит другие нуклеозиды, сегмент В может также содержать и другие нуклеозидные связи, отличные от фосфодиэфирной, например, (возможно, независимо выбранные из) фосфоротиоатную, фосфодитиоатную, боранофосфатную или метилфосфонатную. Однако в некоторых воплощениях все межнуклеозидные связи в сегменте В являются фосфоротиоатными. В некоторых воплощениях все нуклеозиды сегмента В содержат (возможно, независимо) 2'-ОН углевод рибозу (РНК), или 2'-Н углевод, т.е. РНК или ДНК.
В некоторых воплощениях второй сегмент содержит или состоит по меньшей мере из 1-10 связанных (например, фосфодиэфирными связями) ДНК или РНК-нуклеозидов, например, из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 связанных (например, фосфодиэфирными связями) ДНК или РНК-нуклеотидов.
В некоторых воплощениях сегмент В содержит не более 3 или не более 4 последовательно расположенных ДНК или РНК-нуклеозидов (таких как ДНК-нуклеозиды). Поскольку данный сегмент В может быть очень коротким и не рекрутировать РНКазу Н, большой интерес представляют варианты, когда сегмент В не является частью единой последовательности смежных нуклеиновых оснований, комплементарной мишени. В некоторых воплощениях могут оказаться предпочтительны более короткие сегменты В, например, длиной 1-4 нуклеотида, поскольку они с малой вероятностью могут быть мишенями рестрикционных ферментов, распознающих специфическую последовательность. Следовательно, возможно варьировать чувствительность сегмента В к расщеплению эндонуклеазами и таким образом точно регулировать скорость активации активного олигомера in vivo или внутри клетки. Соответственно, при необходимости очень быстрой активации можно использовать сегменты В большей длины и/или сегменты В, содержащие сайты распознавания рестрикционных ферментов (например, клеточно- или тканеспецифических или дифференциально экспрессируемых).
Как показано в Примерах, сегмент В может быть конъюгирован с функциональной группой (X), такой как конъюгат, реакционноспособная обеспечивающая адресное взаимодействие группа, активная группа или блокирующая группа, посредством линкерной группы, которая может, например, содержать фосфодиэфирную связь, и/или, возможно, подходящей линкерной группы, описанной в данном документе, например, фосфатной нуклеозидной связи (например, фосфодиэфирной, фосфоротиоатной, фосфородитиоатной, боранофосфатной или метилфосфонатной) или триазольной группы. В некоторых аспектах линкерная группа является такой же, как и линкерная группа между сегментами А и В, и соответственно, может представлять собой фосфодиэфирную связь. В некоторых аспектах линкерная группа представляет собой фосфотиоратную связь.
В некоторых воплощениях ДНК- или РНК-нуклеотиды второго сегмента независимо выбраны из ДНК- и РНК-нуклеотидов. В некоторых воплощениях ДНК- или РНК-нуклеотиды второго сегмента представляют собой ДНК-нуклеотиды. В некоторых воплощениях ДНК или РНК-нуклеотиды второго сегмента представляют собой РНК-нуклеотиды.
Применительно ко второму сегменту термины ДНК- и РНК-нуклеозид могут охватывать основания естественного происхождения или искусственного происхождения (также обозначаемые аналогами оснований или модифицированными основаниями).
Считается, что в некоторых воплощениях второй сегмент может также содержать другие нуклеотиды или аналоги нуклеотидов. В некоторых воплощениях второй сегмент содержит только ДНК- или РНК-нуклеозиды. В некоторых воплощениях, когда второй сегмент содержит более одного нуклеозида, межнуклеозидные связи второго сегмента содержат фосфодиэфирные связи. В некоторых воплощениях, когда второй сегмент содержит более одного нуклеозида, все межнуклеозидные связи второго сегмента содержат фосфодиэфирные связи.
В некоторых воплощениях по меньшей мере два последовательно расположенных нуклеозида второго сегмента представляют собой ДНК-нуклеозиды (например, по меньшей мере 3 или 4 или 5 последовательно расположенных ДНК-нуклеотида). В некоторых воплощениях по меньшей мере два последовательно расположенных нуклеозида второго сегмента представляют собой РНК-нуклеозиды (например, по меньшей мере 3 или 4 или 5 последовательно расположенных РНК-нуклеотида). В некоторых воплощениях по меньшей мере два последовательно расположенных нуклеозида второго сегмента представляют собой по меньшей мере один ДНК- и по меньшей мере один РНК- нуклеозид. Межнуклеозидные связи между сегментом А и сегментом В представляют собой фосфодиэфирные связи. В некоторых воплощениях, когда сегмент В содержит более одного нуклеозида, по меньшей мере одна дополнительная межнуклеозидная связь представляет собой фосфодиэфирную - например, линкерная(ые) группа(ы) между 2 (или 3 или 4 или 5) нуклеозидами, примыкающими к сегменту А.
Второй сегмент с одной стороны (5' или 3') фланкирован первым сегментом, например, антисмысловым олигонуклеотидом, а с другой стороны (3' или 5', соответственно) связан с конъюгированным компонентом или аналогичной группой (например, блокирующими компонентом/группой, компонентом/группой, обеспечивающими адресное взаимодействие, или низкомолекулярным терапевтически активным компонентом), возможно посредством линкерной группы (т.е. находящейся между вторым сегментом и конъюгатом/блокирующей и т.п. группой).
В таком воплощении олигонуклеотид по изобретению можно описать согласно следующей формуле:
5'-А-РО-В [Y)X-3' или 3'-А-РО-В[Y)X-5'
где А представляет собой сегмент А, РО представляет собой фосфодиэфирную связь, В представляет собой сегмент В, Y представляет собой необязательную линкерную группу, X представляет собой конъюгат, обеспечивающую адресное взаимодействие, блокирующую или реакционноспособную или активную группу.
В некоторых воплощениях сегмент В содержит в направлении 3'-5' или 5'-3': i) фосфодиэфирную связь с 5' или 3' нуклеозидом сегмента A, ii) ДНК- или РНК-нуклеозид, например, ДНК-нуклеозид, и iii) дополнительную фосфодиэфирную связь.
5'-А-РО-В-РО-3' или 3'-А-РО-В-РО-5'
Дополнительная фосфодиэфирная связь связывает сегмент В нуклеозида с одним или несколькими дополнительными нуклеозидами, например, с одним или несколькими ДНК- или РНК-нуклеозидами, или может связывать с сегментом X (который представляет собой конъюгат, обеспечивающую адресное взаимодействие или реакционноспособную группу или активную группу) возможно, посредством линкерной группы (Y).
В некоторых воплощениях сегмент В содержит в направлении 3'-5' или 5'-3': i) фосфодиэфирную связь с 5' или 3' нуклеозидом сегмента A, ii) ДНК- или РНК-нуклеозиды, связанные фосфодиэфирной связью, например, ДНК-нуклеозиды, и возможно, iii) дополнительную фосфодиэфирную связь:
5'-A-[PO-B]n-[Y]-X 3' или 3'-A-[PO-B]n-[Y]-X 5'
5'-A-[PO-B]n-PO-[Y]-X 3' или 3'-A-[PO-B]n-PO-[Y]-X 5'
Где А представляет сегмент А, [РО-В]n представляет сегмент В, где n составляет от 1 до 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, РО представляет собой необязательную фосфодиэфирную линкерную группу между сегментами В и X (или Y, если таковой существует).
В некоторых воплощениях изобретения предложены соединения одной из следующих формул (или содержащие одну из следующих формул):
5' [Сегмент А] - РО - [сегмент В] 3' - Y - X
5' [Сегмент А] - РО - [сегмент В] - РО 3' - Y - X
5' [Сегмент А] - РО - [сегмент В] 3' - X
5' [Сегмент А] - РО - [сегмент В] - РО 3' - X
3' [Сегмент А] - РО - [сегмент В] 5' - Y - X
3' [Сегмент А] - РО - [сегмент В] - РО 5' - Y - X
3' [Сегмент А] - РО - [сегмент В] 5' - X
3' [Сегмент А] - РО - [сегмент В] - РО 5' - X
Сегмент В может, например, содержать или состоять из:
5' DNA 3'
3' DNA 5'
5' DNA-PO-DNA-3'
3' DNA-PO-DNA-5'
5' DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA 5'
5' DNA-PO-DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA-PO-DNA 5'
5' DNA-PO-DNA-PO-DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA-PO-DNA-PO-DNA 5'
Выбор последовательности второго сегмента:
В некоторых воплощениях при выравнивании сегментов А и В олигонуклеотида с комплементарной последовательностью мишени сегмент В не образует комплементарной последовательности.
В некоторых воплощениях при выравнивании сегментов А и В олигонуклеотида с комплементарной последовательностью мишени сегмент В образует комплементарную последовательность. В данном случае сегменты А и В вместе могут образовывать единую непрерывную последовательность, комплементарную последовательности мишени.
В некоторых воплощениях последовательность оснований в сегменте В подбирают таким образом, чтобы получить оптимальную последовательность сайта расщепления эндонуклеазами, в зависимости от того, какие рестрикционные эндонуклеазы преобладают в ткани-мишени или клетке-мишени или внутриклеточных компартментах. Так, получая клеточные экстракты из целевых и нецелевых тканей, можно подобрать последовательности сайтов расщепления эндонуклеазами для использования в сегменте В в зависимости от рестриктазной активности, преобладающей в нужных клетках-мишенях (например, печени/гепатоцитах) относительно нецелевых клеток (например, почки). Следовательно, можно оптимизировать активность/эффективность соединения подавления мишени в нужной ткани/клетки.
В некоторых воплощениях сегмент В содержит динуклеотид последовательности АА, AT, AC, AG, ТА, ТТ, ТС, TG, СА, CT, CC, CG, GA, GT, GC или GG, где С может представлять собой 5-метилцитозин, и/или Т можно заменить на U. В некоторых воплощениях сегмент В содержит тринуклеотид последовательности AAA, ААТ, AAC, AAG, ATA, АТТ, АТС, ATG, АСА, ACT, АСС, ACG, AGA, AGT, AGC, AGG, ТАА, TAT, ТАС, TAG, ТТА, ТТТ, ТТС, TAG, ТСА, ТСТ, ТСС, TCG, TGA, TGT, TGC, TGG, САА, CAT, САС, CAG, СТА, CTG, СТС, СТТ, CCA, ССТ, ССС, CCG, CGA, CGT, CGC, CGG, GAA, GAT, GAC, CAG, GTA, GTT, GTC, GTG, GCA, GCT, GCC, GCG, GGA, GGT, GGC и GGG где С может представлять собой 5-метилцитозин и/или Т можно заменить на U. В некоторых воплощениях сегмент В содержит тетрануклеотид последовательности АААХ, ААТХ, ААСХ, AAGX, АТАХ, АТТХ, АТСХ, ATGX, АСАХ, АСТХ, АССХ, ACGX, AGAX, AGTX, AGCX, AGGX, ТААХ, ТАТХ, ТАСХ, TAGX, ТТАХ, ТТТХ, ТТСХ, TAGX, ТСАХ, ТСТХ, ТССХ, TCGX, TGAX, TGTX, TGCX, TGGX, СААХ, САТХ, САСХ, CAGX, СТАХ, CTGX, СТСХ, СТТХ, ССАХ, ССТХ, СССХ, CCGX, CGAX, CGTX, CGCX, CGGX, GAAX, GATX, GACX, CAGX, GTAX, GTTX, GTCX, GTGX, GCAX, GCTX, GCCX, GCGX, GGAX, GGTX, GGCX и GGGX, где X может быть выбран из группы, состоящей из А, Т, U, G, С и их аналогов, где С может представлять собой 5-метилцитозин и/или Т можно заменить на U. Считается, что при упоминании нуклеиновых оснований (естественного происхождения) А, Т, U, G, С, их можно заменить аналогами нуклеиновых оснований, которые выполняют функцию, эквивалентную нуклеиновым основаниям естественного происхождения (например, основанием, спаривающимся с комплементарным нуклеозидом).
В некоторых воплощениях соединение по изобретению может содержать более одной конъюгированной группы (или более одной функциональной группы X - такой как конъюгат, обеспечивающая адресное взаимодействие, блокирующая или активированная группа или реакционноспособная или активная группа), например, 2 или 3 таких группы. В некоторых воплощениях сегмент В ковалентно связан, возможно, посредством линкерной группы (например, ненуклеотидной) по меньшей мере с одной функциональной группой, например, с двумя или тремя функциональными группами. В некоторых воплощениях первый сегмент может быть ковалентно связан (например, посредством межнуклеозидных связей, например, фосфодиэфирных связей) с двумя сегментами В, например, одним в положении 5' и одним в положении 3' относительно первого сегмента, при этом каждый сегмент В может быть (возможно, независимо) выбран из сегментов В, описанных в данном документе. Соответственно, один сегмент В может иметь одну или несколько функциональных групп, и второй сегмент В может иметь одну или несколько функциональных групп, при этом функциональные группы каждого сегмента В могут быть независимо выбраны из конъюгата, обеспечивающей адресное взаимодействие группы, блокирующей группы или реакционноспособной/активной группы.
Использование сегмента В, такого как "РО ДНК-линкер", описанный выше, между олигомером и конъюгированным компонентом (X или X-Y) особенно предпочтительно, поскольку обеспечивает однотипное отщепление конъюгированного компонента от последовательности олигомера после доставки олигомера в клетку-мишень (например, гепатоцит). Однотипное отщепление может оказаться полезным для сохранения максимальной внутриклеточной активности родительского соединения, а также усиления профиля безопасности олигомерного конъюгата.
Полиолигомерные соединения
В изобретении предложено полиолигомерное соединение, которое может содержать первый сегмент (сегмент А), (возможно, второй сегмент (сегмент В)) и третий сегмент (сегмент С), где первый сегмент ковалентно связан по меньшей мере с одним дополнительным олигомерным соединением (участком А'), при этом первый сегмент (сегмент А) и сегмент А' ковалентно связаны посредством биорасщепляемого линкера (сегмент В'), который может, например, быть таким, как описанный в данном документе второй сегмент (сегмент В), например, сегмент, содержащий по меньшей мере один, например, два, три, четыре или пять ДНК- или РНК-нуклеозидов (например, ДНК-нуклеозидов), связанных фосфодиэфирными связями. В воплощениях, содержащих сегмент В, сегменты В и В' в некоторых воплощениях могут иметь одинаковую структуру, например, одинаковое число ДНК/РНК нуклеозидов и фосфодиэфирных связей и/или одинаковую последовательность нуклеиновых оснований. В других воплощениях сегменты В и В' могут быть различными. Например, такие полиолигомерные соединения могут иметь следующую структуру: (5'-3' или 3'-5'') конъюгат-РО-ON-PO'-ON', (5'-3' или 3'-5') конъюгат-PO-ON-PO'-ON', где конъюгат представляет собой сегмент С, РО представляет собой сегмент В, РО' представляет собой сегмент В', a ON 1 представляет собой сегмент А, и ON' представляет собой сегмент А'.
Считается, что сегмент А' олигомера в некоторых воплощениях может содержать множество дополнительных олигомерных соединений (например, дополнительные 2 или 3 олигомерных соединения), связанные последовательно (или параллельно) посредством биорасщепляемых линкеров, например: конъюгат-PO-ON-PO-ON'-PO''-ON'' или конъюгат-PO-ON-[PO-ON']n, где n может составлять, например, 1, 2 или 3, a ON' могут быть одинаковыми или различными, и в последнем случае могут иметь одинаковые или различные мишени.
В изобретении предложено олигомерное соединение, содержащее последовательность смежных нуклеотидов формулы [LNAs]7-18-[DNA]1-5-[LNAs]7-18, и ненуклеотидный конъюгат, например, конъюгат GalNAc, например, тривалентный конъюгат GalNAc, например, конъюгированный компонент, выбранный из группы, состоящей из Конъюгатов 1, 2, 3, 4, 1а, 2а, 3а, 4а, или других тривалентных конъюгатов GalNAc, например, описанных в данном документе. Нижний индекс обозначает фосфоротиоатную связь. По меньшей мере одна межнуклеозидная связь, входящая в состав или прилежащая к области -[DNA]1-5- представляет собой фосфодиэфирную связь. В некоторых воплощениях все межнуклеозидные связи в составе или прилежащие к области -[DNA]1-5- представляют собой фосфодиэфирные связи. В некоторых воплощениях область -[DNA]1-5- имеет 2, 3, 4 или 5 последовательно расположенных ДНК-нуклеозида, которые связаны фосфодиэфирными связями. В данном воплощении межнуклеозидные связи между -[DNA]2-5- представляют собой фосфодиэфирные связи, и, возможно, межнуклеозидные связи между областью -[DNA]1-5 и LNA-областью [LNAs]7-18 независимо представляют собой фосфоротиоатную или фосфодиэфирную связи, например, обе могут быть фосфодиэфирными или фосфоротиоатными, или одна может быть фосфодиэфирной, а другая фосфоротиоатной. В воплощении, когда область ДНК представляет собой единственный ДНК-нуклеозид, по меньшей мере одна или обе межнуклеозидные связи, соседствующие с областью ДНК, являются фосфодиэфирными, а если фосфодиэфирной является только одна из них, вторая может быть фосфоротиоатной. Область -[DNA]1-5 можно охарактеризовать как указанный в данном документе сегмент В - т.е. он может представлять собой расщепляемый в физиологических условиях линкерный сегмент, состоящий из нуклеозидов. Каждый [LNAs]7-18 представляет собой LNA-олигомер, содержащий фосфоротиоатные связи, и может, например, быть выбран из группы, состоящей из LNA гэпмера, LNA миксмера или LNA тоталмера. Конъюгат GalNAc может, например, быть расположен в 5' или 3' положении относительно последовательности смежных нуклеотидов. В предпочтительном воплощении по меньшей мере один из LNA-олигомеров или оба полиолигомерных конъюгата представляют собой LNA тоталмер из 7-12, например, из 8, 9 или 10 нуклеотидов длиной. В некоторых воплощениях LNA тоталмер может содержать только LNA-нуклеотиды, например, бета-D-окси LNA-нуклеозиды, которые связаны между собой фосфоротиоатными связями. Например, полиолигомерный конъюгат может содержать последовательность смежных нуклеотидов [LNAs]7-10-[DNA]1-5-[LNAs]7-10, например, [LNAs]7-10-[DNA]2-[LNAs]7-10 or [LNAs]7-10-[DNA]3-[LNAs]7-10 или [LNAs]7-10-[DNA]4-[LNAs]7-10. В одном воплощении последовательность смежных нуклеотидов содержит [LNAs]8-[DNA]1-5-[LNAs]8, например, [LNAs]8-[DNA]2-[LNAs]8, [LNAs]8-[DNA]3-[LNAs]8 или [LNAs]8-[DNA]4-[LNAs]8. Такие полиолигомерные комплексы особенно удобны для обеспечения направленного взаимодействия с микроРНК, например, зрелыми микроРНК. С использованием первого сегмента LNA-олигомера, обеспечивающего направленное взаимодействие с первой мишенью (например, мРНК, микроРНК или вирусной последовательностью) и второго сегмента LNA-олигомера, обеспечивающего направленное взаимодействие со второй мишенью (например, мРНК, микроРНК или вирусной последовательностью), можно получать единые соединения, направленные против двух различных мишеней, например, мишенью первого сегмента олигомера может быть АроВ, а мишенью второго сегмента олигомера может быть другая мРНК, например, мРНК mtGPAT, например:
сегмент С-5' [SEQ ID No 50] - [сегмент B] - [SEQ ID No 59] 3' (например, SEQ ID NO 61:
(тривалентный GalNAc)- GsTstsgsascsascstsgsTsCcaAsTsTscscscstsgsCsCstsGsTsG - 3')
Сегмент С может представлять собой тривалентный конъюгат GalNAc, например, конъюгат 2а, или другой конъюгат GalNAc, изложенный в данном документе. Сегмент В может представлять собой динуклеотид ДНК "ca", в котором межнуклеотидные связи в составе динуклеотида ДНК и примыкающие к динуклеотиду являются фосфодиэфирными.
С использованием первого сегмента олигомера (например, [LNAs]7-10), мишенью которого является первая микроРНК, и второго сегмента олигомера, мишенью которого является вторая микроРНК, можно создать единые соединения, направленные против двух различных целевых микроРНК, например, миРНК-21 и миРНК-221, обе из которых являются мишенями терапии при гепатоцеллюлярной карциноме. В альтернативном случае, первая и вторая мишени могут представлять собой одинаковые микроРНК, например, миРНК-122, миРНК-21, миРНК-155, миРНК-33, миРНК-221, что позволяет доставлять в клетку-мишень два олигомера с одним конъюгированным компонентом.
Это имеет особенно важное значение для рецептор-опосредованной адресной доставки конъюгата, например, доставки конъюгата с использованием асиалогликопротеинового рецептора, когда опосредованный рецептором захват, например, олигомеров, конъюгированных с GalNAc, ограничен доступностью свободных рецепторов на поверхности клетки-мишени, применение полиолигомерных конъюгатов позволит улучшить доставку к клеткам-мишеням. Также важно избегать полного насыщения рецепторов клеточной поверхности, имеющих важную биологическую функцию, при этом использование полиолигомерной стратегии обеспечит эффективную доставку соединения и обеспечит надлежащую фармакологическую эффективность при снижении риска побочных эффектов, связанных с насыщением рецептора/конкуренцией конъюгированного компонента за рецептор. Таким образом, применение полиолигомерного конъюгата представляет собой эффективное решение, позволяющее усилить терапевтический индекс, улучшить доставку и эффективность олигомера при снижении нежелательных побочных эффектов.
Композиции
Олигомер по изобретению может найти применение в фармацевтических составах и композициях. Соответствующие композиции содержат фармацевтически приемлемый разбавитель, носитель, соль или адъювант. WO 2007/031091 описывает подходящие и предпочтительные фармацевтически приемлемые разбавители, носители и адъюванты, которые включены путем ссылки. Подходящие дозировки, составы, способы введения, композиции, дозированные лекарственные формы, комбинации с другими терапевтически активными агентами, пролекарства также описаны в WO 2007/031091 и включены путем ссылки.
Антисмысловые олигонуклеотиды можно смешивать с фармацевтически приемлемыми активными или инертными субстанциями для получения фармацевтических композиций или составов. Композиции и способы составления фармацевтических композиций зависят от ряда параметров, включая способ введения, тяжесть заболевания или вводимую дозу, но не ограничиваются ими.
Антисмысловое соединение может найти примерение в фармацевтических композициях при комбинировании антисмыслового соединения с подходящим фармацевтически приемлемым разбавителем или носителем. Фармацевтически приемлемые разбавители включают фосфатно-солевой буфер (ФСБ). ФСБ представляет собой разбавитель, подходящий для применения в композициях для парентерального введения.
Фармацевтические композиции, содержащие антисмысловые соединения, охватывают фармацевтически приемлемые соли, эфиры или соли таких эфиров или любые другие олигонуклеотиды, при введении которых животному, включая человека, образуется (прямо или опосредовано) его биологически активный метаболит или остаток. Например, в описании также приведены фармацевтически приемлемые соли антисмысловых соединений, пролекарства, фармацевтически приемлемые соли таких пролекарств и другие биоэквиваленты. Подходящие фармацевтически приемлемые соли включают соли натрия и калия, но не ограничиваются ими. В некоторых воплощениях олигомер по изобретению представляет собой пролекарство.
Применение
Олигомеры по изобретению можно применять как реагенты для исследования, например, для диагностики, лечения и профилактики.
В эксперименте, такие олигомеры можно применять в некоторых воплощениях для специфического ингибирования синтеза белка (обычно за счет деградации или ингибирования мРНК и предотвращения образования белка) в клетках и у экспериментальных животных, что позволит провести функциональный анализ мишени или оценить ее пригодность в качестве мишени для терапевтического воздействия.
В терапии, животное или человека, у которого подозревают наличие заболевания или нарушения, поддающегося лечению путем регуляции экспрессии мишени, лечат путем введения олигомерных соединений согласно данному описанию. Также предложены способы лечения млекопитающего, например, человека, у которого подозревают наличие или предрасположенность к заболеванию или состоянию, ассоциированному с экспрессией мишени, путем введения терапевтически или профилактически эффективного количества одного или нескольких олигомеров или композиций по изобретению. Олигомер, конъюгат или фармацевтическую композицию по изобретению обычно вводят в эффективном количестве.
В изобретении также предложено применение соединения или конъюгата для изготовления лекарственного средства для лечения нарушения, согласно данному описанию, или способа лечения нарушения, согласно данному описанию. В некоторых воплощениях заболевание или нарушение представляет собой заболевание или нарушение, ассоциированное или связанное с печенью, например, заболевание или нарушение, выбранное из группы, состоящей из
В изобретении также предложен способ лечения нарушения, согласно данному описанию, указанный способ включает введение соединения по изобретению и/или конъюгата по изобретению, и/или фармацевтической композиции по изобретению нуждающемуся в этом пациенту, в соответствии с данным описанием.
Медицинские показания
В изобретении предложен конъюгат антисмыслового LNA-олигомера для применения в медицине. В изобретении предложен конъюгат антисмыслового LNA-олигомера для применения с целью снижения уровня экспрессируемой в печени РНК. В изобретении предложен конъюгат антисмыслового LNA-олигомера для применения в лечении метаболических заболеваний или нарушений, например, заболеваний или нарушений, затрагивающих печень. В изобретении предложен конъюгат антисмыслового LNA-олигомера для применения в лечении гепатита, например, гепатита В или С.
В некоторых воплощениях заболевание представляет собой заболевание или нарушение, затрагивающее печень. В некоторых воплощениях заболевание или нарушение представляет собой фиброз печени или приводит к фиброзу печени или связано с фиброзом печени. В некоторых воплощениях заболевание или нарушение представляет собой нарушение свертывания крови, например, лечение или предупреждение тромбоэмболических осложнений, таких как тромбоз, эмболия и тромбоэмболия, тромбоз глубоких вен, эмболия легких, инфаркт миокарда и инсульт. Олигомеры, мишенью которых является фактор VII, можно использовать в лечении нарушений свертывания крови или для контролирования свертывания крови у индивида, см. US 2010/0298417 и WO 2012/174154, где приведены примеры антисмысловых олигонуклеотидов, мишенью которых является фактор VII. Олигомеры, мишенью которых является фактор VII, можно также применять в лечении воспалительных заболеваний/нарушений, злокачественных новообразований, ревматоидного артрита и фиброза (см. US 2010/0298417 и WO 2012/174154). В некоторых воплощениях указанное выше заболевание и нарушение можно лечить при помощи соединений по изобретению. В некоторых воплощениях изобретения предложены олигомеры для применения в лечении воспалительных заболеваний/нарушений, злокачественных новообразований, ревматоидного артрита и фиброза; или заболевания или нарушения, выбранного из группы, состоящей из нарушения свертывания крови, например, для лечения или предупреждения тромбоэмболических осложнений, таких как тромбоз, эмболия и тромбоэмболия, тромбоз глубоких вен, эмболия легких, инфаркт миокарда и инсульт.
В некоторых воплощениях заболевание или нарушение представляет собой заболевание или нарушение, затрагивающее печень.
В некоторых воплощениях заболевание или нарушение представляет собой метаболическое нарушение, которое, например, может представлять собой заболевание или нарушение, затрагивающее печень, и/или в некоторых аспектах, сердечно-сосудистое заболевание или нарушение.
Сердечно-сосудистые/метаболические заболевания включают, например, метаболический синдром, ожирение, гиперлипидемию, атеросклероз, нарушение соотношения ЛПВП и ЛПНП, дислипидемии, например, семейную комбинированную гиперлипидемию (СКГЛ), приобретенную гиперлипидемию, резистентную к терапии статинами гиперхолестеринемию, атеросклеротическую болезнь сердца и ишемическую болезнь сердца (ИБС), атеросклероз, болезни сердца, диабет (1 и/или 2 типа), неалкогольный стеатогепатит, острый коронарный синдром (ОКС), хроническую сердечную недостаточность, сердечно-сосудистые заболевания, кардиометаболические нарушения, гиперлипидемию и родственные ей нарушения, метаболический синдром, атеросклероз, хроническую сердечную недостаточность, сосудистые заболевания, болезнь периферических артерий, болезни сердца, ишемию, диабет 2 типа и/или диабет 1 типа.
В некоторых воплощениях заболевание или нарушение выбрано из группы, состоящей из метаболического синдрома, ожирения, гиперлипидемии, атеросклероза, нарушения соотношения ЛПВП и ЛПНП, дислипидемии, например, семейной комбинированной гиперлипидемии (СКГЛ), приобретенной гиперлипидемии, резистентной к терапии статинами гиперхолестеринемии, атеросклеротической болезни сердца и ишемической болезни сердца (ИБС).
В некоторых воплощениях заболевание или нарушение выбрано из группы, состоящей из хронической сердечной недостаточности, сердечнососудистых заболеваний, кардиометаболических нарушений, хронической сердечной недостаточности, сосудистых заболеваний, болезни периферических артерий, болезни сердца, ишемии, острого коронарного синдрома (ОКС).
В некоторых воплощениях заболевание или нарушение представляет собой диабет 2 типа и/или диабет 1 типа.
В некоторых воплощениях заболевание или нарушение представляет собой вирусное заболевание, например, вирусный гепатит, например, гепатит С, гепатит В. В некоторых воплощениях заболевание печени может представлять собой заболевание или нарушение, выбранное из группы, состоящей из неалкогольной жировой болезни печени (НЖАБП) и неалкогольного стеатогепатита.
В изобретении также предложено применение соединения по изобретению в изготовлении лекарственного средства для лечения заболевания, нарушения или состояния, например, указанного в данном документе.
В сущности, некоторые аспекты изобретения относятся к способу лечения млекопитающего, страдающего или предрасположенного к состояниям, связанным с аномальным уровнем мишени, который включает введение млекопитающему терапевтически эффективного количества олигомера, направленного против мишени, содержащего одно или несколько звеньев LNA. Олигомер, конъюгат или фармацевтическую композицию по изобретению обычно вводят в эффективном количестве.
Один из аспектов изобретения относится к применению соединения по изобретению для изготовления лекарственного средства для лечения заболевания, нарушения или состояния, например, указанного в данном документе.
Кроме того, изобретение относится к способу лечения индивида, например, млекопитающего, например, человека, страдающего заболеванием или состоянием, например, указанным в данном документе.
Пациент, нуждающийся в лечении, представляет собой пациента, страдающего или возможно страдающего от заболевания или нарушения.
В некоторых воплощениях термин «лечение», используемый в данном документе, относится как к лечению существующего заболевания (например, заболевания или нарушения, указанного в данном документе), так и к предупреждению заболевания, т.е. к профилактике. В этой связи считается, что в некоторых воплощениях лечение может представлять собой профилактику.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Эксперименты на мышах: Если не указано иначе, эксперименты на мышах проводили следующим образом:
Вводимые дозы и взятие образцов
Использовали мышей линии C57BI6-N в возрасте 7-10 недель, животные были подобраны по возрасту и полу (самки в исследованиях 1, 2 и 4, самцы в исследовании 3). Соединения вводили внутривенно в хвостовую вену. Для взятия образцов сыворотки на промежуточном этапе брали 2-3 капли крови путем пункции лицевой вены, последнее взятие крови осуществляли из нижней полой вены. Сыворотку собирали в пробирки с разделительным гелем (Greiner) и до проведения анализа хранили в замороженном виде. Мышам линии C57BL6 внутривенно вводили антисмысловой олигонуклеотид в однократной дозе 1 мг/кг (или указанное количество) в солевом растворе или только солевой раствор, согласно указанной информации. Животных подвергали эвтаназии, например, на 4-7 день (или в указанное время) после введения и забирали печень и почки.
Выделение РНК и анализ РНК: выделенную из тканей мРНК анализировали с использованием набора для количественного определения мРНК Qantigene ("bDNA-assay", Panomics/Affimetrix), следуя указаниям производителя. Для получения тканевого лизата 50-80 мг ткани лизировали путем соникации в 1 мл лизирующего буфера, содержащего протеиназу К. Лизаты использовали непосредственно для анализа bDNA, без экстрагирования РНК. Наборы праймеров для мишени и GAPDH синтезировали на заказ в компании Panomics. Для анализа результатов единицы люминесценции, полученные для генов-мишеней, нормализовали относительно гена домашнего хозяйства GAPDH.
Исследование АЛТ, ACT и холестерина в сыворотке проводили на автоматическом анализаторе "Cobas INTEGRA 400 plus" (Roche Diagnostics), используя 10 мкл сыворотки. Для количественного определения уровня фактора VII в сыворотке использовали набор для определения ферментативной активности BIOPHEN FVII ((#221304, Hyphen BioMed) согласно инструкциям производителя.
Для количественного определения олигонуклеотидов флуоресцентно-меченные РНК зонды гибридизовали с представляющим интерес олигонуклеотидом в тканевом лизате. Те же лизаты использовали для анализа bDNA, точно измеряя вес образца ткани. Образование гетеродуплексов регистрировали при помощи анионообменной ВЭЖХ и флуоресцентной детекции.
Пример 1. Синтез олигонуклеотидов
Взяв за основу последовательность тридекамера фактора VII мыши, получили следующие LNA-олигонуклеотиды гэпмеры.

Условные обозначения: Заглавные L: бета-D-окси LNA; s: фосфоротиоат; заглавные D: ДНК; (NH2C6): Аминолинкер; (Chol1): холестерин; (C6SSC6): биорасщепляемый дисульфидный линкер.


За исключением конъюгата GalNac соединения синтезировали при помощи твердофазного синтеза с применением доступных для приобретения фосфорамидитов и очищали при помощи ионообменной ВЭЖХ. Тривалентный кластер GalNAc получали согласно US 2012/0157509, содержание которого включено путем ссылки (см. Фиг. 1).
Пример 2. Сравнение конъюгатов GalNac и холестерина при ингибировании фактора VII in vivo
Сравнительное исследование конъюгатов GalNac и холестерина in vivo проводили на мышах, всего использовали 9 групп мышей (n=3). Каждой мыши вводили одну внутривенную дозу LNA соединения, в дозе 1 мг/кг или 4 мг/кг. Контрольная группа получала солевой раствор. У мышей предварительно брали кровь за 1 день до введения, последующие взятия образцов крови осуществляли через 6 ч, 24 ч, 48 ч, а через 3 дня мышей подвергали эвтаназии и забирали печень, почки и образцы крови.
Уровень фактора VII в сыворотке и уровень мРНК определяли с помощью стандартных методов (см. Фиг. 2 и 3). Как FVII GalNac, так и холестерин (соединение с фосфоротиоатными связями) снижали FVII в сыворотке, при этом конъюгаты GalNac показывали большую эффективность по сравнению с конъюгатами холестерина (см. Фиг. 2, 1 мг/кг).
Пример 3. Ингибирование FVII in vivo с использованием конъюгатов GalNac и холестерина, исследование с увеличением дозы Соединения

Заглавные L обозначают LNA-нуклеозиды (например, бета-D-окси LNA), строчные d обозначают ДНК-нуклеозиды. Строчные s обозначают фосфоротиоатные межнуклеозидные связи (сегмент А). Линкер 2РО (сегмент В) находится в положении 5' относительно последовательности сегмента А и содержит два ДНК-нуклеозида, связанных фосфодиэфирными связями, при этом межнуклеозидные связи между 3' ДНК-нуклеозидом сегмента А и 5' LNA-нуклеозидом сегмента А также являются фосфодиэфирными. Линкерная группа (Y) применяется для связывания конъюгированной группы, если таковая присутствует, с сегментом В или А (например, SEQ ID NO 3).
В исследовании in vivo на мышах использовали 16 групп мышей (n=3). Каждой мыши вводили одну внутривенную дозу LNA соединения, в дозе 1, 0,5, 0,25, 0,1 или 0,05 мг/кг. Контрольная группа получала солевой раствор. У мышей предварительно брали кровь за 1 день до введения, последующие взятия проб крови осуществляли в разное время в течение исследования. Мышей подвергали эвтаназии на 4, 14 или 24 день и забирали печень, почки и образцы крови. Схема исследования приведена в таблице ниже.
Выводы: GalNAc, конъюгированный с LNA олигонуклеотидом, мишенью которого является фактор VII (SEQ ID NQ 3 и 6), демонстрировали хорошую активность в отношении белка фактора VII в сыворотке (Фиг. 4) и уровня мРНК в печени (Фиг.5) по сравнению с неконъюгированным LNA олигонуклеотидом (SEQ ID NO 1). Активность выражена даже при очень низких дозах. Кроме того, кластер GalNAc более активен по сравнению с конъюгатом холестерина в отношении белка и мРНК FVII (SEQ ID NO 4 и 7) (Фиг. 4d и Фиг. 5d)). Содержание в тканях печени и почек показано на Фиг. 6, при этом наблюдается, что кластер GalNAc (SEQ ID NO 3 и 6) усиливает захват в печени и уменьшает захват в почках по сравнению с неконъюгированным LNA-олигонуклеотидом, мишенью которого является фактор VII (SEQ ID NO 1). При сравнении LNA-олигонуклеотидов, конъюгированных с GalNAc (SEQ ID NO 3 и 6), и LNA-олигонуклеотидов, конъюгированных с холестерином (SEQ ID NO 4 и 7), отмечено, что их содержание в печени достигает одинакового уровня, но поскольку LNA олигонуклеотиды, конъюгированные с GalNAc, демонстрировали лучшую активность, возможно они обладают более выраженной специфической активностью по сравнению с LNA олигонуклеотидами, конъюгированными с холестерином. По-видимому, РО линкер может усиливать захват тканями (Фиг. 6) и также может обеспечивать большую эффективность (Фиг. 4).
Материалы и методы:
Дизайн эксперимента:
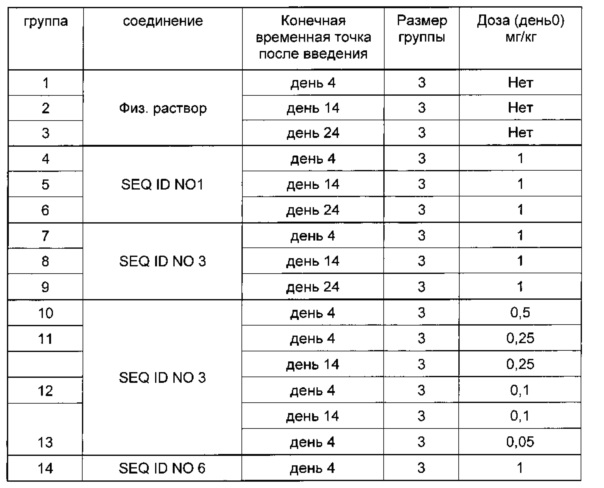
Согласно приведенной выше схеме, самкам мышей проводили внутривенное введение и после эвтаназии забирали печень, почки и образцы крови.
Пример 4. Подавление экспрессии мРНК АроВ in vivo с использованием различных конъюгатов моноGalNAc
Соединения
Олигонуклеотиды синтезировали на универсальных уридиновых носителях, с помощью фосфорамидитного метода на синтезаторе Expedite 8900/MOSS (Multiple Oligonucleotide Synthesis System) в масштабе 4 мкмоль. В конце синтеза проводили отщепление олигонуклеотидов от твердого носителя с использованием водного раствора аммиака в течение 1-2 часов при комнатной температуре, затем удаляли защитную группу в течение 16 ч при 65°С. Олигонуклеотиды очищали при помощи обращенно-фазовой ВЭЖХ и характеризовали при помощи сверхпроизводительной жидкостной хроматографии, молекулярную массу определяли при помощи масс-спектрометрии с ионизацией электрораспылением. Более подробное описание приведено ниже.
Элонгация олигонуклеотидов
Присоединение β-цианоэтил-фосфорамидитов (DNA-A(Bz), DNA-G(ibu), DNA-C(Bz), DNA-T, LNA-5-метил-C(Bz), LNA-A(Bz), LNA-G(dmf), LNA-T или C6-S-S линкера) осуществляли с применением 0,1 М раствора 5'-O-ОМТ-защищенного амидита в ацетонитриле и DCI (4,5-дицианоимидазола) в ацетонитриле (0,25 М) в качестве активатора. На последнем цикле использовали коммерчески доступный фосфорамидит холестерина с C6-линкером в 0,1 М DCM. Тиолирование для введения фосфоротиоатных связей проводили с применением ксантангидрида (0,1 М в смеси ацетонитрил/пиридин 9:1). Для введения фосфодиэфирных связей использовали 0,02 М иод в смеси THF/пиридин/вода 7:2:1. Остальные реагенты представляли собой стандартные реагенты, используемые для синтеза олигонуклеотидов. Для постсинтетического конъюгирования на последней фазе твердофазного синтеза использовали коммерчески доступный фосфорамидит с С6 аминолинкером, а после удаления защитных групп и отщепления от твердого носителя выделяли незащищенный олигонуклеотид. Конъюгаты вводили посредством активации функциональных групп с помощью стандартных методов синтеза.

Заглавные буквы обозначают LNA нуклеозиды (например, бета-D-окси LNA), строчные буквы обозначают ДНК нуклеозиды. Нижний индекс s обозначает фосфоротиоатные межнуклеозидные связи (сегмент А). Цитозины LNA могут представлять собой 5-метилцитозин. Линкер 2РО (сегмент В) находится в положении 5' относительно последовательности сегмента А и содержит два ДНК-нуклеозида, связанных фосфодиэфирными связями, при этом межнуклеозидные связи между 3' ДНК-нуклеозидом сегмента А и 5' LNA-нуклеозидом сегмента А также являются фосфодиэфирными. Линкерная группа (Y) может применяться для связывания конъюгированной группы, если таковая присутствует, с сегментом В или А (например, SEQ ID NO 8 и 11).
Для сравнения конъюгатов моноGalNAc, имеющих разные линкеры, и кластера GalNAc мышам линии C57BL6 вводили внутривенно солевой раствор (контроль) или антисмысловой олигонуклеотид, конъюгированный с моно-GalNAc, не имеющий биорасщепляемого линкера, или имеющий дитио-линкер (SS) или DNA/PO-линкер (РО), (Фиг. 7а) в однократной дозе 1 мг/кг или антисмысловой олигонуклеотид, конъюгированный с моно-GalNAc или с кластером GalNAc, в дозе 0,25 мг/кг (Фиг. 7b). Через 7 дней животных подвергали эвтаназии и выделяли РНК из образцов печени и почек и исследовали на предмет снижения экспрессии мРНК АроВ.
Выводы: По сравнению с неконъюгированным соединением (#12) при конъюгировании с моно-GalNAc в отсутствие биорасщепляемого линкера (#8), или в присутствии DNA/PO-линкера (#10) активность в печени значительно улучшалась (Фиг. 7а). Конъюгирование различных конъюгатов GalNAc, например, моно GalNAcPO (#10) и кластер GalNAc (#11) также позволяет тонко регулировать активность соединения, прицельно направляя ее на печень или почки (Фиг. 7b).
Материалы и методы:
Дизайн эксперимента:

Вводимые дозы и взятие образцов. Мышам линии C57BL6 внутривенно вводили антисмысловой олигонуклеотид в солевом растворе в однократной дозе 1 мг/кг или 0,25 мг/кг или только солевой раствор, как указано в таблице выше. Животных подвергали эвтаназии на 7 день после введения и забирали печень и почки.
Выделение РНК и анализ мРНК. Общую РНК выделяли из образцов печени и почек и анализировали уровень мРНК АроВ, методом гибридизации с разветвленными ДНК-зондами.
Пример 5. Подавление экспрессии мРНК АроВ, содержание в ткани и общий холестерин, при использовании конъюгатов GalNAc in vivo.
Соединения

Заглавные буквы обозначают LNA-нуклеозиды (например, бета-D-окси LNA), строчные буквы обозначают ДНК-нуклеозиды. Нижний индекс s обозначает фосфоротиоатные межнуклеозидные связи (сегмент А). Цитозины LNA могут представлять собой 5-метилцитозин. Линкер 2РО (сегмент В) находится в положении 5' относительно последовательности сегмента А и содержит два ДНК-нуклеозида, связанных фосфодиэфирными связями, при этом межнуклеозидные связи между 3' ДНК-нуклеозидом сегмента А и 5' LNA-нуклеозидом сегмента А также являются фосфодиэфирными. Линкерная группа (Y) может применяться для связывания конъюгированной группы, если таковая имеется, с сегментом В или A(SEQ ID NO 13 и 11).
Мышам линии C57BL6/J вводили внутривенно или подкожно солевой раствор или неконъюгированного антисмыслового LNA-олигонуклеотида (SEQ ID NO 12) в однократной дозе 0,25 мг/кг или эквимолярное количество антисмыслового LNA-олигонуклеотида, конъюгированного с GalNAc1, GalNAc2 или холестерином (2РО), и подвергали эвтаназии на 1-7 день, как указано в таблице ниже (дизайн эксперимента).
Для анализа подавления экспрессии мРНК АроВ из печени и почек выделяли РНК и проводили qPCR с АроВ-специфическими праймерами и зондом. Содержание олигонуклеотидов определяли методом ИФА, а в сыворотке определяли общий холестерин.
Выводы: GalNAc1 и GalNAc2, конъюгированные с антисмысловым LNA-олигонуклеотидом, мишенью которого является АроВ (SEQ ID NO 11 и 13), лучше подавляли экспрессию мРНК АроВ по сравнению с неконъюгированным LNA, мишенью которого является АроВ (Фиг. 8). По-видимому, внутривенное введение конъюгата GalNAc 1 (SEQ ID NO 13) предпочтительнее по сравнению с подкожным введением, что является неожиданным, поскольку для других кластеров GalNAc были получены противоположные результаты (Alnylam, 9th Annual Meeting of the Oligonucleotide Therapeutics Society). Согласно результатам определения общего холестерина, конъюгаты кластера GalNAc (SEQ ID NO 11 и 13) показывают лучшие результаты по сравнению с неконъюгированными или конъюгированными с холестерином соединениями (SEQ ID NO 12 и 14), как при внутривенном, так и при подкожном введении (Фиг. 9, a и b). Содержание олигонуклеотидов в ткани (Фиг. 10, a-f) показывает, что конъюгаты усиливают захват печенью, при этом снижая захват почками по сравнению с родительским соединением. Это отмечается как при внутривенном, так и при подкожном введении. При внутривенном введении GalNAc 1 (SEQ ID NO 13) значительно усиливает захват в печени по сравнению с GalNAc 2 (SEQ ID NO 11), но поскольку оба соединения обладают хорошей активностью, конъюгаты GalNAc 2 по-видимому, обладают более выраженной специфической активностью по сравнению с конъюгатом GalNAc 1, что указывает на то, что конъюгаты GalNAc, не содержащие модулятора фармакокинетики, могут оказаться особенно удобными для антисмысловых LNA-олигонуклеотидов.
Материалы и методы:
Дизайн эксперимента:
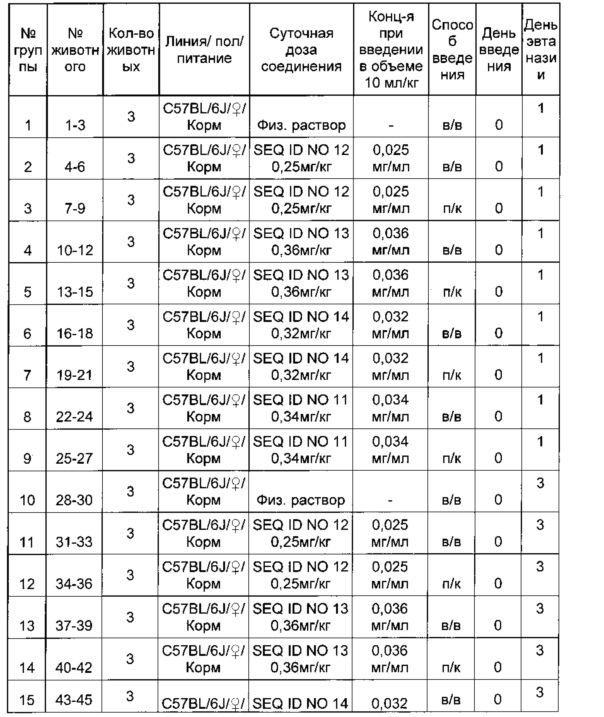
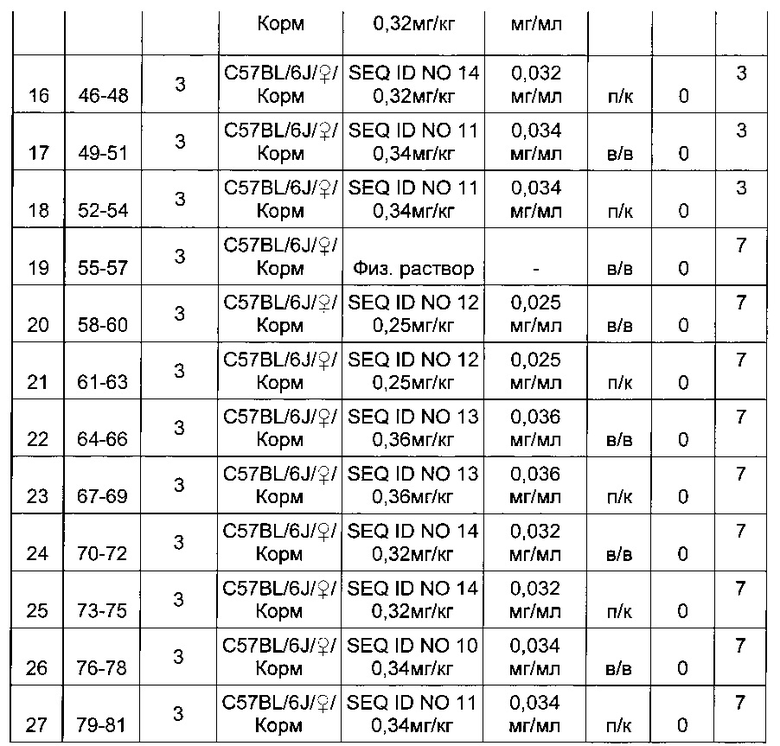
Вводимые дозы. Самки животных линии C57BL/6JBom, весившие по прибытии приблизительно 20 г, получали внутривенно или подкожно соединения в солевом растворе из расчета 10 мл на кг массы тела (массы тела, соответствующей дню 0) или только солевой раствор, как показано в таблице выше.
Взятие образцов ткани печени и почек. Животным проводили анестезию 70% СО2 - 30% O2 и подвергали эвтаназии путем декапитации, как указано в таблице выше. Половину большой доли печени и одну почку измельчали и помещали в реагент RNAlater. Другую половину печени и вторую почку замораживали и использовали для анализа ткани.
Выделение общей РНК и синтез первой цепи. Общую РНК выделяли максимум из 30 мг ткани, гомогенизированной измельчением в шаровой мельнице присутствии лизирующего буфера RLT с использованием набора Qiagen RNeasy (Qiagen, кат. номер 74106) согласно инструкциям производителя. Синтез первой цепи проводили с использованием реагентов Reverse Transcriptase компании Ambion согласно инструкциям производителя.
Для каждого образца 0,5 мкг общей РНК доводили до объема 10,8 мкл свободной от РНКаз водой и смешивали с 2 мкл случайных декамеров (50 мкМ) и 4 мкл смеси дНТФ (по 2,5 мМ каждого дНТФ) и нагревали до 70°С в течение 3 мин, после чего образцы быстро охлаждали на льду. К каждому образцу добавляли по 2 мкл 10× буфера RT, 1 мкл обратной транскриптазы MMLV (100 Ед/мкл) и 0,25 мкл ингибитора РНКаз (10 Ед/мкл), после чего инкубировали при 42°С в течение 60 мин, инактивировали фермент нагреванием при 95°С в течение 10 мин и затем охлаждали образец до 4°С. Образцы кДНК разводили 1: 5 и проводили RT-QPCR с использованием реакционной смеси Taqman Fast Universal PCR Master Mix 2x (Applied Biosystems Cat #4364103) и набора для исследования экспрессии гена Taqman (mApoB, Mn01545150_m1 и mGAPDH #4352339Е) в соответствии с инструкциями производителя на приборе Applied Biosystems RT-qPCR (7500/7900 or ViiA7) в быстром режиме. Содержание олигонуклеотидов в печени и почках определяли методом сэндвич-ИФА.
Исследование холестерина сыворотки: Для получения сыворотки забирали кровь из ретроорбитального синуса непосредственно перед эвтанацией с использованием пробирок S-monovette Serum-Gel (Sarstedt, Nümbrecht, Германия). Общий холестерин в сыворотке определяли с помощью набора АВХ Pentra Cholesterol CP (Triolab, Brondby, Дания) согласно инструкциям производителя.
ПРИМЕР 6: Ингибирование FVII in vivo (низкие дозы, 24 дня)
Использованные соединения - см. Пример 1.
В исследование in vivo на мышах было включено 7 групп мышей (n=3). Каждой мыши вводили одну внутривенную дозу LNA соединения, в дозе 0,25 мг/кг или 0,1 мг/кг. Контрольная группа получала солевой раствор. У мышей предварительно брали кровь за 1 день до введения, последующие взятия проб крови осуществляли на 4, 7, 11, 14, 18 и 24 дни в течение исследования. Мышей подвергали эвтаназии на 24 день и забирали печень, почки и образцы крови. Схема исследования приведена в таблице ниже (дизайн эксперимента). Уровень фактора VII в сыворотке и уровень мРНК определяли с помощью стандартных методов.
Выводы: GalNAc, конъюгированный с LNA-олигонуклеотидом (SEQ ID NO 3 и 6) мишенью которого является FVII, демонстрировали хорошую активность в отношении белка FVII в сыворотке в течение 24 дней (Фиг. 11) и уровня мРНК в печени на 24 день (Фиг. 12) после введения однократной дозы, составлявшей всего 0,1 мг/кг. Очевидно, что кластер GalNAc (SEQ ID NO 3 и 6) обеспечивает большую активность в отношении белка и мРНК FVII по сравнению с конъюгатом холестерина (SEQ ID NO 4 и 7).
Материалы и методы: Согласно приведенной ниже схеме, самцы мышей получали внутривенное введение, печень, почки и образцы крови собирали после умерщвления.
Дизайн эксперимента:
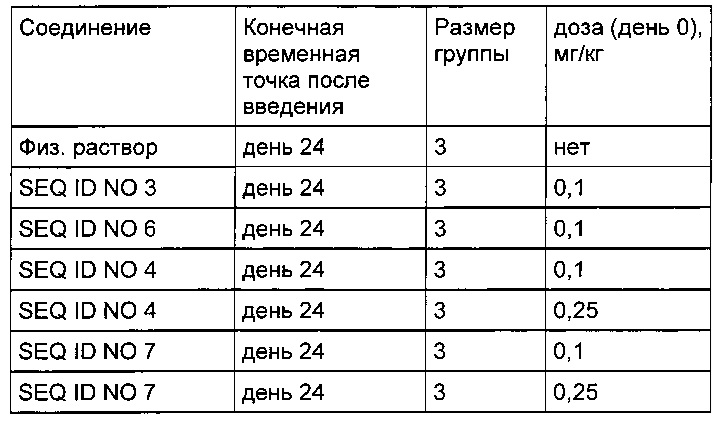
Пример 7. Исследование на приматах - исследование конъюгатов GalNac - мишени PCSK9 и АроВ
Соединения:
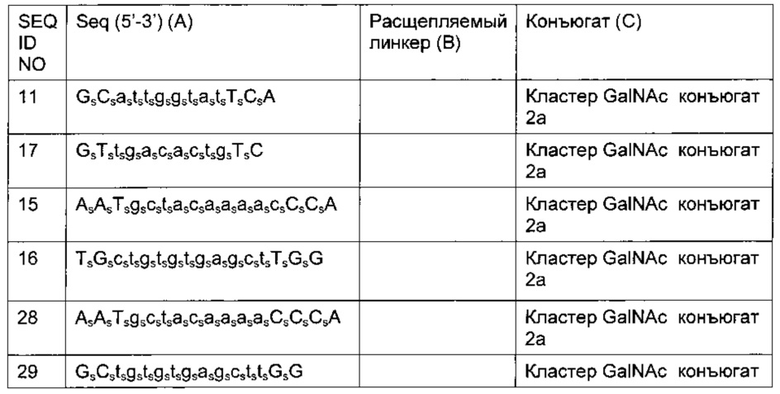

Заглавные буквы обозначают LNA-нуклеозиды (например, бета-D-окси LNA), строчные буквы обозначают ДНК-нуклеозиды. Нижний индекс s обозначает фосфоротиоатные межнуклеозидные связи. Цитозины LNA могут представлять собой 5-метилцитозин.
Основной задачей данного исследования было изучение отдельных липидных маркеров в течение 7 недель после болюсного введения яванским макакам анти-PCSK9 и анти-АроВ LNA, конъюгированных с кластером GalNac (конъюгат 2а), и оценка возможной токсичности соединений для обезьян. Соединения готовили в стерильном солевом растворе (0,9%) в исходной концентрации 0,625 и 2,5 мг/мл.
Самцы (PCSK9) или самки обезьян (АроВ) в возрасте по меньшей мере 24 месяца имели свободный доступ к питьевой воде и каждое животное получало по 180 г корма MWM(E) SQC SHORT expanded (Dietex France, SDS, Saint Gratien, Франция). Общее количество раздаваемого корма на клетку рассчитывали в зависимости от количества животных в клетке на указанный день. Кроме этого, каждое животное получало фрукты или овощи. Животным давали акклиматизироваться к условиям исследования по меньшей мере в течение 14 дней до начала периода лечения. Во время этого периода проводили предварительные исследования. Животным осуществляли внутривенное введение, например, 0,25 мг/кг или 1 мг/кг. Дозу вводили в объеме 0,4 мл/кг. В каждой группе было по 2 животных. Через 3 недели проводили анализ данных и начинали давать соединение второй группе животных, в более высокой или более низкой дозировке, в зависимости от результатов, полученных в первой группе, начальная доза препарата составляла 0,5 мг/кг и 1 мг/кг или менее.
Введение осуществляли однократно в день 1. После инъекции животные находились под наблюдением в течение 7 недель, исследование останавливали на 51 день. День 1 соответствовал 1 дню периода лечения. Клинические проявления, массу тела и потребление пищи (на группу) регистрировали до начала исследования и в ходе исследования.
Образцы крови брали в следующие временные точки:

Биохимические показатели крови
Всем выжившим животным определяли следующие показатели в указанные временные точки:
- полная биохимическая панель (полный перечень приведен ниже) - на -8, 15 и 50 день,
- печеночные пробы (ACT, ЩФ, АЛТ, общий билирубин и ГГТ) - на 4, 8, 22 и 36 день,
- липидный профиль (общий холестерин, ЛПВП, ЛПНП и триглицериды) и Аро-В - на -1, 4, 8, 22, 29, 36 и 43 день.
Кровь (приблизительно 1 мл) забирали в пробирки с литий-гепарином для определения Аро-В, натрия, калия, хлоридов, кальция, неорганического фосфора, глюкозы, ЛПВП, ЛПНП, мочевины, креатинина, общего билирубина, общего холестерина, триглицеридов, щелочной фосфатазы (ЩФ), аланин-аминотрансферазы (АЛТ), аспартат-аминотрансферазы (ACT), креатинкиназы, гамма-глутамилтрансферазы (ГГТ), лактатдегидрогеназы, общего белка, альбумина, соотношения альбумин/глубулины (на биохимическом анализаторе ADVIA 1650).
Анализ крови: Образцы крови брали только у животных 16 группы на -8, -1, 4, 8, 15, 22, 29, 36, 43 и 50 день.
Венозную кровь (приблизительно 2 мл) брали у каждого животного из соответствующей вены в пробирки для получения сыворотки и давали образоваться сгустку по меньшей мере в течение 60±30 мин при комнатной температуре. Кровь центрифугировали при 1000 g в течение 10 минут при охлаждении (устанавливали температуру +4°С). Сыворотку переносили в 3 отдельные пробирки и хранили при 80°С до анализа, который выполняли в компании CitoxLAB, Франция методом ИФА (Circulex Human PCSK9 ELISA, CY-8079, валидированного для образцов, полученных у яванского макака).
Другие анализы: WO 2011009697 & WO 2010142805 описывают способы проведения следующих анализов: qPCR, исследование мРНК PCSK9/АроВ, другие анализы включают определение белка PCSK9/АроВ методом ИФА, анализ Lp(a) в сыворотке методом ИФА (Mercodia No. 10-1106-01), анализ олигонуклеотидов в ткани и плазме (содержание препарата), выделение образцов, стандартных и контрольных проб, определение содержания олигонуклеотидов методом ИФА. Данные для конъюгатов АроВ приведены на Фиг. 16. Соединения 11 и 14, имеющие ту же последовательность олигонуклеотидов, не проявляют значимого фармакологического эффекта в используемой дозе, тогда как соединения SEQ ID NO 17 и 32, имеющие ту же последовательность олигонуклеотидов, оказались эффективны, при этом соединение, конъюгированное с GalNac (SEQ ID NO 17) оказалось существенно более активным, чем соединение, конъюгированное с холестерином. У соединений, мишенью которых является АроВ, не было обнаружено гепатотоксичности или нефротоксичности. Данные для соединений, мишенью которых является PCSK9, приведены в следующей таблице:


У соединений, мишенью которых является PCSK9, не было обнаружено гепатотоксичности или нефротоксичности. Следует отметить, что соединения PCSK9-GalNac быстро и очень эффективно подавляли экспрессию PCSK9, эффект сохранялся в течение длительного времени (на всем протяжении исследования). И быстрое первоначальное снижение экспрессии, и сохранение эффекта в течение длительного времени наглядно свидетельствовали о большей эффективности соединений, конъюгированных с GalNac, указывая на то, что их можно вводить относительно редко и в более низких дозах по сравнению с неконъюгированными родительскими соединениями и соединениями, конъюгированными с использованием альтернативной технологии, например, конъюгированными с холестерином. Аналогичные результаты наблюдались у одного из соединений, мишенью которого является АроВ (см. Фиг. 16), при этом соединение GalNac также оказалось значительно более эффективным по сравнению с соединением, конъюгированным с холестерином, и его действие сохранялось дольше по времени. SEQ ID NO 28 вызывало быстрое и стойкое подавление экспрессии PCSK9 и LDL-C на всем протяжении исследования (отмечалось на 34 день в дозе 2,5 мг/кг, значимое подавление PCSK9 наблюдалось через 48 дней после введения однократной дозы 2,5 мг/кг).
Пример 8: Исследование гепатотоксичности и нефротоксичности на крысах
Токсичность соединений можно оценить в исследованиях на грызунах, например, мышах или крысах. В качестве примера можно привести следующий протокол: Использовали животных линии Wistar Han Crl:WI(Han) в возрасте приблизительно 8 недель. В этом возрасте самцы должны весить приблизительно 250 г. Все животные имели свободный доступ к гранулированному поддерживающему корму SSNIFF R/M-H (SSNIFF Spezialdiäten GmbH, Soest, Германия) и питьевой воде (фильтрованной через 0,22 мкм фильтр), находящийся в бутылях. Введение осуществляли на 1 и 8 день в дозе 10 и 40 мг/кг (подкожно). На 15 день животных подвергали эвтаназии. Образцы мочи и крови собирали на 7 и 14 день. Клинико-патологическое исследование проводили на 14 день. Массу тела определяли до исследования, в 1 день введения и за 1 неделю до вскрытия. Потребление пищи в группе регистрировали ежедневно. Образцы крови брали из хвостовой вены после 6-часового голодания. В сыворотке крови выполняли следующие исследования: количество эритроцитов, средний объем эритроцитов, гематокрит, гемоглобин, средняя концентрация гемоглобина в эритроцитах, среднее содержание гемоглобина в эритроцитах, количество тромбоцитов, количество лейкоцитов, лейкоформула с описанием морфологии клеток, количество ретикулоцитов, натрий, калий, хлориды, кальций, неорганический фосфор, глюкоза, мочевина, креатинин, общий билирубин, общий холестерин, триглицериды, щелочная фосфатаза, аланин-аминотрансфераза, аспартат-аминотрансфераза, общий белок, альбумин, соотношение альбумин/глобулины. В моче определяли α-GST, β-2 микроглобулин, кальбиндин, кластерин, цистатин С, KIM-1, остеопонтин, TIMP-1, VEGF и NGAL. Для количественного определения семи аналитов (кальбиндин, кластерин, GST-α, KIM-1, остеопонтин, TIMP-1, VEGF) использовали панель 1 (панель 1 для оценки нефротоксичности на крысах с помощью магнитных микрочастиц MILLIPLEX® MAP, RKTX1MAG-37K). Для количественного определения трех аналитов (β-2 микроглобулин, цистатин С, липокалин-2/NGAL) использовали панель 2 (панель 2 для оценки нефротоксичности на крысах с помощью магнитных микрочастиц MILLIPLEX® MAP, RKTX2MAG-37K). Определение концентрации данных биомаркеров в моче крыс основано на технологии Luminex хМАР®. Микросферы, покрытые антителами к α-GST, β-2 микроглобулину, кальбиндину, кластерину, цистатину С, KIM-1, остеопонтину, TIMP-1, VEGF и NGAL, помечены двумя флуоресцентными красителями. В моче определяли следующие показатели (на анализаторе ADVIA 1650): белок мочи, креатинин мочи. Количественные показатели: объем, pH (с помощью тест-полосок 10-Multistix SG и мочевого анализатор Clinitek 500), удельный вес (с помощью рефрактометра). Полуколичественные показатели (с помощью тест-полосок 10-Multistix SG и мочевого анализатор Clinitek 500): белок, глюкоза, кетоны, биирубин, нитриты, кровь, уробилиноген, цитология клеточного осадка (микроскопическое исследование). Качественные показатели: Внешний вид, цвет. После эвтаназии определяли массу тела, почек, печени и селезенки и рассчитывали отношение веса органов к весу тела. Образцы почек и печени замораживали или хранили в формалине. Выполняли микроскопический анализ.
Пример 9. Соединения, мишенью которых является АроВ, конъюгированные с FAM меткой.


Заглавные буквы обозначают LNA-нуклеозиды (например, бета-D-окси LNA), строчные буквы обозначают ДНК-нуклеозиды. Нижний индекс s обозначает фосфоротиоатные межнуклеозидные связи. Цитозины LNA могут представлять собой 5-метилцитозин.
Антисмысловые олигонуклеотиды с различными линкерами DNA/PO, меченные FAM, подвергали расщеплению in vitro с использованием нуклеазы S1 - см. таблицу ниже. Гомогенат печени или почек или сыворотка (см. таблицу ниже).
Антисмысловые олигонуклеотиды с различными линкерами DNA/PO, меченные FAM, подвергали расщеплению in vitro с использованием нуклеазы S1 в буфере для нуклеазы (60 Ед в 100 мкл) в течение 20 и 120 мин. Для инактивации фермента к буферному раствору добавляли ЭДТА. Затем раствор анализировали при помощи анионообменной ВЭЖХ на приборе Dionex Ultimate 3000 с использованием колонок Dionex DNApac р-100 и градиента натрия перхлората 10 мМ - 1 М при pH 7,5. Содержание расщепленных и нерасщепленных олигонуклеотидов определяли относительно стандарта, используя флуоресцентный детектор при 615 нм и уф детектор при 260 нм.

Вывод: РО-линкеры (или сегмент В, согласно данному описанию) обеспечивают отщепление конъюгата (или группы С), при этом длина и/или последовательность (состав) линкера позволяет регулировать чувствительность сегмента В к нуклеолитическому расщеплению. Как свидетельствуют результаты 20 мин инкубации с нуклеазой S1 (таблица выше), последовательность DNA/PO линкеров позволяет регулировать скорость расщепления. Таким образом, выбирая последовательность сегмента В (например, DNA/PO линкера), можно также регулировать степень расщепления в сыворотке и клетках тканей-мишеней.
К образцам печени, почки и сыворотки (см. таблицу ниже) добавляли олигонуклеотид SEQ ID NO 21 до концентрации 200 мкг/г ткани. Образцы печени и почки, взятые у мышей NMRI, гомогенизировали в буфере для гомогенизации (0,5% Igepal СА-630, 25 мМ Трис pH 8,0, 100 мМ NaCl, pH 8,0 (доведенном 1 N NaOH). Гомогенаты инкубировали в течение 24 ч при 37°C и затем проводили экстракцию смесью фенол-хлороформ. Содержание расщепленных и нерасщепленных олигонуклеотидов в экстракте печени и почек и в сыворотке определяли относительно стандарта, с помощью ВЭЖХ, как описано выше.

Вывод: РО линкеры (или сегмент В, согласно данному описанию) обеспечивает отщепление конъюгата (или группы С) в гомогенате печени или почек, но не в сыворотке (таблица выше). Примечание: отщепление в описанных выше исследованиях обозначает отщепление расщепляемого линкера, при этом олигомер, или сегмент А, должны оставаться функционально интактными. Подверженность расщеплению в исследованиях, описанных в Примере 9, показывает, является ли линкер биорасщепляемым, или лабильным в физиологических условиях.
Пример 10. Конъюгаты GalNAc. Исследование токсичности на крысах
Методика: См. Пример 8.
Исследования безопасности на крысах проводили в компании CiToxLabs, Франция. Для исследования были отобраны самцы крыс линии Wistar (по 4 на группу), поскольку для крыс Wistar Han, которых использовали для подбора условий исследования (диапазон доз и зависимость от времени), ранее была продемонстрирована возможность прогнозировать нефротоксичность (и в некоторой степени гепатотоксичность) у человека. В день 1 и день 8 животным вводили подкожно конъюгированные LNA соединения (в дозе 10 мг/кг) или соответствующее неконъюгированное «родительское» соединение (в дозе 40 мг/кг). Мочу собирали на 7 день и 14 день и хранили на льду до анализа. Образцы мочи центрифугировали (приблизительно при 380 g в течение 5 мин при +4°С) и исследовали панель маркеров почечного повреждения с помощью многоканального анализа, основанного на технологии Luminex хМАР®.
В панели маркеров почечного повреждения, определяемых в моче, KIM-1 (маркер почечного повреждения, от англ. kidney injury marker 1) показал наибольшие изменения и наиболее четкий сигнал, что согласовывалось с результатами для KIM-1, полученными ранее в ходе мета-анализа маркеров почечного повреждения, определяемых в моче (Vlasakova et al., Evaluation of the Relative Performance of Twelve Urinary Biomarkers for Renal Safety across Twenty Two Rat Sensitivity and Specificity Studies Toxicol. Sci. December 21, 2013).
Использовали соединения: SEQ ID NO 11&17 (мишенью является АроВ) и следующие соединения, мишенью которых является PCSK9, с последовательностями SEQ ID:

Результаты приведены на Фиг. 15, где показано, что применение конъюгатов Galnac позволяет значительно улучшить профиль нефротоксичности родительских LNA соединений. Таким образом, у LNA соединений, конъюгированных с GalNac, не только более выражена активность по сравнению с родительскими соединениями, но и значительно меньше риск нефротоксичности.
Пример 11. Конъюгаты LNA анти-миР и GalNAc
Соединения
Заглавные буквы обозначают LNA, например, бета-D-окси LNA. Строчные буквы обозначают ДНК-нуклеозиды. Нижний индекс s обозначает фосфоротиоатную связь. Другие межнуклеозидные связи представляют собой фосфодиэфирные (фосфатные) связи. Нижний индекс m перед С обозначает 5-метилцитозин в составе LNA (необязательно). В некоторых воплощениях соединения могут также иметь в своем составе цитозин LNA. В некоторых воплощениях группа Конъюгат1а может представлять собой другую группу конъюгата GalNAc, например, описанную в данном документе, такую как группа Конъюгат 2а.
miR-122 (Tiny) 5'-mCsAsmCsAsmCsTsmCsmC-3' (SEQ ID NO 51)
GalNAc-tiny 5'-Conj1a mCsAsmCsAsmCsTsmCsmC-3' (SEQ ID NO 52)
tiny-linker-tiny 5'-mCsAsmCsAsmCsTsmCsmCcamCsAsmCsAsmCsTsmCsmC-3' (SEQ ID NO 53)
GalNac-tiny-linker-tiny 5'-Conj1a mCsAsmCsAsmCsTsmCsmCcamCsAsmCsAsmCsTsmCsmC-3' (SEQ ID NO 54)
В исследование in vivo на мышах было включено 9 групп мышей (n=5). Каждой мыши вводили внутривенно на 0, 2 и 4 день 0,5 мг/кг или 2 мг/кг или эквимолярное количество LNA, конъюгированного с GalNAc, сравниваемого с родительским LNA соединением. Контрольная группа получала солевой раствор (см. описание эксперимента в Таблице 1). Образцы сыворотки брали за 4 дня до введения, в промежуточной точке на 4 день и в конечной точке на 7 день. Образцы печени и почки хранили в RNA later. Валидацию нок-дауна с помощью миР122 проводили, как описано Obad Nat Genet. 2011 Mar 20; 43(4):371-8 (Fig. 17). Уровень холестерина сыворотки анализировали, как описано Elmen J, et al. LNA-mediated микроРНК silencing in non-human primates. Nature. 2008; 452:896-899. (Фиг. 18), а уровень мРНК двух генов, экспрессия которых подавляется миР122 (Aldo А и Bckdk) определяли с помощью стандартного метода QPCR (Фиг. 19). АЛТ определяли для оценки переносимости соединений (Фиг. 20).
Схема исследования


Выводы: Конъюгирование GalNAc с анти-миР122 (SEQ ID 52 и 54) позволило значительно повысить эффективность нокдауна с помощью миРНК122 в печени, что было отмечено по снижению уровня общего холестерина (Фиг. 2) и повышению экспрессии мРНК Aldo А и Bckdk даже в группе, получавшей низкие дозы (3× 0,5 мг/кг, Фиг. 3). На почки анти-миР122 олигонуклеотид эффект не оказывал. Повышение АЛТ было зарегистрировано для SEQ ID 52, при этом при конъюгировании 2 олигонуклеотидов с одним GalNAc (SEQ ID 54) отмечалась тенденция к улучшению.
Пример 12. GalNAc конъюгаты для олигонуклеотидов, мишенью которых является HBV
Олигонуклеотиды синтезировали на универсальных уридиновых носителях, с помощью фосфорамидитного метода на синтезаторе Expedite 8900/MOSS (Multiple Oligonucleotide Synthesis System) в масштабе 4 мкмоль. В конце синтеза проводили отщепление олигонуклеотидов от твердого носителя с использованием водного раствора аммиака в течение 1-2 часов при комнатной температуре, затем удаляли защитную группу в течение 16 ч при 65°С. Олигонуклеотиды очищали при помощи обращенно-фазовой ВЭЖХ и характеризовали при помощи сверхпроизводительной жидкостной хроматоргафии, молекулярную массу определяли при помощи масс-спектрометрии с ионизацией электрораспылением. Более подробное описание приведено ниже.
Элонгация олигонуклеотидов
Присоединение β-цианоэтил-фосфорамидитов (DNA-A(Bz), DNA-G(ibu), DNA-C(Bz), DNA-T, LNA-5-метил-C(Bz), LNA-A(Bz), LNA-G(dmf), LNA-T или C6-S-S линкера) осуществляли с применением 0,1 М раствора 5'-O-DMT-защищенного амидита в ацетонитриле и DCI (4,5-дицианоимидазола) в ацетонитриле (0,25 М) в качестве активатора. На последнем цикле использовали коммерчески доступный фосфорамидит холестерина с C6-линкером в 0,1 М DCM. Тиолирование для введения фосфоротиоатных связей проводили с применением ксантангидрида (0,1 М в смеси ацетонитрил/пиридин 9:1). Для введения фосфодиэфирных связей использовали 0,02 М иод в смеси THF/пиридин/вода 7:2:1. Остальные реагенты представляли собой стандартные реагенты, используемые для синтеза олигонуклеотидов. Для постсинтетического конъюгирования на последней фазе твердофазного синтеза использовали коммерчески доступный фосфорамидит с С6 аминолинкером, а после удаления защитных групп и отщепления от твердого носителя выделяли незащищенный олигонуклеотид. Конъюгаты вводили посредством активации функциональных групп с помощью стандартных методов синтеза.
Очистка при помощи обращенно-фазовой ВЭЖХ:
Неочищенные соединения подвергали очистке с помощью препаративной RP-HPLC на колонках Phenomenex Jupiter С18 10μ 150×10 мм. 0,1 М ацетат аммония pH 8 и ацетонитрил использовали в качестве буферов при скорости тока 5 мл/мин. Собранные фракции лиофилизировали с получением очищенного соединения, обычно в виде белого твердого вещества.
Сокращения:
DCI: 4,5-дицианоимидазол
DCM: дихлорметан
DMF: диметилформамид
DMT: 4,4'-диметокситритил
THF: тетрагидрофуран
Bz: бензоил
Ibu: изобутирил
RP-HPLC: обращенно-фазовая высокоэффективная жидкостная хроматография
LNA гэпмеры:
5'-GsAsGsGscsastsasgscsasgsmCsAsGsG-3' (SEQ ID NO 55)
5'-GsAsGsGsCsastsasgscsasgsmCsAsGsG-3' с 5'-концевым GalNac (Конъюгат 1a). (SEQ ID NO 56)
В области техники есть данные, что вышеуказанный гэпмер (неконъюгированная версия) особенно эффективен против HBV (WO 2011/47312).
Заглавные буквы обозначают LNA нуклеозиды, например, бета-D-окси LNA, строчные буквы обозначают ДНК нуклеозиды, нижний индекс s обозначает фосфоротиоатную связь. Цитозины LNA могут представлять собой 5-метилцитозин.
Антивирусный эффект LNA-олигомера можно оценить in vivo, например, на мышах линии BALB/c или С57В/6, используя для запуска репликации HBV гидродинамическую инъекцию в хвостовую вену плазмиды, например, pAAV/HBV1.3, которая экспрессирует частично повторенную прегеномную РНК HBV (J Virol. 1995 Oct; 69(10):6158-69) или pAAV2/HBV1.3, ее производной (WuxiAppTech, Wuxi, China). Инъекция плазмиды в большом объеме солевого раствора, составляющего 8-12% от массы тела мыши, приводит к накоплению и экспрессии вирусной прегеномной РНК в печени, что впоследствии приводит к развитию острой HBV инфекции. Лечение животных LNA-олигомером можно начинать за 1 или более дней до инъекции плазмиды или через 1 день после инъекции плазмиды. Доставку LNA-олигомера в солевом растворе можно осуществлять путем внутривенной или подкожной инъекции.
Схема исследования

В эксперименте in vivo использовали SEQ ID 55 и SEQ ID 56, последняя последовательность представляет собой GalNAC конъюгат предыдущей (конъюгат 1). Эффективность LNA-соединений в отношении HBV исследовали на модели с гидродинамической инъекцией в хвостовую вену мышам линии Balb/C. LNA-соединения исследовали в эквимолярном количестве; однократная инъекция 2 и 10 мг/кг (SEQ ID 55) и однократная инъекция 2,7 и 13,5 мг/кг (SEQ ID 56). Анти-HBV LNA-соединения сравнивали с солевым раствором и энтекавиром, ингибитором обратной транскриптазы HBV. Энтекавир вводили перорально в ежедневной дозе 0,1 мг/кг. В соответствующих случаях животные получали LNA-соединение за 24 часа до гидродинамической инъекции. Энтекавир давали в суточной дозе, согласно описанию, начиная за 24 часа до гидродинамической инъекции.
Для инициации репликации HBV in vivo всем животным вводили в хвостовую вену 20 мкг ДНК плазмиды pAAV2/HBV в солевом растворе. Инъекции выполняли в солевом растворе, в количестве, эквивалентном 8% массы тела мыши, введение всей дозы продолжалось 5 секунд. Чтобы удостовериться, что животные оправились от гидродинамического шока, их оставляли под наблюдением в течение 2 ч.
На протяжении исследования in vivo у всех животных ежедневно регистрировали изменение массы тела и клинические симптомы. На 1, 3, 5 и 7 день после гидродинамической инъекции у всех животных брали образцы крови из подчелюстной вены, через 4 часа после введения энтекавира. На 7 день, через 4 часа после последнего введения энтекавира у всех животных брали кровь путем пункции сердца после эвтаназии. Выделяли печень и образец подвергали мгновенной заморозке. Все образцы крови собирали в пробирки, содержащие натрий-гепарин.
Часть левой доли печени использовали для определения уровня репликации ДНК HBV при помощи qPCR, выражая результаты как количество копий на единицу веса печени, при этом из общего количества ДНК HBV вычитали количество ДНК pAAV2/HBV. В образцах плазмы, собранных на 7 день, определяли уровень АЛТ методом сэндвич-ИФА (Cusabio; Кат. номер CSB-E16539m). Конъюгаты LNA-олигомеров хорошо переносились, существенного повышения АЛТ не отмечалось.
Вывод: Показано, что соединение SEQ ID 55 в дозах, использовавшихся в данном исследовании, оказывает незначительное влияние на репликацию HBV в печени, хотя в области техники ранее была продемонстрирована его эффективность против HBV (WO 2011/47312). Напротив, соединение SEQ ID 56, имевшее в своем составе тот же олигонуклеотид, только с присоединенным к нему конъюгатом GalNAC, обладает ярко выраженным дозозависимым антивирусным действием на уровень ДНК HBV в печени (Фиг. 22), причем через 8 дней после введения однократной дозы и через 7 дней после инфицирования вирусный титр в печени снижается на 90%. Соединения хорошо переносились, дозозависимого повышения уровня АЛТ на фоне какого-либо из соединений не отмечалось. Несмотря на то, что антисмысловые LNA-олигонуклеотиды эффективно доставляются в печень в отсутствие конъюгации, следует отметить сравнительную неэффективность родительского соединения и выраженное действие конъюгированного соединения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ОЛИГОНУКЛЕОТИДОВ | 2013 |
|
RU2653438C2 |
| ОЛИГОНУКЛЕОТИДЫ ДЛЯ ПОНИЖЕНИЯ ЭКСПРЕССИИ PD-L1 | 2017 |
|
RU2835926C1 |
| МОЛЕКУЛЫ НУКЛЕИНОВЫХ КИСЛОТ ДЛЯ УМЕНЬШЕНИЯ УРОВНЯ мРНК PAPD5 ИЛИ PAPD7 ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННОГО ГЕПАТИТА В | 2018 |
|
RU2766360C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА (А) | 2014 |
|
RU2699985C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА C-III | 2014 |
|
RU2650510C2 |
| ОЛИГОНУКЛЕОТИДЫ ДЛЯ ПОНИЖЕНИЯ ЭКСПРЕССИИ PD-L1 | 2017 |
|
RU2747822C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ HBV И TTR | 2014 |
|
RU2670614C9 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ HBV И TTR | 2014 |
|
RU2782034C2 |
| СОПРЯЖЕННЫЕ АНТИСМЫСЛОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2697152C2 |
| МОЛЕКУЛЫ НУКЛЕИНОВЫХ КИСЛОТ ДЛЯ УМЕНЬШЕНИЯ УРОВНЯ мРНК PAPD5 ИЛИ PAPD7 ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННОГО ГЕПАТИТА В | 2017 |
|
RU2768699C2 |



































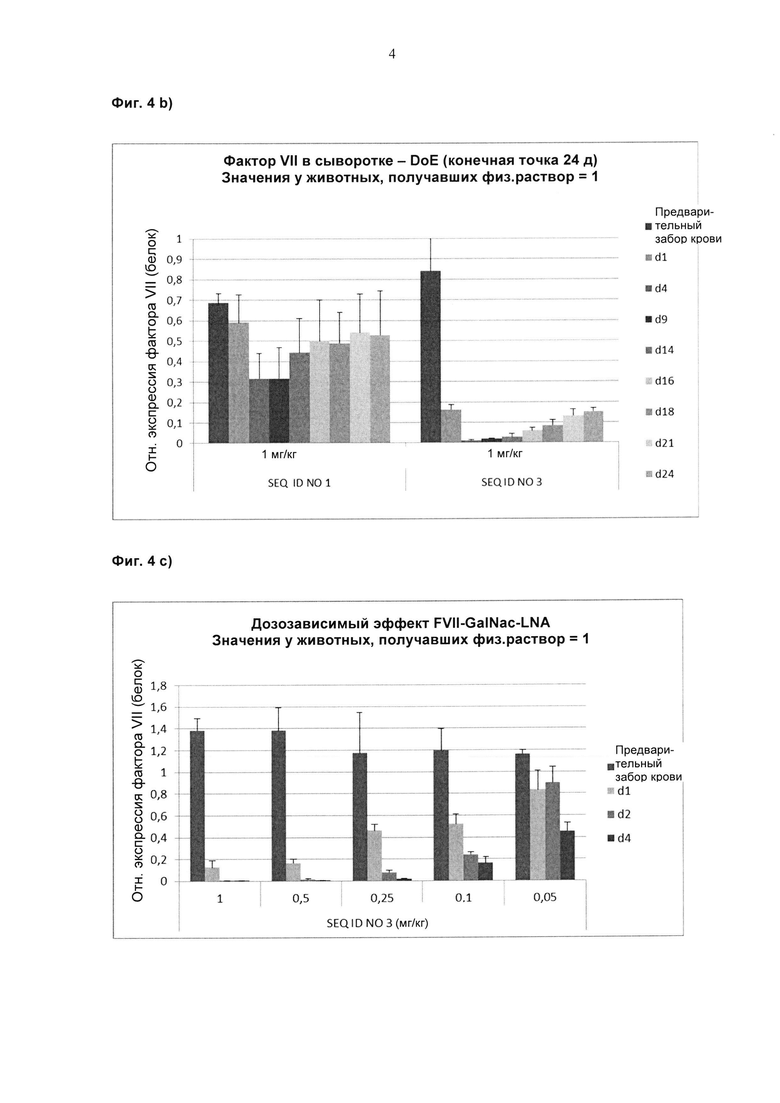

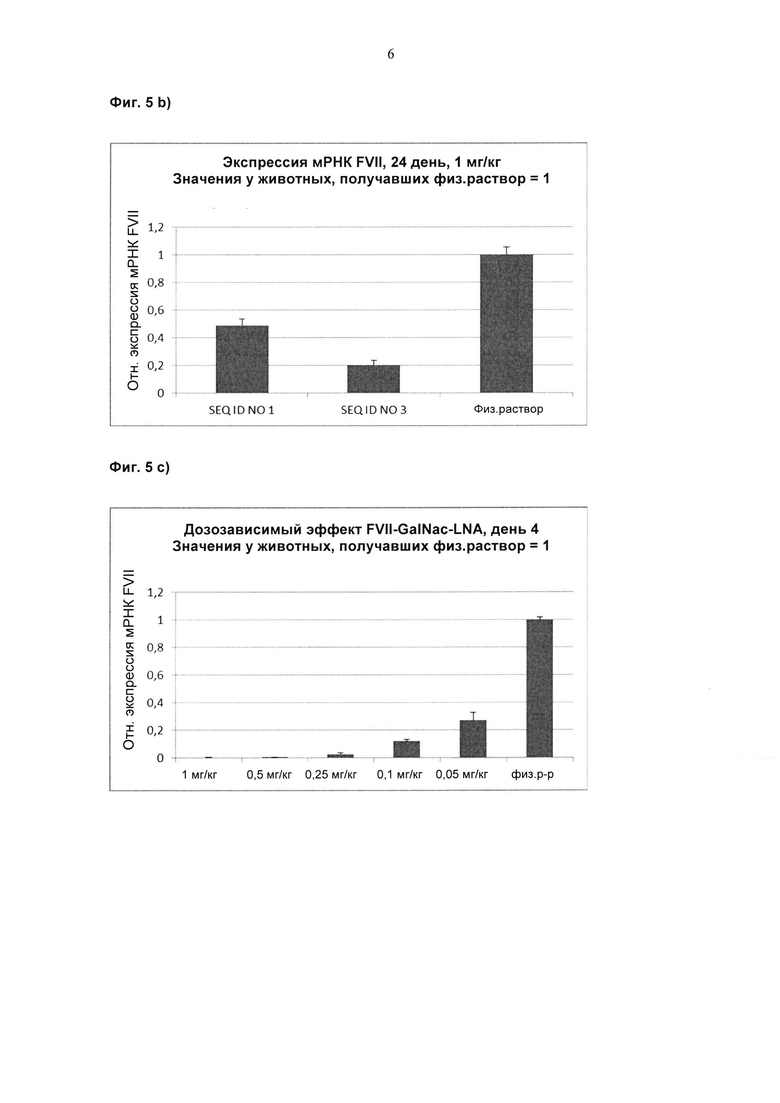

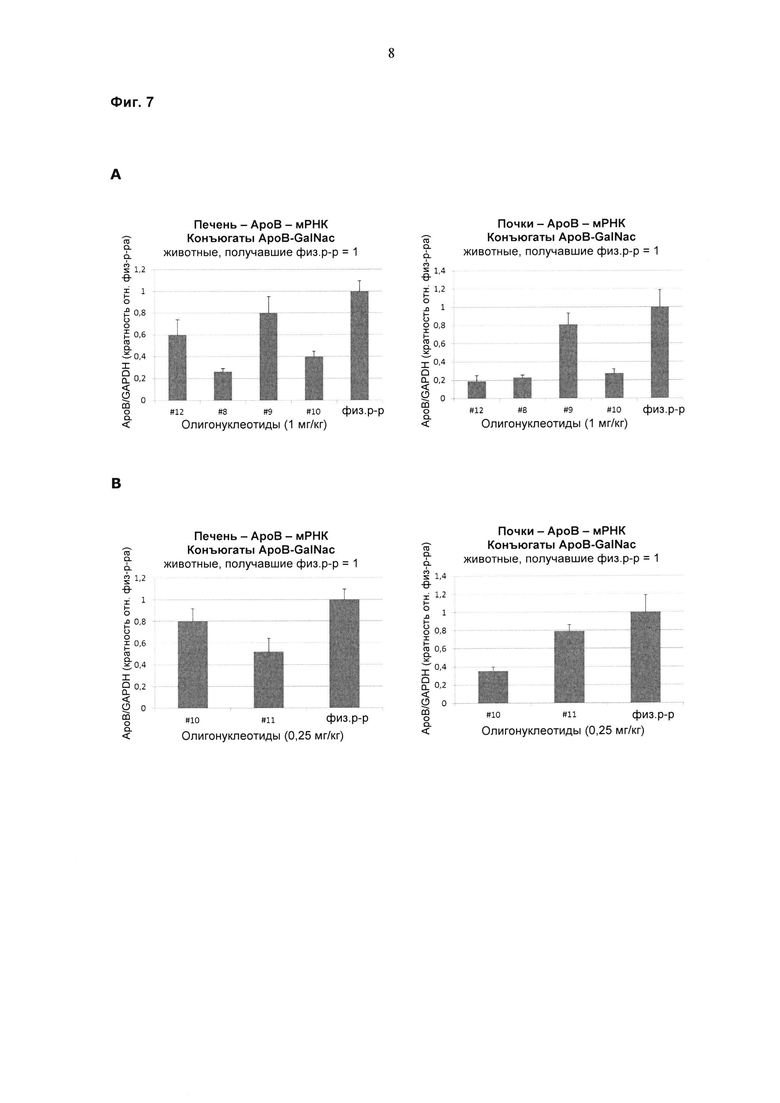

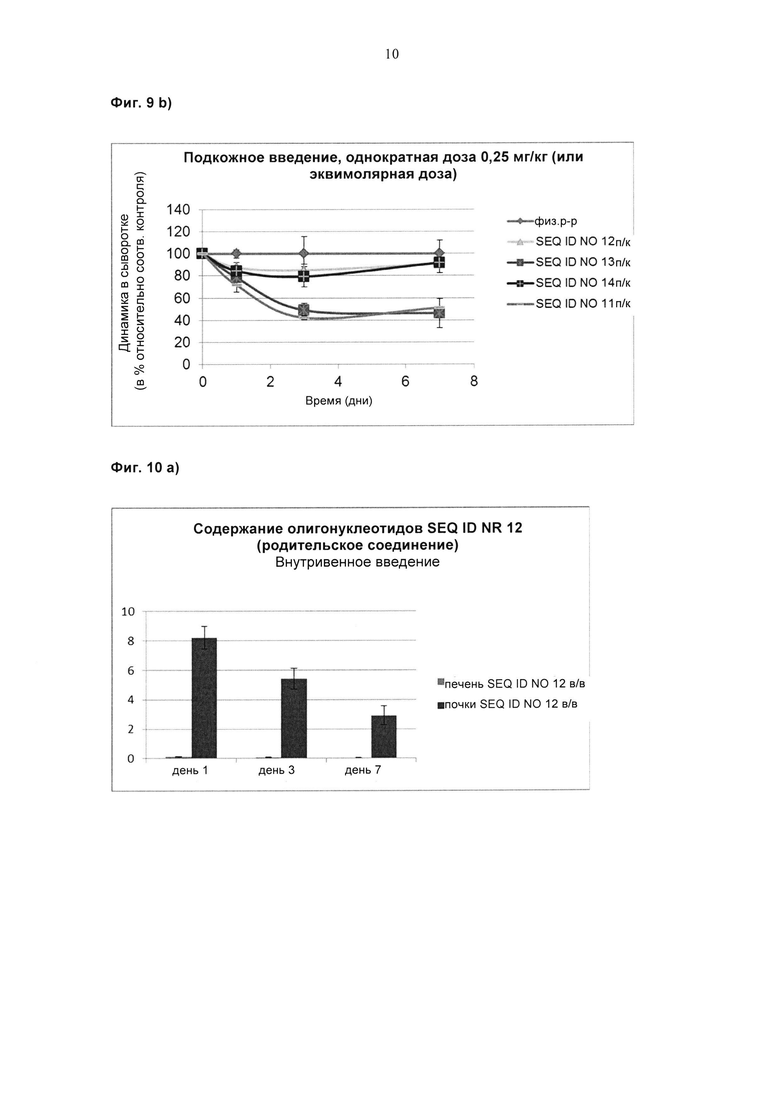









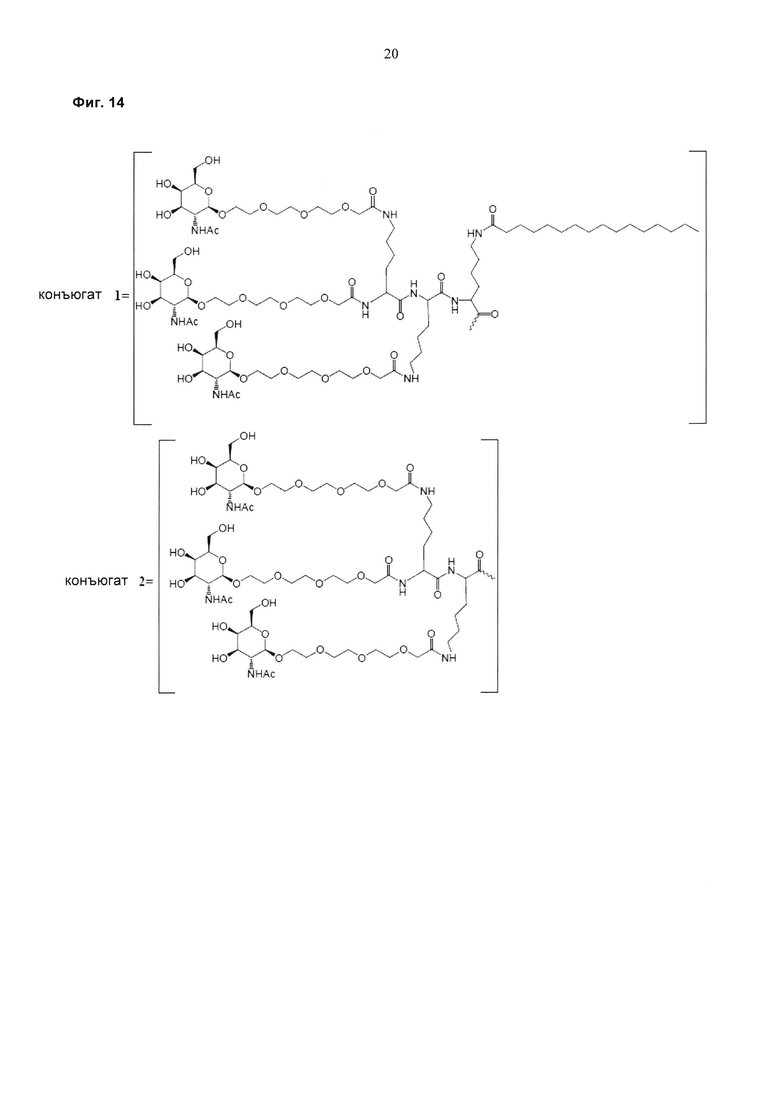




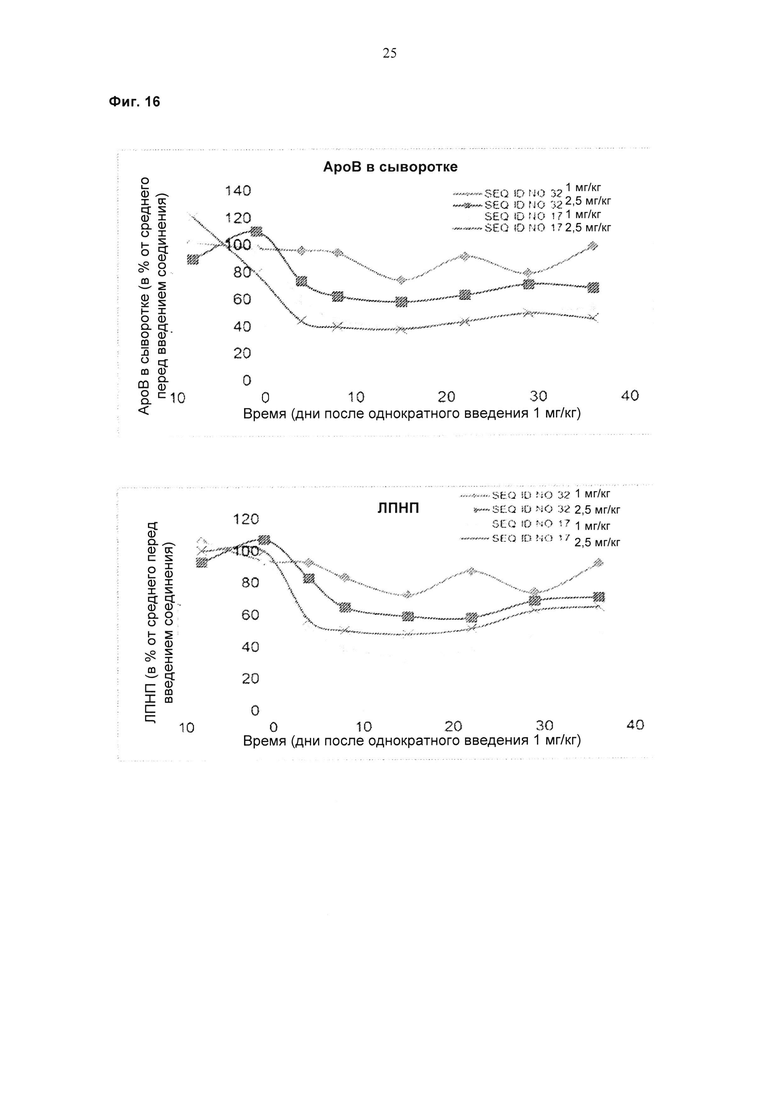




Изобретение относится к области биохимии. Описана группа изобретений, включающая конъюгат, снижающий уровень экспрессированной в печени РНК, содержащий антисмысловой LNA-олигомер и ковалентно связанную с ним конъюгатную группировку, содержащую группу, направленную на асиалогликопротеиновый рецептор и фармацевтическую композицию, содержащую вышеуказанный конъюгат в эффективном количестве. В одном из вариантов изобретения, антисмысловой LNA-олигомер представляет собой гэпмер длиной 10-22 нуклеотида, а группа, направленная на асиалогликопротеиновый рецептор, представляет собой кластер галактозы с двумя или тремя N-ацетилгалактозаминами. Экспрессируемая в печени РНК представляет собой мРНК, выбранную из группы, состоящей из: фактора VII, С6 компонента комплемента, Bcl2, транстиретина (TTR), PCSK9, аполипопротеина В (АроВ), рецептора глюкагона (GCGR), С-реактивного белка (CRP), диацилглицерин ацилтрансферазы 2 типа (DGAT2), глюкокортикоидного рецептора (GCCR), фосфотазы и гомолога тензина (PTEN), тирозинфосфатазы РТР1В, натрий-глюкозного котранспортера 2 типа (SGLT2) и супероксиддисмутазы SOD1 или РНК вируса, например вируса гепатита С или гепатита В. Изобретение расширяет арсенал средств для ингибирования экспрессии РНК. 2 н. и 19 з.п. ф-лы, 21 ил., 17 табл., 12 пр.
1. Конъюгат, снижающий уровень экспрессированной в печени РНК, содержащий антисмысловой LNA-олигомер и ковалентно связанную с ним конъюгатную группировку, содержащую группу, направленную на асиалогликопротеиновый рецептор, где антисмысловой LNA-олигомер представляет собой гэпмер длиной 10-22 нуклеотида, а группа, направленная на асиалогликопротеиновый рецептор, представляет собой кластер галактозы с двумя или тремя N-ацетилгалактозаминами.
2. Конъюгат по п. 1, в котором группа, направленная на асиалогликопротеиновый рецептор, не является Tyr-Glu-Glu-(экссомы мочи, вызванные раком предстательной железыаминогексилGalNac)3 или L3G4 или кластерами галактозы на основе холана.
3. Конъюгат по п. 1, в котором конъюгатная группировка также содержит модулятор фармакокинетики, выбранный из группы, состоящей из С8-С36 насыщенной или ненасыщенной жирной кислоты, стерола, холестерина, пальмитоила, гексадек-8-еноила, олеила, (9Е, 12Е)октадека-9,12-диеноила, диоктаноила и С16-С20 ацила.
4. Конъюгат по п. 1, в котором кластер галактозы состоит из тримера N-ацетилгалактозамина.
5. Конъюгат по п. 1, в котором указанная конъюгатная группировка ковалентно связана с указанным олигомером посредством расщепляемого в физиологических условиях линкера.
6. Конъюгат по п. 5, в котором расщепляемый в физиологических условиях линкер выбран из группы, состоящей из кислотолабильного линкера, дисульфидного линкера, сегмента нуклеозидов, связанных фосфодиэфирными связями (участка В).
7. Конъюгат по п. 3, где модулятор фармакокинетики присоединен к конъюгатной группировке посредством линкера, например расщепляемого в физиологических условиях линкера.
8. Конъюгат по п. 1, в котором олигонуклеотид включает в себя 7-26, например, 7-18, 7-10, 10-16, 12-14 смежных нуклеозидов.
9. Конъюгат по п. 1, в котором антисмысловой LNA-олигомер содержит по меньшей мере 90% фосфоротиоатных межнуклеозидных связей.
10. Конъюгат по п. 1, в котором мишенью олигомера является экспрессируемая в печени нуклеиновая кислота, такая как РНК, например экспрессируемая в печени мРНК или микроРНК, или нуклеиновая кислота вируса.
11. Конъюгат по п. 10, где экспрессируемая в печени РНК представляет собой мРНК, выбранную из группы, состоящей из: фактора VII, С6 компонента комплемента, Bcl2, транстиретина (TTR), PCSK9, аполипопротеина В (АроВ), рецептора глюкагона (GCGR), С-реактивного белка (CRP), диацилглицерин ацилтрансферазы 2 типа (DGAT2), глюкокортикоидного рецептора (GCCR), фосфотазы и гомолога тензина (PTEN), тирозинфосфатазы РТР1В, натрий-глюкозного котранспортера 2 типа (SGLT2) и супероксиддисмутазы SOD1 или РНК вируса, например вируса гепатита С или гепатита В.
12. Конъюгат по п. 10, в котором олигомер представляет собой шортмер.
13. Конъюгат по п. 10, в котором мишенью олигомера является экспрессируемая в печени микроРНК, например миР-122.
14. Конъюгат по п. 10, в котором длина олигомера составляет от 8 до 18 нуклеотидов.
15. Конъюгат по п. 1, мишенью которого является нуклеиновая кислота вируса гепатита В, например последовательность ДНК и/или РНК вируса гепатита В (HBV).
16. Конъюгат по любому из пп. 1-15 для применения в медицине.
17. Конъюгат по любому из пп. 1-15 для применения при лечении метаболических заболеваний или нарушений, например заболеваний или нарушений, затрагивающих печень.
18. Конъюгат по пп. 13-15 для применения при лечении гепатита, например гепатита В или С.
19. Конъюгат по любому из пп. 1-15 для применения в изготовлении лекарственного средства.
20. Фармацевтическая композиция для снижения уровня экспрессируемой в печени РНК, содержащая конъюгат по любому из пп. 1-15 в эффективном количестве и фармацевтически приемлемый разбавитель, носитель, соль или адъювант.
21. Фармацевтическая композиция по п. 20, где композиция содержит буферный солевой раствор.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| WO2007134181 A2 22.11.2007 | |||
| WO2008154401 A2 18.12.2008 | |||
| Fluiter et al | |||
| "In vivo tumor growth inhibition and biodistribution studies of locked nucleic acid (LNA) antisense oligonucleotides", Nucl | |||
| Acid Res., 2003, V.3, 953-962 | |||
| ОЛИГОМЕРНОЕ СОЕДИНЕНИЕ, ПОНИЖАЮЩЕЕ ЭКСПРЕССИЮ ЧЕЛОВЕЧЕСКОГО ГЕНА Bcl-2, КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ ОЛИГОМЕРНОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2004 |
|
RU2377301C2 |
Авторы
Даты
2018-04-02—Публикация
2014-01-30—Подача